
Química
Uniones químicas
Se denomina unión química a la fuerza de interacción entre dos átomos o grupos de átomos con
intensidad suficiente para mantenerlos unidos en una especie diferente. Un enlace químico se
formará si el ordenamiento de átomos posee una energía menor que la de los átomos separados
(estado de mínima energía).
Para explicar cómo se forman las sustancias (moléculas y los compuestos iónicos), Gilbert Lewis
propuso que los átomos se combinan para alcanzar la configuración electrónica más estable o sea
hasta completar sus octetos.
Las partículas (átomos o iones) alcanzan la estabilidad máxima, al ser isoelectrónicas con un gas
noble.
Al estudiar los enlaces químicos se consideran sólo los electrones externos o electrones de
valencia, debido a que al formarse un enlace se ponen en contacto sus regiones más externas. El
sistema de puntos desarrollado por Lewis permite representar a los electrones de valencia, para
ello se indica el símbolo del elemento y un punto por cada electrón. Por ejemplo, a continuación se
presentan los símbolos de puntos de Lewis de diferentes átomos:
Tipos de enlaces
Las uniones químicas se clasifican en iónicas, covalentes y metálicas.
A partir de los valores de electronegatividad es posible predecir si un enlace químico es iónico o
covalente. El tipo de enlace estará dado en relación a la diferencia de electronegatividad entre los
átomos que lo forman.
- Los átomos de elementos con diferencias de electronegatividad mayores o iguales a 2
forman enlaces iónicos. Esta diferencia de electronegatividad se aplica a la mayoría de los
compuestos iónicos, pero existen excepciones. Si tenemos en cuenta el porcentual de
carácter iónico se considera que para una diferencia de electronegatividad de 1,7 el
porcentual de carácter iónico es del 50%. En los enlaces iónicos participan un metal y uno
o más no metales.
- Los átomos de elementos no metálicos cuyas diferencias de electronegatividades son
menores a 2 forman enlaces covalentes.

Química
El enlace iónico
Este tipo de unión resulta de las interacciones electrostáticas entre cationes y aniones.
Según las propiedades analizadas en la unidad 1, los metales alcalinos y alcalino-térreos forman
cationes fácilmente, pues los átomos de estos elementos presentan bajas energías de ionización,
y por otro lado los halógenos, el oxígeno, el azufre y el nitrógeno tienden a formar aniones. Por
esta razón muchos compuestos iónicos están constituidos por un metal del grupo 1 o 2 y uno de
los no metales mencionados.
A la mínima relación entre cationes y aniones que se repite en un cristal, se la denomina unidad
fórmula. Los compuestos iónicos no están formados por moléculas.
Figura 1.Representación de esferas del cristal de NaCl
Cationes (Na
+
) y aniones (Cl
–
) alternados en
una estructura cristalina tridimensional.
Para representar a las unidades fórmulas o a las sustancias iónicas, se utilizan estructuras de
Lewis y fórmulas mínimas. La estructura de Lewis de un compuesto iónico consiste en la
representación de los iones que lo constituyen. La fórmula mínima indica la relación entre el
número de cada uno de los iones que forman una unidad fórmula.
El enlace covalente
Un enlace covalente es aquel en el que los átomos comparten electrones y forman moléculas; y
cada átomo adquiere, en la mayoría de los casos, la configuración electrónica del gas noble más
cercano en la tabla periódica.
Para representar a las moléculas se utilizan estructuras de Lewis, y fórmulas desarrolladas y
moleculares.
Los átomos pueden formar distintos tipos de enlaces covalentes. Según el número de pares de
electrones compartidos, la unión covalente puede ser simple, múltiple y coordinada o dativa:
o Simple: dos átomos se unen por medio de un par de electrones.

Química
o Múltiple: los átomos comparten dos o tres pares de electrones; la unión o enlace se
denomina covalente doble y triple respectivamente.
o Coordinada o dativa: el par de electrones compartido es aportado sólo por uno de los
átomos.
Para representar las fórmulas desarrolladas, se indican los símbolos de los elementos
intervinientes y un guion que representa cada par de electrones compartido; las uniones
covalentes dativas o coordinadas se simbolizan con una flecha desde el átomo menos
electronegativo hacia el más electronegativo.
Excepciones a la regla del octeto
Existen algunas moléculas en las que no se cumple la regla del octeto en por lo menos uno de los
átomos involucrados. Las excepciones pueden ser:
- octeto incompleto
En algunas moléculas el número de electrones que rodea al átomo central es inferior a
ocho. Por ejemplo en la molécula de BeCl
2
el átomo de Be está rodeado por cuatro
electrones y en la molécula de BF
3
, el átomo de B está rodeado por seis electrones.
- octeto expandido
Los átomos de los elementos del tercer período en adelante, constituyen moléculas en las
que hay más de ocho electrones alrededor del átomo central. Por ejemplo en la molécula
de SF
4
, el átomo de S está rodeado de 10 electrones. Además de los orbitales 3s y 3p
tienen orbitales 3d incompletos con los que pueden formar enlaces.
- número impar de electrones
En algunas moléculas, un átomo tiene un número impar de electrones. Por ejemplo la
molécula de NO y la de NO
2
.
Polaridad del enlace
Los enlaces covalentes pueden ser polares o no polares. Una propiedad útil para distinguirlos, es
la electronegatividad.
En un enlace covalente entre 2 átomos del mismo elemento, el par electrónico se comparte de
forma equitativa. A este enlace se lo denomina no polar. Por ejemplo, en la molécula de H
2
(hidrógeno).
En un enlace covalente entre 2 átomos de distintos elementos, los electrones no son compartidos
por igual. Como consecuencia se genera una densidad de carga negativa sobre éste y una
densidad de carga positiva sobre el átomo menos electronegativo. A tal enlace se lo denomina
covalente polar. Por ejemplo, en la molécula de HCl (cloruro de hidrógeno) hay una densidad de
carga negativa sobre el átomo de cloro y una densidad de carga positiva sobre el átomo de
hidrógeno.

Química
Figura 2. Representación de una molécula de HCl
La esfera verde representa a un átomo de cloro y la esfera
amarilla representa un átomo de hidrógeno.
Una medida cuantitativa de la polaridad de un enlace es el momento dipolar (μ) y la unidad en
que se mide es el Debye (D). El momento dipolar es el producto entre la carga y la distancia que
las separa (μ = q x d) en un enlace químico, y es una magnitud vectorial, es decir que se
representa mediante un vector que tiene módulo (intensidad), dirección y sentido.
Número de oxidación
El número de oxidación de un átomo también llamado estado de oxidación, se refiere al número
de cargas que tendría un átomo si los electrones fueran transferidos por completo al átomo más
electronegativo.
Las reglas generales para asignar números de oxidación son:
1. El número de oxidación de cualquier elemento libre es cero. Esto incluye a las sustancias
(simples) formadas por moléculas poliatómicas.
2. Para iones monoatómicos, el número de oxidación coincide con la carga neta del ion.
3. El número de oxidación del elemento oxígeno es – 2, en los peróxidos -1 y en los
compuestos con flúor +2.
4. El número de oxidación del elemento hidrógeno es + 1, y en los hidruros metálicos es -1.
5. El número de oxidación del elemento flúor es -1 en todos los compuestos.
6. En una especie neutra, la suma de los números de oxidación multiplicada por los
respectivos subíndices es igual a cero. En un ion poliatómico la suma de los números de
oxidación multiplicada por los respectivos subíndices es igual a la carga neta del ion.
Estructuras de Lewis
Las estructuras de Lewis son de gran utilidad para representar los enlaces.
Para representar la estructura de Lewis se utilizan:
● los símbolos de los elementos, que representan a los átomos,
● la CEE de cada uno de los átomos de los elementos intervinientes,
● símbolos, como por ejemplo: °, x, , para representar a los electrones externos o de
valencia.

Química
En el caso de los iones se deben agregar:
● signos + y – para indicar la carga de los iones.
● corchetes encerrando el anión,
Ejemplos
Li
2
O, óxido de litio
Para representar una estructura de Lewis, se analiza el tipo de unión química. En este
caso, el litio es un metal cuya electronegatividad es 0,98 y el oxígeno es un no metal de
electronegatividad 3,44, por lo tanto, la diferencia de electronegatividad es mayor que 2,0 y
la unión química es iónica.
La estructura de Lewis de un compuesto iónico consiste en la representación de los iones
que lo constituyen. La fórmula mínima Li
2
O indica que una unidad elemental de óxido de
litio está formada por dos cationes litio y un anión óxido.
Según las configuraciones electrónicas externas del litio y del oxígeno, determinamos las
cargas de los iones respectivos:
CEE
Li
: 2s
1
CEE
O
: 2s
2
2p
4
El átomo de litio forma un catión quedando con la configuración electrónica del gas noble
más próximo (helio, CEE: 1s
2
). Significa que el catión que forma el litio tiene 3 protones y 2
electrones, por tal motivo, queda una carga positiva sin compensar, que le dan la carga al
catión. Su símbolo es Li
+
y su CEEes 1s
2
.
El átomo de oxígeno forma un anión que tiene la configuración electrónica del gas noble
más próximo (neón, CEE: 2s
2
2p
6
).Significa que el anión que forma el oxígeno tiene 8
protones y 10 electrones, por lo tanto, quedan dos cargas negativas sin compensar, que le
dan carga al anión. Su símbolo es O
2-
y suCEEes 2s
2
2p
6
.
La estructura de Lewis del Li
2
O es:
Importante: En las fórmulas de Lewis, representamos de manera diferente a los electrones
de los distintos átomos (círculos, cruces, etc.) como un recurso didáctico. Esto no significa
que los electrones sean diferentes, todos los electrones son iguales e indistinguibles. Además,
los electrones siempre se representan por pares y alrededor del símbolo del elemento (como
se indica en la figura).
Química
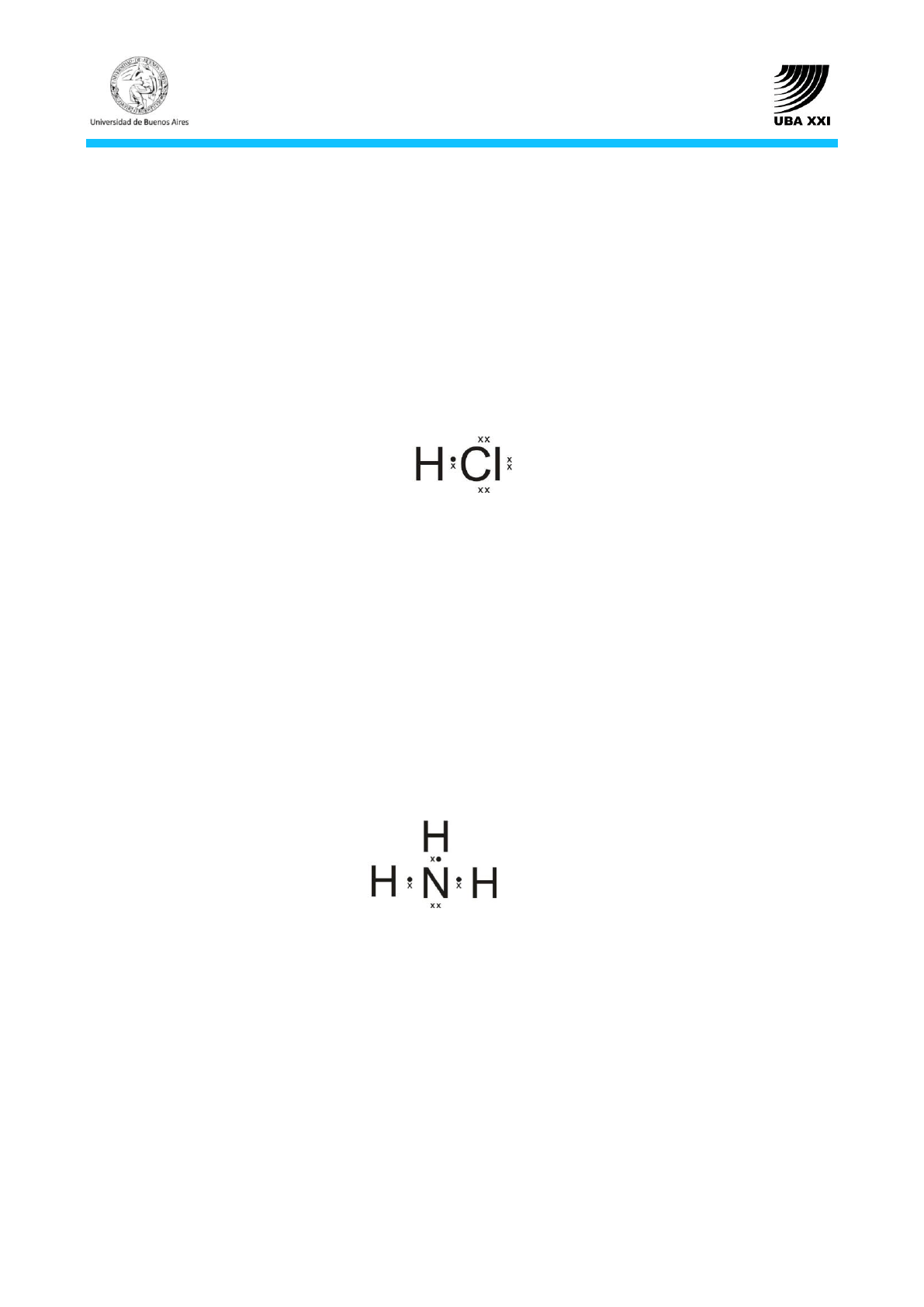
HCl, cloruro de hidrógeno
Para representar la estructura de Lewis del cloruro de hidrógeno se tiene en cuenta que ambos
átomos son no metales y la diferencia de electronegatividad es 0,90, por lo tanto la unión es
covalente.
CEE
Cl
: 3s
2
3p
5
CEE
H
: 1s
1
Al representar el símbolo de puntos para el átomo de cloro, queda un electrón no apareado, por lo
que se establece un enlace covalente con el átomo de hidrógeno. De esta manera, ambos átomos
adquieren la configuración electrónica del gas noble más próximo. La estructura de Lewis es:
A partir de la CEE de los átomos que constituyen a la molécula, escribimos la estructura de Lewis.
CEE
N:
2s
2
2p
3
CEE
H
: 1s
1
,
NH
3
, amoníaco
Al representar el símbolo de puntos para el átomo de nitrógeno, quedan tres electrones no
apareados, por lo que se establecen tres enlaces covalentes con los átomos de hidrógeno. De
esta manera, los átomos adquieren la configuración electrónica del gas noble más próximo. La
estructura de Lewis es:
H
2
CO
3
, ácido carbónico
Para representarla, es conveniente tener en cuenta:
o que la molécula está formada por átomos de no metales, por lo tanto, la unión es
covalente;
o las CEE de cada uno de los átomos involucrados;
o la distribución de los átomos en función de la electronegatividad, el átomo menos
electronegativo ocupa la posición central.
Las CEE de los átomos de los elementos que lo constituyen son:
CE
H
: 1s
1
CEE
C
: 2s
2
2p
2
CEE
O
: 2s
2
2p
4
Química
En el H
2
CO
3
el símbolo del carbono se ubica en el centro rodeado de los símbolos de los átomos
de oxígeno, y el símbolo del hidrógeno se ubica al lado del oxígeno.
Al representar los electrones, conviene colocar primero el electrón del átomo de hidrógeno, luego,
los correspondientes al átomo de oxígeno, que está unido al átomo de hidrógeno, y los electrones
del átomo del carbono; se establecen dos uniones covalentes simples, una entre el hidrógeno y el
oxígeno (H-O) y otra entre el oxígeno y el carbono (O-C). De esta manera, el átomo de hidrógeno
adquiere la CEE de los átomos del gas noble más próximo (He), y el átomo de oxígeno (unido al
de hidrógeno) adquiere la CEE de los átomos del gas noble más próximo (Ne).
Se repite esta secuencia para representar los electrones de los otros átomos de hidrógeno y
oxígeno unidos entre sí al carbono. Para que el átomo de carbono adquiera la CEE de los átomos
del gas noble más próximo (Ne), necesita dos electrones, por eso, establece una unión covalente
doble con el otro átomo de oxígeno y, así, ambos alcanzan el octeto electrónico.
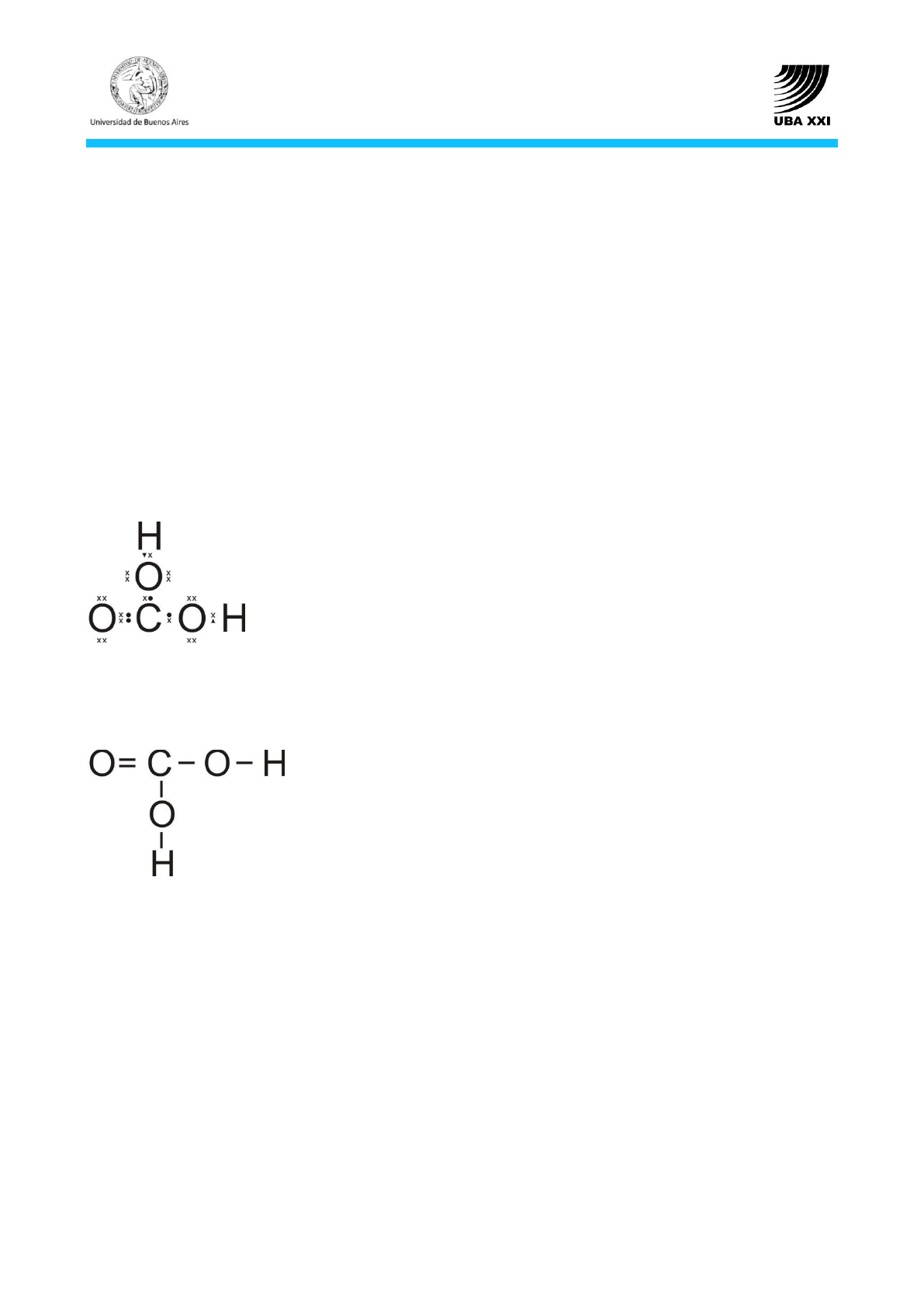
La estructura de Lewis es:
De esta forma, cada átomo adquiere el número de electrones externos
de los átomos del gas noble más próximo: 2 electrones para el Hidrógeno, 8
electrones para el Oxígeno y 8 electrones para el Carbono.
La fórmula desarrollada es:
2
BrO
, ion bromito
Para dibujar la estructura de Lewis, es conveniente:
ubicar en el centro, el símbolo del átomo del elemento que no es oxígeno y rodearlo con
tantos átomos de oxígeno como indica la fórmula;
representar, en un átomo de oxígeno, un electrón por cada carga negativa que posea el
ion;
encerrar el conjunto entre corchetes indicando la carga del ion;
dibujar los electrones en el átomo de oxígeno que tiene el electrón que le da la carga al
anión, y los del no metal, de manera que se establezca una unión covalente simple entre
ambos;
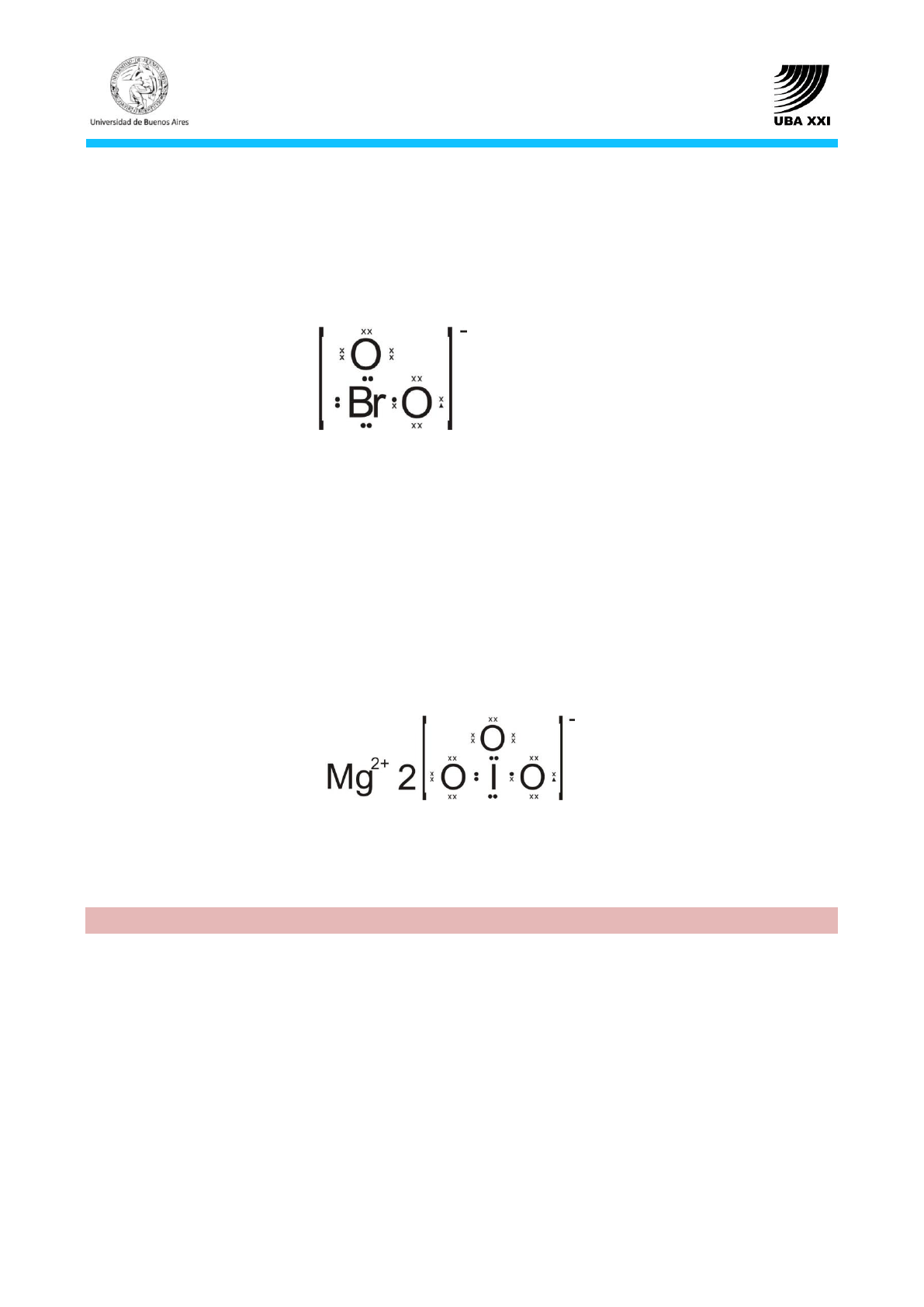
Química
representar los electrones de los demás átomos de oxígeno (si los hubiera).
La estructura de Lewis
2
BrO
del es:
Mg(IO
3
)
2
, yodato de magnesio
Para representar estructura de Lewis de una oxosal, se considera que es un compuesto ternario
iónico, formado por cationes y oxoaniones y que la suma de las cargas de cationes y aniones en
una unidad fórmula es igual a cero. Por lo tanto, para dibujarla, es aconsejable separar cationes
de aniones.
A partir de la fórmula de la sal, se deduce que en una unidad fórmula, por cada catión Mg
2+
, hay
dos aniones
3
IO
. La estructura de Lewis es:
Unión metálica
Los metales, al igual que los compuestos iónicos, no están formados por moléculas. Se considera
que un trozo de metal es “un conjunto de iones positivos (cationes) inmerso en un mar de
electrones móviles”. Como los átomos de los metales tienen baja energía de ionización, los
electrones externos, es decir, los más débilmente unidos al núcleo de cada átomo, se mueven a lo
largo de todo el cristal. No están asociados con ningún núcleo en particular, sino que forman una
nube electrónica que pertenece a toda la red cristalina.

Química
Tipos de sustancias
Las sustancias se clasifican en iónicas, metálicas, moleculares y covalentes (redes). El tipo de
partícula que constituye a una sustancia depende de las uniones químicas
La siguiente tabla resume el tipo de partículas que constituye a los distintos tipos de sustancias y
algunos ejemplos:
Tipo de sustancia
Tipo de partícula
Ejemplos
Iónica
Cationes y aniones
CuSO
4
, KOH, NaNO
3
,
MgO
Metálica
Cationes (núcleo y electrones
internos) y electrones externos
móviles.
Co, Au, Fe, Ag
Molecular (covalente)
Moléculas
O
2
, H
2
O, CCl
4
Covalente (redes)
Átomos
C grafito, C diamante

U 2 Uniones químicas.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.