
Fisiología Módulo 2- Capitulo 4
1
Transporte de sustancias a través de las
membranas celulares
La membrana celular consiste en una BICAPA lipídica con
proteínas de transporte de la membrana celular. La bicapa lipídica
no es miscible con el líquido extracelular ni con el líquido
intracelular. Por tanto, constituye una barrera frente al movimiento
de moléculas de agua y de sustancias insolubles entre los
compartimientos del líquido extracelular e intracelular.
Las moléculas proteicas de la membrana tienen unas
propiedades totalmente diferentes para transportar sustancias.
Sus estructuras moleculares interrumpen la continuidad de la
bicapa lipídica y constituyen una ruta alternativa a través de la
membrana celular. Muchas de estas proteínas penetrantes
pueden actuar como proteínas transportadoras:
Proteínas de los canales
Proteínas transportadoras
Tienen espacios acuosos en
todo el trayecto del interior de
la molécula y permiten el
movimiento libre de agua, así
como de iones o moléculas
seleccionados
Se unen a las
moléculas o iones que se
van a transportar y cambios
conformacionales de las
moléculas de la
proteína desplazan después
las sustancias a través de los
intersticios de la proteína
hasta el otro lado
de la membrana.
Las proteínas de los canales y las proteínas transportadoras habitualmente son selectivas para los tipos
de moléculas o de iones que pueden atravesar la membrana.
El transporte a través de la membrana celular, ya sea directamente a través de la bicapa lipídica o a través
de las proteínas, se produce mediante uno de dos procesos básicos: difusión o transporte activo.
DIFUSION
TRANSPORTE ACTIVO
Movimiento molecular aleatorio de las sustancias
molécula a molécula, a través de espacios
intermoleculares de la membrana o en combinación con
una proteína transportadora.
La energía que hace que se produzca la difusión es la
energía del movimiento cinético normal de la materia.
Movimiento de iones o de otras sustancias a través
de la membrana en combinación con una proteína
transportadora de tal manera que la proteína
transportadora hace que la sustancia se mueva contra
un gradiente de energía, como desde un estado de baja
concentración a un estado de alta concentración. Este
movimiento precisa una fuente de energía adicional,
además de la energía cinética.
DIFUSIÓN
Todas las moléculas e iones de los líquidos corporales están en movimiento constante y de forma
completamente independiente. El movimiento de estas partículas es lo que los físicos llaman «calor»
(cuanto mayor sea el movimiento, mayor es la temperatura), y el movimiento nunca se interrumpe salvo a
la temperatura de cero absoluto.
Cuando una molécula en movimiento, A, se acerca a una molécula estacionaria, B, las fuerzas
electrostáticas y otras fuerzas nucleares de la molécula A rechazan a la molécula B, transfiriendo parte de
la energía del movimiento de la molécula A a la B. En consecuencia, la molécula B adquiere energía
cinética del movimiento, mientras que la molécula A se enlentece, perdiendo parte de su energía cinética.
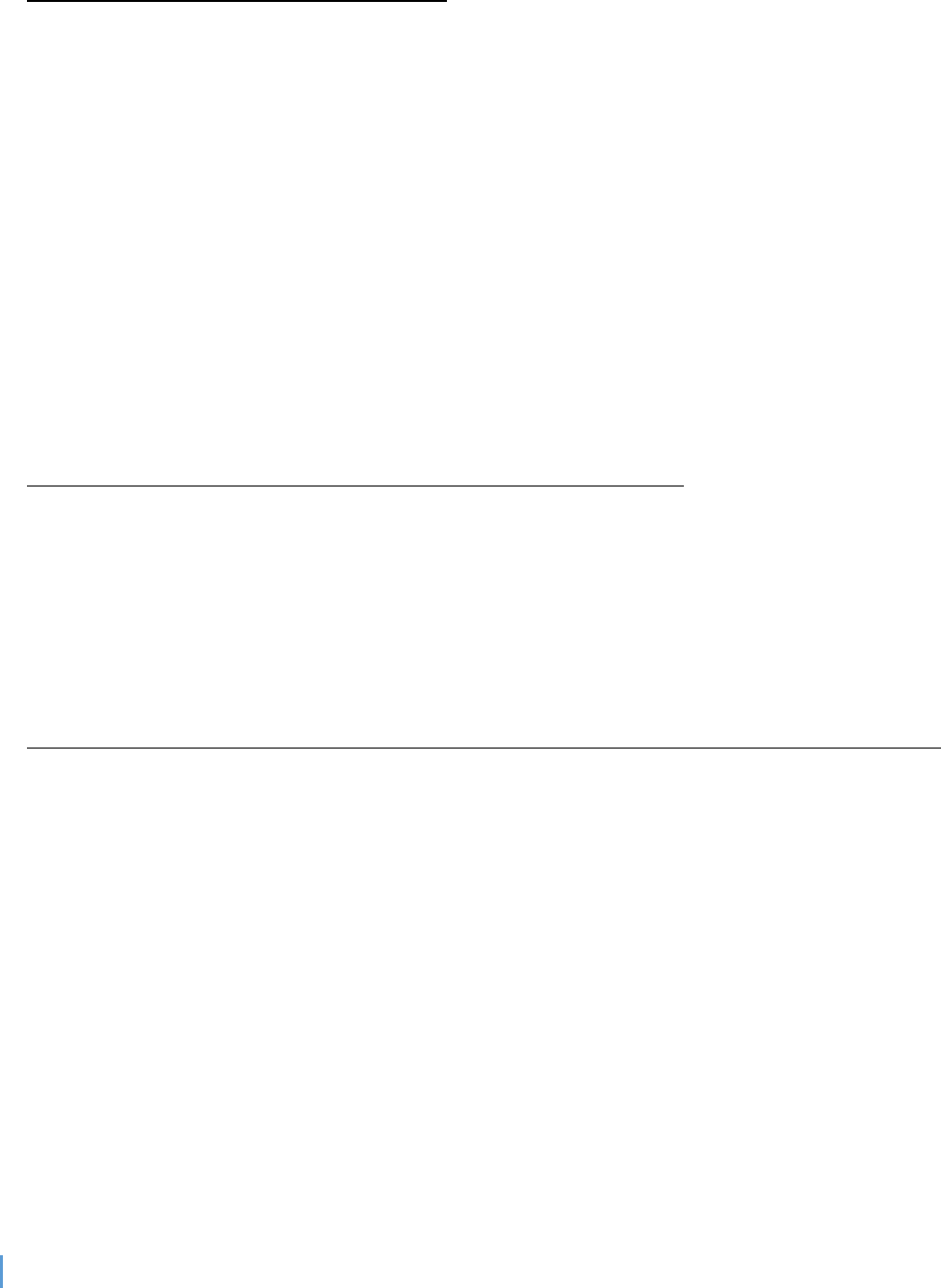
Fisiología Módulo 2- Capitulo 4
2
Una única molécula en una solución rebota entre las otras moléculas primero en una dirección, después
en otra, después en otra, y así sucesivamente, rebotando de manera aleatoria miles de veces por
segundo. Este movimiento continuo de moléculas entre sí en los líquidos o los gases se denomina
difusión.
Los iones difunden de la misma manera que las moléculas completas, e incluso partículas coloidales
suspendidas difunden de manera similar, excepto que los coloides difunden con mucha menos rapidez que
las sustancias moleculares debido a su mayor tamaño.
Difusión a través de la membrana celular
La difusión a través de la membrana celular se divide en dos subtipos, denominados difusión simple y
difusión facilitada.
Difusión simple significa que el movimiento cinético de las moléculas o de los iones se produce a través de
una abertura de la membrana o a través de espacios intermoleculares sin ninguna interacción con las
proteínas transportadoras de la membrana. La velocidad de difusión viene determinada por la cantidad de
sustancia disponible, la velocidad del movimiento cinético y el número y el tamaño de las aberturas de la
membrana a través de las cuales se pueden mover las moléculas o los iones.
La difusión facilitada precisa la interacción de una proteína transportadora. La proteína transportadora
ayuda al paso de las moléculas o de los iones a través de la membrana mediante su unión química con
estos y su desplazamiento a través de la membrana de esta manera.
Se puede producir difusión simple a través de la membrana celular por dos rutas:
1) a través de los intersticios de la bicapa lipídica si la sustancia que difunde es liposoluble, y
2) a través de canales acuosos que penetran en todo el grosor de la bicapa a través de las grandes
proteínas transportadoras.
Difusión de sustancias liposolubles a través de la bicapa lipídica
Un factor importante que determina la rapidez con la que una sustancia difunde a través de la bicapa
lipídica es la liposolubilidad. Por ejemplo, la liposolubilidad del oxígeno, del nitrógeno, del anhídrido
carbónico y de los alcoholes es elevada, de modo que todas estas sustancias pueden disolverse
directamente en la bicapa lipídica y pueden difundir a través de la membrana celular de la misma manera
que se produce difusión de solutos en agua en una solución acuosa. La velocidad de difusión de cada una
de estas sustancias a través de la membrana es directamente proporcional a su liposolubilidad. De esta
manera se pueden transportar cantidades especialmente grandes de oxígeno; por tanto, se puede liberar
oxígeno en el interior de la célula casi como si no existiera la membrana celular.
Difusión de agua y de otras moléculas insolubles en lípidos a través de canales proteicos
Aunque el agua es muy insoluble en los lípidos de la membrana, pasa rápidamente a través de los canales
de las moléculas proteicas que penetran en todo el espesor de la membrana. Muchas de las membranas
celulares del cuerpo contienen «poros» proteicos denominados acuaporinas que permiten selectivamente
el rápido paso de agua a través de la membrana celular. Las acuaporinas están muy especializadas, y
existen al menos 13 tipos diferentes en las diversas células de los mamíferos.
La rapidez con la que las moléculas de agua pueden difundir a través de la mayoría de las membranas
celulares es sorprendente. A modo de ejemplo, la cantidad total de agua que difunde en las dos
direcciones a través de la membrana del eritrocito durante cada segundo es 100 veces mayor que el
volumen del propio eritrocito.
Otras moléculas insolubles en lípidos pueden atravesar los canales de los poros proteicos de la misma
manera que las moléculas de agua si son hidrosolubles y de un tamaño lo suficientemente pequeño. Sin
embargo, a medida que se hacen mayores su penetración disminuye rápidamente. Por ejemplo, el
diámetro de la molécula de urea es solo un 20% mayor que la del agua, y a pesar de ello su penetración a
través de los poros de la membrana celular es aproximadamente 1.000 veces menor que la del agua. Aun
así, dada la sorprendente velocidad de penetración del agua, la magnitud de la penetración de la urea
sigue permitiendo el transporte rápido de la urea a través de la membrana en un plazo de minutos.
Fisiología Módulo 2- Capitulo 4
3
Difusión a través de poros y canales proteicos: permeabilidad selectiva y «activación» de canales
Las sustancias se pueden mover mediante difusión simple directamente a lo largo de trayectos tubulares
(poros) que se extienden desde el líquido extracelular hasta el intracelular, yendo desde un lado de la
membrana hasta el otro.
Los poros están compuestos por proteínas de membranas celulares integrales que forman tubos abiertos a
través de la membrana y que están siempre abiertos. Sin embargo, el diámetro de un poro y sus cargas
eléctricas proporcionan una selectividad que permite el paso de solo ciertas moléculas a su través. Por
ejemplo, los poros proteicos denominados acuaporinas o canales de agua permiten el rápido paso de agua
a través de las membranas celulares, pero impiden el de otras moléculas. En las distintas células del
cuerpo humano se han descubierto al menos 13 tipos diferentes de acuaporinas.
Las acuaporinas tienen un poro estrecho que permite que las moléculas de agua se difundan a través de
la membrana en una única fila. El poro es demasiado pequeño para permitir el paso de iones hidratados.
Los canales proteicos se distinguen por dos características importantes:
1) con frecuencia son permeables de manera selectiva a ciertas sustancias, y
2) muchos de los canales se pueden abrir o cerrar por compuertas que son reguladas por señales
eléctricas (canales activados por el voltaje) o sustancias químicas que se unen a las proteínas de canales
(canales activados por ligandos).
Permeabilidad selectiva de los canales proteicos
Muchos de los canales proteicos son muy selectivos para el transporte
de uno o más iones o moléculas específicos. Esta selectividad se debe a
las características del propio canal, como su diámetro, su forma y la
naturaleza de las cargas eléctricas y enlaces químicos que están
situados a lo largo de sus superficies internas.
Los canales de potasio permiten el paso de iones potasio a través de la
membrana celular con una facilidad aproximadamente 1.000 veces
mayor que para el paso de iones sodio. Este alto grado de selectividad
no puede explicarse completamente por los diámetros moleculares de
los iones, ya que los iones potasio son solo ligeramente mayores que los
de sodio.
Los canales de potasio tienen una estructura tetramérica consistente en
cuatro subunidades proteicas idénticas que rodean a un poro central. En
la parte superior del poro del canal se distribuyen bucles de poro que
forman un estrecho filtro de selectividad. Como revestimiento del filtro de
selectividad hay oxígenos de carbonilo.
Cuando los iones potasio hidratados entran en el filtro de selectividad, interaccionan con los oxígenos de
carbonilo y envuelven la mayoría de sus moléculas de agua ligadas, lo que permite que los iones potasio
deshidratados pasen a través del canal. Sin embargo, los oxígenos de carbonilo están demasiado
separados para permitir su interacción estrecha con los iones sodio, más pequeños, que de este modo son
excluidos en la práctica por el filtro de selectividad y no pueden pasar a través del poro.
Se cree que existen diferentes filtros de selectividad que determinan, en gran medida, la especificidad de
los diversos canales para cationes o aniones o para iones determinados, como sodio (Na+), potasio (K+) y
calcio (Ca++), que consiguen acceder a los canales.
Canal del sodio: mide solo de 0,3 a 0,5 nm de diámetro y sus superficies internas están revestidas con
aminoácidos que tienen una carga intensamente negativa, las cuales pueden arrastrar pequeños iones
sodio deshidratados hacia el interior de estos canales, realmente separando los iones sodio de las
moléculas de agua que los hidratan. Una vez que están en el canal, los iones sodio difunden en una u otra
dirección según las leyes habituales de la difusión. Así, el canal del sodio es altamente selectivo para el
paso de iones sodio.
Fisiología Módulo 2- Capitulo 4
4
Activación de los canales proteicos
Proporciona un medio para controlar la permeabilidad iónica de
los canales. Se piensa que algunas de las compuertas son
realmente extensiones similares a una compuerta de la
molécula de la proteína transportadora, que pueden cerrar la
abertura del canal o se pueden alejar de la apertura por un
cambio conformacional de la forma de la propia molécula
proteica.
La apertura y el cierre de las compuertas están controlados de
dos maneras principales:
1. Activación por el voltaje La conformación molecular de la
compuerta o de sus enlaces químicos responde al potencial
eléctrico que se establece a través de la membrana celular. Por
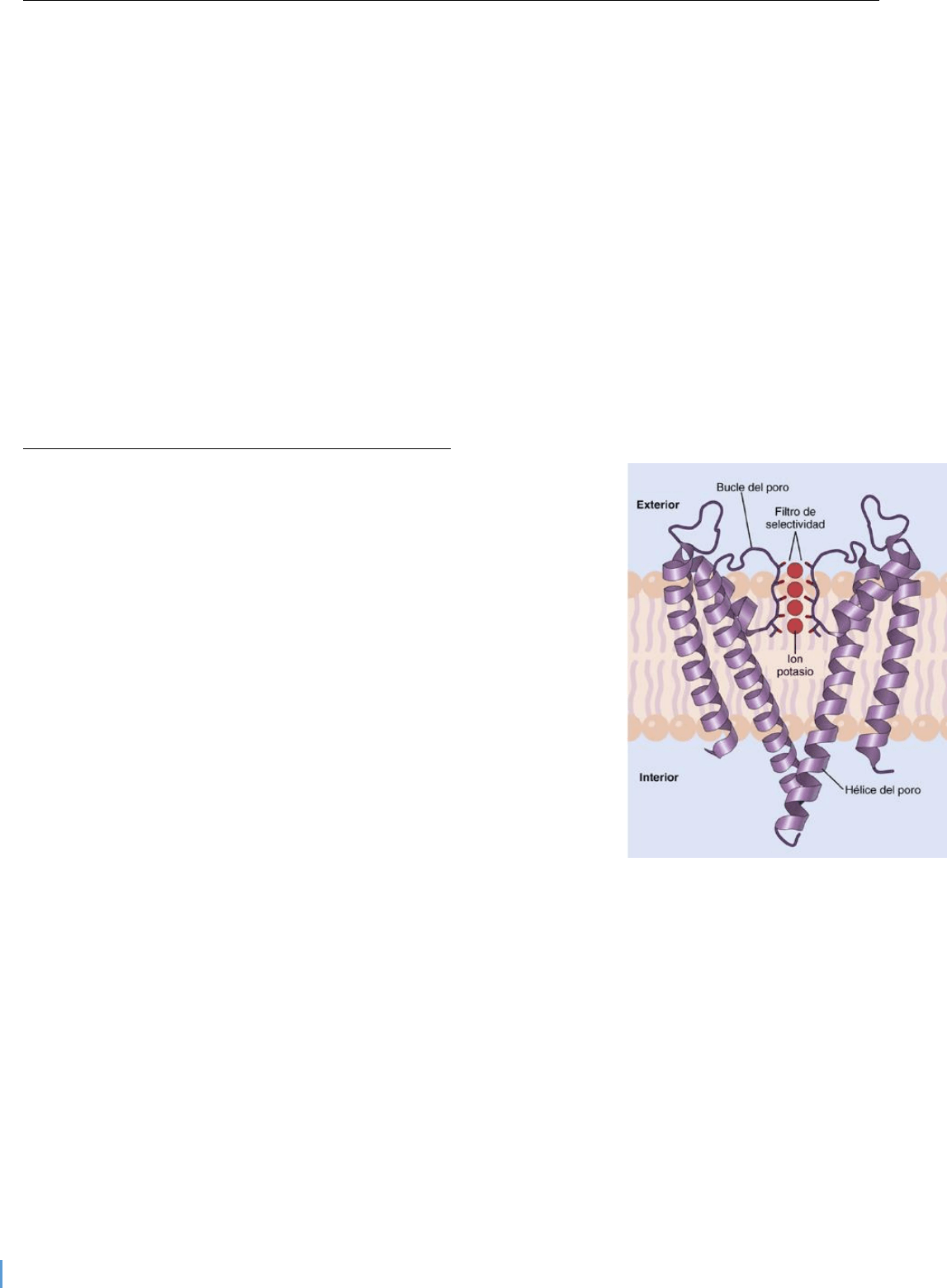
ejemplo, en la imagen superior de la figura 4-5, una carga
negativa intensa en el interior de la membrana celular podría hacer probablemente que las compuertas de
sodio del exterior permanezcan firmemente cerradas; por el contrario, cuando el interior de la membrana
pierde su carga negativa estas compuertas se abrirían súbitamente y permitirían que el sodio entrara a
través de los poros de sodio. Este proceso es el mecanismo básico para generar los potenciales de acción
nerviosos que son responsables de las señales nerviosas. En la imagen inferior de la figura 4-5 las
compuertas de potasio están en los extremos intracelulares de los canales de potasio, y se abren cuando
el interior de la membrana celular adquiere carga positiva. La apertura de estas compuertas es
responsable en parte de poner fin al potencial de acción.
2. Activación química (por ligando) Las compuertas de algunos canales proteicos se abren por la unión
de una sustancia química (un ligando) a la proteína, que produce un cambio conformacional o un cambio
de los enlaces químicos de la molécula de la proteína que abre o cierra la compuerta. Uno de los casos
más importantes de activación química es el efecto de la acetilcolina sobre el denominado canal de la
acetilcolina. La acetilcolina abre la compuerta de este canal, dando lugar a la apertura de un poro de carga
negativa de aproximadamente 0,65 nm de diámetro que permite que lo atraviesen moléculas sin carga o
iones positivos menores de este diámetro. Esta compuerta es muy importante para la transmisión de las
señales nerviosas desde una célula nerviosa a otra y desde las células nerviosas a las células musculares
para producir la contracción muscular.
Estado abierto frente a estado cerrado de los canales activados
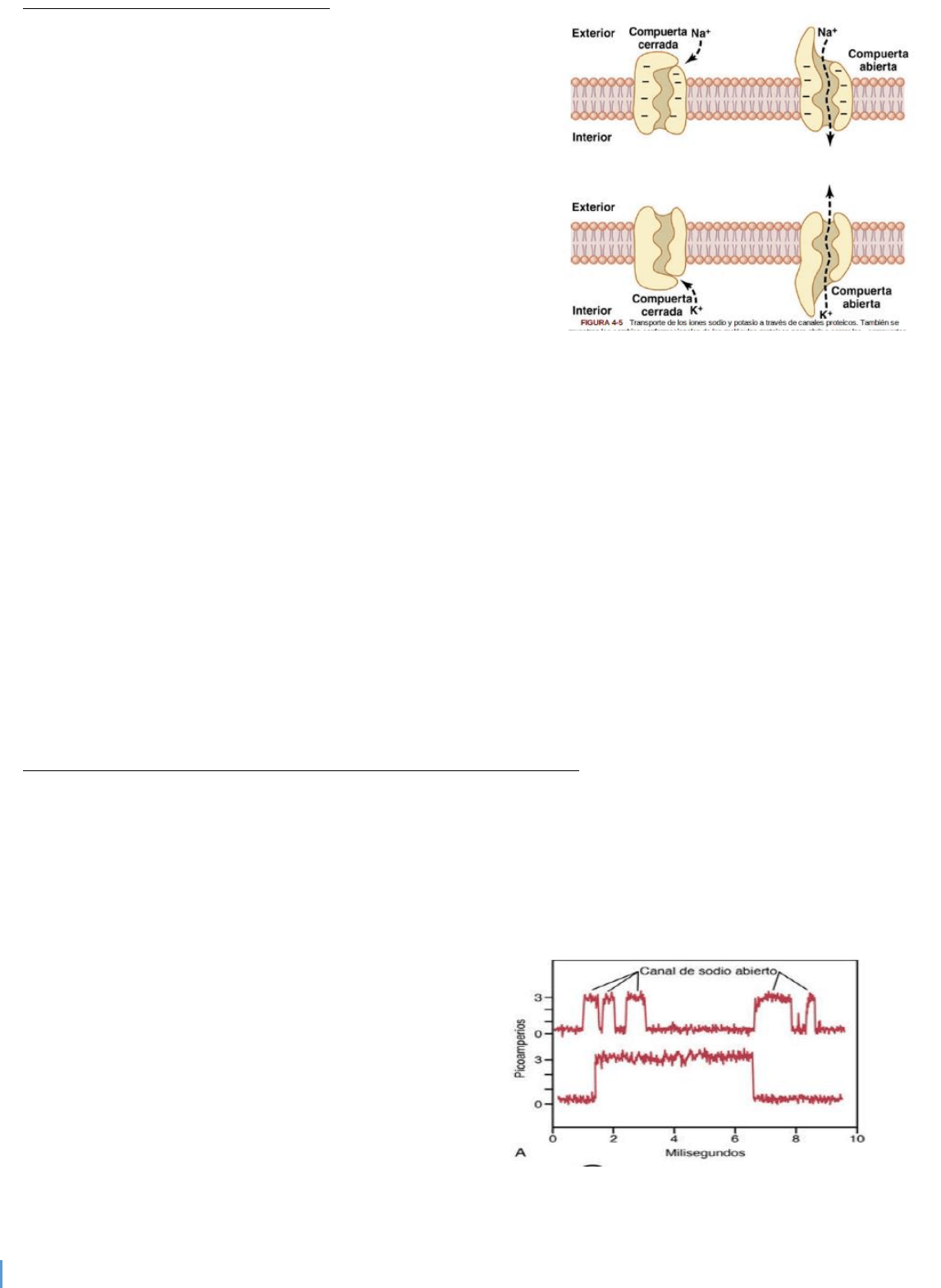
La figura 4-6A muestra una característica interesante de la mayoría de los canales activados por el voltaje.
Esta figura muestra los registros de la corriente eléctrica que fluye a través de un único canal de sodio
cuando hay un gradiente de potencial de aproximadamente 25 mV a través de la membrana. Obsérvese
que el canal conduce la corriente según un mecanismo de «todo o nada». Es decir, la compuerta del canal
se abre súbitamente y después se cierra súbitamente, de modo que cada estado abierto dura únicamente
desde una fracción de milisegundo hasta varios milisegundos, lo que demuestra la rapidez con la que se
producen los cambios durante la apertura y el cierre de las compuertas moleculares proteicas. A un
potencial de voltaje dado, el canal puede permanecer
cerrado todo o casi todo el tiempo, mientras que a otro
nivel de voltaje puede permanecer abierto todo o la mayor
parte del tiempo. A los voltajes intermedios, como se
muestra en la figura, las compuertas tienden a abrirse y
cerrarse súbitamente de manera intermitente, lo que da un
flujo medio de corriente que está en algún punto entre el
mínimo y el máximo.
Fisiología Módulo 2- Capitulo 4
5
La difusión facilitada necesita proteínas transportadoras de membrana
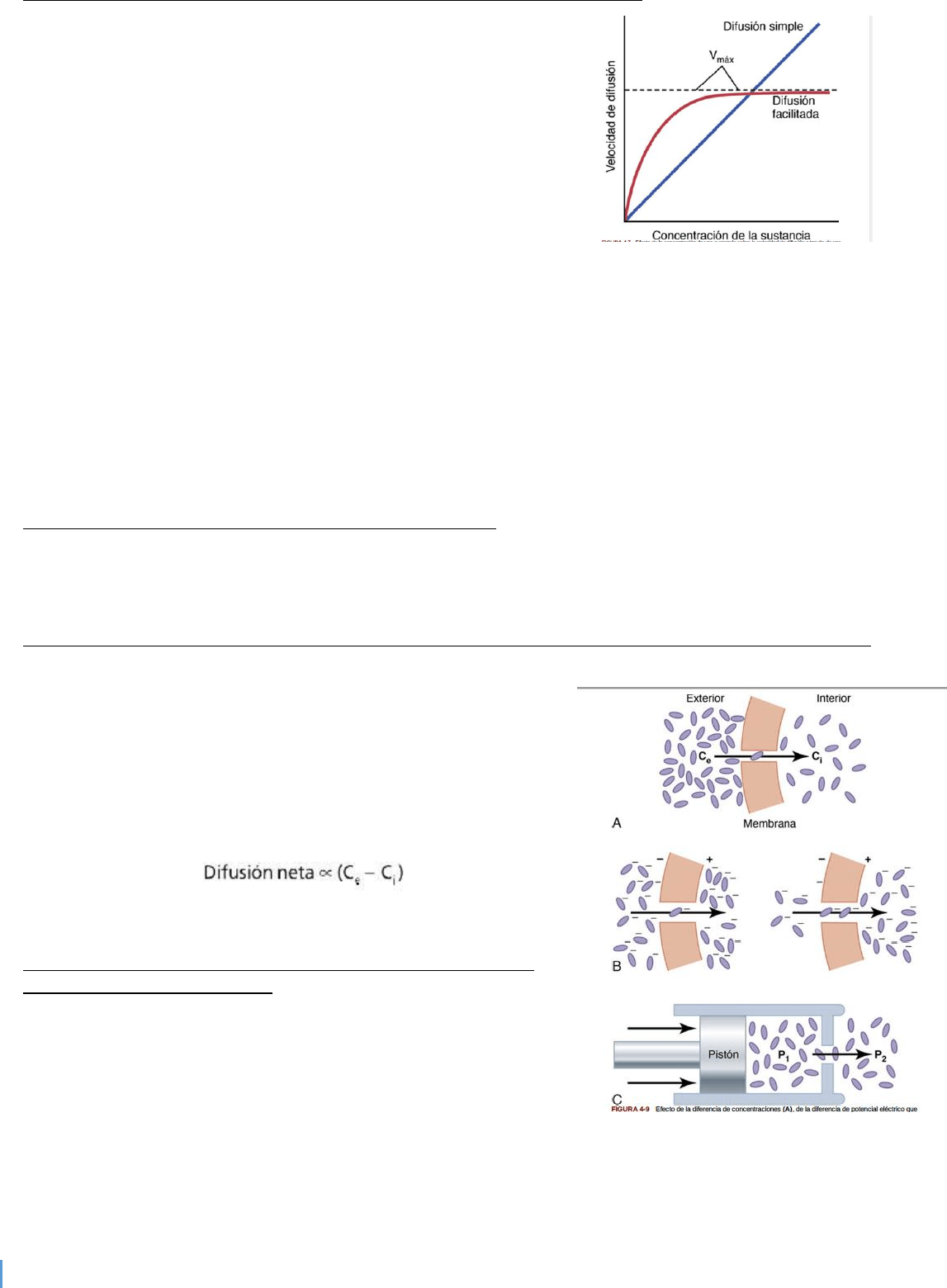
La difusión facilitada difiere de la difusión simple en la siguiente
característica importante: aunque la velocidad de la difusión simple
a través de un canal abierto aumenta de manera proporcional a la
concentración de la sustancia que difunde, en la difusión facilitada
la velocidad de difusión se acerca a un máximo, denominado Vmáx,
a medida que aumenta la concentración de la sustancia que
difunde.
A medida que aumenta la concentración de la sustancia que
difunde, la velocidad de la difusión simple sigue aumentando de
manera proporcional, aunque en el caso de la difusión facilitada la
velocidad de la difusión no puede aumentar por encima del nivel de la Vmáx.
La molécula que se va a transportar entra en el poro y queda unida. Después, en una fracción de segundo
se produce un cambio conformacional o químico en la proteína transportadora, de modo que el poro ahora
se abre en el lado opuesto de la membrana. Como la fuerza de unión del receptor es débil, el movimiento
térmico de la molécula unida hace que se separe y que se libere en el lado opuesto de la membrana. La
velocidad a la que se pueden transportar moléculas por este mecanismo nunca puede ser mayor que la
velocidad a la que la molécula proteica transportadora puede experimentar el cambio en un sentido y en
otro entre sus dos estados. Sin embargo, se debe señalar de manera específica que este mecanismo
permite que la molécula transportada se mueva (es decir, que «difunda») en ambas direcciones a través
de la membrana.
Factores que influyen en la velocidad neta de difusión
Hasta ahora es evidente que muchas sustancias pueden difundir a través de la membrana celular. Lo que
habitualmente es importante es la velocidad neta de difusión de una sustancia en la dirección deseada.
Esta velocidad neta está determinada por varios factores.
La velocidad neta de difusión es proporcional a la diferencia de concentración a través de una membrana
La velocidad a la que la sustancia difunde hacia dentro es proporcional a la concentración de las
moléculas en el exterior, porque esta concentración determina
cuántas moléculas chocan contra el exterior de la membrana cada
segundo. Por el contrario, la velocidad a la que las moléculas
difunden hacia afuera es proporcional a su concentración en el
interior de la membrana. Por tanto, la velocidad de difusión neta
hacia el interior de la célula es proporcional a la concentración en
el exterior menos la concentración en el interior, o:
donde Ce es la concentración en el exterior y Ci es la
concentración en el interior.
Efecto del potencial eléctrico de membrana sobre la difusión de
iones: el «potencial de Nernst»
Si se aplica un potencial eléctrico a través de la membrana las
cargas eléctricas de los iones hacen que se muevan a través de la
membrana aun cuando no haya ninguna diferencia de
concentración que produzca el movimiento. Así la concentración
de iones negativos es la misma a los dos lados de la membrana,
aunque se ha aplicado una carga positiva al lado derecho de la membrana y una carga negativa al
izquierdo, creando un gradiente eléctrico a través de esta. La carga positiva atrae los iones negativos,
mientras que la carga negativa los repele. Por tanto, se produce difusión neta desde la izquierda hacia la
derecha.
Fisiología Módulo 2- Capitulo 4
6
Después de un cierto tiempo se han movido grandes cantidades de iones negativos hacia la derecha,
creando la situación en el que se ha producido una diferencia de concentración de los iones en la dirección
contraria a la diferencia de potencial eléctrico. La diferencia de concentración ahora tiende a mover los
iones hacia la izquierda, mientras que la diferencia eléctrica tiende a moverlos hacia la derecha. Cuando la
diferencia de concentración se hace lo suficientemente elevada, los dos efectos se contrarrestan entre sí.
A la temperatura corporal normal (37 °C), la diferencia eléctrica que permitirá que se alcance el equilibrio
entre una diferencia de concentración dada de iones univalentes, como los iones Na+, se puede
determinar a partir de la fórmula siguiente, que se denomina ecuación de Nernst:
donde FEM es la fuerza electromotriz (voltaje) entre el lado 1 y el lado 2 de la membrana, C1 es la
concentración en el lado 1 y C2 es la concentración en el lado 2. Esta ecuación es muy importante para
comprender la transmisión de los impulsos nerviosos.
Efecto de una diferencia de presión a través de la membrana
En ocasiones se produce una gran diferencia de presión entre los dos lados de una membrana permeable.
Esta diferencia de presión se produce, por ejemplo, en la membrana capilar sanguínea de todos los tejidos
del cuerpo. La presión es aproximadamente 20 mmHg mayor en el interior del capilar que en el exterior.
La presión realmente significa la suma de todas las fuerzas de las diferentes moléculas que chocan contra
una unidad de superficie en un momento dado. Por tanto, al tener una presión mayor en un lado de la
membrana que en el otro, la suma de todas las fuerzas de las moléculas que chocan con los canales de
ese lado de la membrana es mayor que en el otro lado. En la mayor parte de los casos esta situación se
debe a que hay un mayor número de moléculas que choca cada segundo contra la membrana en un lado
que contra la del otro lado. La consecuencia es que se dispone de mayores cantidades de energía para
producir el movimiento neto de moléculas desde el lado de presión elevada hacia el lado de presión baja.
Ósmosis a través de membranas con permeabilidad selectiva: «difusión neta» de agua
Con mucho, la sustancia más abundante que difunde a través de la membrana celular es el agua. Cada
segundo difunde normalmente una cantidad suficiente de agua en ambas direcciones a través de la
membrana del eritrocito igual a aproximadamente 100 veces el volumen de la propia célula. Sin embargo,
normalmente la cantidad que difunde en ambas direcciones está equilibrada de manera tan precisa que se
produce un movimiento neto cero de agua. Por tanto, el volumen celular permanece constante. Sin
embargo, en ciertas condiciones se puede producir una diferencia de concentración del agua a través de la
membrana. Cuando se produce esto, tiene lugar un movimiento neto de agua a través de la membrana
celular, haciendo que la célula se hinche o que se contraiga, dependiendo de la dirección del movimiento
del agua. Este proceso de movimiento neto del agua que se debe a la producción de una diferencia de la
concentración del agua se denomina ósmosis.
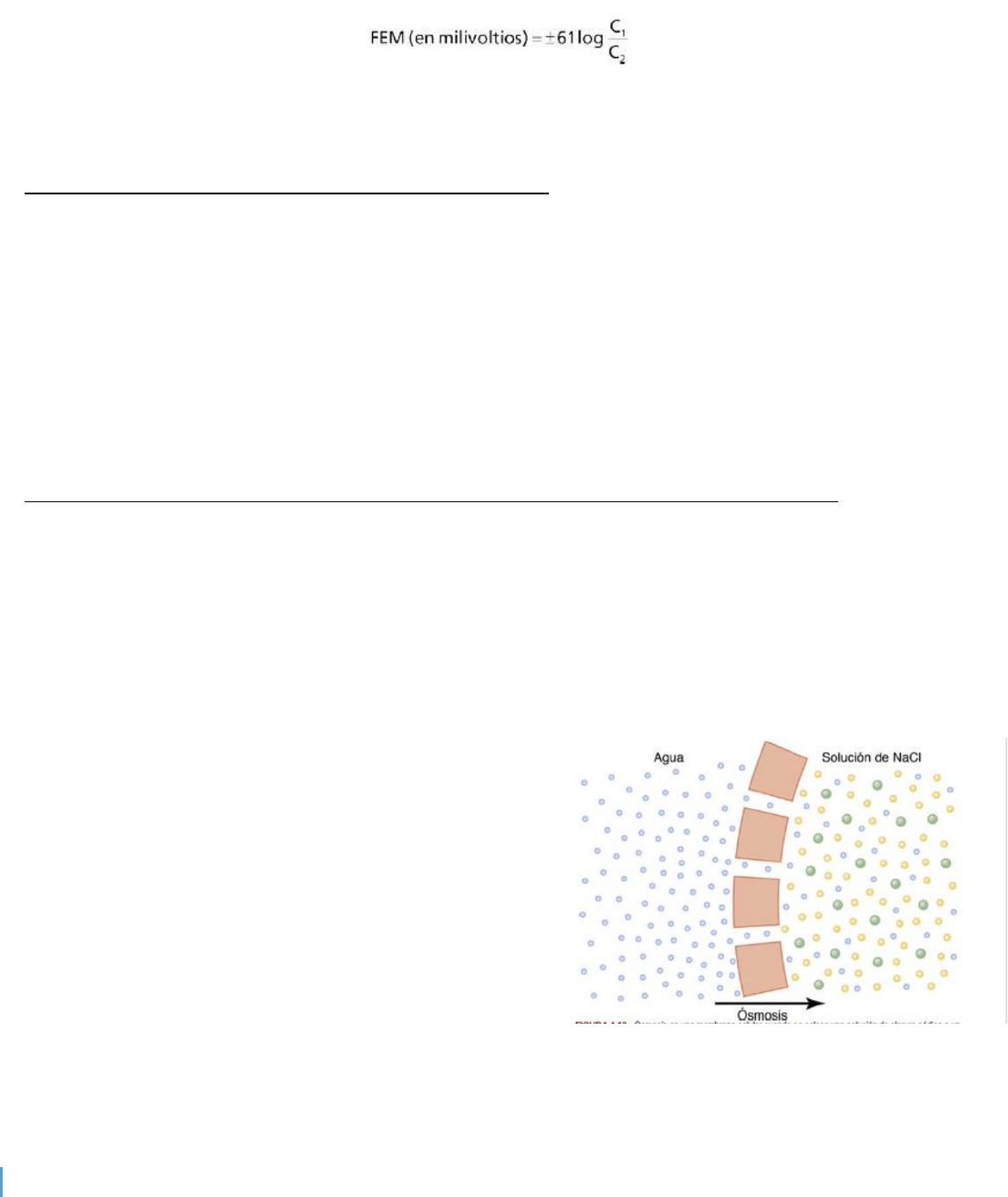
Las moléculas de agua atraviesan la membrana celular
con facilidad, mientras que los iones sodio y cloruro
pasan solo con dificultad. Por tanto, la solución de cloruro
sódico es realmente una mezcla de moléculas de agua
difusibles y de iones sodio y cloruro no difusibles, y se
dice que la membrana es permeable de manera selectiva
al agua, pero mucho menos a los iones sodio y cloruro.
Sin embargo, la presencia del sodio y del cloruro ha
desplazado parte de las moléculas de agua del lado de la
membrana en el que están presentes estos iones y, por
tanto, ha reducido la concentración de moléculas de agua
a una concentración menor que la del agua pura. En consecuencia, en el ejemplo de la figura 4-10, más
moléculas de agua chocan contra los canales del lado izquierdo, en el que hay agua pura, que, en el lado
derecho, en el que se ha reducido la concentración de agua. Así, se produce un movimiento neto de agua
desde la izquierda hacia la derecha, es decir, se produce ósmosis desde el agua pura hacia la solución de
cloruro sódico.

Fisiología Módulo 2- Capitulo 4
7
Presión osmótica
Si se aplicara presión a la solución de cloruro sódico, la ósmosis de
agua hacia esta solución se enlentecería, se interrumpiría o incluso
se invertiría. La cantidad de presión necesaria para detener la
ósmosis se denomina presión osmótica de la solución de cloruro
sódico.
El principio de una diferencia de presión que se opone a la ósmosis
se ilustra en la figura 4-11, que muestra una membrana con
permeabilidad selectiva que separa dos columnas de líquido, una
que contiene agua pura y otra que contiene una solución de agua y
de cualquier soluto que no penetra en la membrana.
La ósmosis de agua desde la cámara B hacia la cámara A hace que
los niveles de las columnas de líquido se separen cada vez más,
hasta que finalmente se produzca una diferencia de presión entre los
dos lados de la membrana que sea lo suficientemente grande como
para oponerse al efecto osmótico. Esta diferencia de presión a través de la membrana en este punto es
igual a la presión osmótica de la solución que contiene el soluto no difusible.
Importancia del número de partículas osmóticas (concentración molar) en la determinación de la presión
osmótica
La presión osmótica que ejercen las partículas de una solución, ya sean moléculas o iones, está
determinada por el número de partículas por unidad de volumen del líquido, no por la masa de las
partículas. La razón de esto es que todas las partículas de una solución, independientemente de su masa,
ejercen, en promedio, la misma cantidad de presión contra la membrana. Es decir, las partículas grandes,
que tienen una masa (m) mayor que las partículas pequeñas, se mueven a velocidades (v) más lentas. Las
partículas pequeñas se mueven a mayores velocidades, de modo que sus energías cinéticas medias (c),
determinadas por la ecuación son las mismas para las partículas pequeñas que para las partículas
grandes.
En consecuencia, el factor que determina la presión osmótica de una solución es la concentración de la
solución en función del número de partículas (que es lo mismo que la concentración molar si es una
molécula no disociada), no en función de la masa del soluto.
«Osmolalidad»: el osmol
Para expresar la concentración de una solución en función del número de partículas se utiliza la unidad
denominada osmol en lugar de los gramos.
Así, se dice que una solución que tiene 1 osmol de soluto disuelto por cada kilogramo de agua tiene una
osmolalidad de 1 osmol por kilogramo, y una solución que tiene 1/1.000 osmoles disueltos por kilogramo
tiene una osmolalidad de 1 mosmol por kilogramo. La osmolaridad normal de los líquidos extracelular e
intracelular es de aproximadamente 300 mosmol por kilogramo de agua.
Un osmol es el peso molecular-gramo de un soluto osmóticamente activo. Por tanto, 180 g de glucosa, que es el
peso molecular-gramos de la glucosa, son equivalentes a un osmol de glucosa porque la glucosa no se disocia en
iones. Si un soluto se disocia en dos iones, un peso molecular gramo del soluto se convertirá en dos osmoles porque
el número de partículas osmóticamente activas es ahora el doble que en el caso del soluto no disociado. Por tanto,
cuando está totalmente disociado, un peso molecular-gramo de cloruro sódico, 58,5 g, es igual a dos osmoles.

Fisiología Módulo 2- Capitulo 4
8
Relación entre osmolalidad y presión osmótica
A la temperatura corporal normal, 37 °C, una concentración de un osmol por litro producirá una presión
osmótica de 19.300 mmHg en la solución. De la misma manera, una concentración de 1 mosmol por litro
es equivalente a una presión osmótica de 19,3 mmHg. La multiplicación de este valor por la concentración
300 miliosmolar de los líquidos corporales da una presión osmótica calculada total de los líquidos
corporales de 5.790 mmHg. Sin embargo, el valor medio de esta variable es en promedio de solo
aproximadamente 5.500 mmHg. La causa de esta diferencia es que muchos de los iones de los líquidos
corporales, como los iones sodio y cloruro, están muy atraídos entre sí; en consecuencia, no se pueden
mover totalmente sin restricciones en los líquidos y generar todo su potencial de presión osmótica. Por
tanto, en promedio la presión osmótica real de los líquidos corporales es de aproximadamente 0,93 veces
el valor calculado.
Aunque en sentido estricto son los osmoles por kilogramo de agua (osmolalidad) los que determinan la
presión osmótica, para las soluciones diluidas como las que se encuentran en el cuerpo las diferencias
cuantitativas entre la osmolaridad y la osmolalidad son menores del 1%. Como es mucho más práctico
medir la osmolaridad que la osmolalidad, esta es la práctica habitual en casi todos los estudios fisiológicos.
«Transporte activo» de sustancias a través de las membranas
En ocasiones es necesaria una gran concentración de una sustancia en el líquido intracelular aun cuando
el líquido extracelular contenga solo una pequeña concentración. Esta situación tiene lugar, por ejemplo,
para los iones potasio.
Por el contrario, es muy importante mantener las concentraciones de otros iones bajas en el interior de la
célula, aunque su concentración en el líquido extracelular sea elevada. Así sucede especialmente para los
iones sodio. Ninguno de estos dos efectos podría producirse por difusión simple, porque la difusión simple
finalmente equilibra las concentraciones a ambos lados de la membrana.
Por el contrario, alguna fuente de energía debe producir un movimiento excesivo de iones potasio hacia el
interior de las células y un movimiento excesivo de iones sodio hacia el exterior de las células. Cuando una
membrana celular transporta moléculas o iones «contra corriente» contra un gradiente de concentración (o
«contra corriente» contra un gradiente eléctrico o de presión), el proceso se denomina transporte activo.
Diferentes sustancias que se transportan activamente a través de al menos algunas membranas celulares
incluyen los iones sodio, potasio, calcio, hierro, hidrógeno, cloruro, yoduro y urato, diversos azúcares
diferentes y la mayoría de los aminoácidos.
Transporte activo primario y transporte activo secundario
El transporte activo se divide en dos tipos según el origen de la energía que se utiliza para facilitar el
transporte: transporte activo primario y transporte activo secundario.
Transporte activo primario
Transporte activo secundario
La energía procede directamente de la
escisión del trifosfato de adenosina (ATP) o de
algún otro compuesto de fosfato de alta
energía.
La energía procede secundariamente de la energía
que se ha almacenado en forma de diferencias de
concentración iónica de sustancias moleculares o
iónicas secundarias entre los dos lados de una
membrana celular, que se generó originalmente
mediante transporte activo primario.
En ambos casos el transporte depende de proteínas transportadoras que penetran a través de la
membrana celular, al igual que en la difusión facilitada. Sin embargo, en el transporte activo la proteína
transportadora funciona de manera diferente al transportador de la difusión facilitada porque es capaz de
impartir energía a la sustancia transportada para moverla contra el gradiente electroquímico.
Osmolaridad es la concentración osmolar expresada en osmoles por litro de solución en lugar de
osmoles por kilogramo de agua.
Fisiología Módulo 2- Capitulo 4
9
Transporte activo primario
La bomba sodio-potasio transporta iones sodio hacia el exterior de las células e iones potasio hacia el
interior.
Entre las sustancias que se transportan mediante transporte activo primario están el sodio, el potasio, el
calcio, el hidrógeno, el cloruro y algunos otros iones.
El mecanismo de transporte activo que se ha estudiado con mayor detalle es la bomba sodio-potasio (Na+-
K+), que es el proceso de transporte que bombea iones sodio hacia fuera a través de la membrana celular
de todas las células y al mismo tiempo bombea iones potasio desde el exterior hacia el interior. Esta
bomba es responsable de mantener las diferencias de concentración de sodio y de potasio a través de la
membrana celular, así como de establecer un voltaje eléctrico negativo en el interior de las células. De
hecho, esta bomba también es la base de la función nerviosa, porque permite transmitir las señales
nerviosas por todo el sistema nervioso.
La proteína transportadora es un complejo formado por dos proteínas globulares distintas: una de mayor
tamaño denominada subunidad α, que tiene un peso molecular de aproximadamente 100.000, y una más
pequeña denominada subunidad β, que tiene un peso molecular de aproximadamente 55.000. Aunque se
desconoce la función de la proteína de menor tamaño (excepto que podría anclar el complejo proteico a la
membrana lipídica), la proteína de mayor tamaño tiene tres características específicas que son
importantes para el funcionamiento de la bomba:
1. Tiene tres puntos receptores para la unión de iones sodio en la porción de la proteína que protruye
hacia el interior de la célula.
2. Tiene dos puntos receptores para iones potasio en el exterior.
3. La porción interior de esta proteína cerca de los puntos de unión al sodio tiene actividad adenosina
trifosfatasa (ATPasa).
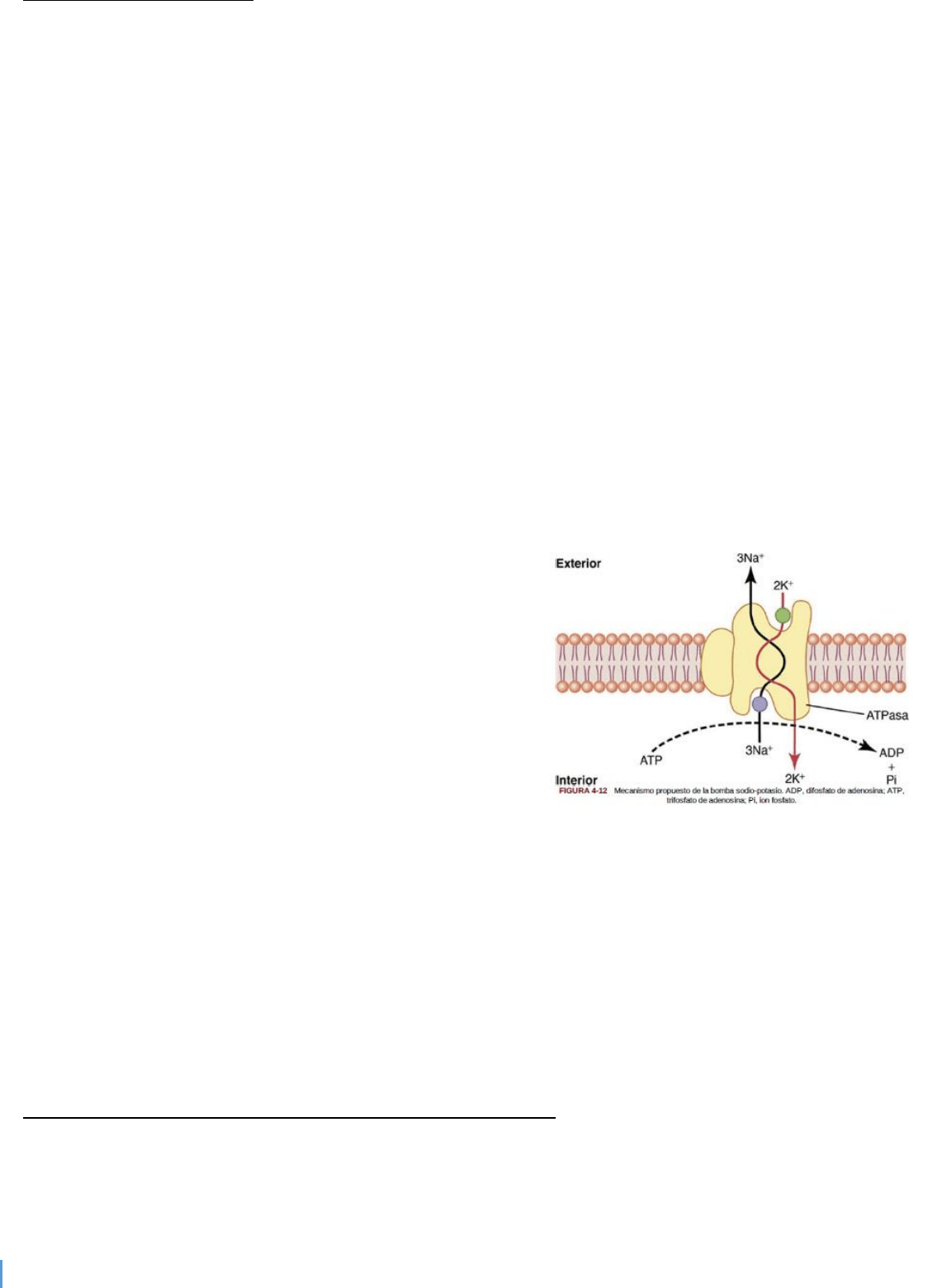
Cuando dos iones potasio se unen al exterior de la proteína
transportadora y tres iones sodio se unen al interior se
activa la función ATPasa de la proteína. La activación de la
función ATPasa conduce a una escisión de una molécula de
ATP, que se divide en difosfato de adenosina (ADP) y libera
un enlace de energía de fosfato de alta energía. Se piensa
que esta energía liberada produce un cambio químico y
conformacional en la molécula transportadora proteica,
transportando los tres iones sodio hacia el exterior y los dos
iones potasio hacia el interior.
Como en el caso de otras enzimas, la bomba Na+-K+-
ATPasa puede funcionar a la inversa. Si se aumentan experimentalmente los gradientes electroquímicos
de Na+ y de K+ en grado suficiente para que la energía que se almacena en sus gradientes sea mayor
que la energía química de la hidrólisis del ATP, estos iones se desplazarán según sus gradientes de
concentración y la bomba Na+-K+ sintetizará ATP a partir de ADP y fosfato.
Por tanto, la forma fosforilada de la bomba Na+-K+ puede donar su fosfato al ADP para producir fosfato o
puede utilizar la energía para modificar su conformación y bombear Na+ fuera de la célula y K+ hacia el
interior de la célula. Las concentraciones relativas de ATP, ADP y fosfato, así como los gradientes
electroquímicos de Na+ y K+, determinan la dirección de la reacción enzimática.
En algunas células, como las células nerviosas eléctricamente activas, el 60- 70% de las necesidades de
energía de las células puede estar dedicado a bombear Na+ fuera de la célula y K+ hacia el interior de la
célula.
La bomba Na+-K+ es importante para controlar el volumen celular
Sin la función de esta bomba la mayoría de las células del cuerpo se hincharían hasta explotar.
El mecanismo para controlar el volumen es el siguiente: en el interior de la célula hay grandes cantidades
de proteínas y de otras moléculas orgánicas que no pueden escapar de la célula. La mayoría de estas
proteínas y otras moléculas orgánicas tienen carga negativa y, por tanto, atraen grandes cantidades de

Fisiología Módulo 2- Capitulo 4
10
potasio, sodio y también de otros iones positivos. Todas estas moléculas e iones producen ósmosis de
agua hacia el interior de la célula. Salvo que este proceso se detenga, la célula se hinchará
indefinidamente hasta que explote. El mecanismo normal para impedir este resultado es la bomba Na+-K+.
Obsérvese de nuevo que este dispositivo bombea tres iones Na+ hacia el exterior de la célula por cada
dos iones K+ que bombea hacia el interior. Además, la membrana es mucho menos permeable a los iones
sodio que a los iones potasio, de modo que una vez que los iones sodio están en el exterior tienen una
intensa tendencia a permanecer ahí. Así, este proceso representa una pérdida neta de iones hacia el
exterior de la célula, lo que inicia también la ósmosis de agua hacia el exterior de la célula.
Si una célula comienza a hincharse por cualquier motivo, la bomba Na+-K+ se activa automáticamente,
moviendo aún más iones hacia el exterior y transportando agua con ellos. Por tanto, la bomba Na+-K+
realiza una función continua de vigilancia para mantener el volumen celular normal.
Transporte activo primario de iones calcio
Otro mecanismo importante de transporte activo primario es la bomba de calcio. Los iones calcio
normalmente se mantienen a una concentración muy baja en el citosol intracelular de prácticamente todas
las células del cuerpo, a una concentración aproximadamente 10.000 veces menor que en el líquido
extracelular.
Este nivel de mantenimiento se consigue principalmente mediante dos bombas de calcio que funcionan
mediante transporte activo primario. Una de ellas, que está en la membrana celular, bombea calcio hacia
el exterior de la célula. La otra bombea iones calcio hacia uno o más de los orgánulos vesiculares
intracelulares de la célula, como el retículo sarcoplásmico de las células musculares y las mitocondrias en
todas las células. En todos estos casos la proteína transportadora penetra en la membrana y actúa como
una enzima ATPasa, con la misma capacidad de escindir el ATP que la ATPasa de la proteína
transportadora de sodio. La diferencia es que esta proteína tiene un punto de unión muy específico para el
calcio en lugar de para el sodio.
Transporte activo primario de iones hidrógeno
El transporte activo primario de los iones hidrógeno es importante en dos localizaciones del cuerpo:
1) en las glándulas gástricas del estómago, y
2) en la porción distal de los túbulos distales y en los conductos colectores corticales de los riñones.
En las glándulas gástricas, las células parietales que están en las capas profundas tienen el mecanismo
activo primario más potente de transporte de iones hidrógeno de todo el cuerpo. Este mecanismo es la
base para secretar ácido clorhídrico en las secreciones digestivas del estómago. En el extremo secretor de
las células parietales de las glándulas gástricas la concentración del ion hidrógeno aumenta hasta un
millón de veces y después se libera hacia el estómago junto con iones cloruro para formar ácido
clorhídrico.
En los túbulos renales hay células intercaladas especiales en la porción distal de los túbulos distales y en
los conductos colectores, que también transportan iones hidrógeno mediante transporte activo primario. En
este caso se secretan grandes cantidades de iones hidrógeno desde la sangre hacia la orina con el
objetivo de eliminar de los líquidos corporales el exceso de iones hidrógeno. Los iones hidrógeno se
pueden segregar hacia la orina contra un gradiente de concentración de aproximadamente 900 veces.
Energética del transporte activo primario
La cantidad de energía necesaria para transportar activamente una sustancia a través de una membrana
viene determinada por cuánto se concentra la sustancia durante el transporte. En comparación con la
energía necesaria para concentrar 10 veces una sustancia, concentrarla 100 veces precisa el doble de
energía, y concentrarla 1.000 veces precisa el triple de energía. En otras palabras, la energía necesaria es
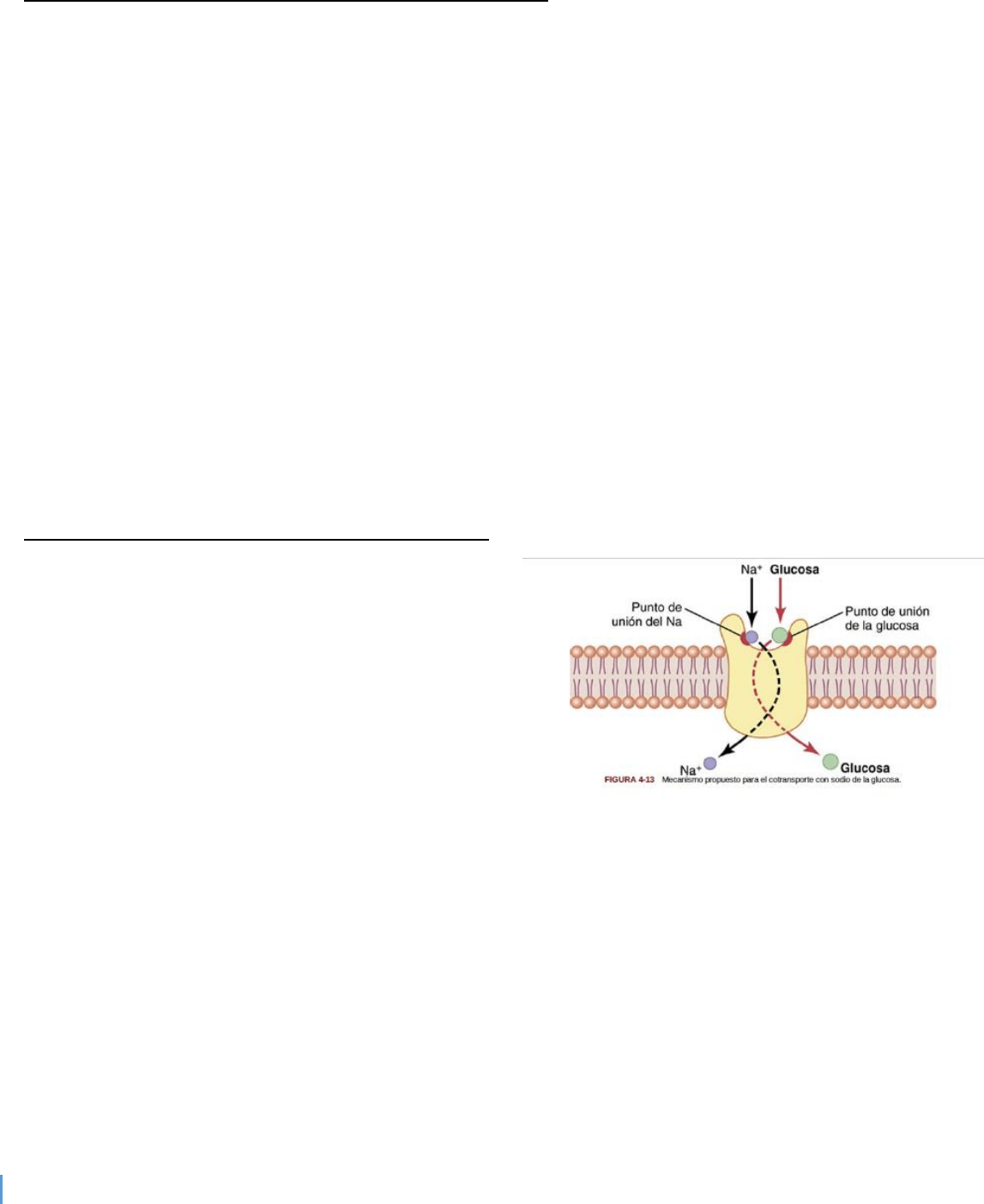
proporcionar al logaritmo del grado en que se concentra la sustancia, según se expresa con la fórmula
siguiente:
Fisiología Módulo 2- Capitulo 4
11
Así, expresado en calorías, la cantidad de energía necesaria para concentrar 10 veces un osmol de una sustancia es
de aproximadamente 1.400 calorías, mientras que para concentrarla 100 veces se necesitan 2.800 calorías. Se puede
ver que el gasto energético para concentrar las sustancias en las células o para eliminar sustancias de las células
contra un gradiente de concentración puede ser muy grande. Algunas células, como las que tapizan los túbulos
renales y muchas células glandulares, gastan hasta el 90% de su energía solo con esta finalidad.
Transporte activo secundario: cotransporte y contratransporte
Cuando los iones sodio se transportan hacia el exterior de las células mediante transporte activo primario
habitualmente se establece un gran gradiente de concentración de iones sodio a través de la membrana celular, con
una concentración elevada fuera de la célula y una concentración baja en su interior. Este gradiente representa un
almacén de energía porque el exceso de sodio en el exterior de la membrana celular siempre intenta difundir hacia
el interior. En condiciones adecuadas esta energía de difusión del sodio puede arrastrar otras sustancias junto con el
sodio a través de la membrana celular. Este fenómeno, denominado cotransporte, es una forma de transporte activo
secundario.
Para que el sodio arrastre otra sustancia con él es necesario un mecanismo de acoplamiento, lo cual se consigue por
medio de otra proteína transportadora de la membrana celular. En este caso el transportador actúa como punto de
unión tanto para el ion sodio como para la sustancia que se va a cotransportar. Una vez que los dos están unidos, el
gradiente de energía del ion sodio hace que este ion y la otra sustancia sean transportados juntos hacia el interior de
la célula.
En el contratransporte, los iones sodio intentan una vez más difundir hacia el interior de la célula debido a su gran
gradiente de concentración. Sin embargo, esta vez la sustancia que se va a transportar está en el interior de la célula
y se debe transportar hacia el exterior. Por tanto, el ion sodio se une a la proteína transportadora en el punto en el
que se proyecta hacia la superficie exterior de la membrana, mientras que la sustancia que se va a contratransportar
se une a la proyección interior de la proteína transportadora. Una vez que ambos se han unido se produce un
cambio conformacional y la energía liberada por la acción del ion sodio que se mueve hacia el interior hace que la
otra sustancia se mueva hacia el exterior.
Cotransporte de glucosa y aminoácidos junto con iones sodio
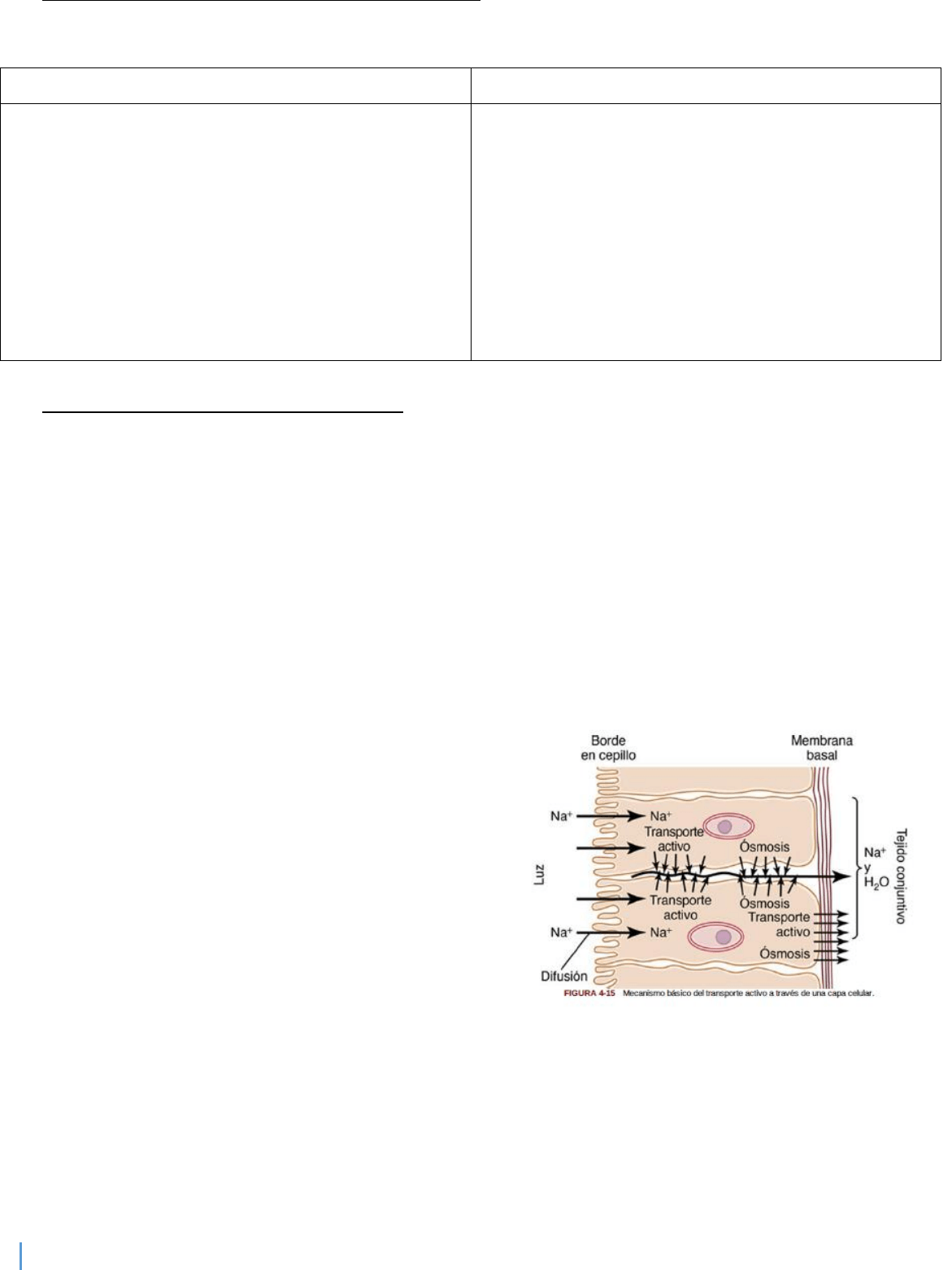
La glucosa y muchos aminoácidos se transportan hacia el
interior de la mayor parte de las células contra grandes
gradientes de concentración; el mecanismo de esta acción es
totalmente mediante cotransporte. Se debe observar que la
proteína transportadora tiene dos puntos de unión en su cara
externa, uno para el sodio y otro para la glucosa. Además, la
concentración de los iones sodio es alta en el exterior y baja
en el interior, lo que suministra la energía para el transporte.
Una propiedad especial de la proteína transportadora es que
no se producirá un cambio conformacional que permita el
movimiento de sodio hacia el interior hasta que también una molécula de glucosa se una. Cuando ambos están
unidos se produce el cambio conformacional y el sodio y la glucosa son transportados al mismo tiempo hacia el
interior de la célula. Por tanto, este es un mecanismo de cotransporte sodio-glucosa.
El cotransporte con sodio de los aminoácidos se produce de la misma manera que para la glucosa, excepto porque
utiliza un grupo diferente de proteínas transportadoras. Se han identificado al menos cinco proteínas
transportadoras de aminoácidos, cada una de las cuales es responsable de transportar un grupo de aminoácidos con
características moleculares específicas.
El cotransporte con sodio de la glucosa y de los aminoácidos se produce especialmente a través de las células
epiteliales del tubo digestivo y de los túbulos renales para favorecer la absorción de estas sustancias hacia la sangre.
Este proceso se analizará en capítulos posteriores. Otros mecanismos importantes de cotransporte al menos en
algunas células incluyen cotransporte de iones cloruro, yoduro, hierro y urato.
Fisiología Módulo 2- Capitulo 4
12
Contratransporte con sodio de iones calcio e hidrógeno
Dos mecanismos de contratransporte (p. ej., transporte en una dirección opuesta al ion primario)
especialmente importantes son el contratransporte sodio-calcio y el contratransporte sodiohidrógeno.
Contratransporte sodio-calcio
Contratransporte sodio-hidrógeno
Se produce a través de todas o casi todas las membranas
celulares, de modo que los iones sodio se mueven hacia
el interior y los iones calcio hacia el exterior, ambos
unidos a la misma proteína transportadora en un modo de
contratransporte. Este mecanismo se produce además
del transporte activo primario de calcio que se produce en
algunas células.
Se produce en varios tejidos. Puede producirse en los
túbulos proximales de los riñones, en los que los iones
sodio se desplazan desde la luz del túbulo hacia el interior
de la célula tubular, mientras que los iones hidrógeno son
contratransportados hacia la luz tubular. Como
mecanismo para concentrar los iones hidrógeno, no es
tan eficaz como el transporte activo primario de los iones
hidrógeno que se produce en los túbulos renales más
distales, aunque puede transportar cantidades muy
grandes de iones hidrógeno, lo que hace que sea clave
para el control del ion hidrógeno en los líquidos
corporales.
Transporte activo a través de capas celulares
En muchas localizaciones del cuerpo se deben transportar sustancias a través de todo el espesor de una
capa celular en lugar de simplemente a través de la membrana celular. El transporte de este tipo se
produce a través de:
1) el epitelio intestinal;
2) el epitelio de los túbulos renales;
3) el epitelio de todas las glándulas exocrinas;
4) el epitelio de la vesícula biliar, y
5) la membrana del plexo coroideo del cerebro, junto con otras membranas.
El mecanismo básico para el transporte de una sustancia a través de una lámina celular es:
1) transporte activo a través de la membrana celular de un polo de las células transportadoras de la capa,
y después
2) difusión simple o difusión facilitada a través de la membrana del polo opuesto de la célula.
La figura 4-15 muestra un mecanismo para el
transporte de los iones sodio a través de la capa
epitelial de los intestinos, de la vesícula biliar y de los
túbulos renales. Esta figura muestra que las células
epiteliales están conectadas entre sí íntimamente en
el polo luminal por medio de uniones. El borde en
cepillo de las superficies luminales de las células es
permeable tanto a los iones sodio como al agua. Por
tanto, el sodio y el agua difunden fácilmente desde la
luz hacia el interior de la célula. Después, en las
membranas basales y laterales de las células los
iones sodio son transportados activamente hacia el
líquido extracelular del tejido conjuntivo circundante y
hacia los vasos sanguíneos. Esta acción genera un
elevado gradiente de concentración del ion sodio a través de las membranas, que a su vez produce
también la ósmosis de agua. Así, el transporte activo de los iones sodio en las superficies basolaterales de
las células epiteliales da lugar a transporte no solo de iones sodio, sino también de agua.
A través de estos mecanismos casi todos los nutrientes, los iones y otras sustancias se absorben hacia la
sangre desde el intestino. Estos mecanismos constituyen también la forma en la que algunas sustancias
se reabsorben desde el filtrado glomerular por los túbulos renales.

Transporte de sustancias a través de las membranas celulares - Modulo 2 - Cap 4.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.