11.8 TRADUCCIÓN DE LA INFORMACIÓN GENÉTICA 461
11.8
TRADUCCIÓN DE LA INFORMACIÓN
GENÉTICA
La síntesis o traducción de proteínas es la actividad sintética
más compleja en una célula. El ensamblado de una proteína re-
quiere todos los diferentes tRNA con sus aminoácidos unidos,
ribosomas, un mRNA, algunas proteínas con funciones distintas,
cationes y GTP (trifosfato de guanosina). La complejidad no es
sorprendente si se considera que la síntesis de proteína necesita
la incorporación de 20 aminoácidos diferentes en la secuencia
precisa dirigida por un mensaje codificado en un lenguaje que
emplea diversos elementos. En la descripción siguiente se anali-
zan sobre todo los mecanismos de traducción que operan en las
células bacterianas, que son más simples y mejor conocidos. El
proceso es muy similar en las células eucariotas.
La síntesis de una cadena polipeptídica puede dividirse en
tres actividades distintas: inicio de la cadena, elongación o alarga-
miento de la cadena y terminación de la cadena. A continuación se
describe cada una de estas actividades.
Inicio
Una vez que se une a un mRNA, el ribosoma siempre se mueve
a lo largo del mRNA de un codón al próximo, esto es, en bloques
consecutivos de tres nucleótidos. Para asegurar que los tripletes
se lean, el ribosoma se une al mRNA en un sitio preciso denomi-
nado codón de inicio, el cual se codifica como AUG. La unión a
este codón pone al ribosoma de manera automática en el marco
de lectura de tal modo que el ribosoma lee el mensaje entero, de
manera correcta, desde este punto de inicio. Por ejemplo, en el
caso siguiente:
—CUAGUUACAUGCUCCAGUCCGU—
el ribosoma se mueve del codón de inicio, AUG, a los próximos
tres nucleótidos, CUC, luego a CAG, y así de forma sucesiva a lo
largo de toda la secuencia.
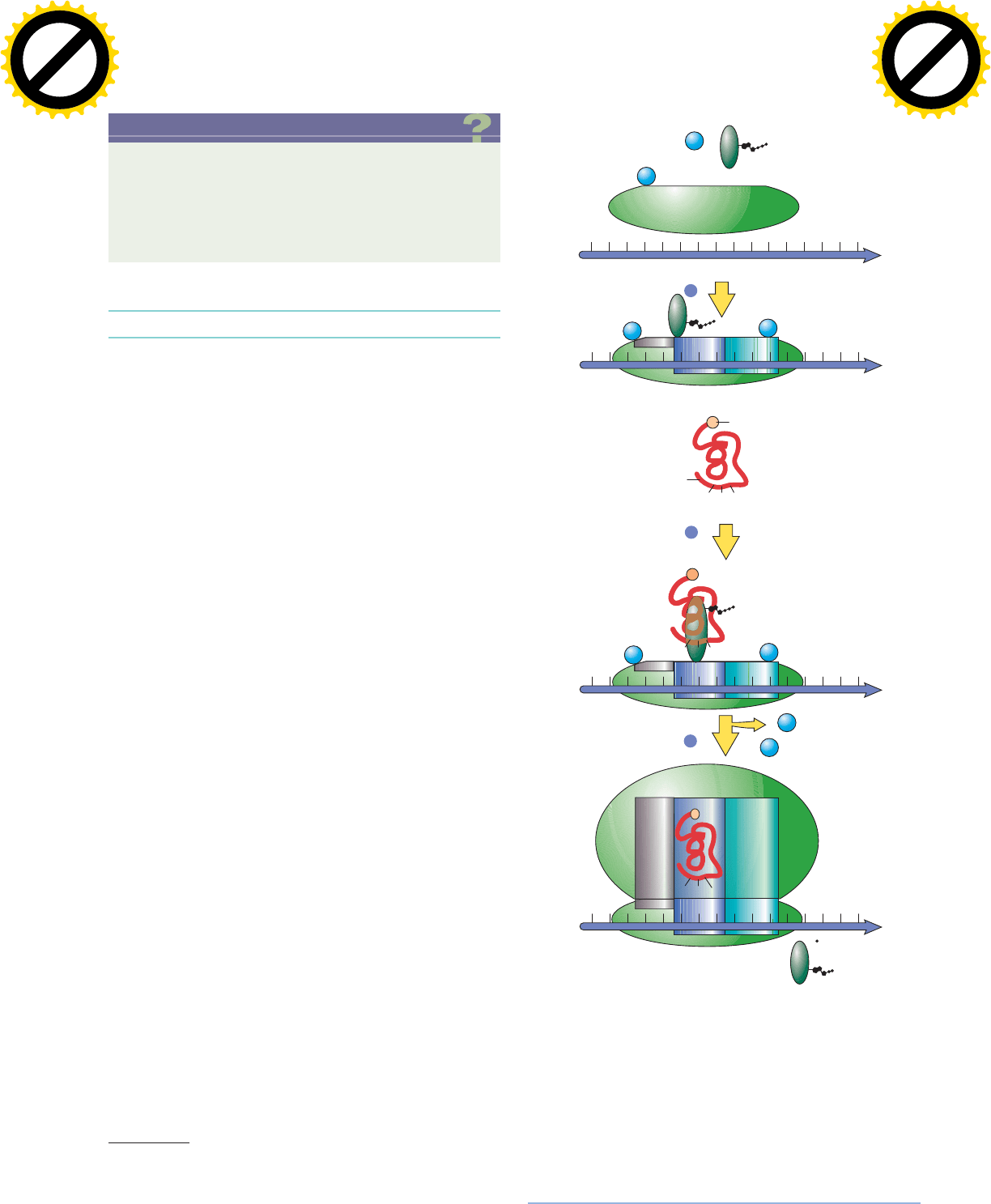
En la figura 11-46 se ilustran los pasos básicos del inicio de
la traducción en las células bacterianas.
Paso 1: traslado de la subunidad ribosómica pequeña
al codón de inicio
Como se advierte en la figura 11-46, un
mRNA no se une a un ribosoma intacto, sino a las subunidades
pequeña y grande en estadios separados. El primer gran paso de
inicio es la unión de la subunidad ribosómica pequeña a la pri-
mera secuencia AUG (o una de las primeras) en el mensaje, que
sirve como el codón de inicio.
8
¿De qué manera la subunidad
REVISIÓN
1. ¿Por qué se dice de los tRNA que son moléculas
adaptadoras?, ¿qué aspectos de la estructura de los
tRNA tienen en común?
2. Describa la naturaleza de las interacciones entre los tRNA
y las aminoacil-tRNA sintetasas y el tipo de interacción
entre tRNA y mRNA. ¿Cuál es la hipótesis del bamboleo?
8
GUG también es capaz de servir como un codón de inicio y se encuentra en
una cantidad muy pequeña de mensajes naturales. Cuando se utiliza GUG, la
N-formilmetionina no deja de usarse para formar el complejo de inicio a pesar
del hecho de que los codones GUG internos codifican a la valina.
IF3
IF3
IF1
IF1
GTP
IF2
fMet
+
mRNA
5'
GTP
IF2
mRNA
5'
1
AUG
tRNA
fMet
UAC
UC
IF3
IF2
IF1
mRNA
5'
AUG
IF1
IF3
2
A
IF2
PA
GDP
P
i
UAC
mRNA
5'
AUG
3
E
+
FIGURA 11-46 Inicio de la síntesis de proteínas en bacterias. En el paso
1, el inicio de la traducción comienza con la vinculación de la subunidad
ribosómica 30S con el mRNA en el codón de inicio AUG, un paso que
requiere IF1 e IF3. La subunidad ribosómica 30S se une al mRNA en
el codón de inicio AUG como resultado de una interacción entre una
secuencia nucleotídica complementaria en el rRNA y mRNA, como se
revisa en el texto. En el paso 2, la formilmetionil-tRNA
fMet
se relaciona
con el mRNA y el complejo de la subunidad ribosómica 30S mediante
el enlace a IF2-GTP. En el paso 3, la subunidad 50S se une al complejo, el
GTP se hidroliza y el IF2-GDP se libera. El tRNA iniciador entra al si-
tio P del ribosoma, mientras que todos los tRNA subsecuentes ingresan
al sitio A (fig. 11-49).
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m

462 Capítulo 11 EXPRESIÓN DEL MATERIAL GENÉTICO: DE LA TRANSCRIPCIÓN A LA TRADUCCIÓN
pequeña selecciona el codón inicial AUG a medida que se opo-
ne a uno interno? Los mRNA bacterianos poseen una secuencia
específica de nucleótidos (secuencia Shine-Dalgarno, nombrada
así por sus descubridores) que se localiza cinco a 10 nucleó-
tidos antes del codón de inicio. La secuencia Shine-Dalgarno
es complementaria de una secuencia de nucleótidos próxima al
extremo 3' del RNA ribosómico 16S de la subunidad ribosómica
pequeña.
unión con el mRNA. El tRNA iniciador unido a una metionina
también se une a una subunidad 40S antes de su interacción con
el mRNA. El tRNA iniciador entra en el sitio P de la subunidad
en asociación con eIF2-GTP. Una vez que estos sucesos se llevan
a cabo, la subunidad ribosómica pequeña con sus factores de ini-
cio relacionados y el tRNA (que juntos integran un complejo de
preinicio 43S) está listo para encontrar el extremo 5' del mRNA,
que tiene el casquete de metilguanosina (pág. 442).
Al principio, el complejo 43S se desplaza hacia el mRNA
con la ayuda de un grupo de factores de inicio que ya se encuen-
tran unidos al mRNA (fig. 11-47). Entre estos factores figuran
los siguientes: 1) el eIF4E se une al casquete 5' del mRNA de
eucariotas; 2) el eIF4A se moviliza a lo largo del extremo 5' del
mensaje y remueve cualquier región de doble cadena que po-
dría interferir con el movimiento del complejo 43S a lo largo del
mRNA, y 3) el eIF4G sirve como un puente entre el extremo
5' con el casquete y el extremo 3' poliadenilado del mRNA (fig.
11-47). De esta forma, el eIF4G convierte un mRNA lineal en
un mensaje circular.
Una vez que el 43S se une al extremo 5' del mRNA, el com-
plejo recorre el mensaje hasta alcanzar una secuencia nucleotídi-
ca que reconoce (por lo general el 5'⎯CCACCAUGC⎯3') que
contiene el codón de inicio AUG. Luego que el complejo 43S
alcanza al codón apropiado AUG, eIF2-GTP se hidroliza, eIF2-
GDP (y otros eIF asociados) se eliminan y la subunidad grande
(60S) se une al complejo para completar el inicio.
9
La función del ribosoma
Tras alcanzar el punto en el cual
se ha ensamblado por completo un ribosoma, es posible ver de
manera más detallada la estructura y función de esta estructura
de múltiples subunidades. Los ribosomas son máquinas molecu-
lares, similares en algunos aspectos a los motores moleculares
descritos en el capítulo 9. Durante la traducción, un ribosoma
sufre un ciclo repetitivo de cambios mecánicos que se realizan
La interacción entre estas secuencias complementarias en el
mRNA y el rRNA lleva a la unión de la subunidad 30S al codón
de inicio AUG.
Para el inicio se requieren factores de inicio Varios de los pasos
que se describen en la figura 11-46 requieren la ayuda de pro-
teínas solubles, los denominados factores de inicio (designados
como IF en procariotas y eIF en eucariotas). Las células bac-
terianas necesitan tres factores de inicio (IF1, IF2 e IF3), los
cuales se unen a la subunidad 30S (paso 1, fig. 11-46). El IF2 es
una proteína que une GTP requerido para la unión del primer
aminoacil-tRNA. El IF3 puede prevenir que la subunidad gran-
de (50S) se una en forma prematura a la subunidad pequeña 30S
y también facilita la entrada del aa-tRNA inicial. El IF1 facilita
la unión de la subunidad 30S al mRNA y puede prevenir que el
aa-tRNA entre a un sitio erróneo en el ribosoma.
Paso 2: traslado del primer aa-tRNA al ribosoma
Si se
examinan las asignaciones de codones (fig. 11-41), se puede ob-
servar que AUG codifica no tan sólo al codón de inicio; es el
único codón que codifica a la metionina. En realidad, la me-
tionina siempre es el primer aminoácido que se incorpora en el
extremo aminoterminal de la cadena naciente del polipéptido.
(En procariotas, la metionina inicial porta un grupo formilo,
que la convierte en N-formilmetionina.) Luego, la metionina
(o N-formilmetionina) se elimina por medios enzimáticos de la
mayoría de las proteínas recién sintetizadas. Las células poseen
dos metionil-tRNA: uno se utiliza en el inicio de la síntesis de
proteína y otro diferente para incorporar residuos de metionilo
en el interior del polipéptido. El aa-tRNA iniciador entra en el
sitio P del ribosoma (que se revisa más adelante) donde se une a
los codones AUG del mRNA y el factor de inicio IF2 (paso 2,
fig. 11-46). IF1 e IF3 se liberan.
Paso 3: ensamblado del complejo de inicio comple-
to
Una vez que el tRNA iniciador se une al codón AUG y
el IF3 se desplaza, la subunidad grande se une al complejo y el
GTP unido a IF2 se hidroliza (paso 3, fig. 11-46). Es probable
que la hidrólisis de GTP genere un cambio conformacional en el
ribosoma necesario para la liberación de IF2-GDP.
Inicio de la traducción en eucariotas
Las células eucario-
tas necesitan por lo menos 12 factores de inicio que incluyen un
total de más de 25 cadenas polipeptídicas. Como se indica en
la figura 11-47, varios de estos eIF (p. ej., eIF1, eIF1A y eIF3)
se unen a la subunidad 40S, que prepara a la subunidad para su
eIF1AeIF3
eIF2-GTP
Subunidad 40S
Complejo 43S
tRNA
Met
Proteína de unión
a poli (A) (PABP)
eIF4G
eIF4A
AUG
eIF4E
Complejo del mRNA
mRNA
3'
5'
AAAAAAAAAAA
+
FIGURA 11-47 Inicio de la síntesis de proteínas en eucariotas. Como se
señala en el texto, el inicio comienza con la unión de dos complejos, uno
(llamado complejo 43S) contiene la subunidad ribosómica 40S unida a
varios factores de inicio (eIF) y el tRNA iniciador, mientras que el otro
posee el mRNA unido a un grupo separado de factores de inicio. Esta
unión es mediada por una interacción entre eIF3 en el complejo de 43S
y eIF4G en el complejo del mRNA. Una vez que el complejo de 43S se
ha unido al extremo 5' del mRNA, recorre el mensaje hasta alcanzar el
codón de inicio apropiado AUG.
9
No todos los mRNA se traducen a partir de la unión de la subunidad
ribosómica pequeña en el extremo 5' del mensajero. Muchos mRNA virales y un
pequeño número de mRNA celulares, casi siempre utilizados durante la mitosis
o los periodos de estrés, se traducen como efecto de la unión del ribosoma al
mRNA en un sitio ribosómico interno de entrada (IRES), el cual puede localizarse
a cierta distancia del extremo 5' del mensajero.
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m

con la liberación de energía por la hidrólisis de GTP. A diferen-
cia de la miosina o la cinesina, las cuales de forma simple se mue-
ven a lo largo de una estructura física, los ribosomas se desplazan
a lo largo de una cinta de mRNA (que contiene la información
codificada). En otras palabras, los ribosomas son máquinas pro-
gramables: la información almacenada en los mRNA determina
la secuencia de los aminoacil-tRNA que el ribosoma acepta du-
rante la traducción. Otra característica que distingue a los ri-
bosomas de muchas otras máquinas celulares es la importancia
de los RNA que lo componen. Los RNA ribosómicos ejercen
funciones esenciales en la selección de los tRNA y aseguran una
traducción precisa al unir factores proteínicos y polimerizar ami-
noácidos (se revisa en la sección Vías experimentales al final del
capítulo).
En años pasados progresó mucho la comprensión de la
estructura de los ribosomas bacterianos. Los estudios iniciales
que emplearon la microscopia crioelectrónica de alta resolución
(sección 18.8) revelaron que el ribosoma tenía una estructura
muy irregular con lóbulos, protuberancias, canales y puentes (fig.
2-56). Estos estudios también proporcionaron información so-
bre los principales cambios conformacionales que ocurren en las
subunidades pequeña y grande durante la traducción. Durante
los años 1990 se hicieron grandes avances en la cristalización
de los ribosomas y para el final de esa década aparecieron los
primeros informes sobre la estructura de los ribosomas de proca-
riotas obtenida por cristalografía de rayos X. La figura 11-48a y b
muestra la estructura general de las dos subunidades ribosómicas
de un ribosoma bacteriano, tal como lo revela la cristalografía
con rayos X.
Cada ribosoma tiene tres sitios para la vinculación con mo-
léculas de RNA de transferencia. Estos sitios, denominados sitio
A (aminoacilo), sitio P (peptidilo) y sitio E (de salida), reciben
cada tRNA en pasos sucesivos del ciclo de elongación, como se
describe en la siguiente sección. Las posiciones del tRNA unido
a los sitios A, P y E de las subunidades pequeña y grande de los
ribosomas se muestran en la figura 11-48a,b. Los tRNA se unen
dentro de estos sitios y abarcan el espacio entre las dos unidades
ribosómicas (fig. 11-48c). Los extremos de los anticodones de
los tRNA unidos hacen contacto con la subunidad pequeña, la
cual tiene una función importante al decodificar la información
contenida en el mRNA. En cambio, los extremos que unen a
los aminoácidos del tRNA contactan a la subunidad grande, que
posee una función relevante al catalizar la formación del enlace
peptídico. Otras características importantes reveladas por estos
estudios estructurales de alta resolución incluyen lo siguiente:
1. La interfase entre las subunidades grande y pequeña forma
una cavidad relativamente espaciosa (fig. 11-48c) ocupada
casi de modo exclusivo por RNA. La cadena lateral de la
subunidad pequeña que limita a esta cavidad se extiende a lo
largo de una hélice continua de RNA bicatenario. Esta hélice
aparece sombreada en la estructura bidimensional del rRNA
16S en la figura 11-3. Las superficies de las dos subunidades
que se limitan la una a la otra contienen los sitios de unión
para el mRNA y el tRNA que entra y son de importancia
clave para la función del ribosoma. El hecho de que estas su-
perficies se integren en su mayor parte con RNA apoya la
propuesta de que los ribosomas primigenios estaban forma-
dos casi de manera exclusiva por RNA (pág. 448).
(a')
(c)
30S
3'
70S
30S
50S
tRNA
mRNA
Sitios de
unión para tRNA
Sitio decodificado
A
P
E
Residuos
de aminoácidos
Canal de salida
Sitio
del factor
de unión
Centro del
peptidilo
de transferencia
50S
(b')
(b)(a)
FIGURA 11-48 Modelo de un ribosoma bacteriano basado en datos de
cristalografía de rayos X que muestra los tRNA unidos a los sitios A,
P y E de las dos subunidades ribosómicas. (a-b) Vista de las subuni-
dades 30S y 50S, respectivamente, con los tres tRNA unidos mostrados
en la interfase entre las subunidades. (a'-b') Representaciones que co-
rresponden a las estructuras que aparecen en las partes a y b. El dibujo
en a' de la subunidad 30S ilustra las localizaciones aproximadas de los
anticodones de los tres tRNA y sus interacciones con los codones com-
plementarios del mRNA. El dibujo en b' de la subunidad 50S muestra
los sitios del tRNA en dirección inversa. El aceptor terminal de amino-
ácidos de los tRNA de los sitios A y P están muy próximos en el sitio del
peptidilo de transferencia de la subunidad, en donde ocurre la formación
del enlace peptídico. Los sitios de unión para los factores de elongación
EF-Tu y EF-G se hallan en la protuberancia hacia el lado derecho de la
subunidad. (c) Dibujo del ribosoma procariota 70S que señala el espacio
entre las dos subunidades ocupado por cada molécula de tRNA y el con-
ducto dentro de la subunidad 50S a través del cual el polipéptido recién
formado sale del ribosoma. ( : J H. C .,
H F. N, S 285:2100, 1999; ', ' :
A. L, S 285:2078, 1999; © 1999 A
A A S.)
11.8 TRADUCCIÓN DE LA INFORMACIÓN GENÉTICA 463
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m

464 Capítulo 11 EXPRESIÓN DEL MATERIAL GENÉTICO: DE LA TRANSCRIPCIÓN A LA TRADUCCIÓN
2. El sitio activo, donde se unen de modo covalente los amino-
ácidos, también se conforma con RNA. Esta porción catalíti-
ca de la subunidad grande reside en una cavidad profunda, la
cual protege al enlace peptídico recién formado de la hidróli-
sis por el solvente acuoso.
3. El mRNA se halla en un canal estrecho que rodea el cuello
de la subunidad pequeña y pasa a través de los sitios A, P y E.
Antes de entrar al sitio A, el mRNA se deshace de cualquier
estructura secundaria que pudiera tener mediante la actividad
helicasa del ribosoma.
4. Un túnel se proyecta a través del núcleo de la subunidad gran-
de desde el sitio activo. Dicho túnel provee una vía de paso
para la translocación del polipéptido durante la elongación a
través del ribosoma (fig. 11-48c).
5. La mayor parte de las proteínas de las subunidades ribosó-
micas tiene múltiples sitios de unión a RNA y se ubica en
posiciones ideales para estabilizar la estructura terciaria del
complejo del rRNA.
Elongación
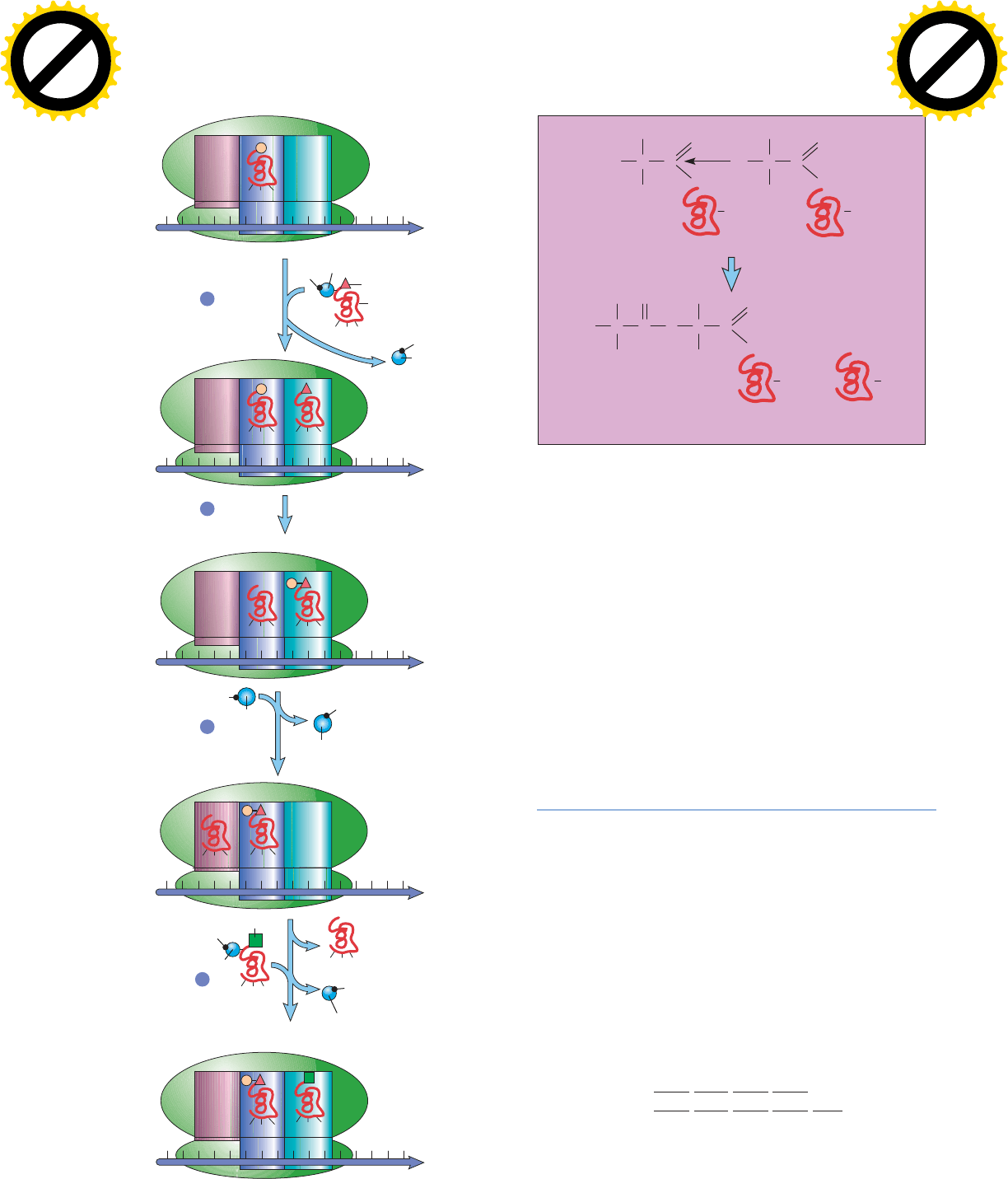
Los pasos básicos del proceso de elongación de la traducción en
células bacterianas se ilustran en la figura 11-49. Esta serie de
pasos se repite una y otra vez conforme se polimerizan los ami-
noácidos en la cadena polipeptídica en crecimiento.
Paso 1: selección del aminoacil-tRNA
Con el tRNA
iniciador cargado y en posición dentro del sitio P, el riboso-
ma queda disponible para la entrada de un segundo aminoacil-
tRNA en el sitio A vacante, lo cual representa el primer paso
de la elongación (paso 1, fig. 11-49a). Antes de que el segundo
aminoacil-tRNA, se una de manera eficiente al mRNA expues-
to en el sitio A, debe combinarse con un factor de elongación
de proteína unido a GTP. Este factor de elongación particu-
lar se conoce como EF-Tu (o Tu) en procariotas y eEF1α en
eucariotas. El EF-Tu es necesario para liberar los aminoacil-
tRNA hacia el sitio A del ribosoma. Aunque cualquier comple-
jo aminoacil-tRNA⎯Tu-GTP puede ingresar al sitio, sólo el
que tiene el anticodón complementario del codón del mRNA
alojado en el sitio A activará los cambios conformacionales ne-
cesarios dentro del ribosoma que hacen que el tRNA perma-
nezca unido al mRNA en el centro de decodificación. Una vez
que el aminoacil-tRNA⎯Tu-GTP correcto se une al codón del
mRNA, el GTP se hidroliza y el complejo Tu-GDP se libera,
con lo cual se abandona el aa-tRNA unido al sitio A del riboso-
ma. La regeneración de Tu-GTP a partir del Tu-GDP liberado
requiere otro factor de elongación, el EF-Ts.
Paso 2: formación del enlace peptídico
Al final del pri-
mer paso, los dos aminoácidos, unidos a sus tRNA separados, se
yuxtaponen en una posición en la que pueden reaccionar entre
sí (fig. 11-48a',b'). El segundo paso en el ciclo de elongación es
la formación de un enlace peptídico entre estos dos aminoácidos
(paso 2, fig. 11-49a). La formación del enlace peptídico se realiza
cuando el nitrógeno del grupo amino del aa-tRNA en el sitio
A reacciona con el carbón del grupo carbonilo del aminoácido
unido al tRNA del sitio P, con lo que se desplaza el tRNA del
sitio P (fig. 11-49b). Como resultado de esta reacción, el tRNA
unido al segundo codón en el sitio A tiene un dipéptido unido
y de esa forma el tRNA en el sitio P se desacila. La formación
del enlace peptídico ocurre de manera espontánea sin la utiliza-
ción de energía externa. La transferasa de peptidilo, un com-
ponente de la subunidad grande ribosómica, cataliza la reacción.
Durante años se asumió que la transferasa de peptidilo era una
de las proteínas del ribosoma. Sin embargo, conforme resultó
evidente la potencia catalítica del RNA, la atención se volvió al
RNA ribosómico como catalizador para la formación de enlaces
peptídicos. En la actualidad se ha demostrado que la actividad
de la transferasa de peptidilo reside en la molécula grande de
RNA ribosómico de la subunidad ribosómica grande (véase la
fotografía en la página inicial de este capítulo). En otras palabras,
la transferasa de peptidilo es una ribozima (se describe en la sec-
ción Vías experimentales al final del capítulo).
Paso 3: translocación
La formación del primer enlace pep-
tídico deja un extremo de la molécula de tRNA del sitio A to-
davía fijado a su codón complementario sobre el mRNA y el
otro extremo de la molécula fijado a un dipéptido (paso 2, fig.
11-49a). El tRNA del sitio P queda entonces desprovisto del
aminoácido. El siguiente paso, llamado translocación, se ca-
racteriza por un movimiento parecido al de un trinquete de la
subunidad pequeña con respecto a la grande. Como resultado, el
ribosoma se mueve tres nucleótidos (un codón) por el mRNA en
sentido 5'→3' (paso 3, fig. 11-49a). La translocación se acom-
paña del movimiento del dipeptidil-tRNA del sitio A al sitio P
del ribosoma, todavía enlazado por hidrógeno con el segundo
codón del mRNA, y del movimiento del tRNA desacilado del
sitio P al sitio E. Se visualizó una etapa intermedia en el proceso
de translocación al microscopio crioelectrónico que muestra que
los tRNA ocupan “estados híbridos” con translocación parcial.
En estos estados híbridos, los extremos del anticodón del tRNA
todavía están en los sitios A y P de la subunidad pequeña, mien-
tras que los extremos aceptores de los tRNA ya se movieron a los
sitios P y E de la subunidad grande. La translocación es impulsa-
da por cambios en la conformación de otro factor de elongación
(EF-G en bacterias y eEF2 en eucariotas) después de la hidróli-
sis de su GTP unido. Luego de esta reacción, EF-G-GDP sale
del ribosoma.
Paso 4: liberación del tRNA desacilado
En el paso final de
la elongación (paso 4, fig. 11-49a), el tRNA desacilado sale del
ribosoma y deja vacío el sitio E.
Por cada ciclo de elongación, por lo menos dos moléculas
de GTP se hidrolizan: una durante la selección de la aminoacil-
tRNA y una durante la translocación. Cada ciclo de elongación
toma alrededor de casi 0.05 s, la mayor parte de ese lapso tal vez
perdido en buscar los aa-tRNA del citosol circundante. Una
vez que el peptidil-tRNA se ha movido del sitio P por translo-
cación, el sitio A está de nueva cuenta disponible para la entra-
da de otro aminoacil-tRNA, en este caso uno con un anticodón
complementario del tercer codón (fig. 11-49a). Cuando el tercer
tRNA cargado se vincula con el mRNA en el sitio A, el dipép-
tido del tRNA del sitio P se transfiere al aa-tRNA del sitio A y
forma el segundo enlace peptídico y, en consecuencia, un tripép-
tido fijado al tRNA del sitio A. El tRNA del sitio P otra vez se
encuentra desprovisto del aminoácido. A la formación de enlaces
peptídicos le sigue la translocación del ribosoma al cuarto codón
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
E
E
E
PA
E
UAC
mRNA
Formación del
enlace peptídico
Translocación
5'
AUGUUU
PA
UAC
mRNA
5'
AUG
GTP
AAA
Fenilalanina
Phe-tRNA
Entrada del aa-tRNA
AAA
EF-Tu
EF-Tu
GTP
UCG
UAC
GDP
Serina
GDP
GDP
GTP
UUU
PA
UAC
UA
A
C
mRNA
5'
AUG
AAA
UUU
PA
AAA
mRNA
5'
U
U
UUAG
G
C
Liberación del tRNA desacilado
(a)
Péptido C
HO
R
tRNA
2
+ tRNA
1
CN
H
H
R'
CC
O
O
Péptido C
H
R
tRNA
1
tRNA
2
Sitio P Sitio A
C
H
N
H
:
O
O
C
H
R'
C
O
O
(b)
E
PA
UCG
mRNA
5'
UUUAGC
A
UG
AAA
EF-Tu
EF-Tu
EF-G
EF-G
1
2
3
4
FIGURA 11-49 Pasos en la elongación del polipéptido recién forma-
do durante la traducción en bacterias. (a) En el paso 1, un aminoacil-
t RNA cuyo anticodón es complementario del segundo codón del mRNA
entra al espacio vacío A del ribosoma. La unión del tRNA se acompaña
de la liberación de EF-Tu-GDP. En el paso 2, la formación del enlace
peptídico se acompaña de la transferencia de la cadena polipeptídica
naciente desde el tRNA en el sitio P hacia el aminoacil-tRNA en el sitio
A, con lo cual se forma un dipeptidil-tRNA en el sitio A y un tRNA
desacilado en el sitio P. La reacción la cataliza en parte el rRNA que
actúa como ribozima. En el paso 3, la unión de EF-G y la hidrólisis de su
GTP adjunto resultan en la translocación del ribosoma sobre el mRNA.
La translocación opera junto con el movimiento del tRNA desacilado
y la peptidil-tRNA en los sitios E y P, respectivamente. En el paso 4, el
tRNA desacilado deja el ribosoma y un nuevo aminoacil-tRNA entra al
sitio A. (b) Formación del enlace peptídico y el desplazamiento poste-
rior del tRNA desacilado. Un ribosoma puede catalizar la incorporación
de cerca de cinco aminoácidos por segundo a un polipéptido en creci-
miento, lo cual es casi 10 millones de veces mayor que lo observado en
la reacción no catalizada que emplea los sustratos modelo en solución.
y la expulsión del tRNA desacilado y el ciclo está listo para co-
menzar otra vez.
Se ha observado en esta sección de qué manera el riboso-
ma se mueve tres nucleótidos (un codón) a la vez a lo largo del
mRNA. La secuencia particular de codones en el mRNA que
utiliza un ribosoma (p. ej., el marco de lectura) se fija en el mo-
mento en que el ribosoma se une al codón de inicio al comien-
zo de la traducción. Algunas de las mutaciones más nocivas son
aquellas en las que un solo par de bases se agrega o se elimina del
DNA. Considérese el efecto de la adición de un solo nucleótido
a la siguiente secuencia:
⎯ AUG CUC CAG UCC GU →
⎯ AUG CUC
GCA GUC CGU ⎯
El ribosoma se mueve a lo largo del mRNA en un marco de
lectura incorrecto desde el punto de la mutación a través del
resto de la secuencia codificante. Las mutaciones de este tipo se
conocen como mutaciones por cambio en el marco de lectura.
Tales mutaciones codifican una secuencia del todo anormal de
11.8 TRADUCCIÓN DE LA INFORMACIÓN GENÉTICA 465
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m

466 Capítulo 11 EXPRESIÓN DEL MATERIAL GENÉTICO: DE LA TRANSCRIPCIÓN A LA TRADUCCIÓN
aminoácidos desde el punto donde ocurrió la mutación. Puede
observarse que, después de más de dos décadas en las cuales
se asumió que el ribosoma siempre se mueve de un triplete al
próximo, se descubrieron varios ejemplos en los que los mRNA
contenían una señal de recodificación que daba lugar a que el
ribosoma cambiara su marco de lectura, ya sea al retrasar un
nucleótido (un desplazamiento de −1 en la lectura) o saltar un nu -
cleó tido (un desplazamiento a +1 en el marco de lectura).
Una gran cantidad de antibióticos ejerce su efecto al inter-
ferir con diferentes aspectos de la síntesis de proteínas en células
bacterianas. Por ejemplo, la estreptomicina actúa por medio de la
unión selectiva a la subunidad ribosómica pequeña de las bacte-
rias y provoca que ciertos codones del mRNA se lean de manera
errónea, de tal modo que se incrementa la síntesis de proteínas
aberrantes. Debido a que el antibiótico no se une a los ribosomas
eucariotas, carece de efecto en la traducción en el mRNA de la
célula del hospedador. La resistencia por parte de la bacteria a
la estreptomicina puede estudiarse al observar los cambios de las
proteínas ribosómicas, en particular S12.
Terminación
Como se muestra en la figura 11-41, tres de los 64 codones tri-
nucleotídicos funcionan como codones de terminación que con-
cluyen el ensamblado del polipéptido en lugar de codificar un
aminoácido. No existen tRNA cuyos anticodones sean comple-
mentarios de los codones de detención o de paro.
10
Cuando el
ribosoma alcanza uno de estos codones, UAA, UAG o UGA, la
señal interpretada es la de detener todo el alargamiento adicional
y liberar al polipéptido relacionado hacia el último tRNA.
La terminación requiere factores de liberación. Los factores
de liberación (RF) pueden dividirse en dos grupos: los RF clase
I, que reconocen los codones de detención en el sitio A del ri-
bosoma, y los RF clase II, que son proteínas de unión con GTP
(proteínas G) cuyas funciones no se conocen bien. Las bacterias
tienen dos RF clase I: RF1, que reconoce los codones de deten-
ción UAA y UAG, y RF2 que reconoce los codones de de-
tención UAA y UGA. Los organismos eucariotas tienen un solo
RF clase I, eRF1, que reconoce los tres codones de detención.
Los RF clase I entran al sitio A del ribosoma, donde se cree que
un tripéptido conservado en un extremo del factor de liberación
interactúa en forma directa con el codón de detención en el sitio
A, en forma diferente a como lo haría una tripleta anticodón
de una molécula de tRNA que podría interactuar con un codón
codificante en ese sitio. El enlace éster que vincula la cadena po-
lipeptídica naciente con el tRNA se hidroliza luego y se libera
el polipéptido completo. En este punto, la hidrólisis del GTP
unido con el RF clase II (RF3 o eRF3) conduce a la liberación
del RF clase I del sitio A del ribosoma. Los pasos finales de la
traducción incluyen la liberación del tRNA desacilado del sitio
P, disociación del mRNA del ribosoma y desensamble del ribo-
soma en sus subunidades grande y pequeña como preparación
a otra ronda de traducción. Estos pasos finales requieren varios
factores proteínicos. En las células bacterianas, tales proteínas in-
cluyen EF-G, IF3 y RRF (ribosome recycling factor, factor recicla-
dor de ribosoma), lo que fomenta la separación de la subunidad
ribosómica.
Vigilancia y control de calidad de mRNA
Como los tres codones de terminación pueden formarse por
cambios de una sola base de muchos otros codones (fig. 11-41),
cabe esperar mutaciones que produzcan codones de detención
dentro de la secuencia codificante de un gen. Las mutaciones
de este tipo, denominadas mutaciones finalizadoras, se han es-
tudiado por décadas y a ellas se atribuye cerca de 30% de las
alteraciones hereditarias en seres humanos. Los codones de ter-
minación prematura, como también se les llama, son asimismo
introducidos comúnmente en los mRNA durante el empalme.
Las células poseen un mecanismo de vigilancia del mRNA capaz
de detectar mensajes con codones de terminación prematuros.
En la mayor parte de los casos, los mRNA que contienen ta-
les mutaciones se traducen sólo una vez antes de destruirse de
manera selectiva por un proceso llamado deterioro mediado
por falta de codificación (NMD, nonsense mediated decay). El
sistema NMD protege a la célula de la producción de proteínas
cortas no funcionales.
¿Cómo puede una célula distinguir entre un codón de ter-
minación legítimo que se supone termina la traducción de un
mensaje y el codón de terminación prematura? Para resolver
este acertijo, deben recordarse los sucesos que ocurren durante el
procesamiento del pre-mRNA en las células de los mamíferos.
No se mencionó antes, pero cuando un empalmosoma remueve
un intrón, un complejo de proteínas se deposita en el transcrito
20 a 24 nucleótidos en dirección 3' de la unión exón-exón re-
cién formada. Este conglomerado de proteínas se conoce como
complejo de unión exónico (EJC, exon-junction complex), el cual
permanece unido al mRNA hasta que éste se traduce. En un
mRNA normal, el codón de terminación casi siempre está pre-
sente en el último exón y el EJC está justo proximal a ese sitio.
Se piensa que cuando un mRNA sufre su ciclo inicial de tra-
ducción, los EJC son desplazados por el avance en el ribosoma.
Considérese lo que pasaría durante la traducción de un mRNA
que tuviera un codón de terminación prematura. El ribosoma
se detendría en el sitio de la mutación y entonces se disociaría,
dejando cualesquiera EJC que estuvieran unidos al mRNA en
dirección 3' del sitio de la terminación prematura. Esto pone en
marcha una serie de sucesos que llevan a la destrucción enzimá-
tica del mensaje anormal.
El NMD es mejor conocido por su participación en la eli-
minación de mRNA transcrito desde genes mutantes, como los
causantes de la fibrosis quística o la distrofia muscular. Varias
10
Existen excepciones menores a este enunciado. Se ha señalado en el capítulo
que los codones determinan la incorporación de 20 aminoácidos diferentes.
En el estado actual de los hechos, hay un aminoácido 21, el denominado
selenocisteína, que se incorpora dentro de un pequeño número de polipéptidos.
La selenocisteína es un aminoácido raro que contiene al metal selenio. Por
ejemplo, en mamíferos esto ocurre en una docena de proteínas. La selenocisteína
tiene su propio tRNA, llamado tRNA
Sec
, pero no posee su propia aa-tRNA
sintetasa. Este tRNA en particular lo reconoce la seril-tRNA sintetasa, la cual
se une a una serina en el extremo 3' del tRNA
Sec
. Después de la unión, la serina
se altera de manera enzimática y crea una selenocisteína. A ésta la codifica el
codón UGA, que es uno de los tres codones de terminación. En la mayor parte
de las circunstancias, el UGA se interpreta como una señal de terminación. Sin
embargo, en unos cuantos casos al UGA le sigue una región de plegamiento en
el mRNA que se une a un factor de elongación especial que da lugar a que el
ribosoma sea capaz de reclutar un tRNA
Sec
en el sitio A más que un factor de
terminación. Un vigésimo segundo aminoácido, pirrolisina, es codificado por otro
codón de terminación (UAG) en el código genético de algunas arqueobacterias.
La pirrolisina tiene sus propios tRNA y aa-tRNA sintetasa.
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m
Click to BUY NOW!
P
D
F
-
X
C
h
a
n
g
e
E
d
i
t
o
r
w
w
w
.
t
r
a
c
k
e
r
-
s
o
f
t
w
a
r
e
.
c
o
m

Traducción_Biolcelularymol_Karp.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.