1
TRABAJO PRÁCTICO N.º 2
2021
COMPONENTES QUÍMICOS DE LAS CÉLULAS PARTE I:
AGUA Y PEQUEÑAS MOLÉCULAS
OBJETIVOS
-
Analizar las propiedades fisicoquímicas del agua del agua, su capacidad como
disolvente y su relación con los sistemas biológicos.
-
Aplicar los conceptos teóricos a la resolución de problemas
-
Conocer la estructura y función de las pequeñas moléculas y cómo interactúan
entre sí para formar moléculas más complejas.
-
Comprender cómo participan las distintas moléculas orgánicas dentro del esquema
general del metabolismo.
UNIDAD DE CONOCIMIENTO
CONOCIMIENTOS PREVIOS REQUERIDOS:
Átomo: Definición. Constitución: partículas subatómicas. Número atómico y número
másico. Isótopos. Unidad de masa atómica (uma) y peso atómico relativo. Cantidad
de materia: mol. Electrones de valencia. Tabla periódica. Concepto de
electronegatividad. Moléculas: Definición. Moléculas simples y compuestas.
Enlaces químicos entre átomos: Regla del octeto. Enlaces iónicos y covalentes.
Estados de oxidación. Peso molecular. Mol de moléculas.
Soluciones: Concepto de soluto y solvente. Unidades de concentración.
Características salientes del átomo de carbono. Grupos funcionales principales y
familias de compuestos orgánicos resultantes.
TEMARIO
Componentes químicos de la célula. Elementos característicos en los organismos
vivos.
El agua: estructura y función en los seres vivos. Contenido y distribución del agua
corporal.
Enlaces por puente de hidrógeno en el agua y su importancia en las propiedades
físicas de la misma.
El agua como disolvente: sustancias hidrofílicas. Interacciones intermoleculares:
fuerzas de van der Waals y puentes de hidrógeno.
Compuestos hidrofóbicos y anfipáticos. Interacciones hidrofóbicas: un tipo especial
de interacciones intermoleculares entre moléculas hidrofóbicas determinadas por el
entorno acuoso.
Propiedades constitutivas y coligativas de las soluciones. Ósmosis y presión
osmótica. Osmolaridad: soluciones hipo-, hiper- e iso-osmóticas.
Membrana permeable, impermeable, semipermeable y selectivamente permeable:
coeficiente de reflexión y concepto de osmolaridad efectiva. Tonicidad. Equilibrio
osmótico entre compartimientos acuosos corporales.
Disociación del agua. Concepto de pH como una medida de la concentración de H
+
.
Ácidos y bases. Escala de pH. Sistemas buffer.
Moléculas de la célula (biomoléculas): características generales. Moléculas
orgánicas pequeñas: azúcares simples, aminoácidos, ácidos grasos y nucleótidos.
Estructura, nomenclatura y función. Propiedades físicas y químicas de las distintas
familias.

2
Azúcares simples: Importancia biológica de los monosacáridos. Rol en la
energética de la célula y en la biosíntesis de macromoléculas. Unión de
monosacáridos para generar disacáridos, oligosacáridos y polisacáridos. Disacáridos
de interés biológico: estructura y función. Importancia de los oligosacáridos en la
señalización y reconocimiento celular.
Ácidos grasos: su rol energético y su participación en la formación de fosfolípidos y
triglicéridos. Ácidos grasos esenciales y semiesenciales.
Aminoácidos: grupos funcionales que los caracterizan. Unión peptídica.
Clasificación general de los aminoácidos de acuerdo a su cadena lateral (R).
Aminoácidos esenciales. Aminoácidos no proteicos.
Nucleótidos: estructura general. Funciones: formación de macromoléculas (ADN y
ARN), relación con procesos energéticos y de transferencia de energía, coenzimas
nucleotídicas y nucleótidos cíclicos como moléculas señalizadoras. Importancia
biológica y ejemplos de cada tipo.
VOCABULARIO ESPECIFICO DEL TEMA
Enlaces de hidrógeno – ósmosis – tonicidad – anfipático – hidrofóbico – hidrofílica –
polar – pH – solución – suspensión – micelas – monocapa – bicapa – sillar
estructural – monómero – polímero – polimerización – biosíntesis – biodegradación –
reducción – oxidación – aldosa – cetosa – carbono asimétrico – isomería óptica -
oxhidrilo hemiacetálico y hemicetálico.
BIBLIOGRAFIA
Becker W.M y col. “El mundo de la célula” Ed. Pearson – 2007 -
Rawn, J. David. Bioquímica. Interamericana. McGraw-Hill.1989
Karp, G. “Biología Celular y Molecular”. 6ª Edición. Ed. McGraw-Hill Interamericana.
2010.
Herrera, E. Elementos de Bioquímica. Interamericana.McGraw-Hill. 1993.
Blanco, A. “Química Biológica”. 8
a
Edición. Editorial El Ateneo. 2015
Cingolani H., Houssay A. y col. “Fisiologia Humana de Houssay”. Editorial El Ateneo.
7° Edición 2000.
UNIDAD DE ACCION
En su casa: el estudiante deberá investigar usando como base el temario propuesto
y contestar el cuestionario guía de estudio a los efectos de autoevaluar si ha
adquirido los conceptos fundamentales requeridos para el abordaje del trabajo
práctico. Utilizando los conocimientos teóricos adquiridos intentará plantear una
solución de los ejercicios de aplicación.
Podrá además ejercitarse luego de la clase resolviendo los problemas adicionales.
En clase: el estudiante deberá participar en la discusión del temario y resolver con la
ayuda del docente los problemas de aplicación, con el fin de reafirmar los conceptos
teóricos estudiados en su casa y evacuar las posibles dudas.
3
Donde i (factor de van ’t Hoff) es el número de partículas generadas por la disociación de
una molécula de soluto. Su valor varía de acuerdo con la sustancia considerada: para
sustancias no disociables, i = 1, mientras que para sustancias que se disocian i es mayor,
por ejemplo para el NaCl que se disocia totalmente en iones Na
+
y Cl
-
, el valor de i es 2.
[Osm] = i x
[M]
CONCEPTOS TEORICOS COMPLEMENTARIOS
PROPIEDADES COLIGATIVAS:
Conjunto de propiedades de una solución denominadas que dependen únicamente de la
concentración de partículas en solución y no son influidas por el tamaño, ni por la carga,
ni por las características químicas del soluto.
Estas propiedades son:
-Presión osmótica
-Descenso del punto de congelación (de la solución con respecto al solvente puro)
-Aumento del punto de ebullición (de la solución con respecto al solvente puro)
-Disminución de la presión de vapor (de la solución con respecto al solvente puro)
Osmolaridad:
Unidad utilizada para expresar la concentración de partículas de soluto de una
solución. La osmolaridad (Osm) de una solución indica el número de moles de
partículas (osmoles) presentes en un litro (L) de solución.
Osmolaridad [Osm] = n° moles de partículas / L
Dado que:
n° moles de partículas = i x n° moles de moléculas
Entonces:
Osmolaridad [Osm] = i x
Por lo tanto:
“La osmolaridad de una solución se puede calcular mediante la ecuación”
Ejemplo:
Na3PO4= 3Na
+
+PO
4
3-
→ i = 4
Si en la solución acuosa [Na3PO4] = 3 M → [Osm] = 3 x 4 Osm = 12 Osm
Si en la solución acuosa [Na3PO4] = 2 mM → [Osm] = 2 x 4 mOsm = 8 mOsm
Dadas dos soluciones A y B:
-
sí [Osm]A = [Osm]B se dice que las soluciones son isoosmolares
-
sí [Osm]A > [Osm]B se dice que la solución A es hiperosmolar respecto a la B
-
sí [Osm]A < [Osm]B se dice que la solución A es hipoosmolar respecto a la B
Ósmosis
Si en un recipiente se coloca una solución A separada de otra solución B por una
membrana semipermeable (permeable al agua pero completamente impermeable a
todos los solutos), se producirá un flujo de agua desde la solución con menor [Osm]
hacia la solución con mayor [Osm]: este fenómeno se conoce como ósmosis.
DATO: al fenómeno de ósmosis sólo contribuyen las partículas que NO atraviesan la membrana y se
las denomina partículas osmóticamente activas.
n° moles de moléculas / L
Molaridad
[M]

4
= i x [M] x R
x T
= [Osm]
RT
PRESIÓN OSMÓTICA ()
Es la presión que debe aplicarse a una solución para evitar el flujo neto de agua
desde el agua pura a la solución a través de una membrana semipermeable. (O sea
para evitar ósmosis frente al agua pura).
La presión osmótica () de una solución se puede calcular mediante la siguiente
ecuación:
Donde: [M] es la concentración del soluto en moles/litro; i es el factor de van’t Hoff; R es la
constante general de los gases ideales, y T es la temperatura absoluta.
Una expresión equivalente es:
Esta ecuación evidencia que a una determinada temperatura la presión osmótica
teórica de una solución depende exclusivamente de su osmolaridad.
Dadas dos soluciones A y B:
-
Si A = B se dice que las soluciones son isoosmóticas
-
Si A > B se dice que la solución A es hiperosmótica respecto a la B
-
Si A < B se dice que la solución A es hipoosmótica respecto a B
Para membranas semipermeables la presión osmótica depende exclusivamente de
la [Osm] de la solución.
Si dos soluciones acuosas (A y B) se ponen en contacto mediante una membrana
semipermeable:
-
sí [Osm]A = [Osm]B (isoosmolares) ➔ A = B (isoosmóticas) no habrá flujo
neto de agua a través de la membrana ➔ no habrá ósmosis.
-
sí [Osm]A > [Osm]B (A hiperosmolar) ➔ A > B (A hiperosmótica) habrá
flujo neto de agua a través de la membrana desde B hacia A➔ habrá ósmosis
desde B hacia A.
-
sí [Osm]A < [Osm]B (A hipoosmolar) ➔ A < B (A hipoosmótica) habrá flujo
neto de agua a través de la membrana desde A hacia B➔ habrá ósmosis
desde A hacia B.
PRESIÓN OSMÓTICA EXPERIMENTAL (
E
)
El valor de presión osmótica calculado a partir de las osmolaridades (
T
) coincidirá
con el valor experimental (
E
) sólo si la membrana que separa las dos soluciones es
impermeable a todos los solutos presentes.
Si hay alguna permeabilidad al soluto, por mínima que sea, se encontrará
experimentalmente un valor de presión osmótica MENOR a la teórica.
DATO: a la presión osmótica experimental sólo contribuyen las partículas que NO atraviesan la
membrana y se las denomina partículas osmóticamente activas.
Podemos intentar corregir esta desviación con respecto a lo esperado, introduciendo
un coeficiente () denominado coeficiente de reflexión:
E
= x [Osm] x R x T
¿Por qué de "reflexión"? Porque este coeficiente representa la fracción de moléculas
del soluto que chocan contra la membrana y no la atraviesan (se reflejan hacia el
5
mismo compartimiento). Si la reflexión es total, la membrana es impermeable a ese
soluto, vale 1 y ese soluto contribuye en su totalidad al cálculo de la osmolaridad
efectiva. Si la reflexión es nula, la membrana es totalmente permeable a ese
soluto, vale 0 y dicho soluto no contribuye al cálculo de la osmolaridad efectiva. Si
la reflexión es parcial, el valor de será un número >0 y <1, y ese soluto sólo
contribuye parcialmente al cálculo de la osmolaridad efectiva.
Es difícil encontrar una membrana que sea permeable al agua e impermeable a
TODOS los solutos. Puede ser que una membrana sea impermeable al cloruro y al
sodio, pero no a la urea y por ello se dice que son membranas de permeabilidad
selectiva. ¿Qué pasaría si la diferencia de osmolaridad la creásemos con urea, por
ejemplo? Si la membrana es TAN permeable al agua como a la urea, simplemente
no tendríamos oportunidad o tiempo de ver el flujo osmótico, ya que rápidamente se
disiparía el gradiente de concentración de urea. Se diría que la membrana es
permeable.
Podríamos seguir analizando indefinidamente los posibles solutos que se nos
ocurran hasta el infinito y confeccionar toda una gradación de membranas en función
de su permeabilidad diferencial para cada soluto.
Por lo tanto, la
E
de una solución depende de la concentración de partículas
osmóticamente activas la cual está determinada por dos factores:
-
la concentración de partículas en solución dada por [Osm]
-
la permeabilidad de la membrana a las distintas partículas que se cuantifica
por el coeficiente de reflexión ().
La concentración de partículas osmóticamente activas viene dada por el producto:
x [Osm]) y se lo denomina OSMOLARIDAD EFECTIVA.
Se define el término tonicidad para describir el comportamiento osmótico de una
solución separada de otra solución por una membrana bien definida (p. ej., una
membrana plasmática). La solución de referencia será:
isotónica: si no existe flujo neto de solvente a través de la membrana plasmática
(para lo cual deberá tener la misma osmolaridad efectiva que el interior celular).
hipertónica: si existe flujo neto de solvente a través de la membrana plasmática
desde el medio intracelular hacia la solución (para lo cual deberá tener una
osmolaridad efectiva mayor que el interior celular).
hipotónica: si existe flujo neto de solvente a través de la membrana plasmática
desde la solución extracelular hacia el interior celular (para lo cual deberá tener una
osmolaridad efectiva menor que el interior celular).
La osmolaridad de una solución es una propiedad intrínseca de la misma que
describe la concentración de partículas presente en ella. Si consideramos que 290
mOsm es la osmolaridad plasmática normal, las soluciones con una osmolaridad de
290 mOsm son isoosmolares, las soluciones con osmolaridades >290 mOsm son
hiperosmolares y las que tienen osmolaridades <290 mOsm son hipoosmolares.
En cambio la tonicidad de una solución (relacionada a la osmolaridad efectiva) es
una propiedad que depende tanto de la permeabilidad de la membrana celular para
las distintas partículas presentes en la solución como de la osmolaridad de la misma.
Para solutos cuyo coeficiente de reflexión () es menor que uno (solutos
penetrantes), es importante distinguir entre osmolaridad y tonicidad.
“Para solutos no penetrantes (=1) la distinción entre osmolaridad y tonicidad es
meramente teórica”.

6
Cuando se utilizan los términos isotónica, hipertónica e hipotónica, se están
comparando dos soluciones entre si (p. ej., el LIC: líquido intracelular y el LEC:
líquido extracelular) separadas por una membrana bien definida (p. ej., una
membrana celular). Una solución es isotónica cuando su osmolaridad efectiva es
igual que la de la solución de referencia, que para nuestros fines es el LIC. Una
solución hipertónica es aquella que tiene una osmolaridad efectiva mayor que la
solución de referencia y una solución hipotónica tiene una osmolaridad efectiva mas
baja.
Los desplazamientos de H
2
O entre los compartimentos intracelular e intersticial se
deben a alteraciones de la osmolaridad efectiva del LEC, o tonicidad. Desde el punto
de vista clínico, esos cambios de la tonicidad suelen deberse a disminuciones de la
[Na
+
] en el plasma y el LEC (hiponatremia), a aumentos de la [Na
+
] (hipernatremia)
o a incrementos de la concentración de glucosa (hiperglucemia).
Los cambios de la concentración de un soluto que atraviese la membrana plasmática
con gran facilidad, como la urea, que se acumula en pacientes con insuficiencia
renal, no tienen ningún efecto sobre la tonicidad.
Intercambio de agua a través de la pared capilar
La barrera que separa el plasma sanguíneo y los compartimentos intersticiales (la
pared capilar) es, en una primera aproximación, libremente permeable a solutos
menores que las proteínas plasmáticas. Por tanto, la única fuerza osmótica neta que
actúa a través de la pared capilar es la causada por la distribución asimétrica de las
proteínas entre el plasma y el líquido intersticial. Se pueden utilizar varios términos
para referirse a la fuerza osmótica generada por estas proteínas plasmáticas que no
atraviesan la membrana celular, como presión osmótica proteica, presión osmótica
coloide y presión oncótica. Estos términos son sinónimos y pueden representarse
por el símbolo
oncótica
. La diferencia de presión oncótica (Δ
oncótica
), que tiende
a movilizar el H
2
O desde el intersticio al plasma, se contrarresta por la diferencia de
presión hidrostática a través de la pared capilar (ΔP), que desplaza el líquido del
plasma al intersticio.
ISÓMEROS
Se denominan isómeros a las sustancias que poseen una misma fórmula molecular
pero distinta estructura química y que, por lo tanto, acusan distintas propiedades. Se
distinguen dos tipos de Isómeros: estructurales (de cadena, de posición o de
función) y espaciales o estereoisómeros (geométricos y ópticos).
7
CUESTIONARIO GUIA DE ESTUDIO
1-
¿Cuál es la composición química del agua? ¿A través de qué tipos de enlaces se
unen sus átomos constituyentes? ¿Qué estructura tridimensional adoptan estos
átomos en la molécula de agua?
¿Por qué el agua es una molécula polar?
• Composición química del agua: 2 moleculas de hidrogeno y 1 molécula de
oxigeno
• Sus átomos constituyentes se unen a través de un enlace covalente
(compartiendo electrones)
• Forma tetraédrica. El ángulo formado por los enlaces del oxígeno con los
átomos de hidrogeno es como Sí estos estuvieran dirigidos hacia dos vértices
de un tetraedro regular, mientras que el oxígeno estuviera en el centro del
mismo. Por ello la molécula de agua es ANGULAR.
• Una molécula de agua es polar debido a que, aunque su carga neta sea cero,
la distribución de los electrones de la molécula presenta cierta orientación. El
átomo de oxígeno, con 8 protones en su núcleo, atrae con mayor fuerza a los
electrones del enlace con el átomo de hidrógeno, es decir, es más
electronegativo. Por lo tanto, en el ACHO está polarizado, existiendo una
densidad de carga negativa en torno del oxigeno y sus pares de electrones no
compartidos y una densidad de carga positiva en torno a los átomos de
hidrógeno. Debido a la geometría molecular angular de estos dipolos de
enlace se suman y junto al dipolo que generan los padres, no en las antes del
oxígeno forman un dipolo permanente. La condición dipolar del agua no
implica que la molécula tenga carga, ya que la molécula es eléctricamente,
neutra.
2-
a)
Teniendo en cuenta la composición química y la estructura tridimensional de
la molécula de agua, ¿qué tipos de enlace pueden formarse entre sus
moléculas?
Entre sus moleculas se forman enlaces PUENTES DE HIDROGENO
mediante los pares de electrones libres en el oxigeno
b)
Enuncie las características del enlace de hidrógeno y explíquelas.
Son relativamente débiles en comparación con enlaces covalentes o
iónicos, pero fuertes incorporación con interacciones dipolo-dipolo. La
fuerza de un enlace de hidrógeno entre moléculas de agua es
aproximadamente de 4 kilocalorías por MOL, mientras que la fuerza
del enlace oh es de 110 kilocalorías por MOL.
Tiene carácter bidireccional cuanto más lineal sea la orientación del
átomo de hidrógeno, y los dos átomos electronegativos implicados.
Tiene una longitud de enlace características, ya que existe una
distancia entre el átomo de hidrógeno y el átomo al que se une
covalentemente de 0,099 Nano milímetros. Y una distancia entre el
átomo de hidrógeno y el que se une por fuerzas electrostáticas de
0,177 nm, existiendo una distancia total entre 2 átomos de oxígeno de
0,276 nm.
Los enlaces puentes de hidrogeno se forman cuando un hidrogeno se
une a un elemento muy electronegativo (o, f, n) por un enlace
covalente, el cual mediante atracción dipolo se une a otro hidrogeno.

8
3-
a)
¿Cuántos enlaces de hidrógeno puede formar una molécula de agua con sus
vecinas si se encuentra en el seno del agua líquida? ¿Y si se encuentra en la
superficie?
En el seno del agua líquida el agua puede formar 2-4 enlaces
En la superficie va a poder formar solo 2 debido a que por encima de las
moleculas se encuentra al aire, solo puede formar enlaces con las
moleculas adyacentes.
b)
Defina tensión superficial
TENSION SUPERFICIAL:
Es un fenómeno por el cual la superficie de los líquidos tiende a
comportarse como una película delgada. La tensión superficial mide las
fuerzas internas que hay que vencer para poder expandir el área
superficial de un líquido midiendo la fuerza por unidad de longitud. En
Newton por metro. La energía necesaria para crear una nueva área
superficial trasladando las moléculas de la masa líquida, la superficie de la
misma es lo que se llama tensión superficial. A mayor tensión superficial
mayor es la energía necesaria para transformar las moléculas interiores
del líquido a moléculas superficiales.
Cantidad de energia que se requiere para que un líquido aumente su
superficie. Gracias a esto, por ejemplo, el mosquito puede apoyar sus
patas en el agua sin deformar la superficie con ellas.
c)
¿De qué forma una molécula de agua que se encuentra en el seno del líquido
logra pasar al estado de vapor? ¿Cuál es la relación con el elevado calor de
vaporización del agua? ¿Por qué sudamos?
• Una molécula de agua que se encuentra en el seno del líquido, logra pasar
el estado de vapor por la ruptura de sus enlaces de hidrógeno y el
posterior agregado de calor para dotar a la molécula de la superficie
energía cinética. El calor de vaporización del agua es mucho mayor que el
de los compuestos del mismo peso molecular y constituye la cantidad de
calor necesario para que un gramo de agua a 100º centígrados se
convierta en vapor. En el caso del agua, este valor es de 540 calorías por
gramo, debido a que primero se deben romper los enlaces de hidrógeno y
luego alcanzar la energía cinética necesaria, lo que no sucede con otros
compuestos.
• Al calentarse su densidad es menor por lo que sube a la superficie
evaporándose, por ejemplo cuando sudamos el cuerpo libera agua hacia
la piel debido a que este esta caliente, y al tener un alto calor de
vaporización, el agua se lleva el calor consigo terminando de evaporarse y
enfriando nuestro cuerpo
4-
¿Cómo varía la densidad del agua con la temperatura? Explique por qué es
posible la vida en ríos y lagos que se congelan durante el invierno.
La densidad de la mayoría de las sustancias aumenta con el enfriamiento
debido a la reducción del movimiento molecular, durante el cual se forman
cristales fuertemente empaquetados. La densidad del agua también
aumenta a medida que disminuye la temperatura, alcanzando el máximo
valor a los 4º centígrados, pero a temperaturas inferiores a 4 ° centígrados.
La densidad del agua comienza a decrecer debido a la formación de
9
cristales mantenidos por enlaces de hidrógeno, donde cada molécula de
agua se encuentra unida a otras 4. La estructura tridimensional adoptada
por las moléculas evita así que las moléculas se acerquen demasiado
entre sí, ocupando más volumen y teniendo menos densidad.
Debido a que el hielo es menos denso que el agua líquida, el hielo flota
sobre esta que se congela direccionalmente desde la superficie hasta el
fondo. De esta forma se evitan efectos destructivos sobre la flora y fauna
Marina y sirve de manta protectora para los seres vivos acuáticos ante el
frío extremo, ya que las capas inferiores quedan unos pocos grados por
encima de 0º centígrados, que es cuando el agua es más densa.
El agua aumenta su densidad a medida que disminuye su temperatura,
pero el agua alcanza su mayor densidad a los 4ºC para luego comenzar a
disminuir
Esto permite la vida en ríos y lagos en ivierno que están congelados ya
que, al tener menor densidad bajo los 4ºC, el agua congelada se
encuentra por la superficie, dejando abajo agua líquida apta para la vida.
El agua pura (destilada) alcanza un máximo de densidad a 4ºc y es igual a 1.
Así, la densidad disminuye con el aumento de la temperatura y mientras más
fría sea, el agua será más densa.
Es posible ya que en los lagos se forma hielo, con una densidad 0,9, la cual
va a flotar y va a ser como una “franja” la cual separe el agua del ambiente,
permitiendo así que continúe siendo liquida y que haya vida en ella.
5-
¿Cuál es la condición necesaria para que una sustancia sea soluble en un
disolvente? Tenga en cuenta las interacciones SOLUTO-SOLUTO, SOLVENTE-
SOLVENTE y SOLUTO-SOLVENTE, y las fuerzas involucradas. En función de su
respuesta, ¿para qué tipo de sustancias el agua será un buen disolvente?
Para que una sustancia sea soluble en un disolvente es necesario que la
fuerza de atracción entre las moléculas solvente puro sean fuertes, ya que si
no lo son, éstas se dispersan y acaban por evaporarse. Al mismo tiempo para
hacer misiles, dos sustancias deben poder interactuar y para que esto
suceda, las fuerzas de atracción entre Soluto soluto y solvente solvente no
pueden ser mayores que las fuerzas soluto solvente.
Por estas razones, el agua es un buen disolvente para:
compuesto de iónicos donde la interacción entre el agua y los iones positivos
o negativos es mayor que la interacción entre ellos. En estos casos, el agua
neutraliza sus cargas para poder pasarlos a una fase acuosa y luego los
rodean. Una aureola de hidratación o esfera de solvatación para que no
vuelvan a unirse.
Compuestos polares no iónicos que interactúan por medio de grupo oxidrilo y
carboxilo con los puentes de hidrógeno del agua dando soluciones estables.
Compuestos antipáticos que cuentan con una zona hidrofóbica y una zona
hidrofílica. En contacto con una superficie acuosa se disponen con sus
porciones hidrofílica, sin contacto con el agua y con sus porciones y los
fabricas en contacto con el aire.
Para que una sustancia sea soluble en un disolvente es necesario que las
fuerzas de atracción entre las moléculas del solvente puro sen fuertes ya que,
si no lo son, se dispersan y se evaporan.
Al mismo tiempo, para ser miscibles 2 sustancias debe poder interactuar, y
para que esto suceda las fuerzas de atracción entre soluto – solvente y
solvente – solvente no deben ser mayores que las fuerzas de soluto –
solvente.
10
Relación polar – polar. No polar – no polar
Por ello el agua es buen disolvente para compuestos iónicos, compuestos
polares no iónicos, compuestos anfipáticos.
6-
Teniendo en cuenta la alta energía de los enlaces iónicos presentes en una
estructura cristalina, ¿podría explicar cómo es posible que una sustancia como el
cloruro de sodio sea soluble en agua? Defina esfera de solvatación.
El cloruro de sodio en Estado sólido es una estructura cristalina mantenida
por fuerzas electrostáticas. Cuando se introduce en agua limpia, las fuerzas
de entre disolvente y los sillones. ¿NA más y cloro menos, son más fuertes
que las que mantienen Unidos a estos guiones en el cristal, por lo que el
cristal se disuelve y los iones de na más y el menos? En solución acuosa, se
rodean de una esfera de dipolos del solvente conocida como esfera de
solvatación.
Los dipolos del disolvente se disponen así con sus cargas opuestas a las del
guión más cercanas al mismo. En torno al NA más se encuentran en forma
más cercana a los átomos de oxígeno de las moléculas de agua con densidad
de carga negativa, mientras que en torno al cloro se disponen en forma más
cercana, en los átomos de hidrógeno de las moléculas de agua con densidad
de carga positiva.
El cloruro de sodio es soluble en agua ya que las moléculas polares del agua
rodean los iones. Los hidrógenos rodean al cl- y los o- al Na+ separando los
componentes, disolviendo la sal en agua creando así, este complejo llamado
ESFERA DE SOLVATACION
7-
Explique por qué las sustancias apolares son insolubles en agua. ¿Cómo se
denominan estas sustancias? ¿Qué entiende por interacción hidrofóbica?
Son moleculas no polares no son solubles en agua ya que no puedan
reaccionar con esta molécula que al ser una molécula polar solo reacciona
con la moléculas polares. La INTERACCION HIDROFOBICA es cuando se
añade una sustancia hidrofóbica a un medio acuoso generando que el agua
la rechace generando que la sustancia se centre en un punto.
Son insolubles en agua ya que estas moléculas no tienen regiones de cargas
parciales positivas o negativas por lo que no son atraídas electrostáticamente
por las moléculas de agua.
Estas sustancias se denominan HIDROFOBICAS
8-
a. ¿Qué entiende por solución? En una solución acuosa, defina soluto y solvente.
SOLUCION: Mezcla homogénea de una sustancia y un solvente. Soluto es
aquella sustancia que se disuelve en el solvente y se encuentra en menor
concentración. El solvente es la sustancia que está en mayor proporción en
una solución y disuelve al soluto
Una solución es la mezcla homogénea de una o más sustancias disueltas
en otra sustancia en mayor proporción. El soluto es la sustancia que se
disuelve (en menor cantidad) y el solvente la que lo disuelve (en mayor
cantidad)
b. ¿En qué unidades puede expresarse la concentración de soluto en una
solución?
Kg
c. ¿Puede decirse que el interior celular es una solución acuosa? ¿Por qué?
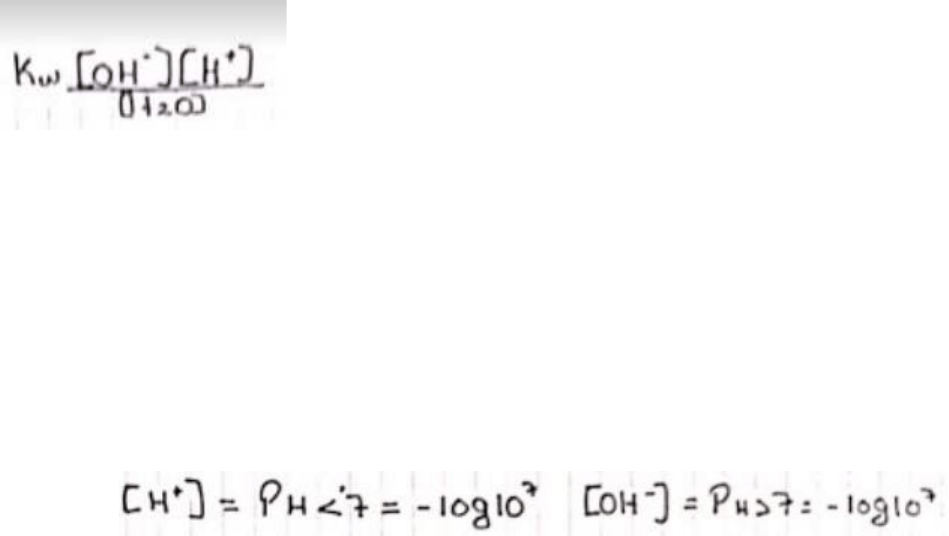
11
Sí, ya que el mayor porcentaje de las celulas es agua y los procesos ocurren en
el medio acuoso
9-
a. Escriba la constante de disociación del[ agua pura, ¿cómo se denominan los
iones resultantes?
Los iones resultantes son el protón hidrogeno [H+] y el Oxhidrilo [OH-]
a. ¿Qué entiende por ácidos y bases?
Un ácido es una sustancia capaz de ceder protones al disociarse
(donador de protones). Y una base es una sustancia capaz de tomar
protones al disociarse (aceptor de protones).
Un ácido es una sustancia que contiene un exceso de protones (H+)
mientras que una base es una sustancia que contiene un exceso de
oxhidrilos (OH-)
b. ¿De qué maneras alternativas puede expresarse la concentración de H
+
y OH
-
en soluciones acuosas diluidas de ácidos o bases? Escala de pH.
Mediante la escala de pH
c. ¿En qué casos hablamos de ácidos y bases fuertes y cuándo nos referimos a
ácidos y bases débiles? ¿Cuáles de ellos son importantes como
amortiguadores de cambios de pH?
Los ácidos y bases fuertes se disocian completamente en agua.
Los ácidos y bases débiles se disocian parcialmente en agua y se utilizan
como amortiguadores.
10-
a. ¿A qué se denominan propiedades coligativas? Menciónelas.
DEPENDEN sólo de la CONCENTRACIÓN DE PARTÍCULAS DE
SOLUTO disueltas y NO de su naturaleza
o Descenso de la presión de vapor
o Aumento del punto de ebullición
o Descenso del punto de fusión
o Presión osmótica
b)
¿Qué se entiende por gradiente? Defina el término difusión. ¿Por qué el
fenómeno de ósmosis puede definirse como un caso especial de difusión? Defina
presión osmótica.
GRADIENTE: Variación de una cantidad a partir de un punto o línea
12
DIFUSION: Pasaje a través de una membrana a favor de gradiente
La osmosis es un caso especial de difusión ya que solamente difunde el
solvente
PRESIÓN OSMÓTICA: Presión, fuerza aplicada que contrarresta la
fuerza aplicada por la osmosis.
c)
¿Cómo se relaciona la osmolaridad de una solución con la molaridad de la
misma?
Ya que la osmolaridad depende del índice de Van Hoff multiplicado por la
molaridad del soluto
La molaridad mide el número de moles de un soluto por unidad de
volumen de una solución; la osmolaridad mide el número de osmoles de
soluto participantes por unidad de volumen de una solución.
d)
Diferencie entre osmolaridad y tonicidad
La osmolaridad tiene que ver con la cantidad de soluto total de una
solución y su pasaje. Mientras que la tonicidad involucra los solutos que
no transportan la membrana por lo que se tiene en cuenta el tipo de
membrana y el índice de reflexión
e)
Defina solución isotónica, hipotónica, hipertónica
Isotónica: Cuando no existe flujo neto de solvente a través de la
membrana plasmática. Por lo que ambas soluciones tienen la misma
presión osmótica
Hipotónica: Cuando hay flujo neto de solvente a través de una
membrana, de la solución que se difunde es hipotónica ya que presenta
una concentración de soluto menor a la otra solución. Cuando la solución
A tiene menor presión osmótica que B
Hipertónica: Cuando hay flujo neto a través de una membrana la solución
que “recibe” el solvente es hipertónica ya que presenta una concentración
de soluto mayor que la otra solución. Cuando la solución A tiene mayor
presión osmótica que B.
13
11-
Teniendo en cuenta que el agua es la fase continua de los seres vivos. ¿En qué
compartimentos se la encuentra en un organismo pluricelular?
El agua se encuentra dentro de las celulas y en el espacio intercelular,
difundiéndose por sistemas de membranas.
En los organismos pluricelulares complejos el agua presenta una
distribución diferencial, de tal manera que hay mayor cantidad en los
tejidos químicamente más activos: 86 % en el tejido nervioso y tan sólo el
20 % en los huesos o en los dientes.
12-
a. ¿Qué son las pequeñas moléculas y cuáles tienen importancia biológica?
Las pequeñas moleculas son aquellas que están constituidas
mayormente por carbono y que luego conforman las macromoléculas de
gran importancia biológica
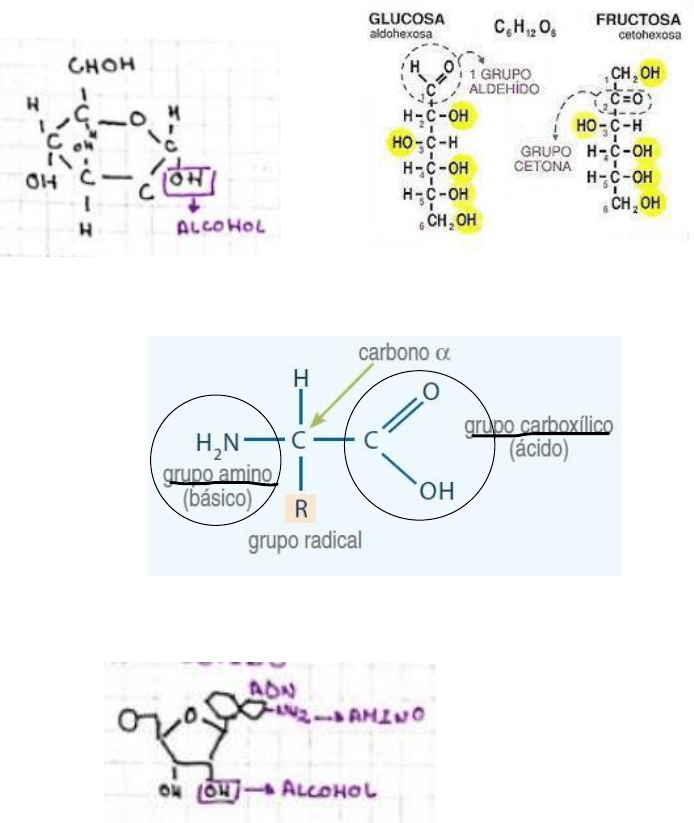
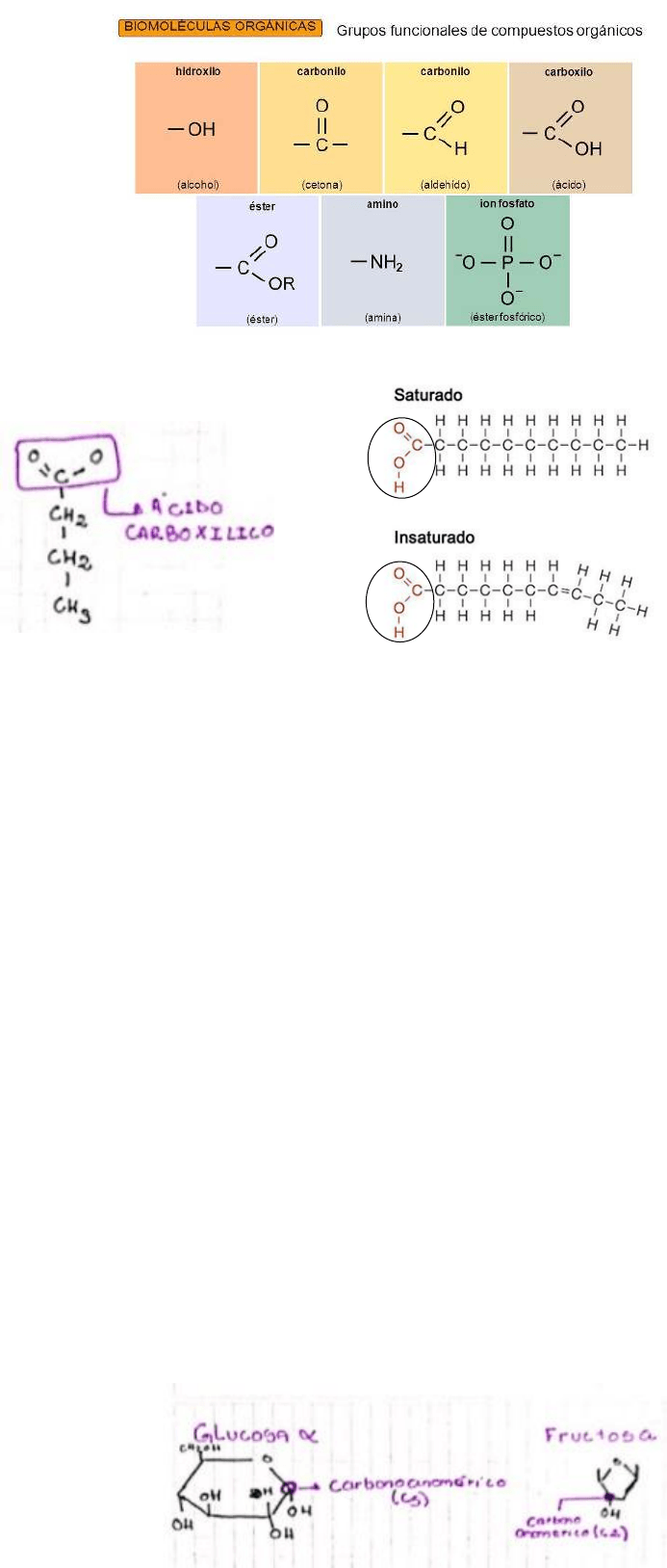
b. Represente las fórmulas químicas generales de las pequeñas moléculas.
Identifique los grupos funcionales característicos y señálelos.
Pequeñas:
Monosacáridos:
Aminoácido:
Nucleótidos
14
Ácidos grasos:
13-
a) Clasifique los monosacáridos de acuerdo con: número de carbonos y posición
del grupo carbonilo ¿Cuál es la aldosa de mayor importancia biológica? ¿Por qué?
Según el número de carbonos:
o Triosas: 3 c.
o Tetrosas: 4 c.
o Pentosas: 5 c.
o Hexosas: 6 c.
o Heptosas: 7 c.
Según el grupo funcional, su posición:
o ALDHEIDOS: Si el grupo carbonilo se encuentra en los extremos
del monosacárido. (Aldosas)
o CETONAS: Si el grupo carbonilo se encuentra en e medio del
monosacárido. (Cetosas)
La aldosa de mayor importancia biológica es la glucosa, que actúa como
fuente de energia para las celulas eucariontes
b)
¿Qué estructuras presentan algunos monosacáridos en solución acuosa?
Represente las estructuras cíclicas (fórmulas en perspectiva de Haworth) de la
glucosa y la fructosa señalando el carbono anomérico.
Presentan estructura cíclica ya que así son más estables
15
c)
¿Cómo se denomina la unión entre 2 azúcares simples? ¿Qué tipos de uniones
conoce? Mencione los disacáridos de mayor interés biológico.
La unión entre dos azucares simples se denomina UNION O-
GLICOSIDICA
Los disacáridos de mayor importancia biológica son:
Maltosa α (1->4). Presenta poder reductor. α glucosas.
Isomaltosa α (1->6). Poder reductor. α glucosas.
Lactosa β (1->4). Poder reductor β glucosa + β galactosa.
Sacarosa α (1->2). No tiene poder reductor. Β fructosa + α glucosa
Celobiosa β (1->4). Poder reductor. Β glucosas.
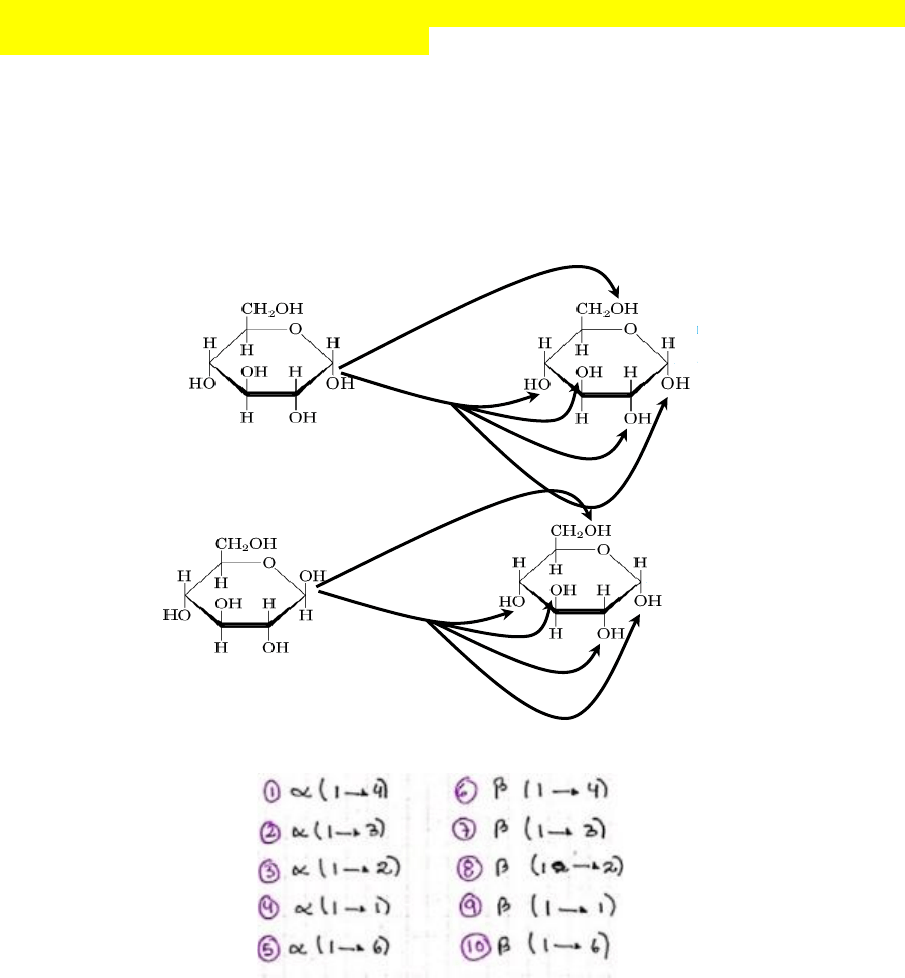
d)
En el siguiente gráfico indique el nombre específico que recibirá el enlace según
el grupo OH que participe en cada caso.
• el tipo de enlace entre este y los metales no es covalente, sino iónico o de
coordinación.
• El grupo OH se enlaza a un radical denotado con la letra R (si es alquílico) o
con la letra Ar (si es aromático). Para no hacer distinción entre ambos, a
veces se representa enlazado a una “onda”. Así, dependiendo de qué esté
detrás de esa “onda”, se habla de un compuesto orgánico o de otro.
¿En qué casos el producto resultante de la unión carecerá de poder reductor?
En los casos α (1->1) y β (1->1)
Este documento contiene más páginas...
Descargar Completo
TP2 AGUA Y PEQUEÑAS MOLÉCULAS (1).docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.