Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
1
22 de noviembre de 2020
TEÓRICO IV: METABOLISMO DE LOS HIDRATOS DE CARBONO,
“GLUCÓLISIS”.
I. REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA.
1.- DISPONIBILIDAD DE SUSTRATO: Ejemplo, una enzima está saturada por la alta disponibilidad de sustrato,
por lo que todos sus sitios activos están ocupados, por ende, su velocidad máxima ya está alcanzada.
2.- INHIBICIÓN POR PRODUCTO DE LA REACCIÓN: Ejemplo, la G-6-P es el producto de la reacción catalizada por
la HEXO Y GLUCOQUINASA, cuando se acumula este producto, funciona como inhibidor de la reacción.
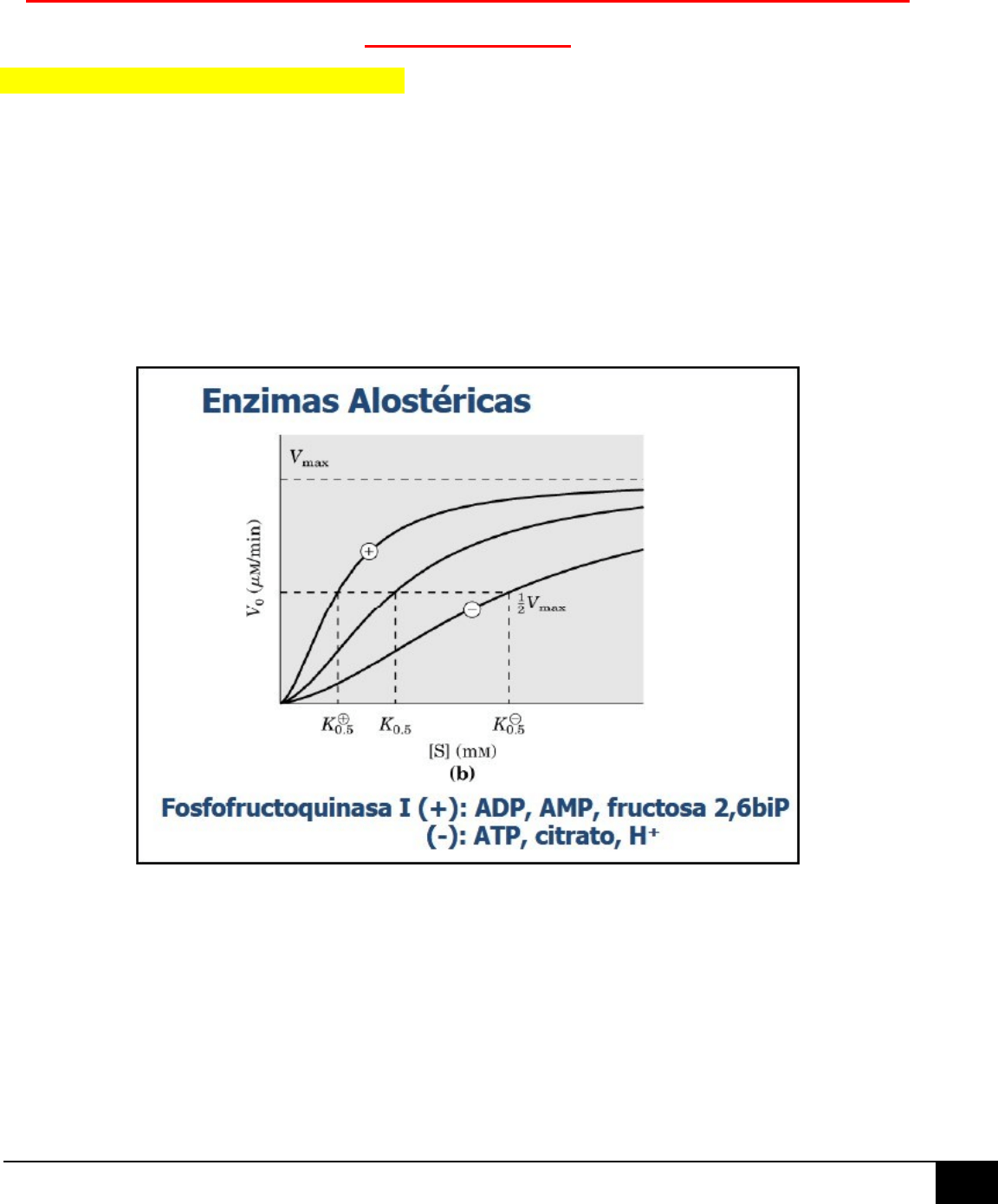
3.- MODULACIÓN ALOSTÉRICA (A CORTO PLAZO): En enzimas alostéricas, un compuesto se puede unir a un
sitio alostérico, actuando como modularor que puede o aumentar la actividad catalítica (modulador positivo,
disminuye Km, aumenta afinidad de la enzima por el sustrato) o disminuir la actividad catalítica (modulador
negativo, aumenta Km, disminuye la afinidad de la enzima por el sustrato).
Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
2
22 de noviembre de 2020
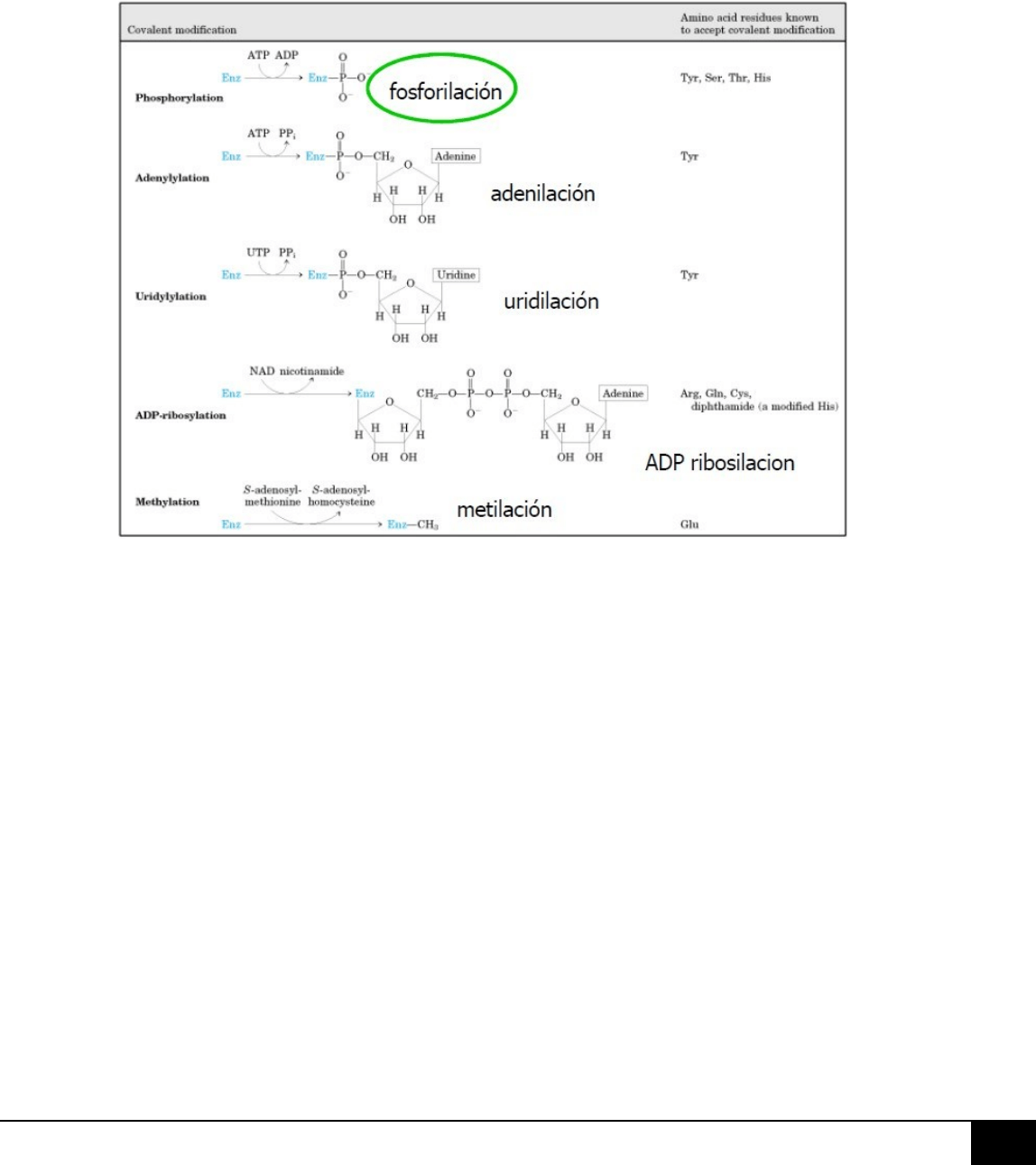
4.- MODIFICACIÓN COVALENTE REVERSIBLE (A CORTO PLAZO): Se produce cuando un grupo se une
covalentemente a la enzima. El grupo más común es el FOSFATO que generalmente se une a las cadenas de:
SERINA, TREONINA O TIROSINA (OH) por unión éster.
La agregación del fosfato cambia la conformación de la proteína y por ende, su actividad.
5.- CONVERSIÓN DE ZIMÓGENO EN ENZIMA (IRREVERSIBLE): Una proteína que aún no tiene actividad
enzimática es ESCINDIDA para que se convierta en enzima activa (ej. Protrombina). Esto se produce
generalmenten en enzimas de tipo digestivas.
6.- UNIÓN O LIBERACIÓN DE SUBUNIDADES PROTEÍCAS: Proteínas que están conformadas por 2
subunidades: UNA CATALÍTICA y UNA REGULATORIA, las cuales se tienen que separar para que cumplan sus
funciones. Ejemplo: Proteína quinasa A.
7.- CANTIDAD DE ENZIMA (A LARGO PLAZO): Se incita a la transcripción de ARNm que codifique nuevas
enzimas.
Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
3
22 de noviembre de 2020
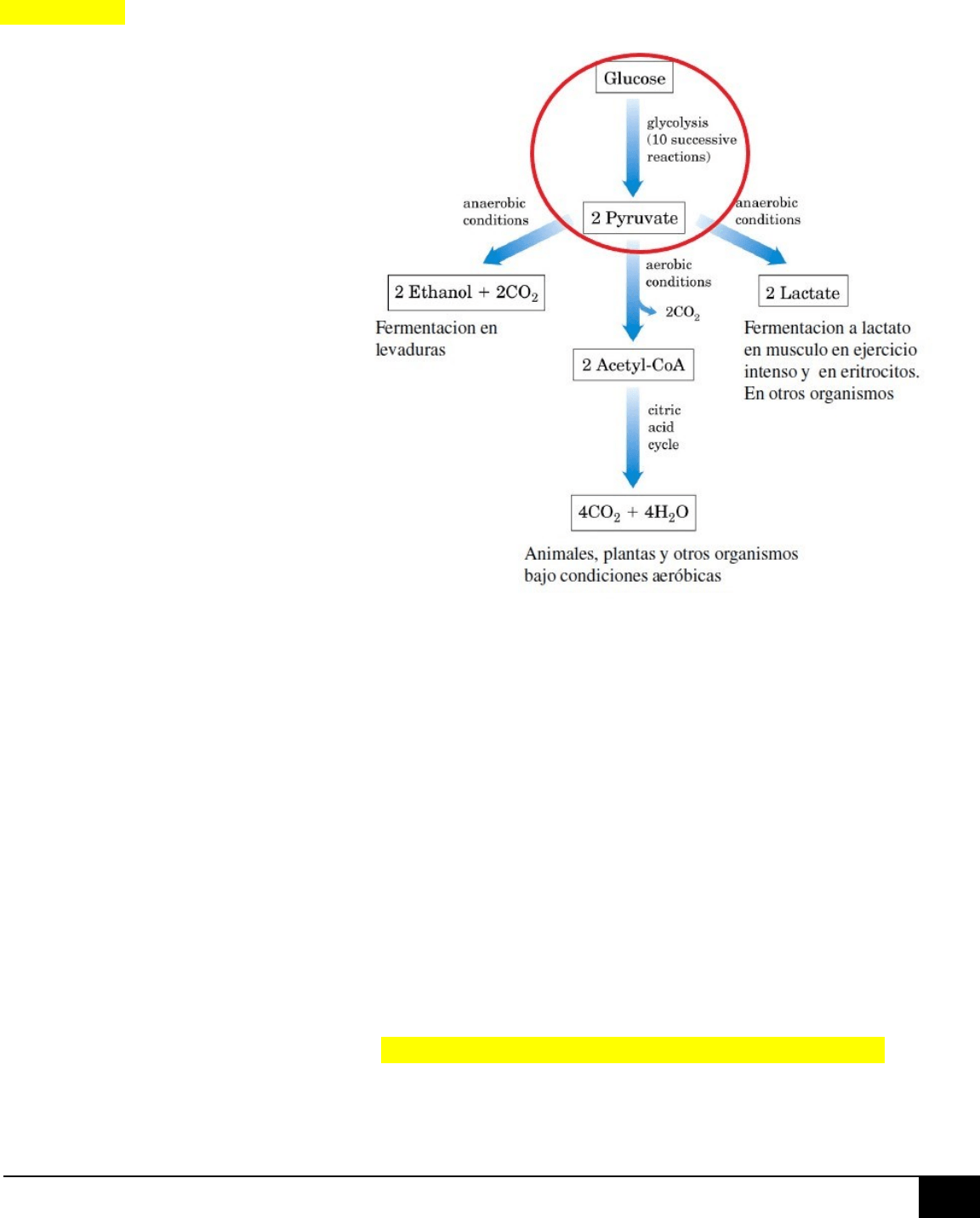
II. GLUCÓLISIS.
10 reacciones.
Ocurre en el
CITOSOL en
AUSENCIA DE OXÍGENO.
Oxidación de la glucosa a
PIRUVATO.
Los tejidos en general degradan el
piruvato a CO
2
+ H
2
O.
Los eritrocitos y el músculo activo
degradan el piruvato a LACTATO.
Una molécula de glucosa genera
2
ATP netos
, los cuales se generarán
a través de
FOSFORILACIÓN A
NIVEL DE SUSTRATO.
1 GLUCOSA de 6C se va a oxidar a
2 PIRUVATOS DE 3C cada uno.
El proceso se divide en dos fases:
- FASE PREPARATORIA:
Fosforilación de la glucosa y
conversión en gliceraldehído 3P.
- FASE DE BENEFICIOS: Conversión oxidativa del gliceraldehído 3P en piruvato y formación de ATP.
F A S E P R E P A R A T O R I A
1. FOSFORILACIÓN DE LA GLUCOSA:
Regulada.
HEXOQUINASA (tejidos), GLUCOQUINASA (hígado).
Se produce porque GLUT solo transporta glucosa libre (sin fosforilar), por lo que este mecanismo
permite el mantenimiento de la glucosa dentro de la célula.
Gasto de ATP.
2.- CONVERSIÓN DE GLUCOSA-6-P → FRUCTOSA-6-P:
FOSFOGLUCOSA ISOMERASA.
3.- FRUCTOSA-6-P → FRUCTOSA-1,6-BiP.
Regulada.
FOSFOFRUCTOKINASA 1 (PFK1) ← ENZIMA MÁS IMPORTANTE EN REGULACIÓN GLUCÓLISIS.
Gasto de ATP.

Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
4
22 de noviembre de 2020
4.- ESCINCIÓN DE LA FRUCTOSA-1,6-BiP → DIHIDROXIACETONA FOSFATO y GLICERALDEHÍDO-3-P:
ALDOLASA.
La dihidroxiacetona debe convertirse en gliceraldehído-3-P.
5.- DIHIDROXIACETONA-P → GLICERALDEHÍDO-3-P:
Hasta este punto el resultado neto del proceso ha sido:
1 MOL DE GLUCOSA → 2 MOLES DE GLICERALDEHÍDO-3-P.
F A S E D E B E N E F I C I O S
6.- 2 MOLÉCULAS DE GLICERALDEHÍDO-3-P → 2 MOLÉCULAS DE 1,3-BIFOSFOGLICERATO:
GLICERALDEHÍDO-3-FOSFATO-DESHIDROGENASA.
Se forma un NADH
+
el cual puede pasar su poder reductor directamente al citosol o a la
mitocondria.
Se produce una fosforilación sin gasto de ATP. FOSFORILACIÓN A NIVEL DE SUSTRATO.
El 1,3-BPG es el precursor del 2,3-BPG; modulador heterotrópico negativo de la Hb.
7.- 1,3.BIFOSFOGLICERATO → 3-FOSFOGLICERATO:
FOSFOGLICERATO KINASA.
Síntesis de ATP.
8.- 3-FOSFOGLICERATO → 2-FOSFOGLICERATO:
FOSFOGLICEROMUTASA.
9.- 2-FOSFOGLICERATO → FOSFOENOLPIRUVATO:
ENOLASA.
Produce agua.
El fosfoenolpiruvato es un compuesto rico en energía.
10.- FOSFOENOLPIRUVATO → PIRUVATO:
Regulada.
PIRUVATO KINASA.
Síntesis de ATP.
DESTINO DEL PIRUVATO EN ANAEROBIOSIS (EN AUSENCIA DE OXÍGENO = ERITROCITOS, MÚSCULO ACTIVO):
Eritrocitos y células musculares en actividad física.
Piruvato SE REDUCE A LACTATO.
Para realizar este proceso se oxida el NADH
+
, que aporta el protón para reducir el piruvato.
Esta OXIDACIÓN DEL NADH
+
es fundamental para que se mantenga su disponibilidad, y así continuar con
el proceso de gucólisis.

Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
5
22 de noviembre de 2020
REGULACIÓN DE LAS ENZIMAS DE GLUCÓLISIS
(PROCESOS IRREVERSIBLES)
I. HEXOQUINASA/GLUCOQUINASA = Glucosa → Glucosa-6-Fosfato.
1. HEXOQUINASA:
Michaeliana, curva hiperbólica.
Bajo Km = Alta afinidad por la glucosa.
INHIBICIÓN POR PRODUCTO: Acumulación de GLUCOSA-6-P.
SÍNTESIS DE NUEVA ENZIMA (LARGO PLAZO): Insulina induce a la síntesis de más hexoquinasa.
Aumenta la Vmáx.
2. GLUCOQUINASA:
Alostérica, curva sigmoidea.
Alto Km = Baja afinidad por la glucosa.
Predomina en hígado (GLUT-2).
ALTA CONCENTRACIÓN DE GLUCOSA EN SANGRE: Activación.
SÍNTESIS DE NUEVA ENZIMA (LARGO PLAZO): Insulina induce síntesis de más glucoquinasa. Aumenta
Vmáx.
SECUESTRO AL NÚCLEO: Cuando aumenta la concentración de Fructosa-6-P, la GK es secuestrada al
núcleo, por lo que se inhibe la fosforilación de la glucosa (inhibición por producto).
LIBERACIÓN DEL NÚCLEO: Cuando aumenta la concentración de Glucosa, la GK es liberada desde el
núcleo por lo que se activa la fosforilación de la glucosa.
II. FOSFOFRUCTOQUINASA 1 (PFK1) = Fructosa-6-p → Fructosa-1,6-bifosf.
Alostérica, curva sigmoidea.
Su regulación es la más importante de la glucólisis.
MODULACIÓN ALOSTÉRICA:
- Moduladores positivos:
Alta concentración de AMP (baja en la carga energética de la célula), Fructosa-2,6-BiP.
- Moduladores negativos:
Alta concentración de
ATP (producto final de la vía), alta concentración de protones, citrato.
FRUCTOSA-2,6-BIFOSFATO es el principal mecanismo regulador de la PFK1, es un modulador
alostérico positivo que aumenta la actividad enzimática de la PFK1 por lo que induce a una mayor
fosforilación de la fructosa-6-P, y por ende, una glucólisis activa.
Hay dos mecanismos principales de regulación de la F-2,6-BiP:
1.- A TRAVÉS DE LA “ENZIMA BIFUNCIONAL” (PFK2/PBPasa): Esta enzima controla los niveles de F-2-
6-BiP. Dependiendo de qué dominio esté activo habrá alta o baja concentración de F-2,6-BiP.
- ACTIVO DOMINIO QUINASA: Alta concentración de F-2,6-BiP en la célula→modulación positiva de la
PFK1→Mayor fosforilación de F6P→Mayor actividad glucolítica.
- ACTIVO DOMINIO FOSFATASA: Baja concentración de F-2,6-BiP en la célula→baja actividad de la
PFK1→Menor fosforilación de F6P→Menor actividad glucolítica.

Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
6
22 de noviembre de 2020
2. HORMONALMENTE EN HÍGADO:
- GLUCAGÓN (Ayunas, baja glicemia): Activación proteína G→Adelinato ciclasa→AMPc→Activación
PKA→Fosforilación DOMINIO QUINASA enzima bifuncional→Inactivación dominio quinasa enzima
bifuncional→ Baja concentración de F-2,6-BiP en la célula→baja actividad de la PFK1→Menor
fosforilación de F6P→Menor actividad glucolítica.
- ADRENALINA (Estrés, lucha o huida): Activación receptor β-adrenérgico→Activación proteína
G→Adelinato ciclasa→AMPc→Activación PKA→Fosforilación DOMINIO QUINASA enzima
bifuncional→Inactivación dominio quinasa enzima bifuncional→ Baja concentración de F-2,6-BiP en la
célula→baja actividad de la PFK1→Menor fosforilación de F6P→Menor actividad glucolítica.
- INSULINA (Periódo posprandial, alta glicemia): Insulina+Receptor→Activación segundo
mensajero→Estimulación FOSFATASA I (PP1)→Defosforilación DOMINIO QUINASA enzima
bifuncional→Activación dominio quinasa enzima bifuncional→Aumento fosforilación F6P→Alta
concentración de F-2,6-BiP en la célula→Alta actividad PFK1→Mayor fosforilación de F6P→Mayor
actividad glucolítica→Aumento síntesis de ATP.
(NO OLVIDAR QUE ESTAS TRES HORMONAS SON HIDROSOLUBLES, DE NATURALEZA PEPTÍDICA, POR LO QUE
NO PUEDEN ENTRAR A LA CÉLULA Y NECESITAN UN SEGUNDO MENSAJERO).
3. HORMONALMENTE EN CORAZÓN: A diferencia de lo que sucede en el hígado, en el corazón, la acción
de la adrenalina busca aumentar la glucólisis, y por ende, proveer mayor cantidad de ATP.
- ADRENALINA:
Activación receptor β-adrenérgico→Activación proteína G→Adelinato
ciclasa→AMPc→Activación PKA→PKA FOSFORILA UNA ISOENZIMA DE LA ENZIMA
BIFUNCIONAL→Fosforilación del dominio fosfatasa de la enzima bifuncional→Inhibición dominio
fosfatasa de la enzima bifuncional→Activación dominio quinasa de la enzima bifuncional→Aumento
fosforilación F6P→ Alta concentración de F-2,6-BiP en la célula→Alta actividad PFK1→Mayor
fosforilación de F6P→Mayor actividad glucolítica→Aumento síntesis de ATP.
III. PIRUVATO QUINASA = Fosfoenolpiruvato → Piruvato.
Alostérica, curva sigmoidea.
MODULACIÓN ALOSTÉRICA:
Moduladores positivos:
- Aumento en la concentración de FRUCTOSA-1,6-BIFOSFATO (Da cuenta de una glucólisis frenada).
-
ADP.
Moduladores negativos:
- ATP.
- Alanina (piruvato).
- AcetilCoA.
- Ac. Grasos.
MODULACIÓN COVALENTE REVERSIBLE (SOLO EN HÍGADO):
- GLUCAGON/ADRENALINA: Activación proteína G→Adelinato ciclasa→AMPc→Activación
PKA→Fosforilación PIRUVATO QUINASA→Inhibición piruvato quinasa→Disminución actividad piruvato
quinasa→Menor conversión a piruvato.
- INSULINA (Estimula su síntesis): Defosforilación PIRUVATO QUINASA→activación piruvato
quinasa→Aumento actividad piruvato quinasa→Mayor conversión a piruvato.

Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
7
22 de noviembre de 2020
GLUCÓLISIS ACTIVA EN HÍGADO:
- Alta glucemia, período posprandial, hay insulina.
GLUCÓLISIS INACTIVA EN HÍGADO:
- Baja glucemia, ayuno/actividad física/estrés, hay
glucagón.
GLUCÓLISIS ACTIVA EN MÚSCULO:
- Actividad física/estrés, hay adrenalina.
Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
8
22 de noviembre de 2020
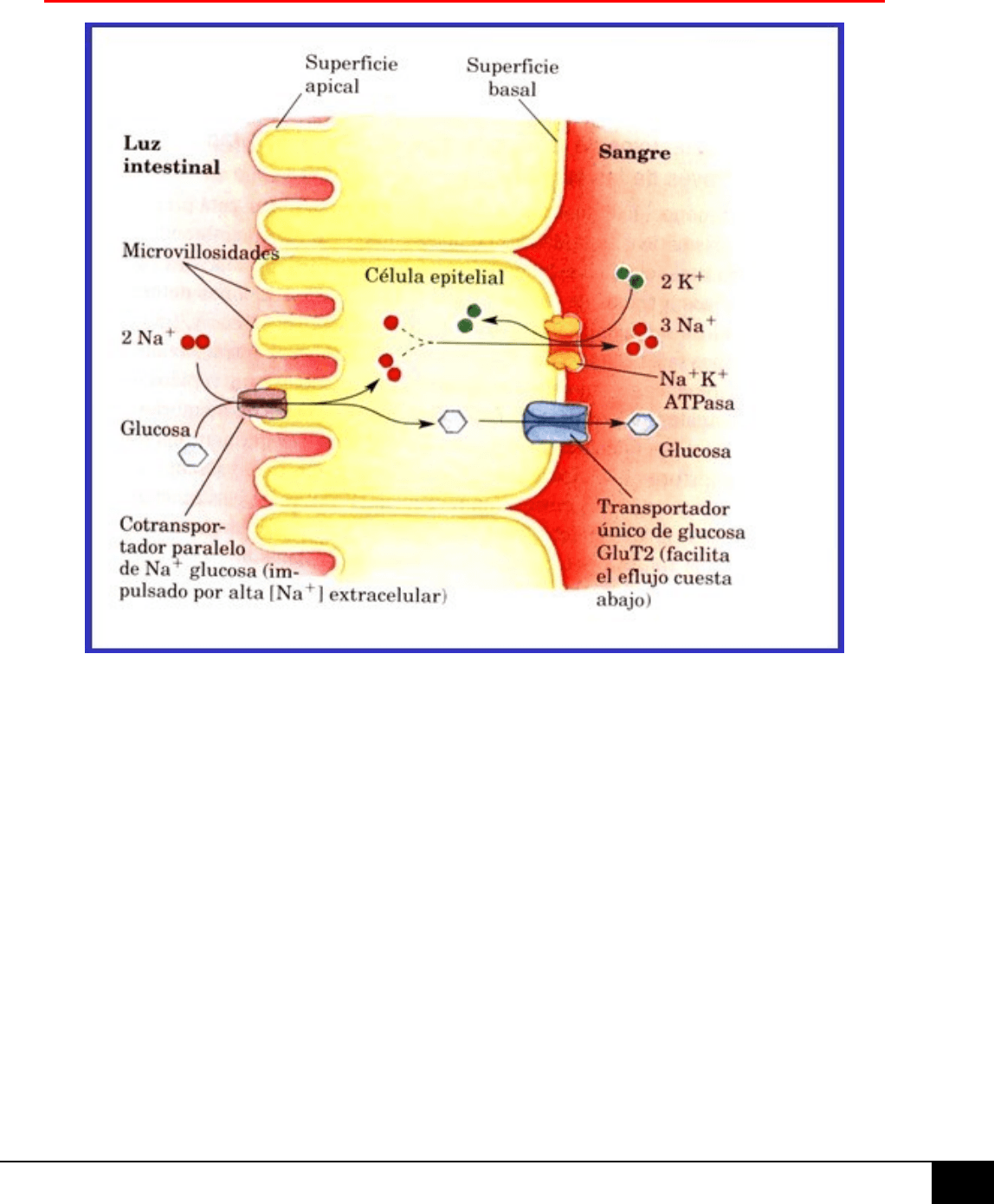
ANEXO: ENTRADA Y SALIDA DE GLUCOSA EN LAS CÉLULAS.
Absorción intestinal de la glucosa se produce a través de un tipo de CO-TRANSPORTADOR ACTIVO
SECUNDARIO; no está impulsado directo por el gasto de ATP, sino por el uso del gradiente de entrada del
SODIO (el cual fue sacado de la célula por la bomba sodio-potasio). Este transportador se llama: SGLT-1.
(2Na
+
/1Glu.)
Una vez dentro del enterocito esa glucosa debe salir (por la membrana basal) al líquido intersticial y
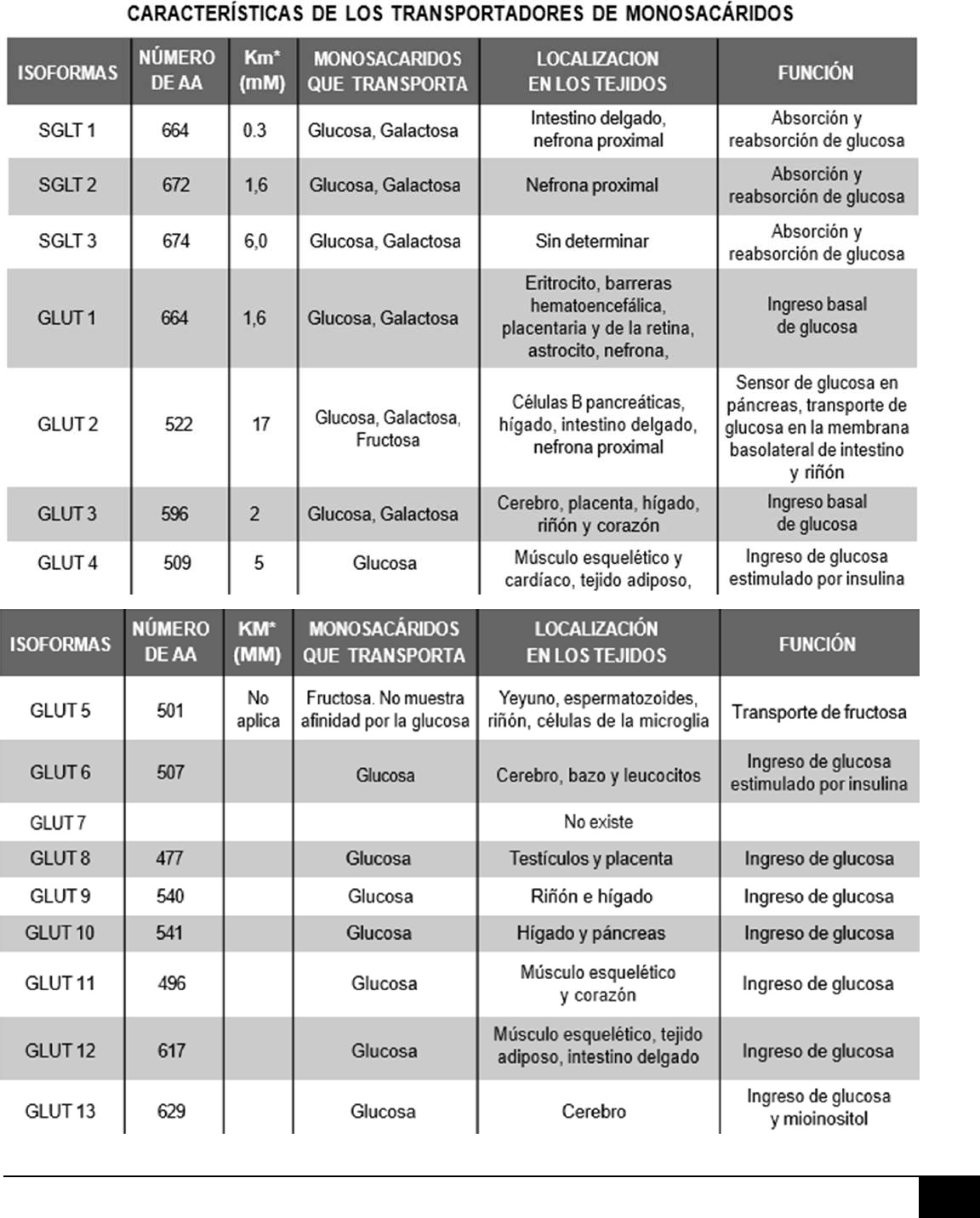
finalmente a la sangre, esto se produce gracias al transportador GLUT-2.
El GLUT-2 es un UNI-TRANSPORTADOR PASIVO, transporta solo una molécula de glucosa por vez. Su
transporte es por lo tanto una DIFUSIÓN FACILITADA A FAVOR DE GRADIENTE.
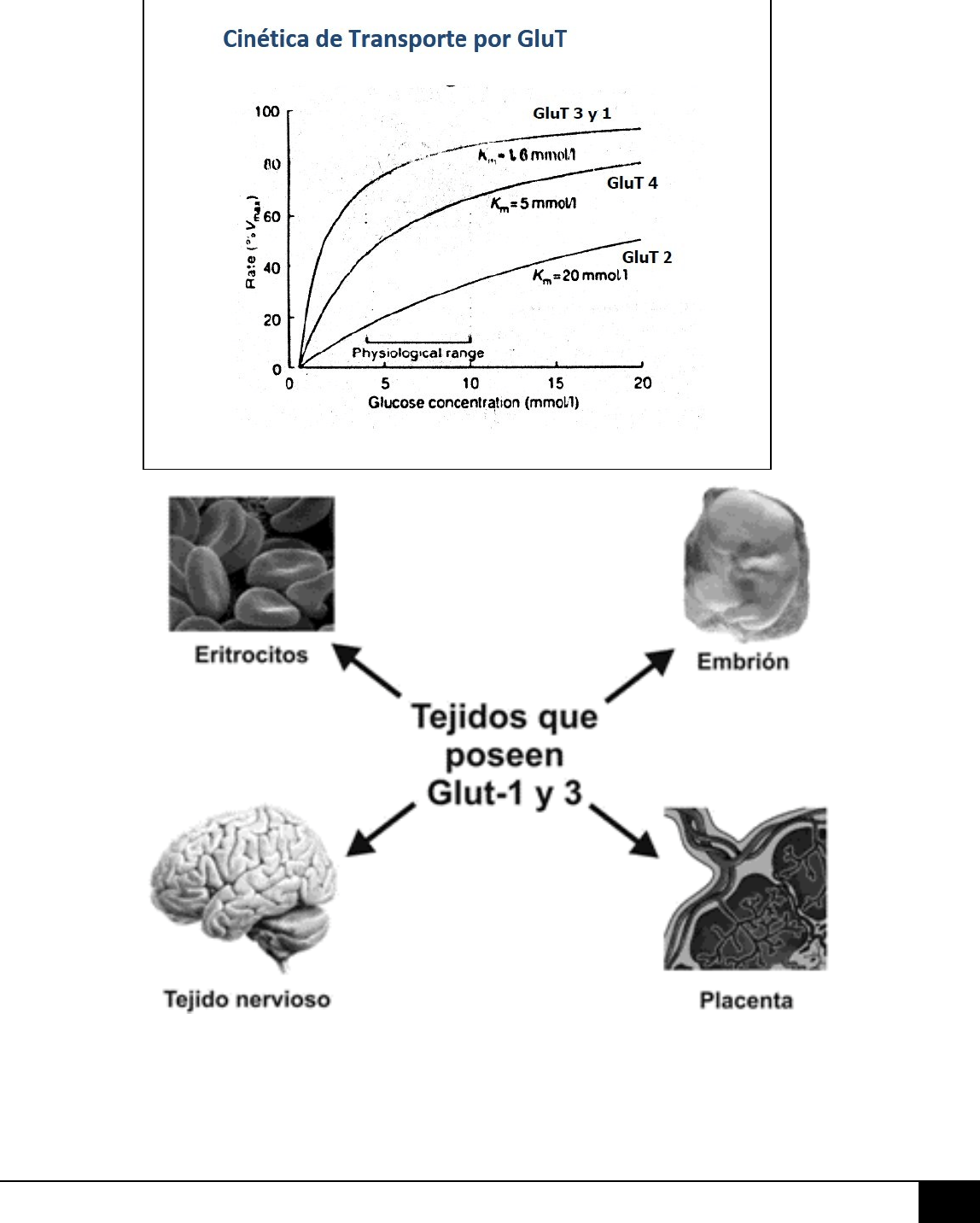
AFINIDAD POR LA GLUCOSA (Km):
GLUT 3 y 1 > GLUT 4 > GLUT 2.

Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
9
22 de noviembre de 2020
NO HAY QUE OLVIDAR QUE EL SENTIDO DEL TRANSPORTE DE LA GLUCOSA VA A DEPENDER DE SU
GRADIENTE DE CONCENTRACIÓN.
En
HÍGADO predomina el GLUT-2, su Km es alto porque tiene baja afinidad con la glucosa en
comparación con otros miembros de su familia. Esto tiene un aspecto funcional debido a que, como su
afinidad por la glucosa es baja, hará entrar glucosa al hígado CUANDO LA CONCENTRACIÓN DE GLUCOSA
ES ALTA. Esto es en período posprandial, y tiene como objetivo, aumentar las reservas de glucógeno. Esto
quiere decir que el transporte de glucosa a través del GLUT-2 es PROPORCIONAL A LA CONCENTRACIÓN
DE GLUCOSA EN SANGRE.
En los
TEJIDOS SENSIBLES A INSULINA (LINFOCITOS, ADIPOCITOS, MIOCITOS) predomina el GLUT-4,
aquí el
transporte de glucosa es DEPENDIENTE DE INSULINA. En este tipo de tejidos, los transportadores
en ausencia de insulina están insertos en la membrana de vesículas transportadoras. Cuando la glucemia
está alta, y las células beta-pancreáticas liberan insulina, los receptores de insulina de la membrana de
linfocitos, adipocitos y miocitos, realizan una cascada de reacciones (que involucran acciones de
proteínas kinasas) que incitan a la liberación de esos transportadores en la membrana plasmática,
aumentando así la captación de glucosa. Por lo tanto, la insulina afecta el parámetro de Vmáx.
El Km de los GLUT 3 y 1 es muy bajo, de hecho, es menor que el rango fisiológico, lo que habla de su alta
afinidad por la glucosa. Este aspecto es muy necesario si se toma en cuenta que esto transportadores
están principalmente en TEJIDO NERVIOSO, el cual debe tener una provisión constante de glucosa,
independiente a su concentración en sangre. Por eso se dice que aquí el transporte de glucosa NO ES
PROPORCIONAL A LA CONCENTRACIÓN DE GLUCOSA EN SANGRE.
Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
10
22 de noviembre de 2020
Elisa Lara. Cátedra de Bioquímica. Medicina, UNCo.
11
22 de noviembre de 2020

TEÓRICO IV GLUCÓLISIS.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.