
!
1!
CALOR Y TEMPERATURA
1. Introducción
2. Equilibrio térmico y temperatura
3. Gases ideales
4. Dilatación térmica
5. Calorimetría
6. Propagación del calor
1.- INTRODUCCIÓN
En este tema y en el siguiente desarrollaremos algunas de las ideas
que constituyen las bases de la Termodinámica y, en particular, en este tema
introduciremos los conceptos de calor y temperatura.
La Termodinámica es la parte de la Física que se dedica al estudio de
las transformaciones de energía donde intervienen calor, trabajo mecánico y
otros aspectos de la energía, así como la relación que existe entre
transformaciones y las propiedades de la materia.
Inicialmente la Termodinámica surgió del estudio de la producción de
trabajo mecánico a partir de fuentes de calor y su interés se centró en las
aplicaciones técnicas de las máquinas térmicas. Sin embargo, hoy en día la
Termodinámica interviene con amplitud en dominios de la Física (fenómenos
superficiales, pilas, magnetismo), de la Química (reacciones químicas,
equilibrios), de la Ingeniería (refrigeración, turbinas, motores), de la Biología
(fenómenos bioenergéticos), de la Meteorología (humedad, predicción del
tiempo), etc. Dede un punto de vista histórico, la Termodinámica se desarrolló
durante los siglos XVIII y XIX cuando las nociones de calor y temperatura no
se comprendían completamente. Evolucionó hasta constituir una teoría formal
y elegante cuyos resultados y métodos llegaron a ser extremadamente
importantes para fines de ingenierÍa. debido a que más o menos por aquella
época se desarrollaron las máquinas de vapor.
Puede decirse que la Termodinámica clásica estudia aquellos
fenómenos físicos macroscópicos relacionados con el calor y la temperatura.
limitándose al estudio de los estados de equilibrio y a las transformaciones
que pueden representarse por una serie continua de estados de equilibrio.
Una muestra de sustancia. tanto si es sólida. líquida o gaseosa. Puede
describirse de dos formas básicas:
Augusto Beléndez Vázquez
Departamento de Física, Ingeniería de Sistemas y Teoría de la Señal
Universidad de Alicante (2017)
!
2!
(a) En función de los átomos y moléculas que la constituyen, de las
interacciones entre estos componentes y de los límites impuestos por la forma
de la muestra o del recinto que la contiene. Esta descripción recibe el nombre
de microscópica y su estudio corresponde a la Teoría Cinética y a la Mecánica
Estadística.
(b) En función de las propiedades macroscópicas de la muestra, que
pueden determinarse por medidas prácticas; estas medidas sólo detectan
valores medios de las coordenadas atómicas de las partículas. Tales son la
masa, el volumen, la densidad, la presión, la temperatura, el calor específico,
la constante dieléctrica, los módulos de elasticidad, etc. Este tipo de
descripción, característica de la Termodinámica, recibe el nombre de
macroscópica.
La Termodinámica es, pues, una disciplina “fenomenológica”, que
estudia los fenómenos que ocurren en los sistemas desde un punto de vista
macroscópico en función de las propiedades físicas observables y medibles.
Por ello, no realiza ninguna hipótesis sobre la constitución íntima de la
materia y sus principios son independientes de una imagen molecular. La
validez de sus ecuaciones descansa en la creencia de que los fenómenos físícos
cumplen hoy, y seguirán cumpliendo siempre, los llamados principios
termodinámicos, extraídos de nuestra experiencia en el mundo macroscópico
en que vivimos.
Algunas de las magnitudes macroscópicas que se utilizan en
Termodinámica son la presión, p, de un gas o fuerza por unidad de área que
ejerce el gas sobre una superficie, el volumen, V, de ese gas o el número de
moles, n, que especifica la cantidad de gas. Otras magnitudes macroscópicas
son la temperatura, T, la energía interna, U y la entropía, S. Estas propiedades
caracterizan al sistema, de modo que el estado de un sistema termodinámico
se describe mediante los valores que poseen dichas magnitudes.
2.- EQUILIBRIO TÉRMICO Y TEMPERATURA
2.1.- Equilibrio térmico
El estado de equilibrio de un sistema físico depende de la proximidad
de otros sistemas y de la naturaleza de la superficie que les separa. Si esta
superficie es buena conductora del calor, la experiencia nos dice que el
sistema modifica su estado hasta alcanzar un nuevo equilibrio: se trata de una
superficie diatérmica. Por ejemplo. si se aproxima un vaso metálico que
contiene una mezcla de agua con hielo a un radiador eléctrico se observa como
!
3!
el hielo se funde. La pared del vaso es una pared diatérmica. En cambio. si la
superficie de separación está formada por una sustancia mala conductora. el
equilibrio del sistema no se modifica y la superficie es adiabática. Es lo que
ocurre si la mezcla de agua con hielo está encerrada en un vaso Dewar de
dobles paredes con vacío entre ambas.
Admitimos que todo sistema no en equilibrio sometido a condiciones
exteriores constantes alcanza finalmente un estado de equilibrio (postulado de
existencia del equilibrio termodinámico).
2.2.- Principio cero de la Termodinámica
Cuando un sistema A está en contacto prolongado con un sistema B a
través de una pared diatérmíca, se dice que los dos sistemas están en contacto
“térmico”. Sus variables termodinámicas se modifican espontáneamente y
cuando esta evolución se detiene se dice que los sistemas han alcanzado “el
equilibrio térmico”.
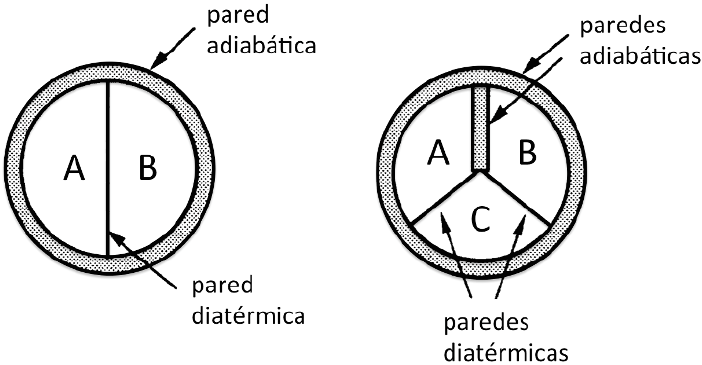
Supongamos que tenemos ahora tres sistemas A, B y C como se
muestra en la figura, de modo que A y B están separados mediante una pared
adiabática, pero ambos están en contacto térmico con el sistema C a través de
una pared diatérmica. Por tanto A y B están en equilibrio térmico con C. La
experiencia nos dice que entonces A y B están en equilibrio térmico entre sí.
Estos resultados constituyen el llamado principio cero de la
Termodinámica, que puede enunciarse del siguiente modo:
(a) Dos sistemas aislados. A y B. puestos en contacto prolongado
alcanzan el equilibrio térmico.
!
4!
(b) Si dos sistemas A y B separadamente están en equilibrio térmico
con un tercero, C, están también en equilibrio térmico entre sí (propiedad
transitiva).
El concepto de temperatura está íntimamente relacionado con el
estado de equilibrio térmico entre dos sistemas. Así, dos sistemas en equilibrio
térmico tienen la misma temperatura. Si dos sistemas se ponen en contacto y,
al hacerlo, sus variables termodinámicas comienzan a cambiar, entonces los
sistemas no estaban a la misma temperatura; sin embargo, llegarán a estar a
una temperatura común cuando se alcance el equilibrio térmico. El principio
cero es la base de las medidas termométricas. Dos cuerpos A y B están a igual
temperatura cuando puestos por separado en contacto con un termómetro C,
éste indica valores iguales en su escala.
2.3.- Temperatura, termómetros y escala de temperaturas del gas ideal
La temperatura se describe subjetivamente en términos tales como
“caliente” y “frío”, de modo que “caliente” corresponde a una temperatura más
alta que “frío”. Sin embargo, estos términos no tienen un significado objetivo
consistente: Podemos apreciar variaciones de temperatura de acuerdo con las
variaciones de intensidad de estas sensaciones, pero el sentido del tacto carece
de sensibilidad y alcance necesarios para dar una forma cuantitativa de esta
magnitud.
Las variaciones de temperatura de un cuerpo van casi siempre
acompañadas de una variación de las magnitudes observables o
macroscópicas que caracterizan el estado de dicho cuerpo. Así ocurre, por
ejemplo, con la longitud de una columna líquida o de un alambre, la
resistencia eléctrica de un metal, la presión (o el volumen) de un gas a
volumen (o presión) constante, etc. Teniendo esto en cuenta, podemos decir
que:
“Un termómetro es cualquier dispositivo o sistema que se utiliza para
conectar el valor de una de sus variables observables con la temperatura”.
Un termómetro deberá tener algunas características importantes. La
propiedad que los caracterice (longitud, presión, resistencia, etc.) deberá variar
con la temperatura de una manera fácilmente medible. Sus indicaciones
deberán ser reproducibles y su construcción debe ser tal que pueda duplicarse
fácilmente. La sensibilidad de sus indicaciones no deberá depender del tipo de
material utilizado en su construcción, y deberá ser capaz de medir
temperaturas en un margen amplio.
!
5!
Para definir una escala termométrica, T, se elige una función
termométrica, x, normalmente lineal
T = ax + b.
La pendiente a y la ordenada
en el origen b pueden determinarse definiendo arbitrariamente la temperatura
de dos estados reproducibles de algún sistema patrón. Otra posibilidad es
elegir b = O y determinar a definiendo arbitrariamente la temperatura de un
solo estado patrón y entonces
T = ax.
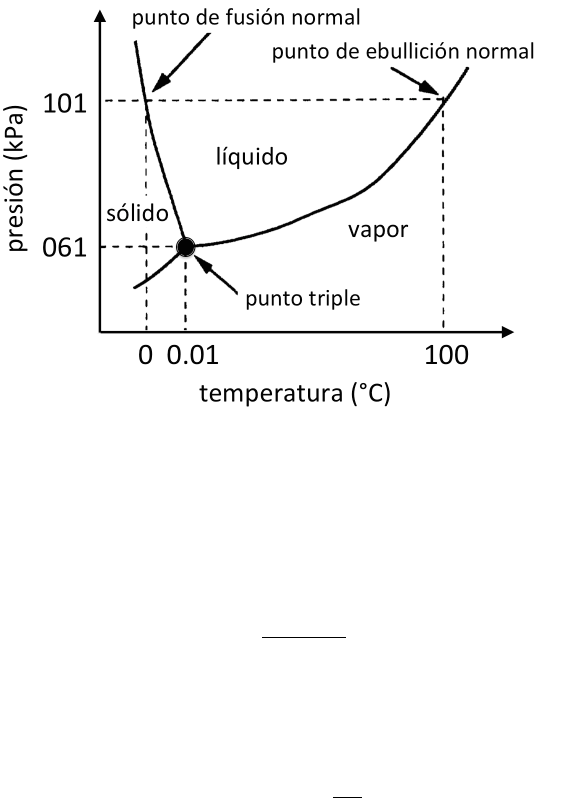
Por convenio, se elige el punto triple
del agua como dicho estado patrón. En este punto coexisten en equilibrio el
hielo, el agua líquida y el vapor de agua y este equilibrio se verifica a una
presión de 4.58 Torr (610 Pa) y a una temperatura determinada.
Arbitrariamente se le atribuye la temperatura de 273.16 K (kelvin) que
corresponde a una temperatura de 0.010º C en la escala familiar de grados
centígrados. Por tanto el kelvin, unidad de temperatura en el S.I., es la
fracción 1/273.16 de la temperatura del punto triple del agua.
Con este criterio, si x es la variable termométrica, la temperatura T
correspondiente está relacionada con x mediante la relación
T = a x.
Llamando
x
3
al valor de x a la temperatura del punto triple del agua, se cumplirá:
a =
273.16
x
3
!
!
y, por tanto, para cualquier otra temperatura:
T = 273.16
x
x
3
!
!
ecuación que define perfectamente la escala de temperatura.
!
6!
Ejemplos de termómetros son el termómetro de mercurio (ya en
prohibidos) en el cual la magnitud termométrica x es la longitud de una
columna de mercurio dentro de un capilar de vidrio. El termopar, que
consiste en dos empalmes de dos alambres de metales diferentes. Si uno de los
empalmes (o soldaduras) se mantiene a una temperatura de referencia (como
un baño de agua y hielo) y el otro a otra temperatura distinta, existirá una
diferencia de potencial entre ambos empalmes. Esta diferencia de potencial se
utiliza para medir la temperatura. Otro termómetro eléctrico es el termómetro
de resistencia, basado en que la resistencia eléctrica de un conductor (el
termómetro) varía con la temperatura.
Se elige como termómetro patrón el termómetro de gas a volumen
constante, operando en condiciones tales que el resultado de la medida sea
independiente del gas elegido (gas ideal). Consta de una cámara que contiene
un gas y de un mecanismo para asegurar que el volumen ocupado por el gas
permanezca constante. En él se mide la presión, y ésta sirve para determinar
la temperatura, eligiendo que la temperatura sea proporcional a la presión del
gas.
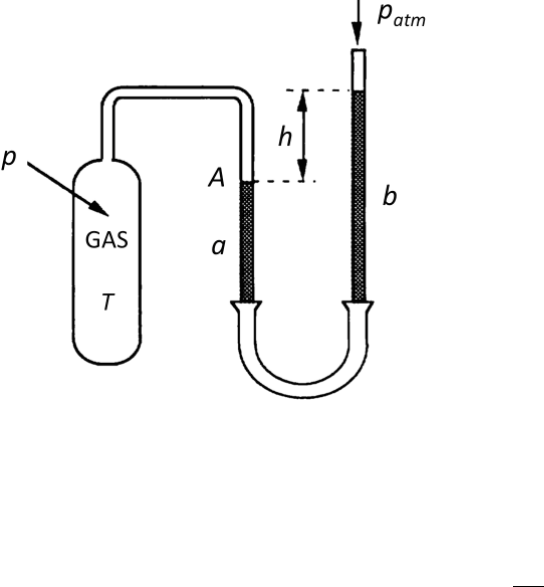
El volumen del gas se mantiene
constante ajustando el mercurio de
modo que la parte superior de la
columna a esté siempre en un mismo
punto capilar A. La presión se mide
observando la diferencia de alturas h
entre las columnas a y b, de modo
que:
p = p
atm
+
ρ
gh
!
donde
ρ
es la densidad del mercurio y
g la aceleración de la gravedad.
Si p
3
es la presión del recinto que contiene el gas cuando éste se
encuentra a la temperatura del punto triple, la temperatura T vendrá dada por
la expresión:
T = 273.16
p
p
3
!
!
siendo p la presión medida.!
Cuanto menor es la presión del gas, la temperatura es más baja, de
modo que cuando p tiende a cero, T también tiende a cero, el cero absoluto de
temperatura.

!
7!
El gas más útil para este tipo de termómetros es el helio, que
permanece gaseoso a las más bajas temperaturas, aunque también suele
utilizarse hidrógeno. Las temperaturas así definidas se llaman temperaturas
absolutas o del gas ideal, pues prácticamente coinciden con las definidas
mediante el gas ideal, en el que se verifica
T /T
0
= p / p
0
.
Otras escalas de temperatura son las siguientes:
(a) Escala Celsius o centígrada, t
C
, en la que la temperatura del punto
de fusión normal del agua corresponde a 0° C y la del punto de ebullición
normal a 100° C. Podemos escribir:
t
C
= T − 273.15
!
(b) Escala Fahrenheit, t
F
, en la que la temperatura del punto de
fusión normal del agua corresponde a 32° F, y la del punto de ebullición
normal a 212° F. Podemos escribir:
t
F
=
9
5
t
C
+ 32
!
t
C
=
5
9
t
F
+ 32
( )
!
(c) Escala Réamur, t
R
, en la que la temperatura del punto de fusión
normal del agua corresponde a 0° R y la del punto de ebullición normal a 80°
R, de modo que:
t
R
=
4
5
t
C
!
3.- GASES IDEALES
3.1.- Ecuación de estado de los gases ideales
Las condiciones en que existe un material dado se describen con
cantidades físicas como presión (p), volumen (V), temperatura (T) y cantidad de
sustancia (n). Estas variables describen el estado del material y se llaman
variables de estado.
El gas ideal es un modelo idealizado que funciona mejor a presiones
muy bajas y altas temperaturas, cuando las moléculas del gas están muy
separadas y en rápido movimiento. La ecuación de los gases ideales es:
!
8!
pV = nRT
donde p es la presión, V el volumen, n el número de moles, T la temperatura
absoluta y R la constante de los gases ideales, cuyo valor numérico depende de
las unidades del resto de magnitudes físicas que aparecen en la ecuación. En
unidades del SI con p en Pa, V en m
3
, n en mol y T en K:
R = 8.31 J
.
mol
-1
.
K
-1
Si p se expresa en atmósferas (atm) y V en litros (L), entonces la constante de
los gases ideales se expresa en la forma:
R = 0.082 atm
.
L
.
mol
-1
.
K
-1
Para una cantidad fija de gas (n = constante) y dos estados 1 y 2, se
cumple:
p
1
V
1
T
1
=
p
2
V
2
T
2
!
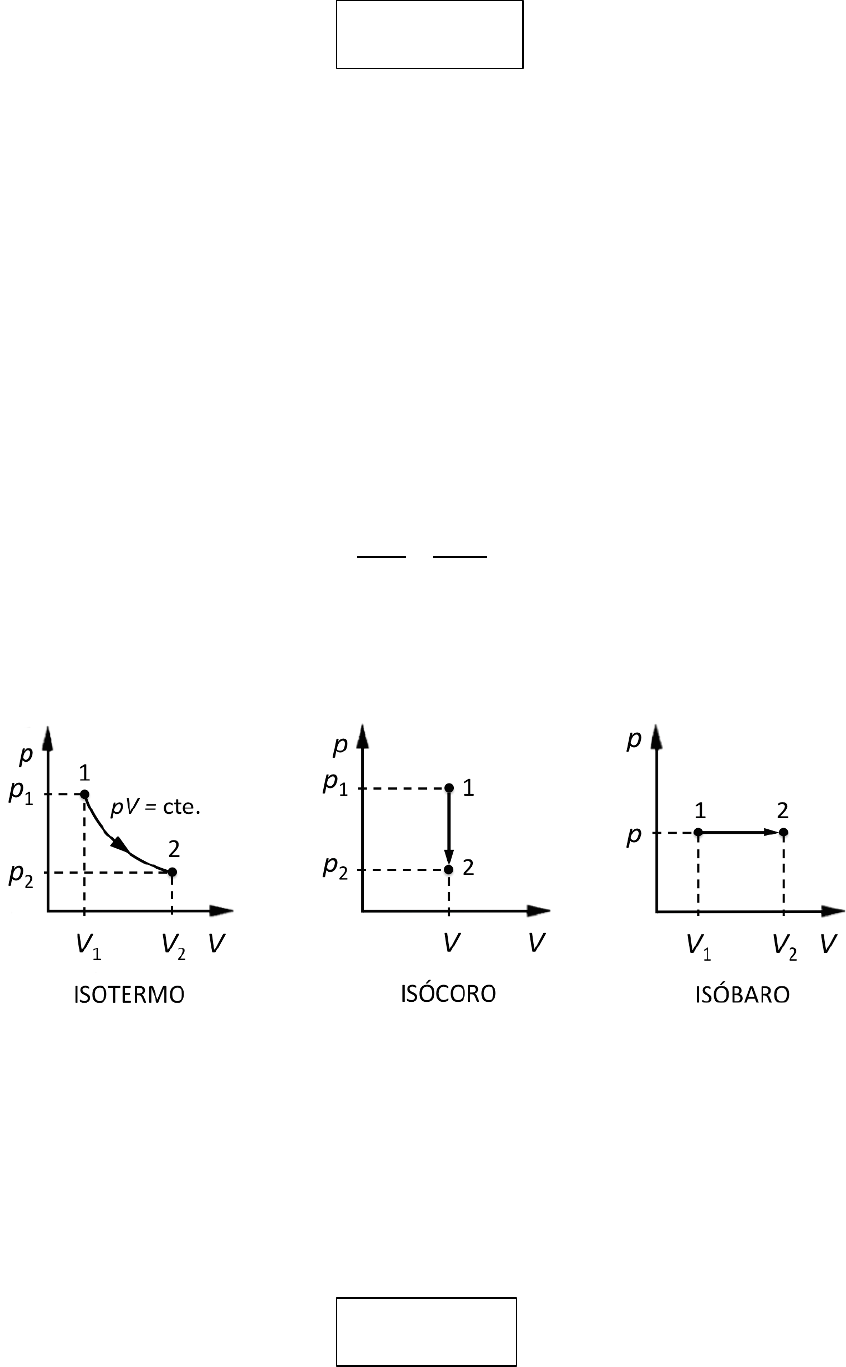
Vamos a considerar los casos a temperatura constante (isotermo), volumen
constante (isócoro) y presión constante (isóbaro).
!!!!!!!!!!!!!!!! !!!!!!!!!!!!!! !
3.2.- Ley de Boyle-Mariotte
Para un proceso isotermo, es decir, a temperatura constante (T =
constante) y para una cantidad fija de gas (n = constante), se cumple:
pV = constante
que escrita para dos estados 1 y 2 toma la forma:
p
1
V
1
= p
2
V
2
!
que es la ley de Boyle-Mariotte.

!
9!
3.3.- Ley de Gay-Lussac
Para un proceso isócoro, es decir, a volumen constante (V = constante)
y para una cantidad fija de gas (n = constante), se cumple:
p
T
=
constante
que escrita para dos estados 1 y 2 toma la forma:
p
1
T
1
=
p
2
T
2
!
que es la ley de Gay-Lussac.
3.4.- Ley de Charles
Para un proceso isóbaro, es decir, a presión constante (P = constante)
y para una cantidad fija de gas (n = constante), se cumple:
V
T
=
constante
que escrita para dos estados 1 y 2 toma la forma:
V
1
T
1
=
V
2
T
2
!
que es la ley de Charles.
4.- DILATACIÓN TÉRMICA
La mayoría de las sustancias se expanden o dilatan al aumentar la
temperatura y se contraen cuando ésta disminuye.
4.1.- Dilatación lineal
Consideremos una barra cuya longitud L
0
a una temperatura T
0
pasa
a ser L a otra temperatura T. La variación
ΔL = L − L
0
es el cambio de longitud
de la barra debido al cambio de temperatura. Experimentalmente se encuentra
!
10!
que ∆L es proporcional al cambio de temperatura
ΔT = T − T
0
y a la longitud
inicial de la barra L
0
. Esto es:
ΔL =
α
L
0
ΔT
siendo
α
una constante de proporcionalidad, distinta para cada sustancia, que
se denomina coeficiente de dilatación lineal.
De la ecuación anterior podemos escribir:
L = L
0
(1 +
α
ΔT )
y también:
y en el límite cuando T tiende a cero, entonces:
α
= lim
ΔT →0
1
L
0
ΔL
ΔT
=
1
L
0
dL
dT
Por ejemplo, para el alumimio
α
= 2.4 x 10
-5
K
-1
y para el hormigón
α
=
0.7 - 1.4 x 10
-5
K
-1
.
4.2.- Dilatación superficial
Cuando se calienta una lámina de material, aumenta tanto su
longitud como su anchura. Consideremos una lámina rectangular de lados a
0
y b
0
a la temperatura T
0
. Si se calienta a la temperatura T, estas dimensiones
se convierten en:
α
=
1
L
0
ΔL
ΔT

!
11!
a = a
0
(1 +
α
ΔT )
!
b = b
0
(1 +
α
ΔT )
!
!
Si el área inicial de la lámina era
S
0
= a
0
b
0
, su área después de
calentada será:
S = ab = a
0
b
0
(1 +
α
ΔT )(1 +
α
ΔT ) = S
0
[1 + 2
α
ΔT + (
α
ΔT )
2
]
Como
α
tiene un valor pequeño,
α
2
aún será más pequeño y el término
(
α
ΔT )
2
puede despreciarse. Por tanto:
S = S
0
(1 + 2
α
ΔT )
Si definimos el coeficiente de dilatación superficial
γ
tal que:
S = S
0
(1 +
γ
ΔT )
se deduce que
γ
= 2
α
.
También podemos calcular
γ
mediante:
γ
=
1
S
0
dS
dT
Aunque este resultado se ha deducido para el caso especial de una
lámina rectangular, sigue cumpliéndose para una lámina de forma cualquiera.
4.3.- Dilatación cúbica o volumétrica
!
12!
V = V
0
(1 + 3
α
ΔT )
!
siendo V el volumen a la temperatura T y V
0
el volumen a la temperatura T
0
.
Además
β
= 3
α
es el coeficiente de dilatación cúbica o volumétrica de la
sustancia, de modo que:
V = V
0
(1 +
β
ΔT )
Esta ecuación se cumple independientemente de la forma del cuerpo. También
podemos definir el coeficiente de dilatación cúbica mediante la siguiente
expresión:
β
=
1
V
0
dV
dT
!
Por ejemplo, para el mercurio
β
= 18 x 10
-5
K
-1
y para el metanol
β
=
112 x 10
-5
K
-1
.
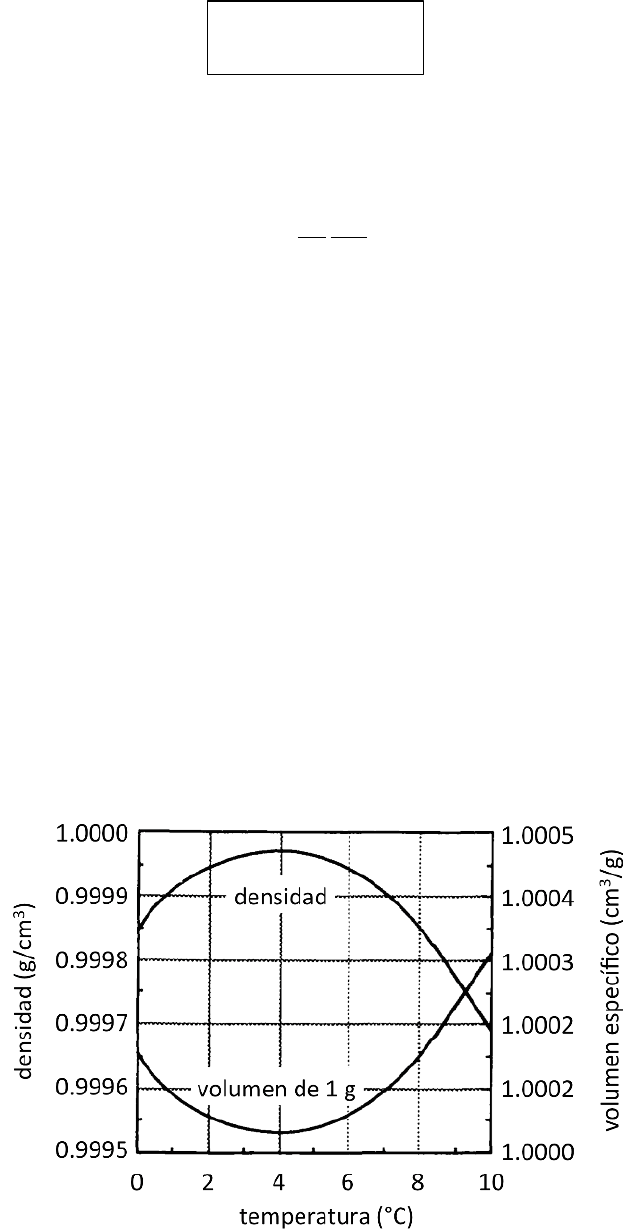
El agua, como puede verse en la siguiente figura, presenta una
situación anómala, pues en el intervalo de temperaturas comprendido entre 0
°C y 4 °C disminuye el volumen al crecer la temperatura, comportamiento
contrario al de la mayor parte de las sustancias. Esto es, entre 0 ºC y 4 ºC el
coeficiente de dilatación del agua es negativo. Por encima de los 4 °C el agua se
dilata cuando se calienta. Como el volumen de una masa dada de agua es más
pequeño a 4 °C que a cualquier otra temperatura, la densidad del agua es
máxima a 4 °C. A esta propiedad del agua se debe el que los lagos y estanques
se hielan primero por su superficie libre, pues el hielo debido a su menor
densidad se sitúa en la superficie libre del liquido y aísla el resto del agua de
nuevas pérdidas caloríficas. La expansión térmica anómala del agua se debe a
la interacción de las moléculas del agua, que posee una forma inusual.

!
13!
5.- CALORIMETRÍA
La energía transferida a través de los límites de un sistema debido a
una diferencia de temperaturas, constituye el calor. En esta definición viene
implícito el hecho importante de que un cuerpo no contiene calor, sino que
sólo denominamos con este nombre la energía en tanto cruza los límites. Es
decir, el calor es un fenómeno transitorio. Si consideramos el cuerpo caliente
como un sistema y el frío como otro. llegamos a la conclusión de que
originalmente ni uno ni otro contienen calor (contienen energía. desde luego).
Al poner ambos sistemas en comunicación térmica el calor se transfiere del
cuerpo caliente al frío hasta que se establece el equilibrio térmico. La
temperatura es como un potencial que gobierna el paso de calor.
Puesto que el calor es una forma de energía, debe medirse en
unidades energética. y. por tanto, en Julios en el S.I. Una unidad práctica del
calor es la caloría (cal), que vale:
1 cal = 4.186 J
Fue Joule el que encontró este equivalente mecánico del calor, en un
dispositivo formado por un calorímetro lleno de agua y en cuyo interior había
una paletas conectadas a un eje que giraba mediante un mecanismo formado
por una masa m unida a un hilo. Si inicialmente la masa está en reposo, al
bajar una altura h disminuye su energía potencial en un valor mgh, aumenta
su energía cinética en
1
2
mv
2
y comprobó que también aumentaba la
temperatura del agua en un valor ∆T debido a que pasa energía calorífica al
agua a causa de la fricción de las paletas con el agua. Se cumplirá:
mgh −
1
2
mv
2
= J M ΔT
donde M es la masa del agua contenida en el calorímetro y J es el equivalente
mecánico del calor, cuyo valor es J = 4.186 J/cal.
5.1.- Capacidad calorífica y calor específico
Si se mete una cucharita fría en una taza de café caliente, la cuchara
se calienta y el café se enfría para acercarse al equilibrio térmico. La
interacción que causa estos cambios en la temperatura es básicamente una
transferencia de energía de una sustancia a otra. La transferencia de energía
que se da exclusivamente por una diferencia de temperatura se llama flujo de
calor o transferencia de calor, y al energía transferida se llama calor. Usamos el
símbolo Q para la cantidad de calor.
!
14!
La caloría es la cantidad de calor necesaria para elevar la
temperatura de 1 g de agua de 14.5ºC a 15.5ºC. La relación entre el julio y la
caloría es:
1 cal = 4.186 J 1 J = 0.24 cal
Consideremos un sistema formado por un cuerpo homogéneo. al cual
se entrega una cierta cantidad de calor dQ. La experiencia nos dice que, en
ausencia de cambios de fase. la temperatura del cuerpo se modifica en un
valor dT. Teniendo esto en cuenta. se denomina capacidad calorífica molar,
C, a una magnitud física relacionada con dQ y dT mediante las ecuaciones:
dQ = n C dT C =
1
n
dQ
dT
Q = n C ΔT = n C (T
f
− T
i
)
donde dQ/dT no puede interpretarse como la derivada de Q respecto de T, ya
que Q no es una propiedad del sistema y, por tanto,
Q ≠ f (T ).
La notación dQ
representa simplemente que una pequeña cantidad de calor dQ ocasiona el
cambio de temperatura dT. Por otra parte, C, que es la capacidad calorífica
molar, en el S.I. se mide en J K
-1
mol
-l
.
Normalmente el proceso no viene definido completamente por la
variación de la temperatura. sino que es necesario conocer otras magnitudes
macroscópicas. Los procesos principales son a presión constante y a volumen
constante.
En un sistema pVT la capacidad calorífica a presión constante, C
p
,
verifica la ecuación:
dQ = n C
p
dT C
p
=
1
n
dQ
dT
⎛
⎝
⎜
⎞
⎠
⎟
p=cte
Q = n C
p
ΔT = n C
p
(T
f
−T
i
)
Del mismo modo, la capacidad calorífica a volumen constante, C
v
, cumplirá:
dQ = n C
V
dT C
V
=
1
n
dQ
dT
⎛
⎝
⎜
⎞
⎠
⎟
V =cte
Q = n C
V
ΔT = n C
V
(T
f
−T
i
)
Si lo que se considera es la masa m del sistema, tenemos el calor
específico, c, que en el caso de sólidos y líquidos suele ser en condiciones de
presión constante:
!!!!!
dQ = m c dT c =
1
n
dQ
dT
Q = m c ΔT = n c (T
f
− T
i
)
!
15!
En el S.I. los calores específicos se miden en
J / kg ⋅ K.
Para el agua el
calor específico (a presión constante) es
c = 1 cal / g ⋅ºC
o bien 4186
J / kg ⋅ K.
5.2.- Cambio de estado y calor latente
Cuando se aporta calor a una sustancia puede producirse un efecto
importante y es el denominado cambio de estado o cambio de fase. Al variar
su temperatura por dicha aportación de calor. se pueden modificar de forma
importante las distancias entre sus moléculas. al producirse la variación. En
mayor o menor grado. de las fuerzas de cohesión que las mantienen unidas.
dando lugar a que estas moléculas adquieran una nueva distribución y, por
tanto, un nuevo estado. Casi la totalidad de las sustancias conocidas pueden
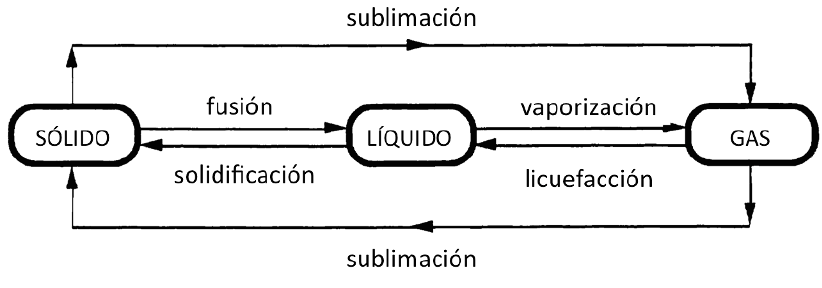
presentarse en tres estados diferentes: sólido. líquido y gaseoso.
Las denominaciones de los pasos de uno a otro estado aparecen en el
siguiente diagrama:
Prácticamente todos los cambios de estado se rigen por unas mismas
leyes que se pueden sintetizar en:
(a) En igualdad de condiciones. todo cambio de estado se produce
siempre a una temperatura determinada.
(b) Mientras se está produciendo un cambio de estado, cediendo o
absorbiéndose calor, no varia la temperatura del sistema.
El proceso de los sucesivos cambios de estado que puede sufrir una
sustancia queda descrito en el esquema de la siguiente figura. Aunque este
diagrama está aplicado al caso del agua a presión atmosférica, es asimismo
válido para cualquier sustancia, con el consiguiente cambio de valores.
Este documento contiene más páginas...
Descargar Completo
Tema-4-Calor-y-temperatura.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.