Reacciones químicas: Reactivos → productos. Se representan mediantes ecuaciones
químicas.
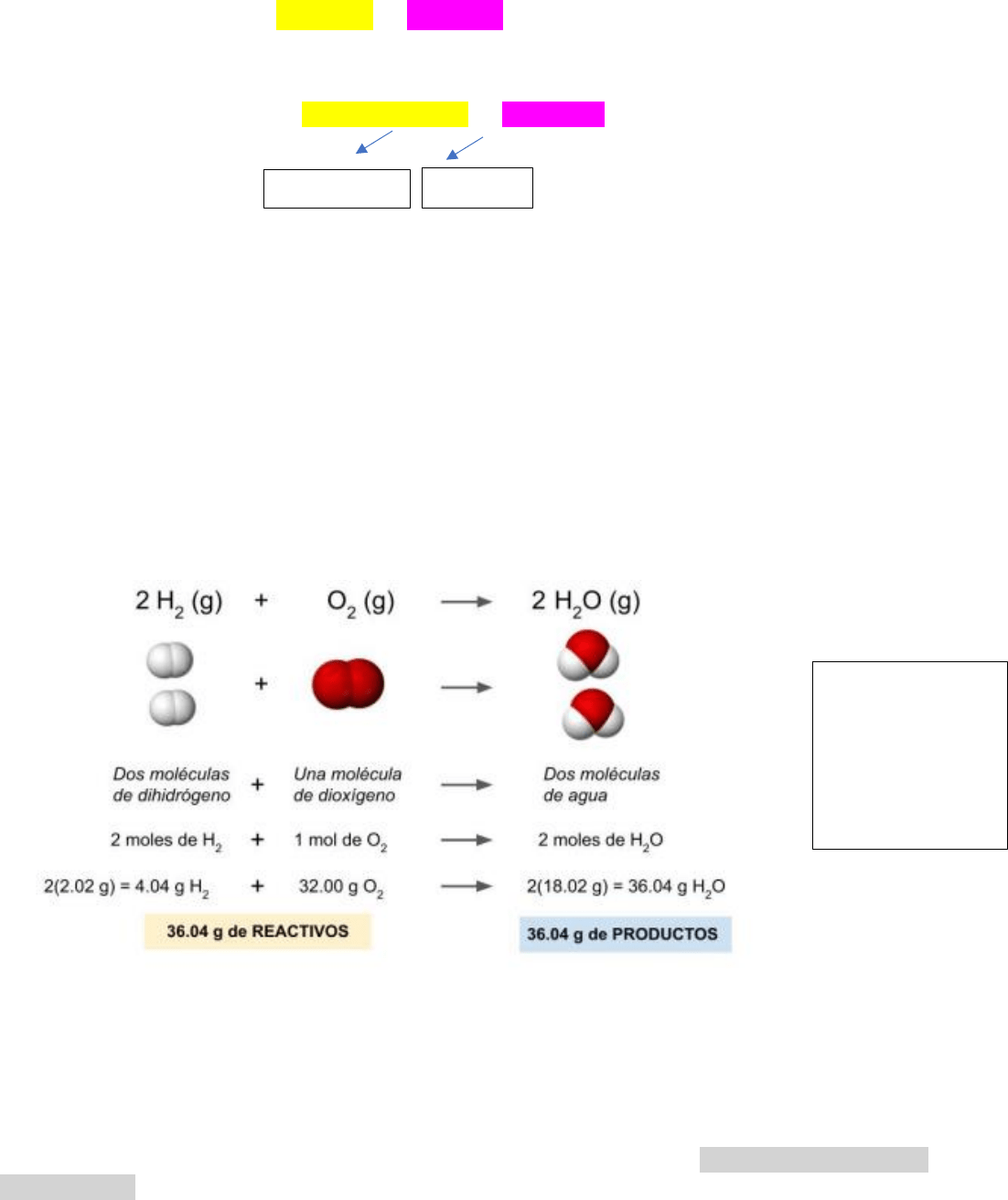
Por ejemplo, para la reacción simple de combustión del hidrógeno gaseoso escribimos la
ecuación química como sigue: 2 H2 (g) + O2 (g) → 2 H2O (g).
Coeficientes estequiométricos: indican cuantas moléculas de cada sustancia participan en la
reacción. Lo único que cambia es la cantidad de la sustancia, no su identidad. EJ: 2 H2O
Es diferente a un subíndice. Si cambia el mismo cambia la identidad de la sustancia. La sustancia
H2O2’ peróxido de hidrógeno o agua oxigenada, es muy diferente del agua.
Dado que en ninguna reacción se crean ni se destruyen átomos, toda ecuación química debe
tener igual número de átomos de cada elemento a ambos lados de la flecha. Cuando se satisface
esta condición se dice que la ecuación está balanceada.
Es común agregar más información a las fórmulas de las ecuaciones balanceadas para indicar
entre paréntesis el estado físico de cada reactivo y producto. Usamos los símbolos (g), (l), (s) y
(ac) para gas, líquido, sólido y disolución acuosa (en agua).
Introducción a la termodinámica y cinética química: estudian si las reacciones químicas
pueden ocurrir o no y a qué velocidad lo hacen.
Termoquímica: rama de la termodinámica que estudia los cambios energéticos de las reacciones.
Indica si la reacción ocurrirá o no pero no la velocidad de la misma Una de las funciones más
utilizadas son la energía libre de Gibbs (G) o simplemente energía libre: se encarga de informar si
la reacción utilizará energía adicional o tendrá lugar sin aportar energía. ΔG = ΔG productos −
ΔG reactivos
La reacción de combustión del hidrógeno, obtenemos la siguiente expresión para la variación de
energía libre de Gibbs: ΔG = 2 ΔG (ΔG 2 ΔG ) H2O − O2 + H2 Conociendo el signo de la variación
de energía libre es posible predecir la espontaneidad de una reacción química, pudiendo darse 3
situaciones:
● ΔG < 0 : Los productos tienen menor energía libre que los reactivos por lo que la reacción ocurre
de forma espontánea y libera energía al ambiente. Estas reacciones se conocen como exergónicas.
Reacción con
produce
Debido a que la
relación del número
de moléculas es
igual a la relación
del número de
moles
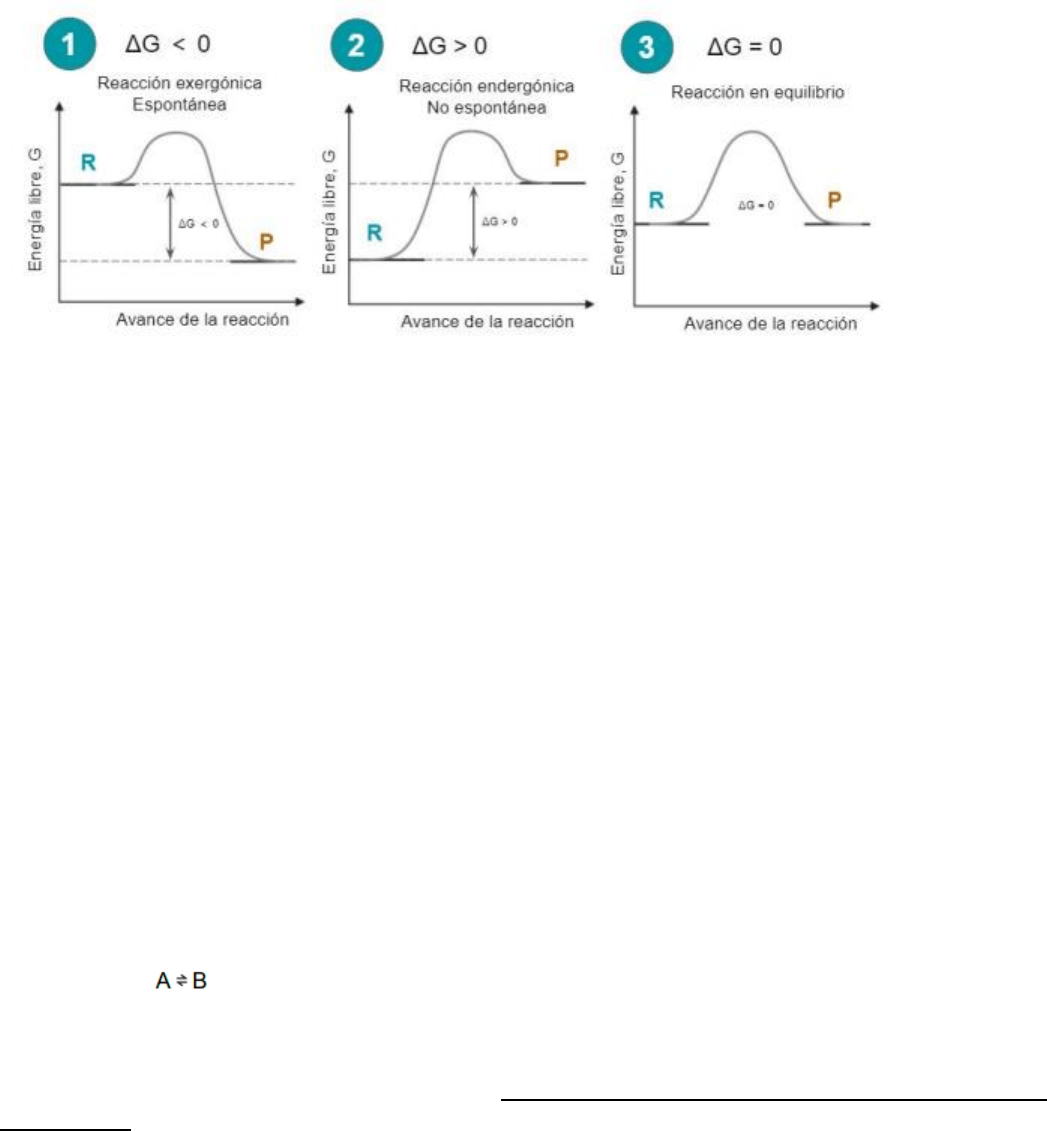
● ΔG > 0 : Los productos tienen mayor energía libre que los reactivos por lo que el signo de la
variación de energía libre es positivo. La reacción no es espontánea en el sentido planteado en la
ecuación química sino que se da en sentido inverso, desde productos a reactivos. Estas reacciones
son llamadas endergónicas.
● ΔG = 0 : Los productos tienen igual energía libre que los reactivos y la reacción se encuentra en
equilibrio. Tanto la reacción directa como inversa ocurren de forma simultánea y a la misma
velocidad. (Equilibrio químico).
Cinética química: estudia la velocidad con la que ocurren las reacciones y los mecanismos por los
cuales se dan.
Para que ocurra la rotura y formación de enlaces químicos, de forma previa a la formación de los
productos, se da una distorsión de los enlaces presentes en los reactivos dando lugar a un estado
de transición de mayor energía libre que reactivos y productos. Una vez superada esta barrera
energética, los reactivos se convierten en productos.
La diferencia de energía libre entre el estado de transición y los reactivos= energía de activación.
La energía de activación está relacionada con la velocidad de la reacción. Si se necesita + energía
la reacción tardara más, si se necesita – tardara menos.
Si se quiere acelerar una reacción química existen dos estrategias principales: suministro de
energía (ej. calor) para que los reactivos superen con mayor facilidad la barrera energética, o
disminución de la energía de activación, realizada por sustancias denominadas catalizadores. En
la célula, los catalizadores biológicos por excelencia son las enzimas, que permiten que las
reacciones ocurran en una escala de tiempo compatible con la vida.
Equilibrio químico: Pocas reacciones químicas se dan en una sola dirección, la mayoría son
reversibles ( ) . Tan pronto como se forman algunas moléculas de producto, comienza el
proceso inverso: estas moléculas reaccionan y forman moléculas de reactivo.
Para describir las reacciones químicas es importante conocer la velocidad a la que éstas ocurren.
La velocidad de una reacción se define como la variación de concentración de reactivos o productos
en el tiempo. Por ejemplo, si reacciona 1 mol de reactivo A en 1 minuto, la velocidad de la reacción
es 1 mol/min.
Cuando la reacción alcanza este estado de equilibrio, las concentraciones de reactivos y productos
permanecerán constantes en el tiempo, sin que se produzcan cambios visibles en el sistema. Sin
embargo, a nivel molecular existe una gran actividad debido a que las moléculas de reactivos siguen
formando moléculas de productos, y éstas a su vez reaccionan para formar moléculas de reactivos.
Como las velocidades de interconversión son iguales (reacción directa e inversa), las
concentraciones de reactivos y productos no experimentan un cambio neto en el tiempo, es decir,
se mantienen constantes.
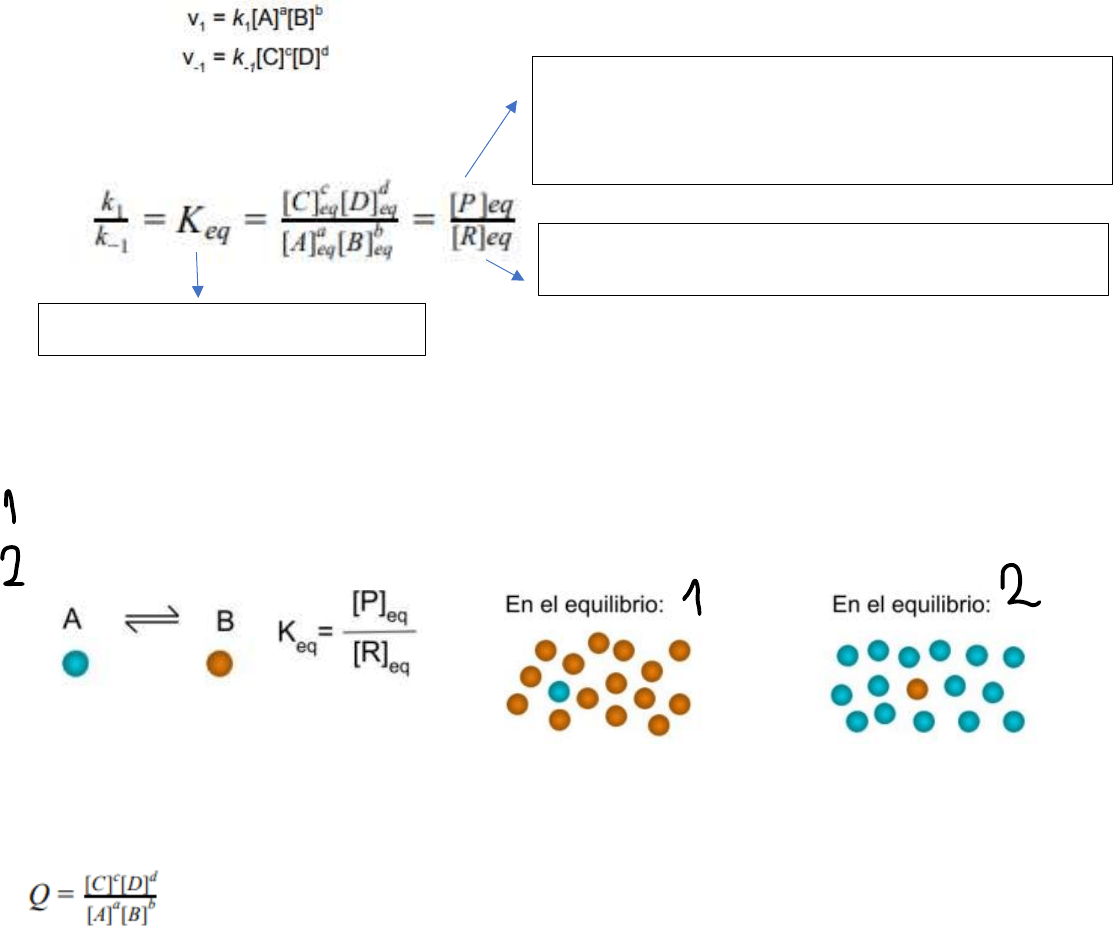
El equilibrio de concentraciones de reactivos y productos no quiere decir que las concentraciones
sean iguales. Ej: puede ocurrir que haya mayor concentración de reactivos o de productos.
Constante de equilibrio Keq: La velocidad de cada reacción está definida por una ley o
ecuación que establece que la velocidad es equivalente a la concentración de reactivos y a una
constante cinética k característica de cada reacción (o constante de velocidad).
el equilibrio las velocidades de la reacción directa e inversa se igualan, por lo que en el equilibrio
v1 = v-1.
Despejando K1 y K-1:
Magnitud de la constante de equilibrio: sirve para saber si se van a producir más reactivos
o más productos.
Keq>1: mayor q de producto. [P]eq mayor a [R]eq.
Keq<1: mayor q de reactivo. [R]eq mayor a [P]eq.
Cociente de acción de masas (Q): sirve para saber si una reacción está en equilibrio o
está alejado de él. Permite predecir la dirección en la cual va a ocurrir el equilibrio. En el equilibrio
se cumple que Q = Keq.
En Q las concentraciones que se utilizan no tienen que ser las de equilibrio como lo son en Keq.
Q>Keq: se favorece la reacción directa.
Q<Keq: se favorece la reacción inversa.
Q=Keq: velocidades de reacción directa e inversa se igualan. Equilibrio.
Multiplicación de las concentraciones de equilibrio de los
productos, cada elevada a una potencia igual a su coeficiente
estequiométrico (cantidad de moléculas de determinada
sustancia).
Lo mismo con las concentraciones de equilibrio de los
reactivos.
Constante para una temperatura dada.

Tema 2. Reacción química y Equilibrio químico.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.