
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
1
Té cnicas histoló gicas
PREPARACIÓN DEL TEJIDO ............................................................................................................................................................................................................. 2
2. FIJACIÓN .................................................................................................................................................................................................................................... 2
3. INCLUSIÓN EN PARAFINA ............................................................................................................................................................................................. 3
6. TINCIÓN ......................................................................................................................................................................................................................................4
OTRAS TÉCNICAS DE TINCIÓN ..............................................................................................................................................................................................4
TINCIONES ESPECIALES PARA TEJIDOS ADIPOSOS Y LÍPIDOS EN GENERAL ............................................................................ 10
INMUNOCITOQUIMICA (INMUNOHISTOQUÍMICA) ......................................................................................................................................... 10
HISTOQUÍMICA ENZIMÁTICA (HISTOENZIMOLOGIA) .................................................................................................................................... 11
RESUMEN ................................................................................................................................................................................................................................................... 11
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
2
PREPARACIÓN DEL TEJIDO
1. TOMA DEMUESTRA
a. necropsia → tejido muerto
b. biopsia→ tejido vivo
i. pinzas
ii. punción
iii. incisional → 1 pedazo
iv. excional→ extracción completa
v. sacabocados
vi. trepanación → taladro quirúrgico
vii. raspado
2. FIJACIÓN
primer paso para conservar la estructura de una muestra. Se logra mediante una sustancia química o mezcla
de estas. Conserva de forma permanente la estructura del tejido para tratamientos posteriores.
a. perfusión
b. inmersión
La muestra debe sumergirse en el fijador inmediatamente después de ser extraída del cuerpo.
VOLUMEN DE SOLUCIÓN TIENE QUE SER 10-20 VECES > QUE EL TAMAÑO DE LA MUESTRA
Se utiliza para:
• detener el metabolismo celular
• impedir la degradación enzimática de las células y los tejidos por autolisis (autodegradación)
• destruir microorganismos patógenos
• endurecer el tejido.
El fijador químico individual mas utilizado es el formol/formalina→formaldehido al 37%, en diluciones variadas
y en combinación con otras sustancias químicas y amortiguadores. Preserva la estructura general de la célula
y de los componentes extracelulares porque reacciona con los grupos amino de las proteínas. mantiene su
capacidad de reaccionar con anticuerpos específicos.
El formaldehido no reacciona con los lípidos, por ende, es mal fijador de las membranas.
1
Toma de
muestra
2
Fijación
3
Inclusión
4
Porceso de
corte
5
Montaje
6
Tinción
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
3
Fijadores físicos → frio, calor, congelación y desecación.
Mezcla fijadora→ bouin (formol, acido acético y acido pícrico) (compuestos).
Otros fijadores:
• para conservar lípidos neutros→ cortes por congelación del tejido fijado en formalina y colorantes que se
disuelven en las grasas.
• Para conservar estructuras de la membrana → fijadores con metales pesados que se unan a los
fosfolípidos.
La composición química de un tejido vivo es muy diferente a un tejido muerto que ha pasado por la acción de
agentes fijadores y de otras reacciones químicas posteriores. Perduran tras la fijación, macromoléculas que no
se disuelven con facilidad: nucleoproteínas, proteínas del citoesqueleto, proteínas extracelulares, componentes
de la membrana celular. Pero hay otras macromoléculas que se pierden si el fijador está en solución acuosa,
como: glucógeno, proteoglucanos y GAG.
3. INCLUSIÓN EN PARAFINA
Su fin es permitir cortes muy delgados.
La sustancia empleada es la parafina→ debido a sus condiciones de penetrabilidad y consistencia.
a. Luego de la fijación la muestra se LAVA y se DESHIDRATA en soluciones alcohólicas de
concentración creciente [70%, 80%, 90%] hasta alcanzar alcohol al 100% [absoluto].
b. Se quita el agua de células y tejidos que componen la muestra, porque la parafina no será miscible
ni en agua ni en alcohol. Luego se debe ACLARAR, se utilizan solventes orgánicos como xileno o
tolueno, que son miscibles [mezclable] tanto en alcohol como en parafina, para extraer el alcohol al
100% antes de la infiltración de la muestra con parafina fundida.
c. Se incluye la parafina, previamente calentada en estufa al 60%, que deberá ocupar todos los
espacios entre las células y en el interior de las mismas.
4. PROCESO DE CORTE
Una vez retirada de la estufa la parafina se enfría y se endurece formando un bloque→ taco. El cual se coloca
en el microtomo que lo va a cortar lo suficientemente delgado (5-10 μm de espesor) con un acuchilla de acero.
5. MONTAJE
Los cortes obtenidos se montan sobre un portaobjetos de vidrio, a los que antes se le ha añadido albúmina,
que sirve de adhesivo.
Para poder realizar la tinción los cortes histológicos se debe disolver y extraer la parafina por acción del xileno
o tolueno → desparafinar.
Luego se debe rehidratar los tejidos mediante el uso de soluciones alcohólicas de concentración decreciente
[100%, 90%, 70%]

Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
4
6. TINCIÓN
El tejido sobre el porta objetos se tiñe con hematoxilina en agua.
Para teñir con eosina, se vuelve a deshidratar la muestra con alcohol de
concentración creciente y después se tiñe con eosina en alcohol.
Luego de la coloración la muestra se hace pasar por xileno o tolueno y se
coloca un medio de montaje no acuoso antes de cubrila con un cubreobjetos
para lograr un preparado permanente.
OTRAS TÉCNICAS DE TINCIÓN
Colorantes básicos → reaccionan con los componentes aniónicos de las células y los tejidos→
heterocromatina y nucleolos, componentes citoplasmáticos, materiales extracelulares (ej.: hidratos de carbono)
(componentes basófilos).
Colorantes ácidos→ reaccionan con los grupos catiónicos en las células tejidos→ filamentos citoplasmáticos,
componentes membranas, fibras extracelulares, colágeno (componentes acidófilos).
Metacromasia→ Ciertos colorantes básicos reaccionan con los componentes del tejido que cambian su color
normal de azul a rojo o púrpura.
De las técnicas de coloración empleadas en la cátedra para la enseñanza, la más frecuente es la coloración di
crómica con hematoxilina y eosina (H y E):
colorante
Color
Colorantes básicos
Verde de metilo
Verde
Azul de metileno
Azul
Pironina G
Rojo
Azul de toluidina
Azul
Colorantes ácidos
Fucsina acida
rojo
Azul de anilina
Azul
Eosina
Rojo
Naranja G
Naranja
Colorante
Carga
Químico
Reaccionan con
Color
Hematoxilina
Positiva (catiónico) en su
parte coloreada
Básico
Grupos aniónicos: (carga -):
• Fosfatos de los ácidos
nucleicos.
• Sulfatos de GAG
(glucosaminoglucanos)
• Carboxilo de las proteínas
Azul
Basofilia→ capacidad de tinción de los colorantes básicos
tiene propiedades tintoriales muy semejantes a las anilinas básicas.
eosina
Negativo (aniónico) en
su parte coloreada
Acido
Grupos catiónicos: (carga +)
• proteínas básicas del citoplasma
Rosado
Acidofilia→ capacidad de tinción de los colorantes ácidos
Colorantes:
• Mono crómica (1)
• Di crómica (2)
• Tri crómica (3)
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
5
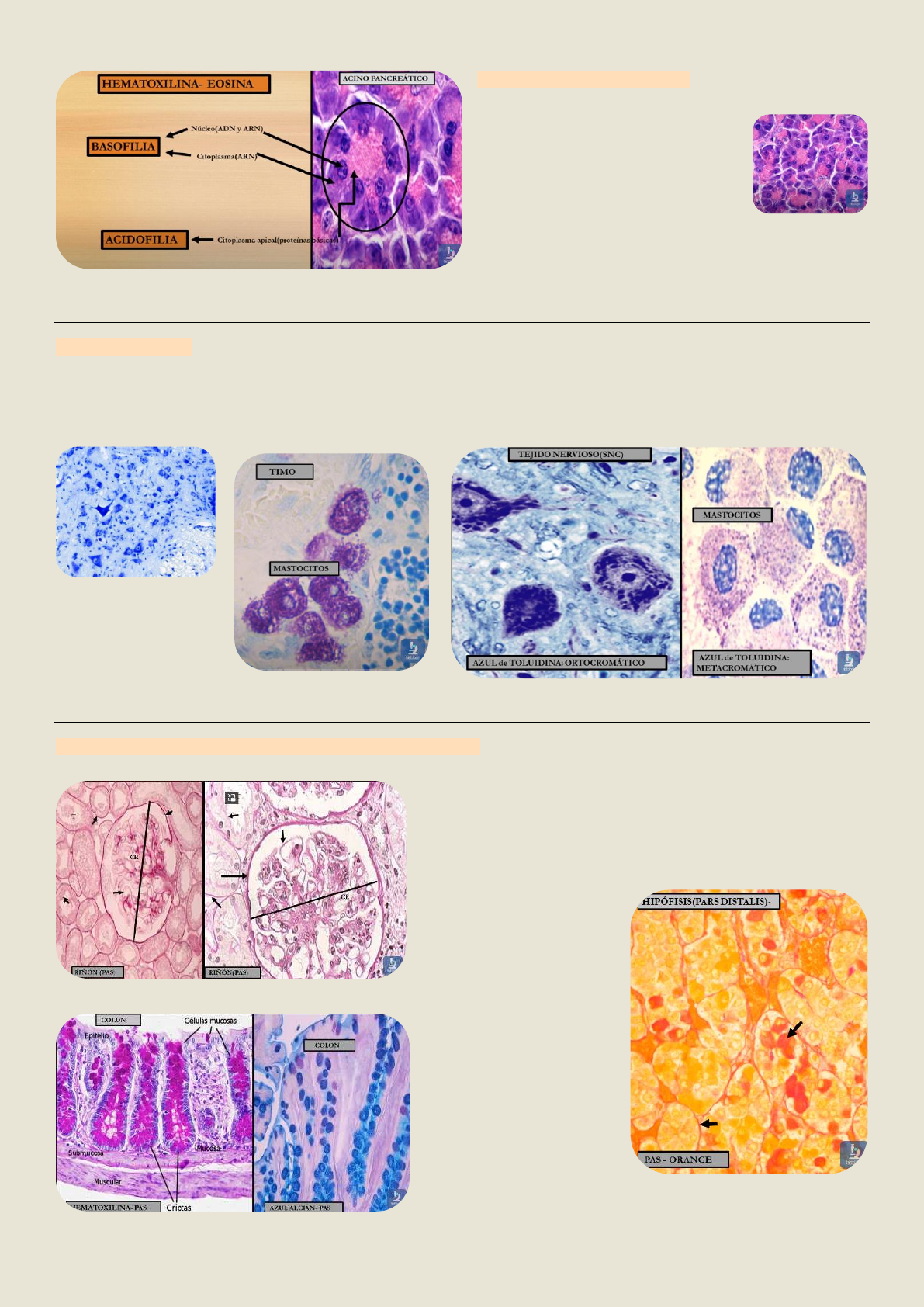
Hematoxilina-Eosina [H-E]
• son utilizadas para poner en
evidencia las características
estructurales.
• Pero no nos permite ver elastina,
fibras reticulares, membranas
basales y lípidos. (imagen: páncreas)
• Coloración di crómica.
Azul de toluidina
• colorante básico (catiónico), que tiñe los tejidos de AZUL (ortocromática).
• cuando se expone a estructuras ricas en → heparina y GAGs, vira a color rojo a purpura (metacromasia).
Reacción del PAS (acido periódico-reactivo de schiff)
• capacidad de la fucsina acida de reaccionar con los
grupos aldehídos→ rojo- purpura.
• Determinala presencia de carbohidratos y glucoproteínas,
macromoléculas de glucógeno.
• Identifica
glucosaminoglucanos
(Gags), mucina, glucógeno,
membranas basales y
fibras reticulares
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
6
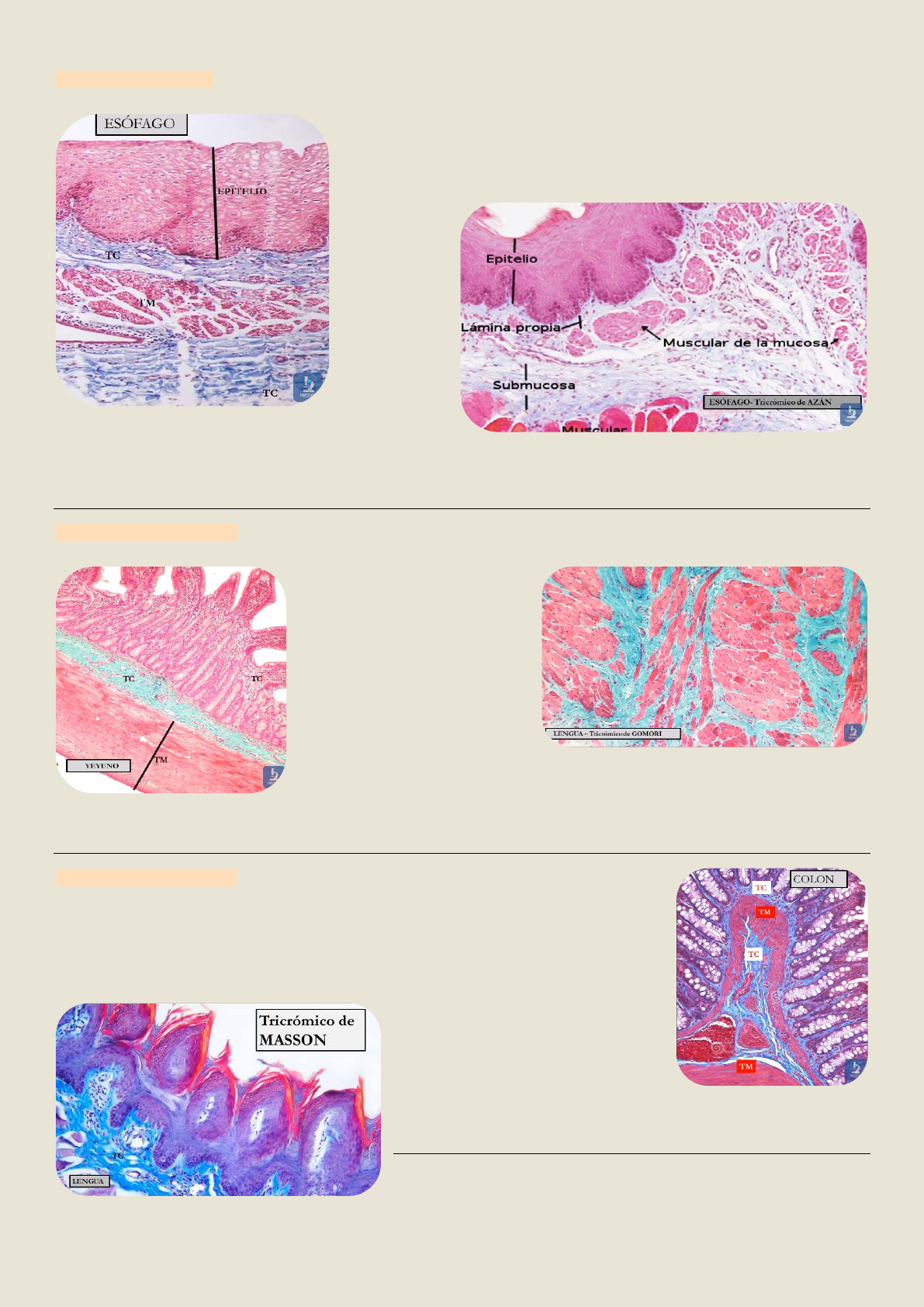
Tricromico de azon
• Azocarmin (acido)→ rojo → núcleos
• Azul de anilina (básico)→ azul → fibras colágenas
• Naranja G (ácidos)→ rojo-amarillo → citoplasmas, eritrocitos y
tejidos
musculares
La variante Mallory (Mallory-azan) reemplaza el azocarmin por fucsina acida.
Tracrómico de Gomori
• Verde luz→ verde → fibras
colágenas
• Cromotropo→ rojo pardo
→ tejidos musculares,
eritrocitos, citoplasma.
• Hematoxilina→ azul→
núcleos
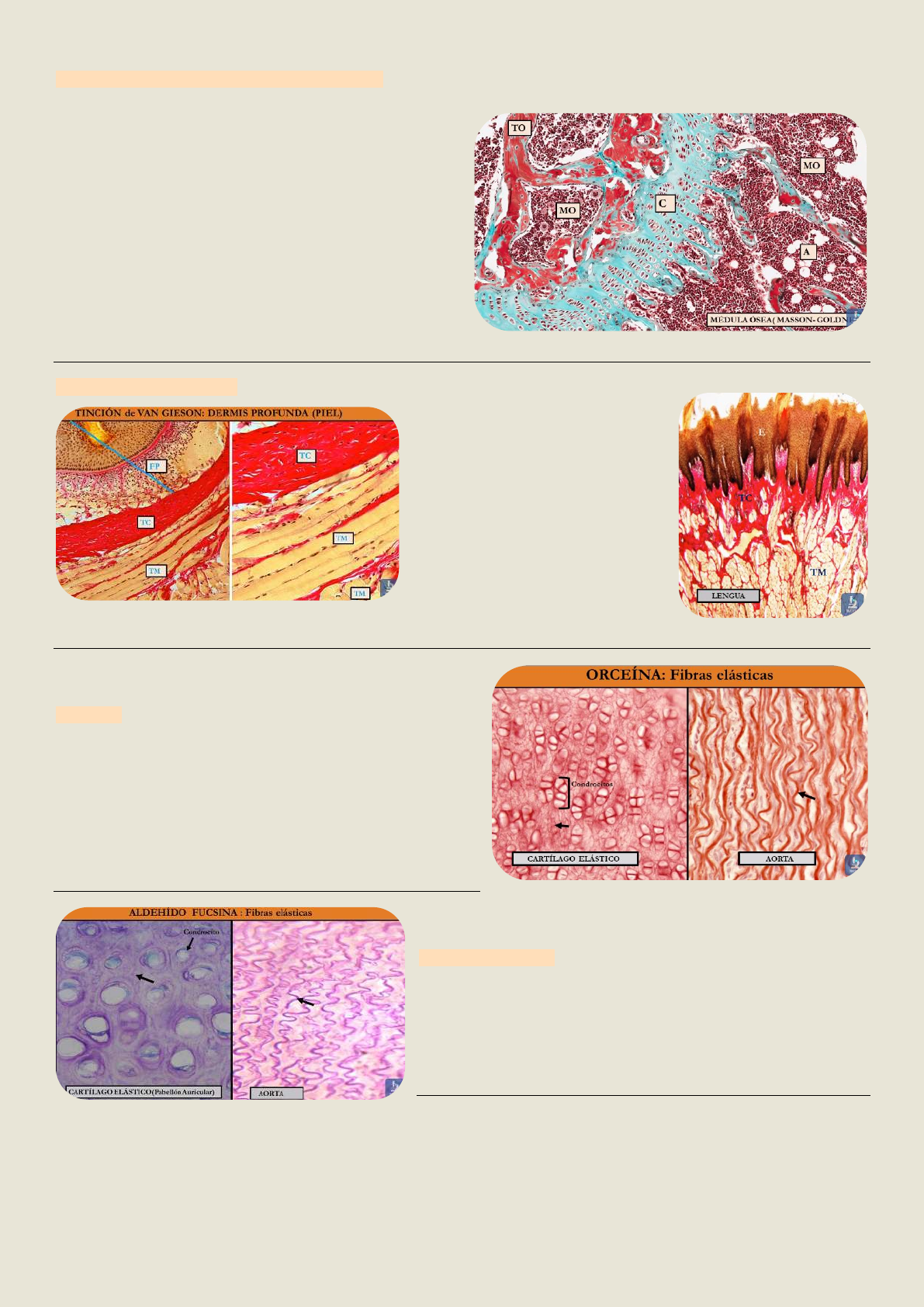
Tricromico de Masson
• Hematoxilina férrica de weigert→ azul-negro → núcleos
• Fucsina acida → rojo intenso a rosado → eritrocitos, citoplasmas y muscular.
• Azul de anilina → verde luz→ azul verdoso → conectivo y fibras colágenas.
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
7
Tricromico de Goldner (Masson-goldner)
• Hematoxilina de Groat→pardo marrón a negro→
núcleos
• Fucsia acida punzo→rojo naranja → citoplasmas y
tejido muscular
• Naranja G→ naranja (rojo naranja)
• Verde luz→ azul verdoso→ conectivo: fibras
colágenas y cartílago.
Tinción de Van Gieson
• Hematoxilina férrica de
weigert→ negro azulado →
núcleos.
• Acido pícrico→ amarillo
anaranjado → citoplasmas y
tejidos musculares.
Orceína
• material elástico→Color pardo
aldehído fucsina
• fibras elásticas→ tono violáceo
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
8
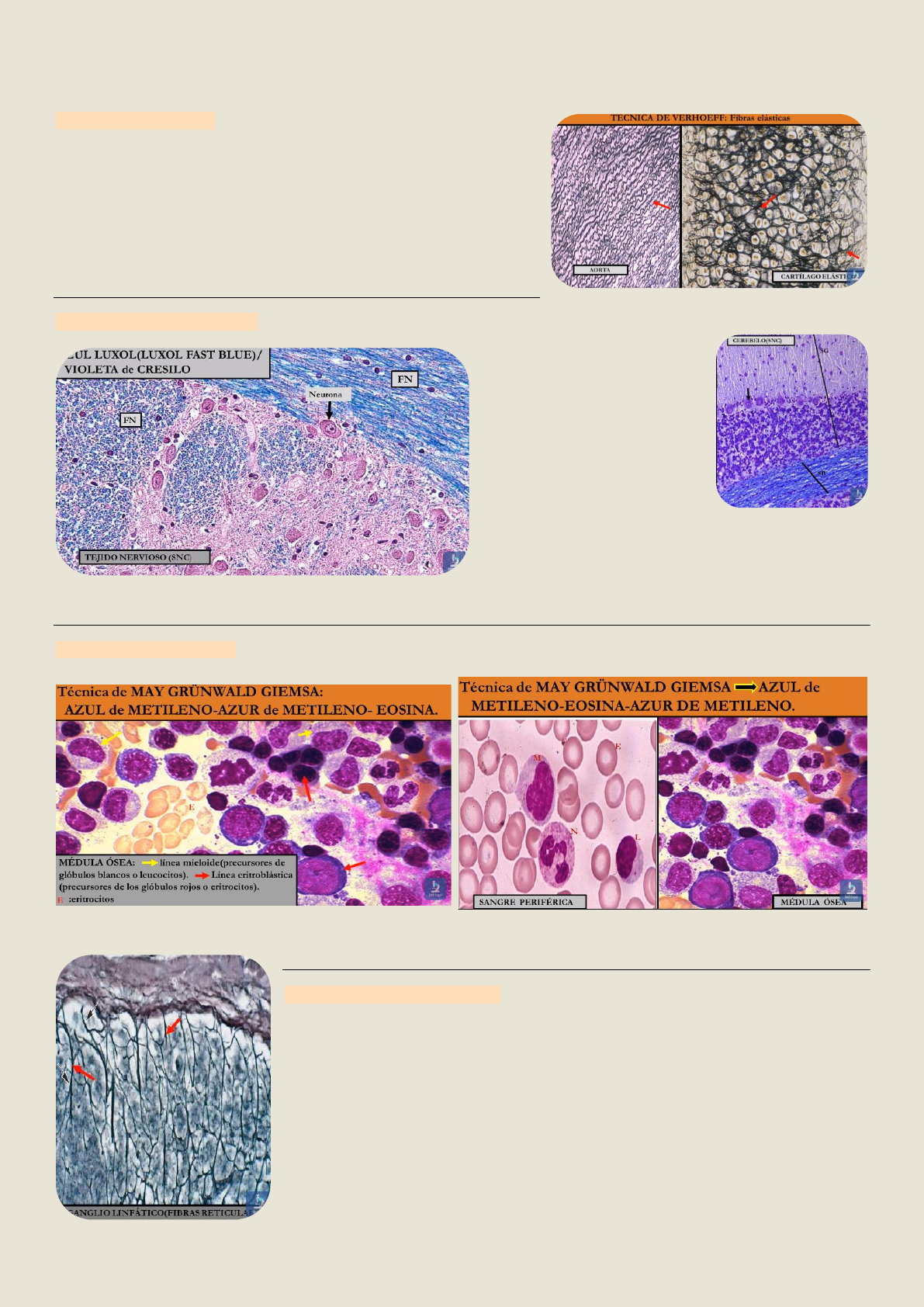
técnica de Verhoeff
• fibras elásticas→negro
azul luxol (luxol fast blue)
• tiñe de color azul a la
mielina(lipoproteína) de las
fibras nerviosas
• el violeta de cresilo
(colarente básico) tiñe las
estructuras acidas→
sustancias de Nissl, núcleo y
nucleolo de las neuronas, núcleos de la Glía
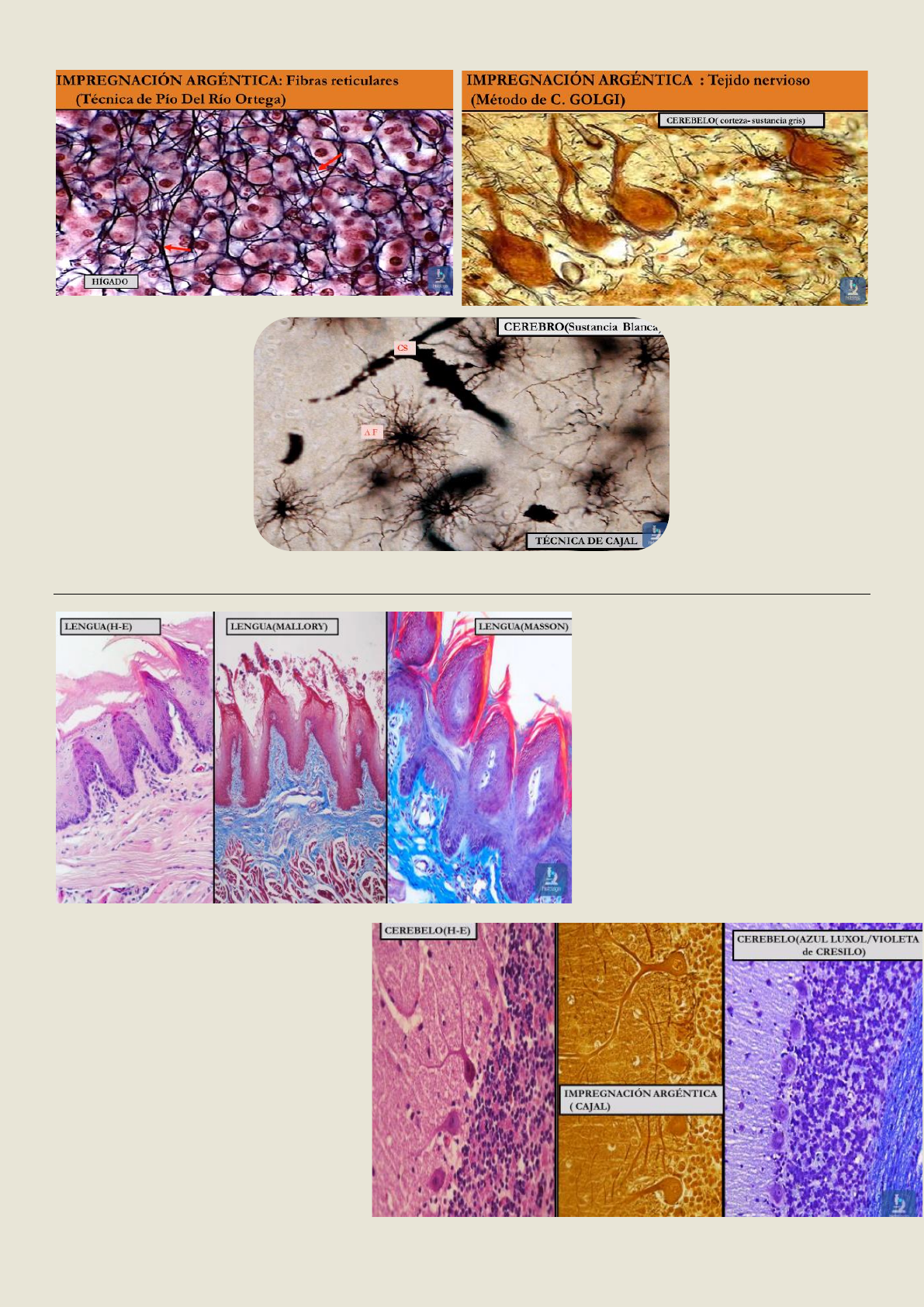
May Grünwald Giemsa
Impregnación argéntica → fibras reticulares y membranas basales.
• Los tejidos son tratados con sales de plata
• Se produce un precipitado al enfrentar las sales a un agente reductor
• Se identifican →fibras reticulares, fibras nerviosas y células de la
neuroglia (SNC)
• Color negro
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
9
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
10
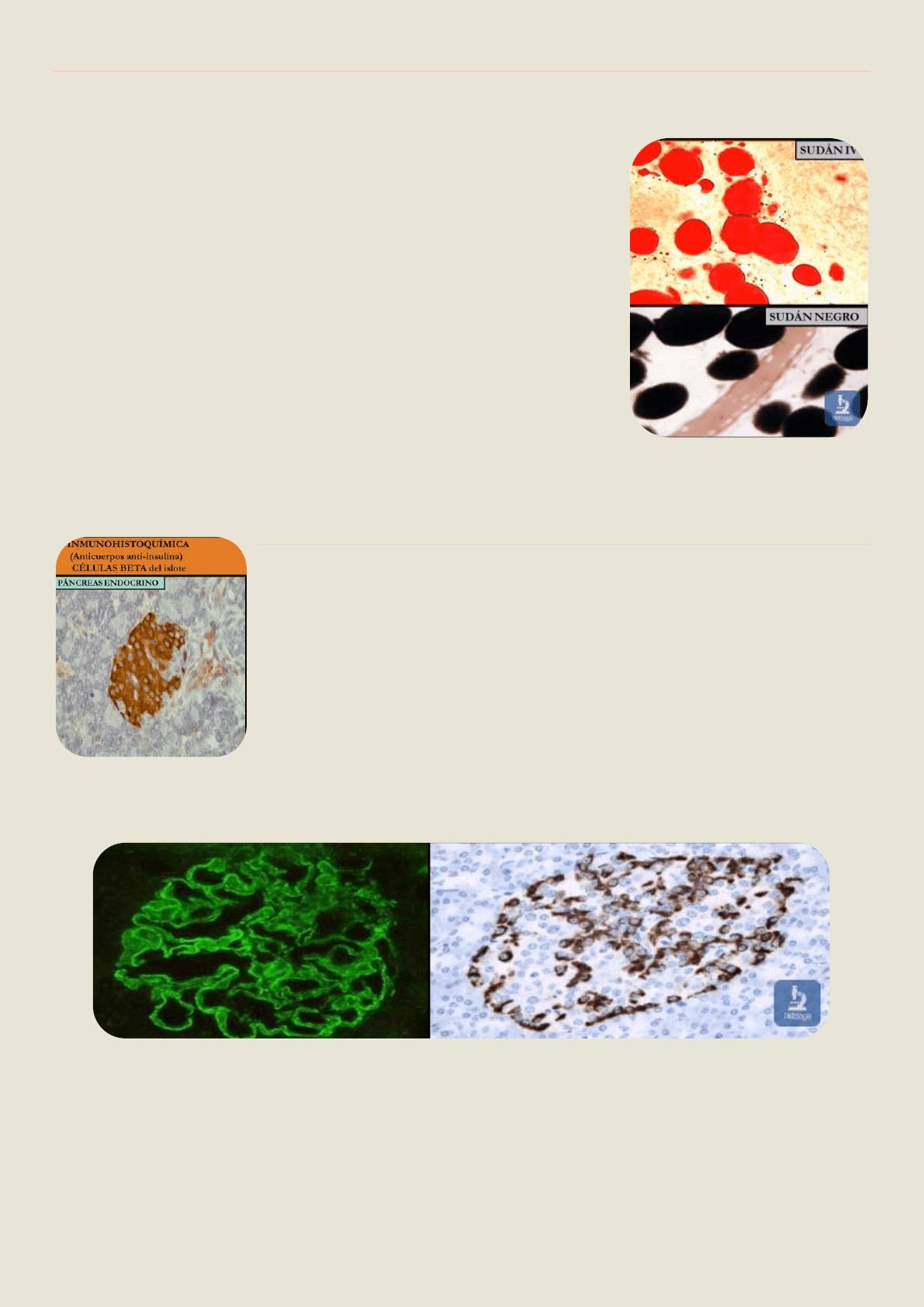
TINCIONES ESPECIALES PARA TEJIDOS ADIPOSOS Y LÍPIDOS EN GENERAL
Los más empleados son:
• Sudan III
• Sudan IV (escarlata R)
• Sudan negro
o Colorante indiferente → sin afinidad por estructuras acidas o básicas.
o Insolubles en agua
o Estos colorantes son mas solubles en los lípidos que en el medio en el que
están disueltos
o Van en soluciones alcohólicas o en una mezcla alcohol/acetona o
alcohol/agua.
o El mejor fijador para estas muestras será el formol.
o Los cortes normalmente son por congelación.
o Los reactivos son → hematoxilina o carmín (para el contraste) → núcleos
azules.
• Escarlata→ grasa roja (sudan III)
• Escarlata R (sudan IV → grasa rojo intenso
• Black→ grasa negra (sudan negro
INMUNOCITOQUIMICA (INMUNOHISTOQUÍMICA)
La inmunohistoquímica nos permite reconocer células del páncreas endocrino y
células de la adenohipófisis, son técnicas muy específicas.
Método que se fundamenta en la reacción especifica entre un antígeno
(componente químico determinado) y su anticuerpo (inmunoglobulina) especifico.
El corte de tejido donde se demostrará la presencia del antígeno se incuba con una
solución que contiene un anticuerpo específico contra el antígeno buscado.
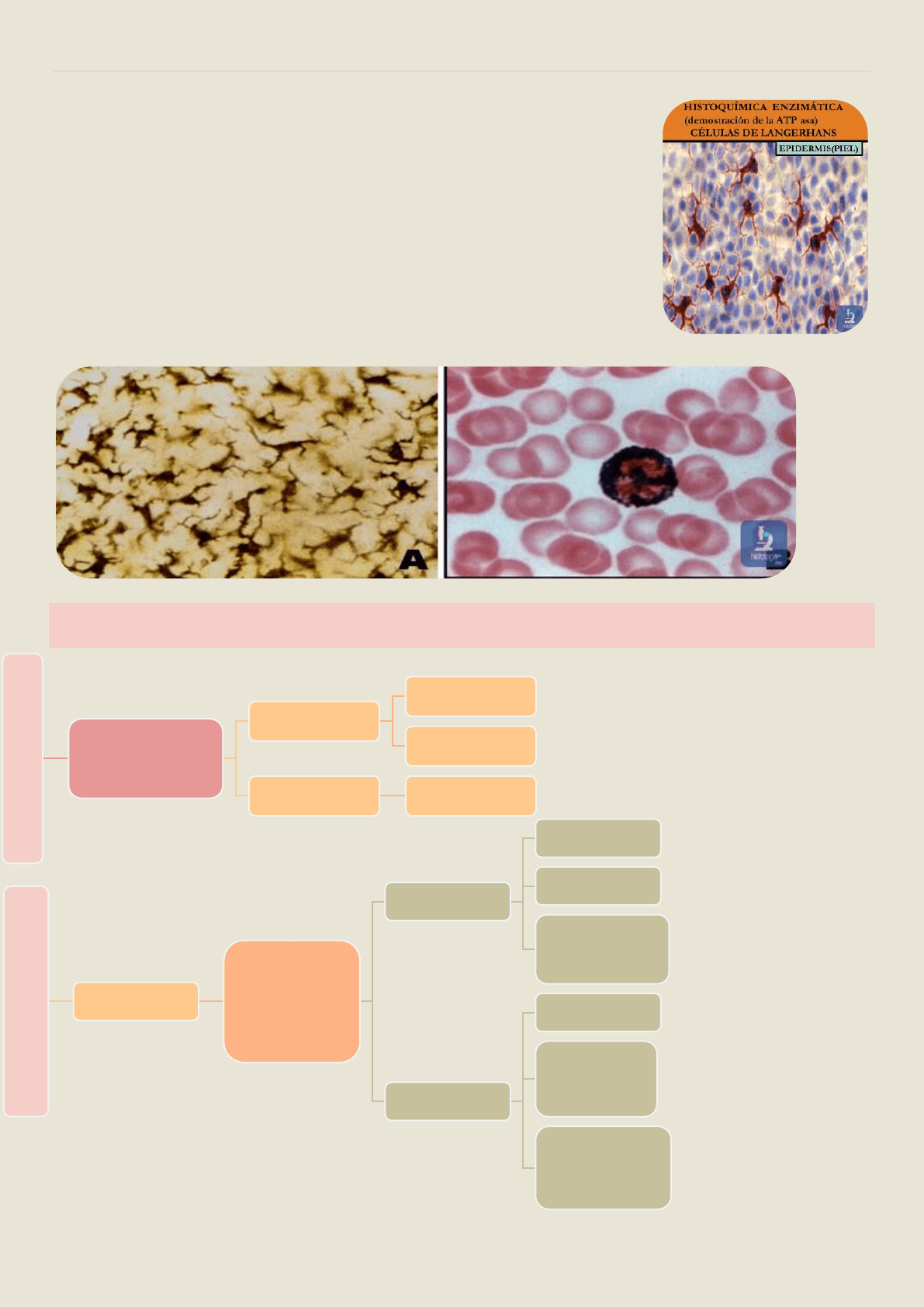
La reacción se puede visualizar de diferentes modos→ el anticuerpo [ se le adosa la
enzima peroxidasa] puede marcarse con una sustancia fluorescente → fluoresceína (imagen izquierda). Y se
detecta la reacción Ag-Ac por histoquímica enzimática (imagen de la derecha)→ Ac anti-glucagon.
Síntesis → la especificidad de la reacción entre un antígeno y un anticuerpo
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
11
HISTOQUÍMICA ENZIMÁTICA (HISTOENZIMOLOGIA)
Método que evidencia actividad enzimática en algunos tejidos, tras el proceso de
fijación.
La reacción enzimática convierte a unos sustratos solubles e incoloros en
productos insolubles y coloreados poniéndose de manifiesto la enzima y el tejido
que la posee.
En A→ la técnica pone en evidencia la enzima ATPasa en las células de
Langerhans, en la epidermis de la piel.
En B → se demuestra la presencia de la enzima peroxidasa en un leucocito
(neutrófilo).
RESUMEN
FINALIDAD→ diagnostico o investigación
TÉCNICAS→ incisional – sacabocados –
punción aspiracional – etc.
FINALIDAD:
• inhibe la autolisis de
los tejidos
• aporta resistencia a
la muestra para
soportar técnica
• evita difusión de
péptidos
primer paso
OBTENCION
DE LA
MUESTRA
biopsia
paciente o
animal vivo
consultorio o
quirofano
necropsia/aut
opsia
se obtiene de
un cadaver
segundo paso
FIJACIÓN
de la muestra
biologica de
interes para
evita su
descomposicio
n natural
químicos
alcohol etilico
95%
liquido de
Helly
formaldehído
10% (mas
usado)
fisicos
desecacion
calor
seco/humedo
congelacion
(rapida
utilizada para
identificar
lipidos)
Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
12
FINALIDAD
• Permitir el paso de la
luz a través de la
muestra. Lo que
permitirá su
visualización en
microscopio óptico
tercer paso
tras 6 a 24
horas de
fijacion segun
el tamaño de la
muestra
DESHIDRATACION
la muestra sera
sumergida en
soluciones
crecientes de alcohol
(70%- 96% - 100%)
para retirar el agua
que contenga la
misma, pero como la
parafina no es
miscible con el
alcohol, se necesita
hacer lo siguiente
cuarto paso
ACLARAMIENTO
los agentes mas
usados son tolueno y
xileno, miscibles tanto
en alcohol como en
parafina, y por lo
tanto permiten que la
parafina penetre en
el tejido
quinto paso
INCLUSION EN
PARAFINA
parafina:
hidrocarbur
o solido a
temperatura
ambiente
por medio de
colocarla en
estufas
especiales de
laboratoria a 60º
C, la volveremos
liquido
la retiramos de la
estufa,
sumergimos
nuestra muestra
allí, y esperamos
que se vuelva
completamente
solida.
asi obtenemos
nuestro taco: que
nos permitirá
cortar en finas
laminas la
muestra
sexto paso
CORTE
seccionaremos
el taco en
laminas (de 5-10
μm). esto se
logra por medio
de un dispositivo
llamado:
MICRÓTOMO
cuanto mas
delgada sea
la lamina,
mejor sera
su calidad,
pero su
realizacion
supone una
dificultad
mayor.

Ipaz Lourdes UNLP miércoles, 16 de marzo de 2022
13
PARA FINALIZAR
Ponemos un cubrebocas
sobre la muestra,
utilizando bálsamo de
Canadá (trementina) entre
la muestra y el
cubreobjetos.
Y ya esta lista para ser
observada con el
microscopio.
septimo paso
MONTAJE
colocaremos
nuestro corte sobre
un protaobjetos con
albûmina, que
funcionara de
adhesivo.
llevaremos ese
portaobjetos a un
baño de flotacion,
que pos su liquido
tibio, permitira que la
paraina se alise y
adhiera mejor al
portaobjetos
octavo paso
RETIRO DE LA
PARAFINA
desparafinare
mos
repitiendo los
pasos de la
inclusion,
pero a la
inversa:
tratamos el
corte con
xileno y luego
lo hidratamos
con soluciones
decrecientes
de alcohol
(100% - 96% -
70%).
retiramos la
parafina e
hidratamos
para permitir
el ingreso de
la coloracion
noveno paso
COLORACION
basicos
acidos
pasos para la
coloracion
1°
sumergimos el
porta objetos con
el corte en
HEMATOXILINA
2°
deshidratamos la
muestra como hicimos
antes, para usar el 2do
colorante (soluble en
alcohol)
EOSINA

Técnicas histológicas S01.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.