TALLER 7 - PROTEÍNAS
Las proteínas realizan la mayoría de las funciones a
nivel celular.
Unión y transporte de oxígeno hacia los tejidos,
sistema inmune: reconocimiento y eliminación de
microorganismos, transmiten señales a nivel sistémico
como hormonas, transportan moléculas, participan en
el sistema complejo en la contracción muscular,
forman parte de la estructura de las células al
componer citoesqueleto, son la mayor parte de las
enzima por lo que son las responsables de acelerar la
velocidad de muchas reacciones.
-Las proteínas son polímeros o cadenas de
aminoácidos con longitud y secuencia variable.
-Los aminoácidos se mantienen unidos por
enlaces peptídicos. son moléculas que cuentan
con un carbono central, el cual tiene unido unα
grupo carboxilo, un grupo amino, un hidrógeno y
un grupo R o lateral que es específico de cada
aminoácido.
-Los aminoácidos, clasificados apolares (enlaces
hidrofóbicos) suelen ubicarse en el interior de la
proteína, Los polares sin carga (enlaces de
hidrógeno) suelen ubicarse en la superficie de las
proteínas, Los polares cargados (interacciones
iónicas)
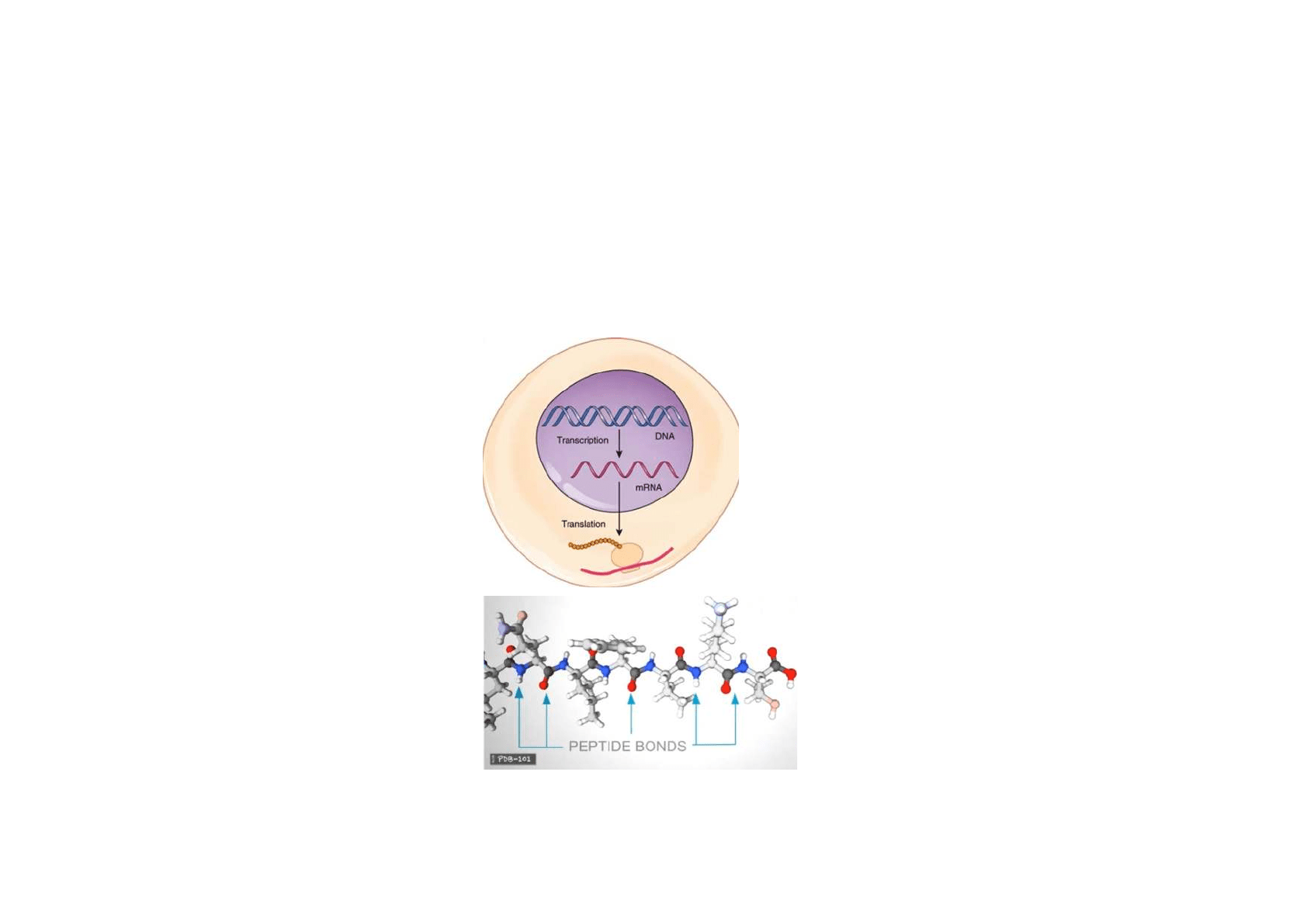
A nivel celular las proteínas están codificadas en
el ADN
, los diferentes genes que codifican para
las proteínas, se transcriben a moléculas de Arn
mensajero, que se transportan en citosol donde el
ribosoma traduce la cadena polipeptídica
utilizando diferentes ARN de transferencia
específicos para cada aminoácido.
El enlace peptídico es un enlace tipo amida entre
el grupo carboxilo de un aminoácido y el grupo
amino del aminoácido adyacente. La formación
de esta de enlace implica la eliminación de una
molécula de agua, esta cadena lineal de
aminoácidos tiene la información para plegarse y
adquirir una estructura tridimensional precisa y
específica, la cual va a determinar la función de
las proteínas.
La proteína tiene estructura y conformación
tridimensional,
sin esa estructura la proteína no
puede cumplir su función. (si a una proteína lineal se la
deja en solución empieza a probar diferentes conformación
posibles, hasta que llega a obtener la única estructura, la
conformación nativa)
A medida que la
cadena polipeptídica adopta una
conformación
se indica qué energía tiene, hasta
que no adopta energía y está e bo n el pozo de
baja energía la proteína sigue intentando
diferentes conformaciones.
La conformación final que corresponde a la de
menor energía suele ser la conformación nativa,
en la cual encontramos a la proteína en
condiciones fisiológicas, generalmente
corresponde a la conformación que más enlaces
puede formar.
NIVELES ESTRUCTURALES DE LAS
PROTEÍNAS
Estructura primaria: enlace peptídico
corresponde con la cadena lineal de aminoácidos
Está constituida por la secuencia de aminoácidos de la cadena polipeptídica.
Las proteínas se diferencian por el número de aminoácidos, el tipo de
aminoácidos o el orden en que se encuentran los aminoácidos dispuestos.
Cualquier alteración en el orden de estos aminoácidos determinará una
proteína diferente.
la manera de nombrar la cadena polipeptídica es la de nombrar desde el
aminoácido con el amino terminal libre, al aminoácido con el carboxilo terminal
libre.
Los enlaces peptídicos son planos y rígidos no rotan pero si existe una
rotación alrededor de estos planos rígidos entre los enlaces covalentes del
nitrógeno y el carbono alfa y el carbono alfa con el carbono del carboxilo.
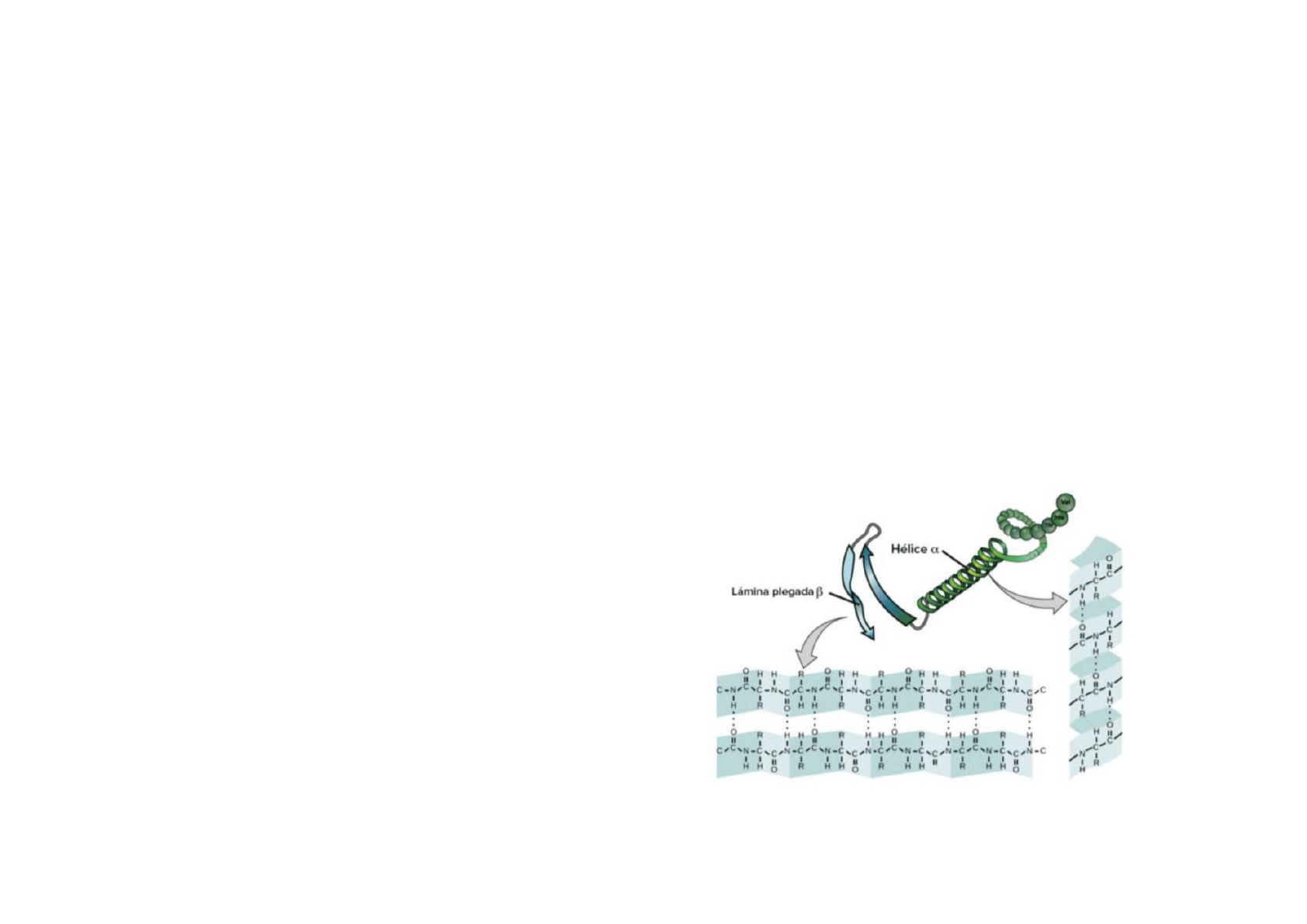
Estructura secundaria: hélices alfa y hojas plegadas beta
La estructura secundaria es el plegamiento que forma la cadena polipeptídica
debido a la formación de interacciones débiles entre los átomos que forman el
enlace peptídico.
El nivel secundario de organización de las proteínas incluye a las siguientes
estructuras que son las más frecuentes: Hélice Láminaα β
Hélice La estructura secundaria en la Hélice Se forma cuando la cadenaα α
polipeptídica se enrolla de manera helicoidal. como una estructura en espiral,
sobre un eje imaginario. El grupo carboxilo de cada aminoácido se une
mediante un puente de hidrógeno al grupo amino de otro aminoácido
Lámina Esta estructura es conocida también como lámina plegada. Laβ
cadena queda estirada y en forma de zigzag formando láminas.Los grupos R
sobresalen de la lámina en ambos sentidos y de manera alterna
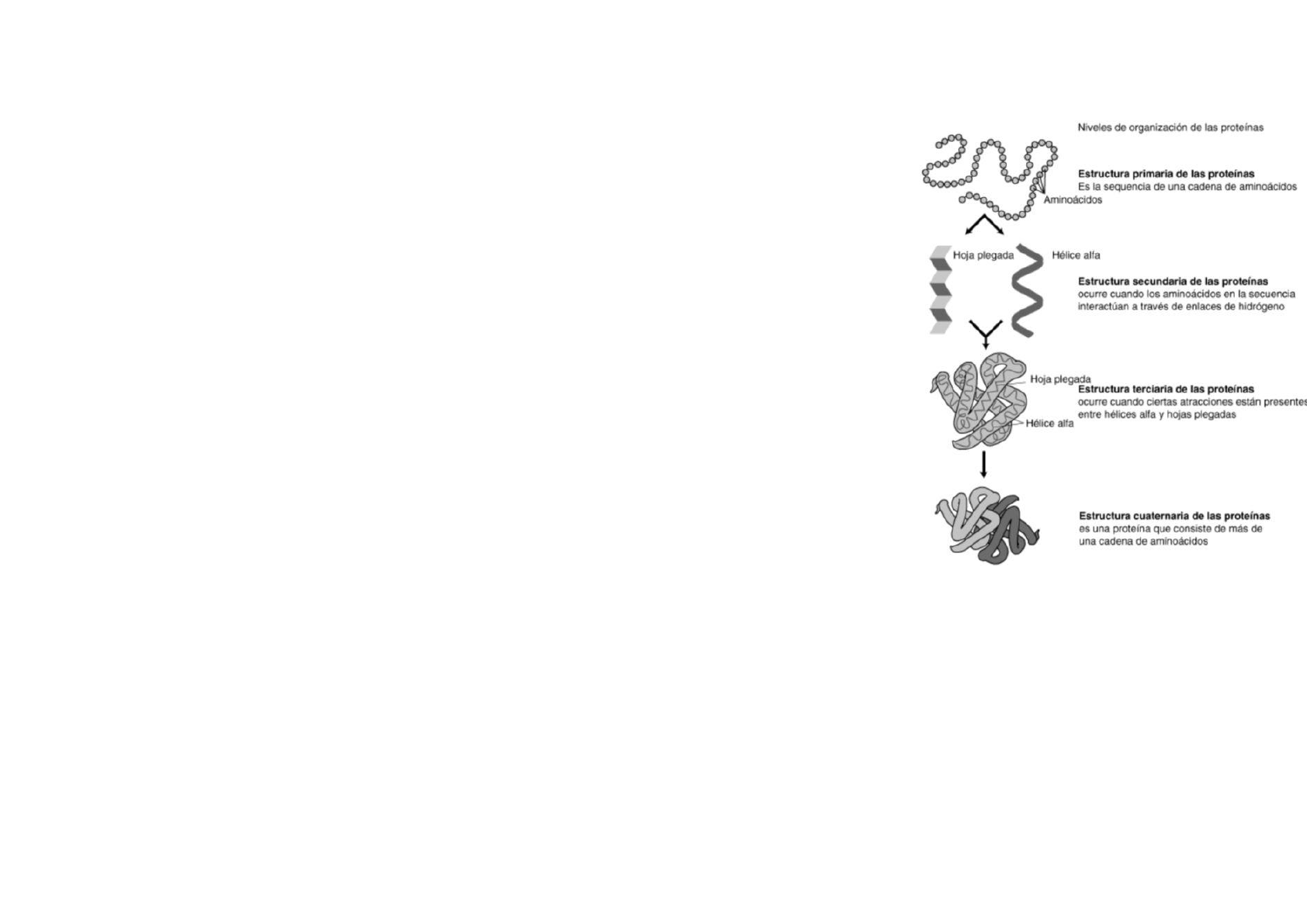
Estructura terciaria
La estructura terciaria ocurre cuando existen
atracciones entre Láminas β y Hélices . Estaα
estructura es específica para cada proteína y
determinará la función de dicha proteína.
Para dar lugar a la estructura terciaria es
necesario que primero se agrupen conjuntos de
estructuras denominadas dominios, que luego se
articulan para formar la estructura terciaria
definitiva.
Se le llama dominio a las regiones de la proteína
que tienen una estructura secundaria definida.
La estructura terciaria da lugar a dos tipos de
proteínas:
1) Proteínas con estructura terciaria de tipo
fibroso:
las hélices- o láminas- que loα β
conforman, mantienen su orden y no tienen
grandes modificaciones, solo ligeros giros
longitudinales.
2) Proteínas con estructura terciaria de tipo
globular
su forma es aproximadamente esférica.
En este tipo de estructuras se forman regiones
con estructuras al azar, hélices- y láminas- yα β
acodamientos.
se estabiliza por interacciones débiles entre los
grupos r de los aminoácidos, de manera de
obtener la conformación de menor energía una
proteína forma el mayor número posible de este
tipo de interacciones, además estas se pueden
estabilizar mediante puentes de sulfuro (entre
átomos de azufre)
Hablamos de desnaturalización de una proteína
en el momento en que se pierde la estructura
terciaria de la proteína y por lo tanto esta pierde
su función, es decir; supone la ruptura de las
interacciones débiles que mantienen la estructura
tridimensional. La mayoría de las proteínas se
pueden desnaturalizar por calor, pH extremos,
entre otros.
Estructura Cuaternaria Solo algunas
proteínas tienen estructura cuaternaria, esta
implica la interacción de más de una cadena
polipeptídica. Es, por lo tanto, la asociación de
diferentes subunidades para formar complejos
funcionales, en forma de dímeros, (unión de dos
monómeros) trímeros (unión de tres monómeros),
etc. de manera genérica se le conoce como
oligómeros.
La disposición de estas subunidades proteicas en
complejos tridimensionales constituye la cadena
cuaternaria.
PROTEÍNAS CONJUGADAS
Son aquellas proteínas que contienen en su estructura además de la cadena o cadenas polipeptídicas otra sustancia que no está formada por aminoácidos.
La sustancia no aminoacídica recibe el nombre de grupo prostético, qué es necesaria para que la proteína desarrolle su función. El grupo prostético puede unirse a
la cadena polipeptídica por enlace covalente o por la interacción no covalente.Una proteína conjugada desprovista de su grupo prostético recibe el nombre de
apoproteína.
TIPOS
GRUPO PROSTÉTICO
EJEMPLO
Lipoproteínas
Lípidos
Beta-lipoproteína
Glucoproteínas
Carbohidratos
Inmunoglobulina G
Fosfoproteínas
Fosfato
Caseína de la leche
Hemoproteínas
Hemo
Hemoglobina
Flavoproteínas
Nucleótidos de flavina
Succinato, deshidrogenasa
Metaloproteínas
Hierro, zinc, calcio,
manganeso
Ferritina, alcohol deshidrogenasa, calmodulina,
superóxido dismutasa.
MODIFICACIONES
Existen modificaciones en las proteínas que ocurren después de ser sintetizadas, dichas modificaciones se denominan modificaciones post traduccionales, algunas
de ellas corresponden a la adición de un grupo metilo un grupo acetilo, o la adición de un lípido o un glúcido entre otras.
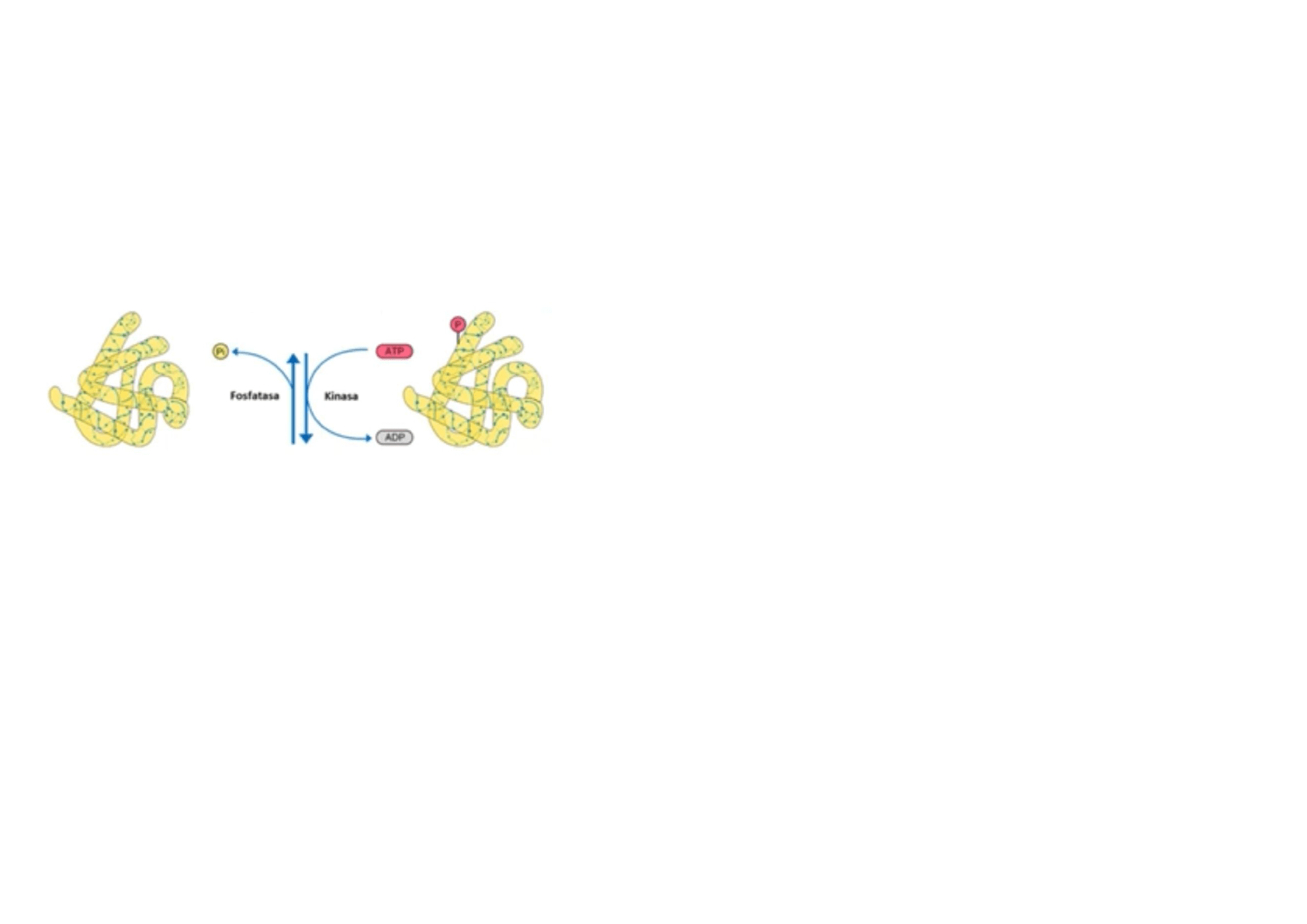
Una de las que ocurre con mayor frecuencia a nivel celular es la
fosforilación, implica la adición de un grupo fosfato a partir de la ATP, a aminoácidos con grupo que
contengan un grupo funcional alcohol. La adición de este grupo fosfato puede inducir la pérdida o la ganancia de una actividad para la proteína, por esto es que la
fosforilación y la desfosforilación suele ser un proceso que se utiliza a nivel celular para regular la función proteica.
Las
quinasas son las enzimas que se encargan de catalizar el proceso de la fosforilación, mientras que las fosfatasas son las encargadas de quitar el grupo fosfato
en las proteínas.
FUNCIÓN DE LA PROTEÍNA
La función de las proteínas depende de que la misma se encuentre en su estado nativo con su estructura terciaria (si es monomérica) o cuaternaria (si es
multimérica) en la conformación adecuada.
Pérdida de estructura —- pérdida de función: desnaturalización
Hablamos de desnaturalización de una proteína en el momento en que se pierde la estructura terciaria de la proteína y por lo tanto esta pierde su función, es decir;
supone la ruptura de las interacciones débiles que mantienen la estructura tridimensional.
Agentes desnaturalizantes: calor, pH,agentes químicos (urea, cloruro de guanidinio)
La desnaturalización no implica ruptura de enlaces peptídicos, solo interacciones débiles.
La ruptura de los enlaces peptídicos se da cuando se liberan péptidos más pequeños o aminoácidos libres. A nivel fisiológico este proceso es catalizado por las
proteasas. Estas enzimas no rompen cualquier enlace peptídico , tienen especificidad y esta depende de los aminoácidos que forman parte de dicho enlace.

PRESENTACIÓN DE LA PROTEÍNA: las diferentes representaciones visuales de las proteínas, nos pueden dar indicios sobre las estructuras y funciones de las mismas.
2- Esta presentación llamada de listón o de diagrama animado, muestra la organización de la cadena de la proteína y enfatiza las hélicesα
3- la representación de las superficies muestra las áreas en la proteína que están accesibles a las moléculas del agua.
TAMAÑO DE LA PROTEÍNA: La mayoría de las proteínas son más pequeñas que la longitud de onda de la luz, ej, la estructura de la hemoglobina es de aprox 6,5
nanómetros de tamaño.
FORMA Y FUNCIÓN: Las proteínas de formas tridimensionales determinan su función,.
Defensa (anticuerpos): Los brazos flexibles de los anticuerpos nos protegen
de enfermedades al reconocer y enlazarse con patógenos y apuntarlos para
que el sistema inmune los destruya
Comunicación (insulina): La hormona de la insulina es una proteína, que al
ser pequeña puede conservar su forma al viajer a través de la sangre para
regular el nivel de glucosa de esta.

Enzimas (Alpha-amilasa): Esta es una enzima
que inicia la digestión de los almidones en
nuestra saliva.
Transportación (bomba de calcio): retículo
sarcoplásmico, la bomba de calcio es ayudada
por el calcio e impulsada por ATPs, para regresar
los iones de calcio al retículo sarcoplasmático
después de cada contracción muscular.
Almacenaje (ferritina): la ferritina es una
proteína esférica con canales que permiten a los
átomos de hierro entrar y salir, dependiendo de
las necesidades del organismo. En su interior
forma un espacio hueco con átomos adheridos a
la pared interior, está almacena hierro en una
forma no tóxica.
Estructura (colágeno): el colágeno forma una
fuerte hélice triple, que es utilizada en todo el
cuerpo para apoyo estructural, las moléculas de
colágeno pueden formar fibras alargadas que se
unen para darles formas a las fibras de colágeno,
este tipo de colágeno es abundante en la piel y
los tendones.


TALLER 7 - PROTEÍNAS.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.