
TEÓRICO 1: PROTEÍNAS PLASMÁTICAS.
PLASMA
.
El plasma es la fracción líquida de la sangre, ya que
la sangre se compone de una parte celular y una no
celular.
Alrededor del 55% de la sangre es plasma. Está
compuesto fundamentalmente por agua (90%).
Además contiene proteínas, glucosa, iones
minerales, hormonas, y CO
2
, entre otros.
El volumen plasmático normal del individuo es el 5%
del peso corporal total, 3500ml.
PROTEÍNAS PLASMÁTICAS.
La concentración de proteínas totales en el plasma
humano es de 7 a 7.5 g/dl. Es la porción principal de
elementos sólidos del plasma.
Funciones
:
● Presión oncótica (es de 28 mm de Hg).
● 15% de la capacidad amortiguadora de la sangre.
● Parte importante del complemento aniónico del plasma (a pH 7.40 la mayor parte en forma
aniónica).
● Unión proteica a las hormonas (evitan que se filtren en los glomérulos; reserva estable de
hormonas).
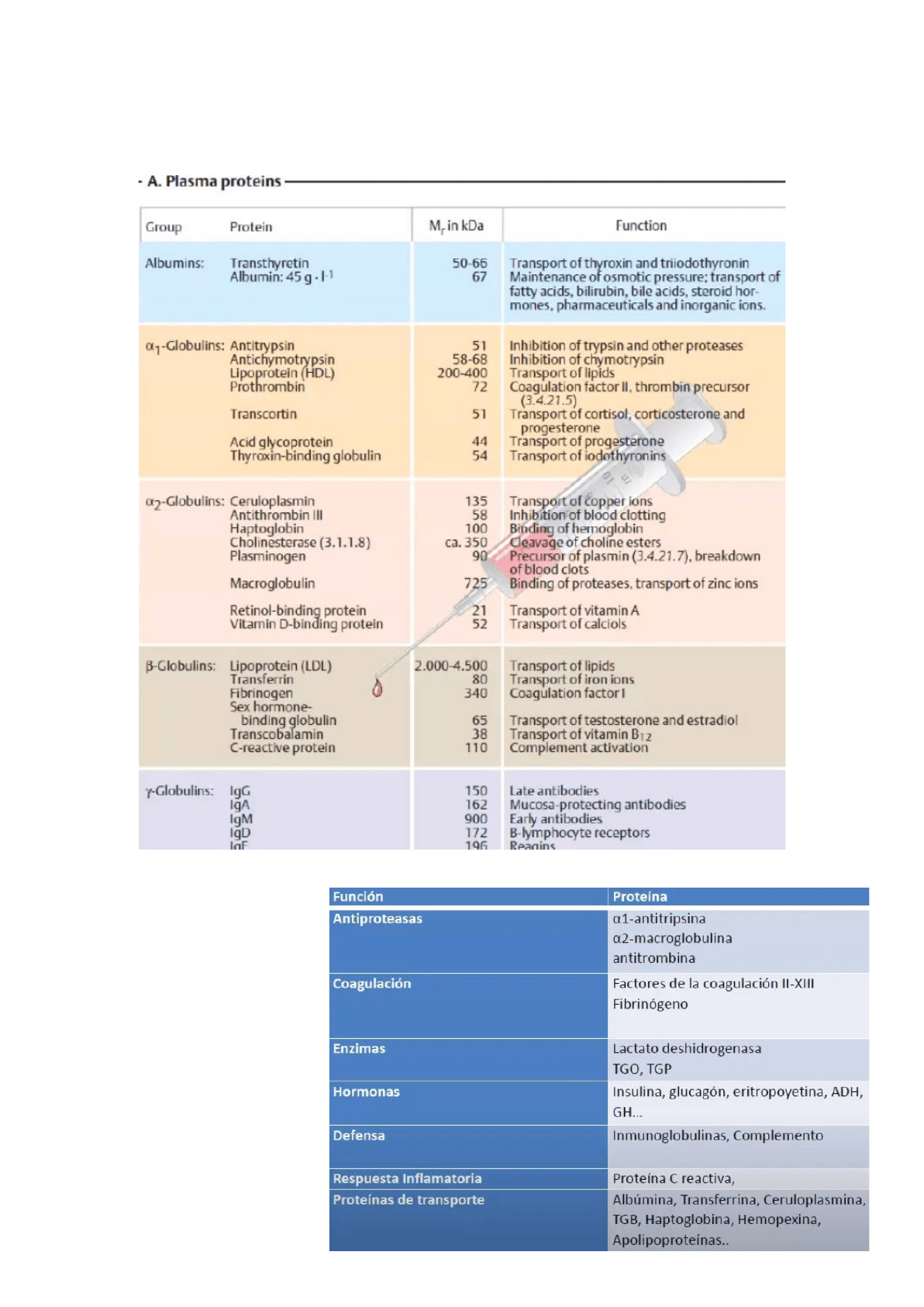
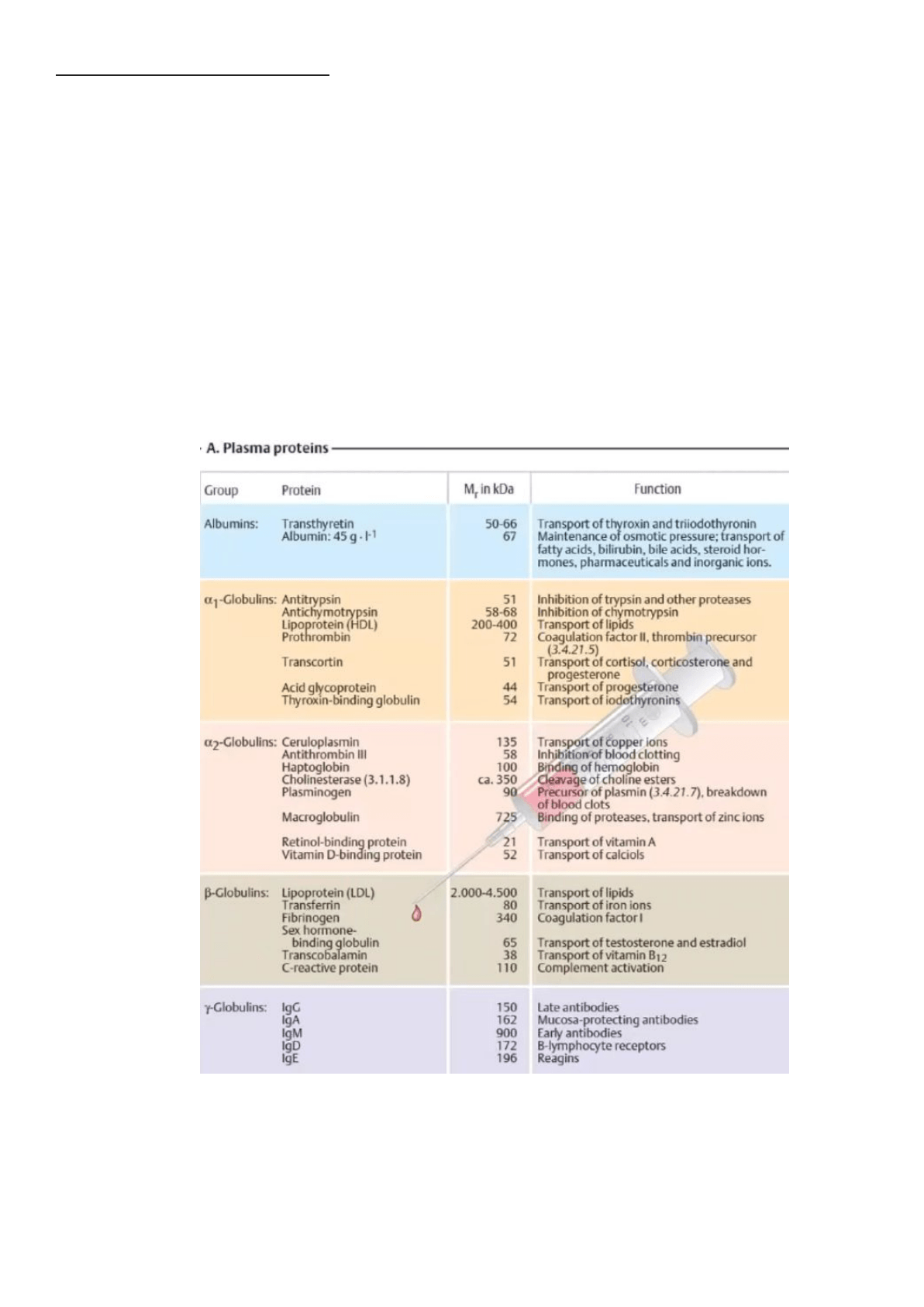
Fracciones de las proteínas plasmáticas:
Ejemplo: Albúmina, alfa-1, alfa-2, beta, y gamma-Globulina.
Estas fracciones se obtienen mediante la electroforesis. La electroforesis es la separación de
proteínas u otros componentes según su tamaño y carga.
En este caso, en las
proteínas plasmáticas
la electroforesis se
hace por medio de
acetato de celulosa a
un pH determinado.
Éstas se siembran y
luego mediante la
aplicación de un campo
eléctrico las proteínas
migran. Una vez que se
termina de generar la
electroforesis, se
obtiene una cierta
cantidad de bandas
que luego mediante una densitometría (transforma las bandas en un gráfico con diferente altura y
tamaño) se obtienen diferentes picos que se han ido determinando en diferentes fracciones de
proteínas plasmáticas. La fracción más abundante es la de la albúmina.
Las proteínas plasmáticas son muy diversas y se encuentran en una gran cantidad. Se dividen
según la cantidad de fracciones que se obtienen en un proteinograma.
Diferentes funciones que
cumplen las diferentes
proteínas plasmáticas:
Las antiproteasas evitan la
acción de proteasas, de decir,
de proteínas que rompen otras
proteínas.

ALBÚMINA.
Es la proteína más abundante de las proteínas plasmática y constituye el 50% de las proteínas
plasmáticas; con una concentración de aproximadamente 0.6mM.
Estructuralmente, presenta una secuencia de 585 aminoácidos, que suma 66 mil Dalton (66 kDa).
Su secuencia es rica en aminoácidos cargados (185 iones por molécula, carga neta a pH 7 de
-19) lo que facilita su solubilidad en medios acuosos.
No se encuentra glucosilada ni presenta otro tipo de
grupo prostético.
La albúmina presenta 35 cisteínas que forman 17
puentes disulfuros restando una sola cisteína reducida, la
cisteína 34.
La estructura cristalográfica muestra que se trata de una
proteína con forma de corazón.
Presenta 67% de alfa-hélice y nada de hoja beta plegada.
Se trata de una proteína monomérica, es decir, tiene una
sola cadena de aminoácidos, con tres dominios (I, II, III)
que se dividen a su vez en subdominios (a, b).
Biosíntesis hepática de la albúmina:
Se sintetiza en el cromosoma 4 y se genera
como un péptido más largo que tiene un
péptido señal de 18 aminoácidos que señaliza
hacia dónde va a ir la albúmina; un propéptido
de 6 aminoácidos; y luego tiene la cadena
principal de 585 aminoácidos.
En el retículo endoplásmico se corta el
péptido señal por medio de una peptidasa quedando
el propéptido inicial de 6 aminoácidos y la cadena.
Se genera la proalbúmina que luego en el aparato de
Golgi o en vesículas de secreción por medio de la
convertasa
se transforma en la albúmina.
Luego va a vesículas de secreción y se va al plasma.
La síntesis es de 10 a 15 gramos por día por lo que en
promedio el hígado produce 12 gramos de albúmina
por día (200 a 400mg/kg/día).

La albúmina es una proteína que tiene una vida media de 20 días y se degrada en todos los
tejidos del músculo, hígado y riñón siendo los responsables del 40-60% del catabolismo de la
albúmina.
El mecanismo de degradación de la albúmina implica la captación de la albúmina por vesículas
endocíticas que se fusionan con lisosomas dando lisosomas secundarios.
La degradación se da si la albúmina está desnaturalizada o alterada, ya que la albúmina nativa no
es degradada por el sistema endosoma-lisosoma.
El producto final de la degradación son aminoácidos libres.
Funciones de la albúmina:
La albúmina es la responsable del 75-80% de la presión oncótica del plasma. La presión oncótica
es la forma de presión osmótica ejercida por las proteínas en el plasma debido a dos efectos:
1. 33% (1/3) se debe a que las proteínas no pueden atravesar las membranas
semipermeables atrayendo los cationes y repeliendo los aniones. Se establece un
gradiente de carga y concentración que determina un gradiente osmótico hacia el espacio
vascular (Efecto Donnan).
2. 66% (2/3) mayor cantidad de moléculas en el espacio intravascular que genera mayor
presión osmótica y permite que no pase demasiada cantidad de líquido hacia el espacio
intersticial cuando no tiene que pasar (Van’t Hoff).
La presión oncótica del plasma es de 28mm Hg (1mOsm), sin embargo, las proteínas generan
19mm Hg dentro de la presión oncótica. 9 de estos 19mm Hg se deben a la unión del sodio a
estas proteínas que produce el Efecto Donnan.
(((19mm de Hg efectos moleculares de las proteínas disueltas + 9mm Hg por sodio unido a las
proteínas produce el Efecto Donnan))).
Dentro de esos 19mmHg que genera la presión oncótica de las proteínas plasmáticas, 80% es
consecuencia de la albúmina y el 20% de otras globulinas. Por lo tanto, la albúmina es la
principal responsable de la presión oncótica en el plasma
.
La albúmina además tiene la función de transporte
. Puede unirse a una gran cantidad de
ligandos
como:
● Ácidos grasos libres
● Calcio
● Hormonas esteroideas
● Bilirrubina
● Triptófano plasmático
● Transporte de cobre (10% del cobre plasmático)
● Fijación de tiroxina y triyodotironina en menor medida a la prealbumina y albúmina fijadora
de la tiroxina
● Transporte de zinc (90% del zinc plasmático)
● Fármacos; sulfonamidas, penicilina G, Dicumarol y ácido salicílico).
Patologías a causa de la albúmina:
En adultos, los valores normales de concentración de albúmina en plasma son 35-50 g/L y puede
variar con la edad y el sexo.
Hiperalbuminemia
: implica valores mayores (>) a 55 g/L y es muy rara, solo se ve en casos de
deshidratación.
Hipoalbuminemia
: es más habitual y puede deberse a menor síntesis, mayor degradación o
pérdida de la circulación hacia el espacio extravascular.
Existe correlación entre los niveles de albúmina y diversas patologías como por ejemplo:
Síndrome nefrótico, sepsis menor (<) a 20 g/L.
Cirrosis hepática severa (deficiencia en la síntesis de albúmina), nefritis glomerular
20-30g/L (mayor pérdida de albúmina).
Hepatitis viral en fase aguda, malnutrición (proteica), artritis reumatoidea,
infecciones severas, se encuentran entre 20-30g/L.
Analbuminemia
: rara, se da con una proporción menor a 1 cada
un millón de personas (<1:1x10 ); es un factor autosómico 6
recesivo. Las personas que tienen analbuminemia, es decir, que
no sintetizan albúmina, sólo tienen edema moderado. Esto se
debe aparentemente a que no se genera albúmina en ningún
momento, por lo que hay una compensación de las otras proteínas
plasmáticas para mantener la presión oncótica en la sangre.
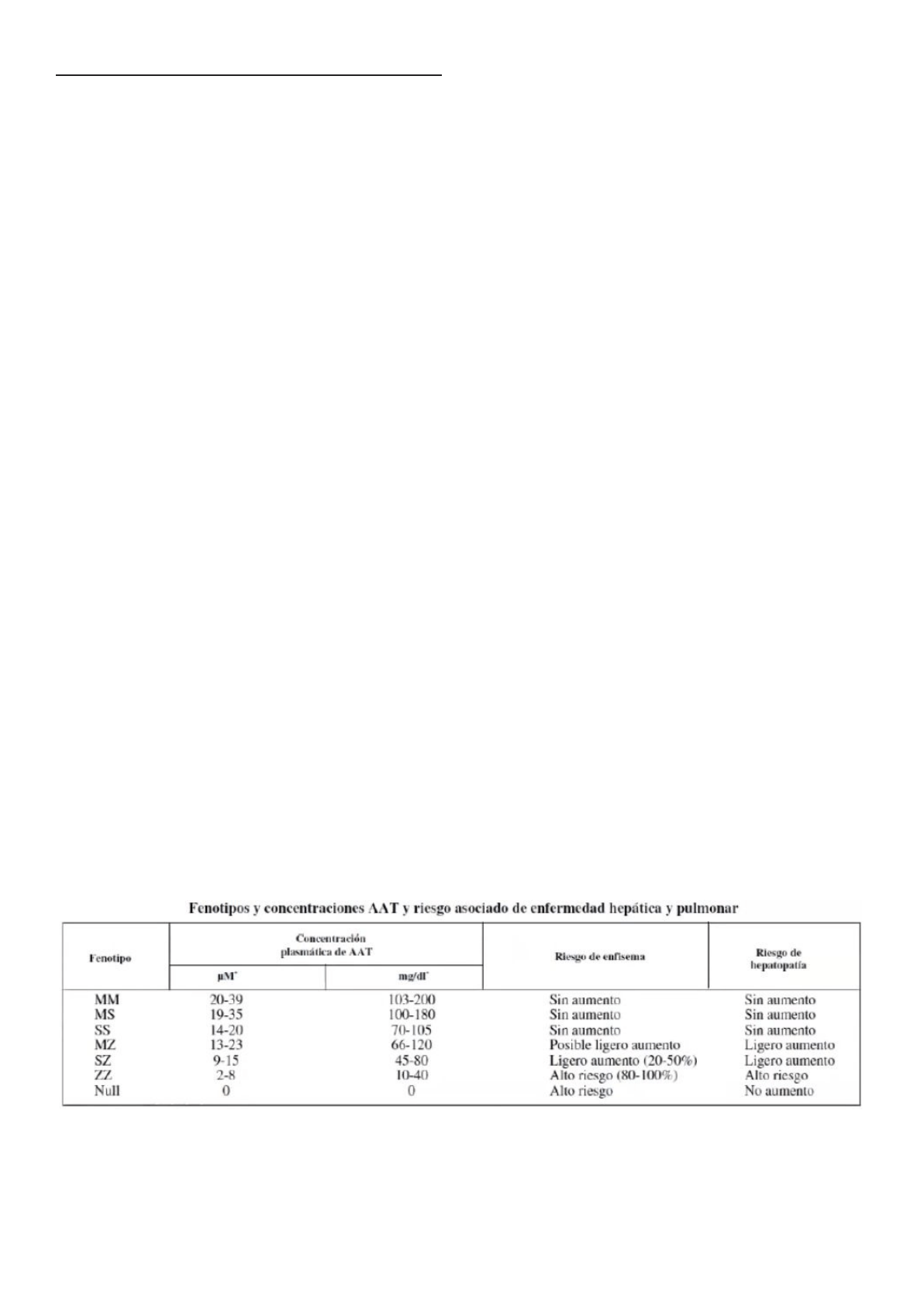
El edema es un exceso de líquido a nivel intersticial observado a nivel de partes blandas y que
predomina en zonas declives.
La instalación de los edemas requiere días a semanas y se manifiesta clínicamente con la
presencia de al menos 5 litros de líquido a nivel intersticial. (SÍNDROME DE GODET O FÓVEA
se ve en la imagen). En zonas donde hay edema, la impresión digital (presiono con el dedo) deja
un hueco.
α-1-ANTITRIPSINA (α 1-ANTIPROTEINASA).
Es el componente principal (>90%) de la fracción (alfa) α 1 del plasma humano (120-220 mg/dl).
Tiene un peso molecular de 52KDa, y al igual que la albúmina, es una proteína de cadena única
de 394 aminoácidos pero presenta 3 cadenas de oligosacáridos.
La α-1-antitripsina se sintetiza en hepatocitos y macrófagos. La α-1-antitripsina pertenece a la
superfamilia de serpinas, inhibidoras de proteasas de Ser (serina).
Si bien se denomina antitripsina también se conoce como inhibidor de peptidasas-1 porque inhibe
una amplia variedad de estas enzimas.
Protege a los tejidos de las enzimas generadas por las células inflamatorias, especialmente de la
elastasa.
Su concentración en plasma aumenta en la inflamación
por lo que también se la considera una
proteína de fase aguda.
Es importante este tipo de proteínas porque lo que hacen es inhibir la acción de proteasas que
son enzimas cuya función es degradar proteínas. Una proteasa que actúa sin control, puede
generar daños a nivel de diferentes tejidos, particularmente frente a la inhibición de la elastasa.
En ausencia de
α-1-antitripsina (antiproteinasa), la elastasa es libre de romper la elastina,
destruyendo el tejido conjuntivo, lo que resulta en:
● Enfermedades respiratorias adquiridas como la enfermedad pulmonar obstructiva crónica
(EPOC) de los fumadores, por oxidación de la Met-358, necesaria para la unión a elastina.
● La deficiencia enzimática hereditaria causa enfisema y cirrosis.
● El efecto genético responsable afecta a 1 entre 3.000-5.000 personas, es una enfermedad
autosómica codominante.

α-2-MACROGLOBULINA.
Es una proteína con un peso molecular de 720KDa; está constituída por 4 subunidades idénticas
de 180KDa; y forma el 8 al 10% de las proteínas totales plasmáticas.
Una de sus funciones es el transporte de zinc, por lo que genera el 10% de dicho transporte.
La α-2-macroglobulina se sintetiza por hepatocitos, monocitos y astrocitos a nivel del sistema
nervioso.
Posee una particularidad bioquímica que es un enlace cíclico tipo ester tiol que es único y está
formado entre una cisteína y un residuo de glutamina.
Al igual que la α-1-antitripsina, también presenta actividad antiproteasa donde el complejo
α-2-macroglobulina-proteasa se elimina por células a través de receptores específicos.
La α-2-macroglobulina presenta unión a citocinas como factor de crecimiento.
HAPTOGLOBINA.
(proteína de transporte, banda alfa-2).
Es una glicoproteína de 91KDa y una concentración normal de 40-180 mg/dL.
La función principal de la haptoglobina es el transporte de hemoglobina (Hb) extracorpuscular,
previniendo la filtración glomerular de la Hb libre.
● Previene la pérdida de hierro.
● Previene la precipitación de Hb en la vía urinaria.
10% de la Hb degradada por día aparece en la circulación como extracorpuscular.
La haptoglobina tiene tres formas polimórficas que son:
● Hp 1-1
● Hp 2-1
● H 2-2
Por ejemplo, en pacientes con anemia hemolítica se encuentran concentraciones bajas de
haptoglobina.
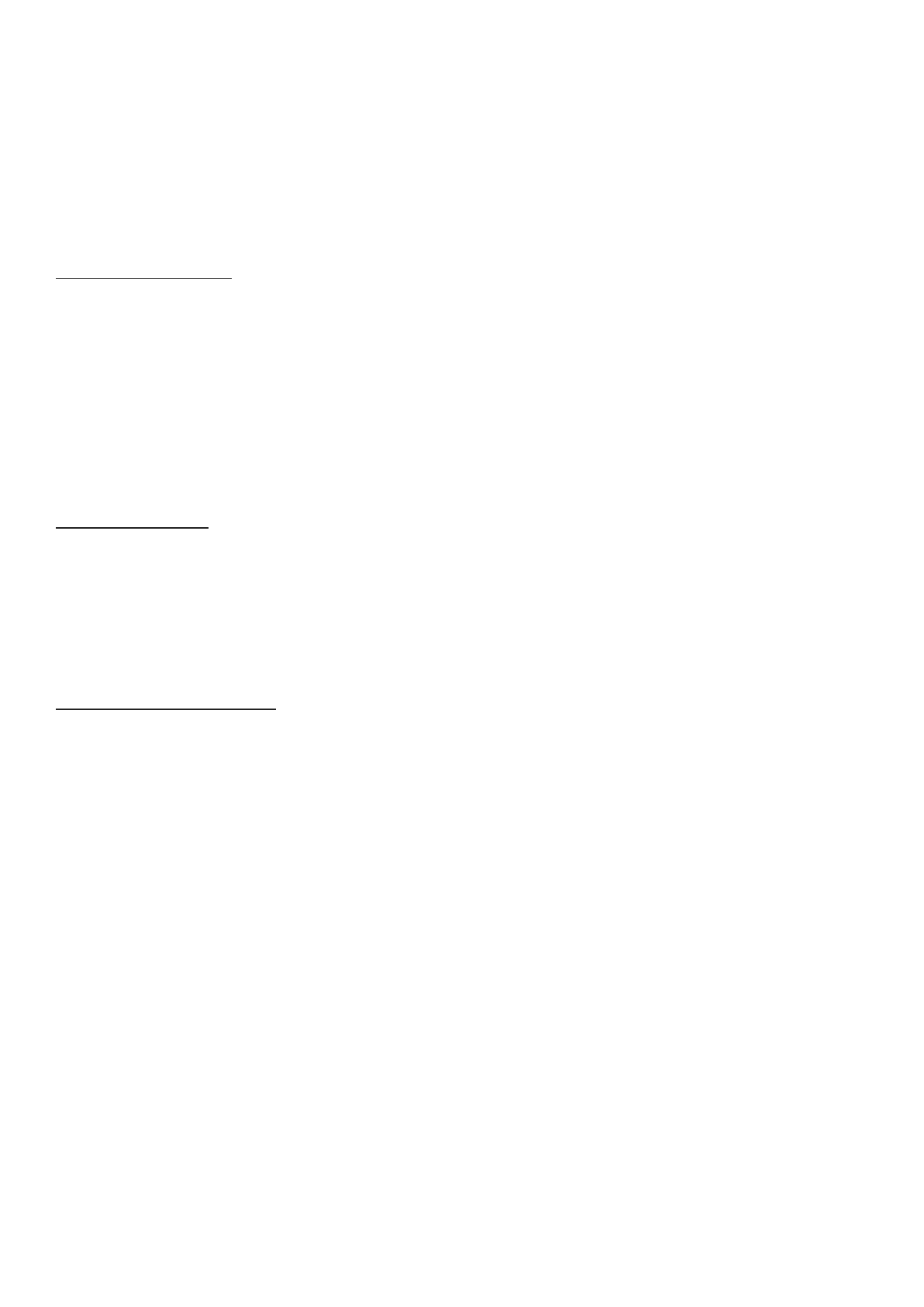
La haptoglobina tiene una vida media corta de 5 días en comparación con la de la albúmina que
es de 20 días.
El complejo Hb-Hp tiene una vida media de 90 minutos.
La haptoglobina también es una proteína de fase aguda y su concentración se incrementa en
estados inflamatorios.
CERULOPLASMINA
. (proteína de transporte; banda alfa-2).
Es una glicoproteína de un peso molecular de 160KDa; presenta color azul debido a su alto
contenido de cobre.
Su función es el transporte de cobre presente en el plasma por lo que transporta el 90%. Cada
molécula se une a seis átomos de cobre en forma íntima.
Muestra actividad ferroxidasa dependiente de cobre. En caso de enfermedad hepática, disminuye.
TRANSFERRINA.
(proteína de transporte; banda beta).
En el plasma el Fe3+ se une a transferrina que es la proteína transportadora específica de hierro.
Tiene dos sitios activos de unión al hierro.
Es una glicoproteína, de forma elipsoidal, de 679 aminoácidos y un tamaño de 80KDa.
PROTEÍNA C REACTIVA
(proteína de fase aguda, banda beta).
La Proteína C reactiva (PCR o CRP) es una proteína plasmática de fase aguda producida por el
hígado.
Es miembro de la familia de las pentraxinas.
● proteínas constituidas por pentámeros unidos formando un anillo.
● circula como un dímero de pentámeros.
La concentración normal es menor a 10mg/L pero su nivel aumenta dramáticamente durante los
procesos inflamatorios.
Este incremento se debe a un aumento en la concentración plasmática de interleuquina 6 (IL-6) y
TNF-α que es producida por macrófagos, células endoteliales, linfocitos T y los adipocitos.
Colabora con el complemento ligándose a células extrañas y dañadas. Estimula la fagocitosis de
macrófagos, los cuales expresan un receptor para PCR, desempeñando un papel importante en
la inmunidad innata.
PROTEÍNAS DE FASE AGUDA.
Son proteínas que aumentan dramáticamente durante procesos agudos como, por ejemplo,
infecciones y procesos inflamatorios de diferente naturaleza.
Entre ellas se encuentran:
● Fibrinógeno.
● α-1-antitripsina.
● Haptoglobina.
● Proteína C reactiva.
El aumento puede ir desde 50% a varios miles de veces.

T1- proteínas plasmáticas. (1).pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.