
Sistema genital masculino - Ross
1
HISTOLOGÍA DEL SISTEMA GENITAL MASCULINO
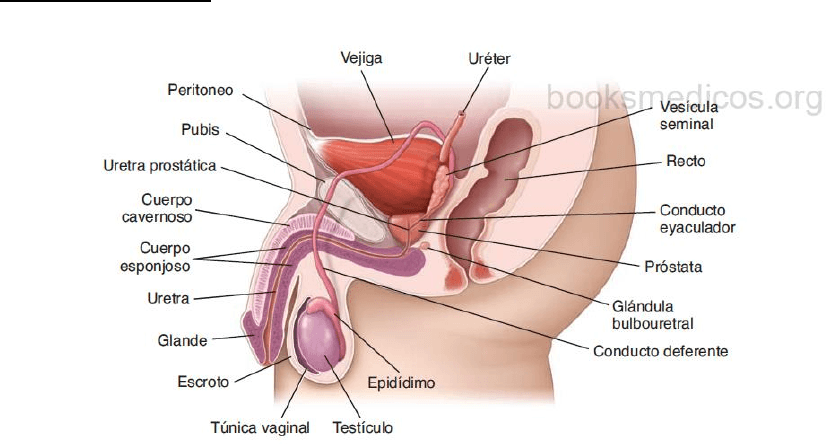
El sistema genital masculino está formado por los testículos, las vías espermáticas, las glándulas
sexuales accesorias y los genitales externos que comprenden el pene y el escroto
Las glándulas sexuales accesorias comprenden las vesículas seminales, la próstata y las glándulas
bulbouretrales. Las dos funciones primarias del testículo son la espermatogénesis (producción de
espermatozoides, denominados gametos masculinos) y la esteroidogénesis (síntesis de andrógenos,
también denominados hormonas sexuales). Los andrógenos, sobre todo la testosterona, son
indispensables para la espermatogénesis, cumplen una función importante en el desarrollo del
embrión XY para que el feto adquiera el fenotipo masculino y son la causa del dimorfismo sexual
TESTÍCULO
Los testículos adultos son órganos ovoides pares que están dentro del escroto fuera de la cavidad
abdominal. Cada testículo se encuentra suspendido en el extremo de un saco musculofascial alargado
que está en continuidad con las capas de la pared anterior del abdomen y se proyecta dentro del
escroto. Los testículos se hallan conectados mediante los cordones espermáticos a la pared abdominal
y están adheridos al escroto por los ligamentos escrotales, que son restos del gubernaculum testis.
Determinación del sexo y desarrollo del testículo
La diferenciación de sexo se logra a través de una cascada de activaciones génicas.
El sexo genético queda determinado en la fecundación por la presencia o la ausencia del cromosoma
Y. Los testículos, sin embargo, no se forman hasta la séptima semana del desarrollo.
El sexo gonadal es determinado por el gen SRY. La expresión del gen SRY en el desarrollo embrionario
inicial desencadena la determinación sexual de las gónadas en los testículos; por lo tanto, es
responsable de la determinación del sexo. Un factor de transcripción denominado factor
determinante testicular (TDF), codificado por el gen SRY, posee un dominio molecular que se fija a
una región específica del ADN y altera su estructura. Éstos a su vez determinan la expresión de otros
genes que inician la formación no sólo de los testículos sino también de otros órganos sexuales
masculinos.
La espermatogénesis requiere que los testículos se mantengan por debajo de la temperatura
corporal normal.
A medida que los testículos descienden de la cavidad abdominal hacia el escroto llevan consigo una
extensión del peritoneo abdominal llamada túnica vaginal, que cubre su superficie anterolateral.
Dentro del escroto la temperatura de los testículos es de 2 a 3 °C más baja que la temperatura corporal.
Esta temperatura más baja es indispensable para la espermatogénesis pero no es necesaria para la
producción hormonal (esteroidogénesis).
El plexo venoso pampiniforme que transporta la sangre desde los testículos hacia las venas
abdominales permite el intercambio de calor entre los vasos sanguíneos y contribuye a mantener los
testículos a una temperatura más baja. La sangre venosa más fresca proveniente del testículo enfría
un poco la sangre arterial antes de que entre en el órgano por un mecanismo de contracorriente
intercambiador de calor. Además, el músculo cremáster, cuyas fibras derivan del músculo oblicuo
interno del abdomen ubicado en la pared abdominal anterior, responde a los cambios de la
temperatura ambiental. Su contracción acerca los testículos a la pared abdominal, mientras que su
relajación los desciende dentro del escroto. Las temperaturas frías también causan la contracción de
una lámina delgada de músculo liso (músculo dartos) en la fascia superficial de las bolsas. La
Sistema genital masculino - Ross
2
contracción del músculo dartos arruga el escroto cuando hace frío para contribuir a regular la pérdida
de calor
Estructura del testículo
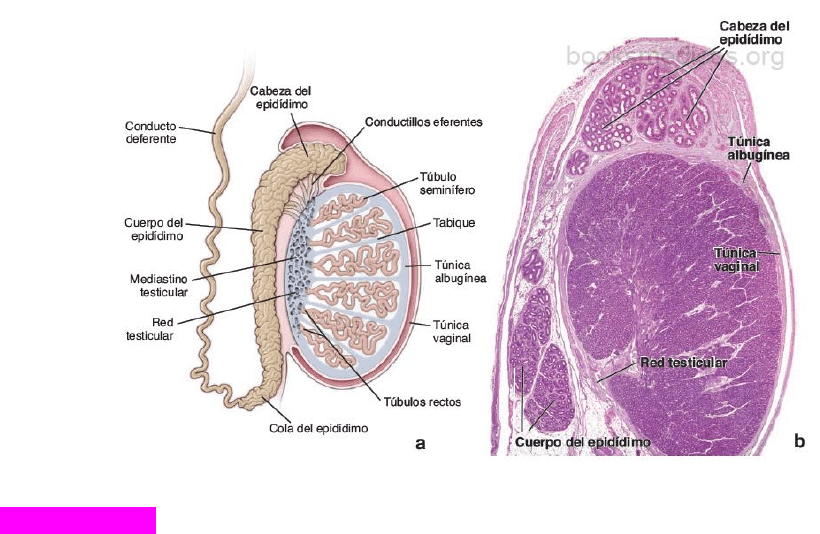
Una cápsula muy gruesa de tejido conjuntivo denso, llamada túnica albugínea, cubre cada testículo.
La parte interna de esta cápsula, la túnica vasculosa, es una lámina de tejido conjuntivo laxo que
contiene vasos sanguíneos.
Cada testículo está dividido en alrededor de 250 lobulillos mediante tabiques de tejido conjuntivo que
se proyectan desde la cápsula. A lo largo de la superficie posterior del testículo, la túnica albugínea
aumenta su espesor y se mete dentro del órgano para formar el mediastino testicular.
Los vasos sanguíneos, los vasos linfáticos y la vía espermática atraviesan el mediastino testicular al
entrar o al salir del testículo.
Cada lobulillo está compuesto por varios túbulos seminíferos muy contorneados.
Cada lobulillo testicular consiste en uno a cuatro túbulos seminíferos en los que se producen los
espermatozoides y un estroma de tejido conjuntivo en la que hay células intersticiales de Leydig que
producen testosterona.
Donde adoptan un curso recto y corto recibe el nombre de túbulo recto (tubulus rectus). Se continúa
con la red testicular que es un sistema de conductos anastomosados dentro del mediastino.
Los túbulos seminíferos consisten en un epitelio seminífero rodeado por una túnica propia.
El epitelio seminífero es un epitelio estratificado complejo y poco habitual que está compuesto por
dos poblaciones celulares básicas:
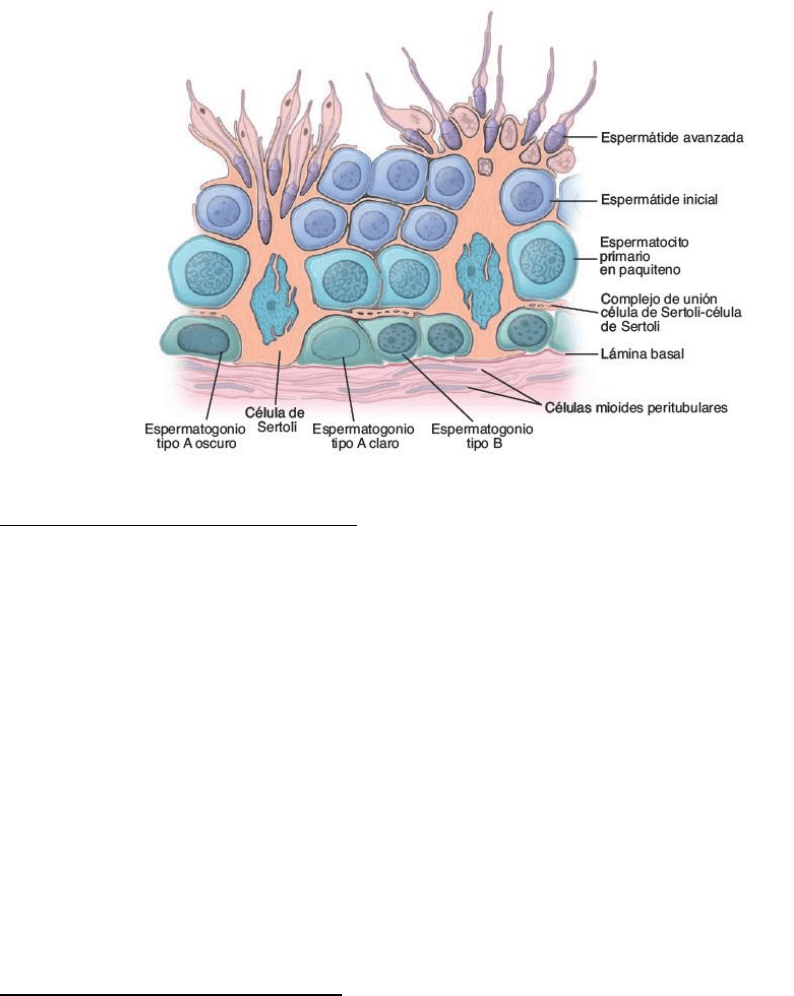
• Las células de Sertoli, también conocidas como células de sostén. Estas células no se dividen
después de la pubertad. Las células de Sertoli son células cilíndricas con evaginaciones apicales
y laterales extensas que rodean las células espermatógenas contiguas y ocupan los espacios
que hay entre ellas. Las células de Sertoli le imparten organización estructural a los túbulos
porque se extienden a través de todo el espesor del epitelio seminífero.
Sistema genital masculino - Ross
3
• Las células espermatógenas con regularidad se dividen y se diferencian en espermatozoides
maduros. Estas células derivan de las células germinativas primordiales originadas en el saco
vitelino que colonizan las crestas gonadales durante la etapa inicial del desarrollo de los
testículos.
Las células espermatógenas se organizan en capas mal definidas de desarrollo progresivo entre células
de Sertoli contiguas. Las células espermatógenas más inmaduras, llamadas espermatogonios, están
apoyadas sobre la lámina basal. Las células más maduras, llamadas espermátides, están adheridas a
la porción apical de la célula de Sertoli en contacto con la luz del túbulo.
La túnica (lámina) propia, está compuesta por tres a cinco capas de células mioides (células
peritubulares contráctiles) y fibrillas colágenas ubicadas por fuera de la lámina basal del epitelio
seminífero. Las contracciones rítmicas de las células mioides crean ondas peristálticas que contribuyen
amover los espermatozoides y el líquido testicular a lo largo de los túbulos seminíferos hacia las vías
espermáticas. Por fuera de la capa mioide hay vasos sanguíneos y una vasculatura linfática extensa, así
como células de Leydig.
Como una consecuencia normal del envejecimiento, la túnica propia aumenta de espesor. Este
engrosamiento se acompaña de una disminución del ritmo de producción de espermatozoides y una
reducción general del tamaño de los túbulos seminíferos. El engrosamiento excesivo de la túnica
propia en la juventud se asocia con la infertilidad.
Células de Leydig
Las células de Leydig (células intersticiales) son células poliédricas grandes Posee característica de
células secretoras de esteroides.
Las células de Leydig se diferencian y secretan testosterona durante las primeras etapas de la vida
fetal. La secreción de testosterona es necesaria en el desarrollo embrionario, la maduración sexual y
la función reproductora:
• En el embrión, la secreción de testosterona y otros andrógenos es indispensable para el
desarrollo normal de las gónadas en el feto masculino. Además de la testosterona, las células

Sistema genital masculino - Ross
4
de Leydig segregan proteína 3 similar a la insulina (INSL3) que estimula el descenso de los
testículos durante el desarrollo.
• En la pubertad, la secreción de testosterona inicia la producción de espermatozoides, la
secreción de las glándulas sexuales accesorias y el desarrollo de las características sexuales
secundarias. La secreción de INSL3 también promueve las divisiones meióticas en los túbulos
seminíferos.
• En el adulto, la secreción de testosterona es indispensable para el mantenimiento de la
espermatogénesis y de las características sexuales secundarias, las vías espermáticas y las
glándulas sexuales accesorias. Además de la secreción de INSL3, las células de Leydig producen
y secretan oxitocina. La oxitocina testicular estimula la contracción de células mioides que
rodean los túbulos seminíferos.
Las células de Leydig son activas en la etapa temprana de diferenciación del feto masculino y
después atraviesa un período de inactividad que comienza aproximadamente a los 5 meses de
la vida fetal. Cuando las células de Leydig se exponen a la estimulación gonadotrófica en la
pubertad, otra vez se convierten en células secretoras de andrógenos y permanecen activas
durante toda la vida.
ESPERMATOGÉNESIS
La espermatogénesis, es decir el proceso por el cual se producen los espermatozoides. Comienza poco
antes de la pubertad bajo la influencia de las concentraciones cada vez mayores de gonadotrofinas
hipofisarias y continúa durante toda la vida. Con fines descriptivos, la espermatogénesis se divide en
tres fases distintas.
Fase espermatogónica
Las células madre espermatogónicos sufren divisiones múltiples y generan una progenie
espermatogónica. Los espermatogonios humanos se clasifican en tres tipos de acuerdo con la
apariencia de los núcleos en los cortes histológicos de rutina:
• Espermatogonios tipo A oscuros (Ad). Estas células tienen un núcleo ovoide con cromatina
granular fina intensamente basófila. Se cree que estos espermatogonios son las células madre
del epitelio seminífero. Se dividen con intervalos irregulares para dar origen a un par de
espermatogonios tipo Ad que permanecen como células madre de reserva, o bien, a un par
de espermatogonios tipo Ap.
• Espermatogonios tipo A claros o pálidos (Ap). Estas células tienen un núcleo ovoide con
cromatina granular fina poco teñida. Los espermatogonios Ap están predestinados a seguir el
proceso de diferenciación que produce los espermatozoides. Sufren varias divisiones mitóticas
sucesivas que aumentan su cantidad. Los espermatogonios tipo Ap son también denominados
células madre de renovación.
• Espermatogonios tipo B. Estas células tienen generalmente un núcleo esferoidal con
cromatina que está condensada en grandes grumos sobre la envoltura nuclear y alrededor del
nucléolo central (v. fig. 22-6). Una característica poco habitual de la división de un
espermatogonio tipo Ad en dos espermatogonios tipo Ap es que las células hijas permanecen
unidas por un puente citoplasmático delgado. Este mismo fenómeno ocurre en cada división
mitótica y meiótica siguiente de la progenie del par original de espermatogonios Ap (fig. 22-
9). Así, toda la progenie de un par inicial de espermatogonios Ap está conectada como si fueran
las perlas de un collar. Estas conexiones citoplasmáticas permanecen intactas hasta las últimas
etapas de la maduración de las espermátides y son indispensables para el desarrollo sincrónico
de cada clon de un par original de células Ap. Después de varias divisiones, los
Sistema genital masculino - Ross
5
espermatogonios tipo A se diferencian en espermatogonios tipo B. La aparición de los
espermatogonios tipo B es el último acontecimiento de la fase espermatogónica.
Fase espermatocítica (meiosis)
En la fase espermatocítica, los espermatocitos primarios sufren meiosis para reducir tanto la
cantidad de cromosomas como el contenido de ADN.
La división mitótica de los espermatogonios tipo B produce espermatocitos primarios. Estos duplican
su ADN poco después de formarse y antes de que comience la meiosis, de modo que cada
espermatocito primario contiene la cantidad normal de cromosomas (2n) pero el doble de cantidad de
ADN (4d). Cada cromosoma se compone de dos cromátides hermanas; de ahí la cantidad 4d de ADN.
La meiosis I trae como consecuencia la reducción de la cantidad de los cromosomas (de 2n a 1n) y de
la cantidad de ADN al estado haploide (de 4d a 2d); por consiguiente, el espermatocito secundario se
caracteriza por una cantidad haploide de cromosomas (1n) y una cantidad 2d de ADN.
Dado que la meiosis II no está precedida por una duplicación del ADN, después de esta división cada
espermátide tiene la cantidad haploide (1n) de cromosomas, cada uno compuesto por una sola
cromátide (1d). A continuación se ofrece una descripción breve de la meiosis espermatocítica.
La profase de la primera división meiótica, en la cual la cromatina se condensa en cromosomas visibles,
dura hasta 22 días en los espermatocitos primarios humanos. Al final de la profase pueden identificarse
44 autosomas y un cromosoma X y otro Y, cada uno con dos hebras cromatínicas (cromátides).
Las células derivadas de la primera división meiótica reciben el nombre de espermatocitos
secundarios. Estas células entran de inmediato en la profase de la segunda división meiótica sin
sintetizar ADN nuevo. La segunda división meiótica es corta y dura sólo algunas horas. Cada
espermatocito secundario tiene una cantidad reducida de cromosomas (1n) que está representada por
22 autosomas y un cromosoma X o Y. Cada uno de estos cromosomas está compuesto por dos
cromátides hermanas.
El espermatocito secundario tiene la cantidad 2d (diploide) de ADN. Durante la metafase de la segunda
división meiótica, los cromosomas se alinean sobre la placa ecuatorial de metafase y las cromátides
hermanas se separan y avanzan hacia polos opuestos del huso. Conforme la segunda división meiótica
se completa y las membranas nucleares se reconstituyen, a partir de cada espermatocito secundario
se forman dos espermátides haploides, cada una con 23 cromosomas de una sola cromátide (1n) y la
cantidad 1d de ADN.
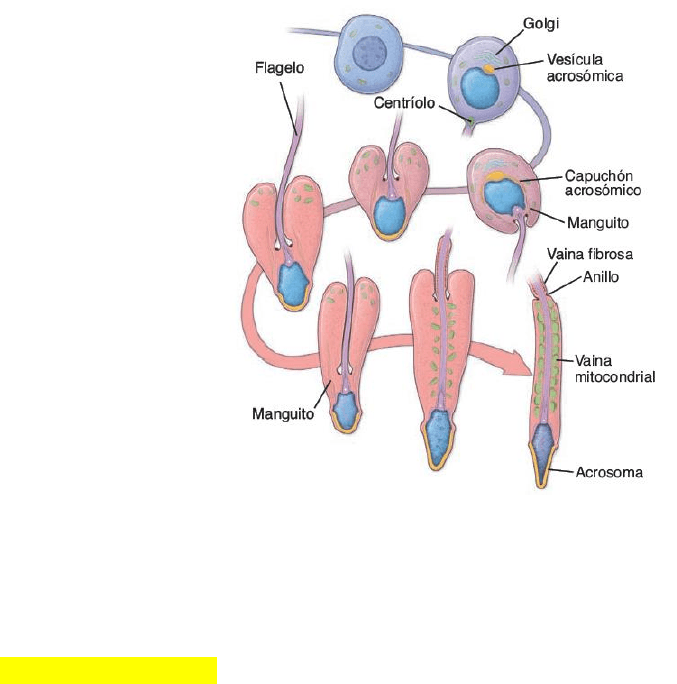
Fase de espermátide (espermiogénesis)
En la fase de espermátide, las espermátides sufren una remodelación celular extensa conforme se
diferencian en espermatozoides maduros.
Cada espermátide producto de la segunda división meiótica es haploide en cuanto a contenido de ADN
(1d) y cantidad de cromosomas (1n) representada por 22 autosomas y un cromosoma X o Y. Ya no
experimentan divisiones adicionales.
Las espermátides haploides sufren un proceso de diferenciación que produce los espermatozoides
maduros, que también son haploides. El estado diploide normal se restaura cuando un espermatozoide
fecunda un ovocito.
Sistema genital masculino - Ross
6
Los espermátides se liberan en la luz de los túbulos seminíferos durante el proceso denominado
espermiación.
Hacia el final de la fase de maduración de la espermatogénesis, las espermátides alargadas se liberan
desde las células de Sertoli en la luz del túbulo seminífero. Este proceso complejo, llamado
espermiación, comprende la eliminación progresiva de complejos de unión célula de Sertoli-
espermátide y el desprendimiento de las espermátides de las células de Sertoli.
El ritmo de la espermiación en el testículo determina la cantidad de espermatozoides en el semen
eyaculado.
Estructura del espermatozoide maduro
El casquete acrosómico que cubre las dos terceras partes anteriores del núcleo contiene
hialuronidasa, neuraminidasa, fosfatasa ácida y una proteasa similar a la tripsina llamada acrosina.
Estas enzimas acrosómicas son indispensables para la penetración de la membrana pelúcida del óvulo.
La liberación de las enzimas acrosómicas cuando el espermatozoide entra en contacto con el ovocito
es el primer paso de la reacción acrosómica. Este proceso complejo facilita la penetración del
espermatozoide y la ulterior fecundación e impide la entrada de otros espermatozoides en el óvulo.
La cola del espermatozoide está subdividida en el cuello, la pieza intermedia, la pieza principal y la
pieza terminal. El cuello corto contiene los centríolos y el origen de las fibras gruesas. La pieza
intermedia contiene las mitocondrias dispuestas en forma helicoidal alrededor de las fibras gruesas y
del complejo axonémico.
Estas mitocondrias proveen la energía para el movimiento de la cola y por ende son las responsables
de la movilidad del espermatozoide. La pieza terminal, que corresponde al flagelo en el
espermatozoide maduro, sólo contiene el complejo axonémico.
Los espermatozoides recién liberados
Los espermatozoides recién liberados son inmóviles y se transportan desde los túbulos seminíferos en
un líquido secretado por las células de Sertoli. El líquido y los espermatozoides fluyen a lo largo de los
túbulos seminíferos, ayudados por las contracciones peristálticas de las células peritubulares
contráctiles de la lámina propia. Luego entran en los túbulos rectos, que son un segmento corto de los
Sistema genital masculino - Ross
7
túbulos seminíferos donde el epitelio consiste sólo en células de Sertoli. En el mediastino testicular el
líquido y los espermatozoides entran en la red testicular, un sistema de conductos anastomosados
revestidos por un epitelio simple cúbico. Desde la red testicular, se desplazan hacia la porción
extratesticular de los conductillos eferentes (ductuli efferentes), que es la primera parte de la vía
espermática, y después hacia el segmento proximal del conducto del epidídimo (ductus epididymis).
Conforme atraviesan los 4 a 5 m de longitud del conducto del epidídimo que es extremadamente
tortuoso, los espermatozoides adquieren movilidad y sufren varios cambios madurativos que
comprenden:
• condensación adicional del ADN nuclear debido a una serie de fenómenos de remodelación
cromatínica que producen el reemplazo de histonas por protaminas. La cabeza del
espermatozoide disminuye de tamaño.
• reducción adicional del citoplasma. Los espermatozoides se hacen más delgados.
• cambios en los lípidos, las proteínas y la glucosilación de la membrana plasmática.
• alteraciones en la membrana acrosomática externa (discapacitación).
El factor de discapacitación asociado a la superficie se agrega para inhibir la capacidad fecundante de
los espermatozoides.
Las contracciones del músculo liso que rodea los conductos cada vez más distales y de calibre mayor
siguen moviendo los espermatozoides por acción peristáltica hasta que alcanzan la porción distal del
conducto del epidídimo, donde se almacenan antes de la eyaculación.
Los espermatozoides pueden vivir varias semanas en la vía espermática del varón pero sobrevivirán
sólo 2 o 3 días dentro del sistema genital femenino. Adquieren la capacidad de fecundar el óvulo sólo
después de haber pasado algún tiempo en el sistema reproductor de la mujer. Este proceso, que
comprende la eliminación y el reemplazo de componentes del glucocáliz (glucoconjugados) de la
membrana del espermatozoide, se denomina capacitación.
TÚBULOS SEMINIFEROS: Ciclo del epitelio seminífero
Las células espermatógenas en diferenciación no están distribuidas al azar en el epitelio seminífero
ya que existen tipos celulares específicos que se agrupan juntos. Estos agrupamientos o asociaciones
ocurren porque hay puentes intercelulares entre la progenie de cada par de espermatogonios tipo Ap
Sistema genital masculino - Ross
8
y porque las células sincronizadas pasan tiempos específicos en cada etapa de la maduración. Todas
las fases de la diferenciación ocurren en forma secuencial en cualquier sitio dado de un túbulo
seminífero porque la progenie de las células madre permanece conectada por puentes citoplasmáticos
y experimenta las divisiones mitóticas y meióticas y la maduración de manera sincrónica.
Cada agrupamiento reconocible o asociación celular se considera una etapa o estadio de un proceso
cíclico. La serie de estadios que hay entre dos apariciones sucesivas del mismo patrón de asociación
celular en cualquier sitio dado del túbulo seminífero, constituye un ciclo del epitelio seminífero.
En el ciclo del epitelio seminífero humano se han podido definir seis estadios o asociaciones celulares
en el ciclo del epitelio seminífero. Estos estadios no están tan claramente delineados como los de los
roedores porque en el hombre las asociaciones celulares ocurren en parcelas irregulares que forman
un patrón en mosaico.
La duración de la espermatogénesis en los seres humanos es de aproximadamente 74 días.
Estudios autorradiográficoss han permitido comprobar que la duración del ciclo del epitelio
seminífero es constante y que tarda alrededor de 16 días en los seres humanos. Y harían falta más o
menos 4,6 ciclos (cada uno de 16 días de duración) o unos 74 días para que un espermatogonio
derivado de un citoblasto completara el proceso de la espermatogénesis. Luego se necesitarían
alrededor de 12 días más para que el espermatozoide atravesara el epidídimo. En el testículo humano
se producen aproximadamente 300 millones de espermatozoides por día. La duración del ciclo y el
tiempo necesario para la espermatogénesis son constantes y específicos de cada especie
Células de Sertoli
Las células de Sertoli constituyen el verdadero epitelio del túbulo seminífero.
Las células de Sertoli (células sustentaculares) son células epiteliales cilíndricas altas que no se dividen
y están apoyadas sobre la lámina basal multiestratificada gruesa del epitelio seminífero. Son las células
de sostén para los espermatozoides en desarrollo que se adhieren a su superficie después de la
meiosis.
El citoesqueleto de la célula de Sertoli contiene: microtúbulos, filamentos intermedios, filamentos de
actina.
Las células de Sertoli se unen entre sí por un complejo de unión célula de Sertoli-célula de Sertoli poco
común. Este complejo se caracteriza, en parte, por una unión excesivamente hermética (zonula
occludens).

Sistema genital masculino - Ross
9
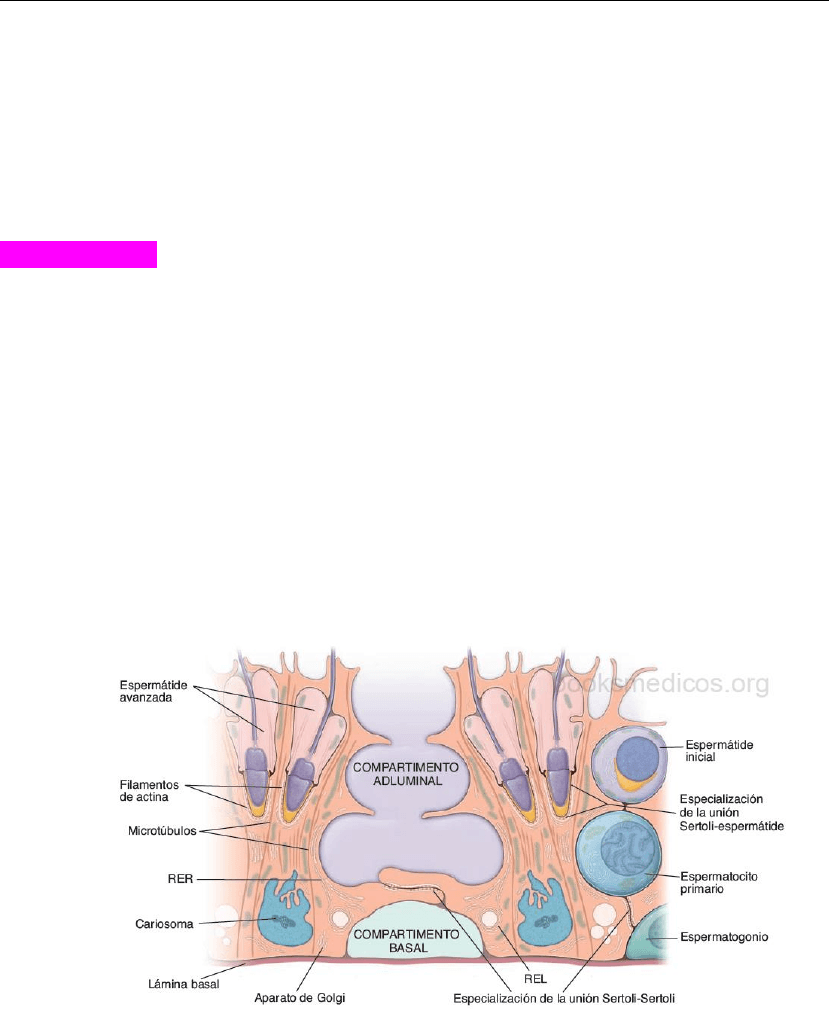
Las uniones célula de Sertoli - célula de Sertoli establecen dos compartimentos epiteliales; un
compartimento epitelial basal y un compartimento adluminal. Los espermatogonios y los
espermatocitos primarios iniciales están restringidos en el compartimento basal (es decir, entre las
uniones célula de Sertoli - célula de Sertoli y la lámina basal).
Los espermatocitos más maduros y las espermátides están restringidos en el lado adluminal de la unión
célula de Sertoli- célula de Sertoli.
El complejo de unión célula de Sertoli-célula de Sertoli forma la barrera hematotesticular.
Esta barrera es indispensable para crear una compartimentación fisiológica dentro del epitelio
seminífero en lo que se refiere a la composición de iones, aminoácidos, hidratos de carbono y
proteínas. Por consiguiente, la composición del líquido en los túbulos seminíferos y las vías
espermáticas difiere considerablemente de la composición del plasma sanguíneo y de la linfa
testicular.
Las proteínas plasmáticas y los anticuerpos circulantes se excluyen de la luz de los túbulos seminíferos.
Los productos de secreción exocrinos de las células de Sertoli, en particular la proteína fijadora de
andrógenos (ABP), que tiene una gran afinidad de unión a la testosterona y la DHT, están muy
concentrados en la luz de los túbulos seminíferos y mantienen una concentración elevada de
testosterona, lo cual provee un microambiente favorable para las células espermatógenas en
diferenciación.
Más importante aún, la barrera hematotesticular aísla las células germinativas haploides
(espermatocitos secundarios, espermátides y espermatozoides), que son genéticamente diferentes y
por ende antigénicas, del sistema inmunitario del varón adulto. Los antígenos producidos por los
espermatozoides, o específicos de estos, están impedidos de alcanzar la circulación sistémica.
Funciones secretoras exocrina y endocrina.
Las células de Sertoli producen factores críticos necesarios para la progresión exitosa de los
espermatogonios hasta convertirse en espermatozoides.
Secretan la proteína fijadora de andrógenos (ABP). La ABP concentra testosterona en el
compartimento adluminal del túbulo seminífero, donde altas concentraciones de testosterona son
esenciales para la maduración normal del espermatozoide en desarrollo.
En las células de Sertoli hay receptores de FSH (hormona foliculoestimulante) y testosterona; en
consecuencia, su función secretora es regulada tanto por la FSH como por la testosterona. Las células
de Sertoli también secretan varias sustancias endocrinas como la inhibina que participa en el circuito
de retrocontrol que inhibe la liberación de FSH desde el lóbulo anterior de la hipófisis. Además, las
células de Sertoli también sintetizan el activador del plasminógeno, que convierte el plasminógeno en
plasmina, una enzima proteolítica activa, transferrina (una proteína transportadora de hierro) y
ceruloplasmina (una proteína transportadora de cobre) Asimismo, las células de Sertoli secretan otras
glucoproteínas que actúan como factores de crecimiento o factores paracrinos, como el factor
inhibidor mülleriano (MIF), el factor de células madre (SCF) y el factor neurotrófico derivado de la línea
celular neuróglica (GDNF).
CONDUCTOS INTRATESTICULARES
Al final de cada túbulo seminífero hay una transición brusca hacia los túbulos rectos. Este segmento
terminal corto del túbulo seminífero está tapizado sólo por células de Sertoli. Cerca de su terminación,
los túbulos rectos se estrechan y su revestimiento epitelial cambia a simple cúbico.

Sistema genital masculino - Ross
10
Los túbulos rectos desembocan en la red testicular, una serie compleja de conductos anastomosados
dentro del tejido conjuntivo muy vascularizado del mediastino testicular. Los conductos de la red
testicular están revestidos por un epitelio simple cúbico.
VIAS ESPERMÁTICAS
Las vías espermáticas derivan del conducto mesonéfrico (de Wolff) y de los túbulos excretores
mesonéfricos.
El desarrollo inicial de las células de Leydig y el comienzo de la secreción de testosterona estimulan el
conducto mesonéfrico (de Wolff) para que se diferencie en la vía espermática del testículo en
desarrollo. La porción del conducto mesonéfrico contigua al testículo en desarrollo adquiere un
trayecto contorneado y se diferencia en el conducto del epidídimo. Además, una cierta cantidad
(aproximadamente 20) de los túbulos excretores mesonéfricos restantes en esta región entra en
contacto con los cordones testiculares en desarrollo y por último se convierte en los conductillos
eferentes que conectan la red testicular en formación con el conducto del epidídimo. La porción distal
del conducto mesonéfrico adquiere una gruesa cubierta de músculo liso y se convierte en el conducto
deferente.
El extremo del conducto mesonéfrico distal da origen al conducto eyaculador y a las vesículas
seminales.
Los conductillos eferentes están revestidos por un epitelio seudocilíndrico estratificado.
En el hombre, unos 20 conductillos eferentes conectan los conductos de la red testicular en el borde
superior del mediastino testicular con la porción proximal del conducto del epidídimo.
Los conductillos eferentes están tapizados por un epitelio seudocilíndrico estratificado en el que hay
cúmulos de células altas y bajas. Dispersas entre las células cilíndricas hay algunas células basales que
actúan como células madre epiteliales. Las células cilíndricas altas son ciliadas.
La mayor parte del líquido secretado en los túbulos seminíferos se reabsorbe en los conductillos
eferentes. El primer sitio de la vía espermática en que aparece una capa de músculo liso es el inicio de
los conductillos eferentes. El transporte de los espermatozoides en los conductillos eferentes se realiza
en gran medida por la acción ciliar y la contracción de esta capa fibromuscular.
EPIDÍDIMO
El epidídimo es un órgano que contiene los conductillos eferentes y el conducto del epidídimo.
El epidídimo es una estructura con forma de semiluna que está apoyada sobre las superficies superior
y posterior del testículo. Mide más o menos 7,5 cm de longitud y está compuesto por los conductillos
eferentes y el conducto del epidídimo, junto con los vasos sanguíneos, el músculo liso y las cubiertas
de tejido conjuntivo asociados.
En el epidídimo se describe una cabeza, un cuerpo y una cola. Los conductillos eferentes ocupan la
cabeza y el conducto del epidídimo ocupa el cuerpo y la cola. Los espermatozoides nuevos que entran
en el epidídimo, provenientes del testículo, maduran durante su paso a lo largo del conducto del
epidídimo, donde adquieren movilidad y la capacidad de fecundar un ovocito. Después de madurar en
el epidídimo, los espermatozoides pueden transportar su contenido haploide de ADN hasta el óvulo y
después de la capacitación pueden unirse a receptores de espermatozoides situados en la membrana
pelúcida del óvulo. Esta unión desencadena la reacción acrosómica en la cual el espermatozoide utiliza
las enzimas de su acrosoma para perforar la cubierta externa del ovocito.

Sistema genital masculino - Ross
11
Las células principales del epitelio seudoestratificado del epidídimo poseen estereocilios.
Al igual que la mayor parte de la vía espermática, el conducto del epidídimo también está revestido
por un epitelio pseudocilíndrico estratificado. En general, contiene dos tipos celulares:
• células principales. Con microvellosidades modificadas largas e irregulares que reciben el
nombre de estereocilios presentes en los polos apicales.
• células basales, pequeñas que descansan sobre la lámina basal. Son células madre del epitelio
del conducto.
Las células epididimarias tienen función tanto absortiva como secretora.
La mayor parte del líquido que no se reabsorbe en los conductillos eferentes se reabsorbe en la porción
proximal del epidídimo. Las células epiteliales también fagocitan cualquier cuerpo residual que no haya
sido eliminado por las células de Sertoli, así como los espermatozoides que se degeneran en el
conducto.
La cubierta de músculo liso del conducto del epidídimo
En la cabeza del epidídimo y en la mayor parte del cuerpo, la cubierta muscular lisa consiste en una
capa delgada de músculo liso circular que se parece a la de los conductillos eferentes.
En la cola se une una capa longitudinal interna y otra externa. Estas tres capas luego se continúan con
las tres capas musculares lisas del conducto deferente, que es el segmento que sigue en la vía
espermática. En la cabeza y en el cuerpo del epidídimo las contracciones peristálticas rítmicas
espontáneas, sirven para mover los espermatozoides a lo largo del conducto. En la cola, que funciona
como el reservorio principal de espermatozoides maduros, ocurren pocas contracciones peristálticas.
Los espermatozoides maduros son impulsados hacia el conducto deferente por las contracciones
intensas de las tres capas musculares lisas después de la estimulación nerviosa adecuada que se asocia
con la eyaculación.
CONDUCTO DEFERENTE
El conducto deferente (vas deferens), es una continuación directa de la cola del epidídimo. Asciende
a lo largo del borde posterior del testículo. Después se introduce en el abdomen como un componente
del cordón espermático al atravesar el conducto inguinal.
El cordón espermático contiene todas las estructuras que se dirigen hacia el testículo o provienen de
él. Además del conducto deferente, el cordón espermático contiene la arteria testicular, arterias
pequeñas para el conducto deferente y el músculo cremáster, el plexo pampiniforme, vasos linfáticos,
fibras nerviosas simpáticas y la rama genital del nervio genitofemoral. Todas estas estructuras están
rodeadas por fascias derivadas de la pared abdominal anterior.
Después de abandonar el cordón espermático, el conducto deferente desciende en la pelvis hasta la
altura de la vejiga, donde su extremo distal se dilata para formar la ampolla del conducto deferente
que recibe el conducto de la vesícula seminal y continúa hasta la uretra a través de la próstata con el
nombre de conducto eyaculador.
El conducto deferente está revestido por un epitelio seudocilíndrico estratificado que se parece mucho
al del epidídimo. Las células cilíndricas altas también poseen estereocilios. Las células basales se
localizan sobre la lámina basal. La mucosa parece tener pliegues longitudinales profundos en la mayor
parte de su longitud.

Sistema genital masculino - Ross
12
Las capas longitudinales desaparecen cerca del origen del conducto eyaculador. El epitelio de la
ampolla y del conducto eyaculador parece tener una función secretora.
GLANDULAS SEXUALES ACCESORIAS
Las dos vesículas seminales segregan un líquido con fructosa abundante.
Las vesículas seminales son un par de glándulas tubulares, alargadas y muy tortuosas, ubicadas en la
pared posterior de la vejiga urinaria paralela a la ampolla de los conductos deferentes.
Un conducto excretor corto que parte de cada vesícula seminal se combina con la ampolla del conducto
deferente para formar el conducto eyaculador. Las vesículas seminales se desarrollan como
evaginaciones de los conductos mesonéfricos (de Wolff) en la región de la ampolla futura. La pared de
las vesículas seminales contiene una mucosa, una capa de músculo liso delgada y una cubierta fibrosa.
La mucosa posee muchos pliegues que aumentan la extensión de la superficie secretora. El epitelio
seudocilíndrico estratificado contiene células cilíndricas altas no ciliadas y células bajas apoyadas sobre
la lámina basal.
La secreción de las vesículas seminales es un material viscoso blanco amarillento. Contiene fructosa,
que es el sustrato metabólico principal para los espermatozoides, junto con otros sacáridos simples,
aminoácidos, ácido ascórbico y prostaglandinas. Si bien las prostaglandinas se aislaron inicialmente en
la próstata (de ahí su nombre), en las vesículas seminales se sintetizan en gran cantidad. La contracción
de la cubierta muscular lisa de las vesículas seminales durante la eyaculación expulsa su secreción hacia
los conductos eyaculadores y contribuye a evacuar los espermatozoides de la uretra. La función
secretora y la morfología de las vesículas seminales están bajo el control de la testosterona.
PRÓSTATA
La próstata es la glándula sexual accesoria más grande del sistema genital masculino. Su forma y su
tamaño son comparables a los de una nuez. La función principal de la próstata consiste en secretar un
líquido claro, levemente alcalino (pH 7,29) que contribuye a la composición del semen.
Está ubicada en la pelvis, debajo de la vejiga donde rodea el segmento prostático de la uretra. Está
compuesta por 30 a 50 glándulas túbuloalveolares dispuestas en tres capas concéntricas: una capa
mucosa interna, una capa submucosa intermedia y una capa periférica que contiene las glándulas
prostáticas principales. Las glándulas de la capa mucosa segregan directamente hacia la uretra; las
otras dos capas poseen conductos que desembocan en los senos prostáticos ubicados a cada lado de
la cresta uretral en la pared posterior de la uretra.
El parénquima prostático adulto está dividido en cuatro zonas que son anatómica y clínicamente
distintas:
• La zona central rodea los conductos
eyaculadores conforme atraviesan la
próstata. Contiene alrededor del 25 % del
tejido glandular.
• La zona periférica constituye el 70 % del
tejido glandular de la próstata. Rodea la zona
central y ocupa la parte posterior y las
porciones laterales de la glándula. La mayor
parte de los carcinomas prostáticos se
originan en la zona periférica de la próstata.
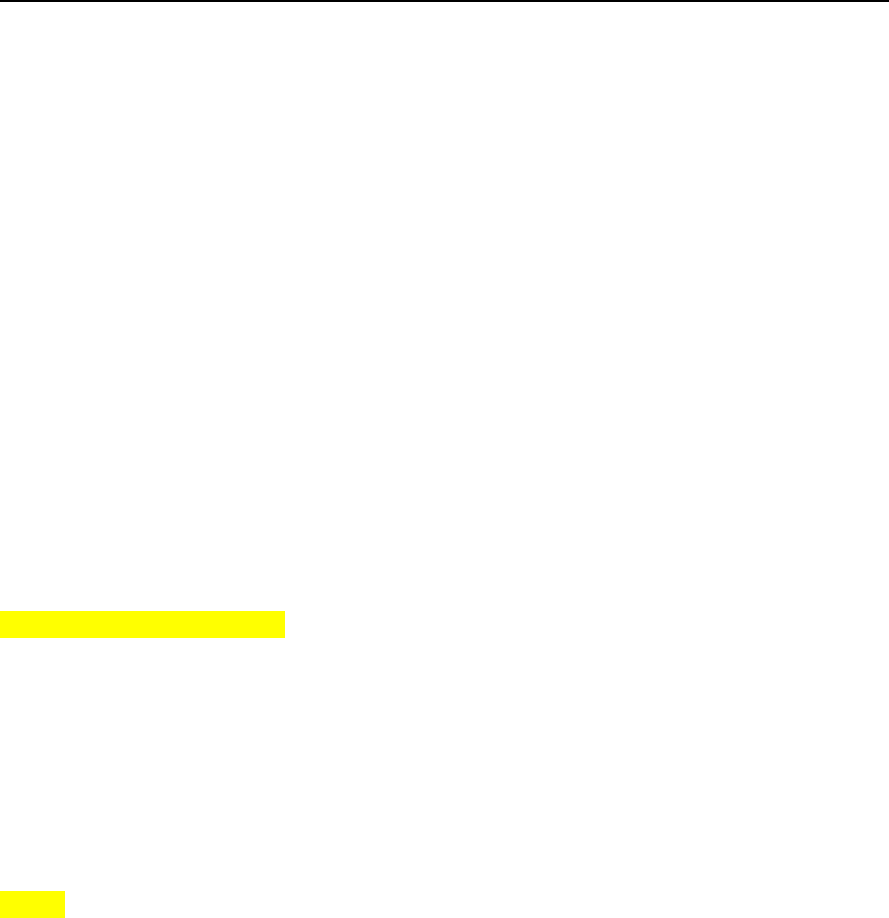
Sistema genital masculino - Ross
13
La zona periférica se puede palpar en el tacto rectal. Esta zona también es la más susceptible
a la inflamación.
• La zona transicional rodea la uretra prostática; constituye el 5 % del tejido glandular prostático
y contiene las glándulas mucosas.
• La zona periuretral contiene glándulas mucosas y submucosas.
La proliferación del epitelio glandular prostático es regulada por la hormona dihidrotestosterona.
En cada una de las zonas prostáticas, el epitelio glandular por lo general es cilíndrico simple pero
pueden haber parcelas de epitelio simple cúbico, plano simple y a veces seudoestratificado.
Se encuentra bajo la influencia de las hormonas sexuales, como la testosterona y los andrógenos
suprarrenales. Estas hormonas se introducen en las células secretoras del epitelio glandular y son
convertidas en dihidrotestosterona (DHT) por la enzima 5α-reductasa. La DHT es unas 30 veces más
potente que la testosterona.
Las células epiteliales prostáticas producen varias enzimas, en particular antígeno prostático específico
(PSA), fosfatasa ácida prostática (PAP) y fibrinolisina, además de ácido cítrico.
• El antígeno prostático específico (PSA), una serina proteasa, uno de los marcadores tumorales
de mayor importancia clínica. En condiciones normales, el PSA se secreta hacia los alvéolos y
en última instancia se incorpora en el líquido seminal. La secreción alveolar es expulsada hacia
la uretra prostática durante la eyaculación por la contracción del tejido fibromuscular de la
próstata. Dado que el PSA predominantemente se libera en la secreción prostática, sólo una
cantidad muy reducida (por lo general menos de 4 ng/ml) circula en la sangre de un hombre
sano.
• La fosfatasa ácida prostática (PAP) es una enzima que regula la proliferación celular y el
metabolismo del epitelio glandular de la próstata
• La fibrinolisina secretada por la próstata sirve para licuar el semen.
GLÁNDULAS BULBOURETRALES
Las dos glándulas bulbouretrales (glándulas de Cowper) son estructuras del tamaño de un guisante
ubicadas en el diagrama urogenital. El conducto de cada glándula atraviesa la fascia inferior del
diafragma urogenital y se une a la porción inicial de la uretra esponjosa. Estas glándulas son
tubuloalveolares compuestas que desde el punto de vista estructural se parecen a glándulas secretoras
de moco. El epitelio cilíndrico simple está bajo el control de la testosterona.
La secreción glandular clara, de tipo mucoso, contiene una gran cantidad de galactosa y galactosamina,
ácido galacturónico, ácido siálico y metilpentosa.
SEMEN
El semen contiene líquido y espermatozoides del testículo y productos de secreción del epidídimo, del
conducto deferente, de la próstata, de las vesículas seminales y de las glándulas bulbouretrales. El
líquido seminal provee nutrientes (p. ej., aminoácidos, citratos y fructosa) y protección a los
espermatozoides durante su paso a través de las vías espermáticas.
El semen es alcalino (pH 7,7) y contribuye a neutralizar el medio ácido de la uretra y la vagina. Los
principales componentes del semen son las secreciones de las vesículas seminales (del 65 % al 75 %) y
de la próstata (del 25 % al 30 %). Otros componentes adicionales incluyen los líquidos testiculares (del
Sistema genital masculino - Ross
14
2 % al 5 %) que no fueron completamente absorbidos en los túbulos rectos así como secreciones de
las glándulas bulbouretrales (de Cowper) que representan menos del 1 %. El semen también contiene
prostaglandinas (producidas por las vesículas seminales) que ejercen su influencia sobre el tránsito de
los espermatozoides en los sistemas genitales masculino y femenino y desempeñan un papel en la
implantación del óvulo fecundado.
PENE
El pene consiste principalmente en dos masas dorsales de tejido eréctil, cuerpos cavernosos, y una
masa ventral del mismo tejido, cuerpo esponjoso, en el que está incluido el segmento esponjoso de la
uretra. Una capa fibroelástica densa, la túnica albugínea, enlaza los tres cuerpos y forma una cápsula
alrededor de cada uno. Los cuerpos cavernosos contienen una abundancia de espacios vasculares
amplios de forma irregular que están revestidos por endotelio vascular. Estos espacios están rodeados
por una capa delgada de músculo liso que forma cordones dentro de la túnica albugínea que
interconectan y entrecruzan el cuerpo cavernoso.
El tejido conjuntivo intersticial contiene muchas terminaciones nerviosas y vasos linfáticos. Los
espacios vasculares aumentan de tamaño y adquieren una rigidez mayor al llenarse de sangre, que
proviene sobre todo de la arteria profunda del pene que se divide en ramas denominadas arterias
helicinas. Estas arterias se dilatan durante la erección para aumentar el flujo sanguíneo hacia el pene.
Existe una anastomosis arteriovenosa (AV) entre la arteria profunda del pene y el sistema venoso
periférico.
La piel del pene es fina y está poco adherida al tejido conjuntivo laxo subyacente excepto a la altura
del glande, donde es muy delgada y está firmemente adherida. En el tejido subcutáneo no hay tejido
adiposo. No obstante, hay una capa delgada de músculo liso que se continúa con el dartos del escroto.
El glande está cubierto por un repliegue de la piel llamado prepucio, que se asemeja a la membrana
mucosa en su aspecto interno. En la piel del pene existen muchas glándulas sebáceas próximas al
glande.
El pene está inervado por fibras somáticas y motoras viscerales (simpáticas y parasimpáticas). Hay una
gran cantidad de terminaciones nerviosas sensitivas distribuidas por todos los tejidos del pene. Las
fibras motoras viscerales inervan el músculo liso de la trabécula de la túnica albugínea y los vasos
sanguíneos. Tanto las fibras nerviosas motoras viscerales como las sensitivas cumplen una función
Sistema genital masculino - Ross
15
esencial en las respuestas de erección y eyaculación. La estimulación parasimpática inicia la erección,
mientras que la estimulación simpática completa la erección y causa la eyaculación, una contracción
rítmica del músculo liso que expulsa semen de la uretra esponjosa.
Embriología:
Los testículos se desarrollan en la pared posterior del abdomen y luego descienden hasta el escroto.
Los testículos se desarrollan retroperitonealmente en asociación estrecha con el sistema urinario en
la pared posterior de la cavidad abdominal. Los testículos, al igual que los ovarios, tienen tres orígenes:
• El mesodermo intermedio forma las crestas urogenitales en la pared abdominal posterior y da
origen a las células de Leydig (células intersticiales) y a las células mioides (células contráctiles
peritubulares).
• El epitelio mesodérmico (mesotelio celómico) cubre las crestas y da origen a los cordones
epiteliales de forma similar a un dedo denominados cordones sexuales primarios. Estos
cordones crecen hacia el mesodermo intermedio subyacente y son colonizados por células
germinativas primordiales. Los cordones sexuales primarios también dan origen a las células
de Sertoli.
• Las células germinativas primordiales migran desde el saco vitelino hacia las gónadas en
desarrollo donde se incorporan a los cordones sexuales primarios. Allí se dividen y se
diferencian en espermatogonios.Como ya se observó, la migración de las células germinativas
primordiales hasta las crestas genitales induce la proliferación de las células mesodérmicas de
las crestas urogenitales y las células del mesotelio celómico para que se desarrollen los
cordones sexuales primitivos. En esta etapa estos cordones consisten en células germinativas
primordiales, células precursoras de las células de Sertoli y una capa circundante de células
mioides. Más tarde, los cordones sexuales primitivos se diferencian en los cordones
seminíferos que dan origen a los túbulos seminíferos, los túbulos rectos y la red testicular. En
la primera etapa del desarrollo los testículos aparecen en la pared abdominal posterior como
primordios indiferenciados derivados de las crestas urogenitales que son idénticas en ambos
sexos. Durante esta etapa indiferente, el embrión tiene la potencialidad de convertirse en un
varón o una mujer. Sin embargo, la expresión del gen SRY, exclusivamente en las células
precursoras de las células de Sertoli, orquesta el desarrollo masculino del embrión. Al principio
de la embriogénesis masculina el mesénquima que separa los cordones seminíferos da origen
a las células (intersticiales) de Leydig que producen testosterona para estimular el desarrollo
del primordio indiferente en un testículo. Además, la testosterona causa la proliferación y la
diferenciación de los conductos mesonéfricos (de Wolf) de los que derivan las vías
espermáticas. También en esta etapa inicial las células (sustentaculares) de Sertoli que se
desarrollan dentro de los cordones testiculares producen otra sustancia hormonal importante
llamada factor inhibidor mülleriano (MIF).
La estructura molecular del MIF es similar a la del factor de crecimiento transformador (TGF). Es una
glucoproteína grande que inhibe la división celular de los conductos paramesonéfricos (de Müller), lo
cual a su vez inhibe el desarrollo de los órganos genitales femeninos.
El desarrollo y la diferenciación de los genitales externos (también a partir de la etapa sexual
indiferente) ocurren al mismo tiempo y se deben a la acción de la dihidrotestosterona (DHT), un
producto de la conversión de la testosterona mediante la 5"-reductasa. Si no hay DHT, sin importar el
Este documento contiene más páginas...
Descargar Completo
SISTEMA GENITAL MASCULINO LATARJET.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.