
Laboratorio I
1
Seguridad
Normas generales
1. Seguir atentamente las indicaciones del/la docente para la ejecución de la actividad.
2. Estar sumamente atento a la hora de manipular materiales de vidrio o sustancias químicas con cierto grado de
peligrosidad.
3. No comer, beber o fumar en el laboratorio.
4. En el caso de un contacto directo con algún reactivo, lavar la zona inmediatamente con abundante agua y, si cae
sobre la ropa, quitarse la prenda y lavar la zona de la piel con la que estuvo en contacto.
5. Siempre usar guardapolvo, calzado cerrado, pantalones largos y cabello recogido. En el caso de manipular algún
elemento o reactivo también se deben utilizar guantes y gafas.
6. Prestar atención a los rótulos y fichas de seguridad de los reactivos químicos.
7. Tener al alcance los materiales necesarios para efectuar la actividad práctica y mantener la limpieza.
8. Tener conocimiento de la técnica experimental a utilizar y de los fundamentos teóricos por los cuales se rige.
9. Realizar las actividades experimentales sin efectuar modificaciones del método, a menos que sean indicadas por
el/la docente.
Protección personal
No podrán ingresar al laboratorio los alumnos que no cuenten con: Guardapolvo y Anteojos de protección.
No se recomienda el uso de minifalda o pantalones cortos, sandalias u ojotas, colgantes y anillos.
Usar pantalón largo, calzado cerrado y cabello recogido.
El guardapolvo tiene que ser de algodón, blanco, manga larga, con broches y puños.
Usar guantes.
Evitar la contaminación de equipos limpios.
No tocar útiles.
Siempre lavarse las manos después de quitárselos.
No reutilizar guantes.
Extraerlos sin tocar la parte exterior contaminada con las manos.
Método de extracción:
I. Saque uno de los guantes desde la muñeca hacia los dedos.
II. Con la mano expuesta saque el segundo guante de la misma manera que sacó el anterior.
III. Descártelos.
IV. Lávese las manos.
Tipos: manoplas, vinilo, latex y nitrilo.
Información
Localice los dispositivos de seguridad más próximos.
Utilice elementos tales como matafuegos, duchas de seguridad, botiquín, salidas de emergencia, etc.
Las duchas de seguridad: equipos de emergencias para los casos de proyecciones, derrames o salpicaduras de
productos químicos sobre las personas, con riesgo de contaminación o quemadura química
Lea las etiquetas de seguridad.
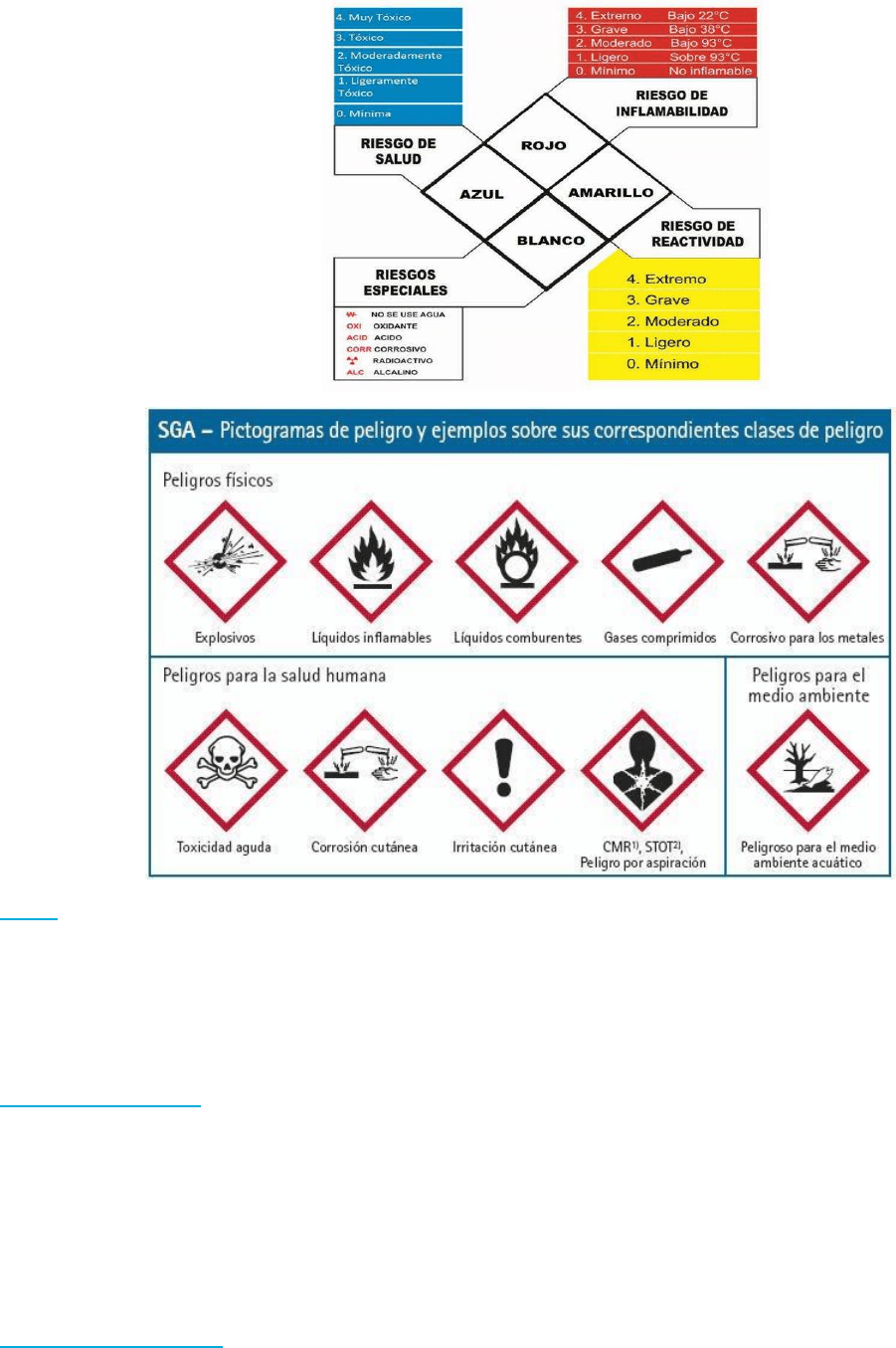
Los envases de reactivos contienen pictogramas y frases que informan sobre las características del producto.
Laboratorio I
2
Frases
R: indica riesgo específico.
R.8: peligro de fuego en contacto con materiales conductibles.
R. 22: nocivo por ingestión.
S: indican consejos de prudencia de cada producto.
S. 2: manténgase fuera del alcance de los niños.
Trabaje con seguridad
Está prohibido fumar, comer y beber dentro del laboratorio.
No inhale, pruebe o huela reactivos químicos.
No usar celular durante la actividad práctica.
Mantenga el área de trabajo ordenada.
Al lavar el material que utilizó hágalo con los elementos de limpieza que encontrará en cada pileta.
No sustituya nunca un reactivo químico por otro en sus experimentos.
No utilice ni limpie nunca ningún frasco de reactivos que haya perdido su etiqueta.
Precauciones específicas
Manipulación de material de vidrio.
No use nunca materiales de vidrio que estén agrietados o rotos

Laboratorio I
3
Deposite el material de vidrio roto, limpio, en los contenedores apropiados, nunca en los cestos de
basura ni piletas.
Cañerías
Celeste: aire comprimido
Blanco: agua destilada
Verde: agua corriente
Amarillo: gas
Calentamiento de líquidos
No caliente nunca un recipiente totalmente cerrado.
Dirija siempre la boca del recipiente en dirección contraria a la suya y a las personas más cercanas.
Manipulación de reactivos químicos
Trabaje siempre bajo campana extractora cuando use sustancias peligrosas.
Está terminantemente prohibido pipetear reactivos con la boca.
Evite todo contacto directo con cualquier reactivo.
Usar propipetas de la manera correcta.
Eliminación de residuos
La eliminación inadecuada o la ausencia de identificación, son causa frecuente de contaminación ambiental y de
accidentes.
Se rige por la ley nacional de residuos N° 24.051.
Se descartan potes, bidones o botellas según corresponda rotulados correctamente.
Los envases solo se llenan hasta un 75% de su capacidad.
Nunca vierta desechos en las cañerías o desagües.
En caso de accidentes
Si se derrama un reactivo
Alertar a compañeros y docentes.
Limpiar inmediatamente siguiendo las instrucciones del docente con los materiales de absorción
adecuados.
En caso de contacto directo con un reactivo.
Es importante actuar rápido.
Lavar la zona afectada con abundante agua.
Quitarse la ropa contaminada.
Si fuera necesario utilice las duchas de seguridad.
Salpicaduras a los ojos
Utilice el lava ojos del pasillo durante 20 minutos.
Acudir a un especialista luego del accidente sin importar lo leve que parezca.
Derrame de líquidos de peligrosidad
Utilizar sustancias absorbentes y luego se debe barrer el material absorbente y desechar en el tacho de
residuos químicos.
Derrame de solidos
Juntar con el cuidado especial que requiera dependiendo del tipo de sólido y luego se debe desechar en
el tacho de residuos químicos.
En caso de incendios
Incendio de reactivos
Si está aislado (en un tubo de ensayos, un vaso de precipitados, etc.) se lo puede ahogar con un vidrio de
reloj.
Si el fuego se expandió en la mesada se puede apagar cubriéndolo con arena o con una tela de amianto.
Incendio de ropas
Pedir ayuda gritando y arrojarse al piso rodando sobre sí mismo para apagar las llamas.
No correr hasta la ducha de seguridad a menos que esté realmente cerca.

Laboratorio I
4
Otra solución también es envolver la zona afectada en tela de amianto. Una vez apagado el fuego, es
importante que la persona permanezca quieta, recostada y protegida del frío hasta que llegue la ayuda
especializada.
Material de laboratorio, Pesada
Material calibrado o volumétrico:
todo aquel que se utiliza para la medición de volúmenes exactos y con un error
determinado. Estos materiales se encuentran calibrados con patrones de volumen a una temperatura específica de
20ºC de manera que en ningún caso podrá calentarse el material volumétrico.
Matraz recipiente de fondo plano con forma de pera que tiene un cuello largo y delgado. Se utilizan
fundamentalmente para la preparación de soluciones.
Pipetas se utilizan para poder trasvasar un determinado volumen de líquido, con un determinado error, y a una
determinada temperatura, de un recipiente que lo contiene a otro. Se dividen en pipetas graduadas y ball pipetas.
Las ball pipetas sólo sirven para medir un único volumen de líquido, pero la precisión con la que lo hacen es muy
elevada en comparación con las pipetas graduadas; estas pueden ser de doble o simple aforo.
Pipeta Ball
Graduada Pipeta
Probeta Recipiente de vidrio para la medida de volúmenes aproximados y, generalmente, variables. No debe
utilizarse para preparar disoluciones en el mismo.
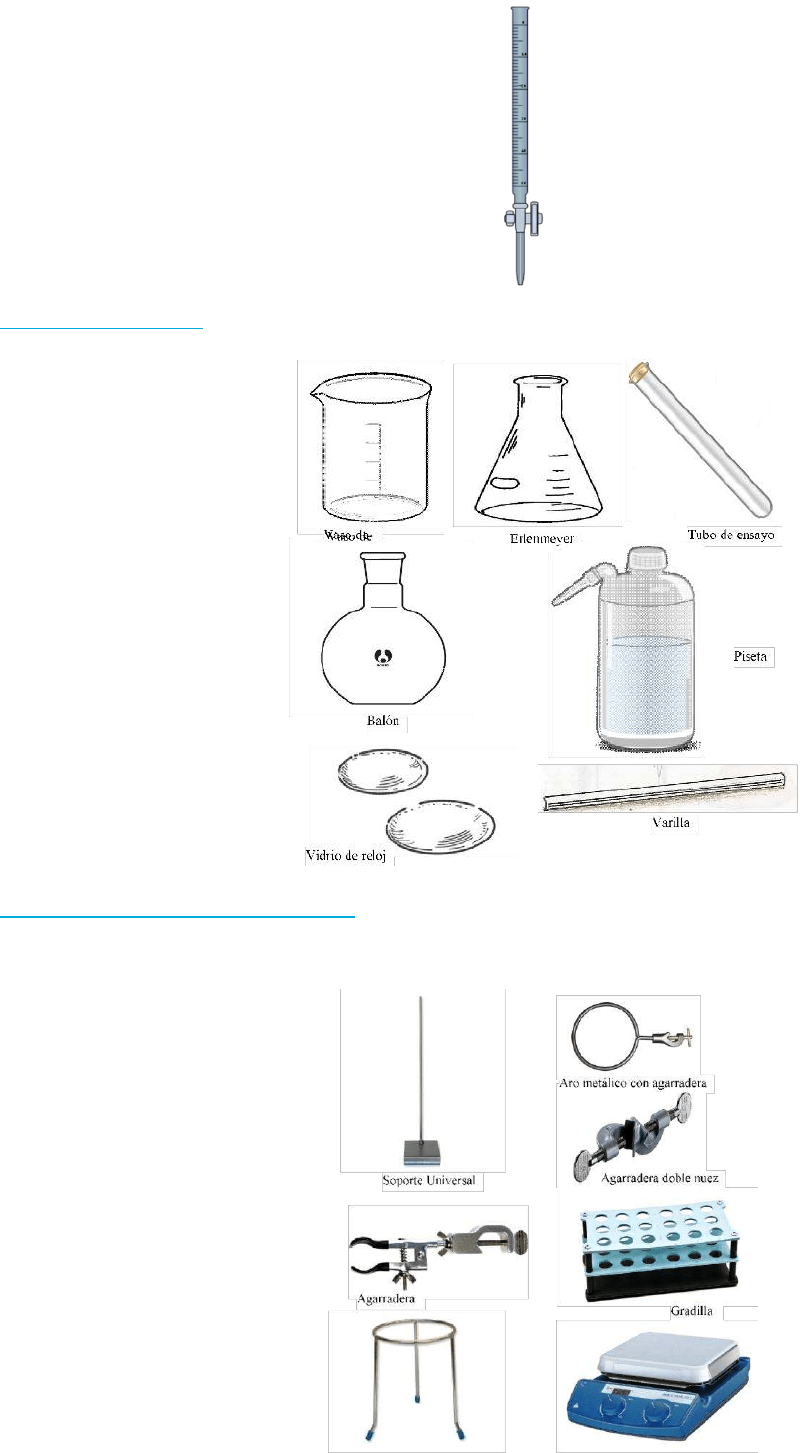
Buretas material graduado que permite eluir volúmenes exactos y variables de líquido. Generalmente utilizados
en técnicas de titulación o valoración (técnica analítica) de reactivos.
Laboratorio I
5
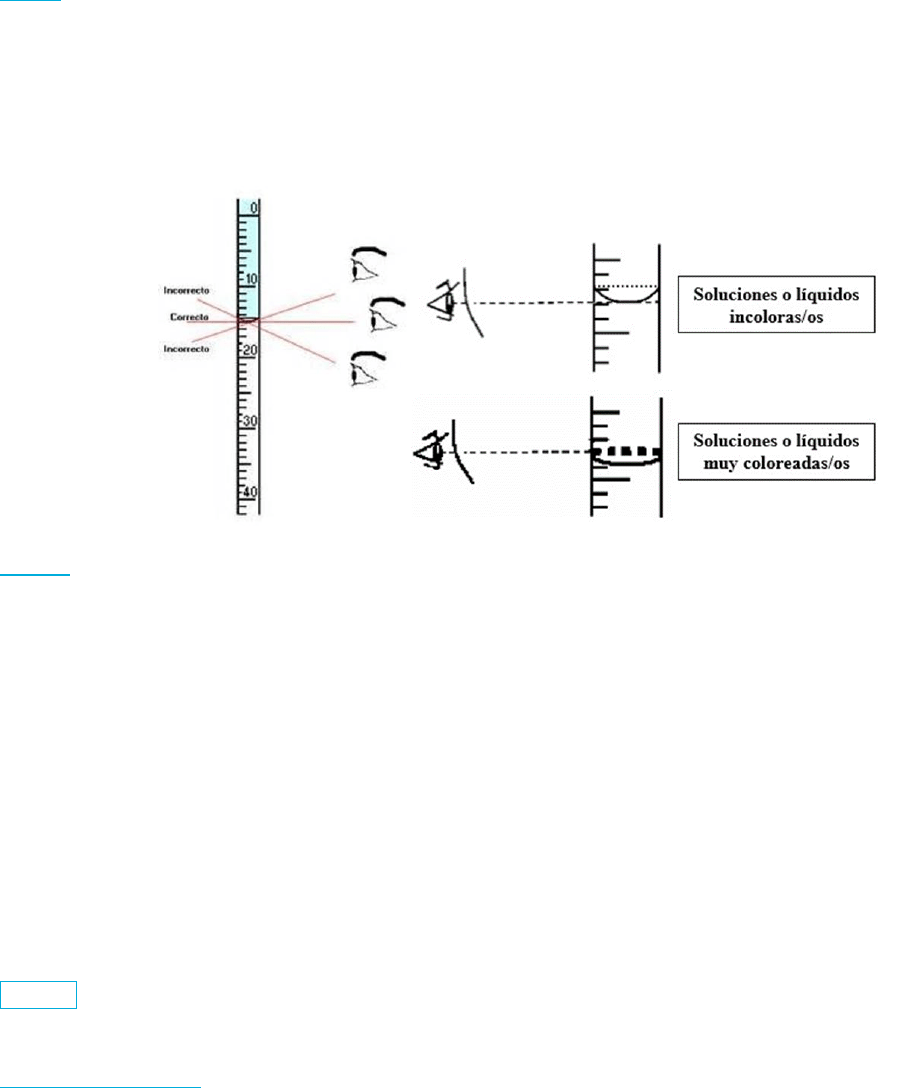
Material no calibrado: aquellos que sirven para contener o manipular sustancias químicas en cualquier estado físico
sin considerarse la cantidad exacta de material que contiene o permite manipular.
Materiales de sostén y calentamiento: elemento auxiliar para el uso de los elementos calibrados o no calibrados, y
permiten mantener los mismos de forma estable en la mesada y evitar roturas, o bien para el armado de sistemas
complejos para procesos de síntesis o análisis.
Laboratorio I
6
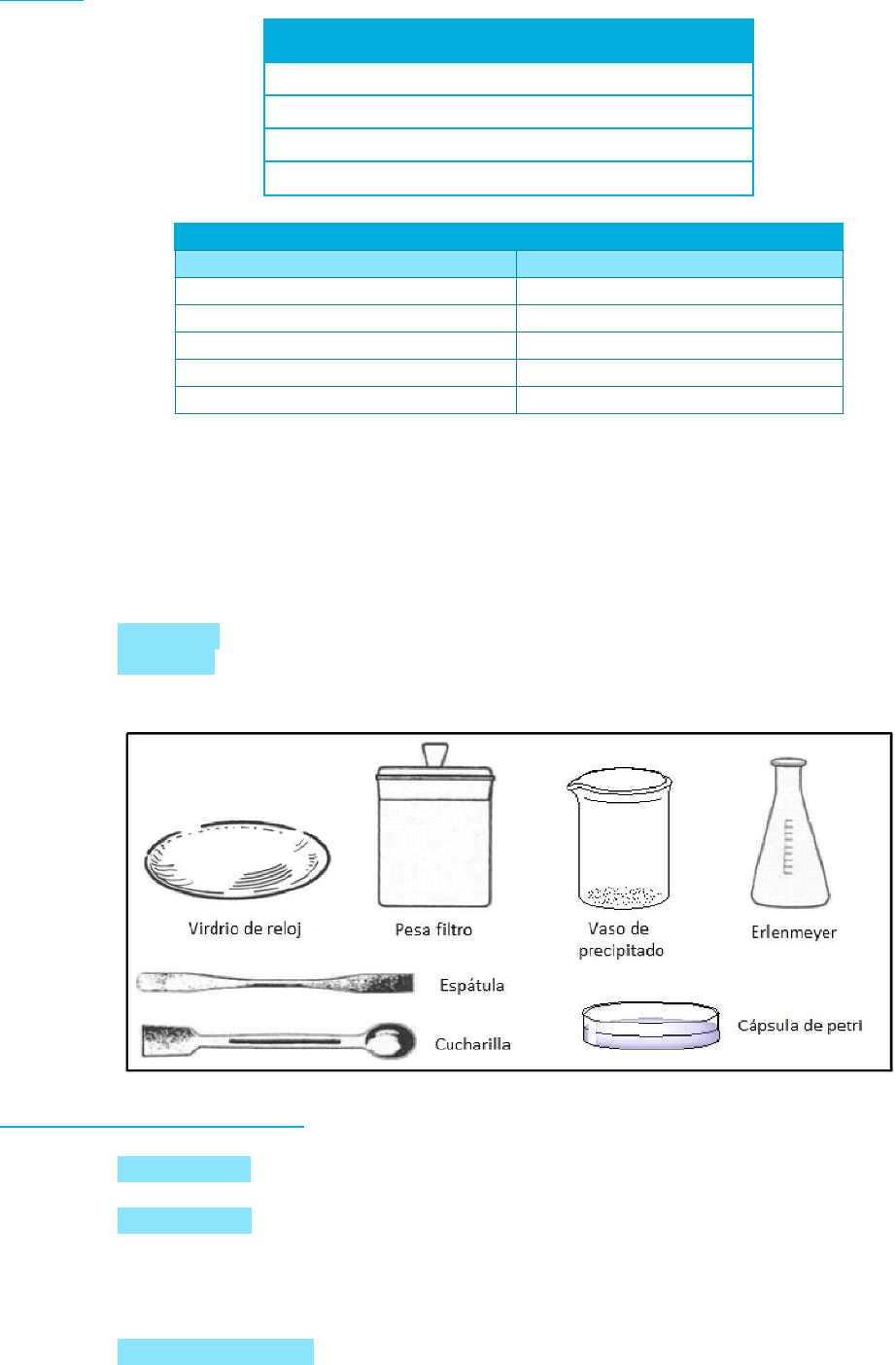
Enrase
Para medir el volumen correctamente es importante que se observe el líquido de forma paralela respecto de
los aforos.
La lectura debe realizarse justo en la tangente del menisco (en la parte inferior del menisco). Si la solución es lo
suficientemente coloreada como para no poder identificar correctamente el aforo o graduación, se
recomienda realizar la lectura tomando como referencia los extremos del menisco, en contacto con las paredes
del recipiente.
Pipeteo
1. Trasvasar un volumen mayor al necesario a una probeta o vaso de precipitado y desde allí utilizar la pipeta.
Nunca debe introducirse la pipeta en el interior de botellas de reactivos o matraces conteniendo soluciones
preparadas para evitar la contaminación de las sustancias químicas de partida en un experimento.
2. Es preferible realizar antes de la medida un enjuague de la pipeta con el líquido a medir y trasvasar para eliminar
cualquier rastro de contaminación que se encuentre en el interior de la misma. Para ello se succiona con una
propipeta (o pera, y nunca con la boca) un pequeño volumen de líquido introduciendo la punta de la pipeta por
debajo del nivel del líquido y se moja por entero las paredes interiores de la pipeta, desechando el líquido
utilizado para los enjuagues en un vaso de precipitado u otro recipiente de características similares.
3. Posteriormente al enjuague, se succiona la muestra introduciendo la pipeta bajo el nivel de líquido hasta superar
el aforo o la graduación para 0 mL emitidos. Utilizando la propipeta, se expulsa parte del líquido sobre el
recipiente para desechos hasta lograr un buen enrase.
4. Con la pipeta enrasada, se sitúa la misma sobre el recipiente donde se desea colocar el líquido y se expulsa el
líquido mediante la propipeta, de preferencia apoyando el extremo de la pipeta sobre las paredes del recipiente
y siempre por encima del nivel de líquido.
Alícuota es una parte que se toma de un volumen o de una masa inicial, para ser usada en una prueba de
laboratorio.
Trasvase cuantitativo: significa pasar una determinada cantidad de sustancia de un recipiente a otro.
1. Una vez realizada una pesada exacta de un sólido, se procede a trasvasarlo a un matraz aforado (volumétrico)
para preparar una disolución de concentración exacta de la muestra.
2. Se coloca un embudo de vástago ancho en el cuello del matraz.
3. Se procede a trasvasar poco a poco el sólido, con el auxilio de una varilla de vidrio.
4. Lavar el interior del recipiente en el que fue pesado el sólido con pequeñas porciones del disolvente en el que
será disuelto, con ayuda de un frasco lavado si el disolvente es agua, lavando finalmente el embudo y la varilla
de vidrio de manera que cualquier partícula sólida sea arrastrada por éste hacia el volumétrico.
5. Si la pesada se realizó en un papel especial para pesar, se deja caer cuidadosamente el sólido hacia el embudo, y
se procede a lavar éste hasta arrastrar todo el sólido contenido en él o adherido a sus paredes interiores.
6. Si se utilizó un vidrio de reloj, debe asegurarse que el embudo tenga un diámetro en su borde superior que
permita el trasvase del sólido sin que se produzcan derrames.
Laboratorio I
7
Balanzas: aparatos destinados a medir las masas de los cuerpos.
Clase de Balanzas
Máxima pesada
Apreciación
Granataria
2,0 kg
0,1 g
Analítica
100 a 200 mg
1 a 0,1 mg
Semi-micro
100 g
0,01 mg
Micro
30 g
0,001 mg
Diferencias
Analítica
Granataria
Más precisa
Menos precisa
Más delicada
Menos delicada
Margen de error menor
Margen de error mayor
Permite determinar masas pequeñas
Permite determinar masas grandes
Requiere mayor mantenimiento
Requiere menor mantenimiento
Precauciones en la pesada:
Tipo de sustancia que se quiere pesar (solidos o líquidos).
Si es volátil (tendencia a pasar a la fase gaseosa) o higroscópica (tendencia a absorber la humedad).
Cuidados que se le debe dar a cada tipo de balanza.
Material utilizado para pesar
Una sustancia a pesar no debe colocarse directamente sobre el platillo, debe colocarse un recipiente sobre el
platillo limpio y en él colocar la sustancia a pesar
Vidrio reloj: es útil para pesar pequeñas cantidades de sustancia que no absorban humedad.
Pesafiltros: al disponer de una tapa permite pesar sustancias higroscópicas, es útil sobre todo cuando
se trabaja con una balanza capaz de apreciar cantidades muy pequeñas.
También se utilizan vasos de precipitados, erlenmeyers, placas de Petri, cápsulas de porcelana, etc.
Métodos para pesar una sustancia
Pesada de sólidos
× Pesada simple: Consiste en determinar el peso de un objeto al sólo colocarlo sobre el platillo de la
balanza.
× Pesada directa: es apropiado cuando la muestra no se altera al exponerse al aire y se quiere tener un
peso exacto de acuerdo al predeterminado. En este método se obtiene primero el peso del recipiente
vacío y seco al cual se va a transferir la sustancia y luego se agrega ésta poco a poco hasta obtener el
peso requerido. La cantidad de sustancia en exceso que se retira, no se devuelve al frasco sino que se
desecha para evitar la contaminación.
× Pesada por diferencia: caracterizado por su rapidez, se utiliza en general para pequeñas muestras que
no necesitan tener un peso predeterminado, pero sí interesa conocer con exactitud la cantidad pesada.

Laboratorio I
8
Evita que éstas estén expuestas a la atmósfera por espacio de varios minutos, pues, por ejemplo,
puede que la sustancia sea higroscópica o volátiles.
Pesada de líquidos:
× No es conveniente pesar líquidos, especialmente, si éstos son corrosivos y/o volátiles. En caso de ser
indispensable pesar un líquido, lo mejor es evitar el uso de recipientes abiertos.
× El método más conveniente consiste en pesar el recipiente vacío con su correspondiente tapón;
introducir luego la muestra líquida a pesar mediante pipeta o tubo de vidrio; finalmente pesar el
recipiente con su contenido. Por diferencia, se determina el peso de la muestra líquida.
Estequiometria
Ecuación química: representación simbólica de una reacción química en términos de las fórmulas químicas, que
consta de dos miembros (reactivos y productos) separados por una flecha que indica el sentido de la reacción.
Reacción química: cuándo se produce un reordenamiento en las combinaciones químicas de los átomos.
Reacciones de precipitación los reactivos solubilizados en la solución generan uno o más productos insolubles
(precipitado) que se separan del medio.
Reacciones de neutralización ácido-base un ácido (compuesto que produce H+) reacciona con una base
(compuesto que genera OH-) para obtener agua más un compuesto iónico llamado sal.
Reacciones de óxido-reducción o rédox se produce la transferencia de electrones de una sustancia a otra, por lo
cual el estado de oxidación inicial de los átomos de reactivos cambia al generarse los productos.
> Esta clasificación incluye los siguientes tipos de reacciones:
Reacciones de combinación dos o más sustancias reaccionan para formar un solo producto.
Reacciones de descomposición un solo reactivo se descompone para formar dos o más sustancias.
Reacciones de desplazamiento un elemento reacciona con un compuesto y desplaza a otro elemento del mismo.
Reacciones de desplazamiento doble o metátesis los reactivos intercambian átomos o iones.
Reacciones de desproporción un mismo elemento en un estado de oxidación, se oxida y se reduce al mismo
tiempo.
Reacciones de combustión generalmente producen una flama y uno de los reactivos es, siempre, oxígeno (a
menudo O2 del aire).
Reactivo limitante: sustancia que se consume completamente en una reacción, es el que determina o limita la
cantidad de producto que se forma.
Rendimiento teórico: cantidad de producto que se calcula que se formará cuando todo el reactivo limitante ha
reaccionado.
Rendimiento real: cantidad de producto que realmente se obtiene en una reacción. El rendimiento real nunca es
mayor que el rendimiento teórico.

Laboratorio I
9
Pureza: porcentaje efectivo de reactivo puro en la masa total.
Error
Números exactos: aquellos cuyos valores se conocen con exactitud.
Números inexactos: aquellos cuyos valores tienen cierta incertidumbre, los números que se obtienen por
mediciones siempre son inexactos.
Forma correcta de escribir una magnitud medida (Magnitud (expresada con el número correcto de cifras) ±
incerteza) seguido de la unidad.
Errores indeterminados, accidentales o al azar: son causados por muchas variables incontrolables las cuales son
parte inevitable de todas las mediciones.
Errores sistemáticos: tienen origen definido, que puede o no ser identificado. Ellos hacen que los resultados de
mediciones repetidas sean todos altos o todos bajos.
Mediciones directas e indirectas: cuando una cantidad x se determina a través de una fórmula en la cual intervienen
otras cantidades a, b, c, etc., cada una de las cuales se mide directamente con algún instrumento, se dice que a, b, c,
etc. son resultado de mediciones directas, mientras que x=f (a, b, c, etc.) es resultado de una medición indirecta.
Propagación de errores: cuando se mide una magnitud L que es función de otras magnitudes medidas x, y, z, las
incertezas en estas mediciones (∆x, ∆y, ∆z) se propagarán al valor de la magnitud L. Es decir que L será calculada en
forma indirecta, por lo tanto se debe encontrar una expresión para su error.
Suma
Resta
Producto
Cociente
Potenciación
Radicación
Exactitud y precisión
Exactitud: indica lo próximo que está una cantidad medida experimentalmente a su valor verdadero.
Precisión: grado de coincidencia entre dos o más medidas de una misma magnitud.
Desviación estándar: La desviación estándar s da idea de la precisión de un conjunto de valores de una magnitud.
La precisión alta, de nada sirve sin exactitud y viceversa. Es necesario o al menos deseable tener un poco de ambas.
En el laboratorio suelen hacerse varios “ensayos” del mismo emprendimiento y se promedian los resultados. La
precisión de las mediciones frecuentemente se expresa en términos de lo que se denomina desviación estándar (s),
la que refleja que tanto difieren las mediciones individuales del promedio. N es el número de mediciones, es el
promedio y
representa las mediciones individuales

Laboratorio I
10
Error de una magnitud: indica la exactitud.
No se puede hablar de incerteza si no sé con qué instrumento se midió o si no está informado el error de la medida.
Peso, masa y fuerza
Movimientos periódicos: ocurre cuando la fuerza sobre un cuerpo es proporcional al desplazamiento del cuerpo a
partir el equilibrio. Si esta fuerza siempre actúa hacia la posición de equilibrio del cuerpo, hay un movimiento
repetitivo, hacia adelante y hacia atrás alrededor de esta posición.
Se dice que un cuerpo realiza un movimiento oscilatorio o periódico cuando se repite a intervalos regulares.
Elongación Es la distancia en un instante dado entre el cuerpo y su posición de equilibrio.
Amplitud (A) Es el máximo valor de la elongación, o sea el apartamiento máximo de la partícula de la posición
media.
Período (T) Es el tiempo que tarda la partícula en completar un ciclo, es decir es el tiempo que demora la partícula
desde cualquier punto, hasta que vuelve a pasar por el mismo punto en el mismo sentido.
Oscilador armónico simple
La constante k se denomina constante de fuerza o constante elástica del resorte, sus dimensiones son N/m y
representa la fuerza necesaria para estirar un resorte una dada extensión.
Frecuencia angular (cuán rápido oscila el resorte)
Péndulo simple: consta de un cuerpo suspendido de una cuerda ligera e inextensible. Cuando se empuja a un lado
de su posición de equilibrio y se suelta, el péndulo oscila bajo la influencia de la gravedad. El movimiento es
periódico y oscilatorio.
Ley de elasticidad de Hooke:
Unidades:
g (aceleración de la gravedad): m.s
-2
m (masa): kg
P (peso): N = Kg.m.s
-2
k (constante elástica): N.m
-1
Separación de mezclas
Características de las mezclas y de los compuestos puros
Mezclas
Compuestos puros
Pueden separarse en sus componentes mediante
cambios físicos.
No pueden separarse en sus componentes por cambios
físicos
Sus composición puede variarse de manera continua
al agregar uno de sus componentes
Su composición es constante la mayor parte de las veces
Sus propiedades están ciertamente relacionadas con
las de sus componentes
Sus propiedades no están relacionadas con las de los
elementos que los constituyen químicamente.
Laboratorio I
11
Materia ¿es uniforme en todas sus partes? NO Mezcla Heterogénea
SI Mezccal Homogénea ¿tiene composicion variable? SI Mezcla Homogénea
(disolución)
NO Sustancia pura
Elemento NO ¿Se puede descomponer en SI Compuesto
sustancias mas simples?
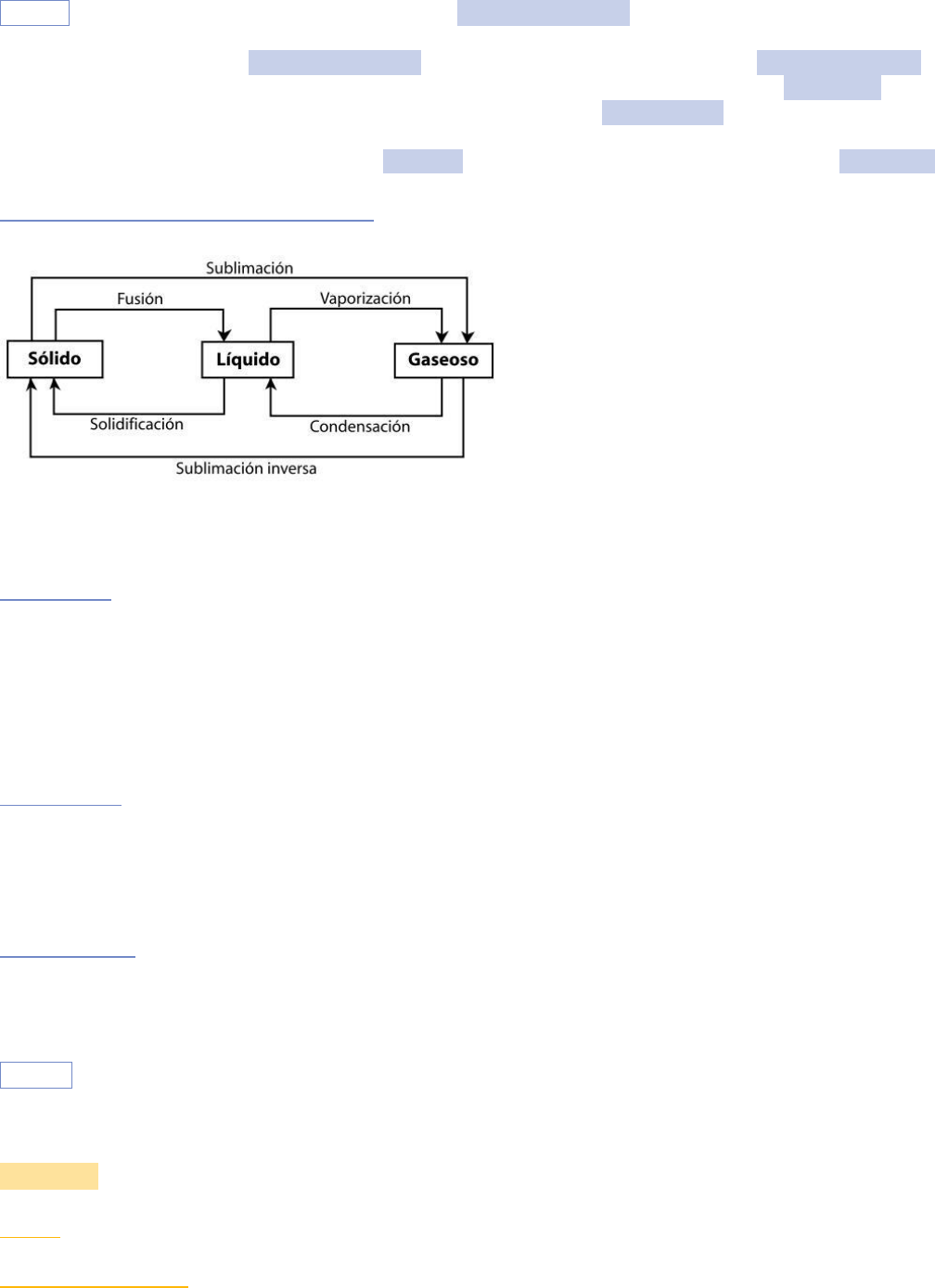
Estados de agregación y cambios de estados
Procesos endotérmicos (absorben calor): fusión, evaporación y sublimación.
Procesos exotérmicos (liberan calor): congelamiento, condensación y deposición (sublimación inversa).
Sólido-Sólido
¿Un componente tiene propiedades magnéticas y el otro no? Magnetismo
¿Las partículas a separar tienen diferente tamaño de grano? Decantación y Tamización
¿Son solubles ambos en agua? Cristalización fraccionada y Cromatografía
¿Es uno soluble en agua y el otro no? Disolución, Extracción, Filtración y Evaporación
¿Son ambos insolubles en agua? Cristalización, Cromatografía en disolvente distinto
¿Es uno sublimable y el otro no? Sublimación
Sólido-Líquido
¿Es el sólido insoluble en líquido? Decantación/ precipitación, centrifugación, filtración (por gravedad/ a
presión reducida)
¿Se quiere aislar el líquido? SI. Destilación
NO.
Evaporación, Recristalización
Líquido- Líquido
¿Son inmiscibles? Extracción, Decantación
¿Son miscibles? Destilación S (∆T < 100
o
C), Destilación F (∆T > 100
o
C), Destilación PR (descomposición a la T de
ebullición)
Coloides sistema conformado por dos o más fases, normalmente una fluida y otra dispersa en forma de partículas
generalmente sólidas muy finas, de diámetro comprendido entre 10⁻⁹ y 10⁻⁵ m. Separación de mezclas, fuerza de
gravedad o centrifuga.
Soluciones
Soluto: sustancia que se disuelve, dispersa o solubiliza y siempre se encuentra en menor proporción, ya sea en peso
o en volumen.
Solvente o disolvente: sustancia que disuelve o dispersa el soluto y generalmente se encuentra en mayor
proporción.
Distintos grados de
interacción molecular

Laboratorio I
12
Solubilidad: máxima cantidad de un soluto que puede disolverse a una determinada cantidad de solvente a una
temperatura dada. La solubilidad depende de la temperatura, presión y naturaliza del soluto y solvente.
Interacciones solvente-solvente se requiere energía para superar las fuerzas intermoleculares. ∆H es positivo.
Interacciones soluto-soluto se requiere energía para superar las fuerzas intermoleculares en el cristal. ∆H es
positivo.
Interacciones soluto-solvente se libera energía cuando las moléculas de solvente solvatan al soluto. ∆H es
negativo.
“similar disuelve similar”
o Sustancias polares o iónicas se disuelven en solventes polares
o Sustancias apolares se disuelven en solventes apolares
Ley de Henry: una temperatura constante, la cantidad de gas disuelto en un líquido es directamente proporcional a
la presión parcial que ejerce ese gas sobre el líquido.
C = solubilidad; p = presión
Clasificación de las soluciones:
Solución diluida/ insaturada: la masa del soluto disuelto con respecto a la de la solución saturada es más
pequeña para la misma temperatura y solvente.
Solución concentrada: la cantidad de soluto disuelto es próximo a la determinada por la solubilidad a la misma
temperatura.
Solución saturada: contiene la máxima cantidad de soluto que puede mantenerse disuelto en una determinada
cantidad de solvente a una temperatura establecida.
Solución sobresaturada: contiene mayor cantidad de soluto que una solución saturada a temperatura
determinada. Esta propiedad la convierte en inestable.
Concentración: cantidad de soluto que hay en una determinada cantidad de solvente o solución.
%P/P: gramos de soluto en 100 g de solución:
%P/V: gramos de soluto en 100 mL de solución:
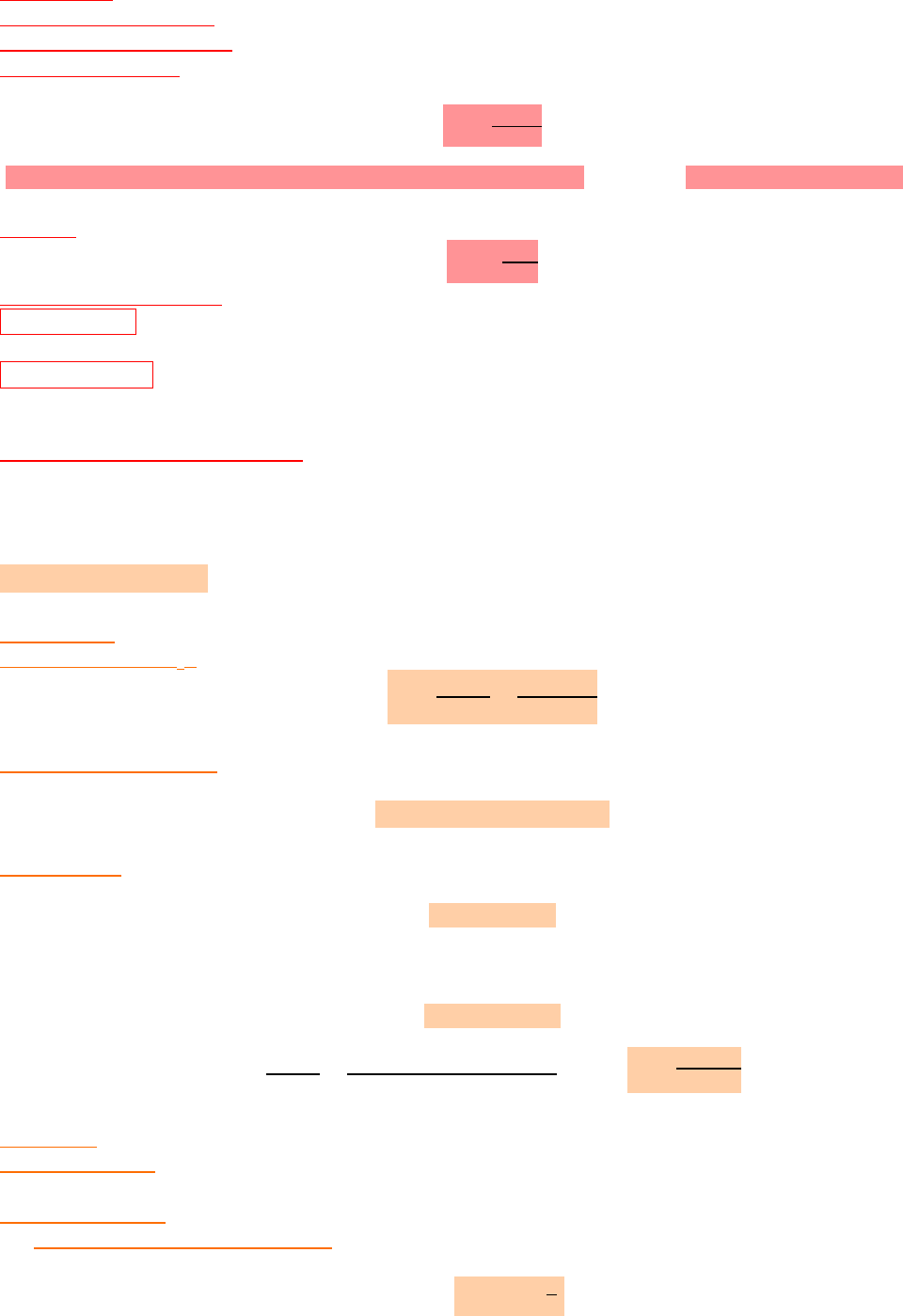
Molaridad (M): número de moles de soluto en 1 L de solución:
Molalidad (m): moles de soluto contenido en 1 Kg de solvente:
Fracción Molar (X): cociente entre el número de moles de un soluto/ solvente en relación con el número de moles
totales de la solución:
Termoquímica y Calorimetría
Sistema Termodinámico: según permeabilidad de las paredes que separan el sistema de los alrededores.
Abierto: intercambio de materia y energía con el ambiente.
Cerrado: intercambio de energía con el ambiente.
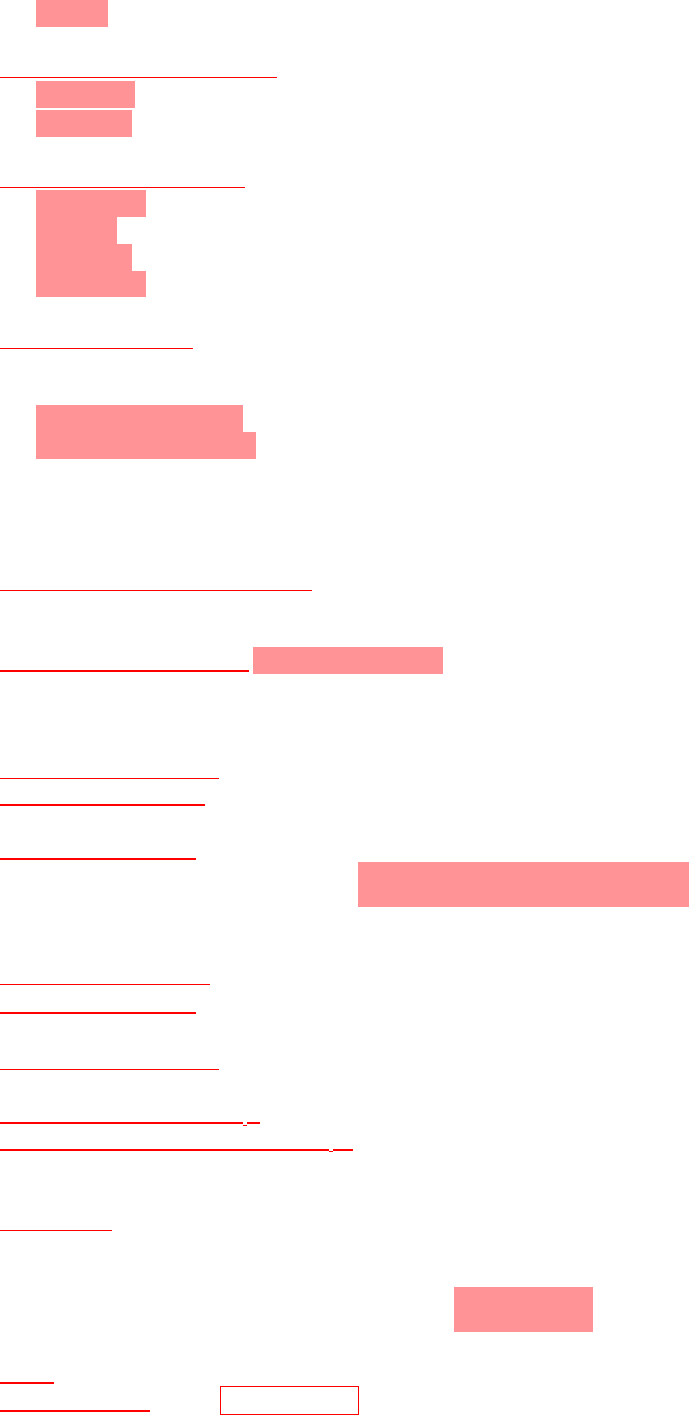
Laboratorio I
13
Aislado: no hay intercambio de materia y energía con el ambiente.
Propiedades Termodinámicas:
Extensivas: depende de la cantidad de materia.
Intensivas: no dependen de la cantidad de materia.
Procesos Termodinámicos:
Isotérmicos: temperatura constante.
Isocoros: volumen constante.
Isobáricos: presión constante.
Adiabáticos: calor constante.
Funciones de Estado: propiedad/ variable del sistema en equilibrio que define el estado del sistema.
Tienen un valor único para cada estado del sistema.
Sus variaciones solo dependen del estado inicial y final.
SI funciones de estado: presión, temperatura, energía interna, entalpia.
NO funciones de estado: calor (q), trabajo (w).
q y w > 0, entra energía en el sistema.
q y w < 0, sale energía del sistema.
Primera Ley de la Termodinámica: la energía se conserva, cualquier energía que un sistema pierda deberá ser
ganada por el entorno y viceversa.
Cambio de energía interna:
positivo; el sistema ganó E de su entorno.
negativo; el sistema perdió E a su entorno.
Procesos endotérmicos: sistema absorbe calor.
Procesos exotérmicos: sistema libera calor.
Entalpia de Reacción:
Si p = cte, el calor intercambiado con el entorno, llamado calor de reacción, es igual a la entalpia de la reacción.
Reacción endotérmica:
Reacción exotérmica:
Entalpia estándar (∆H°): incremento entálpico de una reacción en la cual, tanto reactivo como productos están en
condiciones estándar (p = 1atm; T = 298 K).
Entalpia de Formación (∆H
f
): se calcula a través de sus elementos constituyentes.
Entalpia estándar de Formación (∆H
f
°): cambio de entalpia de la reacción que forma 1 mol de ese compuesto a
partir de sus elementos en estado estándar.
Ley de Hess: una serie de reactivos reaccionan para dar una serie de productos, el calor de reacción liberado o
absorbido es independiente de si la reacción se lleva a cabo en una, dos o más etapas, es decir, que los cambios de
entalpía son aditivos:
Calor:
transferencia de energía entre la materia como resultado de las diferencias en la temperatura.
Unidad de calor: caloría (1 cal = 4,184 J)
Laboratorio I
14
Calorimetría: medición de flujos de calor.
Capacidad calorífica (Cc): energía necesaria para aumentar la temperatura de una sustancia.
Capacidad calorífica molar: capacidad calorífica en mol de sustancia.
Calor específico (Ce): cantidad de calor por gramos de sustancia que necesita un cuerpo para que su temperatura se
eleve.
Entalpia:
Principios de Calorimetria
Primer principio la cantidad de calor necesario para elevar la temperatura de un cuerpo es proporcional a su
masa.
Segundo principio la cantidad de calor necesario para elevar la temperatura de un cuerpo desde un valor A hasta
un valor B es igual a la cantidad de calor que el cuerpo cede cuando su temperatura desciende de B a A.
Ley fundamental de la Calorimetría
Un sistema aislado compuesto por n cuerpos, a diferentes temperaturas, evoluciona espontáneamente hacia un
estado de equilibrio en el que todos los cuerpos tienen la misma temperatura. Los calores intercambiados sumados
con sus signos dan cero.
Densidad y Viscosidad
Densidad (δ): cantidad de masa (m) en un determinado volumen (V). (g/cm
3
| Kg/m
3
)
Densidad Relativa (δ
R
): relación entre la densidad y la densidad de un patrón:
Principio de Arquímedes: todo cuerpo sumergido en el seno de un fluido recibe un empuje (E) de abajo hacia arriba
igual al peso del líquido (P
liq
) desalojado:
Ley de Hooke: los cuerpos elásticos tienen la propiedad de ejercer una fuerza de oposición a una fuerza externa que
tiende a deformarlos:
k = constante de restitución del resorte; (x
l
– x
0
) = deformación del resorte
Si la densidad del solido es mayor que la densidad del líquido de referencia, al introducirlo en el seno del mismo se
hundirá totalmente:
Viscosidad: propiedad de los fluidos que expresa el grado de dificultad para fluir
Fuerza viscosa (F): fuerza tangencial que se opone al movimiento
Tipos de viscosidad
o Viscosidad absoluta/ dinámica (): medida de resistencia a la fluencia de un fluido. Cuanto mayor sea la
viscosidad, más denso será el fluido; cuanto menor sea la viscosidad, más fluido será. (Kg/m.s = Pa.J)
a y b = constantes que dependen del líquido. Temperatura debe expresarse en K.
Laboratorio I
15
o Viscosidad cinemática (): relación entre la viscosidad absoluta y la densidad de masa del fluido (m
2
/s):
Dinámica de fluidos:
Viscosímetro de Ostwald viscosidad cinemática
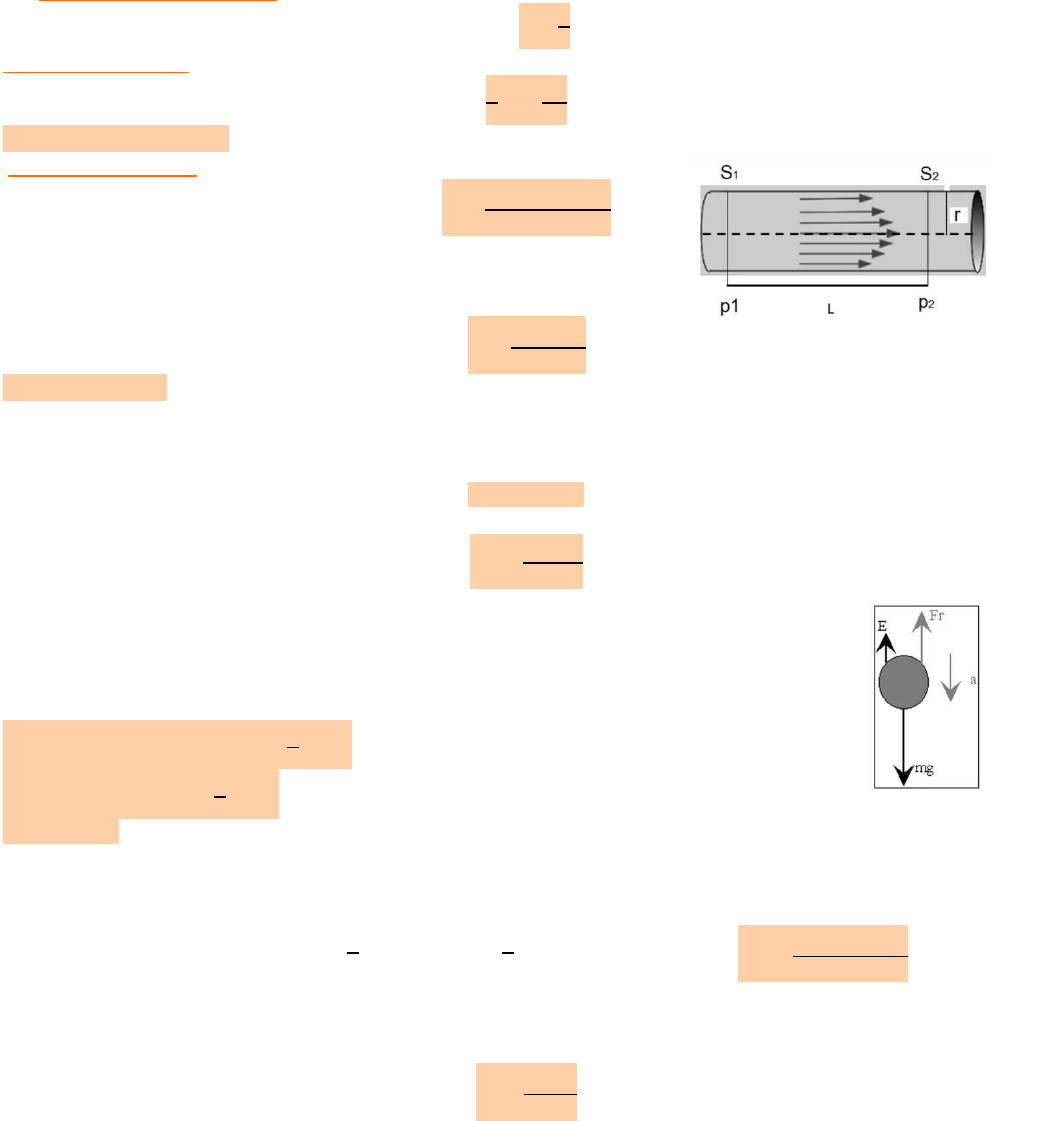
Caudal de Poiseuille:
R = radio; p
1
y p
2
= presión de entrada y salida (p
1
> p
2
); S = secciones (se
considera que S
1
= S
2
; L = longitud; η = viscosidad del fluido
Derivada de un viscosímetro vertical:
Método de Stokes viscosidad dinámica
Se demuestra que para Re (número de Reynolds) pequeños (velocidad muy pequeña y viscosidad muy alta), la fuerza
de rozamiento (F
r
) sobre un cuerpo esférico de radio r, que se mueve con una velocidad v, en un fluido de viscosidad
η está dada por:
Ecuación valida siempre que Re sea menos que 1, para una esfera:
Cuando las tres fuerzas se igual entre sí, se anulan. El impulso de la esfera es cero y la esfera se mueve a velocidad
constante. Se alcanza la velocidad terminal (v
T
).
El tiempo en que se alcanza la velocidad constante, v
T
, es muy pequeño por lo que puede considerarse que todo el
trayecto la esfera se mueve a v constante.

Resumen Lab I.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.