
StuDocu is not sponsored or endorsed by any college or university
Resumen Fisiología renal y equilibrio ácido
Fisiología (Universidad Nacional del Litoral)
StuDocu is not sponsored or endorsed by any college or university
Resumen Fisiología renal y equilibrio ácido
Fisiología (Universidad Nacional del Litoral)
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
Fisiología renal y equilibrio ácido-base.
(Linda S. Constanzo).
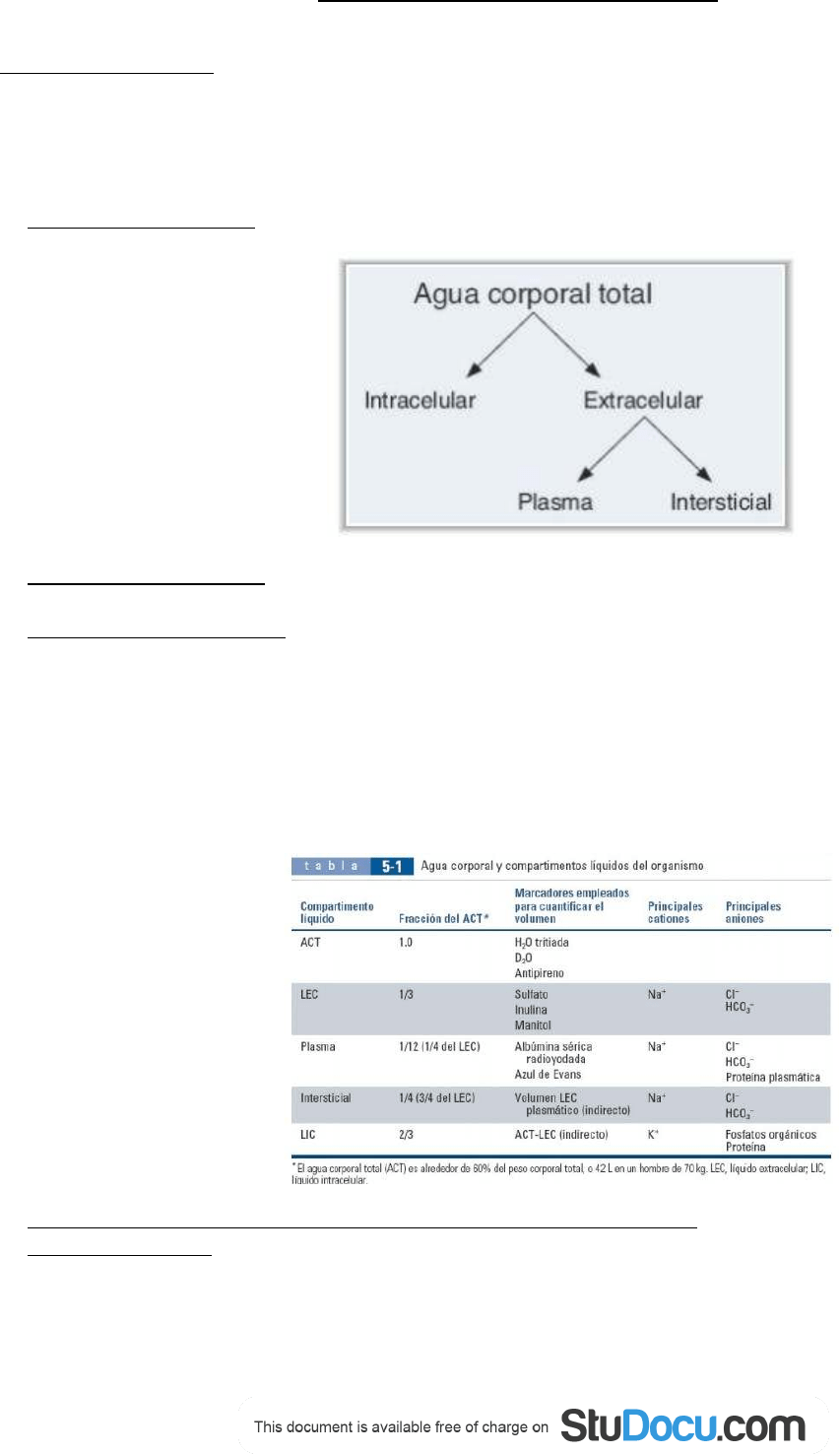
Líquidos corporales.
- El agua corporal total (ACT) representa alrededor de 60% del peso corporal.
- El agua corporal es inversamente proporcional a la grasa corporal.
- El porcentaje de ACT es mayor en neonatos y hombres adultos y menor en mujeres adultas y en adultos con
gran cantidad de tejido adiposo.
A. Distribución del agua:
1. Líquido intracelular (LIC) : es 2/3 del ACT. Los principales cationes del LIC son K+ y Mg 2+. Los principales
aniones del LIC son proteínas y fosfatos orgánicos (ATP, ADP, AMP).
2. Líquido extracelular (LEC): es 1/3 del ACT. Está constituido por el líquido intersticial y el plasma. El principal
catión del LEC es el Na
+
. Los principales aniones del LEC son Cl – y HCO3
−
. El plasma representa 1/4 parte del
LEC. Por lo tanto, es un doceavo del ACT (1/4 × 1/3). Las principales proteínas plasmáticas son albúmina y
globulinas. En cambio, el líquido intersticial representa las 3/4 partes del LEC. Por lo tanto, es una cuarta parte
del ACT (3/4 × 1/3). La composición del líquido intersticial es la misma que la del plasma, excepto que contiene
pocas proteínas. Por lo tanto, el líquido intersticial es un ultrafiltrado del plasma.
3. Entonces, el ACT es 60% del peso corporal, el LIC es 40% del peso corporal, y el LEC es 20% del peso
corporal.
B. Cuantificación de los volúmenes de los compartimentos líquidos :
1. Método de dilución : se administra una cantidad conocida de una sustancia cuyo volumen de distribución es el
compartimento líquido de interés. Se permite que la sustancia se equilibre. Se mide la concentración de la
sustancia en el plasma y se calcula el volumen de distribución como sigue:
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

2. Sustancias empleadas para los principales compartimentos líquidos : ACT (agua tritiada, D2O, y antipireno),
LEC (sulfato, inulina y manitol), plasma (albúmina sérica radioyodada y azul de Evans), intersticial [(se cuantifica
indirectamente (volumen LEC-volumen plasmático)], y en el LIC [(se cuantifica indirectamente (volumen ACT-
LEC)].
C. Desplazamientos de agua entre compartimentos:
1. Principios básicos:
La osmolaridad es la concentración de partículas de soluto.
La osmolaridad plasmática (P
osm
) se estima como sigue:
En el estado estable, la osmolaridad del LEC y la osmolaridad del LIC son iguales.
Para conseguir esta igualdad, el agua se desplaza entre los compartimentos de LEC y LIC.
Se supone que solutos como NaCl y manitol no cruzan las membranas celulares y están confinados al
LEC.
2. Ejemplos de desplazamientos de agua entre compartimentos:
A. Infusión de NaCl isotónico: adición de líquido
isotónico. También se denomina expansión de
volumen isoosmótica. El volumen de LEC
aumenta, pero no cambia la osmolaridad del LEC o
el LIC. Puesto que la osmolaridad no varía, no se
desplaza agua entre los compartimentos de LEC
y LIC. La concentración plasmática de
proteína y el hematocrito disminuyen porque la
adición de líquido al LEC diluye las proteínas y los
eritrocitos. Puesto que la osmolaridad del LEC no
varía, los eritrocitos no se arrugarán ni se
inflamarán. La presión arterial aumenta porque el
volumen del LEC aumenta.
B. Diarrea : pérdida de líquido isotónica. También se
denomina contracción de volumen isoosmótica. El volumen de LEC disminuye, pero no cambia la osmolaridad del
LEC o el LIC. Puesto que la osmolaridad no varía, no se desplaza agua entre los compartimentos de LEC y LIC.
La concentración plasmática de proteína y el hematocrito aumentan porque la pérdida de LEC concentra las
proteínas y los eritrocitos. Puesto que la osmolaridad del LEC no varía, los eritrocitos no se arrugarán ni se
hincharán. La presión arterial disminuye porque el volumen de LEC disminuye.
C. Ingesta excesiva de NaCl : adición de NaCl. También se denomina expansión de volumen hiperosmótica. La
osmolaridad del LEC aumenta porque se han añadido osmoles (NaCl) al LEC. Se desplaza agua del LIC al LEC.
Como consecuencia de este desplazamiento, la osmolaridad del LIC aumenta hasta igualar la del LEC. Como
resultado de la salida de agua de las células, el volumen del LEC aumenta (expansión de volumen) y el volumen
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

del LIC disminuye. La concentración plasmática de proteína y el hematocrito disminuyen debido al aumento del
volumen del LEC.
D. Sudoración en el desierto : pérdida de agua. También se denomina contracción de volumen hiperosmótica. La
osmolaridad del LEC aumenta porque la sudación es hipoosmótica (se elimina relativamente más agua que sal).
El volumen del LEC disminuye debido a la pérdida de volumen en la sudoración. Sale agua del LIC; como
resultado, la osmolaridad del LIC aumenta hasta igualar la osmolaridad del LEC, y el volumen del LIC disminuye.
La concentración plasmática de proteína aumenta debido a la disminución del volumen del LEC. Aunque cabría
esperar que el hematocrito aumentara, se mantiene invariable porque los eritrocitos pierden agua, lo que reduce
su volumen y compensa el efecto concentrador de la disminución del volumen del LEC.
E. Síndrome de secreción inadecuada de vasopresina (SIADH): aumento de agua. También se denomina
expansión de volumen hipoosmótica. La osmolaridad del LEC disminuye porque se retiene un exceso de agua. El
volumen de LEC aumenta debido a la retención de agua. El agua entra en las células; como consecuencia de
esto, la osmolaridad del LIC disminuye hasta igualar la osmolaridad del LEC, y el volumen del LIC aumenta. La
concentración plasmática de proteína disminuye debido al aumento de volumen del LEC. Aunque cabría esperar
que el hematocrito disminuyera, se mantiene invariable porque entra agua en los eritrocitos, lo que aumenta su
volumen y compensa el efecto diluyente del aumento de volumen del LEC.
F. Insuficiencia corticosuprarrenal : pérdida de NaCl. También se denomina contracción de volumen hipoosmótica.
La osmolaridad del LEC disminuye. Como resultado de la ausencia de aldosterona en la insuficiencia
corticosuprarrenal, se reduce la reabsorción de NaCl, y los riñones excretan más NaCl que agua. El volumen del
LEC disminuye. Entra agua en las células; como consecuencia, la osmolaridad del LIC disminuye hasta igualar la
osmolaridad del LEC, y el volumen del LIC aumenta. La concentración plasmática de proteína aumenta debido a
la disminución del volumen del LEC. El hematocrito aumenta debido a la disminución del volumen del LEC y
porque los eritrocitos se inflaman como consecuencia de la entrada de agua. La presión arterial disminuye debido
al descenso del volumen del LEC.
Depuración renal, flujo sanguíneo renal y tasa de filtración glomerular.
A. Ecuación de depuración:
Indica el volumen de plasma del cual se elimina una sustancia por unidad de tiempo.
Las unidades de depuración son mL/min y mL/24 h:
B. Flujo sanguíneo renal (FSR):
Es 25% del gasto cardiaco. Es directamente proporcional al
gradiente de presión entre la arteria renal y la vena renal e inversamente proporcional a la resistencia que opone
la vasculatura renal. La activación del sistema nervioso simpático y la angiotensina II causan vasoconstricción de
las arteriolas renales, que reduce el flujo sanguíneo renal (FSR). A concentraciones bajas, la angiotensina II
constriñe de preferencia las arteriolas eferentes, con lo que “protege” (aumenta) la tasa de filtración glomerular
(TFG). Los inhibidores de la enzima convertidora de angiotensina (IECA) dilatan las arteriolas eferentes y reducen
la TFG. Prostaglandinas E
2
e I
2
, bradicinina, óxido nítrico y dopamina provocan vasodilatación de las arteriolas
renales, que lleva a un aumento del FSR. El péptido natriurético auricular (PNA) causa vasodilatación de
arteriolas aferentes y, en menor medida, vasoconstricción de arteriolas eferentes; de manera global, el PNA
incrementa el FSR.
1. Autorregulación del FSR : se lleva a cabo mediante la modificación de la resistencia vascular renal. Si la
presión arterial varía, se produce un cambio proporcional de la resistencia vascular renal para mantener un
FSR constante. El FSR se mantiene constante en una gama de presiones arteriales entre 80 y 200 mm Hg
(autorregulación). Los mecanismos de la autorregulación comprenden: el mecanismo miógeno, en el que las
arteriolas aferentes renales se contraen en respuesta al estiramiento; y, la autorregulación tubuloglomerular, en
la cual la mayor presión arterial renal causa un aumento del suministro de líquido a la mácula densa.
2. Determinación del flujo plasmático renal: depuración de ácido paraaminohipúrico (PAH ): los túbulos renales
filtran y segregan PAH. La depuración de PAH se utiliza para determinar el flujo plasmático renal (FPR). La
C=
UV
P
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

depuración de PAH mide el FPR efectivo y subestima el FPR real en un 10%. (La depuración de PAH no
determina el flujo plasmático renal de las regiones del riñón que no filtran ni segregan PAH, como el tejido
adiposo).
3. Determinación del FSR: el denominador de esta ecuación, 1 – hematocrito, es la fracción de la volemia
ocupada por el plasma.
C. Tasa de filtración glomerular (TFG):
1. Determinación de la tasa de filtración glomerular (TFG): depuración de inulina. Los túbulos renales filtran
inulina, pero no la reabsorben ni la segregan. La depuración de inulina se utiliza para determinar la TFG,
como se pone de manifiesto en la siguiente ecuación:
2. Estimación de TFG con el nitrógeno de urea sanguínea (BUN) y la [creatinina] sérica : tanto el BUN como la
[creatinina] sérica aumentan cuando la TFG disminuye. En la uremia prerrenal (hipovolemia), el BUN aumenta
más que la creatinina sérica (ya que la hipovolemia aumenta la reabsorción de urea en el túbulo proximal), y
se incrementa la relación BUN/creatinina (> 20 a 1). La TFG disminuye con la edad, aunque la [creatinina]
sérica se mantiene constante debido a la menor masa muscular.
3. Fracción de filtración : es la fracción de FPR que se filtra a través de los capilares glomerulares:
Normalmente es de alrededor de 0.20. Por lo tanto, se
filtra 20% del FPR. El restante 80% abandona los capilares glomerulares por las arteriolas eferentes y pasa a
la circulación capilar peritubular. El aumento de la fracción de filtración incrementa la concentración de proteína
en la sangre capilar peritubular, lo que lleva a una mayor reabsorción en el túbulo proximal. La disminución de
la fracción de filtración reduce la concentración de proteína en la sangre capilar peritubular y la reabsorción en
el túbulo proximal.
Fracciónde filtración=
TFG
FPR
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

4. Determinación de la TFG: fuerzas de Starling : la fuerza impulsora de la tasa de filtración glomerular es la
presión neta de ultrafiltración a través de los capilares glomerulares. En los capilares glomerulares siempre se
favorece la filtración porque la presión de ultrafiltración neta siempre favorece la salida de líquido del capilar.
La TFG puede expresarse mediante la ecuación de Starling:
a. TFG es la filtración a través de los capilares glomerulares.
b. Kf es el coeficiente de filtración de los capilares glomerulares. La barrera glomerular consta del
endotelio capilar, la membrana basal y las hendiduras de filtración entre los podocitos. Normalmente,
las glucoproteínas aniónicas revisten la barrera de filtración y limitan la filtración de las proteínas
plasmáticas, que también tienen carga negativa.
c. P
GC
es la presión hidrostática del capilar glomerular, que es constante en toda la longitud del capilar.
Aumenta por la dilatación de la arteriola aferente o la constricción de la arteriola eferente. El aumento
de la π
GC
eleva la presión neta de ultrafiltración y la TFG.
d. P
BS
es la presión hidrostática del espacio de Bowman y es análoga a Pi en los capilares de la
circulación general. Aumenta por la constricción de los uréteres. El aumento de la PBS reduce la
presión neta de ultrafiltración y la TFG.
e. π
GC
es la presión oncótica del capilar glomerular. Normalmente aumenta a lo largo del capilar
glomerular porque la filtración de agua eleva la concentración de proteína de la sangre capilar
glomerular. Aumenta con la concentración de proteínas. El aumento de la πGC reduce la presión neta
de ultrafiltración y la TFG.
f. π
BS
es la presión oncótica del espacio de Bowman. Suele ser cero (y por lo tanto pasarse por alto)
porque normalmente sólo se filtra una pequeña cantidad de proteína.
5. Cálculo tipo de la presión de ultrafiltración con la ecuación de Starling : en el extremo arteriolar aferente de un
capilar glomerular, PGC es de 45 mm Hg, PBS es de 10 mm Hg y πGC es 27 mm Hg. Valor y el sentido de la
presión neta de ultrafiltración:
6. Variación de las fuerzas de Starling: efecto sobre la TFG y la fracción de filtración :
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
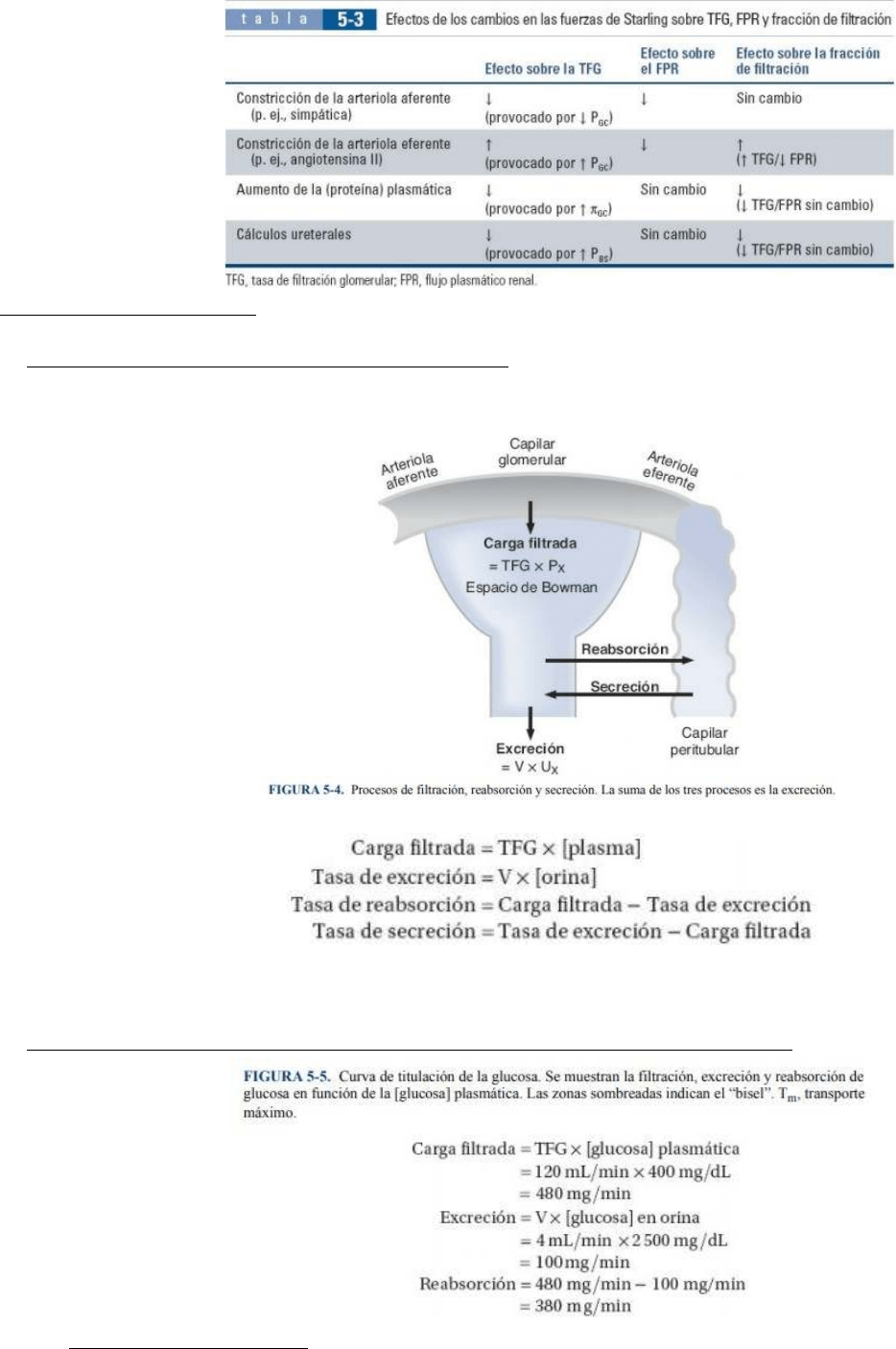
Reabsorción y secreción.
A. Cálculo de las tasas de reabsorción y secreción :
La tasa de reabsorción o secreción es la diferencia entre la cantidad filtrada a través de los capilares
glomerulares y la cantidad excretada en la orina.
Se calcula con las siguientes ecuaciones:
Si la carga filtrada es mayor que la tasa de excreción, entonces ha ocurrido reabsorción neta de la sustancia.
Si la carga filtrada es menor que la tasa de excreción, entonces se ha producido secreción neta de la
sustancia.
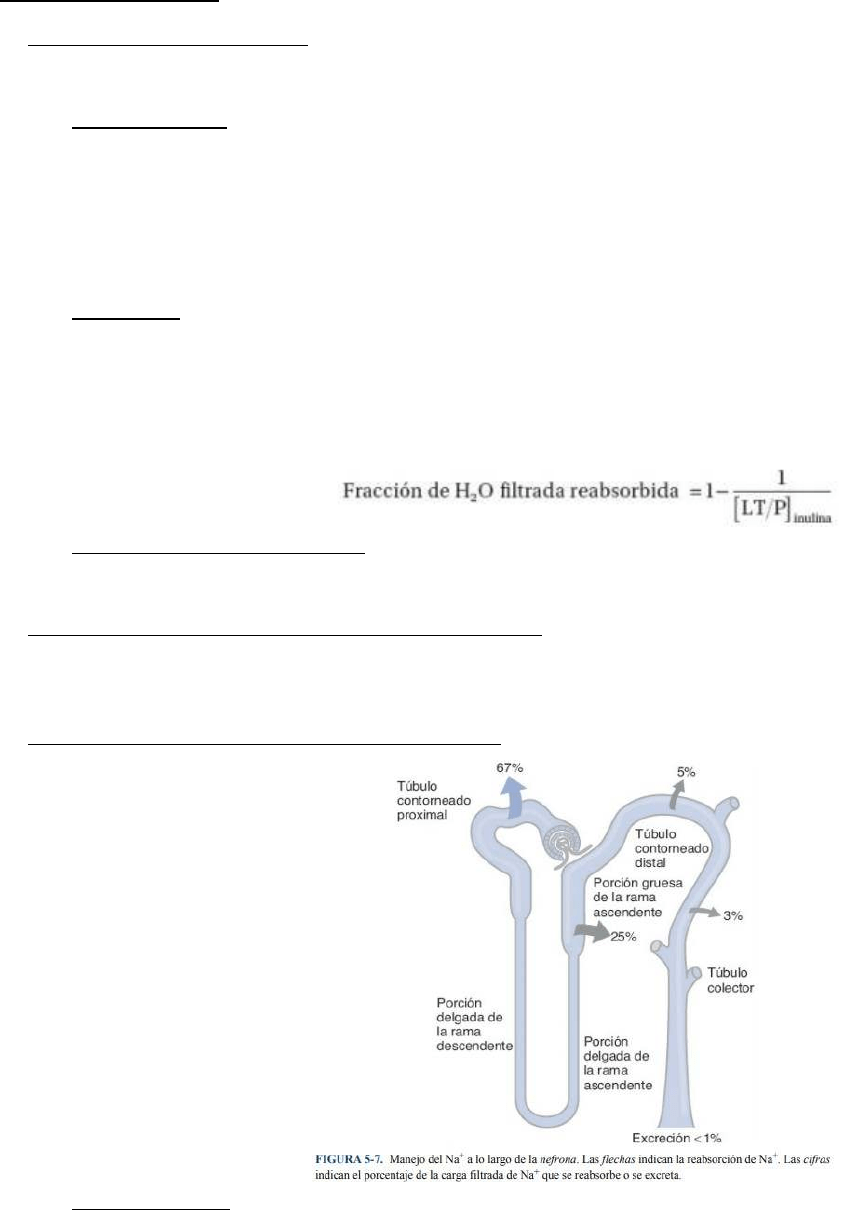
B. Curva de transporte máximo (Tm) de la glucosa: una sustancia reabsorbida:
1. Carga filtrada de glucosa : aumenta de modo directamente proporcional a la concentración plasmática de
glucosa (carga filtrada de glucosa = TFG × [P]glucosa).
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

2. Reabsorción de glucosa : el cotransporte de Na + -glucosa en el túbulo proximal reabsorbe glucosa del
líquido tubular a la sangre. Existe un número reducido de transportadores de Na + -glucosa. A
concentraciones plasmáticas de glucosa menores de 250 mg/dL puede reabsorberse toda la glucosa
filtrada, porque hay muchos transportadores disponibles; en este intervalo, la línea de reabsorción
coincide con la de filtración. c. A concentraciones plasmáticas de glucosa mayores de 350 mg/dL, los
transportadores están saturados. Por lo tanto, el aumento de la concentración plasmática por encima de
350 mg/dL no se traduce en una mayor tasa de reabsorción. La tasa de reabsorción a la cual los
transportadores están saturados es el transporte máximo.
3. Excreción de glucosa : a concentraciones plasmáticas menores de 250 mg/dL, se reabsorbe toda la
glucosa filtrada y la excreción es cero. El umbral (definido como la concentración plasmática a la cual la
glucosa aparece por primera vez en la orina) es de alrededor de 250 mg/dL. A concentraciones
plasmáticas mayores de 350 mg/dL, la reabsorción está saturada (Tm). Por lo tanto, cuando aumenta la
concentración plasmática, la glucosa filtrada adicional no puede reabsorberse y se excreta en la orina.
4. Bisel o chaflán (splay): es la sección de las curvas de glucosa comprendida entre el umbral y el transporte
máximo. Se encuentra entre las concentraciones plasmáticas de glucosa de alrededor de 250 y 350
mg/dL. Representa la excreción de glucosa en orina antes de alcanzar totalmente la saturación de la
reabsorción (Tm). Se explica por la heterogeneidad de las nefronas y la afinidad relativamente baja de los
transportadores de Na + -glucosa.
C. Curva de transporte máximo de ácido paraaminohipúrico (PAH): una sustancia secretada:
1. Carga filtrada de PAH : como sucede con la glucosa, la carga filtrada de PAH aumenta de modo
directamente proporcional a la concentración plasmática de PAH.
2. Secreción de PAH : la secreción de PAH va desde la sangre capilar peritubular al líquido tubular (orina) por
medio de los transportadores del túbulo proximal. A concentraciones plasmáticas bajas de PAH, la tasa de
secreción aumenta con la concentra ción plasmática. Una vez que los transportadores están saturados, el
aumento adicional de la concentración plasmática de PAH no provoca un aumento adicional de la tasa de
secreción (Tm).
3. Excreción de PAH : la excreción de PAH es la suma de la filtración a través de los capilares glomerulares
más la secreción desde la sangre capilar al túbulo. La curva de excreción es más pronunciada a
concentraciones plasmáticas bajas de PAH (más bajas que las del transporte máximo). En cuanto se
excede el transporte máximo para la secreción y todos los transportadores para la secreción están
saturados, la curva de excreción se aplana y se vuelve paralela a la curva de filtración. El FPR se
determina mediante la depuración de PAH a concentraciones plasmáticas de PAH que son más bajas que
las del transporte máximo.
D. Depuración relativa de las sustancias:
1. Sustancias con la depuración más alta : son las que se filtran a través de los capilares glomerulares y se
segregan desde los capilares peritubulares al túbulo (p. ej., PAH).
2. Sustancias con la depuración más baja : son las que no se filtran (p. ej., proteínas) o se filtran y
posteriormente se reabsorben hacia la sangre capilar peritubular (p. ej., Na +, glucosa, aminoácidos,
HCO3
–,
Cl
–)
.
3. Sustancias con depuración igual a la TFG : son marcadores glomerulares. Son las que se filtran
libremente, pero no se reabsorben ni se segregan (p. ej., inulina).
4. Depuración relativa : PAH > K + (alimentación rica en K +) > inulina > urea > Na + > glucosa, aminoácidos
y HCO3.
E. Difusión no iónica :
1. Ácidos débiles : tienen una forma HA y una forma A
−
. La forma HA, sin carga y liposoluble, puede
“retrodifundirse” desde la orina hacia la sangre. La forma A
−
, con carga y no liposoluble, no puede
difundirse desde la orina hacia la sangre. A un pH urinario ácido, predomina la forma HA, hay más
retrodifusión hacia la sangre y menor excreción del ácido débil. A un pH urinario alcalino, predomina la
forma A
−
. hay menos retrodifusión hacia la sangre y mayor excreción del ácido débil. Por ejemplo, la
excreción de ácido salicílico (un ácido débil) puede incrementarse mediante la alcalinización de la orina.
2. Bases débiles: tienen una forma BH
+
y una forma B. La forma B, sin carga y liposoluble, puede
“retrodifundirse” de la orina a la sangre. La forma BH+, con carga y no liposoluble, no puede
retrodifundirse hacia la sangre. A un pH urinario ácido, predomina la forma BH+, hay menos retrodifusión
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
hacia la sangre y mayor excreción de la base débil. Por ejemplo, la excreción de morfina (una base débil)
puede incrementarse acidificando la orina. A un pH urinario alcalino, predomina la forma B, hay más
retrodifusión hacia la sangre y menor excreción de la base débil.
Regulación del NaCl.
A. Terminología de la nefrona :
El líquido tubular (LT) es la orina en cualquier punto de la nefrona. El plasma (P) es el plasma de la circulación
general. Se considera constante.
1. Relación LT/Px: compara la concentración de una sustancia en el líquido tubular en cualquier punto de la
nefrona con la concentración de esa sustancia en el plasma. Si LT/P = 1.0, entonces o bien no se ha
producido reabsorción de la sustancia o la reabsorción de la sustancia ha sido exactamente proporcional a
la reabsorción de agua. Si LT/P < 1.0, la reabsorción de la sustancia ha sido mayor que la reabsorción de
agua, y la concentración de esa sustancia en el líquido tubular es menor que en el plasma. Si LT/P > 1.0,
entonces o bien la reabsorción de la sustancia ha sido menor que la reabsorción de agua o se ha
producido secreción de la sustancia.
2. LT/Pinulina : se utiliza como marcador de la reabsorción de agua a lo largo de la nefrona. Aumenta
conforme se reabsorbe agua. Puesto que la inulina se filtra libremente, pero no se reabsorbe ni se
segrega, su concentración en el líquido tubular es determinada únicamente por la cantidad de agua que
queda en el líquido tubular. La siguiente ecuación muestra cómo se calcula la fracción del agua filtrada
que se ha reabsorbido:
3. Relación [LT/P]x /[LT/P]inulina : corrige la relación LT/Px para considerar la reabsorción de agua. Esta
doble relación proporciona la fracción de la carga filtrada que queda en cualquier punto a lo largo de la
nefrona.
B. Información general sobre la reabsorción de Na
+
:
El Na
+
se filtra libremente a través de los capilares glomerulares; por lo tanto, la [Na
+
] del líquido tubular del
espacio de Bowman es igual a la del plasma (esto es, LT/PNa+ = 1.0). El Na
+
se reabsorbe a lo largo de toda
la nefrona y muy poco se excreta en la orina (< 1% de la carga filtrada).
C. Reabsorción de Na + a lo largo de la nefrona:
1. Túbulo proximal : reabsorbe dos tercios, o 67%, del Na + y el H2O filtrados, más que cualquier otra parte
de la nefrona. Es el lugar donde se produce el llamado equilibrio glomerulotubular. El proceso es
isoosmótico. La reabsorción de Na+ y H2O en el túbulo proximal es exactamente proporcional. Por lo
tanto, LT/PNa+ y LT/Posm = 1.0.
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
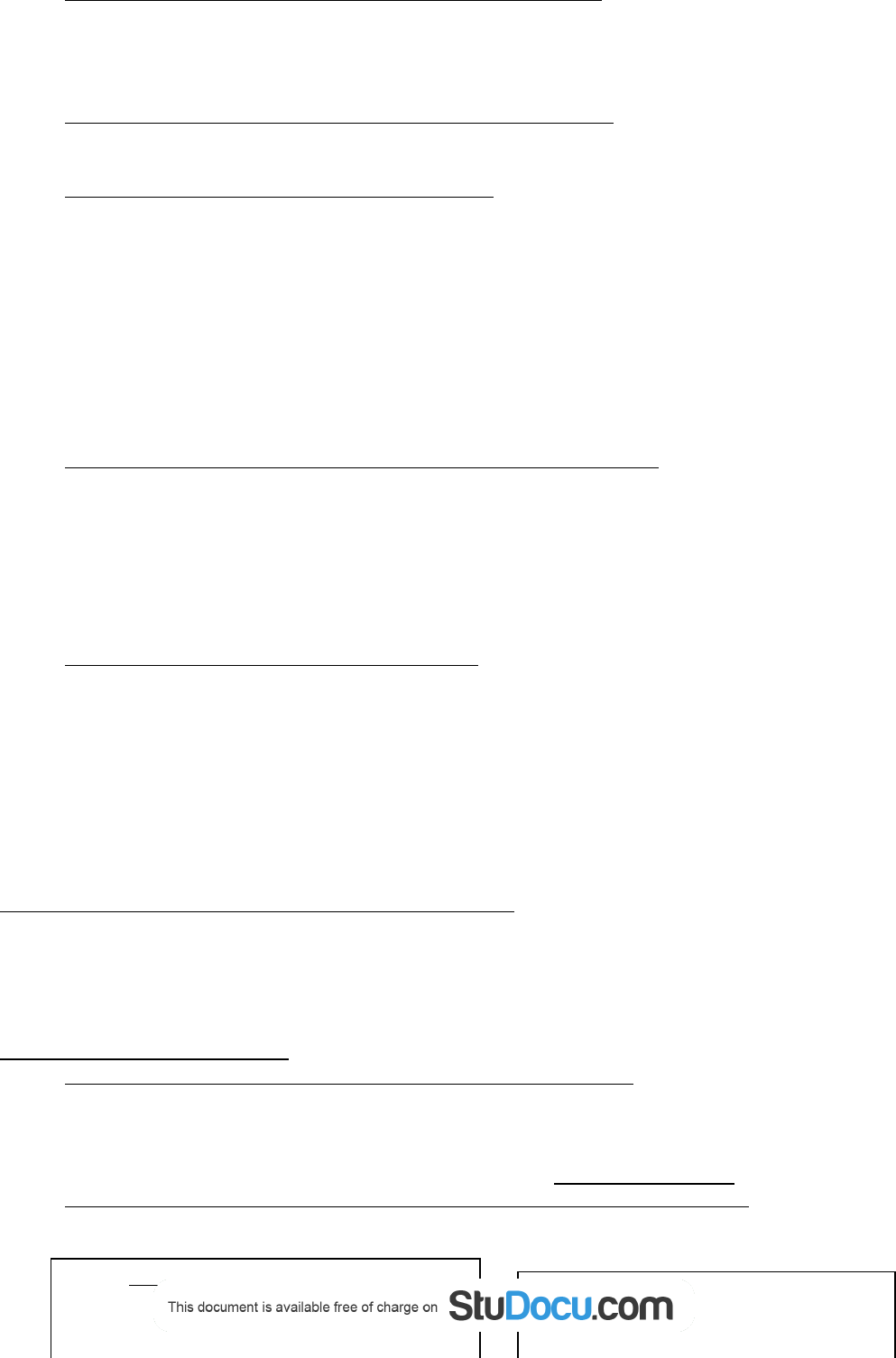
a. Porción inicial del túbulo proximal: características especiales . Reabsorbe Na + y H2O con HCO3–,
glucosa, aminoácidos, fosfato y lactato. El Na + se reabsorbe por cotransporte con glucosa,
aminoácidos, fosfato y lactato. Estos procesos de cotransporte explican la absorción de toda la
glucosa y los aminoácidos filtrados. El Na + también se reabsorbe por contratransporte a través del
intercambio de Na + -H+, que se relaciona directamente con la reabsorción de HCO3 – filtrado.
b. Porción final del túbulo proximal: características especiales . La glucosa, los aminoácidos y el
HCO3
−
filtrados ya se han eliminado completamente del líquido tubular por reabsorción en la parte
inicial del túbulo proximal. En la porción final del túbulo proximal, el Na
+
se reabsorbe con Cl
–
.
c. Equilibrio glomerulotubular en el túbulo proximal . Mantiene una reabsorción fraccionaria constante
(dos tercios, o 67%) del Na + y el H2O filtrados.) El mecanismo del equilibrio glomerulotubular se
basa en las fuerzas de Starling en los capilares peritubulares, que modifican la reabsorción de Na
+ y H2O en el túbulo proximal. La ruta de la reabsorción del líquido osmótico es desde la luz a la
célula del túbulo proximal, luego al espacio intercelular lateral y finalmente a la sangre capilar
peritubular. Las fuerzas de Starling en la sangre capilar peritubular determinan qué cantidad de ese
líquido isoosmótico se reabsorberá. La reabsorción de líquido aumenta con la πc de la sangre
capilar peritubular y disminuye con la disminución de la πc (presión osmótica dentro del capilar. El
aumento de la TFG y la fracción de filtración eleva la concentración de proteínas y la πc de la
sangre capilar peritubular. Este aumento, a su vez, incrementa la reabsorción de líquido. Por lo
tanto, se produce un ajuste de la filtración y la reabsorción, o equilibrio glomerulotubular.
d. Efectos del volumen de LEC sobre la reabsorción tubular proximal : la contracción del volumen de
LEC aumenta la reabsorción. Aumenta la concentración de proteínas y la πc en los capilares
peritubulares y disminuye la Pc capilar peritubular. En conjunto, estos cambios de las fuerzas de
Starling en la sangre capilar peritubular provocan un aumento de la reabsorción tubular proximal.
La expansión del volumen del LEC disminuye la reabsorción. La expansión de volumen disminuye
la concentración de proteínas y la πc en los capilares peritubulares y aumenta la Pc. En conjunto,
estos cambios de las fuerzas de Starling en la sangre capilar peritubular provocan una disminución
de la reabsorción tubular proximal.
e. Relaciones LT/P a lo largo del túbulo proximal: al inicio del túbulo proximal (es decir, en el espacio
de Bowman), la relación LT/P para sustancias libremente filtradas es 1.0, ya que aún no ocurre
reabsorción o secreción. Al avanzar en el túbulo proximal, la relación LT/P para Na + y osmolaridad
permanece en 1.0 porque Na + y soluto total se reabsorben de manera proporcional con agua;
esto es, de manera isoosmótica. Glucosa, aminoácidos y HCO3 – se reabsorben
proporcionalmente más que el agua, de modo que los valores de LT/P se hacen menores de 1.0. Al
principio del túbulo proximal, el Cl – se reabsorbe proporcionalmente menos que el agua, de modo
que su valor de LT/P es mayor de 1.0. La inulina no se reabsorbe, por lo que su valor de LT/P
aumenta de manera continua por arriba de 1.0 a medida que el agua se reabsorbe y la inulina “se
queda atrás”.
2. Porción gruesa de la rama ascendente del asa de Henle : reabsorbe 25% del Na + filtrado. Contiene un
cotransportador de Na + -K+ -2Cl – en la membrana luminal. Es el sitio de acción de los diuréticos de asa.
Es impermeable al agua. Por lo tanto, el NaCl se reabsorbe sin agua. Como resultado, la [Na+] del líquido
tubular y la osmolaridad del líquido tubular disminuyen por debajo de sus concentraciones en el plasma
(esto es, LT/PNa+ y LT/Posm < 1). Así, este segmento se denomina segmento diluyente. Presenta una
diferencia de potencial positivo para la luz.
3. Túbulo distal y conducto colector : juntos reabsorben 8% del Na+ filtrado.
a. Porción inicial del túbulo distal: características especiales. Reabsorbe NaCl mediante un
cotransportador de Na
+
- Cl
–
. Es el sitio de acción de los diuréticos tiazídicos. Es impermeable al
agua, al igual que la porción gruesa de la rama ascendente. Por ello, la reabsorción de NaCl se
produce sin agua, lo que diluye todavía más el líquido tubular. Se denomina segmento diluyente
cortical.
b. Porción final del túbulo distal y conducto colector: características especiales . Tienen dos tipos de
células:
2- Células intercalares:
- Segregan H+ mediante una
H + -ATPasa, que es
estimulada por la
aldosterona.
- Reabsorben K+ mediante
una H+, K+ - ATPasa
1- Células principales:
- Reabsorben Na + y H2O.
- Secretan K+.
La aldosterona aumenta la
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
Regulación del K
+
.
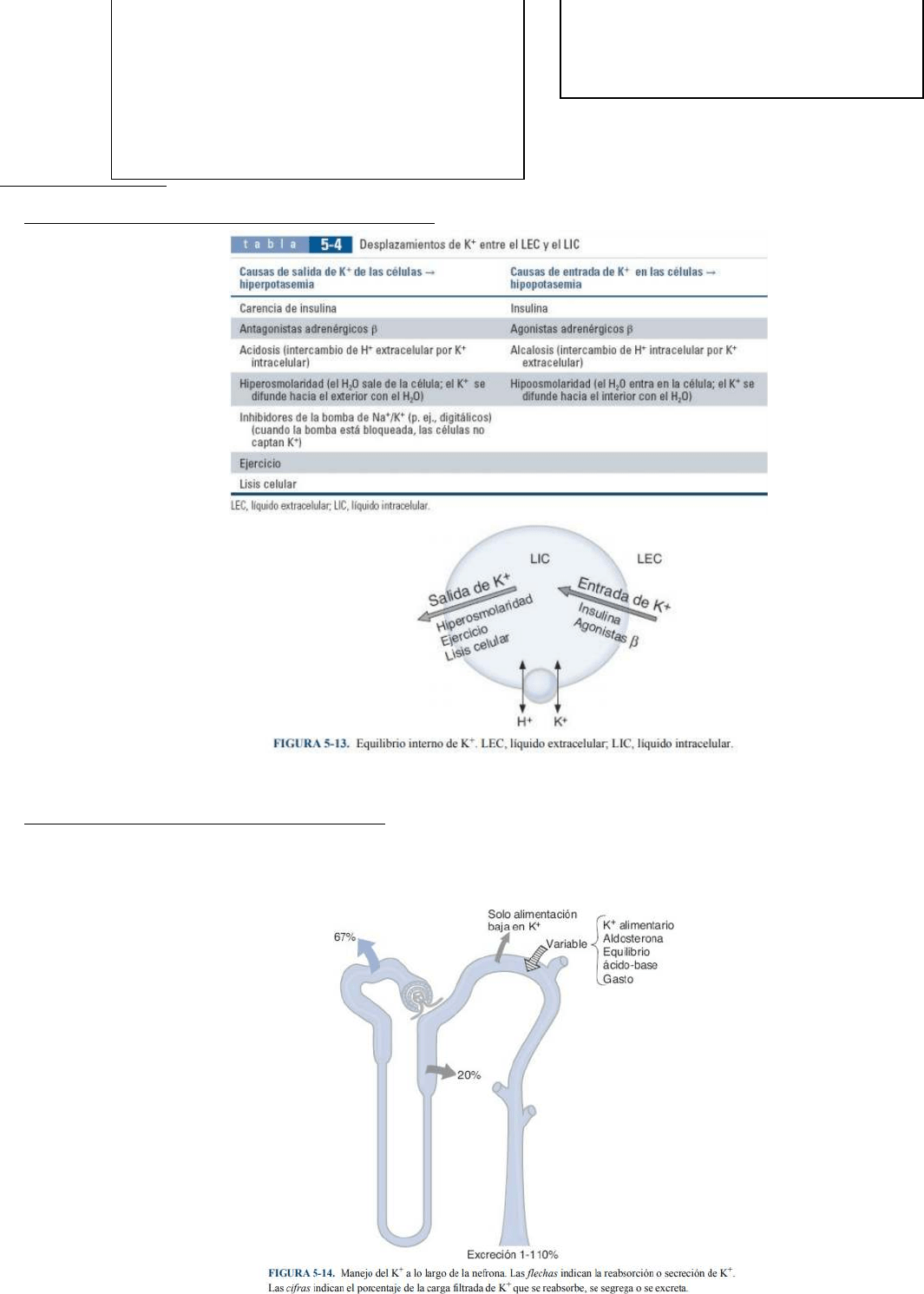
A. Desplazamientos de K+ entre el LIC y el LEC:
La mayor parte del K + del organismo se encuentra en el LIC. La salida de K+ de las células provoca
hiperpotasemia. La entrada de K+ en las células provoca hipopotasemia.
B. Regulación renal del equilibrio de K+: La nefrona filtra, reabsorbe y secreta K+. El equilibrio de K+ se
alcanza cuando la excreción urinaria de K + es exactamente igual al aporte de K + en la alimentación. La
excreción de K + puede oscilar ampliamente entre 1 y 110% de la carga filtrada, según el aporte de K +
alimentario, las concentraciones de aldosterona y el equilibrio ácido-base.
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

1. Capilares glomerulares: la filtración a través de los capilares glomerulares es libre. Por lo tanto, la relación
LT/PK+ en el espacio de Bowman es 1.
2. Túbulo proximal : reabsorbe 67% del K + filtrado junto con Na + y H2O.
3. Porción gruesa de la rama ascendente del asa de Henle: reabsorbe 20% del K + filtrado. En la
reabsorción interviene el cotransportador de Na + -K+ -2Cl – en la membrana luminal de las células de la
rama ascendente gruesa.
4. Túbulo distal y conducto colector : reabsorben o segregan K+, según el aporte de K + alimentario.
a. ReabsorciÓn de k+. Implica una H+, K+ -ATPasa en la membrana luminal de las células
intercalares. Solo ocurre en caso de alimentación baja en K+ (agotamiento de K +). En estas
condiciones, la excreción de K + puede ser de únicamente 1% de la carga filtrada porque el riñón
ahorra todo el K + posible.
b. Secreción de k+. Ocurre en las células principales. Es variable y explica el amplio intervalo de
excreción de K + en la orina. Depende de factores como K + alimentario, concentraciones de
aldosterona, equilibrio ácido-base y diuresis.
Regulación renal de urea, fosfato, calcio y magnesio:
A. Urea:
Se reabsorbe y segrega en la nefrona por difusión, ya sea simple o facilitada, según el segmento de la
nefrona. Cincuenta por ciento de la urea filtrada se reabsorbe en el túbulo proximal por difusión simple. La
urea se secreta en la porción delgada de la rama descendente del asa de Henle por difusión simple (desde la
alta concentración de urea en el líquido intersticial medular). El túbulo distal, los conductos colectores
corticales y los conductos colectores medulares externos son impermeables a la urea; por lo tanto, estos
segmentos no pueden reabsorber urea. La vasopresina (ADH) estimula un transportador de difusión facilitada
para urea (UT1) en los conductos colectores medulares internos. La reabsorción de urea desde estos
conductos contribuye a la recirculación de la urea en la médula interna y a la adición de urea al gradiente
osmótico corticopapilar. La excreción de urea varía con la diuresis. A niveles altos de reabsorción de agua
(baja diuresis) ocurren mayor reabsorción de urea y menor excreción de urea. A niveles bajos de reabsorción
de agua (diuresis alta) se produce menor reabsorción de urea y mayor excreción de urea.
B. Fosfato:
El 85% del fosfato filtrado se reabsorbe en el túbulo proximal por cotransporte de Na + -fosfato. Puesto que
los segmentos distales de la nefrona no reabsorben fosfato, 15% de la carga filtrada se excreta en la orina. La
paratirina u hormona paratiroidea (PTH) inhibe la reabsorción de fosfato en el túbulo proximal mediante la
activación de la adenilato ciclasa, la generación de AMPc y la inhibición del cotrans-porte de Na + -fosfato.
Por lo tanto, la PTH provoca fosfaturia y aumenta el AMPc urinario. El fosfato es un amortiguador urinario de
H+; el H2PO4 – excretado se denomina ácido titulable. El factor de crecimiento de fibriblastos (FGF23), que
es secretado por el hueso, inhibe el cotransporte de Na + -fosfato en la parte inicial del túbulo proximal.
C. Calcio (Ca2+) :
El 60 % del Ca 2+ plasmático se filtra a través de los capilares glomerulares. En conjunto, el túbulo proximal y
la porción gruesa de la rama ascendente reabsorben más de 90% del Ca 2+ filtrado mediante procesos
pasivos acoplados a la reabsorción de Na+. Los diuréticos de asa (p. ej., furosemida) elevan la excreción de
Ca 2+ en la orina. Puesto que la reabsorción de Ca 2+ está vinculada a la reabsorción de Na + en el asa de
Henle, la inhibición de la reabsorción de Na + con un diurético de asa también inhibe la reabsorción de Ca 2+.
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
En conjunto, el túbulo distal y el conducto colector reabsorben 8% del Ca 2+ filtrado mediante un proceso
activo.
D. Magnesio (Mg 2+):
Se reabsorbe en el túbulo proximal, la porción gruesa de la rama ascendente del asa de Henle y el túbulo
distal. En la porción gruesa de la rama ascendente, Mg 2+ y Ca 2+ compiten por la reabsorción; por lo tanto,
la hipercalcemia provoca aumento de la excreción de Mg 2+ (al inhibir la reabsorción de Mg 2+). De modo
similar, la hipermagnesemia aumenta la excreción de Ca 2+ (al inhibir la reabsorción de Ca 2+).
Concentración y dilución de la orina.
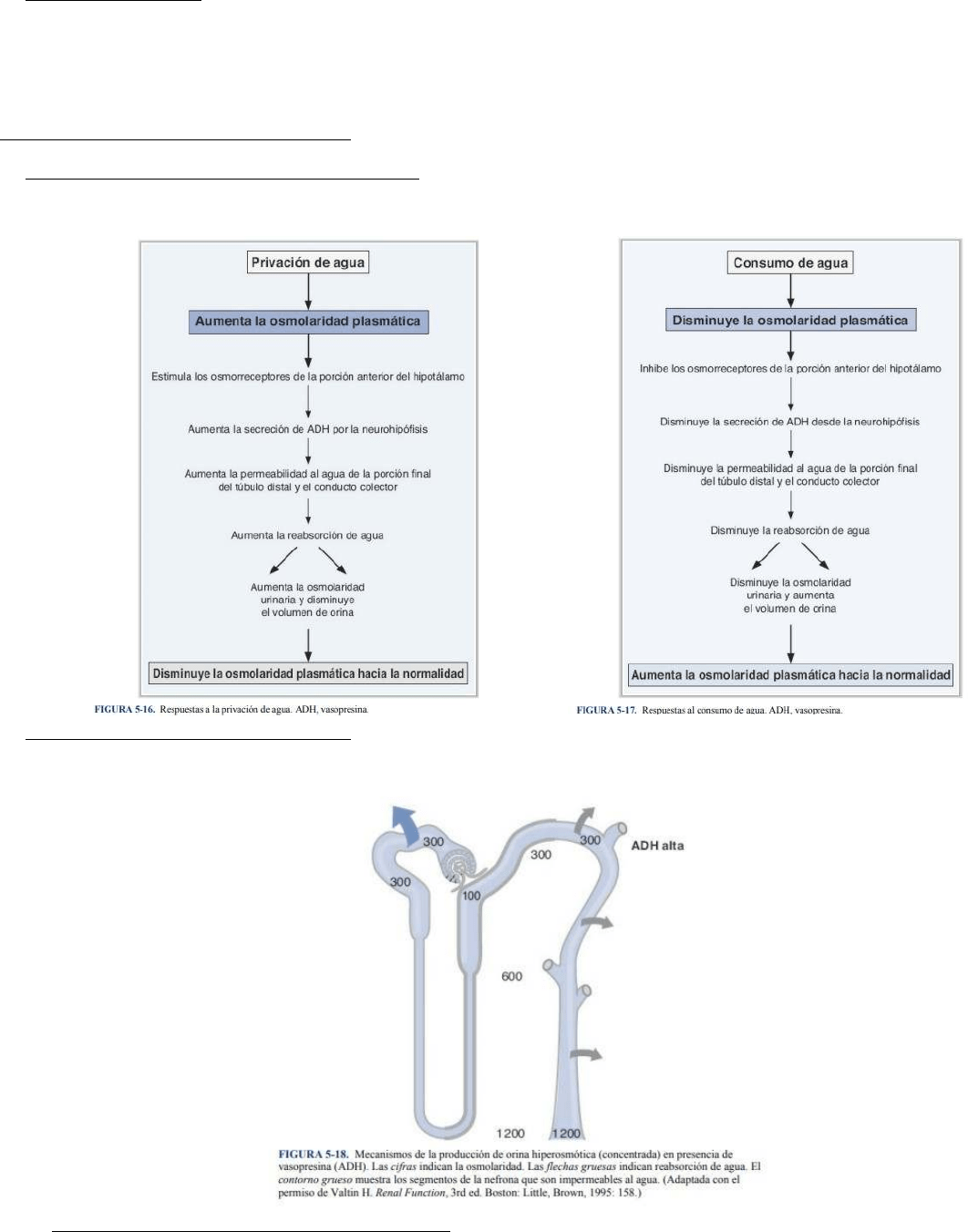
A. Regulación de la osmolaridad plasmática :
Se consigue variando la cantidad de agua excretada respecto a la cantidad de soluto excretado (esto es,
variando la osmolaridad urinaria).
B. Producción de orina concentrada:
También se denomina orina hiperosmótica, y osmolaridad urinaria > osmolaridad sanguínea. Se produce
cuando las concentraciones de ADH circulante son altas.
1. Gradiente osmótico corticopapilar: ADH alta. Es el gradiente de osmolaridad de la corteza (300 mOsm/L) a
la papila (1 200 mOsm/L) y es producido de manera principal por NaCl y urea. Se establece por
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146

multiplicación contracorriente en las asas de Henle y reciclaje de la urea en los conductos colectores
medulares internos. Es mantenido por intercambio a contracorriente en los vasos rectos.
a. Multiplicación a contracorriente en el asa de Henle. Depende de la reabsorción de NaCl en la porción
gruesa de la rama ascendente y el flujo a contracorriente en las ramas descendente y ascendente del
asa de Henle. Es aumentada por la ADH, que estimula la reabsorción de NaCl en la porción gruesa de
la rama ascendente. Por lo tanto, la presencia de ADH aumenta el gradiente osmótico corticopapilar.
b. La ADH también aumenta la recirculación de urea de los conductos colectores en la médula renal
interna al líquido intersticial medular (por estímulo del transportador UT1).
c. Los vasos rectos son los capilares que irrigan el asa de Henle. Mantienen el gradiente corticopapilar al
actuar como intercambiadores osmóticos. La sangre de los vasos rectos se equilibra osmóticamente
con el líquido intersticial de la médula y la papila.
2. Túbulo proximal: ADH alta. La osmolaridad del filtrado glomerular es idéntica a la del plasma (300 mOsm/L).
Dos tercios del H2O filtrada se reabsorben isoosmóticamente (con Na +, Cl –, HCO3 –, glucosa,
aminoácidos, etc.) en el túbulo proximal. LT/Posm = 1 en todo el túbulo proximal porque el H2O se
reabsorbe isoosmóticamente con el solute.
3. Porción gruesa de la rama ascendente del asa de Henle: ADH alta. Se denomina segmento diluyente.
Reabsorbe NaCl por medio del cotransportador de Na + -K+ -2Cl –. Es impermeable al H2O. Por lo tanto, el
H2O no se reabsorbe con el NaCl y el líquido tubular se diluye. El líquido que abandona la porción gruesa
de la rama ascendente tiene osmolaridad de 100 mOsm/L y LT/Posm < 1.0 como consecuencia del proceso
de dilución.
4. Porción inicial del túbulo distal: ADH alta . Se denomina segmento diluyente cortical. Al igual que la porción
gruesa de la rama ascendente, la porción inicial del túbulo distal reabsorbe NaCl, pero es impermeable al
agua. Por consiguiente, el líquido tubular se diluye todavía más.
5. Porción final del túbulo distal: ADH alta . La ADH aumenta la permeabilidad al H2O de las células principales
de la porción final del túbulo distal. El H2O se reabsorbe del túbulo hasta que la osmolaridad del líquido
tubular distal es igual a la del líquido intersticial circundante en la corteza renal (300 mOsm/L). LT/Posm =
1.0 al final del túbulo distal porque se alcanza el equilibrio osmótico en presencia de ADH.
6. Conductos colectores: ADH alta . Al igual que en la porción final del túbulo distal, la ADH aumenta la
permeabilidad al H2O de las células principales de los conductos colectores. Cuando el líquido tubular fluye
por los conductos colectores, pasa a través del gradiente corticopapilar (regiones de osmolaridad
creciente), que se estableció antes por el mecanismo de multiplicación a contracorriente y recirculación de
urea. El H2O se reabsorbe de los conductos colectores hasta que la osmolaridad del líquido tubular es igual
a la del líquido intersticial circundante. La osmolaridad de la orina final es igual a la de la curva del asa de
Henle en la punta de la papila (1 200 mOsm/L). LT/Posm > 1.0 porque se alcanza el equilibrio osmótico con
el gradiente corticopapilar en presencia de ADH.
C. Producción de orina diluida :
Se denomina orina hipoosmótica, y osmolaridad urinaria < osmolaridad sanguínea. Se produce cuando las
concentraciones de ADH circulante son bajas o cuando la ADH es ineficaz.
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
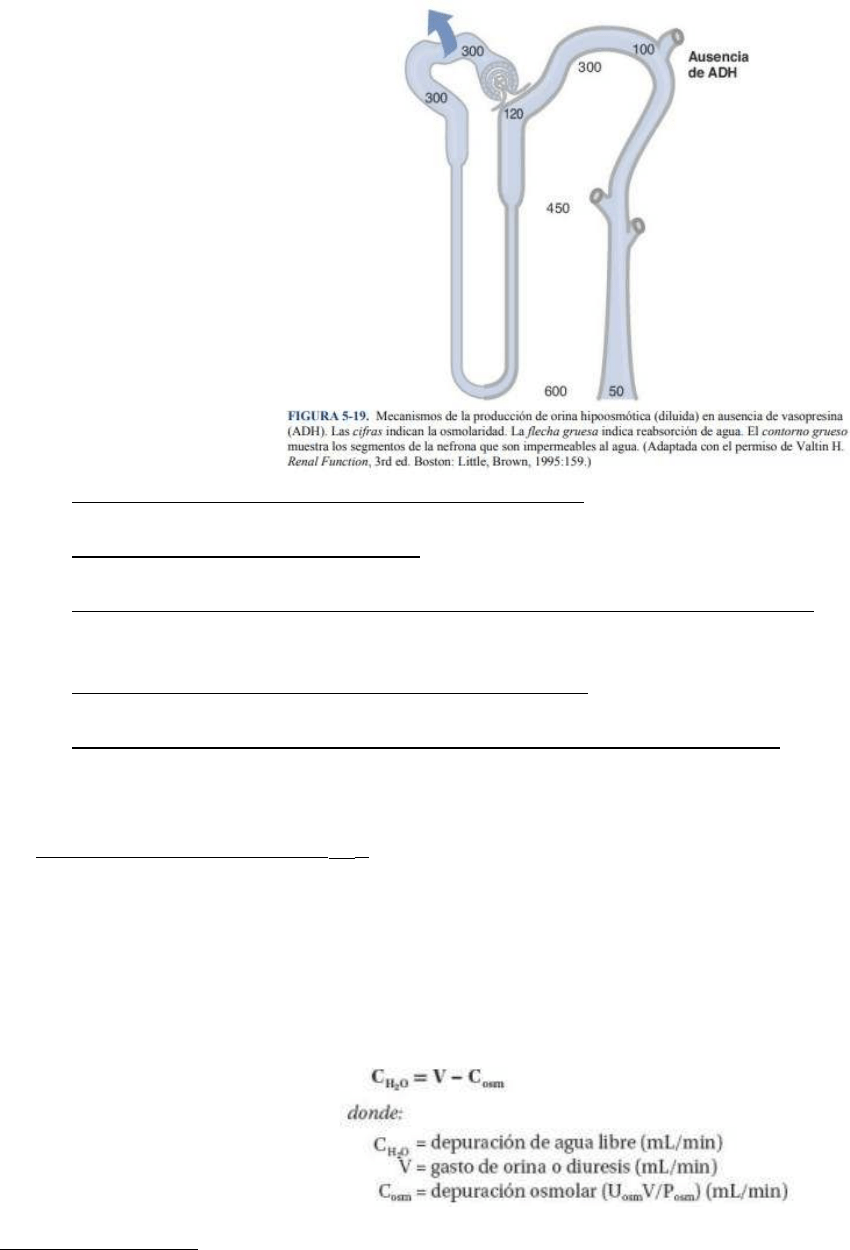
1. Gradiente osmótico corticopapilar: ausencia de ADH . Es menor que en presencia de ADH porque la ADH
estimula la multiplicación a contracorriente y la recirculación de urea.
2. Túbulo proximal: ausencia de ADH . Al igual que en presencia de ADH, dos tercios del agua filtrada se
reabsorben isoosmóticamente. LT/Posm = 1.0 en todo el túbulo proximal.
3. Porción gruesa de la rama ascendente del asa de Henle: ausencia de ADH. Al igual que en presencia de
ADH, el NaCl se reabsorbe sin agua y el líquido tubular se diluye (aunque no tanto como en presencia
de ADH). LT/Posm < 1.0.
4. Porción inicial del túbulo distal: ausencia de ADH . Al igual que en presencia de ADH, el NaCl se
reabsorbe sin H2O y el líquido tubular se diluye todavía más. LT/Posm < 1.0.
5. Porción final del túbulo distal y conductos colectores: ausencia de ADH. En ausencia de ADH, las células
de la porción final del túbulo distal y los conductos colectores son impermeables al H2O. Por lo tanto,
aunque el líquido tubular fluye a través del gradiente osmótico corticopapilar, no se alcanza el equilibrio
osmótico. La osmolaridad de la orina final estará diluida y será de tan solo 50 mOsm/L. LT/Posm < 1.0.
D. Depuración de agua libre (C
H2O
):
Se utiliza para estimar la capacidad de concentrar o diluir la orina. El agua libre, o agua sin solutos, se
produce en los segmentos diluyentes del riñón (esto es, porción gruesa de la rama ascendente y porción
inicial del túbulo distal), donde el NaCl se reabsorbe y el agua libre queda en el líquido tubular. En ausencia
de ADH, esta agua sin solutos se excreta y la CH2O es positiva. En presencia de ADH, esta agua sin solutos
no se excreta, sino que es reabsorbida por la porción final del túbulo distal y los conductos colectores, y la
C
H2O
es negativa.
Cálculo:
Hormonas renales.
Downloaded by Katherine Sanchez ([email protected])
lOMoARcPSD|12873146
Este documento contiene más páginas...
Descargar Completo
resumen-fisiologia-renal-y-equilibrio-acido.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.