Estructura de las Mitocondrias
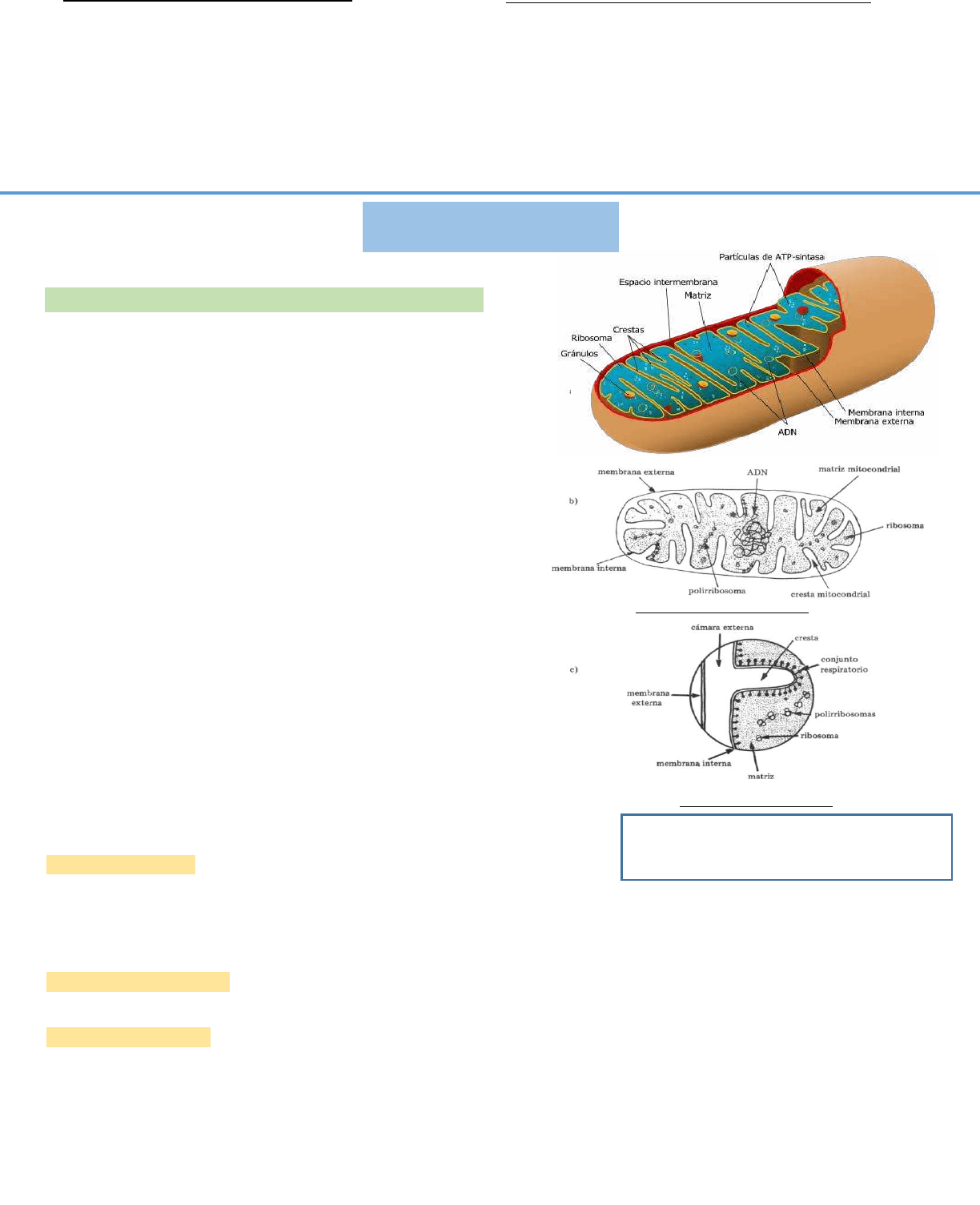
Las mitocondrias están rodeadas por dos membranas, una externa que es
lisa y una interna que se pliega hacia adentro formando crestas. Dentro
del espacio interno de la mitocondria en torno a las crestas, existe una
solución densa (matriz o estroma) que contiene enzimas, coenzimas,
agua, fosfatos y otras moléculas que intervienen en la respiración.
La membrana externa es permeable para la mayoría de las moléculas
pequeñas, pero la interna sólo permite el paso de ciertas moléculas como
el ácido pirúvico y ATP y restringe el paso de otras. Esta permeabilidad
selectiva de la membrana interna, tiene una importancia crítica porque
capacita a las mitocondrias para destinar la energía de la respiración para
la producción de ATP.
La mayoría de las enzimas del ciclo de Krebs se encuentran en la matriz
mitocondrial. Las enzimas que actúan en el transporte de electrones se
encuentran en las membranas de las crestas.
Las membranas internas de las crestas están formadas por un 80 % de
proteínas y un 20 % de lípidos.
En las mitocondrias, el ácido pirúvico proveniente de la glucólisis, se oxida
a dióxido de carbono y agua, completándose así la degradación de la
glucosa.
El 95 % del ATP producido se genera, en la mitocondria.
Las mitocondrias son consideradas organoides semiautónomos, porque
presentan los dos ácidos nucleicos (del tipo procarionte)
Cresta mitocondrial (detalle).
(Son cilíndricas,miden 3um de largo,y 5 um de diámetro)
En las células Suelen hallarse entre 1000 y 2000 mitocondrias
Esquema de un corte al M.E.T.
Importancia de la energía para la célula
- Mantener la estructura organizada de la célula
- Desplazarse
- Ingerir, digerir y procesar el alimento
- Adaptarse a los cambios ambientales
- Crecer y reproducirse
* O sea, la célula necesita energía para mantener su ciclo
vital
Unas funciones de la célula que requieren energía
1) Mitosis y Meiosis
2) Motilidad y Contracción
3) Biosíntesis de Materiales Celulares
4) Transporte Activo
5) Transmisión de Señales
6) Endocitosis y exocitosis
MITOCONDRIAS
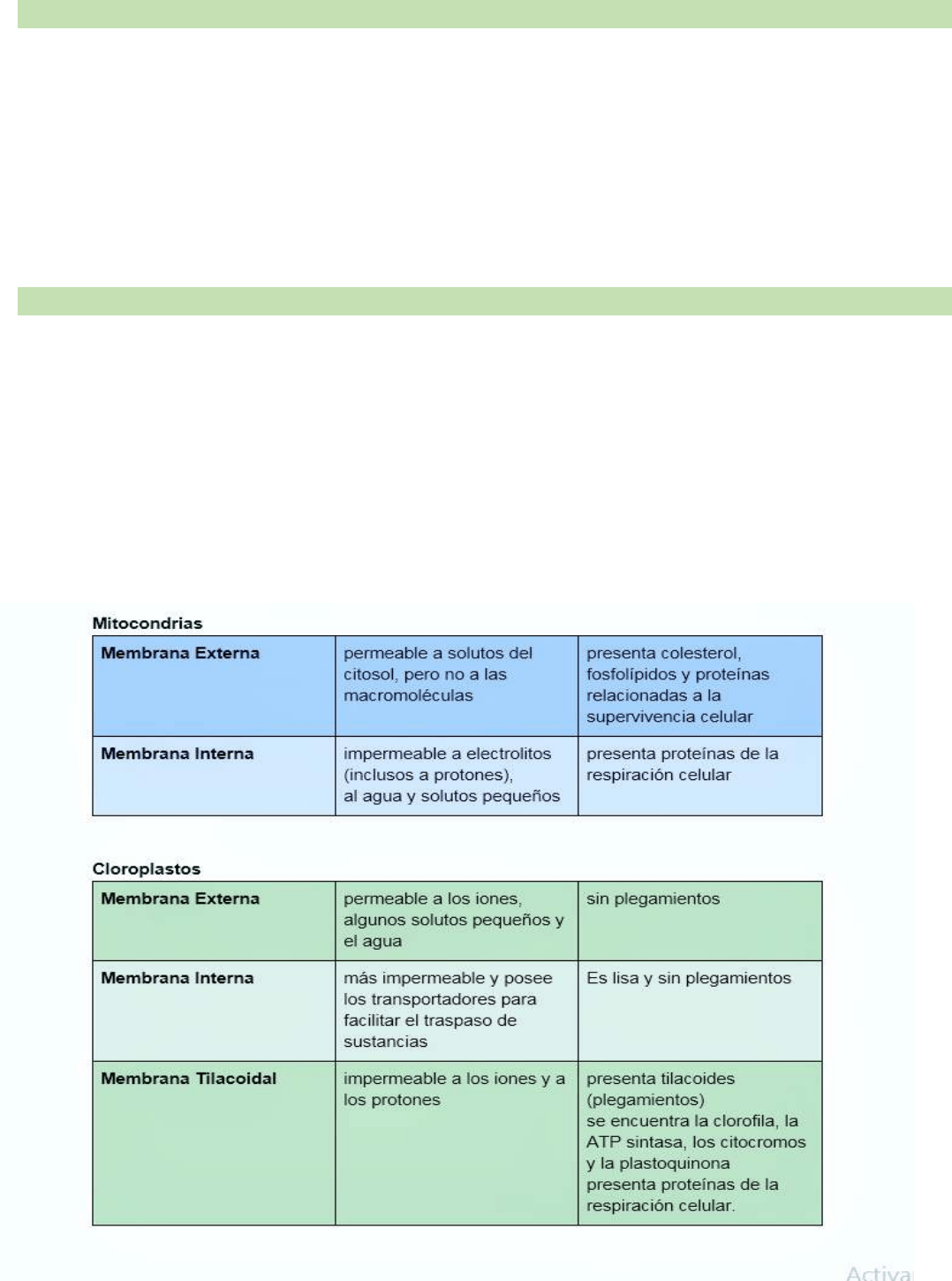
MEMBRANA EXTERNA
- Tiene mayor cantidad de lípidos que proteínas
- Es permeable a todos los solutos existentes en el citosol, pero no a las macromoléculas.
- Presenta diferente composición de colesterol, de fosfolípidos y proteínas relacionadas a la supervivencia celular
- Presenta una proteína relacionada a la supervivencia celular
ESPACIO INTERMEMBRANA
- Elevada concentración de H+
MATRIZ MITOCONDRIAL
- Es un gel denso que posee una enorme cantidad de proteínas solubles, ribosomas (similares a los ribosomas de las procariontes),
ADN mitocondrial y proteínas del ciclo de krebs y de la beta oxidación de ácidos grasos.
- Las enzimas involucradas en la descarboxilación del piruvato se localizan en matriz mitocondrial (ae)
- 3 tipos de ARNm ,2 tipos de ARNr,20 tipos de ARNt
Este archivo fue descargado de https://filadd.com
FILADD.COM
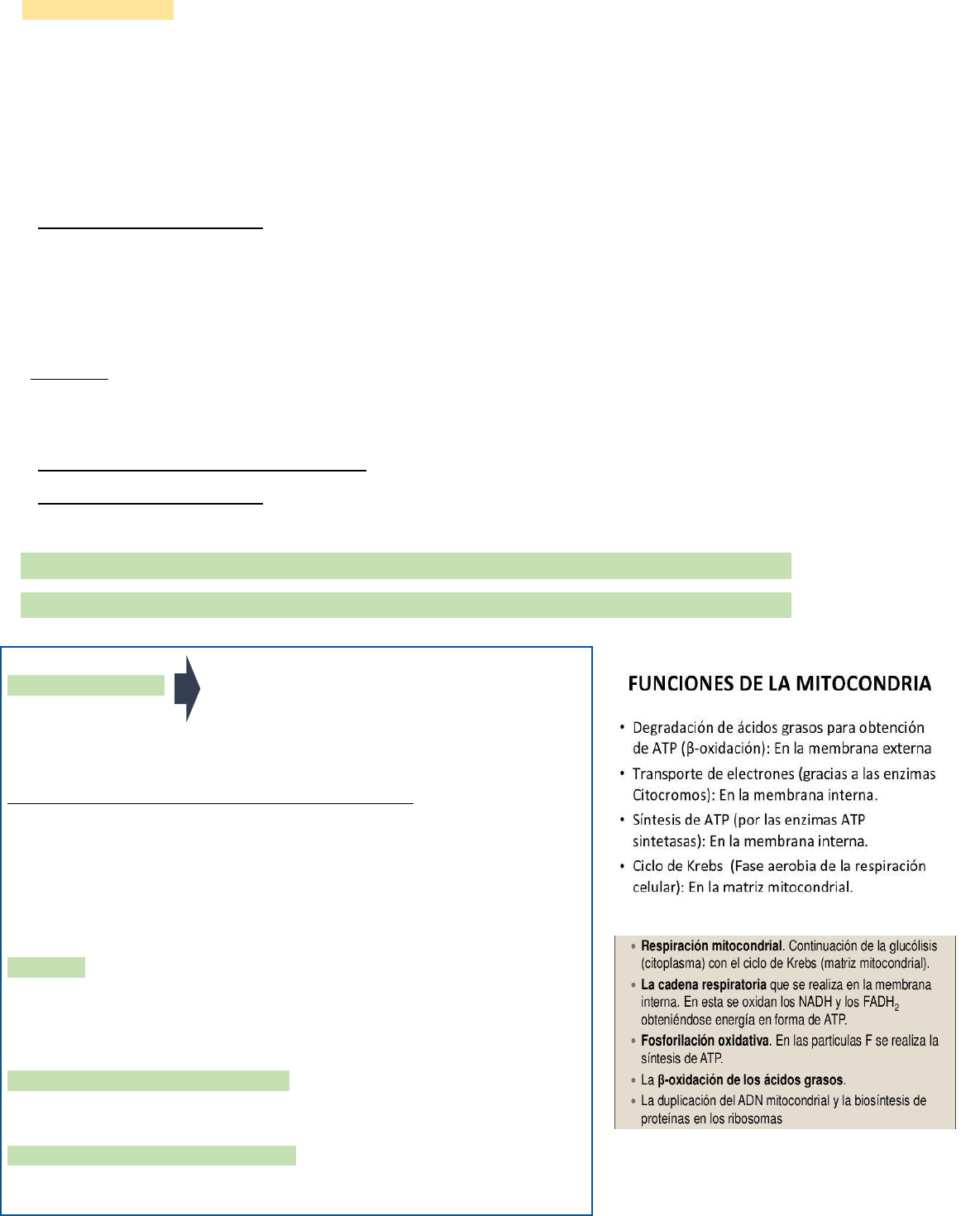
La funcion principal es generar ATP
MEMBRANA INTERNA
- Presenta una serie de pliegues que forman las crestas
- con las crestas la superficie de la membrana interna aumenta de manera significativa
- Posee más cantidad de proteínas que de lípidos
- Presenta las proteínas necesarias para realizar la respiración celular
- Muy impermeable a diferente electrolitos, inclusos a protones
- Impermeabilidad al agua y solutos pequeños
- Presenta proteínas de la familia de los citocromos que son necesarias para realizar la respiración celular
- La proteína de la membrana interna no hidroliza ATP, sino que lo sintetiza.
En ella se localizan:
1) cadena transportadora de electrones
- Conjuntos de macromoléculas compuestos por 4 complejos (entre los cuales se encuentran dos transportadores de
electrones denominados ubiquinoma y citocromo c):
- NADH deshidrogenasa (I)
- Succinato deshidrogenasa (II) - es una de las enzimas del ciclo de Krebs
- Citocromo b-c1 (III)
- Citocromo oxidasa (IV)
2) ATP Sintasa
- Complejo proteico
- Cataliza la formación de ATP a partir de ADP y fosfato
- Responsable de la "fosforilación oxidativa”
3) Un fosfolípido doble - difosfatidilglicerol o cardiolipina
4) Diversos canales iónicos y permeasas
FUNCIONES DE LAS MITOCONDRIAS
(LAS MÁS IMPORTANTES SON CICLO DE KREBS Y FOSFORILACIÓN):
…………………………………………… GLUCOLISIS (SE LLEVA A CABO EN EL CITOPLASMA)
RESPIRACION CELULAR CICLO DE KREBS (SE LLEVA A CABO EN LA MATRIZ MITOCONDRIAL)
……………………………………………. FOSFORILACION OXIDATIVA o transporte de electrones
…………………………………………………….(SE LLEVA A CABO EN LAS CRESTAS )(MEMBRANA INTERNA)
)
Es un proceso por la cual la célula obtiene energía a partir del ATP
GLUCÓLISIS - Gluco = Glucosa | lisis = rompimiento. Es una vía metabólica en la que se produce
la lisis o degradación de la glucosa.
CICLO DE KREBS : Ocurre después de la Glucólisis
CADENA RESPIRATORIA Y FOSFORILACIÓN OXIDATIVA :Electrones provenientes de la Glucólisis y/o
Ciclo de Krebs
APOPTOSIS (muerte celular programada)
- Es un proceso que se dá, por ejemplo, para eliminar células que un tejido tiene de más, para
eliminar células tumorales o células que están infectadas por algún virus. - para que se
desencadene la apoptosis es necesaria la desactivación de la proteína BCL2 que está inserta en
la membrana mitocondrial externa.
REMOCION DE CALCIO CITOPLASMATICO
Se lleva a cabo cuando los niveles de este caution aumentan y alcanzan los niveles que son
tóxicos para la célula
SINTESIS DE AMINOACIDOS Y ESTEROIDES
Este archivo fue descargado de https://filadd.com
FILADD.COM
- Son organelas citoplasmáticas que pertenecen a la família de los plástidos
- juntos con las mitocondrias constituyen las maquinarias bioquímicas que se
encargan de producir las transformaciones energéticas necesarias para
mantener las funciones de las células.
- poseen pigmentos (clorofilas, carotenoides) que en ellos tiene lugar la
fotosíntesis - poseen pigmentos fotosintéticos, como la clorofila.
- sólo se encuentran en las células vegetales (hoja, tallos jóvenes y algunas
algas y bacterias)
- las células de los vegetales superiores tienen entre 20 y 40 cloroplastos
- algunas levaduras tienen solamente 1 cloroplasto
- suele tener forma ovoide, esférica o discoidal.
- son más grandes de lo que las mitocondrias, alcanzando un promedio de 6
micrones
Los cloroplastos son organoides en los que se lleva a cabo la fotosíntesis en
las células vegetales eucariontes. En los procariontes fotosintetizadores no
existen tales organoides. Los pigmentos captadores de energía, se hallan
asociados a las laminillas derivadas de la membrana plasmática.
Generalmente poseen forma discoide, su tamaño es variable (término medio:
4 a 6 nm de longitud). El cloroplasto está limitado por una doble membrana
que no posee clorofila ni citocromos, que envuelve a la matriz o estroma.
Esta posee el 50% de las proteínas, que en su mayoría son solubles; también
contiene ribosomas y ADN de características procarionte. Estas dos últimas
características explican que el cloroplasto sea un organoide semiautónomo.
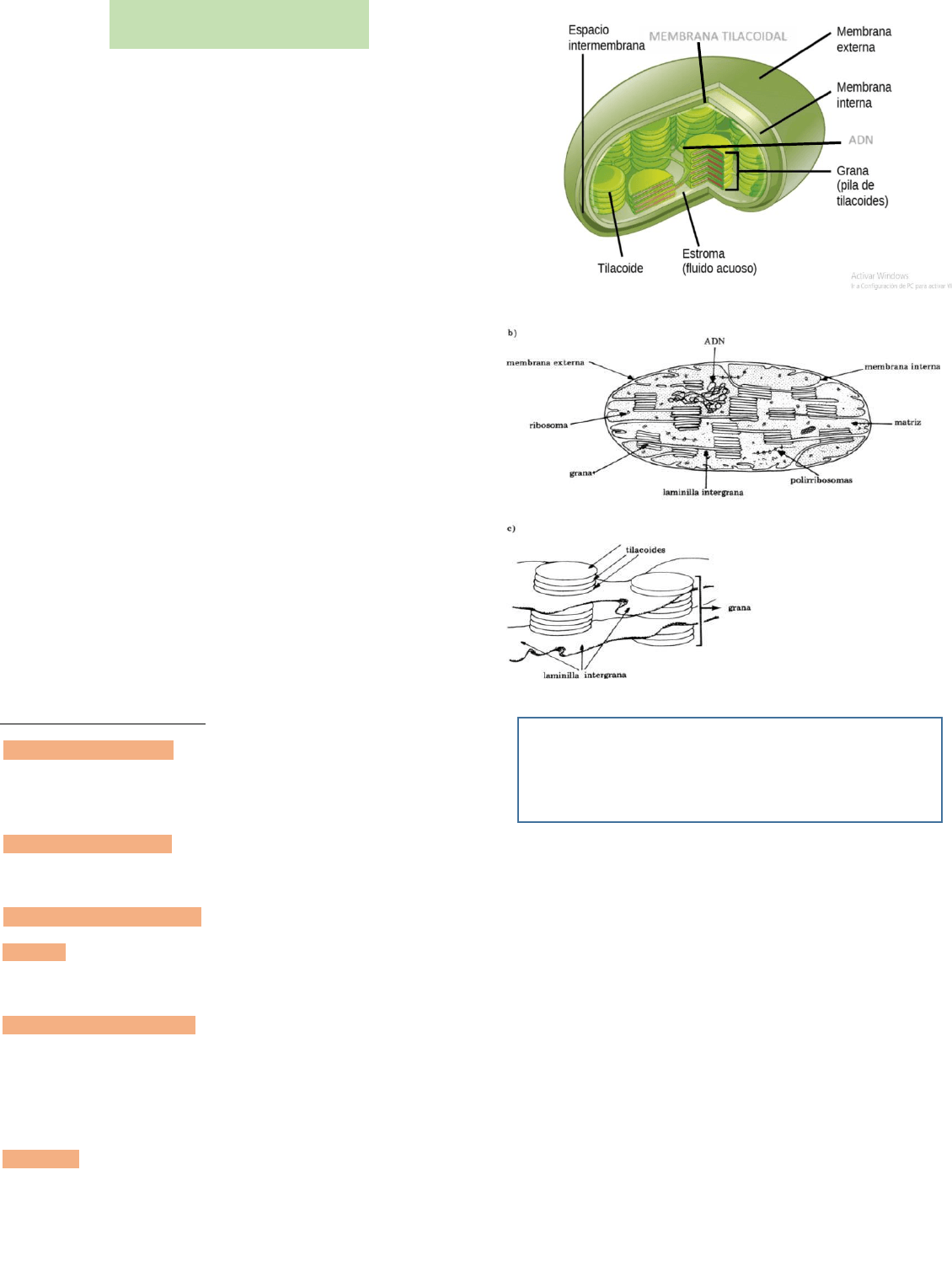
Dentro del estroma se hallan los tilacoides, que son vesículas aplanadas
dispuestas como un retículo membranoso. Su superficie externa está en
contacto con el estroma, la interna limita el espacio intratilacoide. Los
tilacoides se disponen como pilas de monedas para formar las granas, entre
las cuales se extienden laminillas intergrana formando un retículo
membranoso.
LOS CLOROPLASTOS POSEEN:
UNA MEMBRANA EXTERNA
- no presenta plegamientos - mucho más permeable a los iones, algunos
solutos pequeños y el agua - la composición de la membrana externa difiere
de la interna y de la tilacoidal. (autoevaluación)
UNA MEMBRANA INTERNA
- no presenta plegamientos - es lisa - más impermeable y posee los
transportadores para facilitar el traspaso de sustancias
UN ESPACIO INTERMEMBRANA muy delgado
CLOROPLASTOS
ESTROMA - en el estroma se encuentran proteínas solubles, el ADN y los Ribosomas (similares a los ribosomas de las procariontes)
- Los protones son bombeados desde el estroma hacia el espacio del tilacoide por el complejo de citocromos (ae)
- presenta algunas proteínas necesarias para realizar la respiración celular.
UNA MEMBRANA TILACOIDAL - se encuentra en el interior del cloroplasto (el interior del cloroplasto es llamado estroma) - se repliegan entre sí
forman los tilacoides - presenta plegamientos que forman unas estructuras llamadas tilacoides (auto evaluación) - son impermeables a los iones
(esto es muy importante para la fotosíntesis) - es impermeable a los protones (autoevaluación) - se encuentra la clorofila y también están otras
proteínas encargadas de la fotosíntesis, como la ATP sintasa, el sistema de los citocromos y la plastoquinona - presenta algunas proteínas necesarias
para realizar la respiración celular. La membrana tilacoidal responde al modelo del mosaico lipoproteico. Se encuentra en ella el 50% de los lípidos
del cloroplasto y entremezclados moléculas de clorofila, carotenoides, plastoquinonas que intervienen en la fotosíntesis.
TILACOIDES - constituyen sacos aplanados agrupados como pilas de monedas. Cada pila de tilacoides recibe el nombre de granum (plural, GRANA),
MEMBRANA TILACOIDAL
ADN
esquema de la ultraestructura al M.E.T
grana de un cloroplasto
* OTROS MIEMBROS DE LA FAMILIA DE LOS PLÁSTIDOS SON LOS
LEUCOPLASTOS, QUE SON INCOLOROS Y DENTRO DE ELLOS SE
ENCUENTRAN LOS AMILOPLASTOS QUE SON LAS CÉLULAS
ENCARGADAS DE PRODUCIR Y ALMACENAR ALMIDÓN.
Este archivo fue descargado de https://filadd.com
FILADD.COM

LA FUNCIÓN PRINCIPAL DE LOS CLOROPLASTOS ES LA FOTOSÍNTESIS
Se llevan a cabo las funciones :
-Ciclo de Calvin --------
-Fosforilación oxidativa
-síntesis de hidratos de carbono
FOTOSÍNTESIS
- Es la síntesis de compuestos orgánicos complejos a partir de compuestos inorgánicos utilizando la energía proveniente de la luz
- Por medio de la clorofila contenida en los cloroplastos, los vegetales verdes son capaces de absorber la energía que la luz solar emite como
….fotones y transformarla en energía química.
- Consiste en la combinación de CO2 y H2O para formar hidratos de carbono con liberación de O2
- Los hidratos de carbono formados por la fotosíntesis son sacáridos solubles
- Es el proceso inverso a la glucólisis y al ciclo de krebs
- El rendimiento de la fotosíntesis depende de diversos factores, como la intensidad de la luz (así como su color y el tiempo de iluminación), la
disponibilidad de agua en el suelo, la concentración de dióxido de carbono (CO2) en el aire y la temperatura ambiental.
HAY DOS ETAPAS:
1) reacciones fotoquímicas (o lumínicas)
- depende de la luz - ocurre en las granas - se obtiene ATP, NADPH y como subproducto el oxígeno
- insertos en la membrana tilacoidal están los componentes moleculares para realizar la fotosíntesis.
……………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Estos componentes se dividen en:
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………
a) fotosistema I - está en la membrana más externa de las granas - P680 es el primer nivel de energía del fotosistema 1
b) fotosistema II - se encuentra en la membrana más interna de las granas
- P700 es el fotosistema 2 que es un nivel medio de energía
- dentro de cada fotosistema se puede distinguir dos zonas: complejo (centro) antena y centro de reacción.
- El recorrido de los electrones durante la etapa fotoquímica de la fotosíntesis es: H2O ---> fotosistema II --->fotosistema I --->NADPH)
- Los electrones que circulan a través de los dos fotosistemas tiene su menor energía potencial a nivel del: NADPH
* LOS FOTOSISTEMAS POSEEN LAS PROTEÍNAS NECESARIAS PARA GENERAR NADPH Y ATP; CLOROFILAS QUE ABSORBEN LA LUZ DE LONGITUDES
DE ONDA DE 700 Y 680 NM RESPECTIVAMENTE; Y UN CENTRO ANTENA Y UN CENTRO DE REACCIÓN.
2) reacciones bioquímicas (o en la oscuridad)
- independiente de la luz (puede ocurrir en la oscuridad)
- ocurre en la estroma
- utiliza ATP y NADPH para, a través de la reducción del dióxido de carbono, formar hidratos de carbono
- a través de un ciclo de reacciones enzimáticas, conocido como ciclo de calvin, se parte de dióxido de carbono y se obtiene los intermediarios
necesarios para la síntesis de glucosa o otros hidratos de carbono, como, así también, de ácidos grasos.
- son necesarias 6 vueltas del ciclo de calvin para que se formen 12 moléculas de gliceraldehido 3-fosfato, los cuales pueden originar recién una
molécula de glucosa.
- la primera fase del ciclo de calvin se llama carboxilación, la segunda reducción y la tercera regeneración.
- Son sustratos del ciclo de Calvin CO2 + ATP + NADPH (ae)
FOTORRESPIRACIÓN
- es el mecanismo por el cual en presencia de luz y baja concentración de dióxido la enzima rubisco incorpora oxígeno en lugar de fijar los átomos
de carbono provenientes del dióxido. Por lo que todo mecanismo termina consumiendo oxígeno y generando dióxido de carbono
- En este proceso participan el cloroplasto, la mitocondria y el peroxisoma
PIGMENTOS FOTOSINTÉTICOS
- absorben la energía luminosa y se excitan (pasan a un estado
de mayor energía)
- cuando se excitan liberan la energía a través de:
emisión de calor
emisión de fluorescencia
transmisión de energía a otra molécula
transformación en energía química
Este archivo fue descargado de https://filadd.com
FILADD.COM
Similitudes entre Mitocondrias y Cloroplastos
- ambas son responsables de los procesos metabólicos para la obtención de energía
- se encuentran en el citoplasma de la célula
- son visibles al microscopio óptico
- están recubiertos por una doble membrana
- entre ambas membranas se genera el espacio intermembrana, que adquiere relevancia en los procesos metabólicos
- en su interior poseen ADN circular, ribosomas y proteínas solubles
- ambas se originaron a partir de células procariontes (teoría endosimbiótica)
- poseen cierta autonomía, ya que pueden sintetizar sus próprias proteínas y reproducirse y dividirse por fisión
binaria al igual lo hacen las bacterias
Diferencias entre mitocondrias y cloroplastos
- generalmente los cloroplastos poseen un tamaño mayor al de las mitocondrias
- las mitocondrias se encuentran en células animales y vegetales. Los cloroplastos sólo en vegetales.
- las mitocondrias poseen dos membranas. Los cloroplastos tres.
- las mitocondrias obtienen energía a partir del proceso de respiración celular (degradación de los hidratos de
carbono con la siguiente producción de dióxido de carbono y agua). Los cloroplastos a través de fotosíntesis.
- en las mitocondrias, el transporte de electrones se produce en la membrana interna. En los cloroplastos, en la
membrana tilacoidal.
- Los cloroplastos poseen pigmentos fotosintéticos, como la clorofila. Las mitocondrias carecen de los mismos.
Este archivo fue descargado de https://filadd.com
FILADD.COM
METABOLISMO
-El metabolismo (del griego “metabole”, cambio) es la totalidad de los procesos químicos de un organismo.
-El metabolismo es “el mapa de rutas” de miles de reacciones químicas que ocurren en la célula.
-Las enzimas dirigen dichas rutas metabólicas, acelerando diferencialmente reacciones determinadas.
- Es un conjunto de reacciones bioquímicas que involucran la SÍNTESIS (anabolismo) o la DEGRADACIÓN (catabolismo) de moléculas en donde
interviene la utilización y/o transformación de energía (energía es lo necesario para producir un efecto).
Como un todo, el metabolismo maneja las fuentes de materia y energía de la célula. Algunas rutas metabólicas liberan energía por ruptura de los
enlaces químicas de moléculas complejas a compuestos más simple.
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
-CATABOLISMO CELULAR o VÍAS CATABÓLICAS: Son procesos de degradación, Su función es reducir, es decir de una sustancia o molécula compleja
hacer una más simple. Son reacciones exergónicas en las que se “libera energía al medio” que se almacena en forma de ATP. SON ESPONTANEAS……
……………………………….
-VÍAS ANABÓLICAS o ANABOLISMO CELULAR: Sintetiza ATP .Son las que consumen energía para construir moléculas de mayor tamaño a partir de
moléculas más simples. Son reacciones endergónicas que “requieren un aporte de energía” que procede de la hidrólisis del ATP. NO SON ESPONTANEAS
Así, la transferencia de energía del catabolismo al anabolismo se denomina acoplamiento energético.
- Procesos metabólicos son procesos por lo cual la célula obtiene, transforma y utiliza la energía necesaria para mantenerla viva.
- Apenas los alimentos son ingeridos, los polisacaridos, lipidos y proteínas son escindidos, por acción de enzimas, en moléculas cada vez más
pequenãs, estableciendo verdaderas cadenas metabólicas.
- La escisión enzimática de los alimentos tiene lugar en tres escenarios orgánicos: el TUBO DIGESTIVO, el CITOSOL y la MITOCONDRIA.
Leyes de la termodinámica
- El universo de estudio está formado por sistema y entorno. EL SISTEMA PUEDE SER:
ABIERTO (INTERCAMBIA ENERGÍA Y MATERIA CON EL ENTORNO),
CERRADO (SÓLO INTERCAMBIA ENERGÍA CON EL ENTORNO) y
AISLADO (NO HAY INTERCAMBIO CON EL ENTORNO)
1ª LEY DE LA TERMODINAMICA
1) La energía total (H) del universo es constante. 2) La energía no puede ser creada ni destruida, sólo transformada
3) Si el sistema absorbe energía, la devuelve al entorno. Es decir, la cantidad total permanece constante.
2ª LEY DE LA TERMODINAMICA
- La entropía del universo tiende al máximo
Energía
- es única, pero se presenta de diferente formas, como cinética, térmica, etc.
- si una degradación ocurre en un paso o muchos pasos, la cantidad de energía liberada por molécula es la misma
- independientemente de la forma como la célula obtiene energía, ella la transforma en energía química, es decir, aquella que está contenida en los
enlaces o uniones entre los átomos que forman una molécula.
- La mayor parte de la energía contenida en las moléculas de los alimentos es extraída mediante una sucesión de oxidaciones, al cabo de las cuales el
oxígeno atmosférico se une al hidrógeno y al carbono liberados por esas moléculas y se forma H2O y CO2, respectivamente.
La energía química que los organismos utilizan en las reacciones metabólicas, proviene de los enlaces químicos de los glúcidos, lípidos y proteínas. Esta
energía potencial que guardan los enlaces químicos, puede ser aprovechada parcialmente por el organismo cuando se rompen esos enlaces químicos. La
energía que no puede ser atrapada por el organismo, se disipa como calor.
En condiciones experimentales controladas, puede medirse y compararse la cantidad de energía que entra y sale de un sistema determinado.
- No toda la energía es utilizada en un trabajo. La energía no utilizada se pierde en forma de calor
Energía Total = Energía Útil + Energía Disipada. 1) la energía total se conoce como H (entalpía) 2) la energía útil se conoce como G
.3) la energía disipada se conoce como T (temperatura) x S (entropía)
Reacciones - Si la reacción que ocurre espontáneamente libera energía es Exergónica, pues la variación de G (energía útil) es negativa - las reacciones que se
necesita energía se llaman Endergónica y la variación de G es positiva - cuando una reacción libera calor se llama Exotérmica y la variación de H es negativa -
cuando absorbe calor se llama Endotérmica y la variación de H es positiva. - para realizar sus funciones la célula necesita energía. Para mantener la energía
total constante, la célula necesita devolver al entorno una cantidad de energía igual. - Los procesos anabólicos son endergónicos y su delta G positivo (ae)
Estado Estacionario - Es cuando la velocidad de intercambio es igual (pero distinta de cero) en ambos sentidos. Por lo tanto las partículas siguen se moviendo y la
cantidad de moléculas es la misma. - la energía que absorben y la energía que devuelven es igual en ambos los sentidos y además distinta de cero.
EXOTERMICA: ES CUANDO UNA REACCION LIBERA CALOR . para tener (ENTALPIA)- H
ENDOTERMICA: ES CUANDO UNA REACCIÓN ABSORBE CALOR . (ENTALPIA) + H
ENERGIA LIBRE : G
Este archivo fue descargado de https://filadd.com
FILADD.COM
ENZIMAS (ENERGIA LIBRE CONSTANTE)
Todas las reacciones que se efectúan en los seres vivos son catalizadas por enzimas. Estas hacen posible que las reacciones metabólicas se
desarrollen a un ritmo razonable, compatible con la vida.
- SON CATALIZADORES BIOLÓGICOS, - Los catalizadores biológicos disminuyen la energía de activación acelerando la velocidad de la reacción
- son moléculas que aumentan la velocidad de una reacción química, participando de la misma, pero sin sufrir modificaciones permanentes.
- las enzimas disminuyen la energía de activación (que es la mínima cantidad de energía que se necesita para que ocurra una reacción química) a
través de la generación de complejos moleculares entre la enzima y el sustrato que poseen una energía de activación menor que el sustrato sólo.
- la molécula sobre la que actúa la enzima recibe el nombre de Sustrato y las que se forman se llaman Productos
- La mayoría de las enzimas son proteínas. Pero hay las ribozimas que son moléculas de ARN con actividad enzimáticas.
- Inhibidor competitivo es una sustancia que compite con el sustrato por el sitio activo de la enzima
- Inhibidor no competitivo es una sustancia que influye en la afinidad de la enzima por el sustrato sin acoplarse en el sitio activo
Una enzima puede estar formada por una sola cadena de polipéptido, consistir en subunidades múltiples o requerir de componentes no
proteicos. En general las reacciones catalizadas por enzimas se llevan a cabo a presión, temperatura y pH moderado
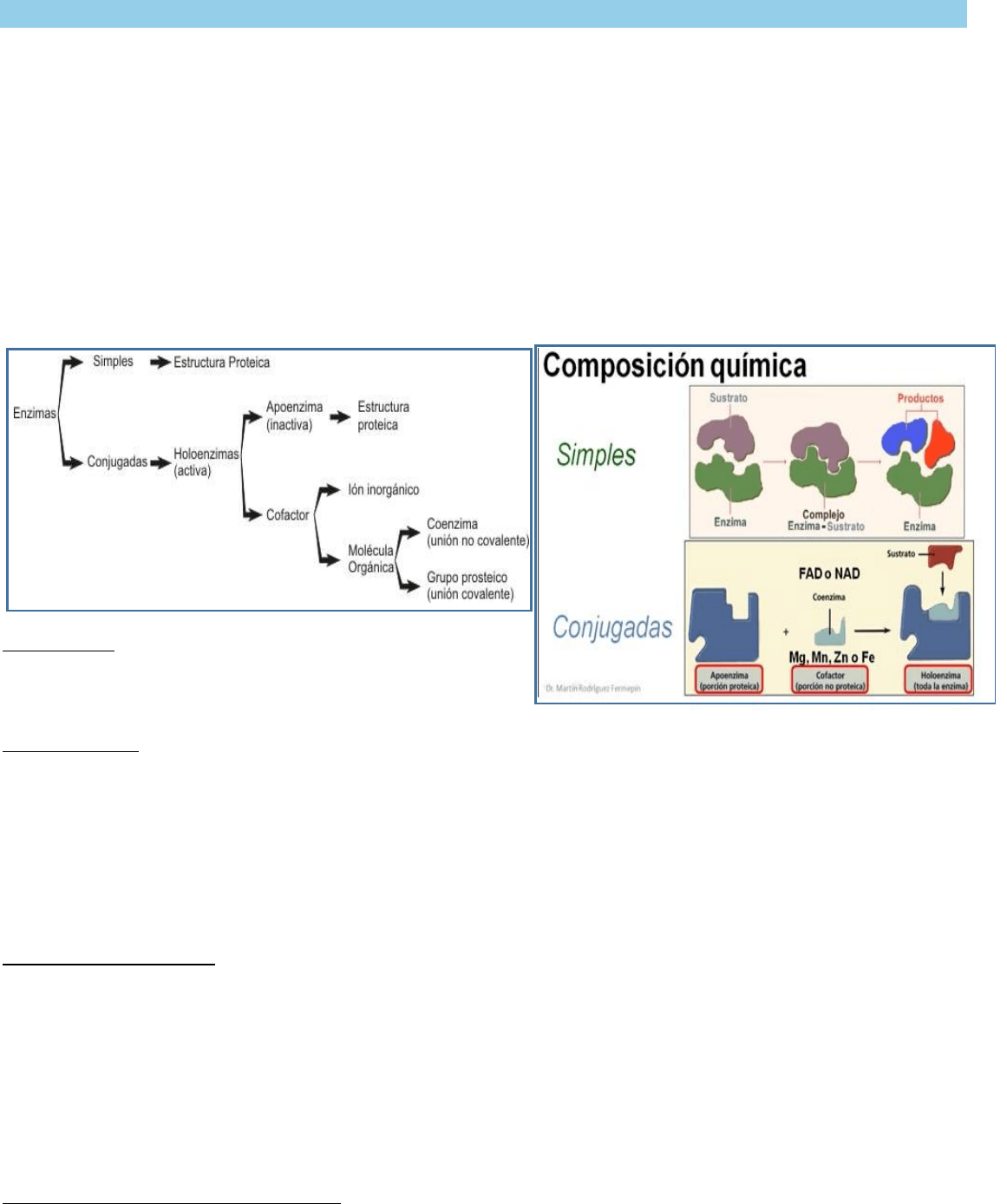
Enzimas simples: son aquellas que constan solo de una estructura proteica.
Pueden estar formadas por una o varias cadenas polipeptídicas,
cuando el sitio activo de la enzima (el sitio que reconoce el sustrato)
está en la própia proteína
Enzimas conjugadas: también llamadas holoenzimas (corresponden a la forma activa) poseen en su estructura una parte no proteica
denominada cofactor (corresponde a iones inorgánico como Mg, Mn, Zn o Fe) y una parte proteica que se denomina apoenzima.
Para que estas enzimas actúen como catalizadores es necesario que la apoenzima se una al cofactor.
El término cofactor puede aplicarse tanto a un Ión como a una molécula orgánica de naturaleza variable (grupo prostético y coenzimas).
Las coenzimas funcionan como portadores de grupos químicos pequeños como ser acetilo, metilo o bien protones y electrones.
Las coenzimas se unen no covalentemente a la apoenzima permitiendo que la holoenzima así formada lleve a cabo reacciones que la
apoenzima sola no puede efectuar. Por ejemplo, ninguna de las cadenas laterales de los aminoácidos es capaz de transportar electrones pero
cuando se agrega por ejemplo la coenzima FAD
+
,
la proteína adquiere esta función.
- si la parte no proteica corresponde a macromoléculas (como FAD o NAD) se llama coenzima
Características de las enzimas
1) Son muy específicas
2) Son altamente eficientes - se requiere baja concentración para que puedan cumplir su función
3) Son reutilizables
4) Mantienen la variación de G - al disminuir solamente la energía de activación no modifican la variación de energía libre de la reacción
5) son susceptibles de seren moduladas o reguladas por diferentes factores, como la temperatura, el pH, la concentración de Sustrato y de la propia
Enzima, y también por la presencia de inhibidores - mecanismo de regulación de la actividad enzimática:
a) Regulan la síntesis - se encuentran las moléculas que actúan en el sitio de regulación del gen específico localizado en el ADN
b) Regulan la degradación - lo hacen a través de la marcación de la enzima con ubiquitina para su posterior destrucción por los proteosomas
c) regulan la actividad catalítica - puede aumentarse o disminuirse, pero sin modificar la cantidad de enzima sintetizada
- La enzima reconoce el sustrato y interactúa con él.
- Tipo de interacción:
a) Llave y la cerradura - sitio activo y sustrato son perfectamente complementarios
b) Ajuste inducido - la unión de la enzima y el sustrato induce un cambio en el sitio activo que permite la complementariedad total entre ellos.
Este archivo fue descargado de https://filadd.com
FILADD.COM
Inhibidores irreversibles: estos inhibidores se enlazan con fuerza a la enzima, generalmente se unen covalentemente a algún aminoácido del sitio
activo. Existen algunos inhibidores que se conocen como sustrato suicida, que se enlazan al centro activo y químicamente se transforma en una especie
reactiva que modifica en forma irreversible al aminoácido del sitio activo.
Inhibidores reversibles: este tipo de inhibidores se disocian fácilmente de las enzimas, dentro de este grupo encontramos los inhibidores competitivos
y los no competitivos.
Los inhibidores competitivos: compiten con el sustrato por el sitio activo de la enzima, y si aumentamos la cantidad de sustrato, el efecto inhibidor se
revierte alcanzándose la velocidad máxima.
Los inhibidores no competitivos: se enlazan a un sitio distinto del sitio activo, de manera que el inhibidor se puede unir a la enzima libre o bien al
complejo enzima sustrato, pero en ninguno de los casos obtendremos productos. El efecto de estos inhibidores no se revierte por el agregado de mayor
cantidad de sustrato, de manera que se llega a una velocidad máxima menor que si no tuviera el inhibidor. NO AUMENTA LA ACTIVIDAD CATALITICA DE LA ENZIMA
Existen distinto tipos de mecanismos regulatorios de la actividad enzimática:
1. Inhibición por producto final: Con frecuencia las enzimas son inhibidas en forma competitiva por los productos de las reacciones que catalizan.
Esto es predecible, ya que la estructura del producto es muy similar a la del sustrato. Esta inhibición ocurre en las últimas etapas de la reacción cuando
hay una gran cantidad de producto y baja concentración de reactivo o sustrato. En la mayoría de los casos, las reacciones metabólicas no ocurren en un
solo paso, sino que son varias y encadenadas formando parte de una ruta metabólica, en donde el producto de una reacción es el sustrato de la
siguiente. Generalmente en estos casos el producto final, es decir el producto de la última reacción de esa vía, actúa inhibiendo a las enzimas que
intervienen en los primeros pasos.
2. Regulación alostérica: Este tipo de regulación ocurre solo en las enzimas alostéricas, que son enzimas que por lo general tienen estructura
cuaternaria y además del sitio activo poseen otro capaz de reconocer efectores, que se denomina sitio alostérico. Los efectores son sustancias que
pueden modular la actividad de las enzimas, algunos efectores aumentan la actividad enzimática, de modo que se conocen como efectores positivos y
otros tienen efecto inhibitorio que se denominan efectores negativos.
3. Regulación por modificación covalente: en este mecanismo algún aminoácido de la enzima se une covalentemente a algún grupo químico y de esta
forma se activa o se inactiva la enzima. El grupo que más frecuentemente interviene en este tipo de regulación es el grupo fosfato (P) y los aminoácidos
que normalmente intervienen son la serina y la treonina.
4. Regulación genética: Involucra el control a nivel del ADN. El ADN es la molécula que almacena la información para la síntesis de proteínas de acuerdo
al siguiente flujo de información.
ATP - la molécula energética por excelencia es el ATP (adenosín trifosfato)
- está formado por una adenina (base nitrogenada), una ribosa (hidrato de carbono) y un grupo fosfato
- la energía es liberada cuando los enlaces de alta energía del ATP se rompen
- Las ATPasas (SE DEGRADA Y SE SINTETIZA PERMAMENTEMENTE) son una clase de enzimas que catalizan la descomposición de ATP en ADP
(adenosín difosfato). Es decir, el ATP pierde un fosfato. Este proceso libera energía.
- Las ATP sintasas son enzimas que catalizan la síntesis de ATP (adenosín trifosfato), a partir de ADP (adenosín difosfato) y Pi (fosfato
inorgánico). Este proceso necesita energía. La energía es obtenida desde las células de su entorno. VRF - En un proceso anabólico se
Sintetiza ATP - En un proceso anabólico se utiliza ATP
ATP y ADP - El ADP se comporta como una pequeña “batería descargada”, que al cargarse por la unión de un fosfato se convierte en ATP,
la “batería cargada”
- Una vez formado, el ATP sale da la mitocondria y se difunde por la célula, de modo que su energía puede ser usada para las distintas
actividades celulares. Al removerse la energía del ATP, se reconstituye el ADP, que reingresa en las mitocondrias para recibir una nueva
“carga” de energía.
NAD+ y NADP+: (nicotinamida adenina dinucleótido y nicotinamida adenina dinucleótido fosfato). Son coenzimas que intervienen en las
reacciones de oxido-reducción, son moléculas que transportan electrones y protones. Intervienen en procesos como la respiración y la
fotosíntesis.
FAD+: También es un transportador de electrones y protones. Interviene en la respiración celular.
Coenzima A: Es una molécula que transporta grupos acetilos, interviene en la respiración celular, en la síntesis de ácidos grasos y otros
procesos metabólicos.
SON REVERSIBLES
Este archivo fue descargado de https://filadd.com
FILADD.COM

RESPIRACION CELULAR
La célula viva se asemeja a una industria química donde miles de reacciones ocurren dentro de un espacio, en este caso, un espacio
microscópico. Por ejemplo, los azúcares son convertidos en aminoácidos y viceversa. El glucógeno es ensamblado a partir de miles de
moléculas de glucosas; las proteínas a partir de aminoácidos. Por otro lado, estos polímeros serán hidrolizados cuando las necesidades
de la células así lo requieran.
- la degradación de los alimentos empieza en el tubo digestivo. Allí, los hidratos de carbono se degradan a monosacáridos (glucosa), los
lípidos se convierten en ácidos grasos y glicerol, y las proteínas en aminoácidos.
– La glucólisis es la segunda etapa de la degradación de los glúcidos (la primera empieza en el tubo digestivo). La descarboxilación
oxidativa es la tercera, el ciclo de krebs es la cuarta y la fosforilación oxidativa es la quinta. - La degradación de ácidos grasos se llama
Beta-oxidación y se lleva a cabo en las mitocondrias - En el ciclo de krebs cada acetil CoA genera un ATP, tres NADH y FADH2, y la
energía contenida en los NADH y FADH2 es transferida al ATP al cabo de la fosforilación oxidativa.
1) GLÚCIDOS - LOS GLÚCIDOS SON DEGRADADOS EN LAS SEGUINTES ETAPAS
Glucólisis - Gluco = Glucosa | lisis = rompimiento - se lleva a cabo en el citoplasma y no requiere oxígeno, es decir se degrada en
condiciones anaeróbicas - es una vía metabólica en la que se produce la lisis o degradación de la glucosa a través de numerosas
reacciones enzimáticas.
- a partir de la glucosa (que está formada por 6 átomos de carbono) se obtienen 2 moléculas de 3 átomos de carbono cuyo producto
final se llama Piruvato o ácido pirúvico.
- como resultado final de la glucólisis se obtiene: 2 PIRUVATOS + 2 [NADH + H+] + 2 ATP
- las enzimas que presentan una regulación importante en la vía glucolítica son:
HEXOQUINASA, FOSFOFRUCTOQUINASA Y LA PIRUVATO QUINASA.
……………………………………………………………………………………………………………………………………………………………………………………………………………………
- En la presencia de O2 el Piruvato puede entrar en el Ciclo de Krebs (vía aeróbica)
- Ya en la ausencia de O2, el Piruvato puede realizar la fermentación la cual, dependiendo del tipo de célula involucrada, dará como
producto final Etanol o Ácido Láctico, en lo que se conoce como vía anaeróbica.
- como los glóbulos rojos no tienen mitocondrias, obtienen energía debido a glucólisis
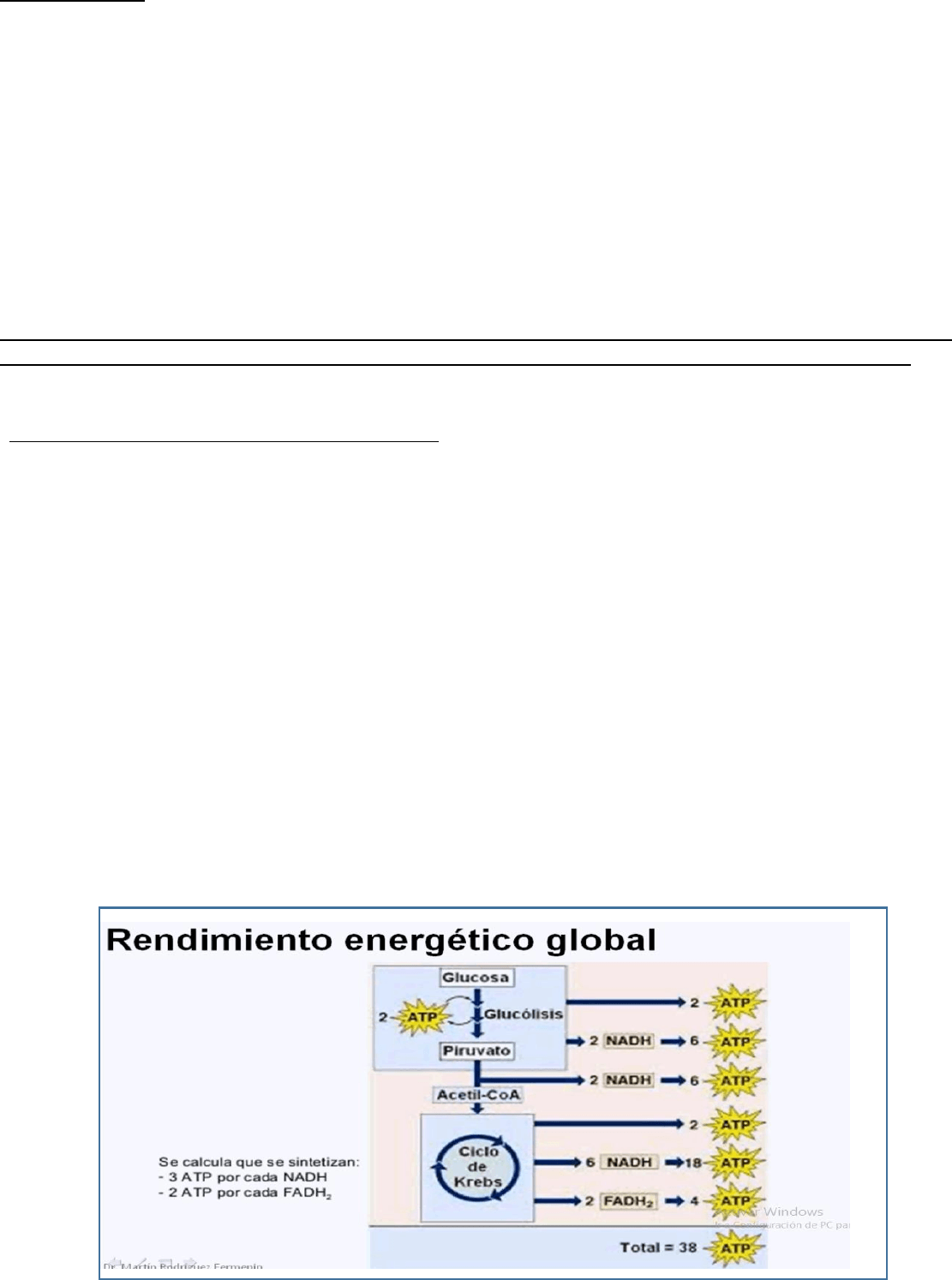
- el rendimiento global máximo de ATP que se puede obtener a partir de una molécula de glucosa es de 38 ATP.
- Durante la glucólisis, los átomos de carbono de la glucosa se oxidan al cederle electrones y protones al NAD+.
* en la Glucólisis se obtiene 4 ATP, pero el proceso consume 2 ATP. Entonces, el producto final son 2 ATP.
2) DESCARBOXILACIÓN OXIDATIVA
- Se lleva a cabo en las mitocondrias - Cada Piruvato (3 carbonos) se convierte en un Acetilo (2 carbonos).
- El Acetilo se liga a una coenzima y se convierte en Acetil CoA.
- El carbono del piruvato es removido junto con dos oxígenos, lo que produce CO2. En conjunto estas reacciones reciben el nombre de
descarboxilación oxidativa.
- La reducción del piruvato se lleva a cabo en anaerobiosis (ae)
- Durante la descarboxilación oxidativa se forma 1 NADH por cada Acetilo.
- a continuación, los átomos de carbono e hidrógeno del acetilo son oxidados y generan CO2 y H2O. Las oxidaciones liberan energía que
pasa al ATP. Las oxidaciones y formación de ATP ocurren en dos tiempos: el primero (ciclo de krebs) genera CO2 y el segundo (cadena
respiratoria) genera H2O
1. Por acción de la piruvato deshidrogenasa, cada piruvato (3C) se convierte en un acetilo(2C)
2. El acetilo se liga a la Coenzima A (CoA) con la que compone la acetil CoA.
3. El carbono del piruvato es removido junto a 2 oxigenos, lo que produce CO2
4. El piruvato cede también un hidruro (H-)
5. Se genera energía suficiente para producir un NAD+, este recibe el H- y se transforma en NADH por cada acetilo producido.
La energía almacenada en ese NADH es transferida al ATP.
Los atomos de C y H del acetilo son oxidados y se produce H2O Y CO2. Esto ocurre en dos tiempos, en el primero se genera CO2, en el
segundo H2O
Este archivo fue descargado de https://filadd.com
FILADD.COM
3) CICLO DE KREBS
- Ocurre después de la Glucólisis - se lleva a cabo en la matriz mitocondrial y en condiciones aeróbicas
- Proveniente del citosol, el piruvato ingresa en la matriz mitocondrial, donde por acción de la Piruvato deshidrogenasa pierde
un carbono y se convierte en el grupo acetilo de la Acetil CoA. Así, el Ciclo de Krebs comienza con la unión del Acetil CoA con
el Ácido Oxalacético para generar una molécula de Ácido Cítrico.
- por cada glucosa se forman 2 Piruvatos y, por lo tanto, 2 Acetil CoA. Cada acetil genera 1 ATP, 3 NADH y 1 FADH2, por lo
que al cabo de las dos vueltas que se necesitan para metabolizar a los dos acetilos surgen 2 ATP + 6 [NADH + H+] + 2 [FADH2]
- recibe el nombre de ciclo porque comienza con la unión del Acetil CoA a una molécula de Oxaloacetato y termina con la
Oxaloacetato que puede unirse nuevamente a la Acetil CoA y continuar con el ciclo
- cada vuelta completa consta de 7 reacciones enzimáticas - Las enzimas del complejo piruvato deshidrogenasa son las
enzimas responsables del ciclo de krebs y de la beta-oxidación. - El ciclo de Krebs depende del oxígeno debido a los
metabolitos que allí se requieren, aunque el oxígeno no participe directamente en el ciclo.
Es el primer tiempo, de la energía liberada una pequeña fracción se utiliza para generar ATP de forma directa, pero la mayor
parte es utilizada para reducir tres NAD+ que se convierten en NADH y un FAD, que pasa a su estado reducido o FADH2
4)CADENA RESPIRATORIA Y FOSFORILACIÓN OXIDATIVA
- se lleva a cabo en las crestas (membrana interna) - depende de oxigeno
- Los NADH y los FADH2 son oxidados, de modo que vuelven a convertirse en NAD+ y FAD.
- Los electrones provenientes de la Glucólisis y/o Ciclo de Krebs van a circular por una serie de proteínas de la llamada Cadena
Respiratoria (o cadena transportadora de electrones). Durante el pasaje de estos electrones se van produciendo un bombeo
de moléculas de hidrógeno desde la matriz mitocondrial hasta el espacio intermembranoso, de forma que se produce un
gradiente electroquímico entre estos dos espacios. Después, estos protones vuelven a la matriz por intermedio de la
ATP Sintasa, y así se genera ATP, en un proceso llamado Fosforilación Oxidativa.
- los componentes de la cadena respiratoria se encuentran anclados y distribuidos en la membrana mitocondrial interna.
En conjunto forman un complejo multi enzimático representado pelas enzimas NADH-Q reductasa, (Q)-ubiquinona,
citocromo reductasa, citocromo c, y citocromo oxidasa.
- como producto final del traspaso de electrones de un complejo a otro, así como de la generación de protones y de la
oxidación de oxígeno, se obtiene H2O. - - cuando ambos nucleótidos son oxidados, la energía depositada en sua moléculas se
libera y es transferida al ADP, el cual, dado que se fosforila, se convierte en ATP.
- La fosforilación oxidativa consiste en la síntesis de ATP, utilizando la energía liberada del transporte de electrones de la
cadena respiratoria
La fosforilación es la adición de un grupo fosfato a cualquier otra molécula.
La fosforilación más importante para el metabolismo es la fosforilación del ADP, es decir, la adición de un grupo fosfato al
ADP para formar ATP
Este archivo fue descargado de https://filadd.com
FILADD.COM

RESUMEN DE LAS ECUACIONES DE LA FOTOSÍNTESIS
Ecuación general de las reacciones dependientes de la luz:
12 H
2
O + 12 NADP
+
+ 18 ADP + 18 P
i
6 O
2
+ 12 NADPH + 12 H
+
+ 18 ATP
Ecuación general de las reacciones independientes de la luz:
12 NADPH + 12 H
+
+ 18 ATP + 6 CO
2
C
6
H
12
O
6
+ 12 NADP
+
+ 18 ADP + 18 P
i
+ 6 H
2
O
Procediendo a la simplificación de los elementos comunes en ambos lados de las ecuaciones acopladas, se obtiene la ecuación global
simplificada de la fotosíntesis:
6 CO
2
+ 12 H
2
O C
6
H
12
O
6
+ 6 O
2
+ 6 H
2
O
RESUMEN DE LAS PRINCIPALES REACCIONES DE LA FOTOSÍNTESIS
Serie de reacciones
Resumen del proceso
Materiales necesarios
Productos finales
Reacciones dependientes de la luz
(en la membrana tilacoidal)
Se utiliza la energía de la luz solar para
dividir el agua, sintetizar ATP y reducir el
NADP
Reacciones fotoquímicas
Se energiza la clorofila, el centro de reacción
envía un electrón energizado hacia un
aceptor de electrones
Energía lumínica, pigmentos como
la clorofila
Transporte de electrones
Los electrones son transportados a lo largo
de una cadena de aceptores de electrones
en las membranas tilacoidales; los
electrones , reducen el NADP
+
, la división del
agua genera H
+
, que se acumulan dentro de
los tilacoides.
Electrones, NADP
+
, H
2
.
NADPH + H
+
+ O
2
; H
+
Quimiósmosis
Se bombea H
+
a través de la membrana
tilacoidad, formando un gradiente de
protones; esos protones regresan a través
de los conductos especiales de la membrana
formados por el complejo proteínico CF
0
-
CF
1
; se produce ATP.
Un gradiente protónico y un
potencial de membrana; ADP +
P
i
(fosfato inorgánico)
ATP
Reacciones independientes de la
luz (en el estroma)
Fijación de CO
2
. El CO
2
se combina con un
compuesto orgánico
Ribulosa bifosfato, CO
2
, ATP,
NADPH + H
+
La teoría quimiosmótica explica: 1)La relación existente entre el gradiente de protones y la síntesis de ATP.
2). La síntesis de ATP en mitocondrias y cloroplastos.
3). La relación existente entre el transporte de electrones y el bombeo de protones.
Este archivo fue descargado de https://filadd.com
FILADD.COM

La comunicación intercelular y la transmisión intracelular de señales
- la Comunicación Celular es la capacidad de las células de intercambiar información fisicoquímica con el medio ambiente y con otras células - la
comunicación celular es un mecanismo homeostático porque tiene como objetivo mantener las condiciones fisicoquímicas internas adecuadas
para la vida de la célula frente a los cambios externos. - Los organismos unicelulares reciben sinal del medio, por ejemplo de otras células para la
reproducción. - los pluricelulares se comunican para coordinar el trabajo en conjunto. - En los organismos multicelulares complejos tanto la
supervivencia de las células como las actividades que éstas realizan dependen de estímulos externos provenientes de otras células.
La comunicación celular permite a la célula realizar tareas de: 1) Supervivencia o Muerte Celular 2) Diferenciación 3) Multiplicación (proliferación)
4) Degradación o síntesis de sustancias 5) secreción 6) incorporación de solutos o macromoléculas 7) contracción 8) movimiento (movilización) 9)
conducción de estímulos eléctricos
Etapas en el proceso de comunicación celular 1) síntesis de la señal por la célula emisora 2) secreción de la señal por la célula emisora 3)
transporte de la señal a la célula diana 4) reconocimiento de la señal por el receptor de la célula diana 5) transmisión intracelular de la señal
(transducción de señal) 6) respuesta (cambios en el status celular) 7) terminación de la respuesta (degradación de la señal)
Inducción
En la mayoría de los organismos superiores existen dos métodos fundamentales de comunicación intercelular: un sistema fundado en las
neuronas o células nerviosas y otro basado en las hormonas. En ambos sistemas las células se comunican entre si a través de mensajeros
químicos.
Las neuronas envían mensajes a sus células efectoras (células blanco), que pueden ser células musculares, células glandulares u otras neuronas.
Para enviar su mensaje, la neurona libera una sustancia química, un neurotransmisor. El neurotransmisor es liberado en sitios específicos
llamados sinapsis
[1] . Las moléculas de neurotransmisor se unen a receptores, situados en la superficie de la célula blanco, y provocan de esta
forma cambios físicos y químicos en la membrana celular y en el interior celular.
Por lo tanto diremos que en general, la acción de estimular a las células desde el exterior se llama inducción y se realiza a través de sustancias
producidas por células inductoras. La célula que es sensible al inductor se denomina célula inducida, blanco o diana y presenta para el
mismo receptores específicos (fig. 7.1), que pueden ubicarse en la membrana plasmática, el citoplasma o en el núcleo. Estos receptores son
proteínas o complejos proteicos. Tipos de inducciones
1. Endocrina: una glándula libera hormonas (inductor) que pueden actuar sobre células u órganos situados en cualquier lugar del cuerpo
(células blanco). Por lo tanto podemos decir que células inductoras e inducidas se encuentran distantes.
Las glándulas endocrinas liberan hormonas al torrente sanguíneo: las células o tejidos blanco poseen receptores que reconocen exclusivamente
los diferentes tipos de moléculas hormonales. Así un receptor reconoce exclusivamente una hormona. Una célula puede tener distintos tipos de
receptores, y así reconocer diferentes hormonas. Ej. Insulina, glucagón, hormonas adenohipofisiarias, etc. Cuando la célula inductora y la célula
blanco se hallan distantes entre sí, la sustancia inductora ingresa en la sangre y a través de ella alcanza a la célula inducida - en este caso, las
sustancias inductoras se denominan hormonas. - A esta categoría pertenecen también las secreciones neuroendocrinas
2. Paracrina: Una célula o un grupo de ellas liberan una hormona que actúa sobre las células adyacente que presenten el receptor adecuado.
De esta forma la célula inductora e inducida se encuentran próximas. Ej. Prostaglandinas
- Cuando la célula inductora se halla cerca de la célula inducida - la sustancia inductora recorre un corto trecho de la matriz extracelular para
alcanzar a la célula blanco
3. Autocrina: Una célula libera una hormona que actúa sobre la misma célula. Ej. Prostaglandinas
la sustancia inductora es secretada y recibida por la propia célula
4. Neuroendocrina: Una neurona libera su neurosecreción al torrente sanguíneo. Ej. Oxitocina, ADH, hormonas liberadoras e inhibidoras
hipotalámicas
5. Por contacto directo: La hormona o molécula inductora es retenida en la membrana plasmática de la célula inductora, por lo tanto no se
secreta. Las células deben ponerse en contacto, para que la sustancia inductora tome contacto con el receptor localizado en la membrana
plasmática de la célula inducida. Ejemplo de este tipo de comunicación tienen lugar en algunas respuestas inmunológicas. la sustancia inductora
es retenida en la membrana plasmática de la célula inductora y no se secreta. Por lo tanto, para que la sustancia inductora pueda entrar en
contacto con el receptor se necesita que la célula inductora se traslade hasta el lugar de la célula inducida
6. Yuxtacrina ( a través de uniones comunicantes, nexus o gap: Las células conectadas a través del establecimiento de este tipo de uniones
firmes, puede responder de forma coordinada ante un inductor que se une a alguna de las células que están comunicadas. A través de estas
uniones pasan pequeñas moléculas como los segundos mensajeros.
Especificidad - Cada sustancia inductora actúa sobre ciertas células (especificidad) - La especificidad de las sustancias inductoras se corresponde con la
especificidad de los receptores, que son moléculas o asociaciones moleculares (generalmente glicoproteína)
Este archivo fue descargado de https://filadd.com
FILADD.COM

Características del complejo inductor- receptor
Cuando una hormona pasa a la circulación sanguínea, puede alcanzar todos los tejidos del cuerpo, sin embargo, por lo general su acción
sólo se evidencia en un limitado número de células. Como señaláramos, el receptor es por lo general un complejo proteico específico al
que cada inductor se une selectivamente, de este modo la sustancia inductora y su receptor forman un complejo que presenta las
siguientes características:
a) Adaptación inducida - la fijación de la sustancia inductora al receptor requiere una adaptación estructural recíproca entre ambas
moléculas
b) Saturabilidad - El número de receptores existente en cada célula es limitado un eventual aumento en las concentraciones del
inductor, pondría en evidencia la saturabilidad del sistema.
c) Reversibilidad - La unión sustancia inductora-receptor es reversible, ya que el complejo se separa un tiempo después de su formación -
el receptor puede unirse a otras moléculas de ligando. El complejo inductor-receptor se disocia después de su formación.
* El complejo ligando receptor es específica, reversible y saturable
La interacción inductor-receptor es la primera de una serie de reacciones consecutivas
que se propagan por el interior de la célula, mientras que el último eslabón de esta serie puede considerarse cómo la respuesta.
Como ya lo adelantáramos y de acuerdo a la ubicación de los receptores específico, los inductores se pueden clasificar en dos grupos: a)
los que se unen a receptores de membrana y b) los que ingresan a la célula y se unen a receptores citosólico.
A su vez las moléculas que actúan como hormonas pueden clasificarse de acuerdo a su estructura química en cuatro categorías:
1. Esteroides: Las hormonas esteroides son derivados del colesterol. Ejemplos de las hormonas esteroides son los glucocorticoides, los
mineralocorticoides, los esteroides sexuales, la vitamina D y el ácido retinoico.
2. Derivados de aminoácidos: hormonas derivadas del aminoácido tirosina. Conocidas como aminohormonas. Existen dos tipos de
aminohormonas las que interactúan con receptores de membrana (adrenalina y noradrenalina, producidas por la glándula suprarrenal) y
las que se unen a receptores citosólicos (por ejemplo, la hormona tiroidea producida por la glándula tiroides).
3. Péptidos o proteínas: Son cadenas de aminoácidos. Ejemplos de hormonas peptídicas son la oxitocina y la hormona antidiurética.
Ejemplos de hormonas proteicas son la Insulina y la hormona del crecimiento. Estas proteínas y otros factores de crecimiento son
mitógenos potentes. (es decir activan la mitosis).
4. Derivados de ácidos grasos: Las prostaglandinas y las hormonas juveniles de los insectos son hormonas derivadas de ácidos grasos.
Debemos recordar que estas moléculas son mensajeros químicos, cuya función es coordinar las respuestas de las distintas poblaciones
celulares en un organismo pluricelular. Sin embargo, estos mensajeros químicos no actúan de la misma forma. Por ejemplo las hormonas
peptídicas y proteicas debido a su tamaño y polaridad, no pueden atravesar la membrana plasmática y deben unirse a receptores
dispersos en la superficie externa de la célula. Estos son los llamados receptores de membrana, que en general son glicoproteicos. Los
receptores de membrana detectan la llegada de una hormona y activan una ruta de transmisión de señales intracelular, que en ultima
instancia regula los procesos celulares. Por lo tanto en este caso podemos decir, que la membrana plasmática celular constituye una
barrera que se opone al flujo de información. En la membrana plasmática se alojan mecanismos que transducen las señales externas, en
otras internas, responsables últimos de la regulación de las funciones celulares. En general vamos a denominar a las señales externas
(hormonas), como primeros mensajeros, y a las señales internas como segundos mensajeros. El proceso de generar los segundos
mensajeros, depende de una serie de proteínas de la membrana celular. Los segundos mensajeros son en general moléculas de pequeño
tamaño, cuya rápida difusión permite que la señal se propague rápidamente por todo el interior celular.
El otro tipo de señales extracelulares (inductores) son las hormonas esteroideas y las hormonas tiroideas, que por su naturaleza
hidrofóbica (liposoluble), pueden difundir a través de la membrana plasmática, e interactuar directamente con receptores que se
encuentran en el interior de la célula, por ejemplo en el citosol . Una vez que el inductor, interactua con el receptor citosólico, formando
un complejo Hormona-Receptor, este complejo ingresa al núcleo donde activan genes específicos.
representa la secuencia precisa de componentes en una respuesta celular a una hormona peptídica
Hormona unida al receptor proteína G AC proteinquinasa fosforilación de proteína
Este archivo fue descargado de https://filadd.com
FILADD.COM

Receptores Los receptores pueden estar en el citosol o en la membrana plasmática
a) Inducciones celulares mediadas por receptores citosólicos - Las hormonas esteroideas, las hormonas tiroideas, la vitamina D y el ácido
retinoico son sustancias inductoras que se unen con receptores de las células inducidas situados en el citosol - estos señales (de naturaleza
hidrofóbica) pueden atravesar la membrana plasmática por difusión e ingresar a la célula, donde se unen a un receptor específico, formando un
complejo hormona-receptor que es capaz de se translocar hasta el núcleo, unirse al ADN y modificar la transcripción de ARN Mensajero. - en
ausencia de la sustancia inductora, el receptor permanece en el citosol unido a la chaperona hsp90
b) Inducciones celulares mediadas por receptores localizados en la membrana plasmática
- las señales hidrofílicas (como neurotransmisores y factores de crecimiento) poseen en general naturaleza proteica - se unen a receptores que
se encuentran en la membrana plasmática de las células inductoras. - ponen en marcha en las células inducidas una serie de reacciones
moleculares hasta que se llega a la respuesta celular. - Entre las moléculas que intervienen en la mayoría de las vías de señales abundan las
quinasas.
Receptores membranosos y enzimas - existen receptores membranosos que al ser inducidos:
1) adquieren actividad enzimática o activan a una enzima independiente;
2) Activan a proteína G. - están formados por una proteína integral que atraviesa una sola vez la membrana - Los que adquieren actividad
enzimática pueden ser de guanilato ciclasa, de serina-treonina quinasa, de tirosina fosfatasa o de tirosina quinasa - Los que activan a una enzima
es siempre una tirosina quinasa
Tirosina Quinasa - Pertenecen a una familia de moléculas llamadas factores de crecimiento - comienza cuando se une al ligando y se forman
dímeros que activa a la proteína quinasa presentes en el receptor a las cuales pueden fosforilar a las tirosina - un ejemplo es el receptor para
insulina
Receptores acoplados a Proteína G - receptores localizados en la membrana plasmática que al ser inducidos activan a proteínas G.
- presentes sólo en eucariontes - atraviesan 7 veces a la membrana plasmática - Al ser activada, la proteína G activa o inactiva a una enzima de
la membrana plasmática o abre o cierra canales iónicos, dependiendo del tipo de Proteína G:
a) Proteína Gs - activa la enzima Adenilato Ciclasa (AC)
- Por activación conducen al aumento de la concentración citoplasmática de AMPc, con posterior activación de la PKA
b) Proteína Gi - inhibe al AC
c) Proteína Gq - activa a la enzima Fosfolipasa C (PLC)
d) Proteína Gk - activa canales de K+ (potasio)
Más acerca de la Proteína G - está localizada en la membrana plasmática, en la cara citosólica - está formada por 3 subunidades alfa, beta y
gama. - tiene actividad GTPasa, es decir, puede degradar a un nucleótido trifosfatado que es el GTP - La subunidad alfa posee actividad GTPasa
(ae) - en su forma inactiva está unida GDP - la proteína G se activa cuando el GDP es reemplazado por un GTP
- La activación de la proteína G se produce cuando la sustancia inductora se une al receptor, pues éste se pone en contacto con la subunidad alfa
y hace que su GDP sea reemplazado por un GTP. Ello permite que se separe de las subunidades beta y gama, que en forma separada (en forma
activa) pueden activar a otras enzimas, como la AC y PLC. - cuando la sustancia inductora se desliga del receptor y la transmisión de la señal
concluye, la proteína G se inactiva debido a que la GTPasa de la subunidad alfa hidroliza el GTP a GDP y P - como la proteína GTPasa degrada el
GTP, queda unida al GDP y se vuelve a inactivar y así se finaliza la respuesta.
Transducción de Señal - la unión de una molécula señalizadora (o ligando) a sus receptores específicos desencadena una serie de reacciones en
el interior de la célula. Esto proceso se conoce como Transducción de Señal.
- los mediadores esenciales de este proceso son los llamados mensajeros intracelulares o segundo mensajeros (la llegada de la sustancia
inductora es considerada el primer mensajero).
- los segundos mensajeros son moléculas que transduce señales extracelulares corriente abajo la célula hasta inducir un cambio fisiológico en un
receptor (o efector), como puede ser por ejemplo una enzima metabólica, una proteína reguladora de genes o una proteína del citoesqueleto
- ejemplos de segundo mensajero: cAMP, DAG, IP3, Ca2+
- el producto final desencadenará, entonces, una respuesta que llevará a un cambio en la fisiología celular, como cambios en el metabolismo, en
la expresión de genes o en la forma celular.
Amplificación de la señal - las cascadas de reacciones producidas por distintas enzimas que se activan por proteínas G unidas a receptores de
membranas pueden ser amplificadas
Este archivo fue descargado de https://filadd.com
FILADD.COM
Muerte Celular
- La muerte de las células es un fenómeno común durante el desarrollo embrionario, necesario para remover tejidos provisorios (por ejemplo,
las membranas interdigitales durante la formación de los dedos), eliminar células superfluas (como ocurre con casi la mitad de las neuronas en
el curso de la neurogénesis), generar conductos, formar orificios, etc - También se producen muertes celulares durante la vida posnatal,
cuando el organismo necesita remodelar tejidos o remover células dañadas, innecesarias, redundantes, envejecidas o peligrosas para su salud,
como lo son las células infectadas, las tumorales o las autorreactivas
- la comunicación celular es un proceso homeostático que permite el equilibrio de la célula frente a cambios externos. Estos cambios pueden
hacer la célula adaptarse. Cuando no se adaptan o fallan los mecanismo de adaptación, ocurre una lesión celular, que puede ser reversible o
irreversible. - Cuando la lesión es reversible, las organelas dañadas son eliminadas por un proceso llamado autofagia, que permite la célula
volverse al equilíbrio. Autofagia - generan energía en metabolitos mediante la digestión de sus proprias organelas y macromoléculas - son
mecanismos de degradación de componentes celulares - eliminan organelas dañadas
- permite la supervivencia de células que son privadas de nutrientes o de factores de crecimiento - la autofagia forma autofagosomas, en lo
cual el contenido a se degradar se encuentra dentro de una doble membrana - los autofagosomas se fusionan con los lisosomas formando los
Autolisosomas, que son encargados de degradar a las organelas y macromoléculas
- cuando la lesión es irreversible, lleva a la muerte celular, que puede ser:
a) Apoptosis - muertes celulares programadas o fisiológicas - a diferencia de la necrosis, la apoptosis requiere energía en forma de ATP y
carece de inflamación local - es regulado por una variedad de caminos de senãlización intracelular - existen dos vías: intrínseca (o
mitocondrial) y extrínseca (o de receptores de muerte) - en ambas las vías están involucradas una familia de proteínas denominadas caspasas
b) Necrosis - muertes celulares accidentales producidas por traumatismo, sustancias tóxicas, obstrucciones vasculares, etc. - proceso con
ausencia de ATP - se caracteriza por la inducción de inflamación local. - la ruptura de los lisosomas libera las enzimas contenidas en esos,
llevando a la degradación del material genético y degradación de las membranas plasmáticas y proteínas (como el citoesqueleto)
Apoptosis x Necrosis - En la apoptosis ocurre la condensación del citoplasma y del material genético, con fragmentación del ADN y formación
de corpos apoptóticos, que son removidos por fagocitosis, lo cual no genera un proceso de inflamación local - En la necrosis ocurre una
ruptura de la membrana plasmática con liberación de contenido citoplasmático y la degradación del mismo, tanto de las proteínas, de los
lípidos y del material genético. Genera proceso de inflamación local
* Una lesión a nivel celular: Es el resultado de un estímulo nocivo, o de una falla en los mecanismos de adaptación frente a estímulos
estresantes por parte de la célula (ae)
La OXIDACIÓN en los sistemas biológicos es una deshidrogenación, es decir, la pérdida de un átomo de hidrógeno (H), o lo que es equivalente la
pérdida de un protón (H
+
) y su electrón (e
-
) correspondiente; o la ganancia de oxígeno. La enzima que cataliza la oxidación de una molécula debe
presentar una coenzima de óxido-reducción como por ejemplo NAD
+
, capaz de aceptar los hidrógenos.
La REDUCCIÓN en los sistemas biológicos es una hidrogenación, es decir, la ganancia de un átomo de hidrógeno, lo que es equivalente a la ganancia
de un protón (H
+
) más su electrón (e
-
) correspondiente, o la pérdida de oxígeno. La enzima que cataliza la reducción de una molécula debe presentar
una coenzima reducida como por ejemplo NADH, capaz de ceder hidrógenos.
La oxidación y la reducción siempre ocurren simultáneamente porque los electrones que pierde un átomo o molécula oxidados son aceptados por
otro átomo o molécula que se ha reducido en el proceso.
Este archivo fue descargado de https://filadd.com
FILADD.COM
Este documento contiene más páginas...
Descargar Completo
RESUMEN DE BIO CELULAR 2DO PARCIAL UBA XXI (1).pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.