
CAPÍTULO 38 Función renal y micción
639
tantes son conservados mientras los residuos son eliminados
en la orina. Asimismo, la composición de la orina puede variar
para preservar la homeostasis del líquido de todo el organismo
(líquido extracelular [ECF]). Esto se logra a través de muchos
mecanismos reguladores homeostásicos cuya función es modi-
ficar la cantidad de agua y solutos presentes en la orina. Desde
la pelvis renal, la orina pasa hacia la vejiga y es expulsada hacia
el exterior mediante la micción. Los riñones también son ór-
ganos endocrinos y elaboran cininas (cap. 33), así como 1,25-
dihidroxicolecalciferol (cap. 23); además, sintetizan y secretan
renina (cap. 39).
639
CAPÍTULO
38
Función renal
y micción
SECCIÓN VIII FISIOLOGÍA RENAL
OBJETIVOS
Después de revisar este capítulo, el lector será capaz de:
Describir las características morfológicas de una nefrona típica y su riego sanguíneo.
■
Definir la autorregulación y enunciar las principales teorías propuestas para explicar la au- ■
torregulación en los riñones.
Definir la tasa de filtración glomerular, describir de qué manera puede medirse y enumerar
■
los principales factores que la afectan.
Describir el control tubular del sodio ionizado (Na
■
+
) y el agua.
Describir la reabsorción tubular y la secreción de glucosa y iones potasio (K
■
+
).
Caracterizar de qué manera opera el mecanismo de contracorriente en el riñón para produ-
■
cir una orina hipertónica o hipotónica.
Enumerar las principales clases de diuréticos y sus mecanismos de acción para aumentar el
■
flujo urinario.
Describir el reflejo de micción y dibujar un cistometrograma.
■
En los riñones, se filtra un líquido parecido al plasma a través de
los capilares glomerulares hacia los túbulos renales (filtración
glomerular). A medida que este filtrado glomerular pasa por
los túbulos, se reduce su volumen y se modifica su composición
por el fenómeno de reabsorción tubular (extracción de agua y
solutos del líquido tubular) y secreción tubular (secreción de
solutos hacia el líquido tubular) para formar la orina que en-
tra en la pelvis renal. Una comparación de la composición del
plasma y una muestra de orina promedio ilustra la magnitud
de algunos de estos cambios (cuadro 38-1). Destaca el modo
en que el agua y los electrólitos así como metabolitos impor-
INTRODUCCIÓN
640
SECCIÓN VIII Fisiología renal
El glomérulo, el cual tiene un diámetro de casi 200 μm, se
forma por la invaginación de un penacho de capilares hacia el
extremo dilatado y ciego de la nefrona (cápsula de Bowman).
Los capilares reciben riego de una arteriola aferente y son
drenados por una arteriola eferente, la cual es un poco más
pequeña (fig. 38-2); a partir del glomérulo, se forma el filtra-
do. Dos capas celulares separan la sangre del filtrado glomeru-
lar en la cápsula de Bowman: el endotelio capilar y el epitelio
especializado de la cápsula. El endotelio de los capilares glo-
merulares es fenestrado y presenta poros de 70 a 90 nm de diá-
metro. El endotelio de los capilares glomerulares se encuentra
rodeado completamente por la membrana basal glomerular
junto con células especializadas llamadas podocitos. Los po-
docitos tienen múltiples seudópodos que se interdigitan (fig.
38-2) para constituir hendiduras de filtración en la pared ca-
pilar. Dichas hendiduras muestran una amplitud aproximada
de 25 nm y cada una está cerrada por una membrana delgada.
La membrana basal glomerular, o lámina basal, no contiene
espacios o poros visibles. Las células estrelladas denominadas
células del mesangio se hallan entre la lámina basal y el endo-
telio. Éstas son similares a las células llamadas pericitos, las
cuales se encuentran en las paredes de los capilares en otras
partes del cuerpo. Las células del mesangio son muy frecuen-
tes entre dos capilares adyacentes y, en estos lugares, la mem-
brana basal forma una vaina compartida por los dos capilares
(fig. 38-2). Las células del mesangio son contráctiles e inter-
vienen en la regulación de la filtración glomerular. Las células
del mesangio secretan la matriz extracelular, captan complejos
inmunitarios y participan en la evolución de las enfermedades
glomerulares.
Respecto de la función, la membrana glomerular hace posible
el paso libre de sustancias neutrales de hasta 4 nm de diámetro
y excluye casi por completo las que tienen un diámetro mayor
de 8 nm. Sin embargo, las cargas en las moléculas lo mismo
que su diámetro generan un efecto a su paso hacia la cápsula de
Bowman. El área total del endotelio de los capilares glomerula-
res a través del cual ocurre la filtración en el ser humano es de
casi 0.8 m
2
.
En la figura 38-1, se muestran las características generales de
las células que constituyen las paredes de los túbulos. No obs-
tante, existen subtipos celulares en todos los segmentos, y las
diferencias anatómicas entre ellos se correlacionan con las dife-
rencias en la función.
El túbulo contorneado proximal humano tiene una lon-
gitud de 15 mm, aproximadamente y 55 μm de diámetro. Su
pared está constituida por una sola capa de células, las cuales
se interdigitan entre sí y se fijan por medio de uniones apicales
apretadas. Entre las bases de las células, se encuentran exten-
siones del espacio extracelular denominadas espacios interce-
lulares laterales. Los bordes luminales de las células poseen un
borde “en cepillo” estriado, formado por muchas microvello-
sidades.
El túbulo contorneado proximal se endereza y la siguiente
porción de cada nefrona corresponde al asa de Henle. La re-
gión descendente del asa y la parte proximal de la extremidad
ascendente están constituidas por células permeables delgadas.
Por otra parte, la porción gruesa de la rama ascendente (fig.
38-1) está formada por células gruesas que presentan muchas
mitocondrias. Las nefronas con glomérulos en las porciones
externas de la corteza renal poseen asas de Henle cortas (ne-
fronas corticales), en tanto aquéllas con glomérulos en la re-
ANATOMÍA FUNCIONAL
Nefrona
Cada túbulo renal individual y su glomérulo constituyen una
unidad (nefrona). El tamaño de los riñones entre las diferentes
especies es variable, lo mismo que el número de nefronas que
contiene. Cada riñón humano tiene aproximadamente 1.3 mi-
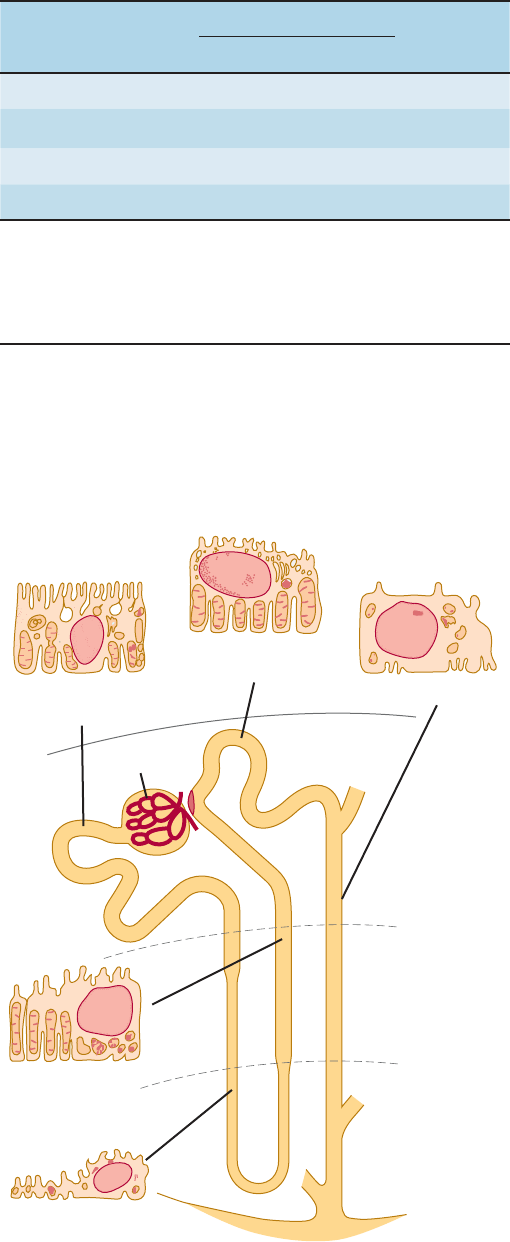
llones de nefronas. En la figura 38-1, se muestran las estructuras
específicas de la nefrona de manera esquemática.
CUADRO 381 Concentraciones urinarias y plasmáticas
típicas de algunas sustancias fisiológicamente
importantes
Concentración
Sustancia Orina (U) Plasma (P) Cociente U/P
Glucosa (mg/100 ml) 0 100 0
Na
+
(meq/L)
90 140 0.6
Urea (mg/100 ml) 900 15 60
Creatinina (mg/100 ml) 150 1 150
Túbulo contorneado
proximal
Túbulo contorneado
distal
Túbulo colector
Corteza
Médula
externa
Médula
interna
Asa de Henle,
rama descendente
Asa de Henle,
rama ascendente
gruesa
Glomérulo
FIGURA 381 Diagrama de una nefrona yuxtaglomerular. Se
muestran también las principales características histológicas de las
células que constituyen cada porción del túbulo.
CAPÍTULO 38 Función renal y micción
641
tituir túbulos colectores; éstos poseen aproximadamente 20
mm de longitud y pasan a través de la corteza renal y la médula
para desembocar en la pelvis del riñón, en los vértices de las
pirámides medulares. El epitelio de los túbulos colectores está
constituido por células principales (células P) y células inter-
caladas (células I). Las primeras, que son las predominantes,
se observan relativamente altas y presentan pocos organelos.
Ellas intervienen en la reabsorción de iones sodio y en la de
agua estimulada por la vasopresina. Las segundas, las cuales es-
tán presentes en menor número y también se encuentran en
los túbulos distales, tienen más microvellosidades, vesículas
citoplásmicas y mitocondrias. Ellas se ocupan de la secreción
de ácido y del transporte de bicarbonato (HCO
3
–
). La longitud
total de las nefronas, incluidos los túbulos colectores, fluctúa
entre 45 y 65 mm.
Las células renales que parecen tener una función secretora
no sólo son las células yuxtaglomerulares, sino también algunas
gión yuxtamedular de la corteza (nefronas yuxtamedulares)
tienen asas largas, las cuales se extienden hasta las pirámides
medulares. En el ser humano, sólo 15% de las nefronas tiene
asas largas.
El extremo grueso de la rama ascendente del asa de Henle
llega al glomérulo de la nefrona de la cual se origina el túbulo
y se aloja entre sus arteriolas aferente y eferente. Las células es-
pecializadas en el extremo forman la mácula densa, la cual está
cercana a la arteriola eferente y, sobre todo, a la aferente (fig.
38-2). La mácula, las células lacis, las circunvecinas y las células
yuxtaglomerulares secretoras de renina en la arteriola aferente
forman el aparato yuxtaglomerular (fig. 39-9).
El túbulo contorneado distal comienza en la mácula den-
sa y tiene aproximadamente 5 mm de longitud. Su epitelio es
más bajo comparado con el del túbulo proximal y, aunque es-
tán presentes algunas microvellosidades, no hay un borde “en
cepillo” distintivo. Los túbulos distales se fusionan para cons-
A
Túbulo proximal
Cápsula
Eritrocitos
Lámina basal
glomerular
Espacio de Bowman
Células
yuxtaglomerulares
Fibras nerviosas
Músculo liso
Mácula densa
Túbulo distal
Célula del
mesangio
Prolongaciones
del podocito
Arteriola
aferente
Arteriola
eferente
B
Capilar
Capilar
Capilar
Capilar
Podocito
Prolongación
del podocito
Lámina
basal
Citoplasma de la
célula endotelial
Célula del mesangio
C
Podocito
Endotelio
Endotelio
Lámina basal
Lámina basal
D
Prolongaciones
de los podocitos
Hendidura
de filtración
Espacio de
Bowman
Lámina basal
Fenestraciones
Luz capilar
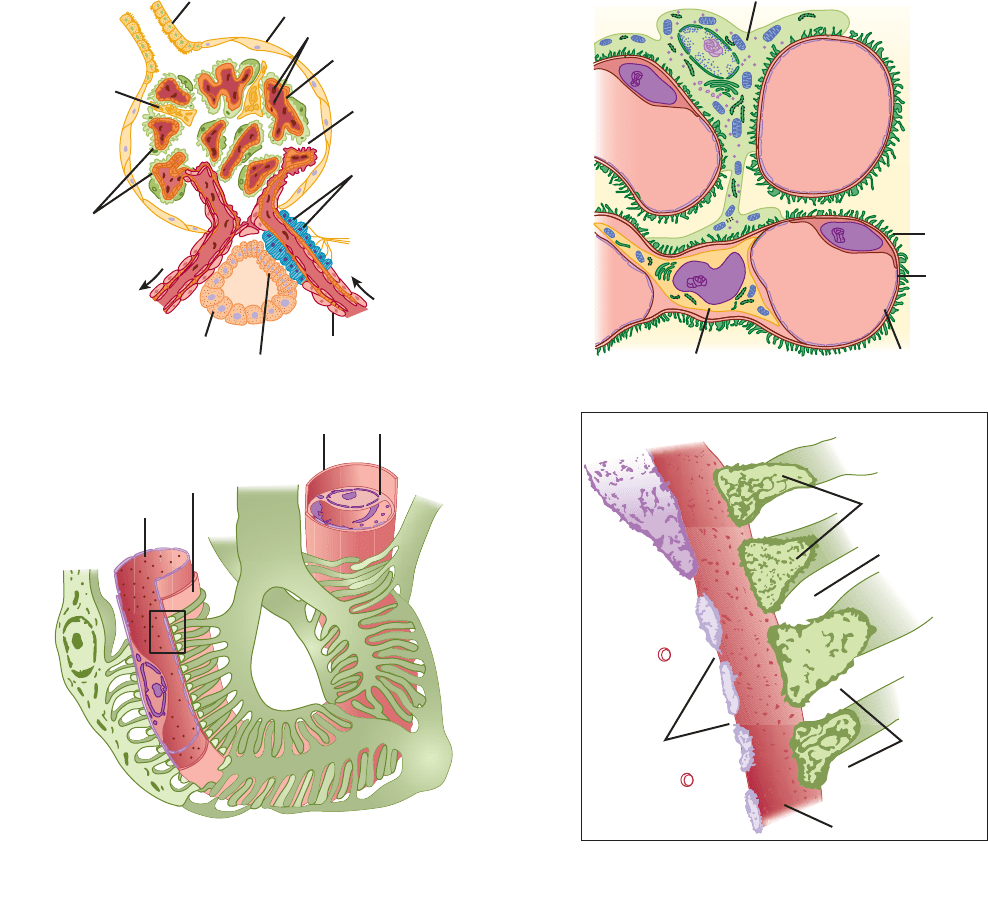
FIGURA 382 Detalles estructurales del glomérulo. A) Corte a través del polo vascular que muestra las asas capilares. B) Relación de las cé-
lulas del mesangio y los podocitos con los capilares glomerulares. C) Detalle del modo en que los podocitos forman hendiduras de filtración en la
lámina basal y la relación de la lámina con el endotelio capilar. D) Crecimiento del rectángulo en C para demostrar las prolongaciones del podocito. El
material borroso en sus superficies es polianión glomerular.
642
SECCIÓN VIII Fisiología renal
mérulo. Los capilares experimentan coalescencia para formar la
arteriola eferente, la cual, a su vez, se divide en capilares que
riegan los túbulos (capilares peritubulares) antes de drenar ha-
cia las venas interlobulillares. Por tanto, los segmentos arteriales
entre los glomérulos y los túbulos son, desde el punto de vista
técnico un sistema portal, y los capilares glomerulares consti-
tuyen los únicos capilares del organismo que drenan hacia las
arteriolas. Sin embargo, existe relativamente escaso músculo liso
en las arteriolas eferentes.
Los capilares que drenan los túbulos de las nefronas corticales
forman una red peritubular, en tanto las arteriolas eferentes de
los glomérulos yuxtamedulares drenan no sólo hacia la red peri-
tubular, sino también hacia los vasos que forman asas delgadísi-
mas (los vasos rectos). Estas asas se sumergen en las pirámides
medulares adyacentes a las asas de Henle (fig. 38-3). Los vasos
de las células del tejido intersticial de la médula renal. Ambas
se denominan células intersticiales medulares de tipo I. Éstas
contienen gotitas de lípidos y quizá secretan prostaglandinas,
sobre todo PGE
2
. La prostaglandina 2 también es generada por
las células de los túbulos colectores; la prostaciclina (PGI
2
) y
otras prostaglandinas son secretadas por las arteriolas y los glo-
mérulos.
VASOS SANGUÍNEOS
En la figura 38-3, se muestra un esquema de la circulación renal.
Las arteriolas aferentes son ramas cortas y rectas de las arterias
interlobulillares. Cada una se divide en múltiples ramas capila-
res para formar el penacho de vasos que se encuentra en el glo-
Corteza renal
Glomérulos
superficiales
Vena interlobulillar
Lecho capilar
peritubular
Vena
arqueada
Arteria
arqueada
Vasos rectos
ascendentes
Vasos rectos
descendentes
Asa de Henle
Vena
interlobulillar
Arteria
interlobulillar
Médula renal
(pirámide)
Arteriola
eferente
Arteriola
aferente
Arteria
interlobulillar
Glomérulo
yuxtamedular
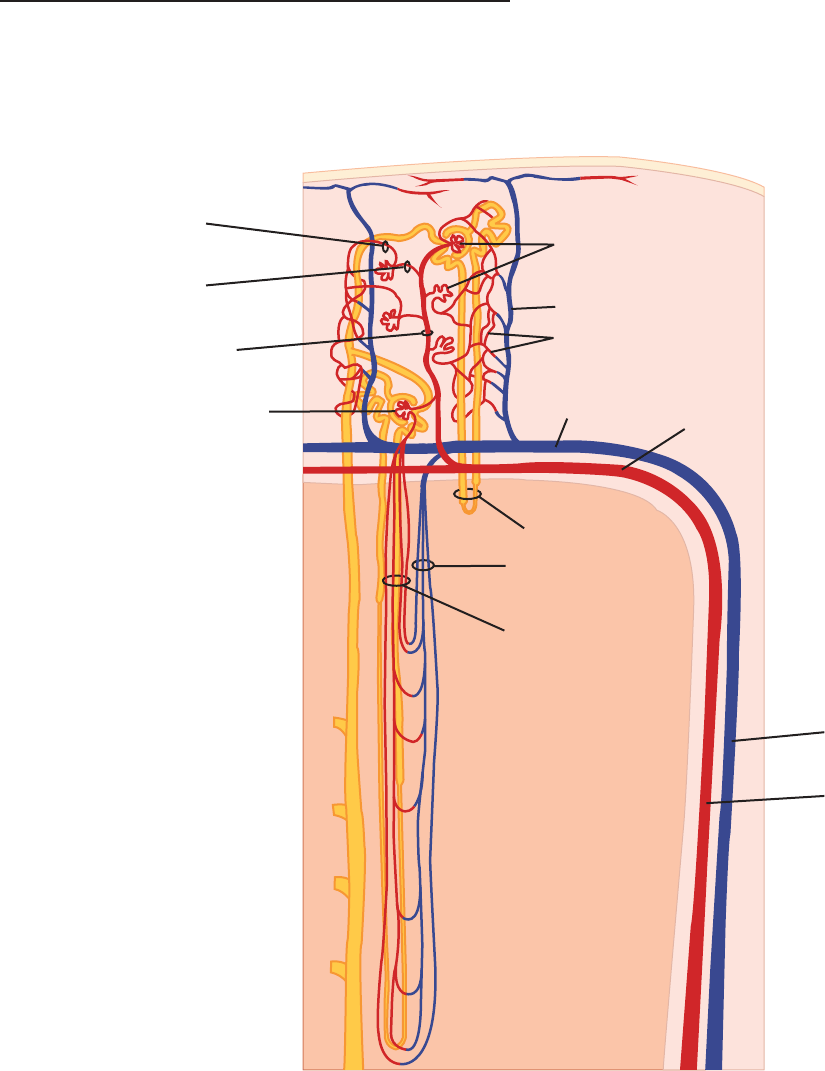
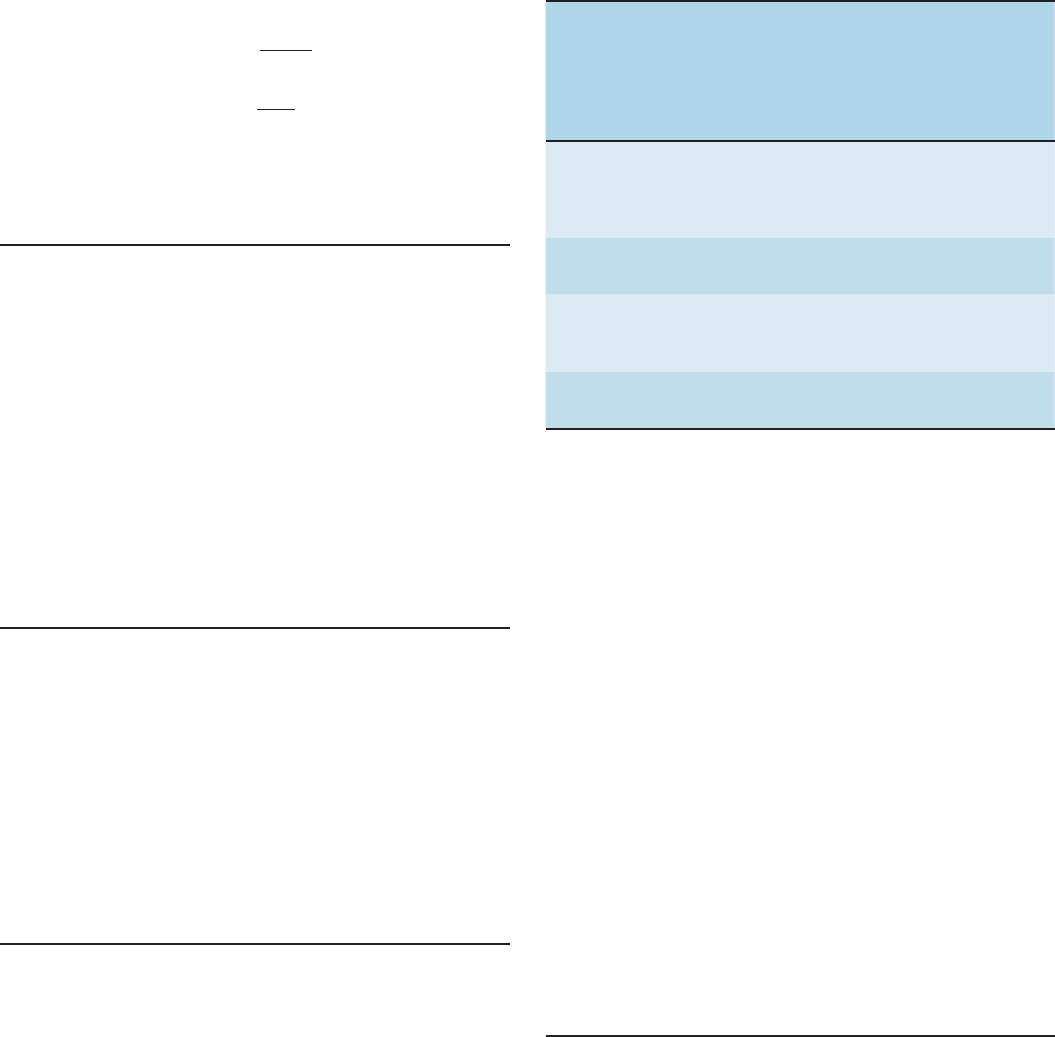
FIGURA 383 Circulación renal. Las arterias interlobulillares se dividen en arqueadas, que emiten arterias interlobulillares en la corteza. Las
arterias interlobulillares originan una arteriola aferente para cada glomérulo. La arteriola eferente de cada glomérulo se ramifica en capilares que
abastecen de sangre a los túbulos renales. La sangre venosa entra en las venas interlobulillares, la cual, a su vez, fluye por medio de las venas arquea-
das hasta las venas interlobulillares.
(Modificada de Boron WF, Boulpaep EL: Medical Physiology. Saunders, 2003.)

CAPÍTULO 38 Función renal y micción
643
sanguíneo renal puede medirse mediante flujómetros electro-
magnéticos o de otro tipo o se determina al aplicar el principio
de Fick (cap. 33) al riñón; es decir, con la cuantificación de la
cantidad de una sustancia absorbida por unidad de tiempo y al
dividir este valor por la diferencia arteriovenosa de la sustancia a
través del riñón. Dado que el riñón filtra el plasma, el flujo plas-
mático renal equivale a la cantidad de una sustancia excretada
por unidad de tiempo dividida por la diferencia arteriovenosa
renal, siempre y cuando la cantidad en los eritrocitos no se mo-
difique durante su paso a través del riñón. Cualquier sustancia
excretada puede utilizarse si se puede medir su concentración en
el plasma arterial y venoso renal, y si aquélla no es metabolizada,
almacenada o producida por el riñón y, en sí, no afecta al flujo
sanguíneo.
El flujo plasmático renal es susceptible de cuantificar me-
diante la infusión de ácido p-aminohipúrico (PAH) y al valorar
sus concentraciones en orina y plasma. El ácido p-aminohipúri-
co es filtrado por los glomérulos y secretado por las células tu-
bulares, de manera que su cociente de extracción (concentra-
ción arterial menos la concentración venosa renal dividida por
su concentración arterial) es elevada. Por ejemplo, cuando se
suministra ácido p-aminohipúrico con infusión en dosis bajas,
90% de éste en la sangre arterial es eliminado en un solo paso
a través del riñón. Por tanto, se ha vuelto un lugar común calcu-
lar el “flujo plasmático renal” al dividir la cantidad de ácido p-
aminohipúrico en la orina por la concentración plasmática del
mismo, haciendo caso omiso de la concentración en la sangre
venosa renal. Se puede utilizar el plasma venoso periférico ya
que su concentración de este ácido es esencialmente idéntica
a la que se encuentra en el plasma arterial que llega al riñón.
El valor obtenido debe llamarse flujo plasmático renal efecti-
vo (ERPF) para indicar que no se midió la concentración en el
plasma venoso renal. En seres humanos, dicho flujo promedia
alrededor de 625 ml/min.
ERPF =
U
PAH
V
·
P
PAH
= Aclaramiento de PAH (C
PAH
)
Ejemplo:
Concentración de ácido p-aminohipúrico en la orina (U
PAH
):
14 mg/ml
Flujo de orina (V
·
): 0.9 ml/min
Concentración de ácido p-aminohipúrico en el plasma (P
PAH
):
0.02 mg/ml
ERPF =
14 × 0.9
0.02
= 630 ml/min
Cabe hacer notar que el flujo plasmático renal efectivo deter-
minado de esta manera corresponde al aclaramiento del ácido
p-aminobutírico. Más adelante se describe con detalle el concep-
to del aclaramiento.
El flujo plasmático renal efectivo puede convertirse en el flujo
plasmático renal (RPF) efectivo:
Cociente de extracción de ácido p-aminobutírico promedio: 0.9
ERP
Cociente de extracción
=
630
0.9
= RPF efectivo = 700 ml/min
rectos descendentes poseen un endotelio no fenestrado, el cual
contiene un transportador facilitado para la urea y, los vasos rec-
tos ascendentes, presentan un endotelio fenestrado, compatible
con su función de conservar los solutos.
La arteriola eferente de cada glomérulo se divide en capilares
que riegan múltiples neuronas diferentes. Por ende, el túbulo de
cada nefrona no necesariamente recibe sangre sólo de la arterio-
la eferente de la misma nefrona. En seres humanos, la superficie
total de los capilares renales es casi igual al área de superficie to-
tal de los túbulos y ambas miden alrededor de 12 m
2
. El volumen
de sangre presente en los capilares renales en un determinado
momento es de 30 a 40 ml.
LINFÁTICOS
Los riñones tienen un riego linfático abundante que drena a tra-
vés del conducto torácico hacia la circulación venosa en el tórax.
CÁPSULA
La cápsula renal es delgada pero firme. Si el riñón se vuelve
edematoso, la cápsula limita el edema y aumenta la presión del
tejido (presión intersticial renal). Esto disminuye la tasa de fil-
tración glomerular y al parecer intensifica y prolonga la anuria
en la insuficiencia renal aguda.
INERVACIÓN DE LOS VASOS RENALES
Los nervios renales pasan adyacentes a los vasos sanguíneos
renales conforme entran en el riñón; contienen muchas fibras
eferentes simpáticas posganglionares y algunas fibras aferentes.
Asimismo, parece haber una inervación colinérgica a través del
nervio vago, pero es dudosa su función. La inervación pregan-
glionar simpática se deriva sobre todo de los segmentos dorsal
inferior y lumbar alto de la médula espinal, y los cuerpos celu-
lares de las neuronas posganglionares se encuentran en la cade-
na del ganglio simpático, en el ganglio mesentérico superior y a
lo largo de la arteria renal. Las fibras simpáticas se distribuyen
principalmente en las arteriolas aferente y eferente, los túbulos
proximal y distal, así como las células yuxtaglomerulares (cap.
39). Además, hay una inervación noradrenérgica densa de la
rama ascendente gruesa del asa de Henle.
Las aferentes nociceptivas que median el dolor en la nefro-
patía siguen un trayecto paralelo a las eferentes simpáticas que
ingresan a la médula espinal en las raíces dorsales de la colum-
na dorsal y lumbar superior. Otras aferentes renales al parecer
median un reflejo renorrenal por el cual un incremento de la
presión ureteral de un riñón, lleva a una disminución de la ac-
tividad del nervio eferente en el riñón contralateral; esta reduc-
ción permite un incremento en la excreción de sodio ionizado
y agua.
CIRCULACIÓN RENAL
FLUJO SANGUÍNEO
En un adulto en reposo, los riñones reciben 1.2 a 1.3 L de sangre
por minuto, o un poco menos del 25% del gasto cardiaco. El flujo
644
SECCIÓN VIII Fisiología renal
los nervios renales en el metabolismo del sodio ionizado, lo cual
en parte se debe a que casi todas las funciones renales parecen
normales en los pacientes con riñones trasplantados, y es necesario
que transcurra algún tiempo para que dichos riñones adquieran
una inervación funcional.
La potente estimulación de los riñones por los nervios nora-
drenérgicos simpáticos origina una reducción intensa del flujo
sanguíneo renal. Este efecto es mediado por los receptores adre-
nérgicos α
1
y, en menor grado, por los receptores adrenérgicos
α
2
postsinápticos. Alguna descarga tónica ocurre en los nervios
renales en reposo en animales y seres humanos. Cuando desciende
la presión arterial sistémica, la respuesta vasoconstrictora producida
por una disminución de la descarga de los nervios barorreceptores,
comprende una vasoconstricción renal. El flujo sanguíneo renal
se reduce durante el ejercicio y, en menor grado, al levantarse desde
la posición de decúbito supino.
AUTORREGULACIÓN DEL FLUJO
SANGUÍNEO RENAL
Cuando el riñón recibe un flujo sanguíneo a presiones modera-
das (90 a 220 mmHg en el perro), la resistencia vascular renal
varía con la presión de manera que el flujo sanguíneo renal es re-
lativamente constante (fig. 38-4). La autorregulación de este tipo
ocurre en estos órganos y varios factores contribuyen a ello (cap.
33). La autorregulación renal se presenta en riñones desnervados
y en los aislados sin riego sanguíneo, pero la impide la utilización
de fármacos que paralizan el músculo liso vascular. Aquélla tal
vez se produce, en parte, por una respuesta contráctil directa para
distender el músculo liso de la arteriola aferente. Quizá también
intervenga el óxido nítrico (NO). Asimismo, a presiones de per-
fusión bajas, la angiotensina II parece participar al constreñir las
arteriolas eferentes y, por tanto, al conservar la tasa de filtración
A partir del flujo plasmático renal, con el cual es posible calcu-
lar el flujo sanguíneo renal al dividir por 1, menos el hematócrito:
Hematócrito (Hct): 45%
Flujo sanguíneo renal = RPF ×
1
1‒ Hct
= 700 ×
1
0.55
= 1 273 ml/min
PRESIÓN EN LOS VASOS RENALES
Se ha medido directamente la presión de los capilares glomeru-
lares en las ratas y se ha observado que es bastante más baja que
la prevista, basándose en mediciones indirectas. Cuando la me-
dia de la presión arterial periférica tiene cifras de 100 mmHg, la
presión en los capilares glomerulares corresponde a 45 mmHg,
aproximadamente. La presión desciende a través del glomérulo
sólo 1 a 3 mmHg, pero surge un decremento adicional en la ar-
teriola eferente, de manera que la presión en los capilares peritu-
bulares es igual a cerca de 8 mmHg. La presión en la vena renal
tiene valores de cerca de 4 mmHg. Los gradientes de presión son
similares en los monos “ardilla” y probablemente en los seres
humanos, con una presión en los capilares glomerulares que co-
rresponde a casi 40% de la presión arterial periférica.
REGULACIÓN DEL FLUJO SANGUÍNEO RENAL
La noradrenalina constriñe los vasos renales y su máximo efecto
inyectada ocurre en las arterias interlobulillares y en las arterio-
las aferentes. El riñón necesita dopamina y produce vasodilata-
ción renal y natriuresis. La angiotensina II lleva a cabo su efecto
constrictor sobre las arteriolas aferente y eferente. Las prosta-
glandinas aumentan el flujo sanguíneo de la corteza renal y dis-
minuyen el flujo sanguíneo de la médula renal. La acetilcolina
también genera vasodilatación renal. Una dieta rica en proteínas
aumenta la presión de los capilares glomerulares e incrementa el
flujo sanguíneo del riñón.
FUNCIONES DE LOS NERVIOS RENALES
La estimulación de los nervios renales aumenta la secreción de
renina por una acción directa de la noradrenalina liberada en los
receptores adrenérgicos β
1
en las células yuxtaglomerulares (cap.
39) y aumenta la reabsorción de iones sodio, probablemente por
una acción directa de la noradrenalina sobre las células de los
túbulos renales. Los túbulos proximal y distal, así como la rama
ascendente gruesa del asa de Henle tienen abundante inervación.
Cuando los nervios renales son estimulados en grado creciente
en animales de experimentación, la primera respuesta es un
incremento de la sensibilidad de las células yuxtaglomerulares
(cuadro 38-2), seguido de mayor secreción de renina, luego un
aumento de la reabsorción de iones sodio y, por último, en el
umbral más alto, vasoconstricción renal con disminución de la
filtración glomerular y del flujo sanguíneo renal. Todavía no se
sabe si el efecto sobre la reabsorción de sodio es mediado por
los receptores adrenérgicos α o β y quizá sea mediado por los
dos. Tampoco se ha dilucidado la participación funcional de
CUADRO 382 Respuestas renales a la estimulación
gradual del nervio renal
Frecuencia
de
estimulación
del nervio
renal
(Hz) RSR
a
U
NA
V GFR RBF
a
0.25 Ningún efecto sobre los
valores basales; aumenta el
RSR mediado por estímulos
no neurales.
000
0.50 Aumentado sin modificación
de U
NA
V, GFR o RBF.
000
1.0 Incrementado con
disminución o ningún
cambio en GFR o RBF.
↓
00
2.50 Aumentado con disminución
de U
NA
V, GFR, y RBF.
↓↓↓
a
RSR, tasa de secreción de renina, excreción urinaria de sodio; RBF, flujo sanguíneo renal;
GFR, tasa de filtración glomerular.
Tomado de DiBona GF: Neural control of renal function: Cardiovascular implications. Hy-
pertension 1989;13:539. Con permiso de la American Heart Association.

CAPÍTULO 38 Función renal y micción
645
una sustancia que se filtre libremente a través de los glomérulos
sin ser secretada ni reabsorbida por los túbulos. La cantidad de tal
sustancia en la orina por unidad de tiempo debe proporcionarla
la filtración exacta del volumen de mililitros de plasma que con-
tenía aquella cantidad. Por ende, si se designa la sustancia con la
letra X, el filtrado glomerular equivale a la concentración de X en
la orina (U
X
) por el flujo urinario por unidad de tiempo (V
·
) divi-
didos por la concentración plasmática arterial de X (P
X
) o U
X
V
·
/
P
X
. Este valor se denomina aclaramiento de X (C
X
). Desde luego,
P
X
es igual en todas las partes de la circulación arterial y si X no
experimenta ningún metabolismo en los tejidos, la concentración
de X en el plasma de sangre venosa periférica puede sustituir a la
cifra plasmática en la sangre arterial.
SUSTANCIAS UTILIZADAS PARA MEDIR
LA TASA DE FILTRACIÓN GLOMERULAR
Además del requisito de filtrarse libre y de no ser resorbida ni
secretada en los túbulos, una sustancia apropiada para medir el
filtrado glomerular no debe ser tóxica y tampoco ha de ser me-
tabolizada por el organismo. La inulina, un polímero de fructosa
con un peso molecular de 5 200, presente en las alcachofas de Je-
rusalén (Helianthus tuberosus), satisface estos criterios en los seres
humanos y en la mayoría de los animales, y se utiliza ampliamente
para cuantificar el filtrado glomerular. En la práctica, se aplica por
vía intravenosa una dosis de carga (bolo) de inulina, seguida de
una infusión continua para mantener constante la concentración
en plasma arterial. Después que se equilibra la inulina con los lí-
quidos corporales, se obtiene una muestra de orina en un periodo
exacto y se consigue una muestra de plasma en el momento in-
termedio durante la recolección. Se evalúan las concentraciones
plasmáticas y urinarias de inulina y se calcula el aclaramiento:
U
IN
= 35 mg/ml
V
·
= 0.9 ml/min
P
IN
= 0.25 mg/ml
C
IN
=
U
IN
V
·
P
IN
=
35 × 0.9
0.25
C
IN
= 126 ml/min
En perros, gatos y conejos y en otras especies de mamíferos, el
aclaramiento de creatinina (C
Cr
) también puede utilizarse para
conocer el filtrado glomerular preciso, pero en los primates, in-
cluidos los seres humanos, los túbulos secretan algo de creatinina
y puede reabsorberse una parte de la misma. Además, las valora-
ciones de creatinina plasmática son inexactas a concentraciones
bajas de esta sustancia en virtud de que el método para evaluarla
mide pequeñas cantidades de otros complementos plasmáticos.
Pese a esto, en los pacientes a menudo se cuantifica la depuración
de creatinina endógena. Los valores coinciden muy bien con las
cifras del filtrado glomerular que se determinan con la inulina;
esto se debe a que, aun con el valor elevado de la U
Cr
V
·
como
consecuencia de la secreción tubular, la cifra para la P
Cr
también
es alta como resultado de cromógenos inespecíficos y, por tanto,
los errores tienden a neutralizarse. El aclaramiento endógeno de
creatinina es fácil de definir y constituye un índice valioso de la
función renal, pero cuando se necesitan mediciones precisas del
filtrado glomerular, no parece conveniente basarse en un méto-
do cuya precisión se debe a la compensación de errores.
glomerular. Se considera que ésta es la explicación de la insufi-
ciencia renal, la cual a veces sobreviene en los pacientes con un
flujo sanguíneo renal deficiente que son tratados con fármacos
inhibidores de la enzima convertidora de angiotensina.
FLUJO SANGUÍNEO RENAL
Y CONSUMO DE OXÍGENO
La principal función de la corteza renal es la filtración de gran-
des volúmenes de sangre a través de los glomérulos, de manera
que no es sorprendente que el flujo sanguíneo de la corteza renal
sea relativamente considerable y que se extraiga poco oxígeno
de la sangre. El flujo sanguíneo cortical asciende a casi 5 ml/g de
tejido renal por minuto (en comparación con 0.5 ml/g/min en
el cerebro) y la diferencia del oxígeno de sangre arteriovenosa
en todo el riñón es de sólo 14 ml/L de sangre, en comparación
con 62 ml/L para el cerebro y 114 ml/L para el corazón (cuadro
34-1). La P
2
de la corteza renal tiene valores de casi 50 mmHg.
Por otra parte, la conservación del gradiente osmótico en la mé-
dula renal requiere un flujo sanguíneo relativamente bajo. Por
tanto, no es de sorprender que el flujo sanguíneo sea de casi 2.5
ml/g/min en la porción externa de la médula y de 0.6 ml/g/min
en la porción interna de la médula. Sin embargo, se realiza un
trabajo metabólico, sobre todo para reabsorber sodio ionizado
en la rama ascendente gruesa del asa de Henle, de manera que
cantidades de oxígeno relativamente grandes son extraídas de la
sangre en la médula renal. La P
2
de la médula tiene cifras de casi
15 mmHg. Esto hace que la médula sea vulnerable a la hipoxia
si se reduce más el flujo sanguíneo. El óxido nítrico, las pros-
taglandinas y muchos péptidos cardiovasculares en esta región
funcionan de una manera paracrina para preservar el equilibrio
entre el flujo sanguíneo bajo y las necesidades metabólicas.
FILTRACIÓN GLOMERULAR
MEDICIÓN DE LA TASA DE FILTRACIÓN
GLOMERULAR
La tasa de filtración glomerular (GFR) puede medirse en anima-
les de experimentación y en seres humanos sin lesiones mediante
la cuantificación de la excreción y la concentración plasmática de
800
600
400
200
0
70
140 210
Presión arterial (mmHg)
Filtración glomerular
Flujo sanguíneo renal
ml/min
FIGURA 384 Autorregulación en los riñones.
646
SECCIÓN VIII Fisiología renal
La cantidad de proteína que se halla en la orina normalmente
es menor de 100 mg/día y la mayor parte de ésta no es filtrada,
sino que se deriva de las células tubulares desprendidas. La pre-
sencia de cifras importantes de albúmina en la orina se denomi-
na albuminuria. En la nefritis, las cargas negativas en la pared
glomerular están disipadas y quizás aparezca albuminuria por
este motivo, sin que ocurra un incremento del tamaño de los
“poros” de la membrana.
TAMAÑO DEL LECHO CAPILAR
Las contracciones de las células del mesangio pueden alterar el
coeficiente de ultrafiltración glomerular
y originar un decre-
mento de dicho coeficiente, lo cual se debe en gran parte a una
reducción del área disponible para la filtración. La contracción
de los puntos donde se bifurcan las asas capilares tal vez desvía
el flujo sanguíneo, alejándolo de algunas de las asas y, en otras
TASA DE FILTRACIÓN
GLOMERULAR NORMAL
La velocidad del filtrado glomerular en una persona sana de cons-
titución promedio equivale a alrededor de 125 ml/min. Esta mag-
nitud se correlaciona muy bien con el área de superficie, pero los
valores en las mujeres son 10% más bajos que los correspondientes
a los varones, inclusive después de la corrección con respecto al área
de superficie. Un valor de 125 ml/min es 7.5 L/h, o 180 L/día, en
tanto el volumen urinario normal corresponde a casi 1 L/día. Por
consiguiente, de manera normal se reabsorbe 99% o más del filtra-
do. A una velocidad de filtración glomerular de 125 ml/min, en un
día los riñones filtran un volumen de líquido equivalente a cuatro
tantos del agua corporal total, 15 tantos el volumen del líquido
extracelular y 60 tantos el volumen plasmático.
CONTROL DE LA TASA DE FILTRACIÓN
GLOMERULAR
Los factores que controlan la filtración a través de los capilares
glomerulares son los mismos que los que determinan la filtra-
ción a través de todos los demás capilares (cap. 32), es decir,
el tamaño del lecho capilar, la permeabilidad de los capilares y
los gradientes de presión hidrostática y osmótica a través de la
pared capilar. Para cada nefrona:
GFR = K
f
[(P
GC
– P
T
) – (π
GC
– π
T
)]
K
f
, coeficiente de ultrafiltración glomerular, es el producto
de la conductividad hidráulica en la pared de los capilares glo-
merulares (es decir, su permeabilidad) y el área de superficie
de filtración efectiva; P
GC
, presión hidrostática media en los
capilares glomerulares; P
T
, presión hidrostática media en el tú-
bulo (espacio de Bowman); π
GC
, presión oncótica del plasma
en los capilares glomerulares y, π
T,
presión oncótica del filtra-
do en el túbulo (espacio de Bowman).
PERMEABILIDAD
La permeabilidad de los capilares glomerulares es casi 50 veces
mayor comparada con la de los capilares en el músculo esquelé-
tico. Las sustancias neutrales con diámetros moleculares efecti-
vos menores de 4 nm son filtradas libremente, y la filtración de
las sustancias neutrales con diámetros de más de 8 nm es casi
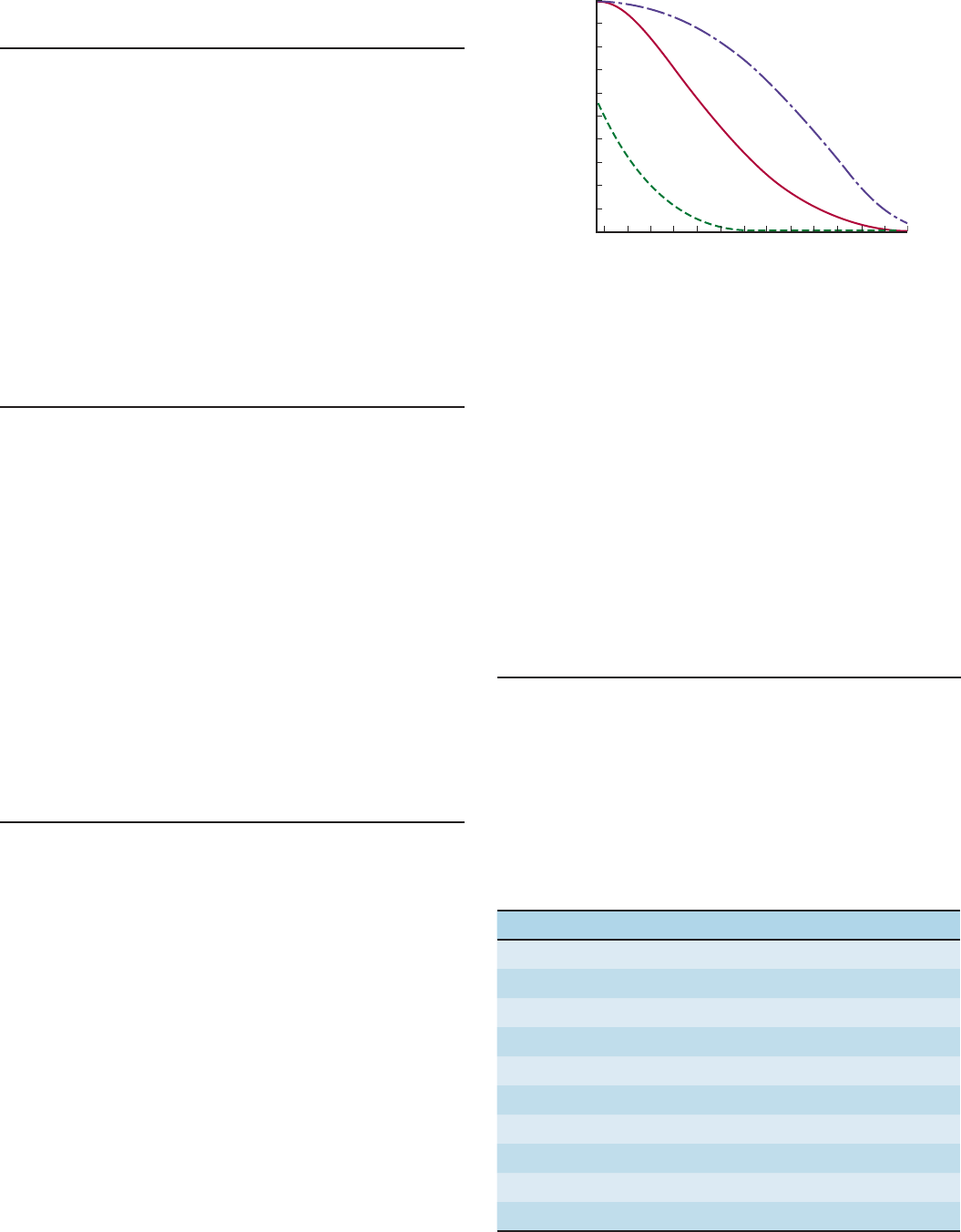
nula (fig. 38-5). Entre estos valores, la filtración es inversamente
proporcional al diámetro. Sin embargo, las sialoproteínas pre-
sentes en la pared de los capilares glomerulares tienen carga ne-
gativa y los estudios con dextranos de carga aniónica y de carga
catiónica indican que las cargas negativas repelen las sustancias
de carga negativa en la sangre, lo cual da por resultado que la
filtración de las sustancias aniónicas de 4 nm de diámetro sea
menor que la mitad de las sustancias neutrales del mismo tama-
ño. Este fenómeno probablemente explica porqué la albúmina,
la cual posee un diámetro molecular efectivo de alrededor de 7
nm, normalmente tenga una concentración glomerular de sólo
0.2% de su concentración plasmática en vez de la concentración
más elevada que cabría esperar con base sólo en el diámetro.
La albúmina presente en la circulación sanguínea muestra carga
negativa. La filtración de sustancias catiónicas es mayor en com-
paración con la de las sustancias neutrales.
1.0
0.9
0.8
0.7
0.6
0.5
0.4
0.3
0.2
0.1
0
4.0
6.0 8.0
Aniónico
Neutral
Catiónico
Diámetro molecular efectivo (nm)
Fracción de aclaramiento
FIGURA 385 Efecto de la carga eléctrica sobre la fracción de
aclaramiento de las moléculas de dextrano de diversos tamaños en
ratas. Las cargas negativas en la membrana glomerular retrasan el paso
de moléculas de carga negativa (dextrano aniónico) y facilitan el paso de
moléculas de carga positiva (dextrano catiónico).
(Con autorización de Brenner
BM, Beeuwkes R: The renal circulations. Hosp Pract [julio] 1978;13:35.)
CUADRO 383 Agentes que producen contracción
o relajación de las células del mesangio
Contracción Relajación
Endotelinas ANP
Angiotensina II Dopamina
Vasopresina PGE
2
Noradrenalina cAMP
Factor activador de plaquetas
Factor de crecimiento derivado de las plaquetas
Tromboxano A
2
PGF
2
Leucotrienos C
4
y D
4
Histamina
PGF
2
, prostaglandina F
2
; ANP, péptido natriurético auricular; PGE
2
, prostaglandina E
2
;
cAMP, monofosfato de adenosina cíclico.

CAPÍTULO 38 Función renal y micción
647
a través de los capilares glomerulares es limitado por el flujo más
que por la difusión. También es notorio que una reducción en
la velocidad de elevación de la curva de Δ producida por un au-
mento en el flujo plasmático renal aumentaría la filtración, ya
que incrementaría la distancia donde tendría lugar la filtración
a través de los capilares.
Es muy variable el alcance del equilibrio de la filtración entre
las especies, y la medición del coeficiente de ultrafiltración glo-
merular conlleva algunas incertidumbres. No está bien dilucida-
do si en el ser humano se logra un equilibrio de la filtración.
CAMBIOS EN LA TASA
DE FILTRACIÓN GLOMERULAR
Las variaciones en los factores descritos en los párrafos prece-
dentes y enumerados en el cuadro 38-4 tienen efectos previsibles
sobre el filtrado glomerular. Las modificaciones en la resistencia
de los vasos renales como consecuencia de la autorregulación
tienden a estabilizar la presión de filtración, pero cuando la pre-
sión arterial sistémica media desciende por debajo del intervalo
de autorregulación (fig. 38-4), el filtrado glomerular se reduce
súbitamente. El filtrado glomerular tiende a mantenerse cuando
la constricción de las arteriolas eferentes es mayor comparada
con la de las aferentes, pero la constricción de unas y otras dis-
minuye el flujo sanguíneo en los túbulos.
FRACCIÓN DE FILTRACIÓN
El cociente de la tasa de filtración glomerular a flujo plasmáti-
co renal, la fracción de filtración, normalmente presenta un
valor de 0.16 a 0.20. El filtrado glomerular varía menos que el
flujo plasmático renal. Cuando hay un descenso de la presión
arterial sistémica, el filtrado glomerular desciende menos que
el filtrado plasmático renal en virtud de la constricción de las
arteriolas eferentes y, por consiguiente, aumenta la fracción de
filtración.
partes, las células del mesangio contraídas se distorsionan y
comprimen la luz de los capilares. En el cuadro 38-3, se enume-
ran los fármacos que se han utilizado para afectar las células del
mesangio. La angiotensina II constituye un regulador importan-
te de la contracción del mesangio y en los glomérulos existen
receptores de angiotensina II. Además, algunas pruebas indican
que las células del mesangio sintetizan renina.
PRESIÓN HIDROSTÁTICA Y OSMÓTICA
La presión en los capilares glomerulares es más elevada si se le
compara con la de otros lechos capilares, en virtud de que las ar-
teriolas aferentes son ramas rectas y cortas de las arterias inter-
lobulillares. Asimismo, las arteriolas eferentes, vasos “corriente
abajo” de los glomérulos, muestran una resistencia relativamen-
te elevada. La presión hidrostática capilar es contrarrestada por
la presión hidrostática generada en la cápsula de Bowman; tam-
bién se neutraliza con el gradiente de presión oncótica generado
en los capilares glomerulares (π
GC
–
π
T
). En situaciones norma-
les, la presión oncótica del filtrado en el túbulo es insignificante,
y el gradiente básicamente es igual a la presión oncótica origina-
da por las proteínas plasmáticas.
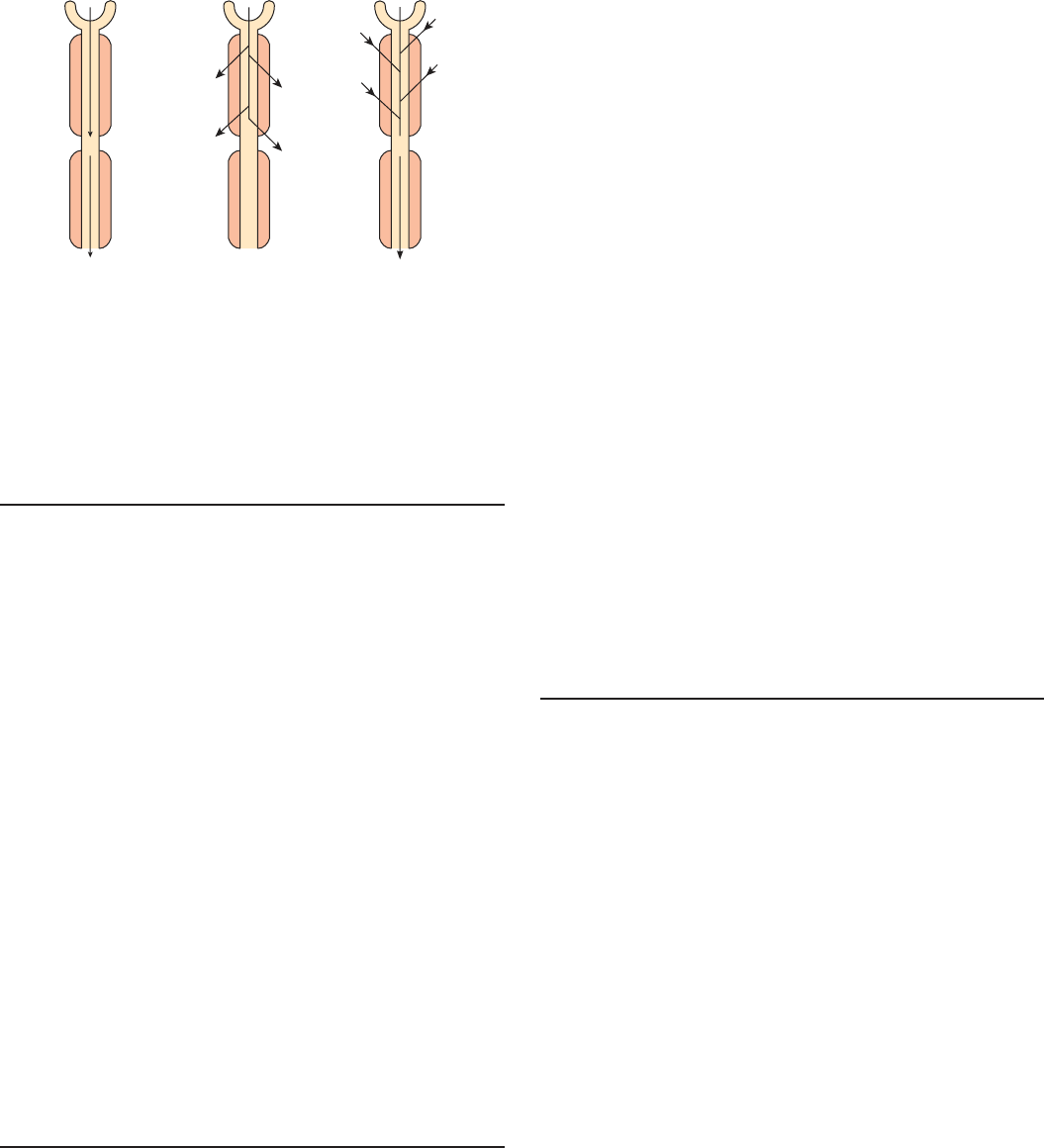
En la figura 38-6, se muestran las presiones efectivas que
se observan en un tipo de ratas. La presión de filtración neta
(P
UF
) tiene cifras 15 mmHg en el extremo aferente de los capi-
lares glomerulares, pero desciende a cero (es decir, si alcanza el
equilibrio de la filtración) proximal al extremo eferente de los
capilares glomerulares. Esto se debe a que el líquido abandona el
plasma y aumenta la presión oncótica conforme la sangre pasa a
través de los capilares glomerulares. En la figura 38-6, también
se muestra la modificación calculada en Δπ y en un capilar glo-
merular idealizado. Es evidente, asimismo, que las porciones de
los capilares glomerulares de modo normal no contribuyen a la
formación del ultrafiltrado glomerular; es decir, el intercambio
(mmHg)
Extremo aferente Extremo eferente
45
10
20
15
45
10
35
0
P
UF
= P
GC
– P
T
–
GC
P
GC
P
T
GC
P
UF
Distancia adimensional a lo largo
de un capilar glomerular idealizado
Presión (mmHg)
60
40
20
0
01
P
FIGURA 386 Presión hidrostática (P
GC
) y presión osmótica (π
GC
)
en un capilar glomerular en la rata. P
T
, presión en la cápsula de Bow-
man; P
UF
, presión de filtración neta. La presión oncótica del filtrado en el
túbulo (π
T
) normalmente es insignificante. De manera que la Δπ = π
GC
.
ΔP = P
GC
– P
T
. (Con autorización de Mercer PF, Maddox DA, Brenner BM: Current
concepts of sodium chloride and water transport by the mammalian nephron. West J
Med 1974;120:33.)
CUADRO 384 Factores que afectan al filtrado
glomerular
Cambios en el flujo sanguíneo renal
Cambios en la presión hidrostática de los capilares glomerulares
Cambios en la presión arterial sistémica
Constricción arteriolar aferente o eferente
Cambios en la presión hidrostática de la cápsula de Bowman
Obstrucción ureteral
Edema renal en el interior de la cápsula renal tensa
Cambios en la concentración de las proteínas plasmáticas:
deshidratación, hipoproteinemia (factores menores)
Cambios en el K
f
Cambios en la permeabilidad de los capilares glomerulares
Cambios en el área de superficie de filtración efectiva
K
f
, coeficiente de ultrafiltración glomerular.
648
SECCIÓN VIII Fisiología renal
Es importante advertir que las bombas y otras unidades de la
membrana luminal son diferentes a las halladas en la membrana
basolateral. Esta distribución diferente hace posible el desplaza-
miento neto de solutos a través de los epitelios.
Al igual que los sistemas de transporte en otras partes, el sis-
tema de transporte activo en los riñones tiene una tasa máxima,
o transporte máximo (Tm), a la cual pueden transportar un
soluto específico. Como consecuencia, la cantidad de un soluto
específico transportado es proporcional a su cifra presente has-
ta el transporte máximo para el soluto, pero a concentraciones
más altas, se satura el mecanismo de transporte y no se aprecia
un incremento de la cantidad transportada. Sin embargo, los
transportes máximos para algunos sistemas son considerables
y es difícil saturarlos.
Asimismo, cabe hacer notar que el epitelio tubular, al igual que el
del intestino delgado, es un epitelio poroso por cuanto las uniones
intercelulares hacen posible el paso de agua y electrólitos en cierta
medida. El grado en el cual la filtración por esta vía paracelular
contribuye al flujo neto de líquido y solutos hacia los túbulos y fue-
ra de los mismos es controvertido dado que es difícil cuantificarlo,
pero pruebas actuales parecen indicar que es un factor importante
en el túbulo proximal. Una indicación de esto es que la paracelina-1,
una proteína ubicada en las uniones intercelulares, se relaciona con
la reabsorción de iones magnesio (Mg
2+
), y una mutación con pér-
dida de función del gen para su síntesis genera una eliminación uri-
naria intensa de magnesio y calcio (Ca
2+
) ionizados.
En el cuadro 38-5, se resumen los efectos de la reabsorción
y la secreción tubular sobre las sustancias de principal interés
fisiológico.
REABSORCIÓN DE IONES SODIO
La reabsorción de iones sodio y cloruro (Cl
–
) desempeña una fun-
ción importante en la homeostasis de los electrólitos y el agua del
organismo. Además, el transporte del sodio ionizado se acopla al
movimiento de hidrogeniones (H
+
), glucosa, aminoácidos, ácidos
orgánicos, fosfato y otros electrólitos y sustancias a través de las
paredes tubulares. En el cuadro 38-6, se enumeran los principales
cotransportadores e intercambiadores que operan en las diversas
porciones de la nefrona. En los túbulos proximales, la región grue-
sa de la rama ascendente del asa de Henle, los túbulos distales y los
túbulos colectores, el ion sodio se desplaza mediante cotransporte
o intercambio desde la luz tubular hasta las células epiteliales de
los túbulos por medio de sus gradientes de concentración y eléc-
trico, y luego es bombeado activamente desde estas células hacia
el espacio intersticial. El ion sodio es bombeado hacia el intersticio
por la Na, K ATPasa activa en la membrana basolateral. Por con-
siguiente, el sodio es transportado de modo activo fuera de todas
los segmentos del túbulo renal, excepto en las porciones delgadas
del asa de Henle. En el capítulo 2, se describe con detalle la opera-
ción de la bomba de sodio ampliamente distribuida. Ésta origina
la extrusión de tres iones sodio en intercambio por dos de potasio,
los cuales son bombeados hacia el interior de la célula.
Las células tubulares de la nefrona están conectadas por unio-
nes justas en los bordes luminales, pero hay un espacio entre las
células en las áreas restantes de sus bordes laterales. Gran parte
del sodio ionizado es transportado de manera activa hacia estas
extensiones del espacio intersticial, los espacios intercelulares
laterales (fig. 38-8).
Normalmente, alrededor de 60% del sodio ionizado filtrado es
reabsorbido en el túbulo proximal, principalmente mediante el
FUNCIÓN TUBULAR
CONSIDERACIONES GENERALES
La cantidad de cualquier sustancia (X) filtrada es el producto del
filtrado glomerular y la concentración plasmática de la sustancia
(C
in
P
X
). Las células tubulares pueden añadir mayor concentración
de las sustancias al filtrado (secreción tubular), pueden retirar
parte de la sustancia o toda la sustancia del mismo (reabsorción
tubular) o pueden hacer ambas cosas. La cantidad de la sustan-
cia excretada por unidad de tiempo (U
X
V
·
) equivale a la cantidad
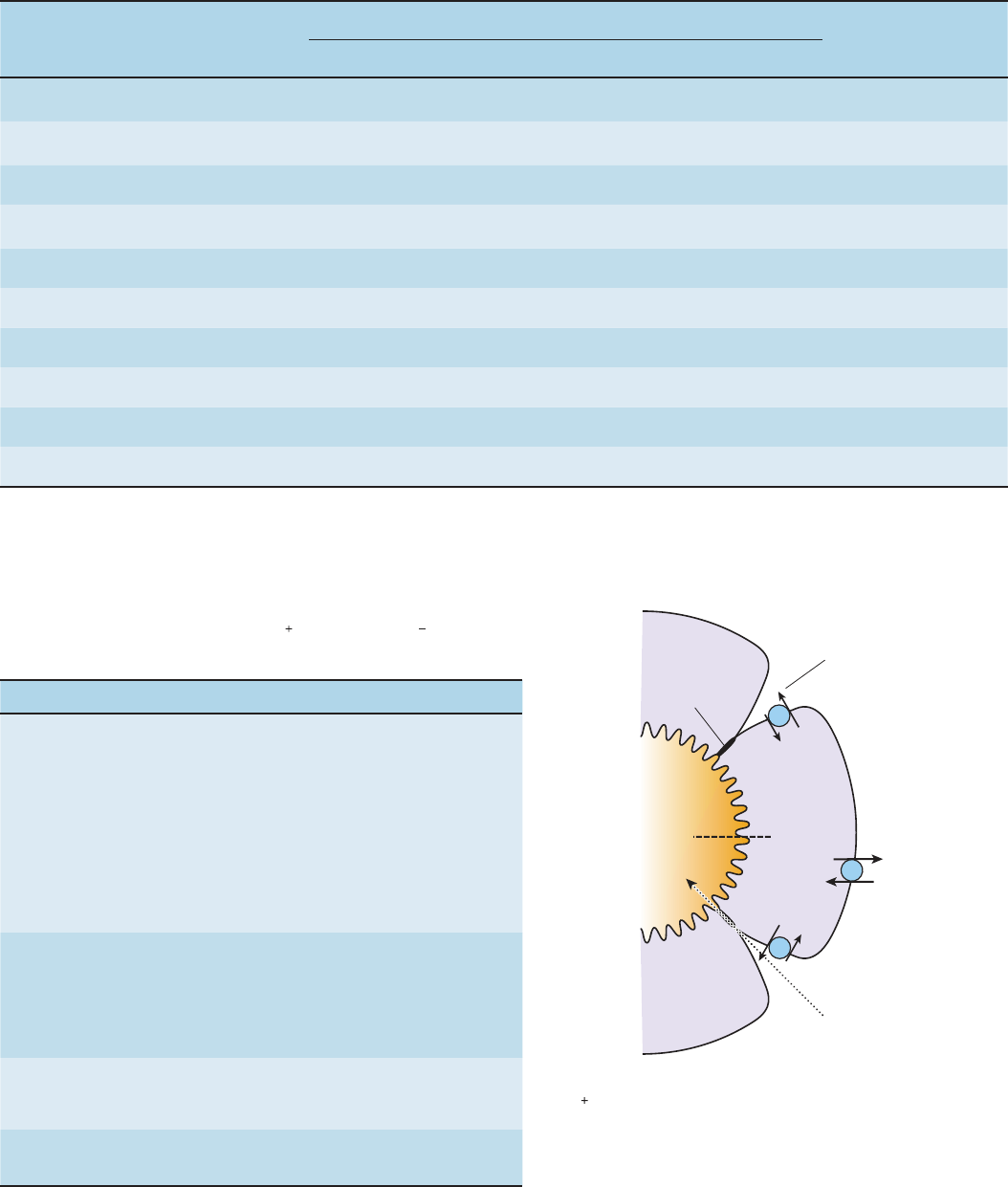
filtrada más la cantidad neta transportada por los túbulos. Esta
última cifra es indicada de manera conveniente por el símbolo
T
X
(fig. 38-7). El aclaramiento de la sustancia equivale al filtrado
glomerular cuando no se produce una secreción tubular neta o
reabsorción, y dicho aclaramiento supera a la tasa de filtración
glomerular si hay una secreción tubular neta y es menor que el
filtrado glomerular cuando ocurre una reabsorción tubular neta.
Gran parte de los conocimientos sobre la filtración glomeru-
lar y la función tubular se ha obtenido mediante el empleo de
técnicas de micropunción. Es factible insertar micropipetas en
los túbulos de riñón viviente y valorar la composición del líqui-
do tubular aspirado con el uso de técnicas microquímicas. Ade-
más, se pueden insertar dos pipetas en un túbulo e irrigarse el
túbulo in vivo. Como alternativa, es posible estudiar in vitro los
segmentos de túbulos aislados irrigados y se pueden desarrollar
células tubulares así como estudiarse en cultivo.
MECANISMOS DE REABSORCIÓN
Y SECRECIÓN TUBULARES
Las proteínas pequeñas y algunas hormonas peptídicas son reab-
sorbidas en los túbulos proximales mediante endocitosis. Otras
sustancias son secretadas o reabsorbidas en los túbulos por di-
fusión pasiva entre las células y a través de éstas por medio de
difusión facilitada a través de gradientes químicos o eléctricos o
el transporte activo en contra de tales gradientes. El movimiento
ocurre por medio de conductos iónicos, moléculas de intercam-
bio, moléculas de cotransporte y bombas. Hoy en día, se han
clonado muchas de ellas y se está estudiando su regulación.
GFR × P
X
+ T
X
= U
X
V
˙
˙
Filtrado
= GFR × P
X
Re-
absorbido
Excretado
= U
X
V
Secretado
T
X
= positivo
GFR × P
X
< U
X
V
Ejemplo: PAH
˙
T
X
= negativo
GFR × P
X
> U
X
V
Ejemplo: Glucosa
˙
˙
T
X
= 0
GFR × P
X
= U
X
V
Ejemplo: Inulina
FIGURA 387 Función tubular. Véase en el texto la explicación de
los símbolos.
CAPÍTULO 38 Función renal y micción
649
Na
+
Na
+
Na
+
, etc.
Na
+
Na
+
K
+
K
+
K
+
Luz
tubular
Unión
intercelular
Espacio
intercelular
lateral
Líquido
intersticial
Na
+
CUADRO 385 Control renal de los diversos componentes del plasma en un adulto normal
con una alimentación promedio
Sustancia
Por 24 h
Porcentaje reabsorbidoFiltrada Reabsorbida Secretada Excretada
Na
+
(meq)
26 000 25 850 150 99.4
K
+
(meq)
600 560
a
502 90 93.3
Cl
–
(meq) 18 000 17 850 150 99.2
HCO
3
–
(meq)
4 900 4 900 0 100
Urea (mmol) 870 460
b
410 53
Creatinina (mmol) 12 1
c
1
c
12
Ácido úrico (mmol) 50 49 4 5 98
Glucosa (mmol) 800 800 0 100
Solutos totales (mosm) 54 000 53 400 100 700 98.9
Agua (ml) 180 000 179 000 1 000 99.4
a
El ion potasio (K
+
)
se reabsorbe y se secreta.
b
La urea se desplaza hacia dentro y fuera de algunas porciones de la nefrona.
c
Secreción variable y probable reabsorción de la creatinina en el ser humano.
CUADRO 386 Proteínas de transporte que intervienen
en el movimiento del ion sodio
(Na ) y el cloruro (Cl ) a través
de las membranas apicales de las células tubulares renales
a
Sitio Transportador apical Función
Túbulo
proximal
CT de Na
+
/glucosa
CT de Na
+
/P
i
CT de Na
+
y
aminoácidos
CT de Na
+
/lactato
Intercambiador de Na/H
Intercambiador de Cl/
base
Captación de Na
+
, captación de
glucosa
Captación de Na
+
, captación de Pi
Captación de Na
+
, captación de
aminoácido
Captación de Na
+
, captación lactato
Captación de Na
+
, extrusión de H
+
Captación de Cl
–
Asa
ascendente
gruesa
CT de Na-K-2Cl
Intercambiador de Na/H
Conductos del K
+
Captación de Na
+
, captación de
Cl
–
, captación de K
+
Captación de Na
+
, extrusión de H
+
Extrusión de K
+
(reciclamiento)
Túbulo
contorneado
distal
CT del NaCl
Captación de Na
+
, captación de Cl
–
Túbulo
colector
Conducto del Na
+
(ENaC)
Captación de Na
+
a
La captación indica el movimiento desde la luz tubular hasta el interior de las células, la extru-
sión es el movimiento desde el interior de la célula hasta la luz tubular. CT, cotransportador; P
i
,
fosfato inorgánico.
Modificado con autorización de Schnermann JB, Sayegh EI: Kidney Physiology. Lippincott-Ra-
ven, 1998.
FIGURA 388 Mecanismo de reabsorción del ion sodio
(Na
) en el túbulo proximal. Este ion
se desplaza fuera de la luz
tubular por medio de un mecanismo de cotransporte e intercam-
bio a través de la membrana apical del túbulo (línea de rayas).
El sodio ionizado es transportado activamente hacia el líquido
intersticial por la Na, K ATPasa que opera en la membrana basola-
teral (línea continua). El ion potasio (K
+
) entra en el líquido inters-
ticial a través de los conductos de potasio. Una pequeña cantidad
de ion sodio, otros solutos y agua (H
2
O) vuelve a ingresar a la luz
tubular mediante el transporte pasivo a través de las uniones
intercelulares (líneas punteadas).
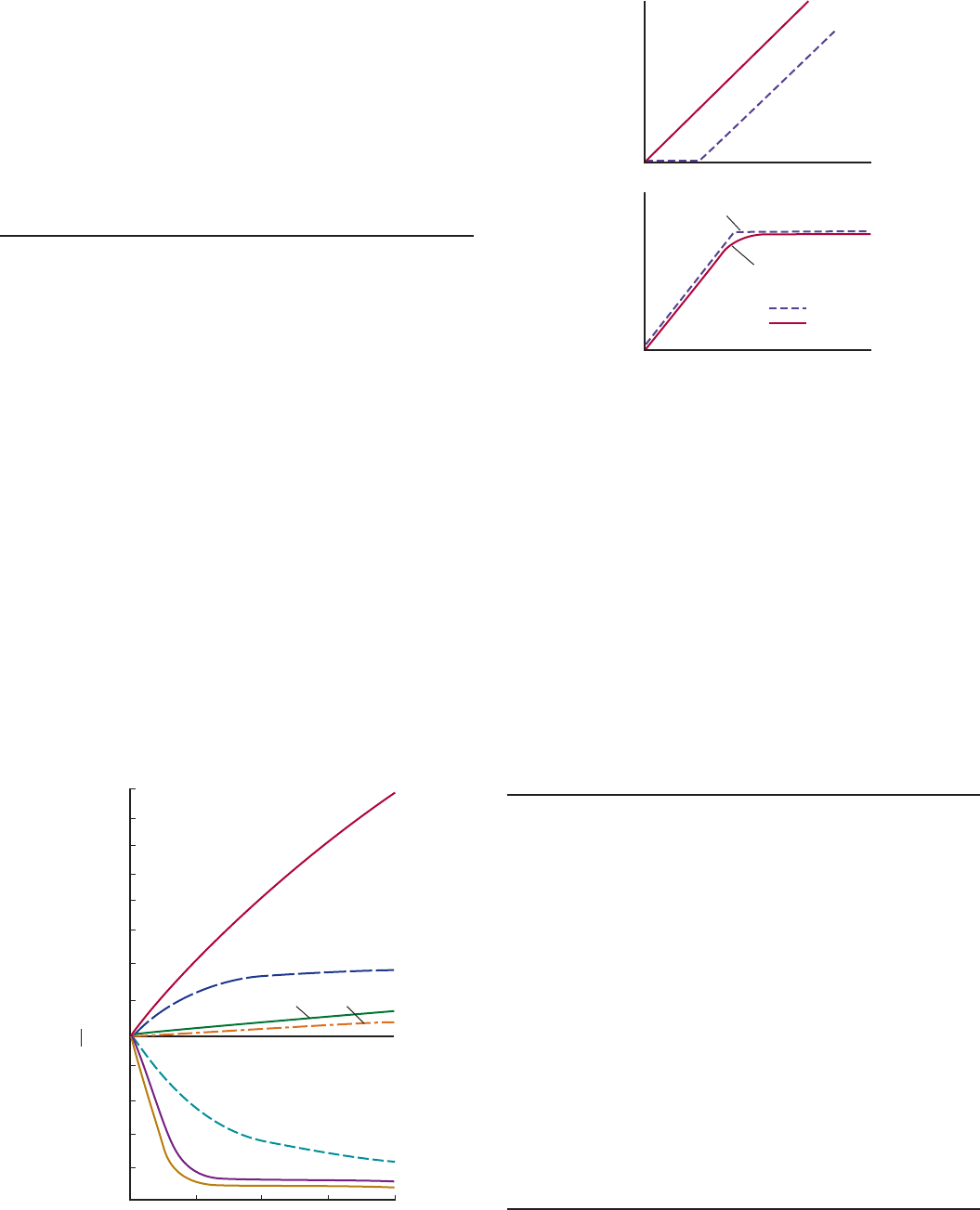
650
SECCIÓN VIII Fisiología renal
renal efectivo es menor comparado con el umbral previsto. Se
obtendría la curva “ideal” que se muestra en este diagrama si el
transporte máximo de glucosa en todos los túbulos fuese idén-
tico, y si toda la glucosa se extrajera de cada túbulo cuando el
volumen filtrado estuviese por debajo del transporte máximo de
glucosa. Esto no ocurre así y, en el ser humano, por ejemplo, la
curva real es redondeada y se desvía bastante de la curva “ideal”.
Esta desviación se denomina desbordamiento. La magnitud de
este último es inversamente proporcional a la avidez con la cual
el mecanismo de transporte fija la sustancia que transporta.
MECANISMO DE TRANSPORTE
DE LA GLUCOSA
La reabsorción de glucosa en los riñones es similar a la de glucosa
en el intestino (cap. 27). La glucosa y el sodio ionizado se unen
al transportador de glucosa dependiente de sodio (SGLT) 2 en la
membrana apical, y la glucosa es transportada hacia la célula a
medida que el ion sodio se desplaza a través de su gradiente eléc-
trico y químico. Este ion es bombeado después fuera de la célula
hacia el intersticio, y la glucosa es conducida por el transportador
de glucosa (GLUT) 2 hacia el líquido intersticial. Por lo menos en
la rata, se observa también cierto transporte por transportador de
glucosa dependiente de sodio 1 y el transportador de glucosa 1.
El SGLT 2 específicamente fija el isómero d de la glucosa y la
tasa de transporte de la d-glucosa es muchos tantos mayor que la de
la l-glucosa. El transporte de glucosa en los riñones es inhibido,
lo mismo que en el intestino, por el glucósido vegetal florizina, el
cual compite con la d-glucosa por la unión al transportador.
OTROS EJEMPLOS DE TRANSPORTE
ACTIVO SECUNDARIO
Al igual que la reabsorción de glucosa, la de aminoácidos es muy
intensa en la primera porción del túbulo contorneado proximal.
La absorción en este sitio se parece a la que ocurre en el intes-
tino (cap. 27). Los principales transportadores en la membrana
intercambio de sodio-hidrógeno (Na-H). Otro 30% es absorbido
a través del cotransportador de Na-2Cl-K en la rama ascendente
gruesa del asa de Henle y casi 7% es absorbido por el cotranspor-
tador de sodio-cloro (Na-Cl) en el túbulo contorneado distal. La
parte restante del ion sodio filtrado, casi 3%, se absorbe a través
de los conductos epiteliales de sodio (ENaC) en los túbulos co-
lectores y ésta es la porción que es regulada por la aldosterona en
los ajustes homeostásicos del equilibrio de sodio ionizado.
REABSORCIÓN DE GLUCOSA
La glucosa, los aminoácidos y el bicarbonato se reabsorben junto
con el ion sodio en la porción inicial del túbulo proximal (fig.
38-9). En una sección más distal del túbulo, se reabsorbe dicho
ion con cloruro. La glucosa suele ser una de las sustancias extraí-
das de la orina mediante un transporte activo secundario. Ella
es filtrada a una tasa aproximada de 100 mg/min (80 mg/100
ml de plasma × 125 ml/min). Básicamente se reabsorbe toda la
glucosa y no más de algunos miligramos aparecen en la orina en
un periodo de 24 h. La cantidad reabsorbida es proporcional a
la filtrada y, por tanto, a la concentración plasmática de gluco-
sa (P
G
) multiplicada por el filtrado glomerular hasta conseguir
el transporte máximo (Tm
G
). Cuando se supera este último,
aumenta la cantidad de glucosa en la orina (fig. 38-10). El trans-
porte máximo de glucosa asciende a casi 375 mg/min en los va-
rones y a 300 mg/min en las mujeres.
El umbral renal para la glucosa es la concentración plasmá-
tica a la cual aparece inicialmente esta sustancia en la orina en
cantidades mayores de las mínimas normales. Cabía esperar
que el umbral renal fuese de casi 300 mg/100 ml, es decir, 375
mg/min (de transporte máximo de glucosa) divididos por 125
ml/min (tasa de filtración glomerular). No obstante, el umbral
renal efectivo es de casi 200 mg/100 ml de plasma arterial, lo
cual corresponde a una concentración en sangre venosa de casi
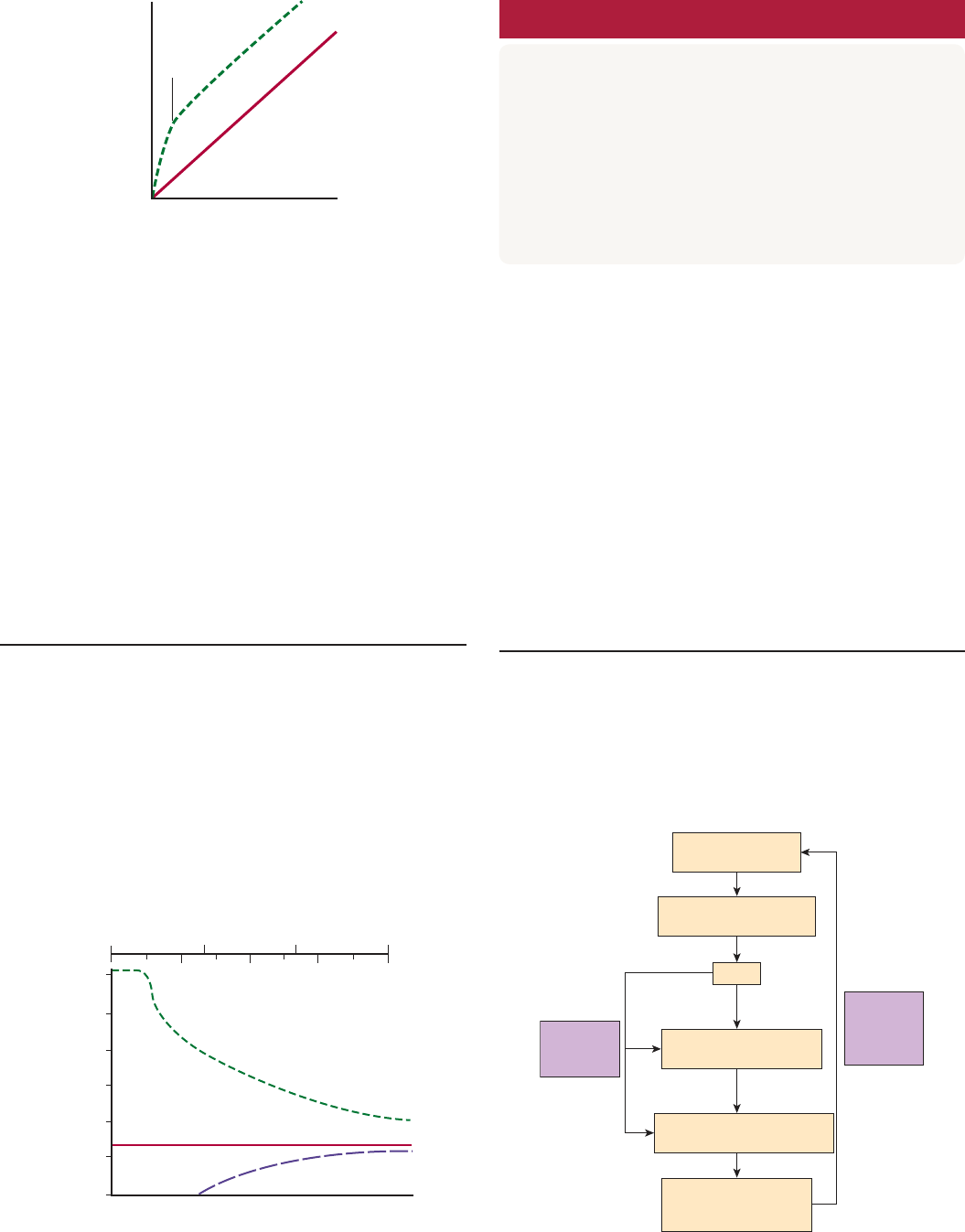
180 mg/100 ml. En la figura 38-10, se muestra porqué el umbral
2.6
2.4
2.2
2.0
1.8
1.6
1.4
1.2
1.0
0.8
0.6
0.4
0.2
0253075100
Glucosa
Amino-
ácidos
Porcentaje de longitud del túbulo proximal
HCO
3
–
osm
Inulina
Cl
–
K
+
Na
+
TF
P
UV
.
Inulina
Glucosa
P
Bisel
“Ideal”
Real
Glucosa plasmática (P
G
)
Tm
G
Glucosa reabsorbida (T
G
)
FIGURA 389 Reabsorción de diversos solutos en el túbulo
proximal. TF/P, índice de concentración líquido:plasma tubular.
(Cortesía
de FC Rector Jr.)
FIGURA 3810 Arriba: relaciones de la concentración plasmática
(P) y la excreción (UV) de glucosa e inulina. Abajo: relación entre la
concentración plasmática de glucosa (P
G
) y la cantidad de glucosa que
se reabsorbe (T
G
).
CAPÍTULO 38 Función renal y micción
651
por encima del transporte máximo de dicho ácido (Tm
PAH
), el
aclaramiento de éste desciende progresivamente. Con el tiempo
se acerca al aclaramiento de la inulina (C
In
) (fig. 38-12), ya que la
cantidad de ácido p-aminobutírico secretada se convierte en una
fracción cada vez más pequeña de la cifra total excretada.
Por lo contrario, el aclaramiento de glucosa es básicamente de
cero a valores de presión parcial de glucosa por debajo del umbral
renal; sin embargo, por arriba del umbral, el aclaramiento de glu-
cosa aumenta hasta llegar al de inulina a medida que se incremen-
ta la presión parcial de glucosa. Ya se describió antes la utiliza-
ción del C
PAH
para conocer el flujo plasmático renal efectivo.
RETROALIMENTACIÓN
TUBULOGLOMERULAR Y EQUILIBRIO
GLOMERULOTUBULAR
Las señales provenientes del túbulo renal en cada nefrona retro-
alimentan para afectar la filtración en su glomérulo. A medida que
aumenta la tasa de flujo a través de la rama ascendente del asa de
Henle y la primera porción del túbulo distal, disminuye la filtra-
ción glomerular en la misma nefrona y, por lo contrario, una re-
ducción en el flujo incrementa el filtrado glomerular (fig. 38-13).
apical cotransportan sodio ionizado, en tanto los transportado-
res en las membranas basolaterales no son dependientes de ion
sodio. Este último es bombeado fuera de las células por la Na, K
ATPasa, y los aminoácidos salen por difusión pasiva o facilitada
hacia el líquido intersticial. Parte del cloruro es reabsorbido con
sodio ionizado y iones potasio en la rama ascendente gruesa del
asa de Henle. Además, se han identificado dos miembros de la
familia de los conductos del cloro en el riñón. Las mutaciones
del gen para uno de los conductos renales se vinculan con cál-
culos renales de calcio e hipercalciuria (enfermedad de Dent),
pero todavía no se ha esclarecido de qué manera está vinculado
el transporte tubular de ion calcio y cloruro.
TRANSPORTE DE ÁCIDO
pAMINOBUTÍRICO
La dinámica de transporte de este ácido ilustra la operación de
los mecanismos de transporte activo que secretan sustancias ha-
cia el líquido tubular (recuadro clínico 38-1). La carga filtrada
de ácido p-aminobutírico es una función lineal de la concentra-
ción plasmática, pero la secreción del mismo aumenta a medida
que se eleva la presión parcial de ácido p-aminobutírico (P
PAH
)
sólo hasta que se alcanza una tasa de secreción máxima de ácido
p-aminobutírico (Tm
PAH
) (fig. 38-11). Cuando la P
PAH
es baja,
el aclaramiento de ácido p-aminobutírico está elevado; pero
cuando aumenta la presión parcial de ácido p-aminobutírico
UV
.
Inulina
P
PAH
Desbor-
damiento
FIGURA 3811 Relación entre las concentraciones plasmática
(P) y la excreción (UV) de ácido p-aminobutírico (PAH) e inulina.
Aclaramiento (ml/min)
Inulina
Glucosa
Concentración plasmática (P)
20 40 60 80
200 400 600
Glucosa, mg/100 ml
PAH, mg/100 ml
PAH
600
500
400
300
200
100
0
FIGURA 3812 Aclaramiento de inulina, glucosa y ácido p-ami-
nobutírico (PAH) a diversas concentraciones plasmáticas de cada
sustancia en el ser humano.
FIGURA 3813 Mecanismos del equilibrio glomerulotubular y
la retroalimentación tubuloglomerular.
Otras sustancias secretadas por los túbulos
Los derivados del ácido hipúrico además del ácido p-aminobu-
tírico (PAH), el rojo fenólico y otros colorantes a base de sulfonf-
taleína, la penicilina y diversos colorantes yodados son secre-
tados activamente hacia el líquido tubular. Las sustancias que
normalmente se generan en el organismo y son secretadas por
los túbulos comprenden diversos sulfatos etéreos, esteroides y
otros glucurónidos, así como el ácido 5-hidroxiindolacético, el
principal metabolito de la serotonina.
RECUADRO CLÍNICO 38-1
Presión arteriolar
renal
Presión de los
capilares glomerulares
GFR
Reabsorción de solutos
en el túbulo proximal
Reabsorción de solutos en
el asa ascendente gruesa
Descarga de sal
y líquido hacia
el túbulo distal
Retroali-
mentación
tubulo-
glomerular
Equilibrio
glomerulo-
tubular

652
SECCIÓN VIII Fisiología renal
cifras demuestran dos hechos importantes. En primer lugar, se
reabsorbe un mínimo del 87% del agua filtrada, aun cuando el
volumen urinario sea de 23 L y, en segundo lugar, la reabsorción
de la parte restante del agua filtrada puede variar sin afectar la
excreción total de solutos. Por tanto, cuando está concentrada la
orina, el agua se retiene más que los solutos y, cuando se halla
diluida, se pierde agua del organismo más que los solutos. Los
dos hechos tienen gran importancia en la regulación de la os-
molalidad de los líquidos corporales. Un control decisivo de la
diuresis de agua lo lleva a cabo la vasopresina, la cual actúa sobre
los túbulos colectores.
ACUAPORINAS
La difusión rápida de agua a través de las membranas celulares
depende de la presencia de los conductos de agua, las proteí-
nas de la membrana integral denominadas acuaporinas. Hasta
el momento, se han clonado 13 acuaporinas. Sin embargo, sólo
cuatro de ellas (acuaporinas 1, 2, 3 y 4) desempeñan una función
decisiva en el riñón. Más adelante, se analizan las funciones que
desempeñan las acuaporinas 1 y 2 en el transporte renal de agua.
TÚBULO PROXIMAL
El transporte activo de muchas sustancias ocurre desde el líquido
presente en el túbulo proximal, pero algunos estudios de micro-
punción han demostrado que el líquido se preserva básicamente
isoosmótico en el extremo del túbulo proximal (fig. 38-9). La
acuaporina 1 se ubica en la membrana basolateral tanto como
en la apical de los túbulos proximales, y su presencia permite el
desplazamiento rápido del agua fuera del túbulo a través de los
gradientes osmóticos establecidos por el transporte activo de so-
lutos y se mantiene la isotonicidad. Dado que el cociente de la
concentración en el plasma (TF/P) de la sustancia no reabsor-
bible inulina corresponde a 2.5 a 3.3 en el extremo del túbulo
proximal, se deduce que para el tiempo en que el filtrado llega a
este punto, se ha retirado 60 a 70% del soluto filtrado y 60 a 70%
del agua filtrada (fig. 38-14).
Cuando se produjo supresión génica de la acuaporina 1 en ra-
tones, la permeabilidad del agua en el túbulo proximal se redujo
80%. Al someter a deshidratación a los ratones, su osmolalidad
urinaria no aumentó (<700 mosm/kg), aun cuando estuviesen
presentes otras acuaporinas renales. En personas con mutacio-
nes que eliminan la actividad de la acuaporina 1, la anomalía del
metabolismo del agua no es tan grave, aunque su respuesta a la
deshidratación está alterada.
Este proceso, denominado retroalimentación tubuloglo-
merular, tiende a conservar la constancia de la carga que llega
al túbulo distal.
El sensor para esta respuesta es la mácula densa. La cantidad
de líquido que entra en el túbulo distal en el extremo de la rama
ascendente gruesa del asa de Henle, depende de la cantidad de
ion sodio y cloruro presente en el mismo. Estos iones ingresan
a las células de la mácula densa a través del cotransportador de
Na-K-2Cl que opera en sus membranas apicales. El aumento
de sodio ionizado produce un incremento de la actividad de la
Na, K ATPasa, y un aumento consecutivo en la hidrólisis de tri-
fosfato de adenosina (ATP) propicia la formación de más ade-
nosina. Tal vez esta última es secretada por la membrana basal
de las células. Ella ejerce su acción a través de los receptores de
adenosina A
1
sobre las células de la mácula densa e incremen-
ta su liberación de iones calcio hacia el músculo liso vascular
en las arteriolas aferentes. Esto genera vasoconstricción de las
arteriolas aferentes y una disminución consecutiva del filtrado
glomerular. Probablemente un mecanismo similar genera una
señal que reduce la secreción de renina por las células yuxtaglo-
merulares adyacentes en la arteriola aferente (cap. 39), pero esto
aún no se ha esclarecido.
Por lo contrario, un incremento del filtrado glomerular origi-
na un aumento de la reabsorción de solutos y, por ende, de agua,
principalmente en el túbulo proximal, de manera que, en gene-
ral, el porcentaje de soluto reabsorbido se mantiene constante.
Este proceso se llama equilibrio glomerulotubular y es muy
notorio para el ion sodio. El cambio en la reabsorción de dicho
ion ocurre al cabo de algunos segundos después de un cambio
en la filtración, de manera que quizás intervenga un factor hu-
moral extrarrenal. Un factor corresponde a la presión oncótica
en los capilares peritubulares. Cuando el filtrado glomerular es
alto, hay un incremento relativamente considerable de la pre-
sión oncótica del plasma que sale de los glomérulos a través de
las arteriolas eferentes y, por consiguiente, de sus ramas capila-
res. Esto eleva la reabsorción de sodio ionizado
del túbulo. Sin
embargo, también intervienen otros mecanismos intrarrenales
aún no identificados.
TRANSPORTE DE AGUA
En situaciones normales, se filtran a través del glomérulo 180 L
de líquido por día, en tanto el volumen urinario promedio por
día asciende a casi 1 L. Se puede excretar la misma cantidad de
soluto por 24 h en un volumen urinario de 500 ml, con una
concentración de 1 400 mosm/kg o en un volumen de 23.3 li-
tros con una concentración de 30 mosm/kg (cuadro 38-7). Estas
CUADRO 387 Alteraciones del metabolismo del agua producidas por la vasopresina en seres humanos. En cada
caso, la carga osmótica expresada es 700 mosm/día
GFR
(ml/min)
Porcentaje de reabsorción
de agua filtrada
Volumen de
orina (L/día)
Concentración de
orina (mosm/kg H
2
O)
Ganancia o pérdida de agua
más que de soluto (L/día)
Orina isotónica con respecto al
plasma
125 98.7 2.4 290 . . .
Vasopresina (antidiuresis máxima) 125 99.7 0.5 1 400 Ganancia de 1.9
Sin vasopresina (diabetes insípida
“completa”)
125 87.1 23.3 30 Pérdida de 20.9
CAPÍTULO 38 Función renal y micción
653
como las glándulas salivales, el tubo digestivo y las vías respi-
ratorias.
El ion potasio se difunde de nuevo hacia la luz tubular y vuel-
ve hacia el intersticio a través de los conductos de ROMK (con-
ducto del potasio de la membrana apical) y otros conductos de
potasio. El cloruro se desplaza hacia el intersticio a través de los
conductos del ClC-Kb (fig. 38-15).
TÚBULO DISTAL
El túbulo distal, sobre todo su primera parte, es en efecto una
extensión del segmento grueso de la rama ascendente; es rela-
tivamente impermeable al agua, y la reabsorción constante de
soluto más que solvente diluye más el líquido tubular.
TÚBULOS COLECTORES
Éstos muestran dos porciones: una cortical y una medular. Los
cambios de la osmolalidad y el volumen en los túbulos colec-
tores dependen de la cantidad de vasopresina que actúa sobre
los túbulos. Esta hormona antidiurética de la neurohipófisis
aumenta la permeabilidad de los túbulos colectores al agua. La
sustancia clave para la acción de la vasopresina sobre los tú-
bulos colectores es la acuaporina 2. A diferencia de las demás
acuaporinas, ésta se almacena en las vesículas intracitoplásmi-
cas de las células principales. La vasopresina hace posible una
inserción rápida de estas vesículas en la membrana apical de
ASA DE HENLE
Según se mencionó antes, las asas de Henle de las nefronas yux-
taglomerulares se sumergen de manera profunda en las pirámi-
des medulares antes de drenar hacia los túbulos contorneados
distales en la corteza, y todos los túbulos colectores descienden
de nuevo a través de las pirámides medulares para drenar en las
puntas de las pirámides hacia la pelvis renal. Hay un incremen-
to graduado de la osmolalidad del intersticio de las pirámides
en el ser humano: la osmolalidad en las puntas de las papilas
puede llegar a casi 1 200 mosm/kg de agua, aproximadamen-
te cuatro tantos la del plasma. La rama descendente del asa de
Henle es permeable al agua, dada la presencia de acuaporina 1
tanto en la membrana apical como en la basolateral, pero la
rama ascendente es impermeable al agua (cuadro 38-8). Los io-
nes sodio y potasio y el cloruro son cotransportados fuera del
segmento grueso de la rama ascendente. Como consecuencia, el
líquido que se halla en la rama descendente del asa de Henle se
vuelve hipertónico a medida que el agua sale del túbulo hacia
el intersticio hipertónico. En la rama ascendente, aquél se torna
más diluido por el desplazamiento de ion sodio y cloruro fuera
de la luz tubular, y cuando el líquido llega a la parte superior del
haz de la rama ascendente (el llamado segmento de dilución) se
vuelve entonces hipotónico con respecto al plasma. Al pasar por
la rama descendente del asa de Henle, se reabsorbe otro 15% del
agua filtrada, de manera que aproximadamente 20% del agua fil-
trada entra en el túbulo distal y, en este punto, el cociente TF/P
de la inulina equivale a casi 5.
En la rama ascendente gruesa, un transportador cotransporta
un ion sodio, un ion potasio y un cloruro desde la luz tubular
hasta las células tubulares. Éste es otro ejemplo del transporte
activo secundario; el sodio ionizado experimenta un transpor-
te activo desde las células hasta el intersticio gracias a la Na, K
ATPasa presente en las membranas basolaterales de las células,
lo cual conserva bajo el ion sodio intracelular. El transportador
de Na-K-2Cl tiene dos dominios transmembrana con aminos y
carboxilos terminales intracelulares; es un miembro de una fa-
milia de transportadores encontrada en muchos otros lugares,
120
100
80
60
40
20
0
Glucosa
Fracción remanente
en el líquido tubular
Osmoles
Agua
Na
+
Creatinina
Inulina
Urea
Túbulo
proximal
Asa de
Henle
Túbulo
distal
Túbulo
colector
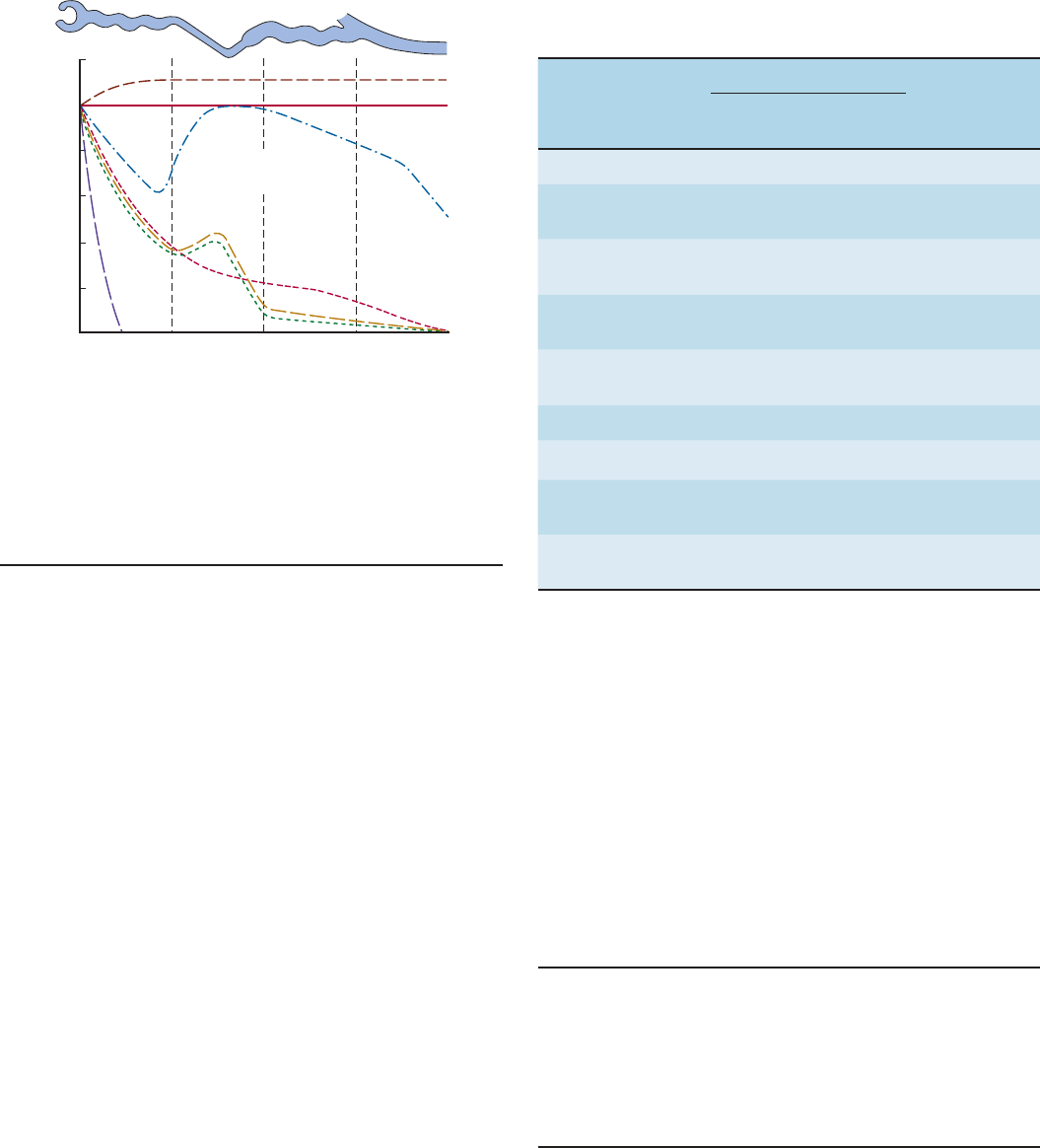
FIGURA 3814 Cambios en el porcentaje de la cantidad
filtrada de sustancias que permanecen en el líquido tubular en
toda la longitud de la nefrona cuando hay presente vasopresina.
(Modificada de Sullivan LP, Grantham JJ: Physiology of the Kidney, 2nd ed. Lea & Fe-
biger, 1982.)
CUADRO 388 Permeabilidad y transporte
en diversos segmentos de la nefrona
Permeabilidad
H
2
O Urea NaCl
Transporte
activo de Na
+
Asa de Henle
Rama descendente
delgada
4++
±
0
Rama ascendente
delgada
0 + 4+ 0
Rama ascendente
gruesa
0
±±
4+
Túbulo contorneado
distal
±±±
3+
Túbulo colector
Porción cortical 3+*0
±
2+
Porción medular
externa
3+*0
±
1+
Porción medular
interna
3+*3+
±
1+
a
Los datos están basados en estudios de riñones de conejos y humanos. Los valores indi-
cados con asteriscos corresponden a cuando está presente la vasopresina. Estos valores
son 1+ si no hay vasopresina. NaCl, cloruro de sodio.
Modificado con autorización de Kokko JP: Renal concentrating and diluting mechanisms.
Hosp Pract [Feb] 1979;110:14.
Este documento contiene más páginas...
Descargar Completo
renal Ganong.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.