Página 1 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
BASES BIOQUIMICAS DE LA ENDOCRINOLOGIA.
RECEPTORES Y TRANSDUCCION DE SEÑALES
Existen diferentes procesos que aseguran el correcto funcionamiento de las diferentes vías metabólicas,
entre las que podemos nombrar en primer lugar a las enzimas modulados a través de sus efectores
alostéricos o por regulación génica, en especial aquellos seres pluricelulares en donde aumenta el grado
de complejidad debido al desarrollo de diversos órganos y tejidos surgió la necesidad de disponer de
sistemas de comunicación que adapten a cada célula destinado para un tipo de función, es decir
estamos hablando del sistema endocrino y el sistema nervioso.
En el sistema endocrino la comunicación esta mediado por hormonas que se vierten a la circulación y
que llegaran a un destino denominado células blanco o diana¨, donde desencadenaran un efecto
determinado, por otra parte muchas hormonas pueden no ser incluidos a la circulación y por lo tanto
desencadenar un efecto intracelular (secreción autacrina) y por último la secreción de una célula
determinada puede hacer efecto sobre la célula contigua (secreción paracrina) como por ejemplo los
eicosanoides, factores de crecimiento y citoquinas.
En el sistema nervioso, la mayoría de las neuronas están comunicadas a través de sustancias
denominados neurotransmisores que serán destinadas a otras neuronas a través de las sinapsis. Sin
embargo las neuronas pueden segregar hormonas como la Oxitocina y vasopresina que nacen desde el
hipotálamo y llegan al lóbulo posterior y a partir de allí ser vehiculizados hasta la glándula mamaria y riñón
respectivamente.
Existen diferentes péptidos, que son producidos en el sistema nervioso y que actúan en el tracto
gastrointestinal, como también la medula adrenal, que puede secretar catecolaminas y actuar como
neurotransmisores en terminales adrenérgicos.
1 RECEPTORES
Los receptores son los sitios específicos a donde actúan las hormonas, neurotransmisores y otros
mensajeros químicos. Estos receptores están constituidos por proteínas en donde la hormona se une
selectivamente a través de una adaptación conformacional y formar un complejo Hormona – Receptor
(HR) que presenta las siguientes características:
a. Adaptación inducida
b. Saturabilidad
c. Reversibilidad
Este concepto es aplicable a todas aquellas macromoléculas que pueden unirse de manera selectiva,
hormonas, neurotransmisores, factores de crecimiento, citoquinas y otras sustancias que inducen a un
cambio conformacional. Existen compuestos similares a los mencionados anteriormente denominados
agonistas que pueden desencadenar al unirse al receptor una respuesta; y por otra parte existen los
antagonistas que no producen respuesta, pero sin embargo se unen al receptor.
Localización de receptores
Estos pueden ser:
a. Receptores intracelulares
b. Receptores de membranas
En el caso de los receptores de membranas se debe de recordar que no es un dispositivo rígido, es decir
que no se mantiene en una misma posición, sino que debido a la fluidez de la membrana plasmática estos
pueden desplazarse en diferentes direcciones a los que llamamos receptores móviles. Otros receptores de
membrana cuando se unen a la hormona son internalizados a través de la endocitosis.
Números de receptores
El número de receptores intracelulares es menor al de los receptores de membrana; sin embargo no es
necesario que la totalidad de las hormonas se unan a todos los receptores, bastará con que sólo el 20% de
receptores esté ocupado por hormonas para desencadenar una respuesta; el 80% restante se denomina
receptores de reserva.
Página 2 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
Al llegar una concentración determinada de hormonas a su receptor, el aumento sostenido de ese nivel
de concentración puede reducir el número de receptores disponibles; a este fenómeno se denomina
desensibilización o down regulation (ej.: internalización de receptores). El fenómeno contrario, el aumento
del número de receptores, regulación incrementadora se denomina up regulation (ej.: inserción de
receptores en la membrana) es decir por deficiencia del ligando específico.
Mecanismo de Acción
El complejo HR debe interactuar diferenciando las estructuras específicas de la célula, es decir de los
que están ubicados en la membrana plasmática o en el interior celular.
2 RECEPTORES INTRACELULARES
Estos receptores se localizan en el citoplasma y en el núcleo. Las hormonas que participan o median
estas acciones son generalmente poco polares y como ejemplos tenemos hormonas esteroideas, tiroideas,
metabolitos activos de vitamina D, retinoides, ácidos grasos, ácidos biliares, xenobióticos y otras moléculas
poco polares.
Cuando el ligando se une a su receptor ESTE EJERCE ACCIÓN DIRECTA SOBRE EL ADN NUCLEAR
REGULANDO LA ACTIVIDAD DE LA TRANSCRIPCIÓN.
Los receptores intracelulares, pueden ser agrupados en 2 familias:
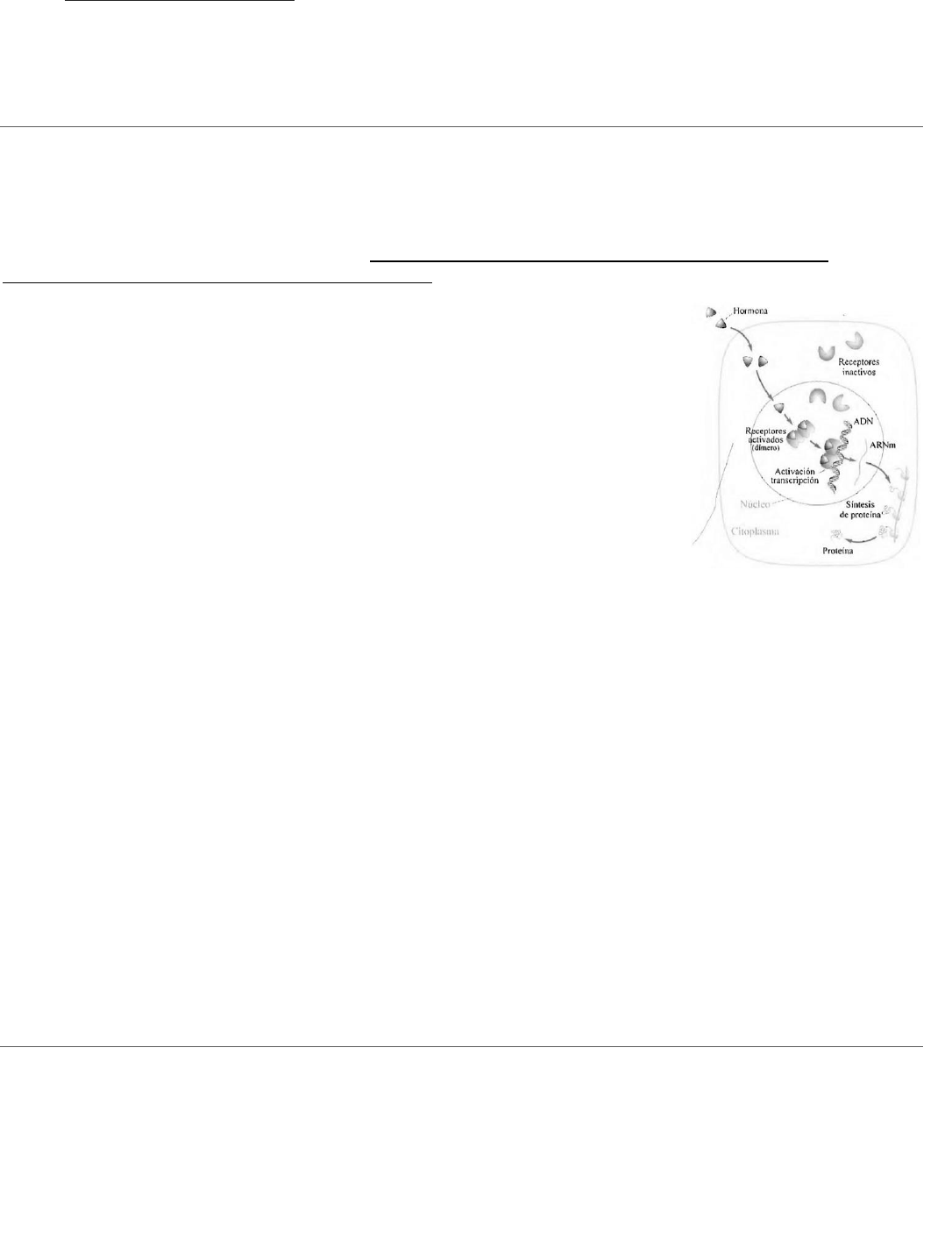
a. Receptores de Esteroides: se localizan en el citoplasma unidos a
proteínas denominadas chaperonas (HSP90, HSP70 y HSP56) que básicamente
los mantienen inactivos; por lo tanto cuando la hormona se une al receptor
provoca el desplazamiento de las chaperonas y por ende un cambio
conformacional, formando dímeros que ingresan al núcleo y a sitios del ADN
llamados ELEMENTOS DE RESPUESTA A LA HORMONA ubicados corriente arriba
del promotor del gen blanco. Como ejemplos podemos nombrar: receptores
de glucocorticoides (GR), de mineralocorticoides (MR), progesterona (PR) y de
andrógenos (AR).
b. Receptores tiroideos o nucleares: se encuentran unidos al ADN en sitios
de elementos de respuesta de manera inactiva. solo el receptor de
estrógenos se encuentra unido a chaperonas y el resto está asociado a una molécula correpresora que
inhibe la transcripción. Una vez formado el complejo hormona-receptor este se desplaza y se dimeriza para
influir sobre la transcripción. Solo el receptor de estrógenos se asocia a homodímeros pero los receptores
tiroideos (TR), de vitamina D (VDR), de retinoides (RAR), de ácidos retinoico (RXR) y receptores activados
por proliferador de peroxisomas (PPAR) forman heterodímeros. Generalmente los TR, VDR; RAR; PPAR; se
une a RXR para formar heterodímeros.
Los receptores intracelulares presentan una estructura con tres dominios funcionales:
1. Extremos n-terminal también llamado sector hípervariable (HV) porque exhibe una gran variabilidad
entre los miembros de su familia, de hecho es el que participa en acciones regulando la transcripción.
2. Dominio central, donde se encuentran los dedos de zinc capaces de interactuar con secuencias
especificas
3. El tercer dominio llamado c-terminal que es el sitio donde se une la hormona.
Receptores activados por proliferador de peroxisomas (PPAR). Están localizados especialmente en hígado,
musculo, tejido adiposo, y sus ligando son productos metabólicos endógenos estimulando a la oxidación
de los ácidos grasos, a nivel del tejido adiposo y musculo. Actúan como factores de transcripción,
regulando la actividad génica. Por otra parte mejoran la tolerancia, a la glucosa y disminuye la resistencia
a la insulina en pacientes con diabetes tipo 2
3 RECEPTORES DE MEMBRANA PLASMATICA.
Estos receptores están ubicados en la superficie de la membrana plasmática, integrando mecanismo
de transducción de señales. El primer mensajero será la hormona, que provoca cambios conformacionales
en el receptor específico para así transmitir a proteína efectoras, activando enzimas o moléculas
pequeñas llamados segundo mensajero, que propagaran la señal intracelular.
Página 3 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
Existen diferentes tipos principales de receptores:
A. Receptores asociados a proteína G, que presenta una estructura de siete hélices α transmembrana,
con un extremo extracelular n-terminal, y otro extremo citosólico c-terminal que interactúa con proteínas
G y la hormona se une al nicho formado por los extremos de cada hélice α transmembrana. Son ejemplos
de estos tipos de receptores los de hormonas paratiroidea, luteinizante, folículo estimulante, tiroestimulante,
ACTH, glucagón, angiotensina II, vasopresina, factor activador de plaquetas, sustancias P, prostaglandina,
adrenérgicos α y β, colinérgicos muscarínicos, serotoninérgicos, dopaminérgicos, de bastoncillos de retina
(rodopsina).
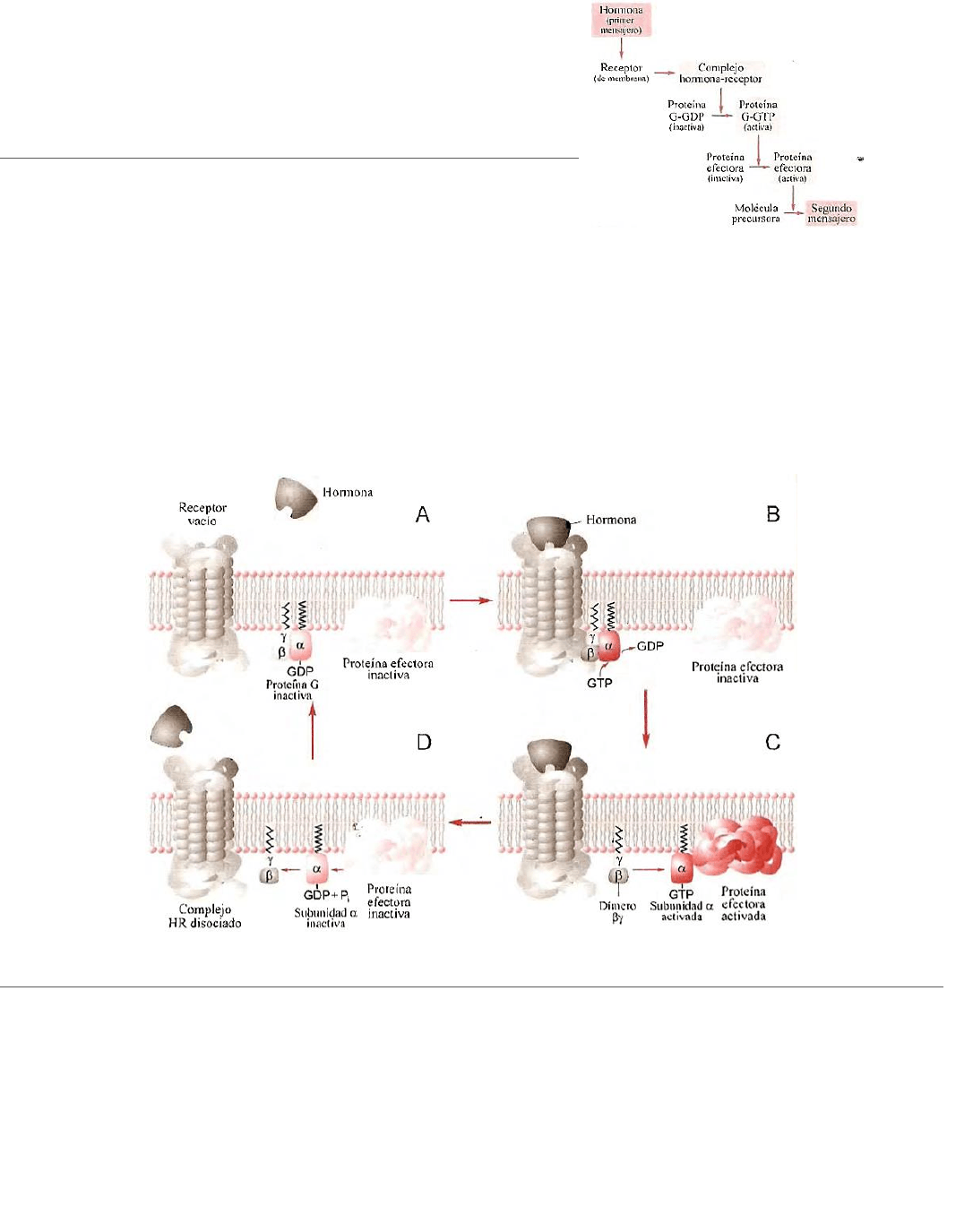
El mecanismo de acción seria de la siguiente manera:
4 PROTEINA G
Se dominan así porque tiene esa propiedad de unirse a
nucleótidos de guanina (GDP o GTP) por lo tanto median
acciones entre los receptores de siete pasos y las proteínas
efectoras intracelulares. Las proteínas G son heterotriméricas, que presentan tres subunidades, α, β y γ, que
están adosados y anclados, a la cara citosólica de la membrana, de estas tres subunidades, la subunidad
α posee gran afinidad por los nucleótidos de GDP o GTP. la subunidad α mientras este unida a GDP se
mantiene asociado a las otras dos subunidades, sin embargo con la llegada de una hormona a su
receptor esta provoca una cambio conformacional haciendo que la subunidad α se disocie del GDP para
unirse a un GTP, y luego la subunidad α se separa de las otras dos subunidades y adquiere actividad
moduladora por ej, activa a la adenilato ciclasa. Finalmente la subunidad α se disocia del GTP y se une a
un GDP para conformar nuevamente el heterotrímero.
Es importante destacar que el dímero βγ actúa en diferentes proteínas ¨blanco¨ en especial en los
canales de K y Ca, adenilato ciclasa, fosfolipasa C y proteínas quinasas.
5 RECEPTORES PROTEINA-TIROSINA QUINASA
Diversos receptores acoplados a proteína G requieren de enzimas integrantes de las señales y que
pueden tener actividad catalítica intrínseca o extrínseca.
a. Receptores con actividad tirosina quinasa intrínseca. Estos receptores están constituidos por un
extremo N-terminal extracelular (unión al ligando), al cual le sigue una hélice α transmembrana y el
extremo C-terminal citosólico (que posee la actividad tirosina quinasa). Como ejemplos tenemos a los
receptores de insulina, formado por dos heterodímeros, αβ unidos por puentes disulfuro, las subunidades α

Página 4 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
esta ubicados en el lado extracelular donde se une la hormona, y la subunidad β presenta un segmento
transmembrana y un dominio citosólico con actividad tirosina quinasa.
Cuando llega el ligando al receptor, este provoca un cambio conformacional que dimeriza (excepto la
insulina) y activa la tirosina quinasa. A continuación se desencadena una cascada de fosforilaciones de
manera cruzada en los restos de tirosina de ambas cadenas, por autofosforilación del receptor y por lo
tanto aumenta la actividad de la quinasa creando una cadena de transducción de señales.
Los restos de fosfotirosina del lado citosólico promueven la unión de otras proteínas, que poseen
dominios SH2, SH3, dado a que estas tienen la capacidad de unirse a restos de tirosina-fosfato y por otra
parte asociar proteínas que posean el mismo dominio de carácter SH. (Imagen 24-7)
b. Receptores asociados a serina-treonina quinasas. estos fosforilan restos de serina-treonina median
acciones de ligandos que pertenecen, a factores de transformación TGF relacionados con hormonas de la
reproducción. Los receptores serina-treonina quinasa, cuando están activados estimulan a proteínas,
como las Smad los cuales efectúan la cadena de señales. Pueden fosforilar receptores tirosina quinasa e
inclusive el de insulina.
c. Receptores asociados a tirosina quinasa extrínseca. estos tipos de receptores no poseen actividad
tirosina quinasa propia pero pueden asociarse a proteínas tirosina quinasa del citoplasma, como ejemplo
tenemos a los receptores de citoquinas, hormonas de crecimiento, prolactina, leptina, que están
conformados de igual manera a los tienen actividad tirosina-quinasa. El mecanismo de acción se produce
una vez que se une al receptor el ligando, provoca un cambio conformacional que lo dimeriza y luego la
porción citosólica interactúa con tirosina quinasa donde el receptor es fosforilado y a su vez interacciona
con proteínas de dominios SH2. Existen dos tipos de familias principales como los Src que participan en
señales desde receptores de citoquinas y desde antígenos de linfocitos T y B, otra familia son las de JAK
asociados a tirosina quinasa Janus.
d. Receptores tirosina fosfatasas. Se encuentran asociados a proteína –tirosina fosfatasas que
escinden los fosfatos insertados en las quinasas como ej tenemos a los CD45 de linfocitos T y B. que
antagonizan las acciones de estas.
e. Receptores asociados a guanilato ciclasa. Estos tipos de receptores catalizan la formación de GMP
cíclico a partir de GTP gracias a la actividad guanilato ciclasa. Su estructura presente una hélice α
transmembrana y un dominio extracelular al cual se une el ligando y otro dominio citosólico con actividad
enzimática. Como ej podemos nombrar a los receptores de péptidos natriuréticos atriales, receptores de
bastoncillos de la retina (rodopsina). Existen receptores intracelulares citosólicos guanilato ciclasa que son
activadas por óxido nítrico y monóxido de carbono.
f. Desensibilización. este fenómeno está vinculado a receptores acoplados a proteína G que pueden
ser internalizadas en la célula por endocitosis, fosforilación y disminución de la síntesis del receptor. La
fosforilación de restos de serina o treonina por quinasas específicas provoca el desacoplamiento del
receptor de la proteína G. por ej el fotorreceptor de la rodopsina.
6 SISTEMAS DE TRANSDUCCION DE SEÑALES
1. Sistema del AMP-3’,5’-cíclico.
Recibe este nombre porque el fosfato forma un ciclo entre los hidroxilos de los carbonos 3 y 5 de la
ribosa, catalizada por una enzima llamada adenilato ciclasa, ubicado en la membrana plasmática y
requiere como cofactor Mg.
La adenilato ciclasa es una proteína integral de membrana plasmática que presenta tres dominios, es
decir un extremo n-terminal citosólico, luego continua con seis hélices α transmembrana, un dominio
citosólico largo donde contiene el sitio catalítico. Casi todas son activadas por la subunidad α
s
de proteína
G y no todas serán inhibidas por α
i;
el CA, Ca-calmodulina y proteína quinasa C tienen efectos sobre estas.
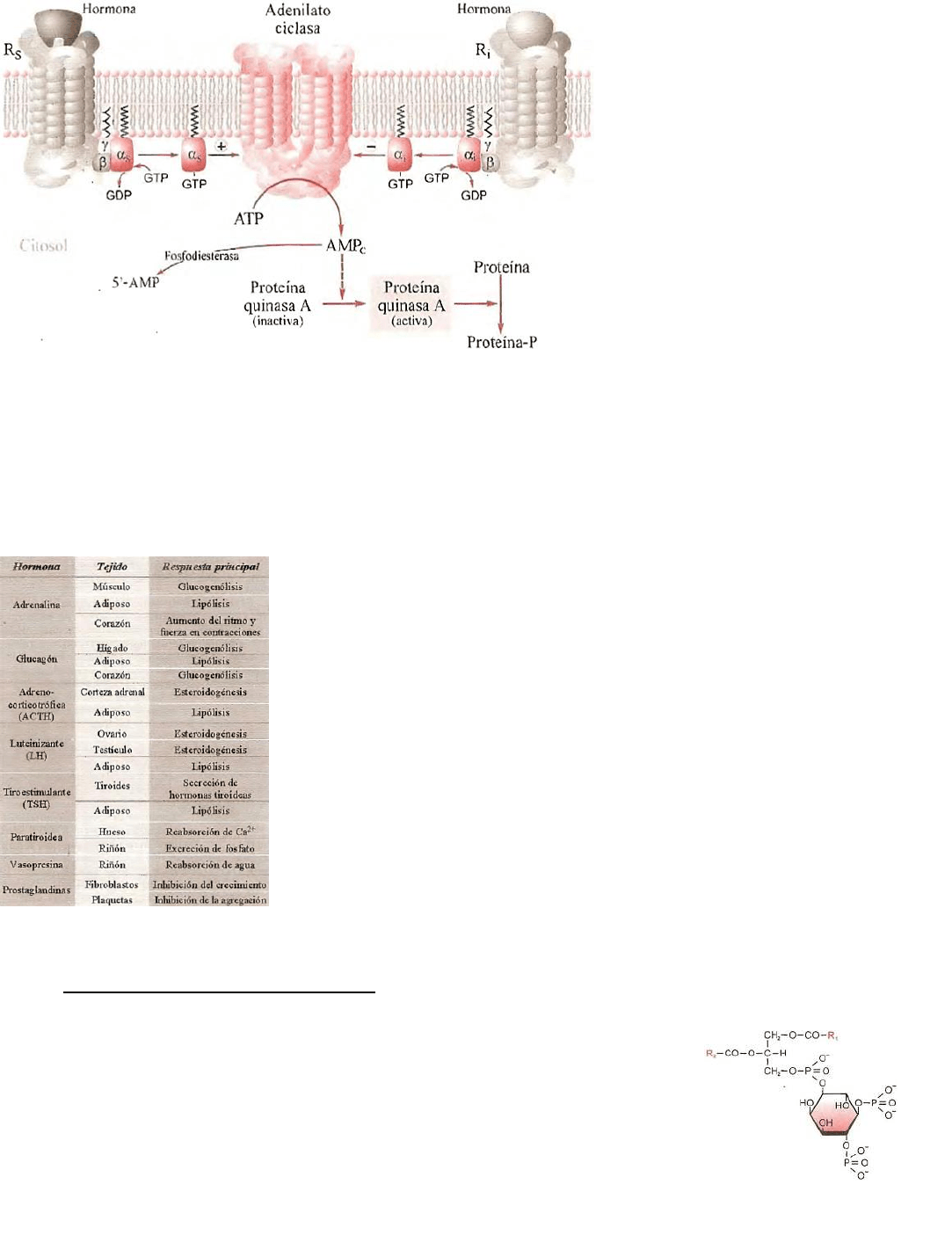
Pero… ¿Cómo funciona el sistema del AMP
c
?...
Bien lo hace de la siguiente manera:
a. Cuando llega un ligando (hormona ej adrenalina) que se une
al receptor este provoca un cambio conformacional que se transmite a
proteínas G. existen receptores y proteínas G estimuladoras (R
s
y G
s
) e
inhibidores (R
i
y G
i
) cuando un ligando estimulador como la adrenalina se
une al receptor (R
s
), interactúa con proteínas G
s.
y por otra parte si se une
un ligando inhibidor al receptor (R
i
) este interactúa con proteínas G
i.
b. La formación del complejo hormona-receptor (HR) permite la interacción de la subunidad α con
GTP para luego separarse de las otras dos subunidades βγ y formar el complejo α
s
-GTP. por otra parte el
receptor asociado de proteína G
i
se separa α
i
-GTP que inhibirá a la adenilato ciclasa.
c. Una vez activada la adenilato ciclasa cataliza la formación de AMPc a partir de ATP y aumenta la
concentración del segundo mensajero o AMPc
Página 5 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
d. Como la subunidad α tiene actividad GTPasa este cataliza la hidrolisis de GTP en GDP y se asocia
nuevamente al dímero βγ.
Existe una toxina producida por Vibrio colerae que provoca el cuadro clínico de Cólera, donde este
promueve la ADP-ribosilación, que bloquea la actividad GTPasa de la subunidad α
s
de la proteína G
s
como
consecuencia tenemos un gran aumento de AMPc y por la activación sostenida de la adenilato ciclasa a
nivel intestinal.
¿Cómo actúa el AMPc?
Al aumentar la concentración intracelular de AMPc este activa a la proteína Quinasa que forma una
unidad tetramérica conformado por dos subunidades reguladoras R y dos subunidades catalíticas C, es
decir que en ausencia de AMPc este se encuentra de manera inactiva, formando una unidad tetramérica,
una vez que el AMPc llega a las subunidades reguladoras R las subunidades catalíticas C se separan de las
subunidades R y comienzan a tener actividad catalítica.
Luego la proteína quinasa A transfiere fosfatos de ATP a restos de serina o treonina de proteínas que
cuando se fosforilan adquieren funcionalidad.
¿Qué acciones desencadena el AMPc?
Fosforilación enzimática (covalente) gracias a la proteína
quinasa dependiente de AMPc que puede estimular o inhibir a otras
enzimas de las vías metabólicas.
Modulación de la actividad de sistemas de transportes de
membrana en inclusive a aquellos que no dependen de fosforilaciones,
por ej estímulos odoríferos asociados a proteína G
olf
A nivel nuclear puede influir sobre la transcripción, en especial
sobre los elementos de respuesta dependientes de AMPc o CRE, que
estimulan la transcripción de enzimas como la fosfoenolpiruvato
carboxiquinasa, tirosina aminotransferasa y diferentes Cit P450.
Fosfodiesterasa. Esta enzima inactiva al AMPc y lo convierte en
adenosina -5’-monofosfato, que carece de actividad. Sustancias como
cafeína, teofilina inhiben a esta enzima y mantienen la acción del AMPc.
Las Catecolaminas a través de receptores adrenérgicos α
i
y la insulina
activan a la fosfodiesterasa y por ende reducen la concentración de AMPc. Las proteínas fosfatasas
escinden estas fosforilaciones.
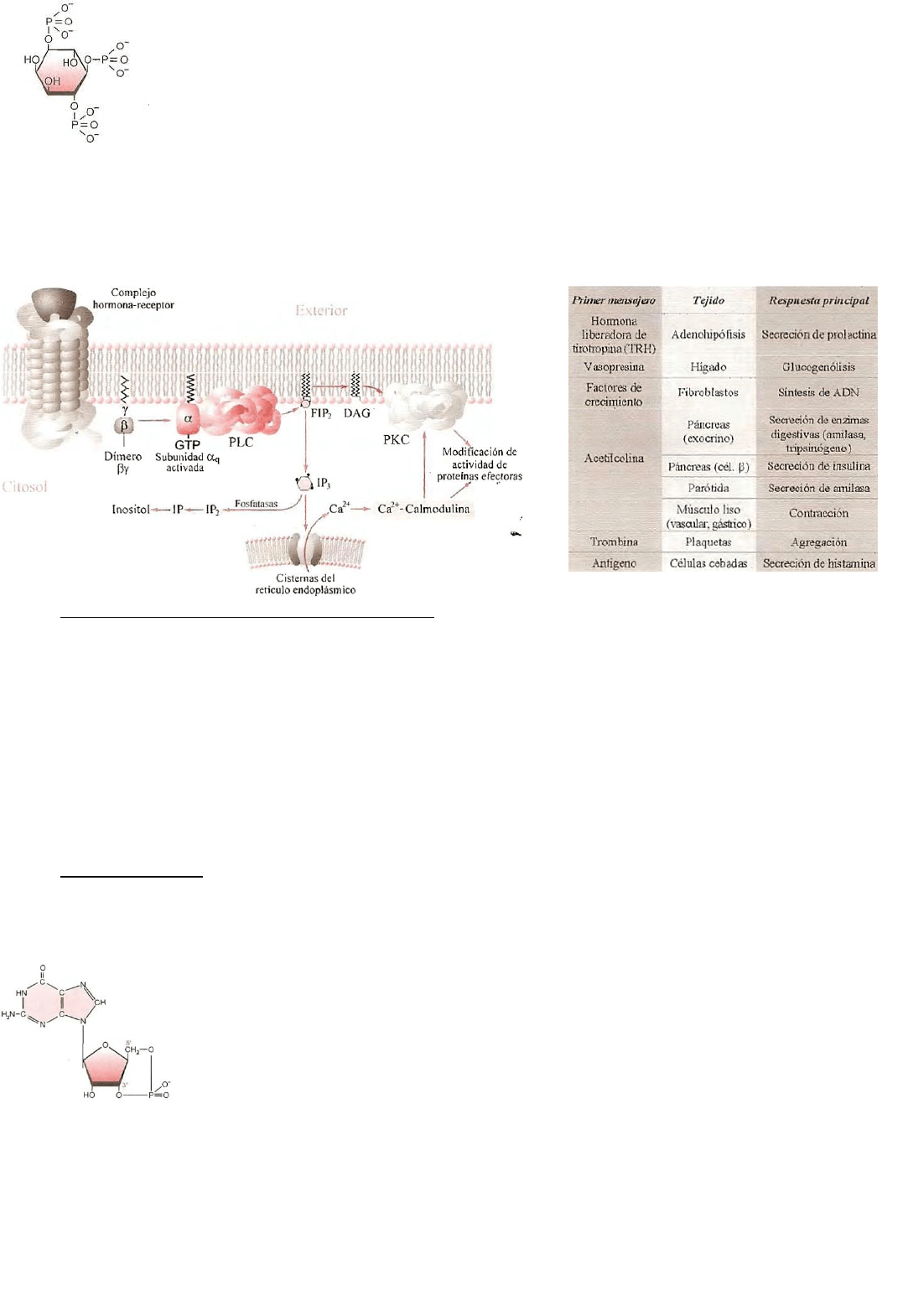
2. Sistema del fosfatidilinositolbisfosfato.
El fosfatidilinositol está presente en la monocapa lipídica interna de la membrana plasmática,
primeramente es fosforilado en los carbonos 4 y 5 del inositol para formar
fosfatidilinositolbisfosfato (FIP
2
), a partir de allí integra un sistema de señal de
transducción.
Cuando el ligando interactúa con el receptor, la subunidad α
q
intercambia
GDP por GTP y se libera del dímero βγ. Una vez formado el complejo α
q
-GTP
este activa a la fosfolipasa C (forma β) para hidrolizar al fosfatidilinositol 4-5
Página 6 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
bisfosfato integrado a la membrana y luego desintegrarse en dos productos como el
diacilglicerol (DAG), e inositol-1-4-5 trifosfato que serán los segundos mensajeros de la
señal. Otra fosfolipasa C, (la forma γ) se asocia a receptores proteína-tirosina quinasa.
El inositol trifosfato (IP
3
) se dirige hacia el retículo endoplásmico (RE) donde
interactúa con receptores para provocar la liberación del Ca++ y desencadenar
diferentes respuestas celulares, para inhibir a la acción del (IP
3
) este debe ser
escindido por una fosfatasa transformándolo en (IP
2
), (IP
1
) e inositol, respectivamente.
El diacilglicerol, queda anclado a la membrana y actúa como segundo mensajero activando a la
proteína quinasa C de la membrana que fosforila factores de transcripción y procesos vinculados a la
multiplicación celular. Para inhibir a la proteína quinasa C el diacilglicerol debe ser hidrolizado. Existe una
sustancia llamado forol de similitud con la estructura del diacilglicerol que induce a la formación de
tumores.
3. Lípidos en sistemas de transmisión de señales.
El diacilglicerol, puede ser obtenido atraves de la fosfolipasa D (PLD) que hidroliza la fosfatidilcolina, y el
ácido fosfatídico obtenido es atacado por el ácido fosfatídico hidrolasa en diacilglicerol y fosfato. El
diacilglicerol comienza a integrarse como segundo mensajero.
La ceramida se puede obtener a partir de la esfingomielina por acción de la esfingomielinidasa que es
activado por ligandos como citoquinas, 1,25-(OH)
2
–D
3
, la ceramida cobra importancia como segundo
mensajero en activaciones de procesos de apoptosis.
El fosfatidilinositol-3-4-5-trifosfato induce la activación de proteína quinasa B y puede ser formado a
partir de fosfatidilinositol-4-5-bisfosfato por la fosfatidilinositol-3-quinasa (PI3K), esta enzima es activada por
factores de crecimiento, hormonas y neurotransmisores.
4. GMP-3’-5’-ciclico
El GMP-3’-5’-ciclico es generado a partir de GTP gracias a la adenilato ciclasa ubicada en la
membrana plasmática y es activada por óxido nítrico y monóxido de carbono. El GMPc participa en
diversas funciones como por ej:
Activa proteína quinasas que participan en el crecimiento y proliferación
celular.
Relajación de musculo liso y por lo tanto es vasodilatadora.
Estimula a la diuresis y natriuresis.
Captación de estímulos luminosos y olfatorios, regulando la apertura y cierre
de canales de Na+ por ej la rodopsina, fotorreceptor de bastoncillos, estimula la
GMPc fosfodiesterasa, disminuyendo el nivel de GMPc para cerrar los canales de
Na+ e hiperpolarizar y generar impulso nervioso responsable de la sensación lumínica.
Página 7 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
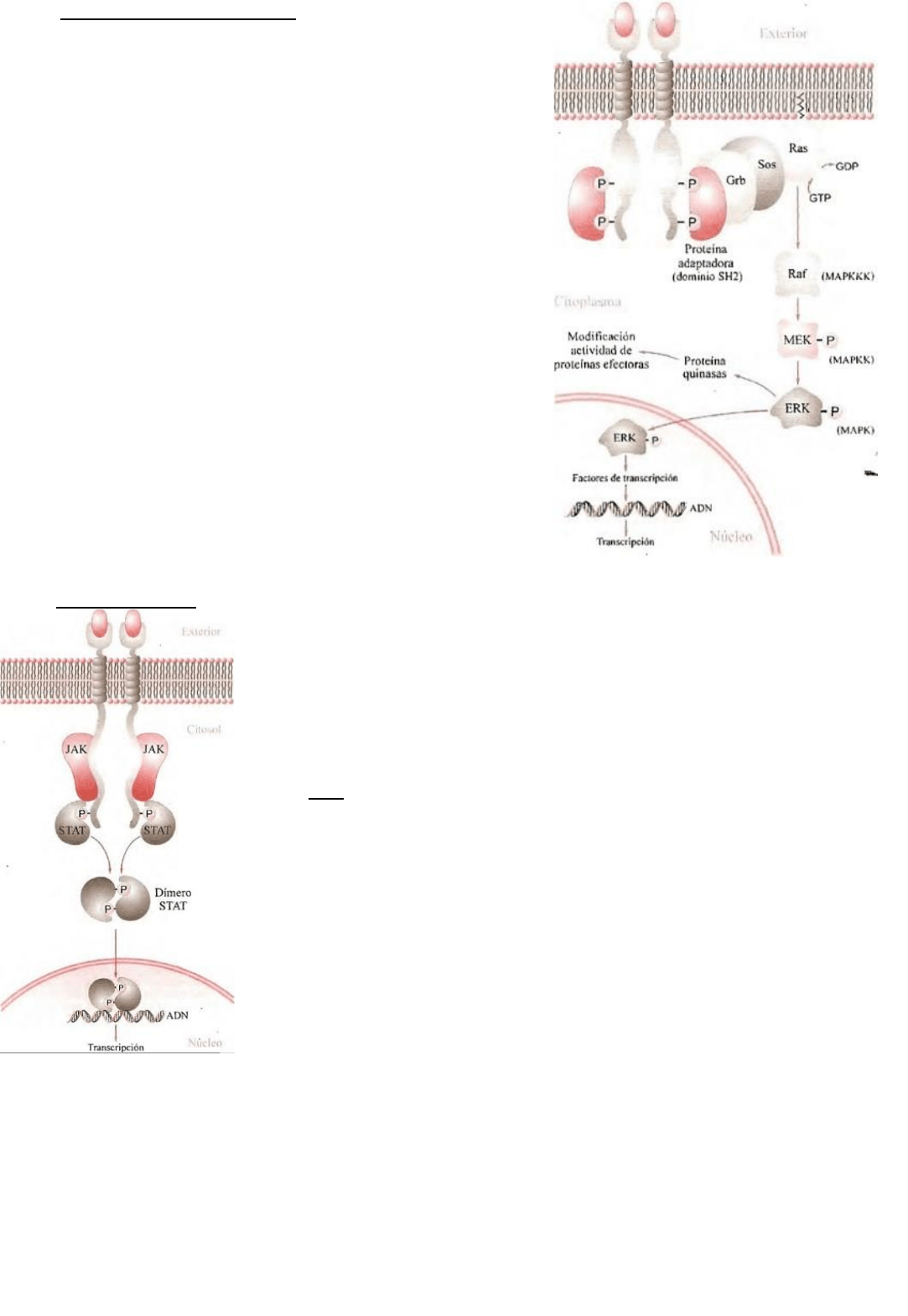
5. Sistemas Ras y quinasas MAP.
Es un sistema que no genera segundos mensajeros de
moléculas pequeñas sino que desencadena una cascada de
proteínas quinasas. Si un receptor con actividad tirosina quinasa
intrínseca o extrínseca es activado por su ligando, por lo tanto se
fosforilarán proteínas con dominios SH2 y SH3 como las Grb que
actúan uniendo proteínas como Sos. El complejo Grb-Sos
interactúa con proteínas del lado citosólico llamados Ras a
quienes los activa.
La proteína Ras, tienen actividad GTPasa y cuando se
encuentran asociados a GDP están de forma inactiva si
interactúan con un complejo Grb-Sos estos intercambian GDP
por GTP que activa a la proteína Ras que posee gran capacidad
de autorregulación por su actividad GTPasa. La estimulación de
Ras comienza una cascada de fosforilaciones en restos de serina-
treonina de las quinasas MAP que a su vez activa a la primera,
segunda y tercera proteína que es la responsable de influir en la
proliferación y diferenciación celular. La activación de Ras-GTP,
activa a su vez a la proteína Raf, y que luego fosforila las
quinasas MAP, regulados por señales extracelulares llamadas ERK.
Estas quinasas fosforilan muchas proteínas y factores de
transcripción en el nucleo.
La proteína Ras participa en la regulación y control de la
multiplicación y diferenciación celular. Una mutación del gen
codificante de Ras desencadena un descontrol en la
proliferación celular y transformarse en tejido maligno
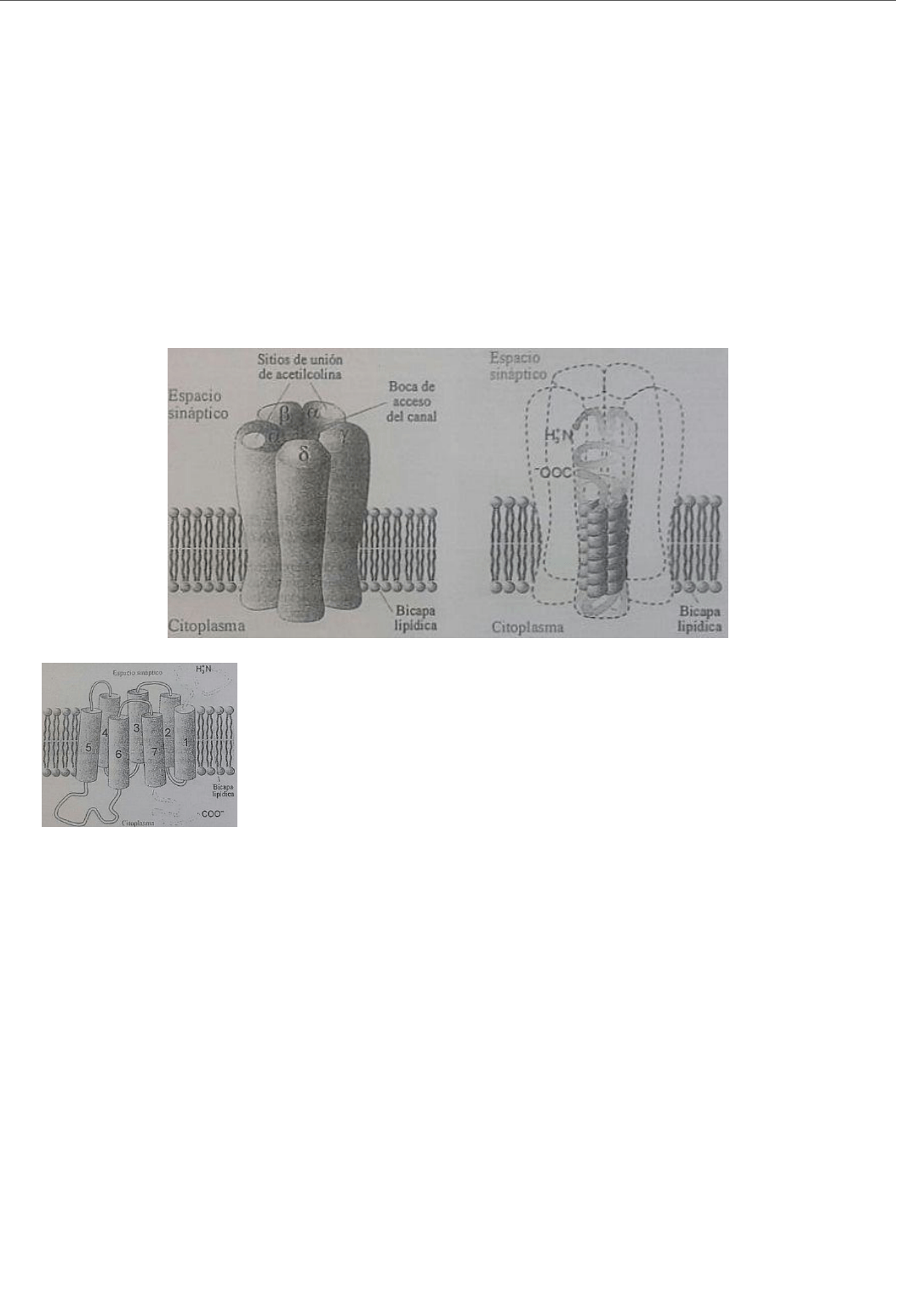
6- Sistema JAK-STAT.
Las proteínas STAT contienen dominios SH2, las hormonas y citoquinas se
asocian a tirosina quinasa tipo Janus (JAK) atraves del receptor cuyo lado
citoplasmático activa quinasas para fosforilar restos de tirosina donde se fijaran
las proteínas STAT con dominios SH2, en una segunda fosforilación las proteínas
STAT se dimerizan y se trasladan al nucleo, para estimular a la transcripción de
sus genes. Esta vía es utilizada por la hormona de crecimiento, prolactina,
diversas citoquinas, interferón γ, etc.
7- TOR.
Es una serina/treonina quinasa y se denomina m-TOR en el caso de los
mamíferos y que tiene capacidad de formar complejos con otras proteínas,
donde m-TOR es el centro catalítico. Existen dos complejos, m-TOR I y m-TOR II
que poseen unidades reguladoras llamada Raptor especifico de m-TORC I y
Rictor en m-TORC II. Ambos complejos difieren en sus funciones y propiedades.
El complejo m-TORC I cuando se activa en el convergen diferentes vías de
señales como ser el de las activadas por insulina, y factores de crecimiento
semejante a la insulina (IGF- I) de las que forman parte, PI3K, PDK1 y AKT, por
factores de crecimientos (EGF) que comprende las MAPK, por niveles de
energía, donde el efector principal es la AMP quinasas (AMPK). Estos estímulos
provocan la activación de m-TORC I iniciando fosforilaciones de diferentes
sustratos, que aumentara la síntesis de proteínas, producción de ribosomas,
proliferación y crecimiento celular, e incremento del metabolismo celular. Caso contrario, la falta de dieta,
factores de crecimiento y señales de estrés celular deprimen el complejo m-TORC I y por ende promueven a
la AUTOFAGIA. El m-TORC I favorece la lipogénesis.
El complejo m-TORC II es activado por factores de crecimiento (por ej. IGF-I) e insulina atraves de PI3K. un
importante sustrato de este complejo es la serina treonina quinasa AKT, que una vez activada por fosforilación
promueve la proliferación, migración celular y regulación de procesos metabólicos. Una de sus funciones
mejor conocida del complejo m-TORC II es el control de la organización del Citoesqueleto de actina.

Página 8 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
8- Señal de Ca++
El calcio intracelular normalmente es de concentración baja 0,1 microM y resulta del balance entre el
medio intracelular y el medio extracelular pero sin embargo diferentes estímulos pueden desencadenar
cambios en las concentraciones de calcio, que sirven como señal, pero a su vez son estrictamente
controlados, gracias a transportadores de flujos rápidos de Ca++, por lo tanto podemos decir que el calcio
cumple funciones de mensajeros de sistemas de señales.
El ingreso de Ca++ del medio extracelular responde a estímulos como despolarización de membranas,
uniones de ligandos exteriores o de diferentes mensajeros químicos desde el interior celular. Por otra parte la
liberación de calcio de compartimientos como retículo sarco - endoplásmico, mitocondrias, aparato de
Golgi, pueden ser estimulados por el mismo calcio o también por segundos mensajeros químicos, como
inositol trifosfato (IP3) producido por la fosfolipasa C que presenta cinco isoformas activadas por diversos
receptores, ADP-ribosa cíclico, acido nicotínico adenina dinucleótido fosfato (NAADP) y esfingosina-1-fosfato,
que impulsan a las salida del Ca++ desde los depósitos intracelulares.
El calcio una vez ingresado hacia el citosol se incorpora a diferentes proteínas que pueden ser, troponina
C, sinaptotagmina, proteínas S100, anexinas y en especial la CALMODULINA. Todas presentan una estructura
en común con dos hélices alfa llamadas E y F dispuestas de manera perpendicular y se los denomina ¨mano
EF¨
La calmodulina, como bien nombramos anteriormente puede fijar 4 átomos de Ca++, es decir que
presenta cuatro sitios de unión al Ca++ en ambos extremos de la molécula
que presenta forma globular, compuestos por manos EF. Entre ambos
segmentos se extiende un largo segmento alfa hélice que sufre cambios
conformacionales una vez que se une el Ca++ y adquiere actividad
reguladora sobre proteínas blanco que integran cascadas de
fosforilaciones y que a su vez regularan otras proteínas quinasas o enzimas,
canales iónicos y factores de transcripción, como por ej el factor de
transcripción CREB, activado por proteína quinasa A, dependiente de
AMPc, estimulado por Ca++-calmodulina.
Tanto las proteínas quinasas y las fosfatasas, cobran gran importancia
fisiológica, en el caso de las proteínas quinasa, que dependen de AMPc,
otras de GMPc, DAG, Ca++ y de receptores tirosina quinasas. La
fosforilación regula diferentes sistemas de transporte, por supuesto debemos
incluir la multiplicación celular, síntesis de ácidos nucleicos y proteínas. Las
proteínas fosfatasas por su parte tienen la misma importancia que las
proteínas quinasas y tiene especificidad por el sustrato y su actividad puede
ser regulada por diversos mecanismos y entre ellos como la fosforilación y
defosforilacion.
Página 9 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
7 RECEPTORES DE NEUROTRANSMISORES
Los receptores de neurotransmisores son glicoproteínas integrales con múltiples segmentos que están
insertados en la membrana plasmática, de las células postsinápticas, existen dos tipos de receptores:
Receptores colinérgicos. la acetilcolina es un neurotransmisor que utiliza este tipo de receptores que
puede desencadenar dos tipos de acciones que son similares a las ejercidas por la nicotina (bloqueadas por
D-tubocurarina), mientras que otras son iguales a las de muscarina (bloqueada por atropina) de allí que se
nombraron dos tipos de receptores dentro de los colinérgicos: NICOTINICOS Y MUSCARINICOS.
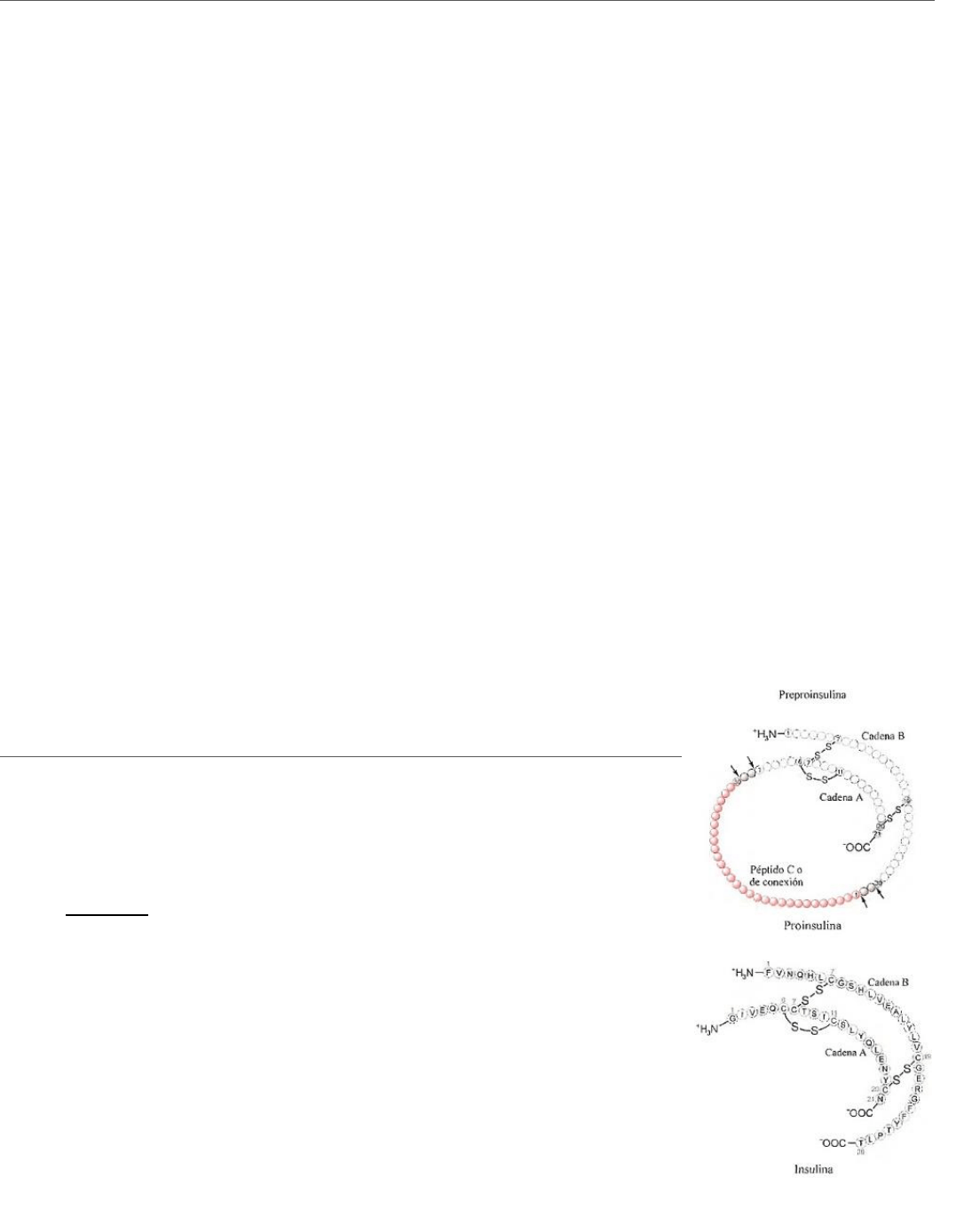
a. Receptores nicotínicos: son glicoproteínas integrales de membrana postsinápticas, presenta cinco
subunidades (α
2,
β, γ y δ) excepto los del sistema nervioso central que poseen (α
2
y β
3
). Dispuestos
alrededor de un canal central que se inserta de manera perpendicular a la superficie celular,
permitiendo sobresalir hacia la hendidura sináptica del citoplasma. Cada monómero de la estructura
del receptor mira atraves de su extremo N-terminal hacia la hendidura sináptica, con cuatro
segmentos hidrofóbicos transmembrana y dos dominios hidrofílicos externos alfa donde se unen dos
neurotransmisores, una vez activados estos receptores por acetilcolina, se promueve la apertura del
poro central aumentando la permeabilidad para el Na+ y K+ y desencadenar la despolarización de
membrana por el ingreso de Na+. Pertenecen a este tipo de receptores lo ionotrópicos.
b. Receptores muscarínicos. son glicoproteínas que presentan siete segmentos de hélices
transmembrana, con un dominio hidrofóbico, glicosilado y pequeñas asas que
unen las hélices 2-3, 4-5 y 6-7 y emergen al espacio sináptico. otras tres asas
hidrofílicas unen las hélices 5-6 y el extremo C-terminal emergen hacia el
citoplasma. Existen tres subtipos de receptores: (M 1) de localización en ganglios
y células exocrinas, (M2) en musculo liso y miocardio, (M3) en musculo liso y
glándulas. Todos estos receptores son metabotrópicos, y los mediadores de sus
acciones son las proteínas G, por ej: los M1, M3, M5 activan a las fosfolipasa C
atraves de proteínas G
q
que desencadenan el aumento de concentraciones de
Ca++ y los receptores M2 y M4 interactúan con proteínas G
i
inhibiendo a la adenilato ciclasa por
reducción del AMPc. En musculo cardiaco estos receptores aumentan la concentración de K+ e
hiperpolarizan la membrana aunque también modulas los canales de Ca++.
Receptores adrenérgicos. Existen dos tipos de receptores adrenérgicos: α y β son glicoproteínas
integrales que pueden ser fosforilados por proteínas quinasas y todos son metabotrópicos. Los receptores β
están mediadas por proteína G
s
por lo tanto activan a la adenilato ciclasa, y eleva el nivel de AMPc
intracelular. Promueven la apertura de los canales de Ca++ en músculos cardiaco y esquelético.
Los receptores adrenérgicos α
1
activan a la fosfolipasa C y por ende promueve la liberación de Ca++
intracelular y activación de proteínas quinasas. Los receptores adrenérgicos α
2
inhiben la adenilato ciclasa,
para disminuir los niveles de AMPc intracelular para desactivar a la proteína quinasa. Los receptores
adrenérgicos α
3
promueven la apertura de los canales de K+ y cierre de los canales de Ca++
Receptores dopaminérgicos. Son metabotrópicos y están asociados a proteína G.
Receptores GABAergicos. Son homologas a los receptores colinérgicos nicotínicos, son ionotrópicos y
permiten el ingreso de Cl- hiperpolarizando la membrana y es por ello su acción inhibitoria.
Página 10 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
BASES BIOQUIMICAS DE LA ENDOCRINOLOGIA (II)
HORMONAS Y OTROS INTERMEDIARIOS QUIMICOS
8 HORMONAS
De acuerdo a su naturaleza química estas pueden ser:
Esteroides: derivan del colesterol (CPPF) por ej. Glucocorticoides, aldosterona y andrógenos que
provienen de la corteza suprarrenal y estrógenos, progesteronas de los ovarios, testosterona de los
testículos y 1,25-(OH)
2
–D3.
Derivados de aminoácidos: como ser la adrenalina o epinefrina, noradrenalina o norepinefrina,
tiroxina y triyodotironina, todos derivados de la tirosina. La melatonina es deriva del triptófano.
Derivados de ácidos grasos. Prostaglandina, tromboxanos y leucotrienos llamados eicosanoides.
Péptidos. Tenemos a la vasopresina, ACTH, MSH, glucagón, gastrina, calcitonina, etc
Proteínas. Hormonas paratiroideas, insulina, prolactina (PR), folículo estimulante (FSH), luteinizante
(LH) etc.
Las hormonas pueden desencadenar diversas acciones:
Actuar sobre mecanismos de transporte en membranas celulares, modificando el flujo de
metabolitos e iones atraves de la membrana.
Modificación de la actividad enzimática. Ejercen propiedades regulatorias donde aumentan o
disminuyen la actividad enzimática.
Acciones sobre la síntesis de proteínas, es decir modulan la síntesis de enzimas y otras proteínas.
Actúan predominantemente a nivel del ADN nuclear, regulando los procesos de transcripción
génica.
Propiedades generales de las hormonas:
Actividad. Muchas hormonas actúan en cantidad mínima y sin embargo desencadenas respuestas
intensas.
Vida media. Las hormonas deben ser degradadas y convertidas en productos inactivos, pues su
acumulación en el organismo puede alterar tras funciones metabólicas.
Velocidad y ritmo de secreción. Las hormonas actúan frente a estímulos por ej la insulina que
actúan en concentraciones elevadas de glucosa.
Especificidad. Cada hormona actúa sobre una célula blanco o diana.
9 PANCREAS
La función de esta glándula es producir y secretar hormonas como insulina
atraves de sus células β, glucagón a través de sus células α las células δ
sintetizan somatostatina y gastrina, y por ultimo las células PP sintetizan
polipéptido pancreático. A continuación veremos solo las tres primeras
hormonas que competen a este capítulo.
a. INSULINA.
La insulina está constituida por dos cadenas polipeptídicas llamadas A
que contiene 21 Aa y otra B que posee 30 Aa. Ambos están unidos por dos
puentes disulfuro, en posiciones 7 y 20 de la cadena A a las cisteínas 7 y 19 de
la cadena B. entre las dos cisteínas de la cadena A de posiciones 6 y 11 se
ubica el tercer puente disulfuro intracatenario. La estructura terciaria y
cuaternaria de la insulina es importante para su determinación de su
actividad.
Existe una diferencia de tres aminoácidos entre la insulina bovina, ovina,
equina de la insulina humana, sin embargo esas hormonas son activas en el
hombre. La insulina bovina difiere en un aminoácido (el Aa-C- terminal
numero 30) de la cadena B y es la alanina, mientras que en la humana es
Página 11 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
treonina. Con procedimientos enzimáticos es posible sustituir esa alanina por treonina y obtener insulina
humana y ser de uso comercial.
La biosíntesis se da en Retículos endoplásmico rugoso de las células β del páncreas primeramente es
sintetizado como preproinsulina de 111 Aa, y dentro de la cavidad del reL pierde el péptido líder de 26 Aa
del extremo N-terminal, para convertirse en proinsulina sin actividad hormonal. Por lo tanto presenta sus
primeros 30 Aa, que corresponden a los de la cadena B de la insulina y los últimos 21 Aa corresponden a los
de la cadena A. entre ambos queda un segmento de 34 Aa, llamado péptido C.
La secreción de la proinsulina se realiza mediante vesículas, que salen del complejo Golgi, a partir de
allí las peptidasas liberan la insulina activa del resto de la cadena y por un lado tendremos el péptido C y
por otra parte la insulina que serán liberados de manera equimolar. La determinación del péptido C
permite conocer la cantidad de insulina endógena. El estímulo más importante para la secreción de
insulina es el aumento de glucosa que una vez dentro de la célula beta debe ser metabolizado y
fosforilado por la glucoquinasa, para luego estimular a la síntesis de insulina y por otra parte poder ingresar
a la vía glucolítica y obtener ATP. El aumento de ATP promueve el cierre de los canales de K+ y por ende
se despolariza la membrana y se abren los canales de Ca++ que estimularan el transporte de las vesículas
para ser exocitadas. El AMPc es otro regulador de la liberación de insulina, porque moviliza el Ca++desde
la mitocondria hacia el citosol.
Las sulfonilureas, produce cierre de canales K+ en el tratamiento de pacientes diabéticos, y con ellos
se elevan los transportes de las vesículas de insulina sin embargo el dióxido abre los canales de k+ e
inhibe la liberación de la insulina.
Niveles elevados de Aa arginina y lisina y ácidos grasos libres promueven la liberación de insulina, y por
otra parte la ingesta de alimentos activa la secreción de hormonas gastrointestinales que impulsan a la
liberación de insulina, como puede verse en situaciones post-prandiales. El glucagón es activador de la
secreción y la estimulación vagal y receptores beta adrenérgicos promueven la secreción y la activación
de receptores α-adrenérgicos inhibe la secreción de insulina.
Los niveles basales de insulina es de 0,4-0,8 ng por ml, luego de ocho minutos después de la ingesta
esta se eleva hasta un máximo que alcanza cerca de los 30-45minutos y llega valores de 4ng por ml.
La degradación, se hace gracias a la insulinasa en hígado, riñón y otros tejidos.
Mecanismo de acción de la insulina: esta hormona actúa sobre un receptor especifico, glicoproteína
integral de membrana, con actividad tirosina-
quinasa en su porción citosólica, presenta
cuatro subunidades por lo tanto es un
heterotetrámero, las subunidades alfa se
encuentran en el lado externo de la
membrana y las subunidades beta atraviesan
toda la membrana, y en su porción citosólica
se ubica el sitio activo serina-tirosina quinasa.
Generalmente se encuentran desde 40 hasta
miles de receptores para la insulina por cada
célula como por ejemplo en hepatocitos.
La insulina una vez que se une al receptor
por las subunidades alfa este provoca un
cambio conformacional que se propaga
hacia las subunidades beta y activa la tirosina
quinasa, por lo tanto el receptor adquiere
capacidad para autofosforilarse, y fosforilar a
otras proteínas que tengan restos de SH2
mediante los cuales se unen al receptor. Las
mejores de estas proteínas son los sustratos del receptor de insulina, (IRS) ubicados en diferentes tejidos ya
sea en hígado y musculo como las (IRS-1 e IRS-2) también IRS-3 en tejido adiposo, fibroblastos y
hepatocitos como así también IRS-4 en riñón embrionario.
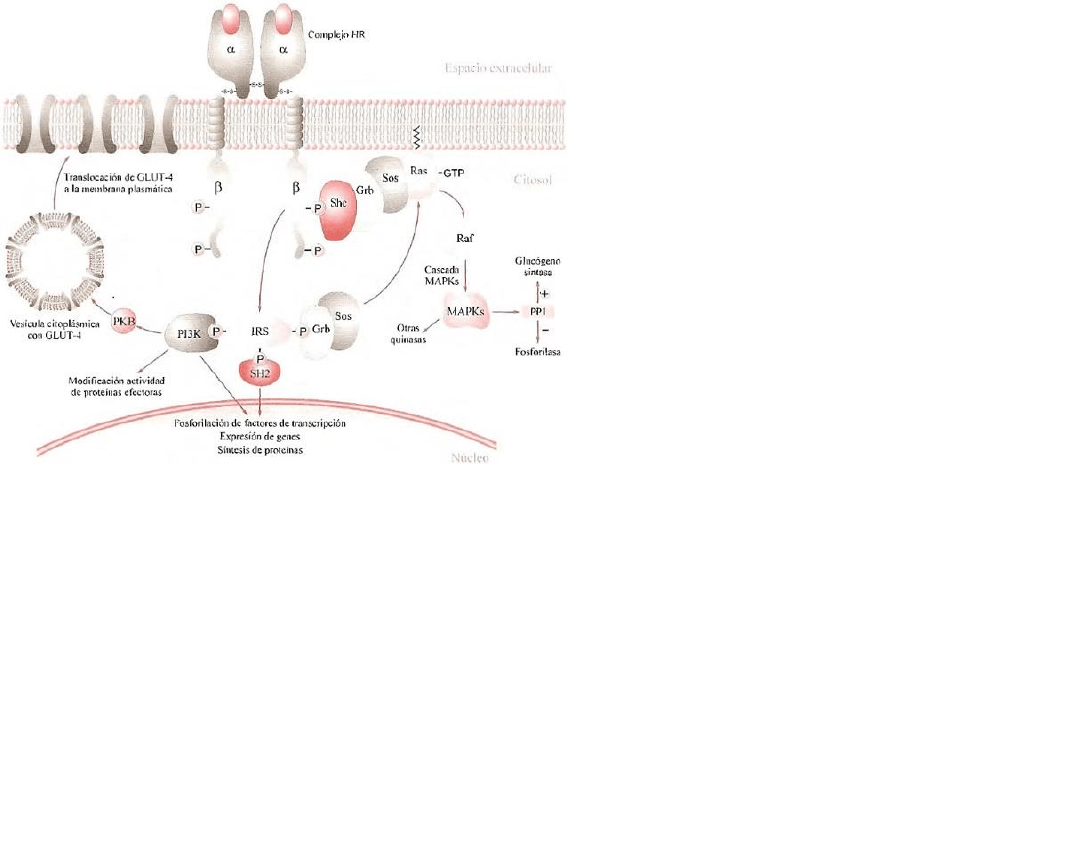
La actividad tirosina-quinasa estimulada por insulina, fosforila proteínas sustratos y las fosfotirosinas de
IRS fijan otras proteínas que contengan dominios SH2 entre ellas la fosfatidilinositol 3-quinasas y Grb-2. Una
de las vías importantes es la de fosfatidilinositol 3-quinasa (PI3K) que se activa por la interacción con la
proteína IRS para formar (PI-3, 4,5-P3) y luego este se une a proteínas con dominios PH. Esta unión
favorece la activación de la proteína quinasa B (PKB) y esta última desencadenara una gran fosforilación
de diversas proteínas efectoras y algunas de ellas son:

Página 12 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
Activación del transporte de glucosa. Esto permite la translocación de transportadores GLUT 4 en
tejido adiposo. En musculo la hipoxia y contracción estimula a la exposición de transportadores.
Síntesis de glucógeno: básicamente inactiva a una enzima que fosforila a la Glucógeno Sintasa
(recordar: que en su manera desfosforilada está activa)
Glucolisis. Fosforila a la FFK II, para proveer fructosa 2,6 bisP que es un potente estimulador de la
FFKI
Gluconeogénesis. Inhibe la glucosa - 6 fosfatasas.
Conversión de glucosa en ácidos grasos. estimula a la conversión de glucosa en ácidos grasos.
Acciones sobre la actividad génica mediadas por la vía de PI3K. estimula a la síntesis de
hexoquinasas en musculo, inhibición de la síntesis de fosfoenolpiruvato carboxiquinasa y activa la síntesis
de glucosa-6-P DH.
Metabolismo del TAG: inhibe a la lipasa sensible a hormonas de los adipocitos por la fosfodiesterasa
que rompe el AMPc e inactiva la lipolisis, por otra parte activa al complejo PDH y Acetil-coa-carboxilasa,
la acción de esta enzima requiere PI3K. también estimula a la lipoproteína lipasa del endotelio vascular
aumentado la oferta de ácidos grasos para la síntesis de TAG por la utilización de glicerol 3-P
Síntesis de proteínas. participa en la regulación del transporte de Aa mediante señales IRS-PI3K y
especialmente lo hace en los factores de iniciación FIe2b y FIe4E, la insulina activa vías mitogénicas, y
estimulan fosfatasas que modulan numerosas enzimas que estimulan la proliferación y diferenciación
celular.
El complejo enzima-receptor es internalizado por endocitosis y se disocia el receptor de la insulina y
regresa a la membrana externa y la insulina es degradada por lisosomas.
Acciones metabólicas.
Los principales tejidos de acción de la insulina son: musculo, tejido adiposo y hepático.
1. Efectos sobre el transporte de metabolitos. Como por ejemplo estimula a la formación de
transportadores GLUT 1 y 3 que actúan en niveles bajos de Glucemia, GLUT 4 mediante sistemas de señales (IRS-
PI3K) en musculo y tejido adiposo que recluta estos transportadores y los expone en la membrana plasmática,
GLUT 1 en tejido miocitos y tejido adiposo.
2. Efectos sobre el metabolismo de hidratos de carbono. En efecto es la hormona HIPOGLUCEMIANTE. Que
actúa en diversos órganos:
Hígado. estimula a la actividad de la glucoquinasa y diversas vías que utilicen la glucosa como sustrato,
por ejemplo la Glucogenogénesis, vía de las pentosas fosfato, lipogénesis, descarboxilación oxidativa
del piruvato, mediante las enzimas que lo catalizan, es decir que la insulina los activa y por otra parte
inhibe aquellas vías que promueven el aumento de la glucemia, por ejemplo la glucogenolisis al cual lo
deprime, como así también a la gluconeogénesis. Y todas las enzimas que participan en dicha vía.
Musculo y tejido adiposo. Mediantes los transportadores GLUT4 promueve el ingreso de glucosa a
ambos tejidos para formar glucógeno.
3. Efectos sobre metabolismo de lípidos. estimula a la lipogénesis dado a que recibe los acetil-coa desde
la descarboxilación oxidativa del piruvato, glucolisis y vía de las pentosas fosfato para obtener NADPH y
síntesis de TAG en hígado, tejido adiposo, glándula mamaria lactante y otros tejidos. Activa a la
liproteina lipasa de capilares periféricos para sacar ácidos grasos de tejido adiposo y sintetizar TAG.
4. Efectos sobre el metabolismo de proteínas. estimulando a la captación de Aa, e incorporándolos a
proteínas, e inclusive induce a los procesos de transcripción y traducción de hecho es posible ver la
disminución de la urea producida en hígado.
5. Efectos sobre potasio.
Acciones paracrinas: en conjunto con la somatostatina, inhibe la síntesis de glucagón
Cuadros clínicos.
Hipofunción: produce un cuadro clínico de diabetes mellitus.
Hiperfunción: en casos de tumores provoca hipoglucemia hasta inclusive shock hipoglucémico, con
pérdidas de conciencia, convulsiones, coma y muerte.
b. GLUCAGON.
Es un polipéptido de 29 Aa que posee metionina y triptófano y carece de cisteina como aminoácidos, se
sintetiza originalmente, como preproglucagón que se convierte en proglucagón y glucagón. El proglucagón
de 160 Aa presenta a su vez péptido relacionado con glicentina, y péptidos tipo glucagón 1 y 2 (GLP 1 y GLP
2). La Glicentina es un polipéptido de 69 Aa que contiene al glucagón de 29Aa y un péptido relacionado. Es
producido en intestino en mayor proporción que en el páncreas, es por ello se lo llama enteroglucagón. A partir
de GLP1 se obtiene la incretina que estimula a la secreción de insulina.

Página 13 de 13
RECEPTORES Y HORMONAS | Lenis Fabio Leonardo
La concentración de glucagón en sangre es de 75pg por ml. La vida media del glucagón es de 6min y el
principal regulador de la secreción del glucagón es exclusivamente el aumento de la glucemia; mientras que la
hipoglucemia lo inactiva.
El incremento de aminoácidos, como arginina, alanina, estimulación del sistema simpático, catecolaminas,
hormonas gastrointestinales y glucocorticoides estimulan la secreción y por otra parte los aumentos de niveles
de ácidos grasos la inhiben.
Mecanismo de acción.
El glucagón actúa sobre receptores de hepatocitos y tejidos adiposos asociados a proteínas G
s
que
estimulan a la adenilato ciclasa para aumentar las concentraciones de AMPc para iniciar la cascada de
fosforilaciones.
Presenta diversas acciones y entre ellas es proveer sustratos que aporten energía a los tejidos.
1) Efectos sobre el metabolismo de hidratos de carbono.
A través del aumento del AMPc y proteína quinasa A estimula a la glucógeno fosforilasas; mientras que por
otra parte inhibe a la glucógeno sintasa. Los puntos de acción de esta hormona son en tejido hepático y no
afecta al tejido muscular. Es importante destacar que el glucagón aumenta los ácidos grasos libres en plasma y
su capacidad de ser Hiperglucemiante se potencia con la gluconeogénesis.
2) Efectos sobre el metabolismo de lípidos
En tejido adiposo incrementa el AMPc para activar a la lipasa sensible a hormonas; por lo tanto se
degradarán los TAG, se liberarán ácidos grasos, aumenta la β – oxidación de ácidos grasos lo que
disminuye las concentraciones de NAD y por ende se reprime la capacidad de oxidar la glucosa. Es por
ello que aumenta las concentraciones de acetil – CoA así como también la formación de cuerpos
cetónicos.
Efectos sobre el metabolismo de nitrogenados
Favorece un balance nitrogenado negativo porque estimula al catabolismo nitrogenado y hay un
aumento de urea, creatinina y ácido úrico por orina.
c. SOMATOSTATINA
Son producidas en las células δ del páncreas y en el enterocitos y células C de tiroides. Casi todos los
estimulantes de la secreción de insulina producen liberación de Somatostatina en páncreas. Tiene
efectos sobre la fosfotirosina fosfatasa y MAP quinasas por lo que tiene acciones antiproliferativas de
Somatostatina sobre células tumorales. Además de tener efectos inhibitorios sobre la secreción de las
hormonas de crecimiento en hipófisis, la Somatostatina deprime las de insulina, glucagón, gastrina,
secretina y VIP.
Receptores I (2).pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.