Introducción. thaiz
La malaria es la infección parasitaria de mayor impacto e incidencia en el mundo. La infección es
causada por parásitos protozoarios pertenecientes al género Plasmodium que invaden inicialmente
el hígado y luego los eritrocitos.
Cuatro especies causan la mayoría de las infecciones humanas: P. falciparum, P. vivax, P. malariae,
y P. ovale, de las cuales P. falciparum es la responsable de la presentación clínica más grave y de
mayor incidencia en casos de desenlace fatal.
Es cosmopolita (Que es común a gran número de países.), pero las zonas palúdicas por excelencia son las
zonas ubicadas entre los trópicos, se presenta en zonas tropicales en África, Asia y Latinoamérica,
es endémico en 91 países y en ocho tiene pequeñas áreas de transmisión
Se presume que la malaria se remonta a la prehistoria, siendo un padecimiento ocasionado por
parásitos y que se puede transmitir entre animales y humanos (zoonótica), que infecto a las especies
de primates del continente africano y que logró afectar a casi todas las áreas del planeta, con
excepción de la Antártica.
Existen muchas referencias sobre fiebres que azotaban a diferentes naciones cada cierto tiempo, por
ejemplo en China hacia el 2700 antes de Cristo, en el antiguo Egipto en el 1570 antes de Cristo y en
Mesopotamia aproximadamente en el 2000 a.C., siendo la medicina natural tradicional el único
recurso para tratarla.
Plasmodium ovale fue descrito por Stevens en 1922 pero hasta hace poco la malaria producida por
este protozoo no ha suscitado gran interés científico al considerarse infrecuente y al cursar con un
cuadro clínico leve fácilmente tratable con cloroquina. Recientemente se han descrito dos sub-
especies genéticamente diferentes de Plasmodium ovale: P. ovale curtisi y P. ovale wallikeri.
Taxonomía
Dominio: Eukarya
Reino: Protista
Filo: Apicomplexa
Clase: Aconoidasida
Orden: Haemosporida
Familia: Plasmodiidae
Género: Plasmodium
Especie: Plasmodium ovale
Morfología
El Plasmodium ovale presenta varios estadíos cuando se encuentra en el torrente sanguíneo. Cada
estadío tiene sus propias características:
Trofozoito
El joven presenta un pigmento que forma pequeñas masas de color marrón oscuro. Así mismo, tiene
forma de anillo que ocupa aproximadamente un tercio del tamaño del eritrocito. El citoplasma
forma un círculo alrededor de la vacuola.
El trofozoito maduro es compacto, generalmente no presenta vacuola y presenta pigmentos como el
trofozoito joven.
Esquizonte
Ocupan más de la mitad del citoplasma del eritrocito. El pigmento se encuentra concentrado en una
masa.
Gametocito
Se presentan dos tipos de gametocitos: macromgametocito y microgametocito.
Macrogametocito
Tienen la cromatina condensada. Puede tener forma oval o redondeada. Presenta un pigmento de
color marrón claro difundido por todo el citoplasma. Éste es homogéneo.
Microgametocito
Mantiene la forma del macrogametocito. El citoplasma es un halo incoloro o pálido. El pigmento se
encuentra distribuido en gránulos pequeños. Tiene la cromatina dispersa.
Características generales
El Plasmodium ovale es un protozoario que es el responsable de un porcentaje pequeño de los casos
de malaria en el mundo.
Es un organismo eucariota unicelular, lo que implica que están conformados por una sola célula y
que dentro de ésta se encuentra un núcleo celular, en el cual se encuentran contenidos los ácidos
nucleicos (ADN y ARN).
Es de vida parasitaria, lo que quiere decir que para desarrollarse completamente, obligatoriamente
necesita encontrarse dentro de las células de un huésped. En este caso, el huésped puede ser el ser
humano o algún otro vertebrado.
De igual forma, requieren de un agente vector, dentro del cual ocurre la fase sexual de su ciclo. El
vector del Plasmodium ovale es la hembra del género Anopheles, un tipo de mosquito.
En lo referente al hábitat, éste es limitado. La especie Plasmodium ovale se encuentra solamente en
África Occidental y algunos países asiáticos como Filipinas e Indonesia. También es común en
Papua Nueva Guinea.
Plasmodium ovale es un organismo cuyas células carecen de flagelos, por lo que su movilidad no
está condicionada por éstos.
Epidemiología:
P. ovale está ampliamente distribuido en zonas tropicales aunque no se han confirmado casos en las
Américas. Se considera que el número global de casos de malaria producidos por P. ovale podría
estar infradiagnosticado, en parte debido a las limitaciones de las técnicas diagnósticas en zonas
endémicas (baja prevalencia de P. ovale diagnosticado por microscopía: dificultades diagnósticas en
parte debidas a la baja parasitemia característica las infecciones por P. ovale asociadas a la falta de
acceso a técnicas que podrían proporcionar un diagnóstico de especie definitivo como la PCR).
Sin embargo, se estima que las dos especies de P. ovale podrían producir más de 15 millones de
casos anuales de malaria en África. Se postula que estas dos especies evolucionaron a partir de un
linaje parasitario ancestral común hace 1-2 millones de años, posiblemente debido a la introducción
de forma independiente de proto-parásitos de primates primitivos a los primeros homínidos. Las dos
especies son simpátricas (existen en la misma área geográfica/país o en áreas que se solapan) tanto
en Asia como en África y en ocasiones se han descrito coinfecciones por las dos especies en el
mismo individuo, lo cual apoyaría la teoría que la separación/ diferenciación biológica y no el
aislamiento geográfico (alopatría) ha impedido la recombinación genética entre P. ovale curtisi y P.
ovale wallikeri. La persistencia de dos especies diferentes podría ser debida a la incompatibilidad
entre los gametocitos de P. ovale curtisi y P. ovale wallikeri o a la producción de esporozoitos no-
infectivos si la fertilización cruzada se produce (aunque estos mecanismos no han sido
documentados previamente en Plasmodium sp. específicamente).
Ciclo de vida de Plasmodium.
La malaria es trasmitida principalmente al humano por la picadura de mosquitos hembra de género
Anopheles, quienes introducen la forma infectante del parásito al torrente sanguíneo. El ciclo de
vida del parásito inicia con el ingreso de los esporozoítos a la circulación luego de la picadura por el
mosquito
El ciclo de vida del parásito posee dos fases, una asexual que se da en el hospedero humano (flechas
azules) y una sexual que se da en el vector Anopheles spp. (flechas rojas).
En el humano, el ciclo empieza con la fase exoeritrocítica (A) cuando por la picadura de mosquitos
hembra del genero Anopheles, se introduce la forma infectante del parásito (esporozoítos) al
torrente sanguíneo (1). Luego los esporozoítos migran al hígado en aproximadamente 30 minutos,
donde logran evadir la respuesta inmune de los macrófagos de Kupffer e infectan los hepatocitos
(2). Una vez dentro del hepatocito maduran, aproximadamente en 4 semanas (tiempo de
incubación) a esquizontes tisulares (3). Además, en las especies de P. vivax y P. ovale existe otra
forma del parásito, el hipnozoíto (4), donde el parásito persiste en forma latente dentro del
hepatocito y es el responsable del fenómeno de recaída meses después de la infección primaria. Con
la ruptura de los esquizontes tisulares se liberan merozoítos al torrente sanguíneo (5), iniciando la
fase eritrocítica del ciclo (B), en la cual los parásitos se adhieren e invaden los eritro citos (6). En
los eritrocitos se desarrolla el estado de trofozoíto que pasa por un proceso de maduración,
acumulando progresivamente hemozoína, pasando por las formas de trofozoíto anular (7),
trofozoíto maduro (8) y esquizonte (9). El esquizonte eritrocítico acumula merozoítos y luego se
rompe (10) liberando merozoítos que invadirán otros eritroci tos para continuar con la etapa de
reproducción asexual eritrocítica del parásito. La liberación periódica de merozoítos de los
esquizontes eritrocíticos produce los paroxismos de la malaria posteriores al primer paroxismo.
Durante la fase eritrocítica, algunos trofozoítos se diferencian (11) a la forma sexual del parásito o
gametocito masculino (microgame tocito) o gametocito femenino (macrogametocito) (12). Los
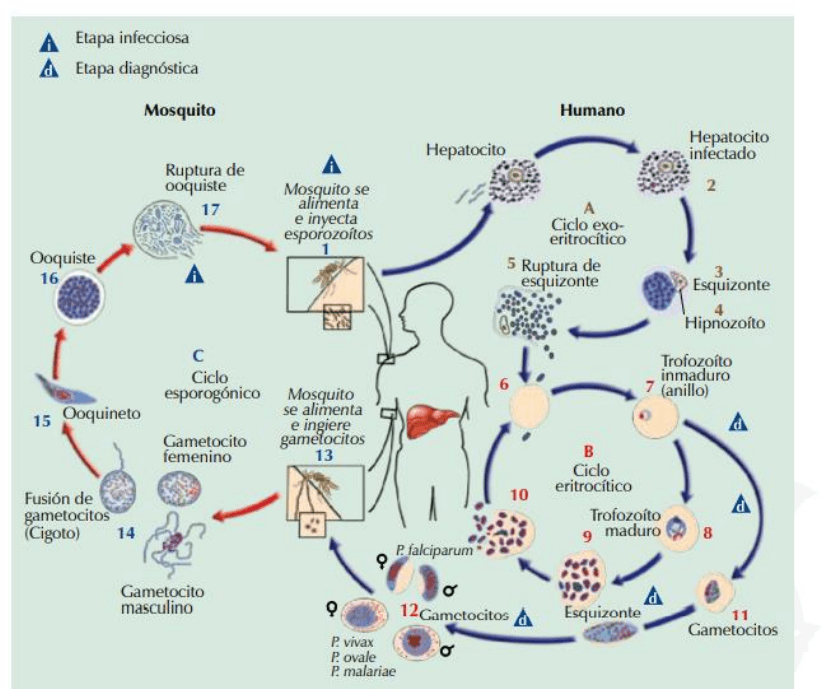
gametocitos circulantes son captados cuando el mosquito pica al hospedero durante la alimentación
(13) y una vez en el intestino del mosquito, los gametocitos se fusionan para formar cigotos (14) e
iniciar la parte sexual del ciclo en el mosquito (C). El cigoto se desarrolla a ooquinetos invasores
(15) que atraviesan el intestino medio y se transforman en un ooquiste (16), que a través de
divisiones mitóticas su cesivas, en 10 a 14 días producen miles de esporozoítos que luego son
liberados del quiste (17) y que migran a las glándulas salivales, desde donde pueden infectar al
humano para reiniciar el ciclo (1).
Signos y síntomas
La malaria se caracteriza por ataques repetitivos en los que se pueden apreciar los
siguientes síntomas:
• Fiebre elevada
• Sudoración intensa
• Escalofríos con temblores que pueden llegar a ser intensos.
• Diarrea
• Vómitos
• Cefalea intensa
• Dolor en los huesos
-Diagnóstico
Lo recomendado es que cuando una persona comienza a manifestar síntomas que puedan
acreditarse a la malaria, es acudir inmediatamente al médico para que este pueda iniciar el
proceso de realizar un diagnóstico acertado.
Son varias las pruebas que pueden aplicarse para diagnosticar esta patología.
Frotis de sangre periférica y gota gruesa
Para la primera, se coloca una gota de sangre en un portaobjetos, para extenderla
posteriormente con ayuda de otro portaobjeto, formando una capa fina.
En la gota gruesa, se colocan varias gotas en un portaobjetos, las cuales se unen y se
extienden, formando una capa uniforme y gruesa. Luego estas muestras son observadas al
microscopio para detectar la presencia del parásito.
Tinciones de sangre
Para el diagnóstico de esta patología, son muchas las tinciones que pueden utilizarse, tales
como: tinción de Giemsa, de Field, de Leishman y tinción con naranja de acridina.
Detección de antígenos parasitarios
Son pruebas rápidas comerciales que buscan detectar proteínas específicas que sintetizan
las diversas especies de Plasmodium. Entre estas se cuenta la proteína 2 rica en histidina
(HRP-2) que produce Plasmodium falciparum y la Lactado deshidrogenasa parasitaria
(LDH) que secretan las 4 especies de
Prueba de Reacción en Cadena de la Polimerasa (PCR)
Es una técnica de diagnóstico molecular que detecta el ADN de cualquiera de las especies
de Plasmodium que causan la malaria.
-Tratamiento Nicole
El tratamiento para la malaria es variado. Siempre va a depender del criterio del médico
tratante.
Entre los medicamentos que se utilizan están la cloroquina y la primaquina, así como
también la quinina. Estos medicamentos han demostrado ser eficaces en la erradicación de
las formas parasitarias.

Plasmodium ovale (1).docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.