
Oxidaciones Biologicas y Bioenergetica
1
OXIDACIONES BIOLÓGICAS
BIOENERGÉTICA:
Las actividades de los seres vivos requieren continuo aporte de energía, ya sea para l síntesis
de componentes celulares, transporte de sustancias a través de membranas contra gradiente
de concentración, la contracción muscular, etc.
En última instancia la energía para los procesos biológicos procede del sol. La energía lumínica
es captada por pigmentos existentes en los vegetales y en algunos microorganismos y
transformada mediante la FOTOSÍNTESIS, en otras formas de energía, principalmente química,
utilizable para la síntesis de sus propios componentes, a partir de sustancias muy simples del
medio (CO, H
2
O, NH
3
, NO
3
). Estos organismos son llamados FOTÓTROFOS.
El resto de los seres vivos necesita incorporar moléculas complejas ya elaboradas. Estos
organismos se denominan QUIMIÓTROFOS, ya que utilizan la energía contenida en esas
moléculas.
POR EJEMPLO LA GLUCOSA ES SINTETIZADA POR ORGANISMOS FOTÓTROFOS A PARTIR DE
CO
2
Y H
2
O, LA REACCIÓN SE PUEDE EXPRESAR DE LA SIGUIENTE FORMA:
6 moles de CO
2
+ 6 moles de H
2
O + 2870 KJ 1 mol C
6
H
12
O
6
+ 6 moles O
2
.
Tanto la transformación de la energía lumínica en los seres fotótrofos, como el
aprovechamiento de energía química en los quimiótrofos, exige la transformación de
compuestos intermediarios especiales, de alto contenido energético, los cuales actúan como
reservorios y transportadores de la energía a utilizar en la realización del trabajo en la célula.
En todos los seres vivientes, el principal compuesto intermediario rico en energía es
ADENOSINA TRIFOSFATO (ATP).
Los organismos aeróbicos, que requieran oxígeno para subsistir, alcanzan la mayor eficiencia
en el aprovechamiento de la energía contenida en las moléculas aportadas por los alimentos.

Oxidaciones Biologicas y Bioenergetica
2
La oxidación de esas moléculas constituye el principal mecanismo para liberar esa energía. En
el caso de la glucosa, su oxidación completa en el organismo libera energía, es decir es una
reacción EXERGÓNICA.
Reacciones EXERGÓNICAS: son aquellas que ceden energía al átomo, la energía de los
productos es menor que la de los reactivos y si la energía es liberada en forma de calor se dice
que es exotérmica.
Una reacción ENDERGÓNICA es aquella que necesita incorporar energía, la energía de los
productos que la de los reactivos. Si la energía que se libera es en forma de calor se dice que es
endotérmica. El cambio de calor producido se denomina ENTALPÍA (AH). Esta entalpía es
negativa cuando se libera calor y positiva cuando se consume calor.
Reacciones acopladas: las reacciones endergónica pueden acoplarse a reacciones exergónicas
para poder llevarse a cabo, de tal modo que la energía liberada en los procesos exergónicos es
utilizada de alguna manera en los endergónicos. Pero no toda la energía es aprovechada (sólo
el 40%), el resto se pierde como calor.
OXIDACIÓN-REDUCCIÓN.
En los seres aeróbicos las oxidaciones son la principal fuente de energía, por eso vamos a
definir algunos conceptos:
En un principio se entendía por oxidación solamente a la combinación de un compuesto con
oxígeno y el proceso inverso se definía como reducción. Luego se comprobó que la oxidación
también implica pérdida de electrones y la reducción es la ganancia de electrones.
La capacidad de un elemento de oxidar a otra y por lo tanto de reducirse, depende de su
avidez por atraer electrones, que se expresa cuantitativamente por el llamado potencial de
reducción. Éste se define como la tendencia de ganar electrones frente a otro elemento, ión o
compuesto.
OXIDACIONES BIOLÓGICAS
Gran parte de los sustratos oxidados en el organismo sufren deshidrogenación donde los
hidrógenos sustraídos al sustrato se unen al oxígeno molecular formando agua.
½
O
2
+ 2H + 2e
-
H
2
O
Éstas reacciones son catalizadas por enzimas (deshidrogenasas), específicas para cada
sustrato, donde los H son captados por la coenzima (NAD o NADP, o FAD).
NAD + 2H
+
+ 2e
-
NAH + H
+
E= -o,32 V.

Oxidaciones Biologicas y Bioenergetica
3
Se trata de una reacción exergónica, si ocurriera en una etapa, se producirá liberación brusca
de calor no aprovechable para la célula. En los procesos biológicos, los H sustraídos no son
directamente oxidados por el oxígeno, sino transferidos, en etapas sucesivas, a distintas
sustancias aceptoras de potencial de reducción creciente. De este modo la energía se libera en
forma fraccionada y puede ser utilizada por la célula.
MITCONDRIA
Las mitocondrias son organelas donde tiene lugar la transferencia ordenada de electrones y la
captación de la energía generada por el flujo de electrones.
La mitocondria posee una membrana externa en contacto con el citosol, permeable a iones ya
que posee poros o canales formado por una proteína llamada porina. Dentro de la membrana
externa, separado de ella por un espacio intermembranoso, se encuentra un segundo saco
cerrado, constituido por membrana interna, que contiene un espacio central o matriz
mitocondrial. Ésta membrana interna posee una permeabilidad muy selectiva, ya que sólo
puede atravesar agua, oxígeno, dióxido de carbono y amoníaco. Presenta invaginaciones
llamadas crestas. La membrana interna contiene cardiolipina, el cual constituye el 80% de sus
componentes. Posee una masa gelatinosa, en la cual se encuentran las enzimas integrantes de
las vías centrales del metabolismo oxidativo y también contiene los integrantes de la cadena
respiratoria, las estructuras y enzimas responsables de la captación del ATP y distintos
sistemas de transporte.

Oxidaciones Biologicas y Bioenergetica
4
CADENA RESPIRATORIA
Las oxidaciones biológicas suceden gradualmente gracias a aceptores que se encuentran en la
matriz interna de la mitocondria, los cuales están dispuestos ordenadamente según un
gradiente de potencial de reducción creciente y asociados íntimamente a las enzimas que
catalizan las transferencias. Éste conjunto se denomina CADENA RESPIRATORIA O CADENA DE
TRANSPORTE DE ELECTRONICO.
Comprende una serie de etapas donde los electrones fluyen naturalmente en el sentido que
les fija el desnivel en el potencial de reducción de los aceptores. Todos los componentes
forman un sistema multienzimático altamente ordenado.
Dos H cedidos en una reacción redox representan la suma de dos protones y dos electrones.
Hidrógenos y electrones son llamados equivalentes de reducción. Los hidrógenos no pasan
directamente de un sustrato dado al oxígeno o a cualquier otro aceptor si no existen enzimas
que catalicen la transferencia.
✓ TRANSFERENCIA DE EQUIVALENTES DE REDUCCION:
NAD: numerosos sustratos oxidables son deshidrogenados en la matriz mitocondrial
por enzimas deshidrogenasas cuya coenzima es un nucleótido de nicotinamida.
AH
2
+ NAD
+
A + NADH + H
+
protón que queda en el medio.
NAD(aceptor de protones y electrones)
A (cuando libera el H queda oxidado).
AH2 + NADP
+
A + NADPH + H
+
Las deshidrogenasas ligadas a NAD o NADP no forman parte de la cadena respiratoria,
se encuentran en la matriz mitocondrial.
El destino de los equivalentes de reducción no es el mismo si son captados por NAD o
NADP. Si son captados por NAD, éste cede H con la finalidad de producir energía en la
cadena respiratoria. Si son captados por NADP, éstos son utilizados en la síntesis de
compuestos.
El NADPH puede transferir H al NAD por enzimas transdeshidrogenasas.
NADPH + NAD NADP + NAD
Oxidaciones Biologicas y Bioenergetica
5
✓ COMPONENTES DE LA CADENA RESPIRATORIA:
La cadena está formada por cuatro complejos más dos integrantes que se encuentran
libres:
1. Complejo I NADH-ubiquinona reductasa: en este complejo el NAD reducido es
oxidado. Éste complejo está formado por 25 cadenas polipéptidas, contiene
una molécula de flavina como grupo prostético y 16 a 24 átomos de hierro en
5 a 8 centros ferro-sulfurados. Los electrones transferidos desde el NADH al
complejo son aptados inicialmente por FMN (flavoproteína), el cual se reduce
el FMNH, luego pasan sucesivamente por átomos de Fe de distintos centros de
FE-S y finalmente cedidos a la ubiquinona coenzima Q. el FMN y los átomos de
fe se oxidan (Fe
+3
capta un e
-
y pasa a Fe
+2
) y la coenzima Q se reduce (CoQH
2
).
La ubiquinona o CoQ es el único aceptor de la cadena respiratoria no unido a
proteínas. Actúa como portador móvil de electrones, ya que los recibe de las
procedencias antes vistas y los transfiere a los aceptores siguientes.
2. Complejo II succinato-ubiquinona reductasa. Posee un grupo prostético FAD y
tres centros Fe-s. transfiere los electrones de reducción hacia la coenzima Q.
3. Complejo III ubiquinona-citocromo C reductasa: contiene citocromos b
566
, b
562
y c
1
y un centro Fe-S. transfiere electrones desde ubiquinona hacia citocromo
c. los citocromos son hemoproteínas con capacidad de aceptor de electrones.
El citoromo c es un transportador móvil que recibe electrones y los transfiere
al siguiente complejo.
4. Complejo IV citocromo oxidasa: en ésta citocromo están incluidos citocromos a
y a
3
y dos iones Cu. Cataliza la reducción de agua. Es el único componente de
la cadena respiratoria con capacidad para reaccionar directamente con el
oxígeno. Una molécula de oxígeno capta 4 protones y 4 electrones para formar
dos moléculas de agua.

Oxidaciones Biologicas y Bioenergetica
6
✓ INHIBIDORES DEL TRSNSPORTE DE ELECTRONES
Actúan al nivel del complejo I, el inhibidor llamado rotenona, producto vegetal,
poderoso veneno de peces como el amital y anestésico como halotano. Estas
sustancias impiden la llegada de hidrógenos precedentes de sustratos oxidados a la
CoQ. El antibiótico antimicina A inhibe el transporte de electrones en el complejo III.
Cianuros, monóxido de carbono y azidas (N
3
-
) inhiben específicamente la citocromo-
oxidasa y bloquean la etapa final de activación del oxígeno.

Oxidaciones Biologicas y Bioenergetica
7
FOSFORILACIÓN OXIDATIVA
Hasta aquí hemos visto el curso de las oxidaciones en las mitocondrias a favor del gradiente
del potencial de oxidación. Se trata de un proceso exergónico que transcurre con disminución
de energía libre. Ahora vamos a analizar cómo esa energía liberada es convertida en ATP. La
unión del ADP + P inorgánico ATP + H
2
O, ésta es una reacción endergónica, que ocurre
cuando se acopla a procesos que suministran la energía necesaria.
La producción de ATP utilizando la energía liberada durante el transporte de electrones se
denomina FOSFORILACIÓN OXIDATIVA.
Tres de las etapas anteriores vistas en la cadena respiratoria producen suficiente energía como
para acoplar la formación de un enlace fosfato de alta energía:
1. L transferencia de H desde NADH a coQ.
2. La cesión de electrones al complejo III.
3. La reacción del complejo IV.
Para cada par de H
+
o electrones transferidos a lo largo de la cadena respiratoria, se unen 3
moléculas de fosfato a tres ADP. Es decir el flujo de un par de electrones permite la síntesis de
moles de ATP.
Esta relación 3 ATP por electrones transferidos es con la coenzima NAD, con FAD la relación es
menor, se producen 2 ATP por cada par de electrones transferidos.
✓ MECANISMO DE FOSFORILACION OXIDATIVA:
El ATP es sintetizado por la actividad
de una enzima localizada en la
membrana mitocondrial llamada ATP
sintetasa. Ésta está constituida por
dos complejos: complejo F
1
formado
por un conjunto de nueve
subunidades polipeptídicas (3α, 3β,
γ, δ y ε). Las subunidades γ, δ, ε
contribuyen a fijar el complejo F
1
.
Normalmente las partículas están
conectadas con le membrana por un
tallo proteínico llamado F
0
. En su
constitución atraviesa una subunidad
α que atraviesa 8 veces la
membrana, dos subunidades y 10
poli péptidos c, éstas últimas forman
un túnel en el centro de la pieza de la pieza F
0
.

Oxidaciones Biologicas y Bioenergetica
8
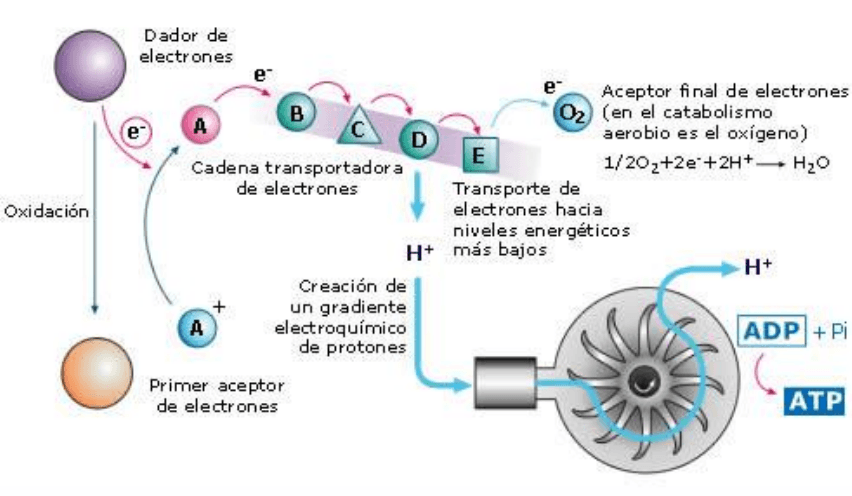
✓ HIPÓTESIS QUIMIO OSMÓTICA DE MITCHELL
Esta teoría abarca la transmisión de la energía producida durante el transporte de
electrones al sitio de fosforilación y la utilización de la energía para la síntesis de ATP.
La hipótesis quimio-osmótica sostiene que simultáneamente con el proceso de transporte
de electrones, en la cadena respiratoria se produce transferencia de protones desde la
matriz mitocondrial hacia el exterior a la membrana interna. El transporte de electrones se
acopla con el bombeo unidireccional de protones, donde se produce una acumulación de
hidrogeniones en el lado citosólico de la membrana formando un gradiente
electroquímico. Aquí hay un potencial protón-matriz que tiende hacer regresar los
protones hacia la matriz, pero las membranas son impermeables, sólo pueden volver por
el canal F
0
del ATP sintetasa. Éste retorno de protones al interior de la mitocondria a favor
del gradiente es la fuerza impulsora de la síntesis de ATP.

Oxidaciones Biologicas y Bioenergetica
9
✓ ACOPLAMIENTO DE TRANSPORTE DE ELECTRONES Y
TRANSLOCAION DE PROTONES
Los dos electrones cedidos por NADH en la cara interna del complejo I se unen al FMN para dar
FMNH. Ésta los transfiere a los centros Fe-S y luego a la CoQ. En esta etapa se produce pasaje
de electrones desde la matriz hacia el lado exterior de la membrana a través del complejo I. el
bombeo unidireccional de H ocurre en los complejo I, II y III.
Ciclo Q: la coenzima Q recibe 2 electrones de NADH o FADH a través de los complejos I y II y
además toma 2 protones de la matriz para convertirse en CoQH
2
. Ésta en forma reducida migra
hacia el complejo III, cede electrones a los centros Fe-S que pasa al citocromo c
1
y finalmente
fuera del complejo al citocromo C, así la CoQH
2
cede un electrón, libera 2protones hacia el
espacio intermembranoso y se oxida nuevamente a coQ. Esto cierra una primera etapa del
ciclo y se inicia una segunda etapa con pasos similares al anterior. El resultado de cada ciclo es
la oxidación de una molécula de CoQH
2
, la expulsión de cuatro protones y la transferencia de
dos electrones al citocromo c.
Luego comienza una etapa final (reducción del oxigeno): los electrones son transportados
desde el citocromo C al complejo IV. Este complejo conduce los electrones a la superficie
interior y allí los dona al oxígeno, pero el transporte de los citocromos transfiere un electrón
por vez, y el oxígeno necesita 4 electrones, si se acopla de a uno por vez, es tóxico, por lo cual
la molécula de oxígeno es fijada en el centro hemo-Cu el citocromo a3 y allí permanece hasta
que llegan los cuatro electrones.
Así se produce una fuerza protón-motriz que tiende hacer regresar los protones al interior de
la mitocondria, pero mediante la ATP-sintetasa, lo cual provee la energía necesaria para la
síntesis de ATP.
✓ SINTESIS DE ATP EN EL COMLPEJO F
0
F
1
El complejo F
0
F
1
se considera como una máquina rotatoria. El flujo de protones ingresa por F
0
,
provee de energía necesaria para provocar el movimiento de rotación del anillo. Los sitios
catalíticos localizados en las subunidades β, pasan por tres estados: cerrado, laxo y abierto.
El ADP y el Pi ingresa en el estado laxo, que se combinan para dar ATO y H
2
O sin gasto de
energía. Se produce entonces un cambio conformacional en la subunidad β y el ATP forado es
retenido (está cerrado). Luego el sitio catalítico adopta la forma abierta y libera el ATP.
Oxidaciones Biologicas y Bioenergetica
10
✓ TRANSPORTE DEL ATP
La mayor parte del ATP generado en las células es sintetizado dentro de las mitocondrias y
consumido fuera de ellas. Casi todo el ATP formado debe ser enviado al exterior de esas
organelas, mientras los componentes necesarios para generarlo deben ingresar a la matriz. El
transporte está a cargo a través de un sistema de co-transporte que intercambia ATP de la
matriz por ADP + Pi del exterior.
✓ INHIBIDORES DE LA FOSFORILACION OXIDATIVA
Existen otros agentes que no bloquean el flujo de electrones, pero disocian a este del
proceso de fosforilación. Éste tipo de sustancias son llamadas desacoplantes. Uno muy
utilizado es el 2,3 –dinitrofenol, transfiere protones desde el lado externo de la
mitocondria hacia la matriz y anula el gradiente de protones creado por la cadena
respiratoria. Los compuestos que transportan iones a través de la membrana se llaman
inóforos. El DNP se comporta como un inóforo de protones. Existen antibióticos de
naturaleza peptídica (valinomicina y nigericina) que actúan como inóforos de K
+
la
transferencia de estos iones pueden interferir, suprimir o disminuir el gradiente de
potencial eléctrico en ambos lados de la membrana y entorpecer la fosforilación oxidativa.
Otra sustancia que interfiere en la fosforilación oxidativa es la oligumicina, el cal se une al
segmento f
0
del ATP sintetasa e interfiere la síntesis de ATP.

Oxidaciones Biologicas y Bioenergetica
11
CICLO DE KREBS
También llamado ciclo del ácido cítrico o ciclo de los ácido tricarboxílicos.
Es un proceso que se realiza en aerobiosis (presencia de oxígeno). Se cumple dentro de las
mitocondrias y comprende una serie de reacciones catalizadas por enzimas en las que se
produce oxidación total de restos acetato, procedentes de distintos orígenes (ácidos grasos,
aminoácidos, hidratos de carbono, etc).
El Acetil coa es un intermediario clave en el metabolismo, se produce por descarboxilación del
piruvato, sino también por oxidación de ácidos grasos y de la cadena carbonada de
aminoácidos. Éste inicia las reacciones combinándose con oxaloacetato.

Oxidaciones Biologicas y Bioenergetica
12
1. FORMACION DEL ÁCIDO CÍTRICO: el Acetil coa se une con el oxaloacetato originando
CITRATO. Ésta reacción es catalizada por la enzima citrato sintasa en presencia de
agua. Es una reacción irreversible.
2. FORMACION DE ISOCITRATO: Por un proceso de isomeración, el citrato se convierte en
ISOCITRATO. Primero se deshidrata a cis-aconitato, luego recupera agua y forma el
isocitrato. Ambas etapas son catalizadas por la enzima aconitasa.
3. OXIDACIÓN DEL ISOCITRATO: el isocitrato experimenta una deshidrogenación para
convertirse en OXALUSICCINATO. La reacción es catalizada por la enzima isocitrato
deshidrogenasa que utiliza NAD (el cual se reduce a NADH
2
) como coenzima y requiere
Mg
++.
4. DESCARBOXILACION DEL OXALOSUCCINATO: la misma enzima responsable del la
reacción anterior cataliza la descarboxilación de oxalosuccinato para dar α-CETO-
GLUTARATO. En esta etapa se libera la primer molécula de CO
2
. La reacción se realiza
en presencia de H
+
y Mg
2+
.
5. DESCARBOXILACIÓN OXIDATIVA DEL α-CETO-GLUTARATO: este proceso es catalizado
por un complejo enzimático llamado complejo α-cetoglutarato deshidrogenasa
formado por 3 enzimas que necesitan las coenzimas pirofosfato de tiamina, ácido
lipoico, CoA, FAD y NAD. Aquí se forma como producto SUCCINIL COA y se libera otra
molécula de CO
2
.
6. FORMACION DE SUCCINATO: La succinil Coa es convertida en SUCCINATO por la
succinato tioquinasa. En esta etapa se requiere guanosina defosfato y foafato
inorgánico. Ésta es la única etapa del ciclo en la cual se genera una unión fosfato de
alta energía a nivel del sustrato. A partir de GTP se puede formar ATP catalizada por
nucleósido difosfato quinasa. GTP + ADP GDP + ATP.
7. DESHIDROGENCIÓN DEL SUCCINATO: el succinato es oxidado a FUMARATO por acción
de succinato deshidrogenasa en presencia de FAD como aceptor de hidrógeo.
8. HIDRATACIÓN DEL FUMARATO: por adición de agua el fumarato se convierte en
MALATO por acción e la enzima fumarasa.
9. OXIDACIÓN DEL MALATO: el malato pierde 2 hidrógenos y se transforma en
OXALOACETATO. La reacción es catalizada por la malato deshidrogenasa, con NAD.
El ciclo se cierra con la formación de OXALOACETATO, compuesto final e inicial de la serie
de reacciones. Durante una vuelta completa se liberan dos moléculas de CO
2
y 8 átomos
de hidrógeno. Tres pares de esos átomos han sido cedidos a NAD y el par restante a FAD,
en la cadena respiratoria esos 4 pares de hidrógeno se unirán al oxígeno formando 4
moléculas de agua.

Oxidaciones Biologicas y Bioenergetica
13
✓ CONSIDERACIONES GENERALES DEL CICLO:
• En la células siempre hay disponibilidad de agua, Acetil coa y Pi.
• Las coenzimas NAD y FAD, son provistas luego de a oxidación e las mimas en la
cadena respiratoria. La oxidación de NADH
2
y FADH
2
en la cadena respiratoria
se efectúa con la reducción final del oxígeno a agua, de modo que el ciclo de
krebs funciona en aerobiosis (presencia de oxígeno).
• Si no hay disponibilidad de oxígeno, la cadena respiratoria no funciona, y
entonces, no hay producción de FAD ni NAD. Entonces el ciclo de krebs
tampoco funciona.
• La localización de todas las enzimas del ciclo en la matriz mitocondrial,
favorece la posterior entrega de coenzimas reducidas a la cadena respiratoria
que se efectúa en la membrana interna de la mitocondria.
✓ PAPEL FUNCIONAL DEL CICLO DE KREBS
Es la vía final común para la oxidación de todos los restos de 2 carbono en forma de Acetil
coa (acetato activo) que se generan en el organismo a partir de glúcidos, ácidos grasos y
aminoácidos.
Cuando se acumula acetato activo, se promueve la formación de oxalo-acetato, con lo cual
se estimula la operación del ciclo.
El funcionamiento del ciclo produce 12 moles de ATP por mol de acetato oxidado. La
oxidación total de la glucosa, teniendo en cuenta los procesos de glucólisis,
descarboxilación del piruvato y ciclo de krebs, produce 38 moles de ATP por mol de
glucosa, lo que significa un total de 277 kcal, osea un rendimiento del 40% de la energía
contenida en un mol de glucosa (686 kcal).
ISOCITRATO A
OXALOSUCCINATO
NADH
3 MOL DE ATP
α CETOGLUTARATO A
SUCCINIL COA
NADH
3 MOL DE ATP
SUCCINIL COA A SUCCINATO
1 MOL DE ATP
SUCCINATO A FUMARATO
FADH
2
2 MOL DE ATP
MALATO A
OXALOSUCCINATO
NADH
3 MOL DE ATP
TOTAL POR ACETATO
12 MOL DE ATP.

Oxidaciones Biologicas y Bioenergetica
14
Oxidaciones Biologicas y Bioenergetica
15
proteinas mio.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.