
Gastón Ejdin
2019
Osmolaridad VS tonicidad
La osmolaridad, en su definición más básica, es una medida de concentración que
expresa la cantidad de osmoles de solución por litro de solución. 1 osmol, a su vez,
representa a 1 mol de partículas, que a su vez refiere a 6,02 × 10²³ partículas. Por
ejemplo, una solución de glucosa 1 osmolar (Osm) contiene 1 osmol de glucosa en
1 litro de solución. ¿Pero la cantidad de osmoles coincide siempre con la cantidad
de moles de soluto? No, no siempre. En el caso de que la molécula sea no
electrolítica (es decir, que al ser introducida en un solvente como agua no se disocie
en iones), la cantidad de osmoles coincidirá con la de moles. Tales son los casos de
la glucosa y la urea. Sustancias como el NaCl (que si son electrolíticas) se disocian
al contactar con el agua en un número determinado de partículas. Este número, que
depende del soluto en cuestión, se calcula a través del coeficiente de Van’t Hoff (i),
de manera tal que el número de osmoles depende del producto entre el número de
moles del soluto y el coeficiente de Van’t Hoff:
Número de osmoles = número de moles . i
Así, en el caso del NaCl, i = 2 y el número de osmoles, al tener 1 mol de NaCl, es de
2 osmoles. A partir de la ecuación anterior, se deduce que:
Osmolaridad = molaridad . i
Como se mencionó anteriormente, la osmolaridad es una medida de concentración.
Si se poseen 2 compartimentos, sean cuales sean, separados por una membrana
semipermeable (permeable al agua e impermeable a cualquier soluto) y en cada
compartimento encontramos 2 soluciones a diferentes concentraciones, podremos
observar 2 cosas:
1. Entre los dos compartimentos se genera un gradiente, es decir, una variación
de cierta magnitud (en este caso, de concentración) en función de la
distancia.
2. Debido a este gradiente, se genera entre ambos compartimentos una fuerza
impulsora que dará origen al movimiento de agua. En este caso, llamaremos
“ósmosis” a este movimiento.
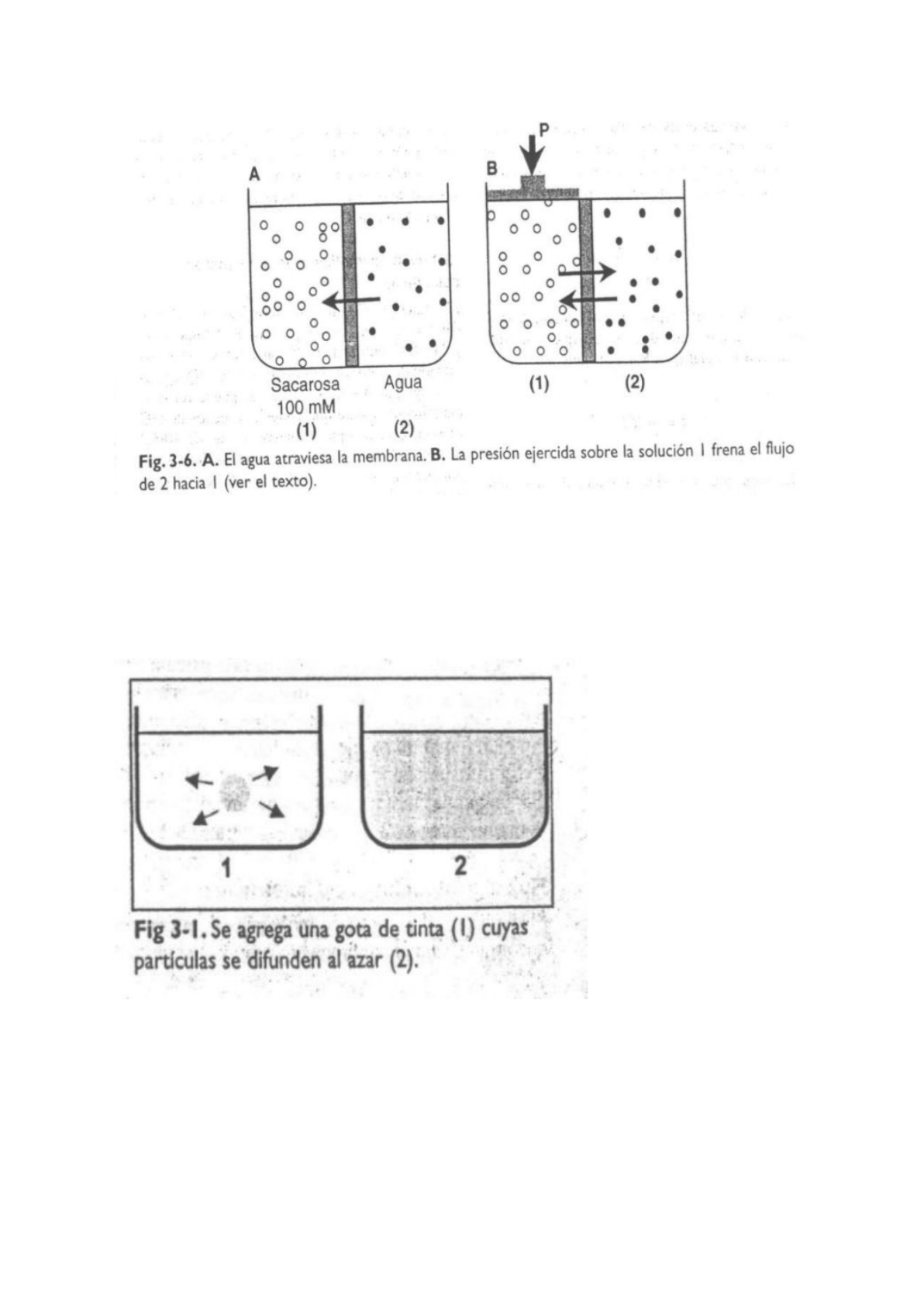
¿Qué es la ósmosis? Es el pasaje de agua desde el compartimento A (que tiene
mayor concentración de la solución) hacia el B (que tiene menor concentración de la
solución).
Gastón Ejdin
2019
¿Y cuál es la diferencia entre la ósmosis y la difusión? Esta última implica la
tendencia que tiene a disiparse una diferencia de concentración entre dos puntos de
1 mismo compartimento. El típico ejemplo es una gota de tinta en un recipiente con
agua que se distribuye en él.
¿Pero puede haber difusión de una solución entre dos compartimentos separados
por una membrana? Si, pero solo si la membrana es permeable al/los soluto/s que
posee dicha solución. Es aquí donde radica la diferencia fundamental entre la
difusión y la ósmosis. Recordemos que en la 1°, la membrana es solamente
permeable al agua e impermeable a cualquier soluto. También recordemos que
ambos procesos respetan los gradientes de concentración (el movimiento se realiza
desde el compartimento de mayor concentración de la solución hacia el de menor).

Gastón Ejdin
2019
Hace mucho que estamos hablando sobre varios temas y nunca apareció la palabra
“tonicidad”. Bueno, llegó el momento. Es muy importante resaltar que es difícil
encontrar en el organismo una membrana impermeable a todos los solutos
existentes. Más frecuente es encontrar aquella que sea permeable a ciertos solutos
e impermeable a otros. Si la membrana dejara pasar agua y solutos por igual, no
veríamos el proceso de ósmosis debido a la rápida disipación del gradiente de
concentración (ya que se está produciendo un movimiento de solutos y solventes
por igual a través de dicha membrana, es decir, difusión). Esto nos lleva a pensar
que si una membrana es permeable a un soluto determinado, por más pequeña que
fuera su permeabilidad, la capacidad que tiene dicho soluto para generar el
fenómeno de ósmosis entre los 2 compartimentos en los que se encuentra se va a
reducir (por lo explicado en este párrafo). Debido a que los solutos en un solvente
se comportan como gases ideales, tienen la capacidad de generar una presión
sobre dicho solvente (presión osmótica) que va a depender de la concentración de
las partículas en solución. Así, decimos que la presión osmótica disminuye al ocurrir
esto. Para calcular a cuánto equivale esta disminución, utilizaremos el coeficiente de
reflexión (de Staverman) para obtener el valor de la tonicidad o presión osmótica
efectiva (por fin, no es cierto?). ¿Efectiva para qué? ¡Para generar el movimiento de
agua por ósmosis!
Presión osmótica calculada . coeficiente de reflexión = presión osmótica efectiva
O, lo que es igual:
Osmolaridad calculada . coeficiente de reflexión = osmolaridad efectiva (tonicidad)
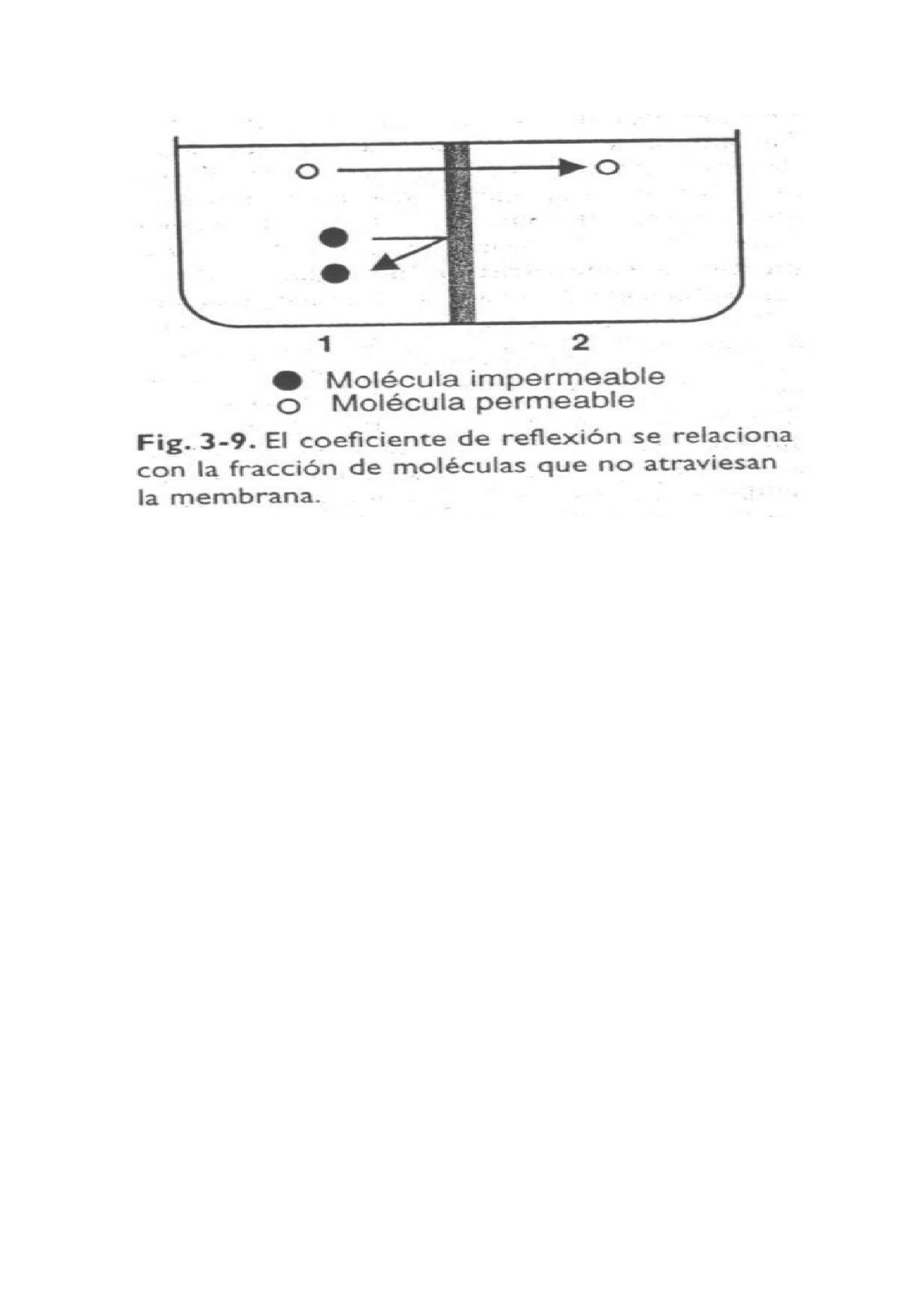
¿Qué es el coeficiente de reflexión? Es una medida que indica la fracción de
moléculas de soluto que chocan contra la membrana, no la atraviesan y se reflejan
hacia el mismo compartimento del que provienen. Si el coeficiente = 1, la reflexión
es total y la membrana será totalmente impermeable al soluto. Caso contrario para
si el coeficiente es = 0. Valores menores a 1 generan que la presión osmótica
efectiva sea menor a la calculada (comprobarlo con las ecuaciones).
Gastón Ejdin
2019
Ya casi terminamos, paciencia.
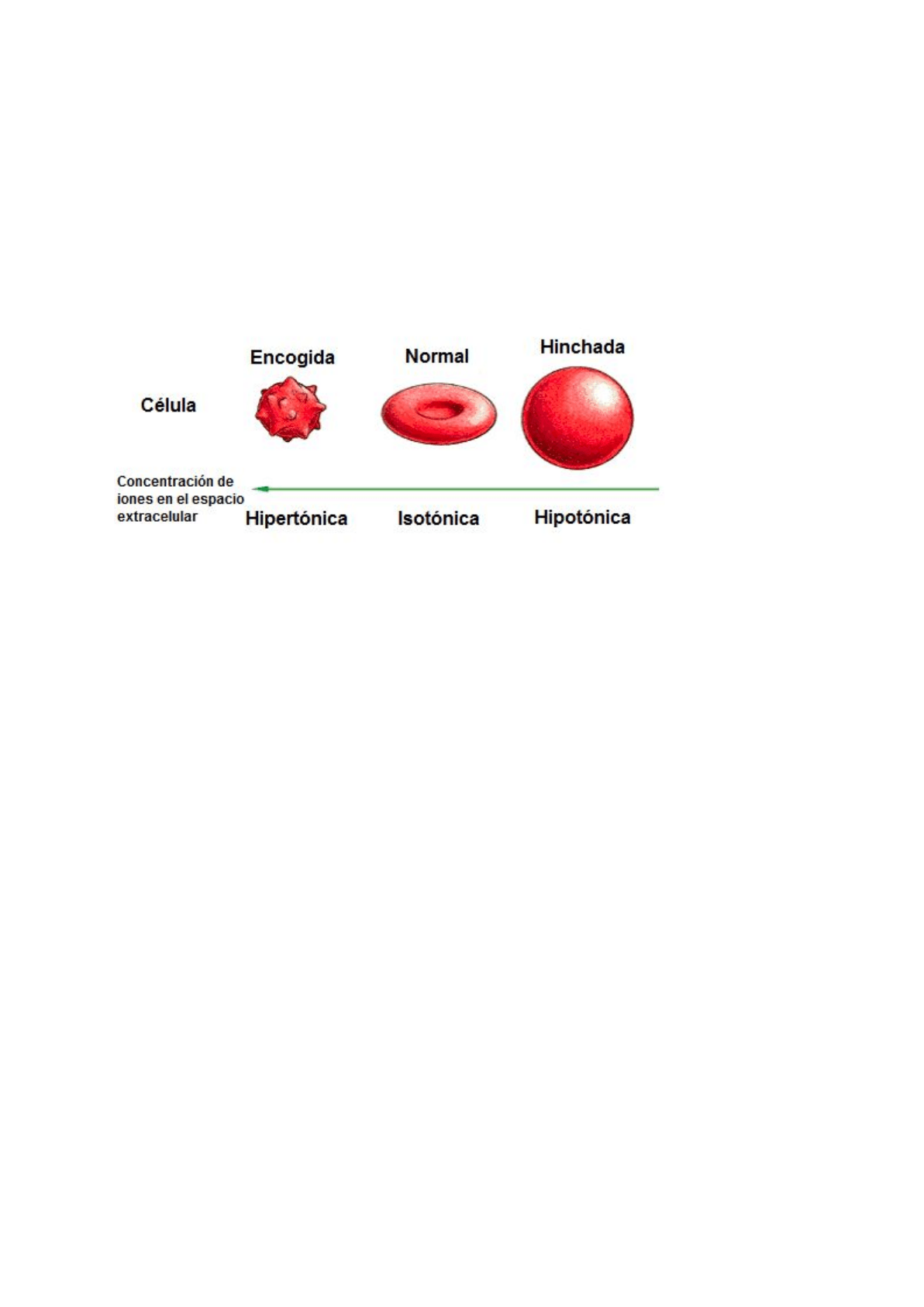
Se dice que una solución es isotónica cuando se sumerge a una célula en ella y no
cambia su volumen debido a que no ha habido un flujo de agua, ya sea desde o
hacia la célula. Así, la tonicidad es igual dentro y fuera de la célula. Al sumergir una
célula en una solución formada por un soluto impermeable (coeficiente de reflexión
= 1) que posee la misma concentración dentro y fuera de la célula, diremos que
dicha solución es isotónica e isoosmótica. Pero si sumergimos la célula en una
solución con igual concentración dentro y fuera de la célula, aunque con un
coeficiente de reflexión menor a 1, dicha solución será isoosmótica, pero no
isotónica (recordemos la ecuación para calcular la tonicidad u osmolaridad efectiva.
Las alteraciones en el balance hidrosalino se corrigen con soluciones isotónicas
(NaCl 0,9% - solución fisiológica, que tiene una osmolaridad parecida a la del
plasma humano - 300 mOsm, considerándose también isoosmótica). Debido a que
el coeficiente de reflexión para el Na es equivalente a 1, esta solución no induce
cambios en el volumen celular. Pero si introducimos por vía endovenosa 300 mOsm
de urea, tendremos una solución isoosmótica, pero no isotónica. ¿Por qué? Porque
el coeficiente de reflexión de la urea es equivalente a 0,2. Es decir, las membranas
celulares son parcialmente permeables a dicho soluto. Así, la osmolaridad calculada
o tonicidad equivale a 60 mOsm y se crea un gradiente osmótico para el movimiento
de agua hacia la célula (debido a que la urea entró en ella y el agua se movilizó con
el fin de disipar dicho gradiente de concentración), que aumenta rápido de volumen
y rompe la membrana celular (hemólisis). En este caso, decimos que la solución es
hipotónica e isoosmótica (nótese que la tonicidad es menor a la osmolaridad
Gastón Ejdin
2019
calculada). ¿Qué sucede si introduzco una solución de NaCl 5% por vía
endovenosa? Exactamente lo contrario. El gradiente de concentraciones generado
entre los dos compartimentos separados por la membrana celular impulsa el
movimiento de agua a través de ella, desde aquel que tenga mayor concentración.
¿Y no se moviliza el NaCl por dicha membrana, como en el caso de la urea? No,
porque a diferencia de ese soluto, la membrana celular es totalmente impermeable
al NaCl. Así, esta solución es hiperosmótica e hipertónica.
Bibliografía
-Parisi, Mario; Temas de Biofísica
; 4ta edición; McGraw-Hill Interamericana; 2010;
Buenos Aires, Argentina.
Osmolariad VS tonicidad.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.