
𝜎
𝜎
𝜎
𝜎
𝜎
𝜎
Diagramas de equilibrio
¿Como se forman los sólidos?
Se obtienen a partir de procesos de enfriamiento de un estado líquido, es decir, un elemento puro (metal, no metal
o un oxido) líquido a altas temperaturas (por arriba del punto de fusión) y luego son sometidos a un proceso de
enfriamiento de manera tal que experimentan transformaciones de estado, es decir, pasan de líquido a sólido.
Los diagramas de equilibrio representan las transformaciones que sufren los materiales.
Se llaman diagramas de equilibrio porque todos nuestros estudios están hechos en base a los siguientes supuestos:
1) Todos los estudios son a presión atmosférica, es decir, la presión no va a ser una variable dentro de las
transformaciones.
2) Todos nuestros análisis están hechos en una situación de equilibrio, es decir, el sistema no está sufriendo
transformaciones de fases. El enfriamiento es muy lento.
Sistema: inicia todas las mezclas posibles que se pueden dar entre dos elementos genéricos A y B.
¿Cómo se forman estos solidos? Son en general policristalinos, es decir, tienen granos /cristales. Suponiendo un
líquido a altas temperaturas, cuando ese líquido comience a enfriarse sucederá que se irá reduciendo el movimiento
de las partículas que lo forman. Las partículas quietas comienzan a formar redes cristalinas. Las redes crecerán en
diferentes direcciones formando granos.
Dentro de cada grano, al producirse el enfriamiento se van agregando celdas unidad hasta formar un grano. Las
diferentes orientaciones de estos granos cuando se unen provocan bordes de grano.
Casos de solubilidad: cuando se mezclan dos elementos A y B se pueden producir diferentes grados de solubilidad,
que significa la posibilidad de que dos elementos A y B formen soluciones sólidas, (de acuerdo a las reglas Humme
Rotery).
Casos de solubilidad posibles:
1) Solubilidad total: A y B son totalmente solubles en estado sólido, es decir, puedo mezclar 70% de a Y 30% de
B y obtener una solución sólida. Genéricamente, puedo mezclar cualquier proporción de A y B y siempre
obtener una solución sólida.
2) Insolubilidad total: Dos elementos A y B que independientemente de las proporciones en que los mezcle no
van a ser capaces de formar soluciones solidas.
Es decir, no cumplirán con alguna de las reglas de Humme Rotery (2, 3, 4).
3) Solubilidad parcial: cuando un elemento es totalmente soluble y el otro es totalmente insoluble, es de
esperarse que existan estados intermedios donde haya solubilidad parcial, A y B se mezclan en diferentes
proporciones y dependiendo de la cantidad de A y de la cantidad de B presente es posible formar soluciones
parciales.
4) Compuestos Inter metálicos: caso particular de mezclas A y B, se forman los compuestos a partir de la
imposibilidad de formar soluciones solidas.
Palabras clave del tema:
- Estado: solido, liquido, gaseoso.
- Componente: identifica de manera genérica un elemento o un compuesto que forma parte del sistema en
análisis.
- Composición: cantidad de cada componente que está presente en la mezcla
- Fase: toda porción física y químicamente diferenciable, pueden tener diferentes estados
- Sistema: todas las mezclas posibles entre A y B
- Solución solida: soluciones que cumplen las reglas de Humme Rotery y donde no se distinguen fases
- Liquidus: línea superior de un diagrama de equilibrio. Tiene la característica de que para temperaturas por
encima de la línea de liquidus, cualquiera de las mezclas entre A y B se encuentran en estado líquido.
- Solidus: línea del diagrama de equilibrio. Se encuentra en la mas baja temperatura y por debajo de esa línea
todas las mezclas entre A y B se encuentran en estado sólido.
- Grados de libertad: movimientos (medidos en temperatura y composiciones)
𝜎
𝜎
𝜎
𝜎
𝜎
𝜎
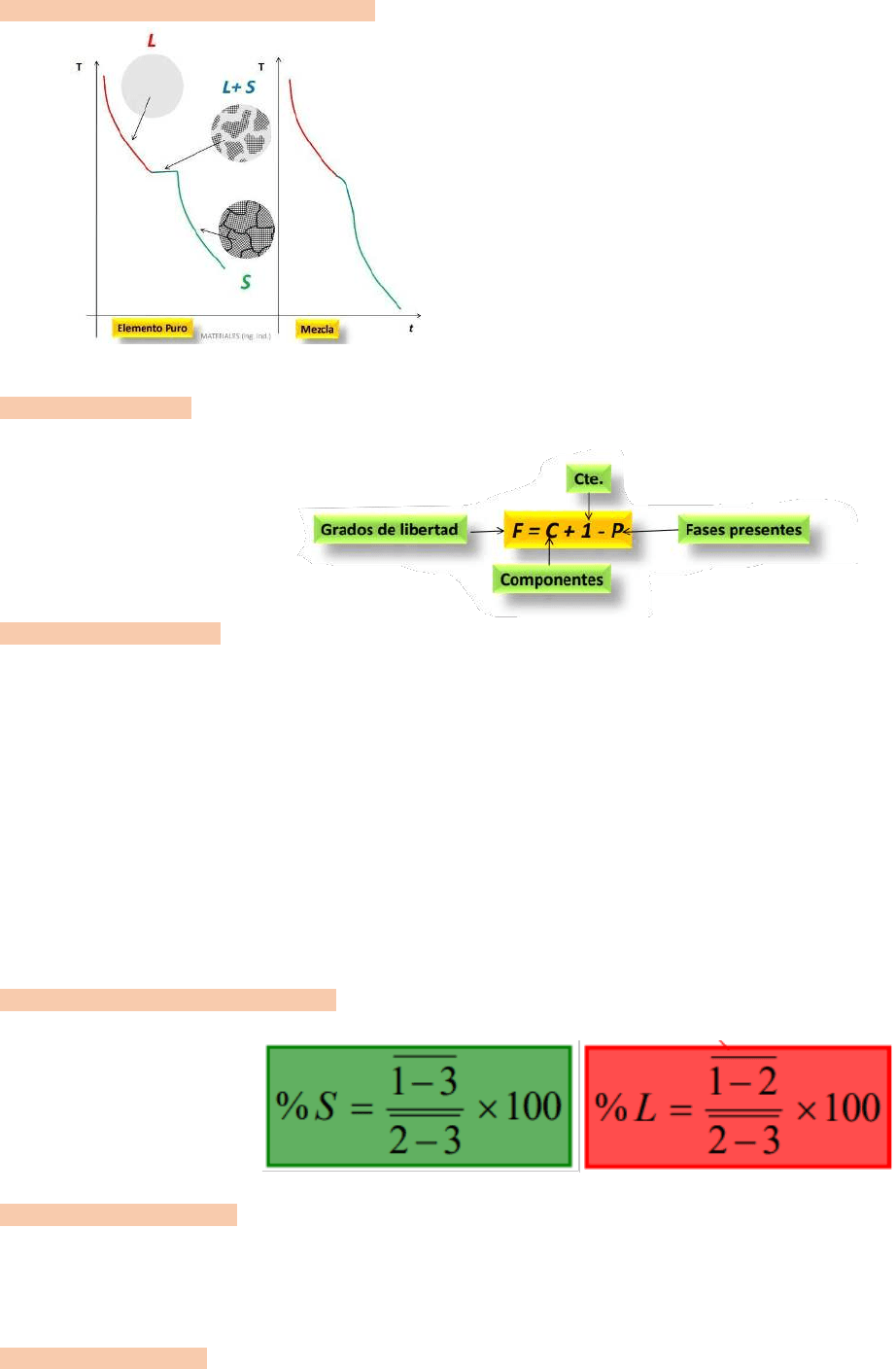
Gráfico de curvas de enfriamiento:
Temperatura en la ordenada y tiempo en la abscisa.
Rojo: Liquido que se enfría.
Azul: deja de cambiar la temperatura, ya que se genera el cambio de
estado.
Verde: solido que se está enfriando.
La primera curva corresponde a un elemento puro y la segunda a una
mezcla.
Ley de Gibbs: concepto relacionado a los grados de libertad que presenta una mezcla a lo largo de su enfriamiento.
Los grados de libertad se ven definidos por la ley de Gibbs o ecuación de Gibbs.
Solubilidad total:
- A y B son totalmente solubles en estado solido
- Forman solución solida
- Característica: solido monofásico
- Para poder trazar el diagrama de equilibrio necesitamos primero trazar las curvas de enfriamiento.
¿Qué nos interesa saber del diagrama de equilibrio? Nos interesa saber cómo están compuestas las fases presentes a
una determinada temperatura.
Cuando hablamos de la composición de las fases presentes nos referimos a que cantidad de A y B hay en el sólido.
Para conocer la cantidad de líquido y solido en cada una de las fases presentes utilizamos una recta auxiliar. La
proyección de los puntos de intersección de la recta auxiliar con las líneas de liquidus y Solidus sobre los ejes de
abscisas.
Regla de las palancas inversas: permite determinar, para una temperatura dada que porcentaje de líquido y que
porcentaje de solido están presentes:
Insolubilidad total:
- A y B son totalmente insolubles en estado sólido.
- Forman una mezcla eutéctica.
- Forman un sólido bifásico.
Palabras clave:
Eutéctico: mezcla fina de fases que en un determinado sistema permanece en estado líquido a la más baja
temperatura
𝜎
𝜎
𝜎
𝜎
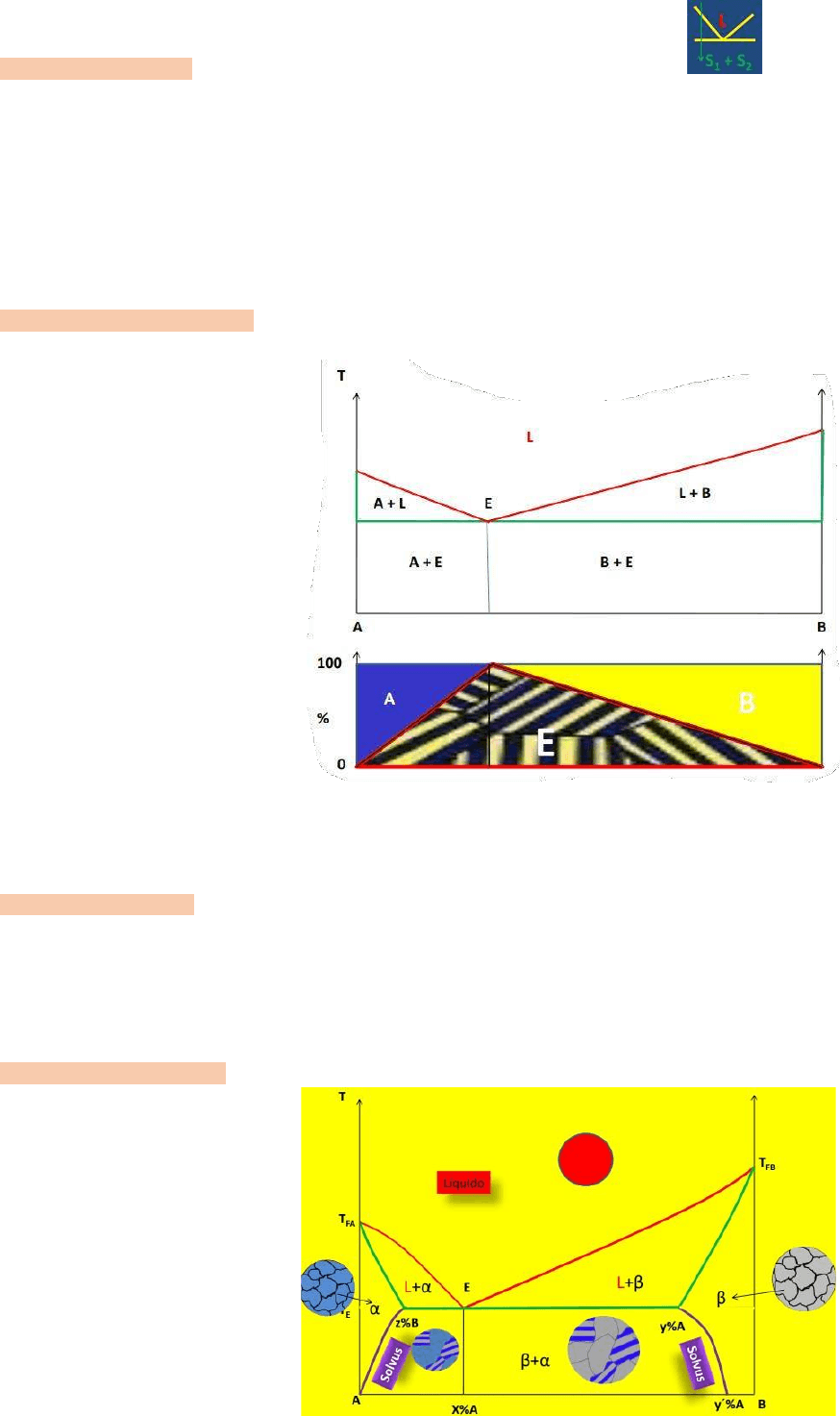
Características: su representación en un diagrama siempre será
Transformación eutéctica: a partir de un líquido, mediante una disminución de temperatura, se forman dos solidos
diferentes S1 y S2.
- Es la aleación del sistema que permanece liquida a más baja temperatura
- Es una mezcla fina de fases
- Existe para una temperatura y composición dadas.
- Solidifica a temperaturas constantes.
- Aplicaciones: soldadura, aleaciones, fusibles.
Diagrama de Tamann: solo es aplicable en insolubilidad total y es para saber qué porcentaje de eutéctico se formó
en las distintas aleaciones que componen el sistema.
Todo lo que se encuentre dentro del triángulo es eutéctico. Lo que se encuentre en el triángulo azul es proeutectico A
y lo que se encuentre en el amarillo es proeutectico B.
Sucede a temperatura ambiente.
Palabras clave:
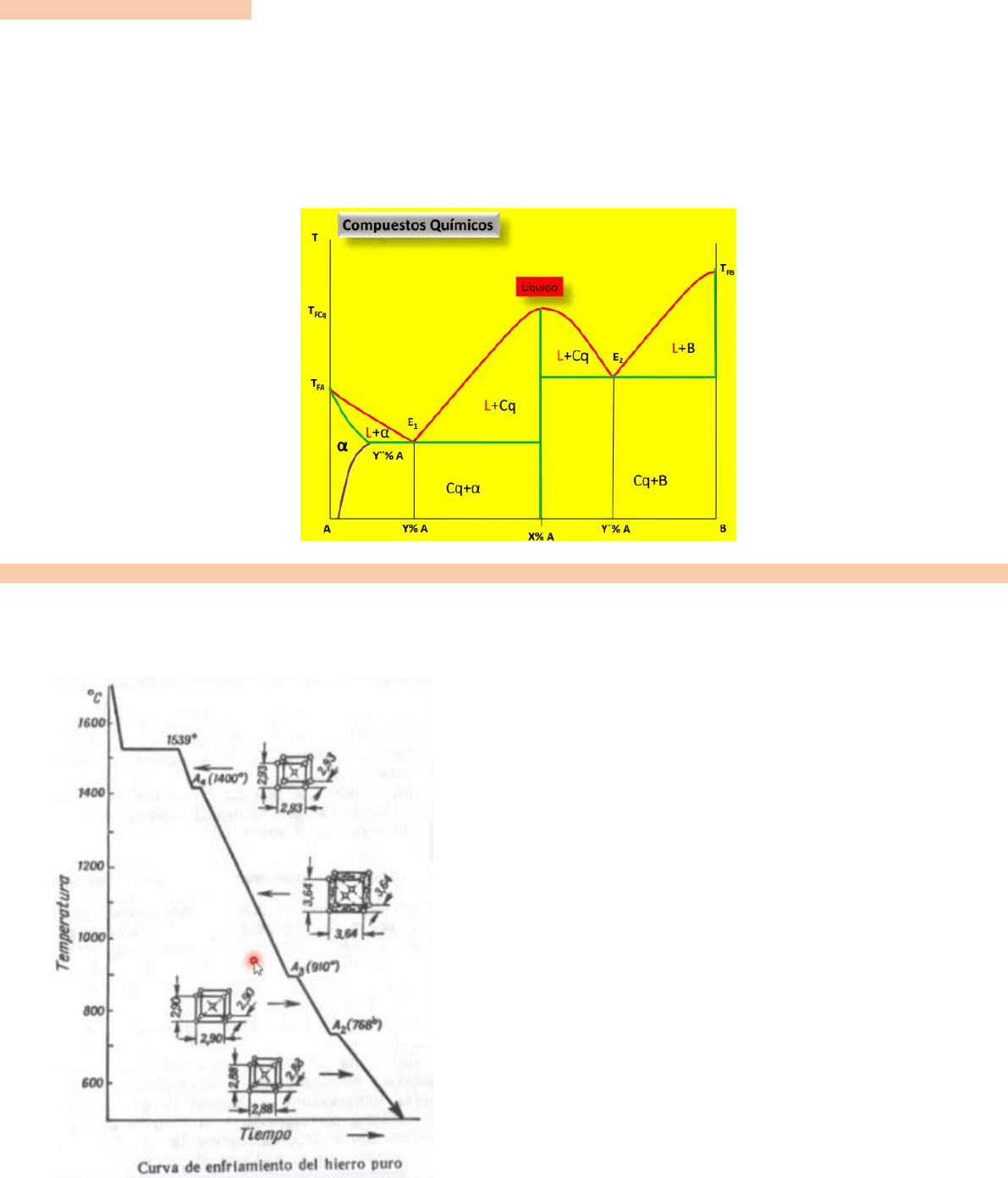
- Solvus: línea que aparece en los diagramas que presentan solubilidad parcial. Representa la variación de la
solubilidad en estado sólido de un componente A en B o B en A.
- Solubilidad parcial: cuando A y B son capaces de formar soluciones solidas solo en determinadas mezclas y a
determinadas temperaturas.
Solubilidad parcial:
𝜎
Inter metálico compuesto: (o compuestos químicos cuando no son metales)
- A y B forman a una determinada proporción un compuesto estequiométrico (responde a formula
estequiométrica).
- A y B pueden ser o no solubles en el compuesto
- Son sólidos monofásicos
- Solidifican a temperatura constante, puede tener un punto de fusión mayor que A y B
- Su estado físico puede ser distinto al de A y B a una temperatura dada
Diagrama Fe – C
El sistema Fr – C es de especial interés ya que da origen a las aleaciones de metales más utilizadas en el mundo, que
son los aceros y las fundiciones. Se las llama a todas aleaciones ferrosas.
Se dividen en dos grandes grupos (aceros y fundiciones).
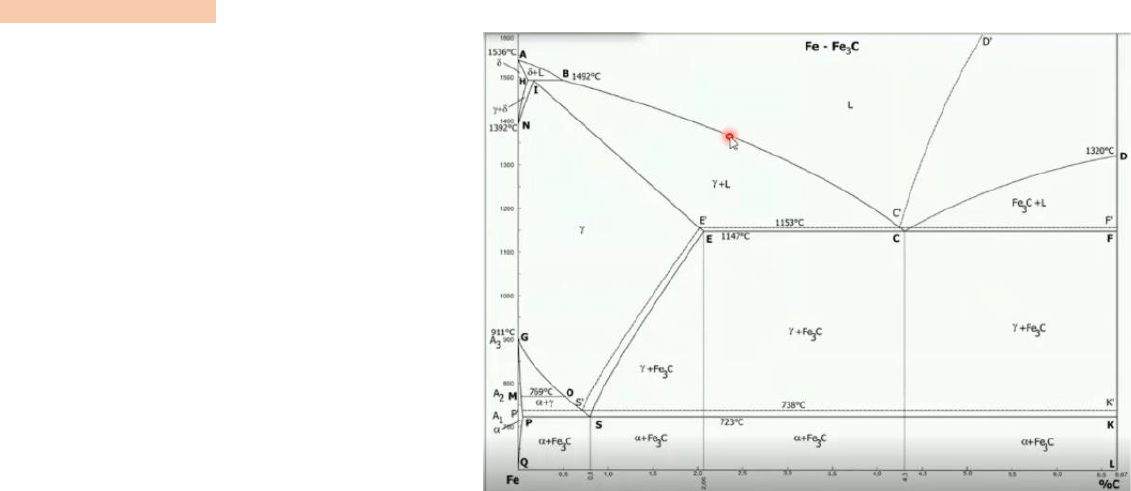
Curva de enfriamiento de Fe puro:
El hierro puro es uno de los elementos que presenta la propiedad
de alotropía (diferentes estructuras cristalinas a diferentes
temperaturas).
Por encima de los 1539ºC el hierro solidifica y lo hace en estructura
del tipo BCC con un parámetro de red de 2.83 Armstrong.
Luego baja a los 1400ºC, allí se produce un cambio de estructura
cristalina y de ser BCC pasa a ser FCC.
La variedad alotrópica señalada con la flecha superior es conocida
como hierro delta.
El segundo tramo donde es FCC se lo conoce como hierro gamma
(flecha siguiente), el parámetro alotrópico crece de 2.83 crece a
3.64.
El hierro gamma está presente hasta los 910ºC donde sufre un
nuevo cambio alotrópico con un parámetro de red un poco mayor,
es 2.9 y se lo conoce como hierro Alpha.
A 768ºC tiene un nuevo cambio, ya no alotrópico ya que no varía el
tipo de red, el cambio es de parámetro, la red cubica pasa de tener
un lado de 2.9 a 2.88. se producen cambios en relación al
magnetismo.
Las letras griegas que utilizamos para identificar las variantes
alotrópicas, son las mismas que usaremos para indicar las
soluciones solidas que forman cada una de ellas con carbono.
𝜎
Diagrama Fe – C:
se puede encontrar como hierro – carbono o
hierro – carburo de hierro.
Esta limitado al 6.67% de carbono.
Se limita así porque el 6.67% con la formula
estequiométrica Fe
3
C forma un
microconstituyente que se llama cementita,
que es un componente químico. El eje
derecho (vertical) de la cementita divide el
diagrama en dos partes, todo a la derecha
del 6.67% no tiene interés tecnológico, son
aleaciones extremadamente duras y frágiles,
no sirven para ningún tipo de aplicación
conocida.
Por eso es que el diagrama se analiza para el
100% de Hierro y solo el 6.67% de carbono.
Las líneas punteadas que se observan, se
trazan porque el diagrama presenta algunas
variaciones.
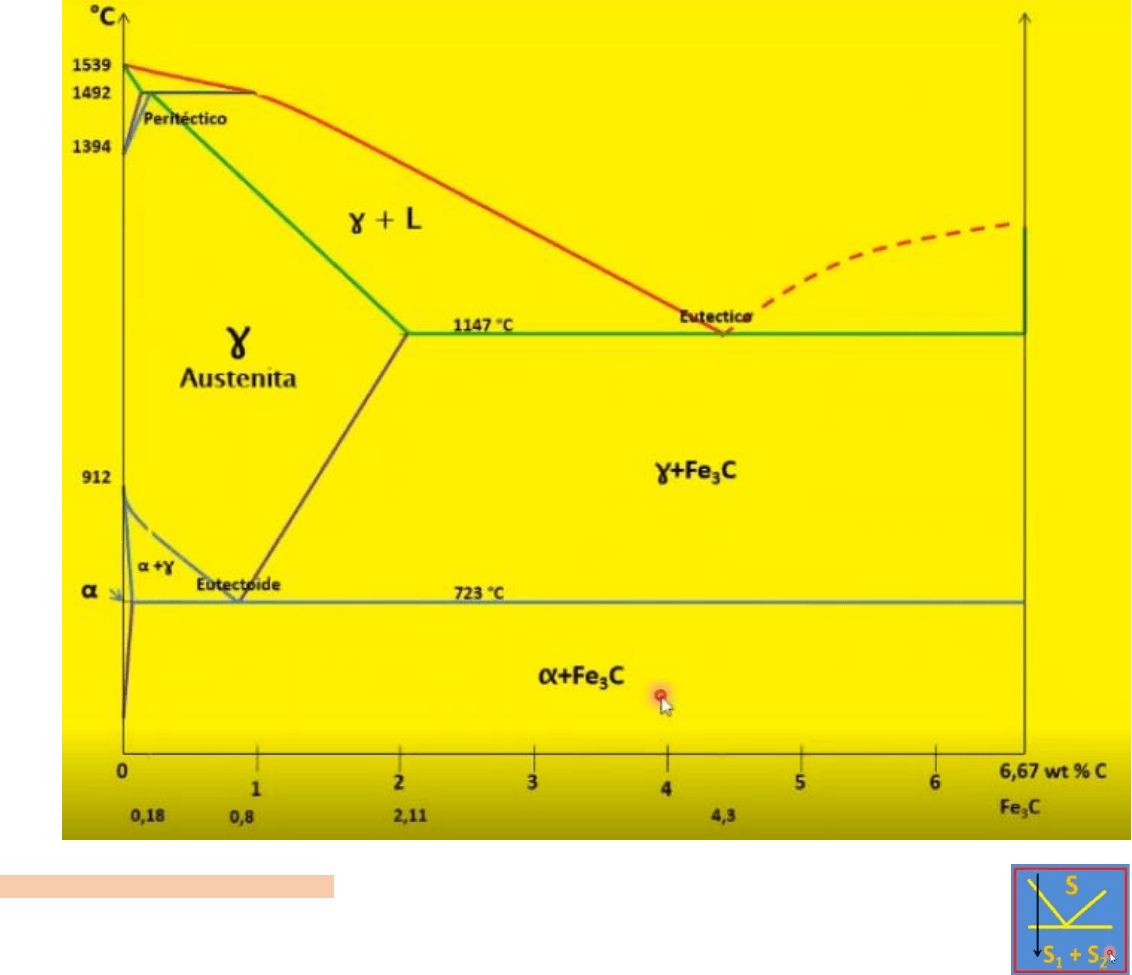
Para dibujar el diagrama, identificaremos primero las rectas horizontales, indican que allí tenemos isotermas
(temperaturas constantes), sabemos que a temperatura constante ocurren las transformaciones como la eutéctica.
En el diagrama observamos a transformación eutéctica en la recta horizontal del medio del diagrama, también
podemos ver otras dos transformaciones que no vimos con anterioridad.
Una es la eutectoide, que se observa en la recta horizontal inferior, y la otra es peritectica que se ve en la línea
horizontal superior.
Entonces, tenemos tres isotermas: la primera a 723ºC (se la conoce como temperatura de eutectoide), la segunda a
1153ºC (temperatura de eutéctico) y la tercera a 1492ºC (temperatura de coulomb), estas dividen el diagrama en tres
partes en el sentido de la temperatura. Si nos fijamos ahora en el sentido horizontal, cada uno de los puntos que
marcamos recién están relacionados a una concentración. El superior a la concentración del peritectico, el inferior a la
concentración del eutectoide y el central a la concentración del eutéctico.
Ahora agregamos el punto E que vemos en la convergencia central del diagrama, al 2.08 de carbono, vemos que es la
máxima solubilidad de carbono en hierro gamma.
Lo primero que hacemos para dibujar el sistema es trazar los ejes de temperatura y composición, para comenzar el
dibujo, ubicamos los puntos característicos marcados anteriormente.
Después de marcar las tres horizontales correspondientes a las temperaturas, marcamos las composiciones que se dan
para cada uno de esos puntos característicos, la primera concentración es la del punto peritectico y este se da para
0.18% de carbono (los aceros tienen un máximo de 1.2% de carbono, eso es considerado un alto porcentaje de
carbono), luego tenemos el eutectoide que es también una transformación que se da a temperatura de 723°C que
tiene las mismas características del eutéctico pero con la diferencia de que se da íntegramente en estado sólido, se da
al 0.8% de carbono. El punto siguiente es el del eutéctico que está al 4.3% de carbono.
El punto de 1539°C que aparece arriba es el punto de fusión del hierro, que será común a la línea de liquidus y Solidus.
El otro punto común a la línea de liquidus y Solidus será el eutéctico porque sabemos que en el eutéctico existe el
líquido que solidifica a temperatura más baja. Si dibujamos la línea de liquidus (rojo) tendrá la forma que indica el
diagrama.
Ahora deberíamos trazar la línea de Solidus que tiene la forma del diagrama (azul). El carbono forma solución solida
con las tres variantes alotrópicas del hierro.
Ahora nos falta resolver lo que sucede cercano al eje de temperatura, retiramos las líneas auxiliares. La isoterma del
peritectico la dibujamos arriba en azul, es una línea bastante particular porque el peritectico es una transformación
que se verifica a temperatura constante y tiene como característica que, de un líquido y un sólido, al atravesar la
temperatura de peritectico se forma un sólido distinto.
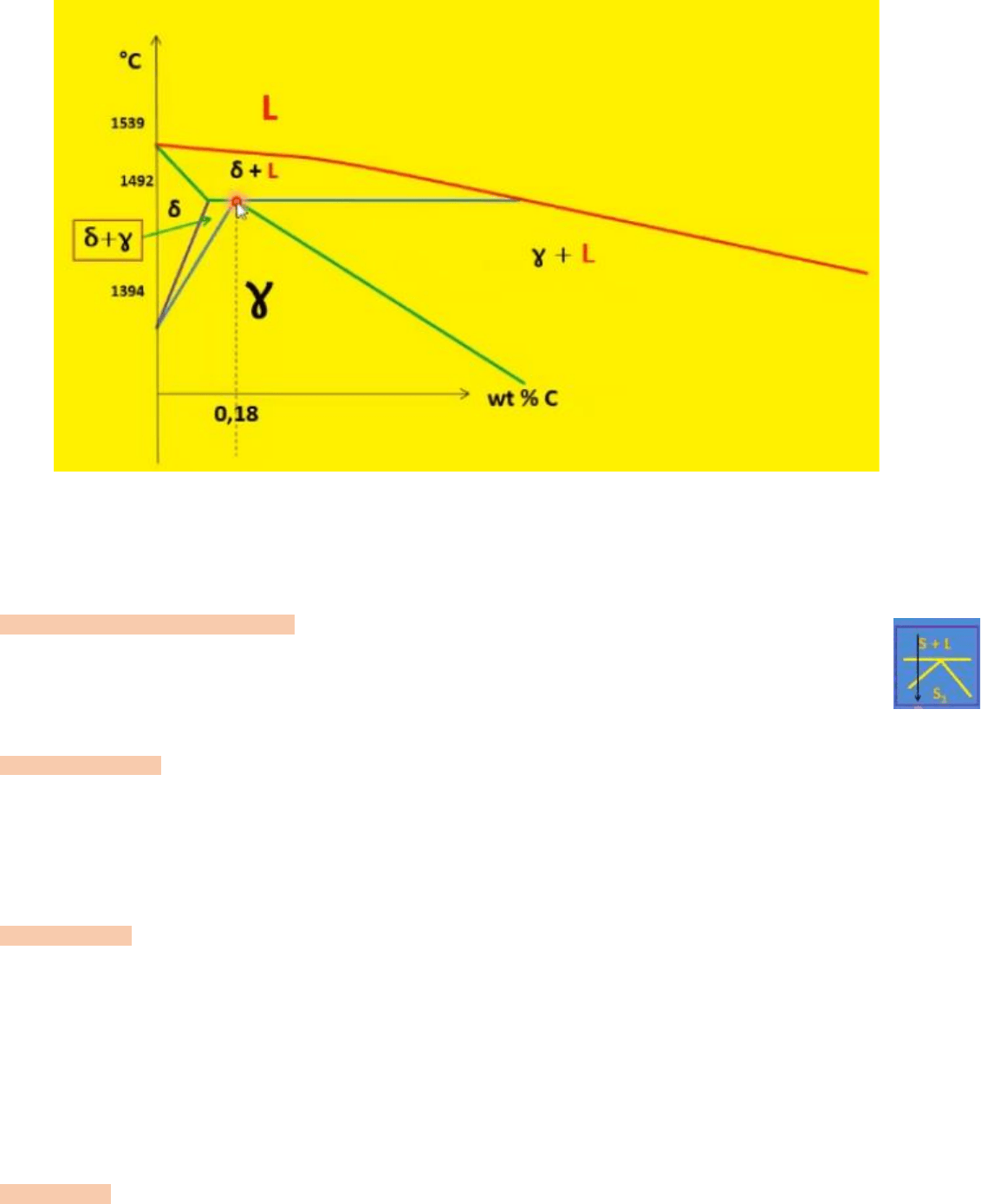
A 1394°C se termina de producir la transformación alotrópica del hierro y se genera la línea de solvus (marca la
variación de solubilidad del carbono en hierro delta) el triángulo va desde el eje de temperaturas al punto peritectico,
si paso exactamente por el punto peritectico voy a ir desde un líquido + solido a un sólido distinto.
Ahora vamos a trabajar en la región del eutectoide. A los 912°C el hierro gamma va a comenzar a transformarse y
tendrá una cierta solubilidad. Tiene una línea de solvus que va a indicar la variación de solubilidad en estado sólido
(solubilidad del carbono en hierro tipo alpha) allí se van a generar las dos líneas del diagrama (línea solvus en lila) y
termina formandosé una V donde vamos desde un sólido a dos solidos distintos.
En líneas generales: en la región de abajo tengo alpha + cementita.
𝜎
El diagrama se termina con una isoterma en 723°C (en azul) ya que hay un cambio de un sólido a dos solidos a
temperatura constante.
El nombre de las soluciones formadas en cada región puede verse en el diagrama
El diagrama completo se vera de la siguiente manera:
Características del eutectoide:
De un sólido a través de un enfriamiento pasamos a dos solidos distintos.
- Es una mezcla fina de fases.
- Existe para una temperatura y composición dadas
Cuando atravieso la temperatura de eutectoide se forma la mezcla fina de fases que se conoce con el nombre “perlita”,
se suele decir que es una mezcla fina de fases alpha y cementita, y su aspecto es el de una huella digital.
Es el microconstituyente eutectoide, es una mezcla de fases formado por capas alternadas de ferrita alpha y cementita,
y está compuesta por un 88% de ferrita y un 12% de cementita, contiene el 0,8% de carbono. Tiene una dureza media
de 250 Brinnel, una resistencia a la tracción relativamente baja, de 80 kg/mm
2
y un alargamiento del 15%, es decir que
antes de romperse se va a deformar un 15%. (ductilidad importante)
El nombre de la perlita se debe a que adquiere un aspecto parecido al de perlas cuando se las ilumina. La
transformación isotérmica en la que se transforma es a los 723°C – 727°C (según la bibliografía que se use).
𝜎
𝜎
𝜎
𝜎
En la región del peritectico tenemos lo siguiente:
Cualquier aleación de este sistema que este dentro de estas composiciones, a esta temperatura (mayor a 1300°C), el
grano habrá crecido tanto que el material tendrá estado de “quemado” y no va a servir para nada. Por lo que se
debería fundir y volver a hacer el acero.
Desde el punto de vista tecnológico, nada interesante pasa en la región mostrada en el diagrama que vemos arriba.
Características del peritectico:
Sabemos que a partir de un sólido + un líquido se forma un sólido distinto.
- Está a 1492°C y al 0,18% de carbono. Este es el punto estable de la austenita (aparece aquí) a
mayor temperatura.
- Existe para una temperatura y composición dadas
Fases solidas:
- Están presentes dentro del diagrama hierro – carbono.
- Fase es toda porción química y físicamente diferenciable.
Individualizando las fases dentro del diagrama podemos observar:
- Ferrita delta: es una disolución de carbono en hierro (variedad alotrópica delta)
- Austenita gamma: disolución de carbono en hierro (variedad alotrópica gamma)
Austenita: es un microconstituyente fundamental en los aceros para los procesos de tratamientos térmicos a los que se
somete a los aceros para mejorar sus características mecánicas.
Es el componente más denso de los aceros y está formada por una solución solida por inserción de carbono en hierro
gamma. La cantidad de carbono disuelto varia del 0.8 a 723°C al 2% que es la máxima solubilidad a 1130°C.
La austenita no es estable a la temperatura ambiente, pero existen algunos aceros al cromo – níquel denominados
austeníticos cuya estructura es austenita a temperatura ambiente.
La austenita está formada por cristales cúbicos centrados en las caras, con una dureza de 300 Brinell, una resistencia a
la tracción de 100 kg/mm
2
y un alargamiento del 30%, no es magnética.
- Ferrita alpha: es una disolución de carbono en hierro (variedad alotrópica alpha)
Ferrita: es una solución solida de carbono en hierro alpha, su solubilidad a la temperatura ambiente es del orden
0,008% de carbono (capacidad baja de disolución de carbono), por esto se considera como hierro puro, la máxima
solubilidad de carbono en el hierro alfa es de 0,02% a 723°C
La ferrita es la fase más blanda y dúctil de los aceros, cristaliza en la red cubica centrada en el cuerpo, tiene una dureza
de 90 Brinell y una resistencia a la tracción de 28 kg/mm
2
llegando hasta un alargamiento del 40%. La ferrita se observa
al microscopio como granos poligonales claros.
Es el microconstituyente más blando que está presente en los aceros.
𝜎
𝜎
𝜎
- Cementita: compuesto químico que se forma con 3 átomos de hierro y uno de carbono, está al 6,67% de
carbono presente en el diagrama
Cementita: es el carburo de hierro, contiene 6,67%C y 93.33%, es el microconstituyente más duro y frágil de los aceros
al carbono, alcanzando una dureza de Brinnel de “700” (68 Rc) (entre comillas porque el límite superior de la dureza
Brinell ronda los 600) y cristaliza en la red ortorrómbica.
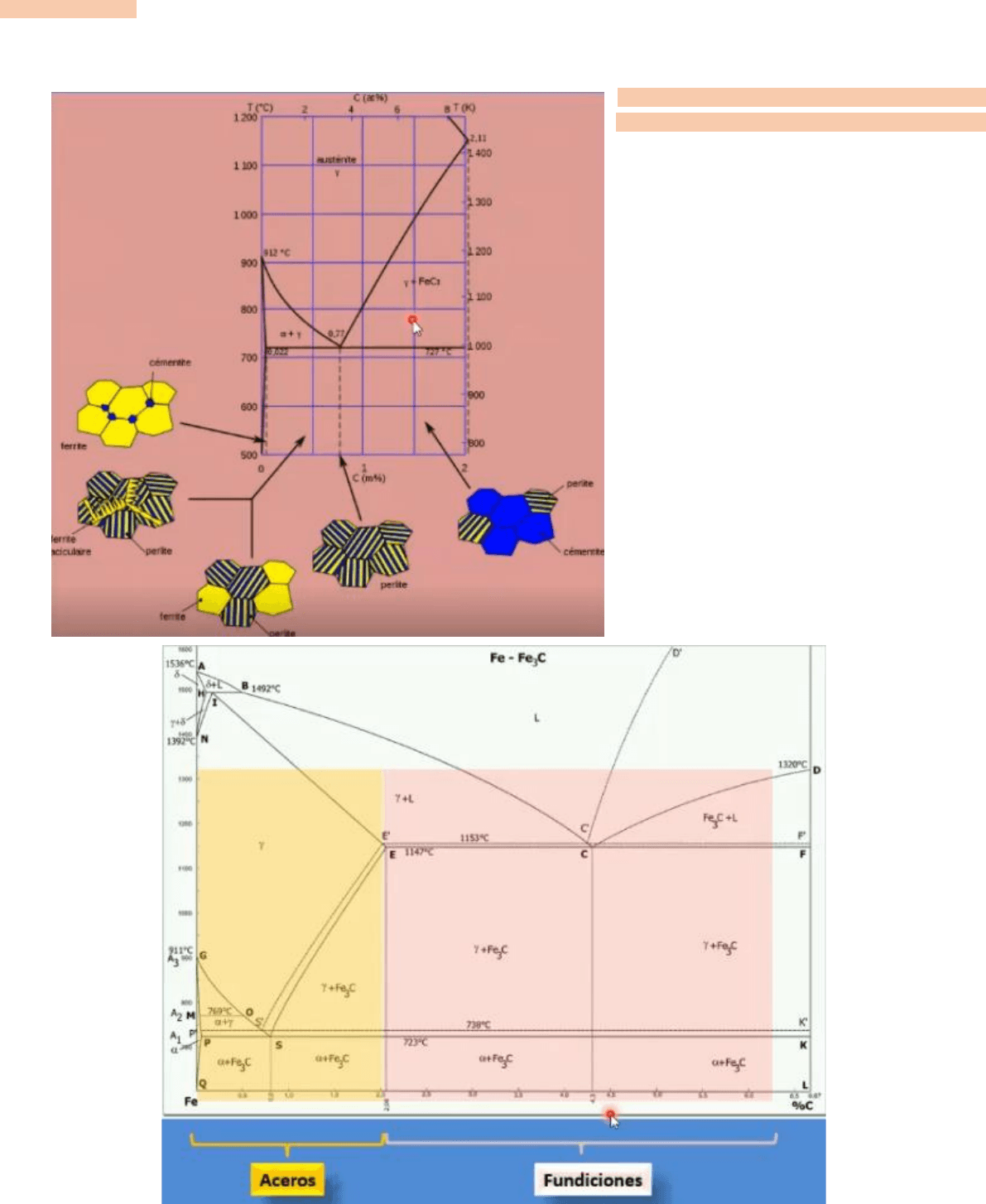
Fases constituyentes de aceros
eutectoides:
Los aceros eutectoides son los que se
encuentran en la parte inferior del
diagrama Fe – C.
El diagrama representa el sistema donde
están los aceros y las fundiciones, el
campo de los aceros va desde el 0 al 2.11%
de carbono, lo cual comprende la región
del eutectoide completa, los aceros a su
vez se dividen en dos subgrupos: los hipo
eutectoides (concentración entre 0 y 0.8%
C) y los hiper eutectoides (0,8 a 2,11%C).
𝜎
𝜎
𝜎
Tratamientos térmicos
Los tratamientos térmicos son procesos tecnológicos que se le aplican a los materiales con el objetivo de modificar sus
propiedades. Como su nombre lo indica está involucrada la temperatura.
Diagrama de equilibrio Hierro – carbono:
En este diagrama vamos a hacer especial hincapié en la Austenita, que es una solución solida de carbono en hierro
gamma, FCC, con una solubilidad máxima del 2,11% a 1147º, y rango de existencia entre 2492º y 723º. La parte inferior
de la región de la austenita involucra a la región del eutectoide que pasara a ser de gran importancia en el tratamiento
de este tema.
Citando este diagrama, lo que vemos es que los primeros tratamientos térmicos que vamos a ver son aplicables
exclusivamente a las aleaciones ferrosas, es decir a los aceros entre el 0% y el 2%, algunos a las fundiciones entre el 2%
y el 4,3% como límite máximo tecnológico de fundición.
La mezcla de fase que se genera a partir de la solidificación eutéctica la llamamos “ledeburita” y la mezcla de fases que
se generaba a partir de la transformación eutectoide la llamamos perlita, y esta perlita no es más que ferrita Alpha más
cementita.
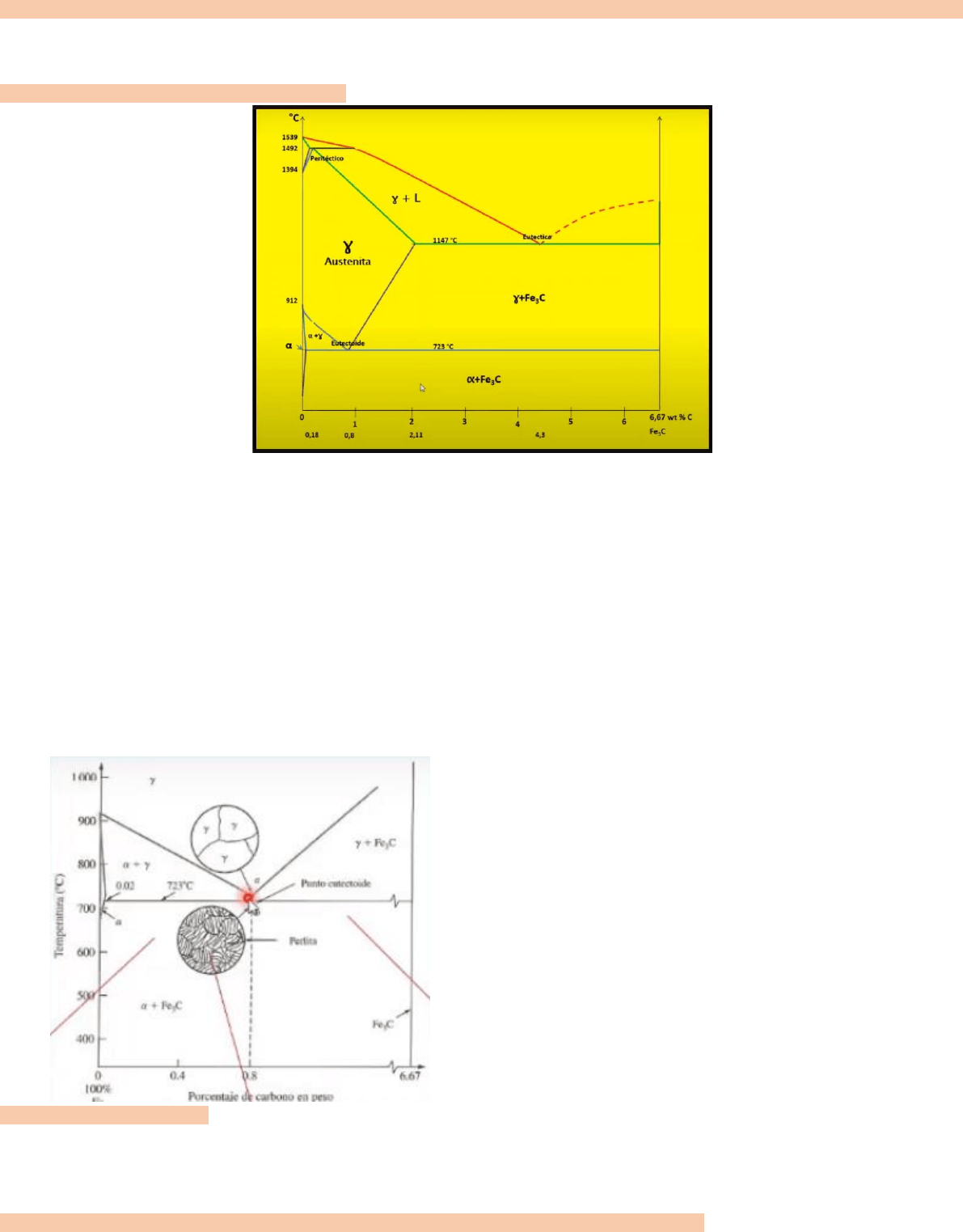
Nos concentraremos en la región del eutectoide, en esta región se verifican algunas líneas que son particulares del
diagrama, la isoterma del eutectoide 723º se lo llama limite critico inferior, y luego tenemos las líneas que son la de
Solvus de la eutenicta a la que llamaremos ACM y la línea superior de los aceros la llamamos hipo eutectoide.
hipos eutectoides van entre 0 y 0,8% e hiper eutectoides entre
0,8% y 2,11% hipotéticos.
En la región del eutectoide, lo que tenemos es, para una aleación
al 0,8% de carbono, que por arriba de los 723º se encuentra en
estado de solución, todo era austenita, si luego lo enfrío tengo
perlita. Que esta esquematizada en la imagen. Vemos perlita
pura.
Tratamiento térmico: es un ciclo de calentamiento, mantenimiento y enfriamiento controlados para modificar las
estructuras y en consecuencia las propiedades asociadas, en los materiales metálicos.
Como el objetivo del tratamiento térmico es modificar la estructura, en consecuencia, tendremos modificaciones en las
propiedades.
Representación gráfica de un tratamiento térmico en función del tiempo y la temperatura:
Decimos que es un ciclo de calentamiento, por lo que habrá un aumento de temperatura a lo largo del tiempo, decimos
que tanto el calentamiento como el mantenimiento y el enfriamiento son controlados, las variables de control que tengo
𝜎
durante el ciclo son el tiempo y la velocidad con que hago variar la temperatura, es decir, cuantos grados va a subir la
temperatura por unidad de tiempo, estará representado por la pendiente de la recta.
Vamos a decir que luego de eso viene un mantenimiento, alcanzada la temperatura necesaria para la realización del
tratamiento térmico, debo mantener la temperatura durante un determinado tiempo. La variable de control que tiene
este ciclo es solo el tiempo, ya que la temperatura se mantendrá constante.
Luego vendrá un ciclo de enfriamiento donde tengo las mismas consideraciones que durante el calentamiento, puedo
variar la pendiente de la recta, con lo que hare que se enfríe más rápido o más lento. Es un proceso reversible (en su
mayoría).
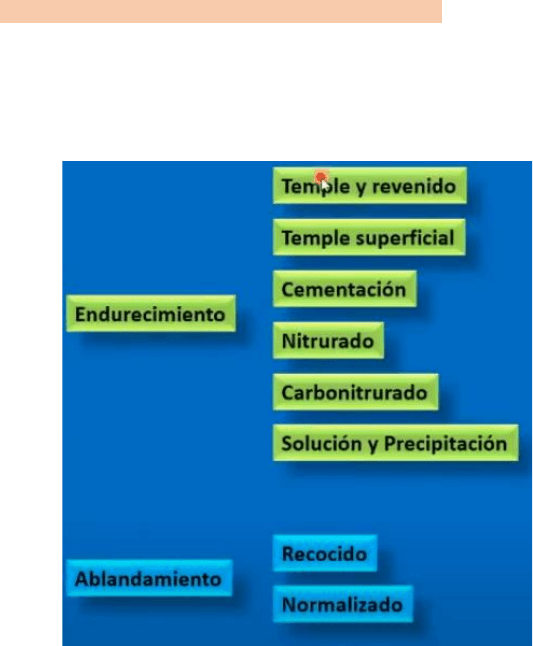
Clasificación de los tratamientos térmicos:
Las propiedades que se pretenden modificar son las propiedades mecánicas, es decir aumentar o bajar su resistencia a
la rotura o dureza. Entonces cuando queremos aumentar la resistencia o la dureza, llamaremos a los tratamientos que
tienen como objetivo esto, tratamientos de endurecimiento. Por el contrario, cuando queremos que un material pierda
dureza o resistencia los llamaremos de manera general tratamientos de ablandamiento.
Cuando se quiere endurecer un acero tenemos varias opciones:
lo más común es hacer un temple y revenido, dentro de los
temples tengo algunas variantes que dependen del modo de
realizarlo, por ejemplo, el temple superficial, el primer
tratamiento tiene como objetivo variar la estructura y las
propiedades de la masa, y el segundo solo de una porción de la
masa (superficial y subsuperficial).
Hay tratamientos termoquímicos como la cementación donde
caliento y agrego una capa de carbono en un área superficial del
material para obtener una estructura particular.
El nitrurado es cuando se agrega nitrógeno, el carbonitrurado es
cuando se agrega carbono y nitrógeno. Los tres son tratamientos
del tipo superficial (solo se cambia la estructura de la capa
superficial) y termoquímicos.
La solución y precipitación es un tratamiento que tiene como
objetivo obtener determinadas propiedades en toda la masa igual
que el temple y revenido pero que obtiene esta mejora de
resistencia y dureza por un mecanismo que es absolutamente
distinto al del temple y revenido, aunque el procedimiento es
exactamente el mismo (aplicable a metálicos no ferrosos).
En el caso de ablandamiento, tenemos dos grandes grupos que son los recocidos y los normalizados, esta clasificación
pretende dar una idea de diferentes tipos de tratamientos.
Entonces concluimos que con un tratamiento térmico se puede aumentar o disminuir las características mecánicas de
un material.
¿Qué sucede con la austenita cuando atraviesa temperaturas conocidas como temperatura de eutectoide (debajo de los
723º)? Trabajaremos con la curva TTT. (temperatura, transformación y tiempo).
𝜎
𝜎
𝜎
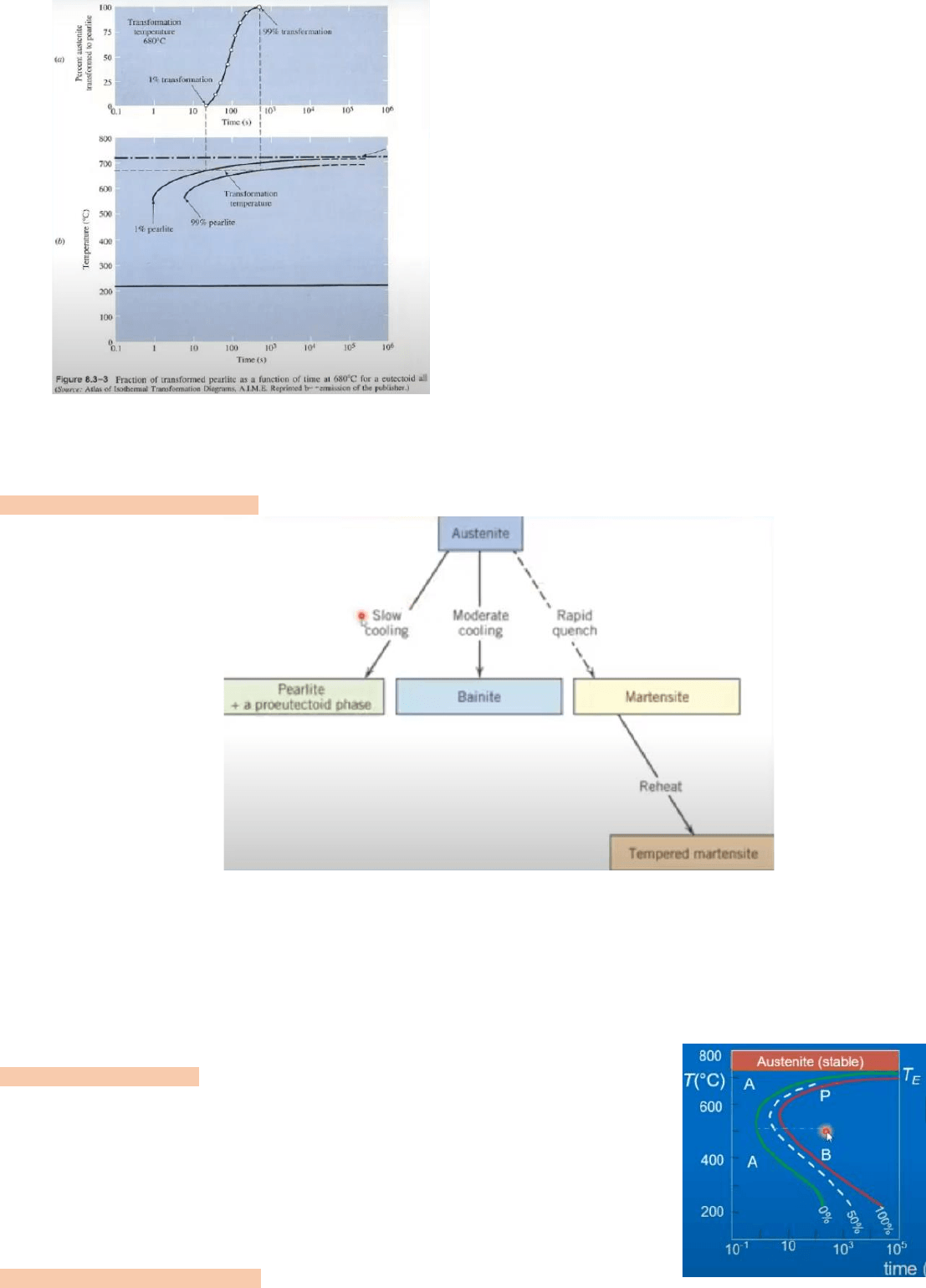
Las curvas representan la transformación isotérmica de la austenita
a temperatura constante.
Si tomo austenita a una temperatura superior a los 723º, y la enfrío
rápidamente, sucederá que la austenita como ha sido enfriada de
esa manera, no tendrá tiempo de transformarse de la variedad
alotrópica FCC que tenía el hierro a 800º, a la BCC que le
corresponde según el diagrama de equilibrio a una temperatura
inferior a los 723º.
Sucederá que, como todos los sistemas tienden al equilibrio, el
estado de equilibrio que debería tener el hierro es BCC, por lo tanto,
si dejo transcurrir el tiempo, la austenita comenzará a tender al
equilibrio.
Por métodos dilatometricos puedo identificar el momento en que la
austenita comienza a formarse, y si voy tomando el tiempo y viendo
como aumenta la transformación, veré cual es el porcentaje de
transformación en base al tiempo.
La curva que vemos arriba representa el proceso de transformación
isotérmica de la austenita, tenemos tiempo en eje de abscisas y
transformación en ordenadas. Se la como curva de la S (se obtiene con la experiencia de Vine y se lleva al diagrama
inferior).
Durante toda la transformación la temperatura se mantiene constante.
Transformaciones posibles:
Bainita: perlita extrafina. Rapid quench: temple. Reheat: recalentar
Cuando se hace el proceso para obtener martensita, se aumenta la resistencia. La martensita es la más resistente, la
martensita revenida es aún más resistente, la bainita menos resistente, la perlita fina menos resistente, la gruesa menos
resistente y la esferoidita (caso particular) mucho menos resistente. La ductilidad se comporta de forma opuesta, será
muy baja en la martensita y muy alta en la esferoidita.
Tendencia general: aumenta la resistencia mientras más rápido enfriamos y aumenta la ductilidad mientras más lento
enfriamos.
¿Qué es la bainita?
Es lo que se obtiene cuando enfrío rápidamente, paso el punto más próximo al eje
de las temperaturas (nariz perlítica). cuando la temperatura está por encima de la
nariz perlítica decimos que existe perlita, si está por debajo existe bainita.
La bainita tiene la característica de ser una especie de perlita extremadamente fina,
formada por ferrita y cementita. Otra característica es que tiene una alta resistencia
y conserva una muy buena ductilidad, comparada con la que se obtiene al tener
martensita.
¿en qué consiste la bainita?
Consiste en una estructura que llamamos de tipo acicular (tiene forma de agujas) de ferrita con pequeñas partículas de

𝜎
𝜎
𝜎
cementita dispersas en ella. El contenido de carbono es típicamente por arriba del 0,1% y la bainita se transforma en
hierro y cementita con la condición de que tenga la temperatura y tiempo suficiente para hacerlo.
Es una estructura donde se presentan estructuras aciculares que producen una fuerte distorsión en la red que producen
un aumento de resistencia en la ferrita (por la presencia de las agujas de la bainita).
Esferoidita: Es una microestructura que se consigue después de tener perlita o bainita por un calentamiento posterior
de la perlita o la bainita.
La perlita al ser recalentada tiende a redondearse, se forman una especie de nódulos o esferas que le dan el nombre a la
esferoidita
¿Qué se consigue en la esferoidización? Conseguimos la máxima ductilidad, es decir, el material se ablanda fuertemente,
adquiere una gran deformación porcentual por rotura y pierde resistencia a la rotura.
Martensita: es otra microestructura que se genera cuando los enfriamientos no están en equilibrio. Si enfrío austenita a
una temperatura muy baja (debajo de los 220°C) y no corto la nariz perlítica (no la toco) sucederá que la austenita no
tendrá tiempo de transformarse en ferrita y cementita (que es lo que debería pasar) y tendré austenita a temperatura
inestable. Si sigo bajando la temperatura sucederá la transformación martensítica, que ya no es isotérmica. Para que
progrese, es decir, que vaya desde 0 a 100 para que la austenita se transforme totalmente en martensita necesito
continuar bajando la temperatura para que aumente la transformación. La estructura resultante es similar a la de la
bainita con una estructura acicular.
No se forma el BCC por ser un enfriamiento desequilibrado y violento. No se produce difusión y hace que la estructura
cristalina sea del tipo BCT, Tetragonal centrada en el cuerpo, que es una deformación fuerte de la BCC.
Entonces, la martensita es un microconstituyente que se consigue por el enfriamiento busco, rápido, ultrarrápido de la
austenita, por temperaturas debajo de los 220°C y mediante un proceso de no difusión se transforma de Austenita
Gamma FCC en martensita BCT de aspecto totalmente acicular, es una estructura fácilmente deformada, por lo que será
muy difícil que en ella se pueda mover una dislocación, por lo que decimos que tiene máxima resistencia, máxima dureza
y máxima fragilidad.
La estructura BCT tiene pocos planos de deslizamiento, esto otorga la máxima dureza y la máxima fragilidad.
Para que haya cada vez más martensita es necesario que se enfríe muy rápidamente.
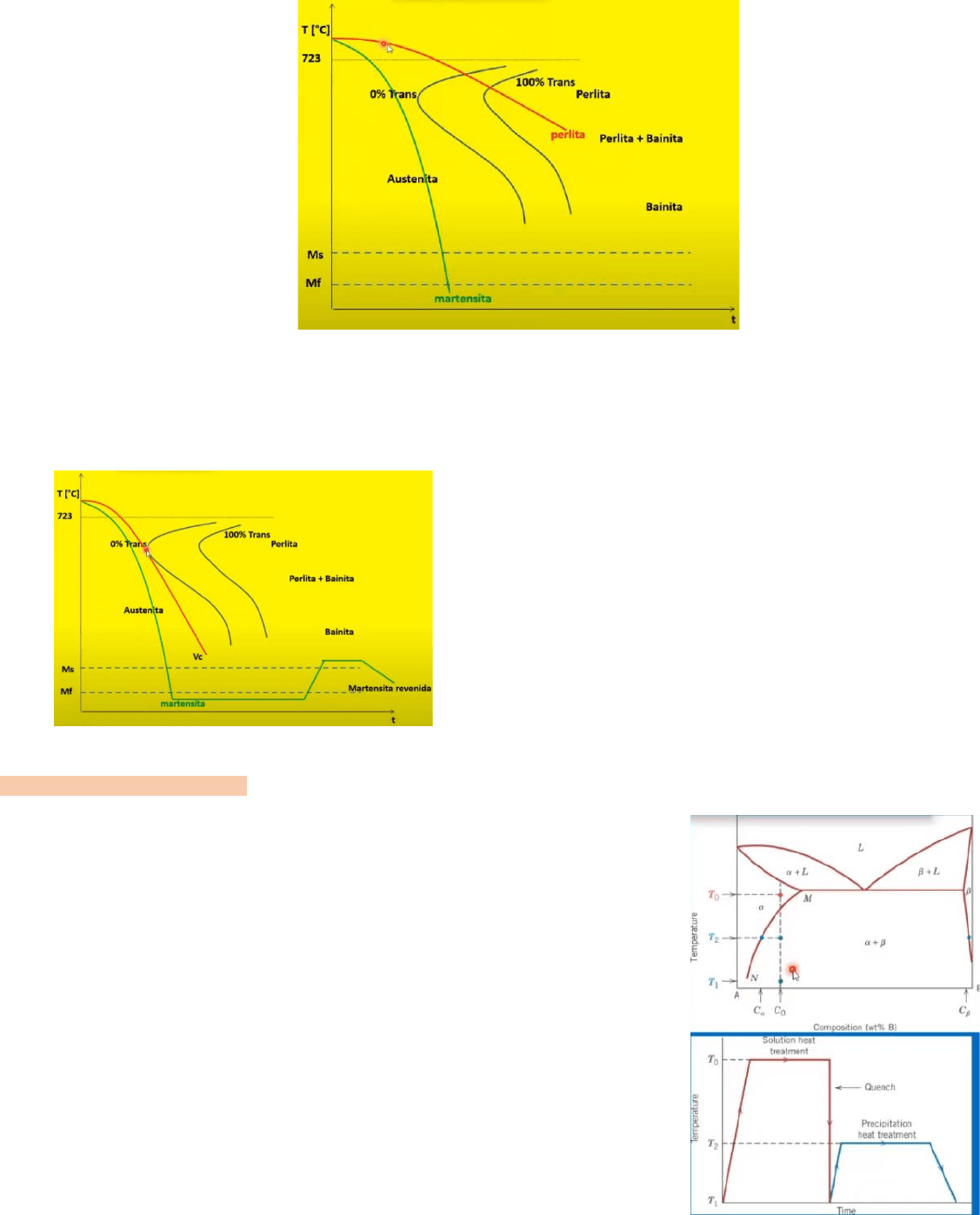
Curvas TTT para acero eutectoide:
¿Cómo hacemos un tratamiento térmico? Lo hacemos mediante la superposición del diagrama TTT y el diagrama que
llamamos de enfriamiento continuo.
𝜎
El diagrama de enfriamiento continuo es el siguiente:
La curva TTT superpuesta con la curva de enfriamiento continuo se utilizan para determinar que voy a obtener en cada
tratamiento térmico.
¿Por qué es importante el temple y el revenido? Porque es el único tratamiento térmico aplicable a los aceros que
permite aumentarles su resistencia.
Las velocidades de enfriamiento rápidas que suelen ser necesarias para obtener el resultado deseado en los tratamientos
térmicos se consiguen con diferentes medios de enfriamiento, pueden ser agua corriendo a alta velocidad, agua sin
movimiento, agua en movimiento con sal, polímeros específicos de
tratamiento, aire, etc. Siempre son métodos violentos para evitar la
formación de materiales que no cumplan con las características
deseadas.
La velocidad de enfriamiento más baja posible necesaria para formar
el elemento deseado, se llama velocidad critica de temple y es la curva
roja del diagrama y tiene la característica de ser tangente a la nariz
perlítica.
Se utiliza esta temperatura para evitar deformaciones o roturas en el
material.
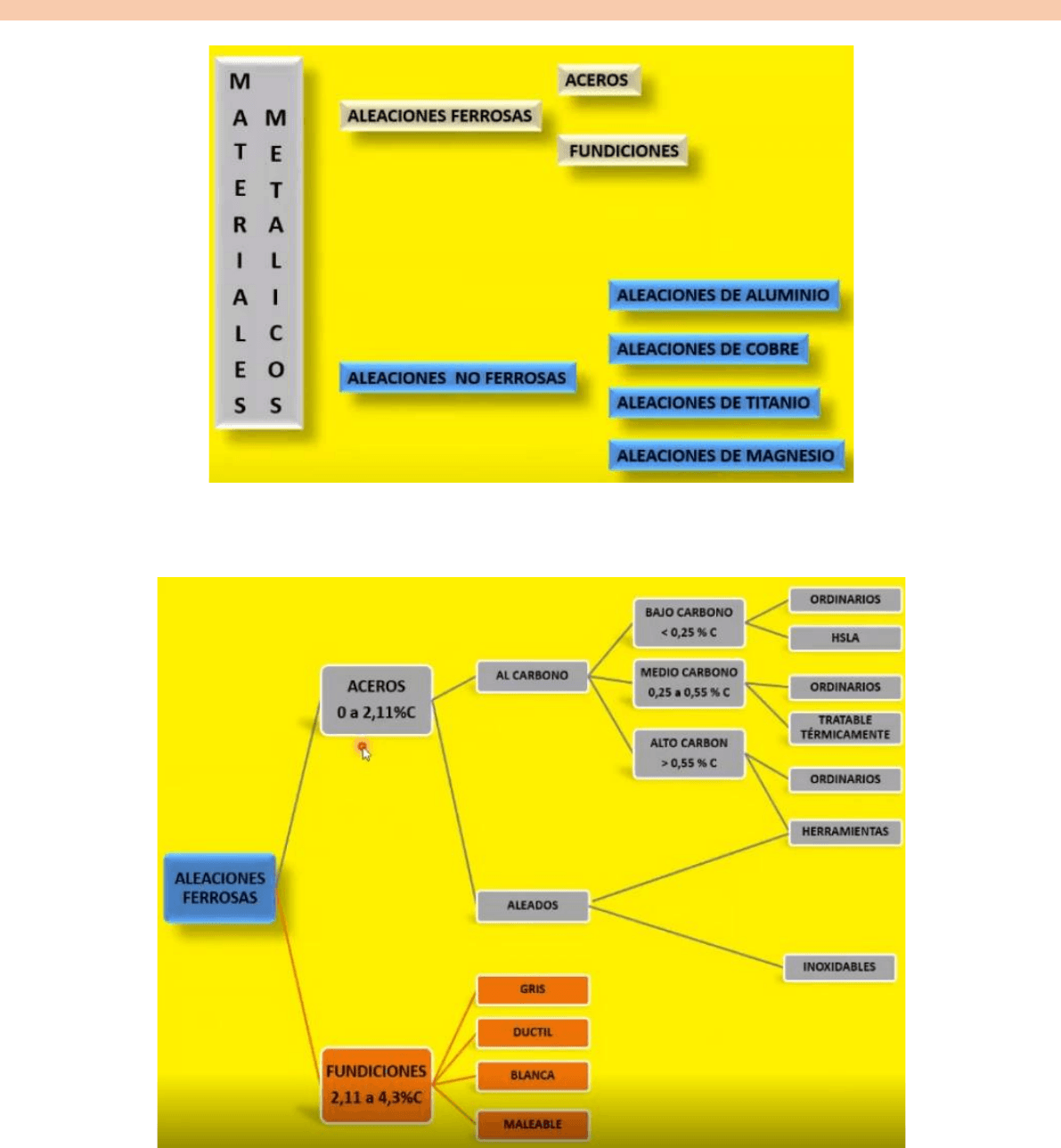
Solución y precipitación: es aplicable, en general a aleaciones no ferrosas. Normalmente aleaciones de aluminio.
El proceso requiere de un calentamiento, enfriamiento rápido y un posterior
calentamiento a temperaturas más bajas. (se llama proceso de envejecido).
Para que se pueda realizar un tratamiento de solución y precipitación en una
aleación es necesario que exista la solubilidad parcial, si no hay solubilidad
parcial no es posible hacer solución y precipitación.
¿Cuáles son las aleaciones susceptibles a ser tratadas por este método? Todas
aquellas que estén en la composición que corte la línea de solvus.
Tomamos una aleación con una concentración cualquiera c0, y la vamos a
calentar hasta una temperatura t0 con el objetivo de que se convierta toda su
masa en Alpha, es decir la vamos a llevar a estado de solución. Luego vamos a
enfriar rápidamente, en este primer proceso, entonces, lo que hicimos fue
disolver todo beta, transformar en Alpha y enfriar rápidamente. Como enfriamos
rápidamente, retenemos Alpha a esa temperatura, pero el diagrama me dice que
tengo Alpha + beta, y como el sistema va a tender al equilibrio, si yo enfrío
rápidamente, Alpha con el paso del tiempo va a tender a formar beta. Lo que va
a pasar es que beta al estar todo nuestro solido a una temperatura baja no va a
poder difundir en grandes distancias si no que lo va a hacer localizadamente
generando partículas de beta adentro de los granos de Alpha.
Las partículas de beta dentro de los granos de Alpha actúan como defectos, y al ser defectos de la estructura cristalina,
las dislocaciones tienden a tener dificultades para moverse. Por lo tanto, aumenta la resistencia a la rotura, el límite
elástico y la dureza del material.
En el temple y revenido de los aceros calentamos, enfriamos rápidamente y volvemos a calentar para revenir. En solución
y precipitado de aleaciones de aluminio calentamos, enfriamos rápidamente y volvemos a calentar a una temperatura
más baja para envejecer.
En el primer proceso, lo que hacemos es obtener una microestructura particular que se llama martensita, en el segundo
proceso obtenemos una fase de partículas finas, dispersas en el seno de los granos de Alpha de manera tal de generar
una cantidad de defectos cristalinos que impiden el movimiento de las dislocaciones de manera que aumenta la
resistencia y dureza del material.
Ambos procesos son materiales que se aplican a materiales distintos.
Materiales metálicos
Clasificación de materiales metálicos:
Los metálicos son los más difundidos en aplicaciones industriales de todo tipo por su uso. Están formado básicamente
por metales, pero no son puros, en general son aleaciones con metales y no metales.
En aleaciones ferrosas podemos observar:
Las cuatro aleaciones de fundición se diferencian entre sí por la morfología de cada una.
Además de los porcentajes de carbono, la diferencia fundamental entre aceros y fundiciones es la forma en que está
𝜎
𝜎
presente el carbono. En los aceros al carbono se lo encuentra formando solución solida con el hierro, en las fundiciones
al carbono se lo encuentra en forma de grafito libre, es un estado similar al de la mina del lápiz. Es carbono en forma de
carbón – grafito.
Alto horno: es una maquina gigantesca donde se obtiene el hierro a partir de mineral de hierro.
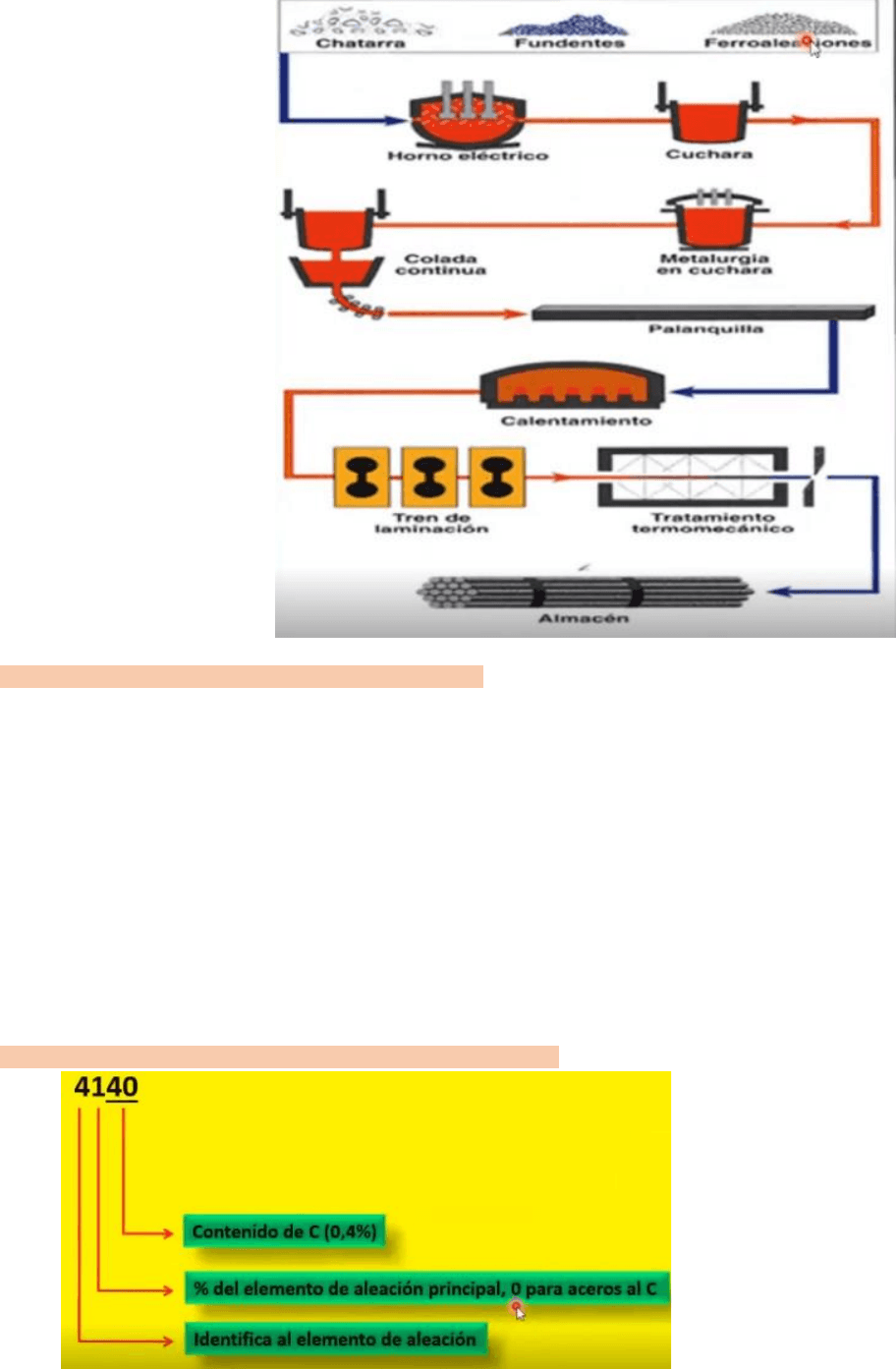
Proceso de obtención con horno eléctrico:
¿Cómo se decide la denominación de un acero?
Existe la normalización, es un documento donde se dan las regulaciones para llevar a cabo un determinado proceso.
La american iron and Steel institute (AISI) así en conjunto con la society of automotive engineers (SAE) revisan los % de
aleación usados en los aceros, determinando el número en el sistema y agregando una letra como prefijo que indica el
método utilizado por la fabricación del acero.
Los prefijos son:
- A = aleación, básico de crisol abierto
- B = carbón, acido convertidor Bessemer
- C = carbón, básico de crisol abierto
- D = carbón, acido de crisol abierto
- E = horno eléctrico
En argentina se usan las AISI y SAE. Suelen ser diferentes para cada país, pero se intenta normalizar en una sola norma
mundial.
La designación SAE para aceros consta de cuatro dígitos:
el primer digito indica el elemento de aleación,
cuando ese digito es 1, estamos en presencia de
un acero al carbono (no tiene otro elemento de
aleación importante).
Es importante recordar que el 40 final indica
porcentaje, pero es 0,4% y no 40%
Este documento contiene más páginas...
Descargar Completo
Preguntero teorico segundo parcial.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.