
1
MATERIAL DE LABORATORIO
Nelia T. Vermouth
Mencionaremos los nombres y usos de algunos de los materiales más
frecuentemente usados en el laboratorio.
Según las aplicaciones de los mismos, podemos dividirlos en seis grupos,
aunque algunos de ellos se podrían ubicar en más de un grupo.
1. para medir volúmenes de líquidos
2. para contener y/o calentar líquidos
3. para calentar sólidos o líquidos
4. para sostener materiales
5. para pesar
6. otros
1.- Para medir volúmenes de líquidos
Los elementos de uso corriente pueden ser de vidrio o de plástico. El
vidrio por su composición química y neutralidad no es atacado generalmente por
las sustancias que va a contener, ni aporta a las mismas partes de él. Últimamente
se fabrican muchos instrumentales de plásticos inertes, rígidos o no, con iguales
resultados a los de vidrio y con mayor duración.
Este instrumental debe ser calibrado o volumétrico y nos permite medir los
volúmenes que escurren o desalojan (pipetas, buretas) o que contienen (probetas,
matraces aforados). Poseen diferentes capacidades.
Pipetas
Las pipetas graduadas son tubos de vidrio perfectamente calibrados, y se
utilizan para medir pequeños volúmenes de líquido que escurren o expelen.
Existen distintos tipos de pipetas con indicaciones precisas de uso. Estas son:
1) Pipetas graduadas o de Mohr: consisten en tubos calibrados, por Ej. de 1mL,
5 mL, 10mL, según su capacidad y sirven para medir volúmenes variables.
2) Pipetas aforadas (ball pipetas): tubos de vidrio calibrados, con una dilatación
central, que permiten medir una cantidad fija y exacta de líquido (desde su
línea de enrase o aforo hasta el extremo inferior, si es de simple enrase, o la
cantidad de líquido que expele entre sus dos aforos, el superior y el inferior,
si es de doble enrase).
Este archivo fue descargado de https://filadd.com
FILADD.COM
2
3) Pipetas Pasteur: Se las utiliza para separar sobrenadantes. No poseen ningún
tipo de graduación.
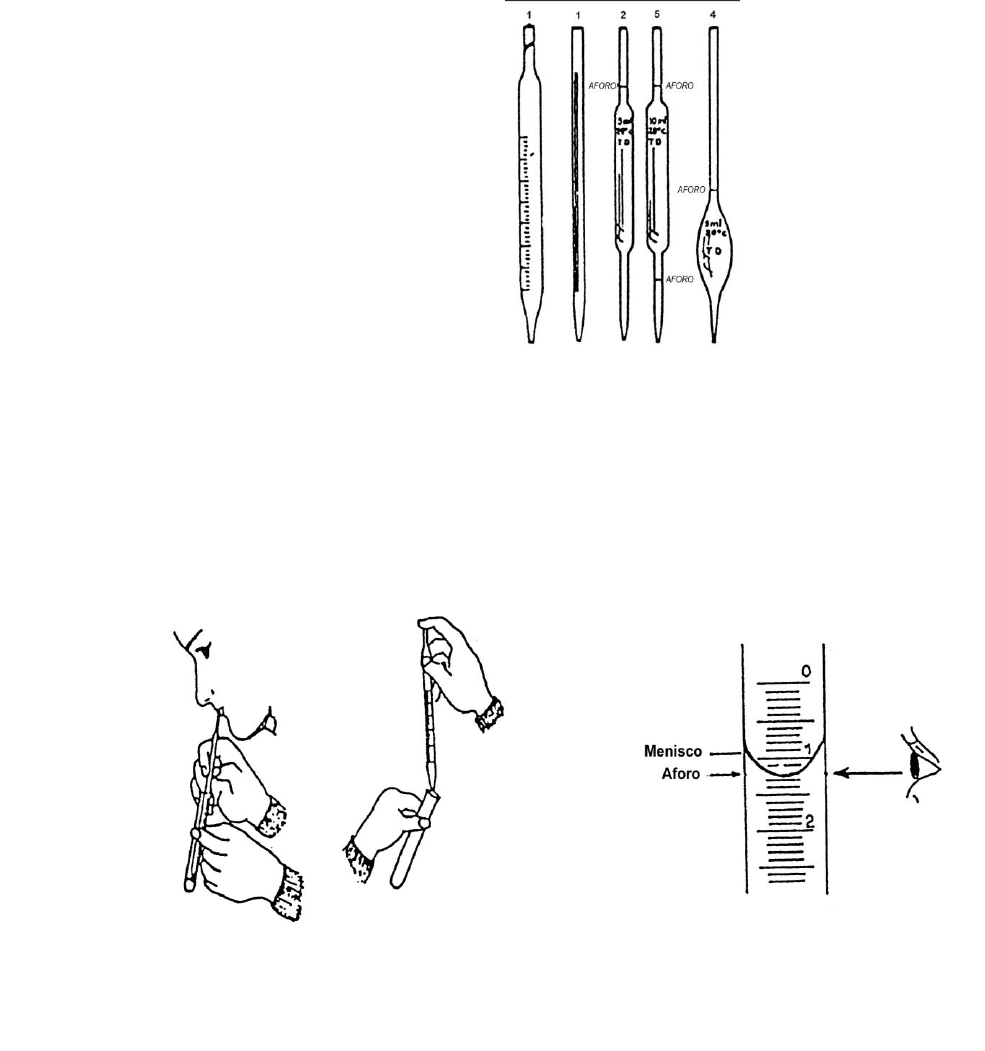
Conviene ensayar el manejo de la pipeta utilizando agua. Después de
aspirar el líquido como indica la Figura 2, se obtura el extremo de la pipeta con el
dedo índice, no con el pulgar! A medida que aspiras observa hasta dónde sube la
columna de líquido dentro de la pipeta, para evitar que llegue a tu boca. Luego
enrasa en cero para después dejar escurrir el líquido gota a gota, hasta conseguir su
salida en forma regular hasta obtener el volumen de líquido que se necesita medir.
Figura 2: Modo de usar la pipeta
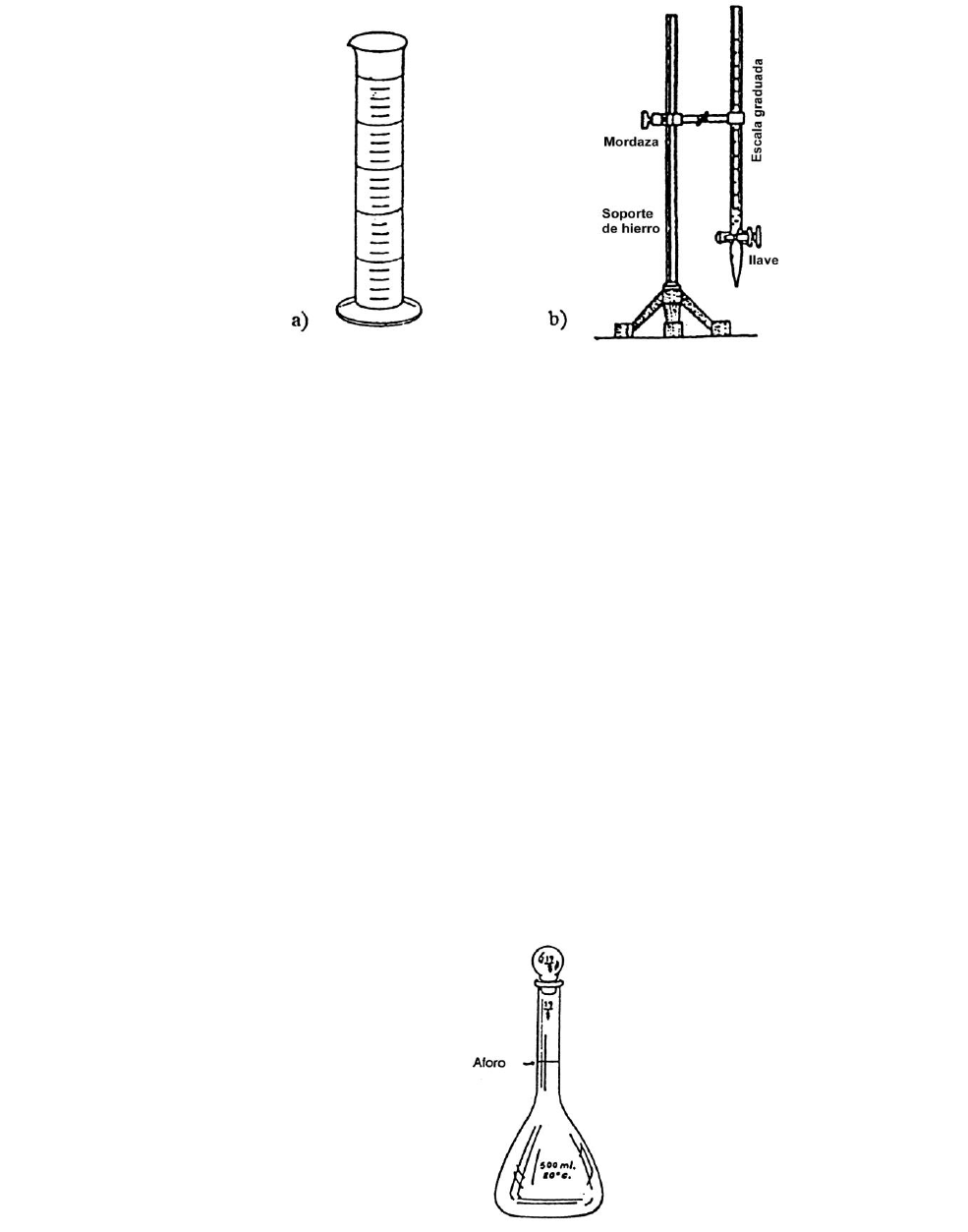
Probetas: son recipientes cilíndricos graduados, que poseen base. Se utilizan
para medir volúmenes de líquidos cuando no es necesaria una gran exactitud. Las
más utilizadas son las de 10, 50 y 100 mL de capacidad.
Figura 1:
1. Pipeta de Mohr
2-4. Pipetas de simple aforo
5. Pipeta de doble aforo
Este archivo fue descargado de https://filadd.com
FILADD.COM
3
Buretas: son tubos de vidrio graduado que poseen una llave o robinete en su
parte inferior, se mantienen en posición vertical con auxilio de un soporte (Fig.
3). Permiten la salida del líquido gota a gota.
Matraces: Los matraces aforados son instrumentos de precisión. Sus fabricantes
indican su capacidad a una temperatura determinada, siempre poseen tapas y se
ofrecen de muy diversos volúmenes, desde 5 a 2.000 mL. Miden con exactitud
los volúmenes que son capaces de contener.
Los matraces poseen siempre base plana, lo que los diferencia de los balones,
que no la poseen (Fig. 4). Son especialmente utilizados para preparar soluciones.
Figura 4: Matraz aforado
Figura 3:
a) Probeta
b) Bureta con soporte
Este archivo fue descargado de https://filadd.com
FILADD.COM
4
2.- Material de laboratorio para contener y/o calentar
El instrumental usado para contener y/o calentar no es calibrado. Se utiliza
como auxiliar de las tareas a realizar y muchos de éstos se fabrican
habitualmente con vidrio térmico, de modo que puedan ser sometidos a la acción
del calor. Los recipientes de fondo plano nunca deben calentarse a fuego directo
(Fig. 5).
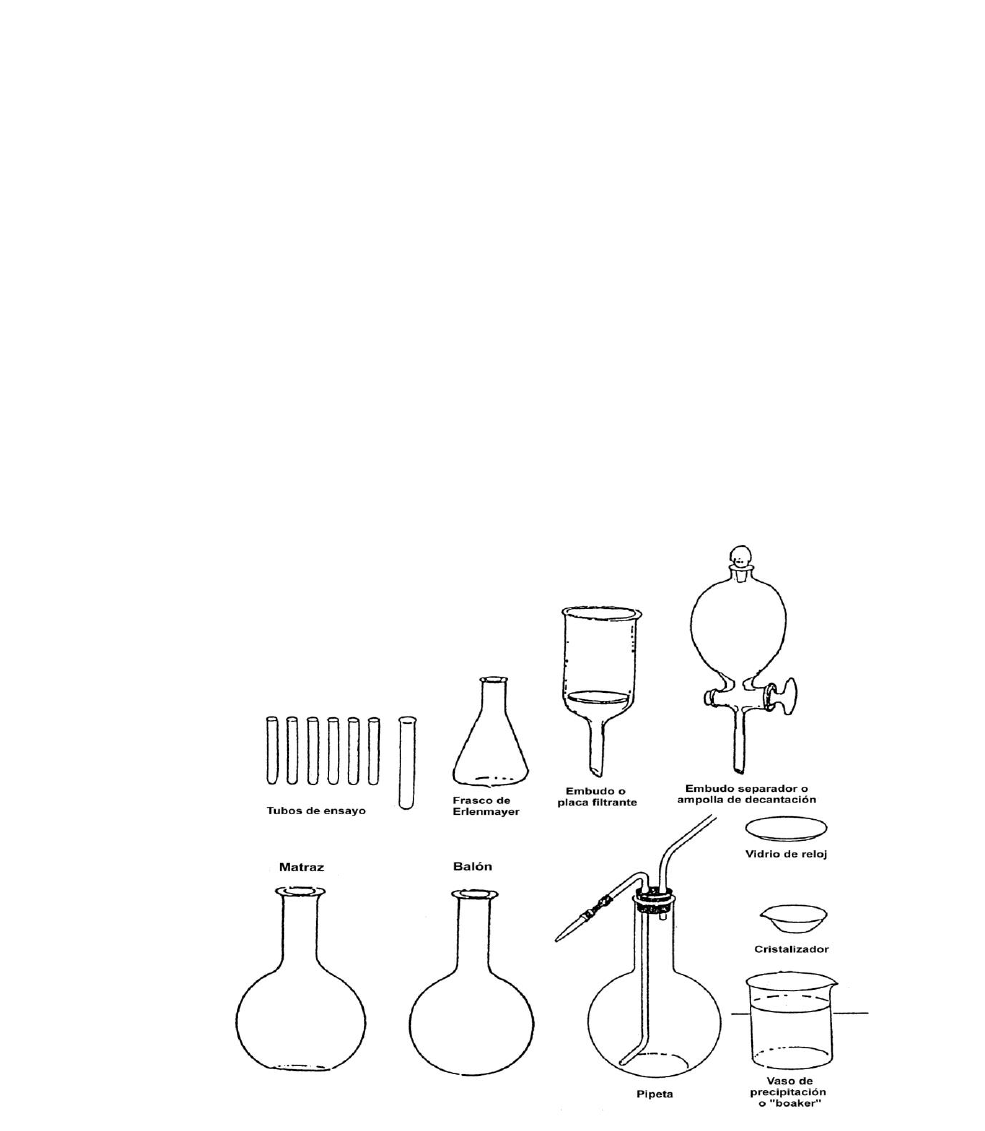
Suelen emplearse:
-cristalizadores, (usados para obtener cristales a partir de una solución),
-vaso de precipitación o beaker (para disolver sustancias),
-tubos en sus distintos tipos (de ensayo, de centrifuga, de hemólisis) y capacidad,
-frasco de erlenmeyer,
-balones (para destilar),
-pisetas (para lavar con agua destilada),
-vidrio de reloj (para pesar sustancias cáusticas),
-desecador, etc.
Figura 5: Instrumental de Laboratorio no calibrado
Este archivo fue descargado de https://filadd.com
FILADD.COM
5
3.- Para calentar sólidos o líquidos
Se utiliza con frecuencia la calefacción con la finalidad de acelerar una
reacción química, facilitar la disolución de una sustancia, etc. Se puede llevar a
cabo utilizando distintos medios, los más comunes son la electricidad y el gas
natural de petróleo.
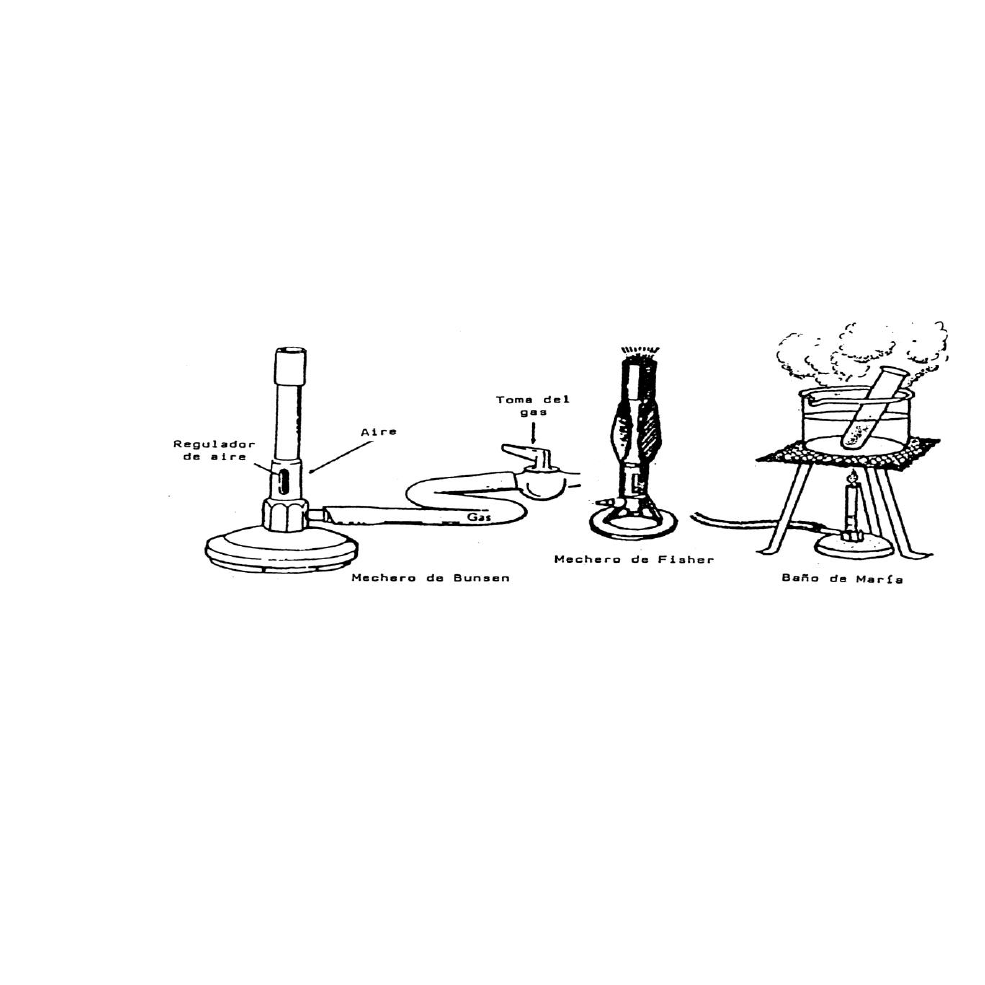
Se utilizan diversos tipos de mecheros a gas natural. El más empleado es
el mechero de Bunsen (Fig. 6). La mezcla de gas con aire en distintas
proporciones, permite modificar las características de la llama y su capacidad
calórica. Un mechero de gas puede ser reemplazado por el mechero de alcohol,
dependiendo de la finalidad de su uso.
Figura 6
Debemos remarcar que cuando se calefaccionan sustancias inflamables no
se debe usar calefacción con llama, sea ésta de mecheros a gas o de alcohol.
El baño de María es habitualmente utilizado en el laboratorio para calentar
sustancias, pues permite obtener una temperatura constante (el punto de
ebullición del agua=100C) y es de fácil implementación (Fig. 6).
La electricidad se utiliza con frecuencia en los calentadores eléctricos
comunes o con resistencias aisladas (denominado manto térmico). En algunos
casos se utilizan lámparas eléctricas especiales (infrarrojas) cuya radiación se
dirige al material a calefaccionar.
Es común también utilizar como fuente de calefacción estufas y hornos,
dotadas de termostatos que permiten obtener temperaturas constantes. Las estufas
se usan para secar diversos materiales, por Ej. a 100-110 C.
Los hornos eléctricos o muflas permiten alcanzar temperaturas mucho
más elevadas (600C o más). Estas se utilizan con el objetivo de calcinar
Este archivo fue descargado de https://filadd.com
FILADD.COM
6
materiales, para analizar a posteriori las cenizas obtenidas. La calcinación
consiste en someter el material en estudio, a altas temperaturas, el que se
introduce en cápsulas de porcelana o de platino. Las altas temperaturas en
ambiente oxigenado destruyen la sustancia orgánica de los materiales en estudio,
al tiempo que evapora el agua que los constituye, obteniendo finalmente sus
cenizas, es decir, la materia inorgánica.
Este procedimiento es muy utilizado en Odontología para determinar la
composición de la materia inorgánica del tejido óseo y de los tejidos dentarios.
4.- Elementos para sostener
Aquí podemos citar varios elementos útiles de empleo frecuente en el
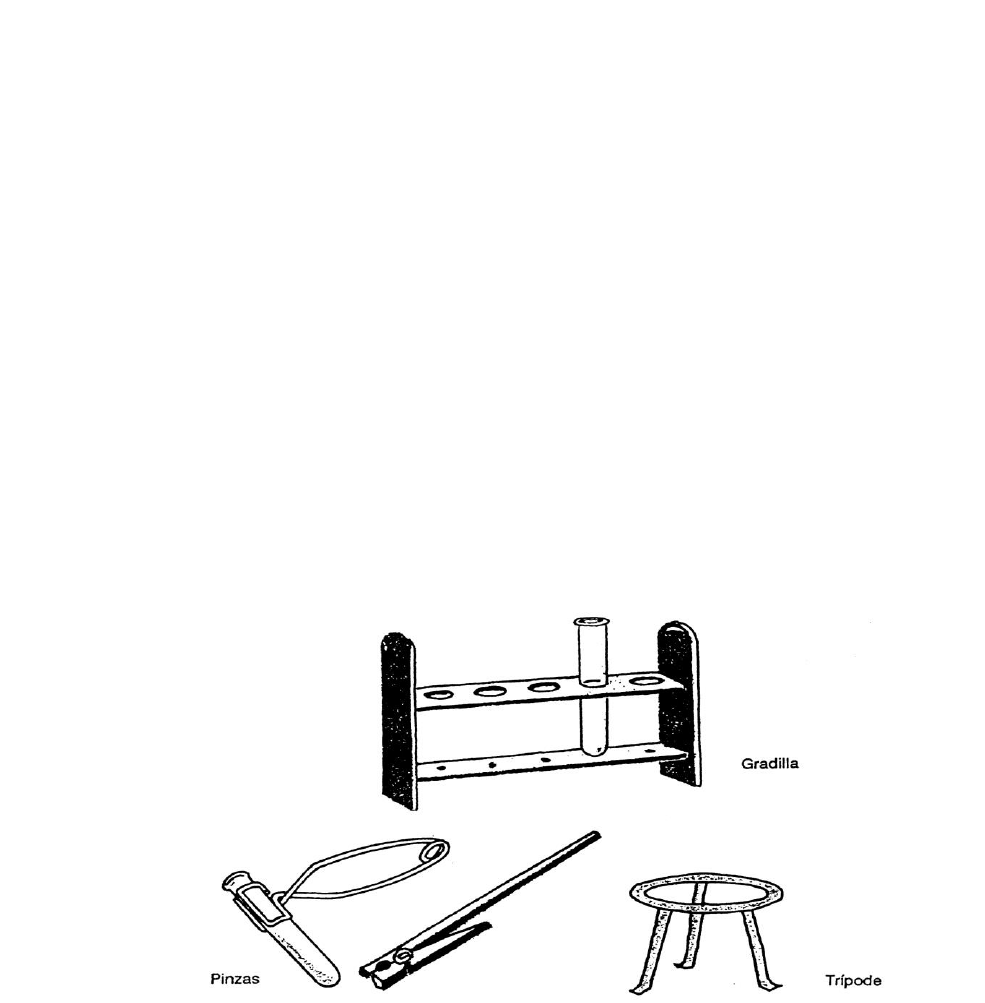
laboratorio (Fig. 7):
Gradillas, para sostener tubos de ensayo, se obtienen de variados materiales
como madera, aluminio, acero inoxidable y plástico.
Pinzas para sostener tubos de ensayos, pueden ser de madera o metálicas.
Trípode, en general de metal (hierro), se utiliza para sostener y proteger (cuando
se acompaña de una tela de amianto) a recipientes de vidrio térmico sometidos a
la acción del calor.
Soporte universal, de hierro (Fig. 3), usado para sostener buretas, agarraderas
para balón, refrigerantes, aro metálicos para embudos, etc.
Figura 7
5. Instrumentos para pesar.
Este archivo fue descargado de https://filadd.com
FILADD.COM
7
Para "pesar" una sustancia es usual emplear las balanzas, instrumentos
destinados a medir masas y no pesos.
En general, la balanza es un instrumento que determina el valor de una masa
desconocida por comparación con patrones de masa conocida, denominados
pesas.
m
d
(masa desconocida) = m
p
(masa conocida)
Recordando que p= m.g ; (p = peso y g= aceleración de gravedad)
En la balanza, la masa desconocida está sujeta a igual aceleración de
gravedad (g) que los patrones de masa conocida con los que se compara, en
consecuencia:
Como el valor de g es el mismo
p
d
= p
p
Por lo tanto, también es válido decir que la balanza determina el peso de un
cuerpo.
Los distintos tipos de balanzas se diferencian por su mecánica, por la
máxima y mínima cantidad de materia (masa) que son capaces de medir, por la
precisión, por la practicidad en el manejo y por su sensibilidad (masa mínima que
puede detectar).
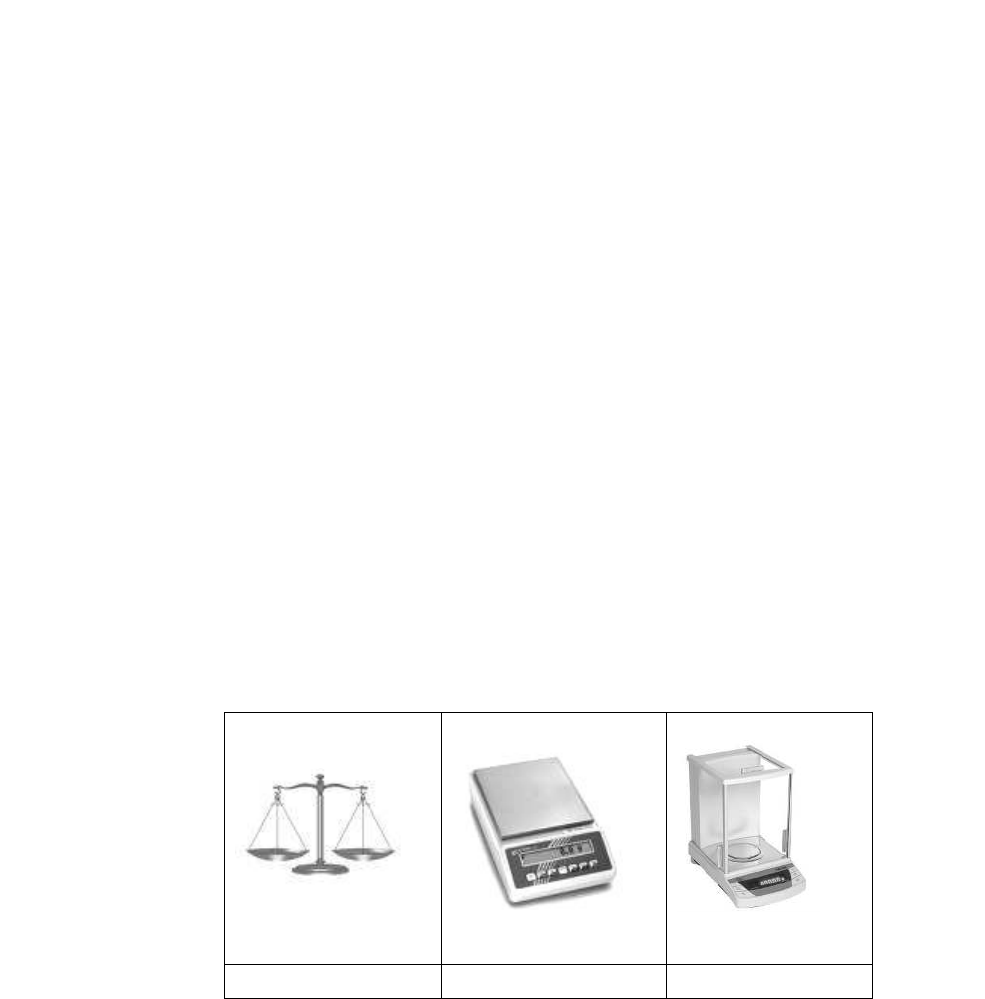
Las granatarias son fáciles de usar y muy útiles cuando no se requiere una
medición exacta; su sensibilidad está en el orden de 10 mg. Las analíticas pueden
detectar 0,1 mg y las más modernas detectan masas aún más pequeñas. La
de dos platillos
granataria
analítica
Este archivo fue descargado de https://filadd.com
FILADD.COM

8
balanza analítica debe ser cuidadosamente tratada y no estar expuesta a corrientes
de aire, radiaciones o vapores.
Las pesadas pueden hacerse de dos maneras:
- pesada directa
- por diferencia
6.- Otros elementos de laboratorio
Se emplean otros elementos para realizar operaciones de laboratorio, los
que se mencionarán a continuación:
Embudo de vidrio o material plástico, de diferentes tamaños. Se puede utilizar
para transvasar líquidos y también, cuando está provisto de un papel de filtro,
para separar una fase sólida de otra líquida por filtración.
Mortero con pilón. Se usa para triturar o moler sólidos. Pueden ser de
porcelana, ágata, hierro, etc. (Fig. 9).
Embudo separador o ampolla de decantación, sirve para separar mezclas de
líquidos no miscibles (Fig. 5).
Embudo de Buchner (placa filtrante). Sirve para filtrar al vacío (Fig. 5).
Termómetro. Para determinar temperaturas en trabajos de laboratorio. El
líquido habitualmente usado es el mercurio, el que por acción del calor se dilata.
Varilla de vidrio, empleada como agitador o para verter líquidos,
empleándosela para dirigir el chorro cuando se realiza un transvasamiento del
líquido.
RECOMENDACIONES PARA TRABAJAR EN UN LABORATORIO
Es sumamente importante antes de ingresar a un laboratorio conocer el
peligro que trae aparejado el manejo inadecuado, tanto de las sustancias
químicas, como del equipamiento e instrumental del laboratorio.
Son condiciones irrenunciables adquirir buenos hábitos de trabajo en los
que prime la seguridad (tanto personal como colectiva), el orden y la limpieza.
Normas de Seguridad en un Laboratorio de Química referidas a:
a) Infraestructura
b) Cuidados personales
Este archivo fue descargado de https://filadd.com
FILADD.COM

9
c) Sustancias Químicas
d) Uso de equipamiento
e) Aplicación de Técnicas
Aquí sólo se mencionarán algunas de ellas que se consideran sumamente
importantes, y que por ende no se pueden desconocer.
En cuanto a la infraestructura es conveniente tener presente que un laboratorio
debe ser un lugar con buena ventilación, la suficiente como para evitar la
acumulación de vapores tóxicos. Es deseable que disponga de dos puertas, de
modo que faciliten una rápida evacuación del mismo en caso de ser necesario.
Además es importante disponer de una buena iluminación natural.
Mantener el lugar de trabajo siempre limpio y seco, sin derrame de líquidos.
Los tapones de los frascos de los reactivos deben depositarse boca arriba sobre la
mesada y deben cerrarse inmediatamente después de su uso, cuidando que sea
con el mismo tapón. Todo frasco que se almacene debe estar perfectamente
etiquetado o rotulado a fin de que toda persona pueda conocer qué sustancia
contiene y su concentración (si corresponde).
Manipulación de sustancias químicas
Toda persona que vaya a hacer uso de reactivos químicos debe conocer los
íconos que identifican las sustancias peligrosas. Un apartado especial lo
constituye la manipulación de sustancias químicas, para lo cual se debe prestar
especial atención a las especificaciones indicadas en el frasco, a fin de conocer
los riesgos que puedan existir.
ÍCONOS DE IDENTIFICACIÓN
CARACTERÍSTICAS
Las sustancias que tienen este ícono son
muy peligrosas, provocan lesiones graves o
incluso la muerte, ya sea por contacto con
la piel, inhalación o por ingestión.
Este archivo fue descargado de https://filadd.com
FILADD.COM

10
Se debe tener la precaución de no respirar
los vapores y evitar el contacto con la piel,
ojos y ropas, ya que estos productos
destruyen tejidos vivos y algunos materiales
Se debe evitar el contacto con la piel y los
ojos y el aspirar sus vapores.
Se debe evitar el contacto con otras
sustancias, en especial con sustancias
inflamables ya que producen una reacción
fuertemente exotérmica.
INFLAMABLE
Estas sustancias líquidas en contacto con
agua o con aire húmedo desprenden gases
extremadamente inflamables en cantidades
peligrosas debido a que arden a
temperaturas muy bajas.
Se deben manipular con suma precaución,
evitando los choques, la fricción, las chispas
y desde luego el fuego debido al peligro de
explosión.
Recordar
Este archivo fue descargado de https://filadd.com
FILADD.COM

11
SUSTANCIA PELIGROSA + ERROR HUMANO = ACCIDENTE
OPERACIONES ELEMENTALES DE LABORATORIO
Pulverización: mediante esta operación se reduce la sustancia a partículas muy
pequeñas con lo cual se aumenta la superficie de contacto con el medio,
facilitándose su disolución o aumentando la capacidad de reacción de la misma.
Esta operación se realiza triturando la sustancia en un mortero de material
apropiado (vidrio, piedra, porcelana, ágata) que debe ser más duro que la
sustancia a pulverizar; utilizando como instrumento de división el pilón o mano
del mortero.
Figura 9: Mortero
Disolución: es la dispersión de una sustancia (soluto) en el seno de otra
sustancia en mayor volumen o cantidad (solvente); se forma un sistema
homogéneo, cuyas partículas son inseparables por métodos físicos o mecánicos
comunes (filtración, decantación, centrifugación) e imposibles de diferenciar por
los aparatos de óptica (microscopio y ultramicroscopio). Cuando el soluto es
sólido suele ser conveniente pulverizarlo para ofrecer una mayor superficie de
contacto con el solvente, favoreciendo así su disolución.
El agua es uno de los solventes más frecuentemente utilizados. Hay solutos
como el NaCl (sal de mesa) que se disuelve fácil y rápidamente en agua. Otros,
por ejemplo: K
2
Cr
2
O
7
son de difícil disolución, en este caso se facilita la opera-
ción agitando la mezcla soluto-solvente para aumentar el contacto entre las
moléculas.
Este archivo fue descargado de https://filadd.com
FILADD.COM

12
En el caso de algunos solutos sólidos, como el CuSO
4
. 5H
2
O (sulfato de
cobre pentahidratado), es necesario calentar la mezcla para aumentar la energía
cinética de las moléculas, disminuir la fuerza de atracción entre las partículas del
sólido y, en consecuencia, favorecer la disolución.
MÉTODOS UTILIZADOS PARA LA SEPARACIÓN DE LOS
COMPONENTES DE UNA MEZCLA
Con el objetivo de conocer la composición de una mezcla o simplemente
ante la necesidad de aislar uno o todos sus componentes, se utilizan distintos
métodos de aislamiento o separación. Así, de la leche se separa primero la
crema con la cual se fabrica la manteca y del resto que queda, puede separarse la
caseína, otras proteínas, la lactosa, sus sales, etc.
Los métodos de separación varían según las características de los
componentes de la mezcla, y pueden clasificarse en:
A) Métodos físicos de separación de sistemas heterogéneos
1- Tamización: cuando una mezcla sólida está formada por componentes
pulverizados, cuyas partículas se diferencian por su tamaño, se la hace pasar a
través de mallas de hilos de seda, de metal u otros materiales, denominados
tamices, cernidores, cedazos o cribas.
Los tamices se diferencian por el tamaño de los poros y se eligen de poros
adecuados para dejar pasar el polvo más fino y retener el más grueso. Este
procedimiento se utiliza para separar las harinas del salvado o afrecho, por
ejemplo en la industria molinera.
2- Centrifugación: cuando la sedimentación o la decantación es muy lenta,
puede acelerarse por acción de la fuerza centrífuga. El aparato en el que se realiza
esta operación se denomina centrífuga. Consta de rotor con porta-tubos en los
que se ubican tubos adecuados con la mezcla a separar, mediante un motor de
velocidad regulable, se hace girar el rotor o cabezal a velocidad que varía desde
varios centenares hasta algunos miles de revoluciones por minuto. La fuerza
centrífuga generada por la rotación aumenta la velocidad de sedimentación de las
partículas más pesadas, quedando superpuesto el componente más liviano. La
separación se cumple en un tiempo mucho más corto que el que se logra dejando
sedimentar las partículas por simple acción de la gravedad (decantación).
Este archivo fue descargado de https://filadd.com
FILADD.COM

13
3- Decantación: consiste en dejar en reposo durante un lapso de tiempo las
mezclas heterogéneas formadas por componentes sólidos y líquidos o líquidos
inmiscibles entre sí, para que la acción de la gravedad los separe. El componente
más pesado o más denso se deposita en el fondo del recipiente (sedimentación).
Se utilizan, para ello, vasos de precipitación o beaker o ampollas de decantación.
4- Filtración: en esta operación se separan las partículas en suspensión
existentes en un líquido o gas, pasando la mezcla a través de un material poroso.
Se emplea el papel de filtro o las placas filtrantes de poros de diferente diámetro.
La elección de estos elementos depende del tamaño de las partículas a retener, de
las propiedades del líquido o gas y de la velocidad con que se requiera hacer la
filtración.
Cuando el papel es atacado por el líquido a filtrar, se lo puede sustituir por
algodón o lana de vidrio.
Si se desea acelerar la filtración se pueden utilizar:
Filtración al vacío: se disminuye la presión en el recipiente que está debajo del
filtro.
5- Diálisis: la presencia de sustancias en solución coloidal conjuntamente con
otras en solución verdadera en el mismo medio, es frecuente en los sistemas
biológicos. En muchas ocasiones es necesario separar las sustancias que están en
solución. Para lograrlo se utilizan membranas semipermeables (de celofán o de
otros materiales naturales: vejiga de cerdo) que se caracterizan por no permitir el
pasaje de macromoléculas y sí permiten el paso de las moléculas de agua o del
solvente del medio y de partículas pequeñas de bajo peso molecular cuyo
diámetro es menor al diámetro del poro de la membrana (Fig. 13), movimiento
que se realizará a favor del gradiente de concentración, es decir de la más
concentrada a la menos concentrada.
Este archivo fue descargado de https://filadd.com
FILADD.COM

14
Membrana semipermeable
DIÀLISIS
Figura 13
Cuando el riñón es incapaz de llevar a cabo la filtración glomerular se
recurre a diálisis (hemodiálisis)
En el plasma sanguíneo se encuentran macromoléculas en solución coloidal
(las proteínas plasmáticas) que pueden ser separadas de moléculas de bajo peso
molecular (iones inorgánicos, urea, glucosa) que se encuentran en solución en ese
medio biológico mediante este procedimiento.
Cuando no se posee dializador, se puede colocar el material a dializar en
simples bolsas de celofán perfectamente cerradas que se suspenden en el líquido
de lavado, renovando el mismo repetidas veces.
6- Fusión: Se utiliza para separar mezclas de sólidos con puntos de fusión muy
diferentes. Al administrar calor, el componente de menor punto de fusión, se
torna líquido. Este se separa del resto y al enfriarse, cristaliza. Es utilizada
también para purificar sólidos.
B) Métodos físicos de fraccionamiento de sistemas homogéneos
1- Cristalización: es la operación que consiste en obtener una sustancia al estado
cristalino a partir de su solución. Se la utiliza no sólo para separar sustancias de
una mezcla, sino también para purificarlas y en muchos casos para identificarlas,
ya que al estado cristalino las distintas sustancias adquieren formas de cuerpos
geométricos perfectamente identificables unos de otros, al microscopio.
La cristalización puede ser:
a) por vía húmeda (a partir de soluciones sobresaturadas).
b) por vía seca: sublimación.
a) Cristalización por vía húmeda: Al calentar una solución de un sólido en un
líquido, se provoca la evaporación parcial del solvente y la solución queda
sobresaturada. Al enfriarse, se separa por precipitación el sólido en forma
cristalina. La cristalización suele emplearse como excelente método de
purificación de sustancias, eliminándose impurezas volátiles y solubles en el
solvente usado. La sustancia a purificar se disuelve y cristaliza varias veces
(recristalización) para lograr mayor grado de pureza.
Este archivo fue descargado de https://filadd.com
FILADD.COM

15
b) Cristalización por vía seca: se puede aplicar este procedimiento para
separación de mezclas que contengan un componente capaz de sublimar. Por
efecto del calentamiento se producen los vapores de esta sustancia (sublima) que
al contactarse con una superficie fría, cristaliza. También se utiliza para
purificar sustancias que subliman.
2- Destilación: se utiliza para separar soluciones de sólido en líquido. Mediante el
calentamiento se alcanza el punto de ebullición del líquido, los vapores pasan al
refrigerante donde se condensan al ser enfriados por una corriente de agua fría y
finalmente el líquido ya destilado, se recoge en un recipiente adecuado.
También se usa para separar soluciones de líquido en líquido aprovechando
los diferentes puntos de ebullición.
-Destilación simple: cuando el soluto es un sólido soluble en el solvente líquido,
se logra la separación destilando el solvente. Por este método se destila el agua
corriente para obtener el agua pura o destilada (destilación simple) con la que se
preparan los reactivos de laboratorio, colutorios de uso odontológico, jarabes, etc.
-Destilación fraccionada: cuando la solución está formada por líquidos de
distintos puntos de ebullición, éstos se podrán separar porque destilarán a medida
que se alcanza la temperatura correspondiente a sus respectivos puntos de
ebullición. Ejemplo: mezcla de agua (P.Eb. 100C) y alcohol etílico (P.Eb.
78C). En este caso destila primero el alcohol porque comienza su ebullición a
menor temperatura. De este modo también se destila el aire líquido para obtener
oxígeno, CO
2
, nitrógeno, gases nobles.
C) Métodos Químicos de separación
Se basan en reacciones químicas en las cuales se originan sustancias que, por su
naturaleza, pueden separarse aplicando los métodos físicos (ejemplo: precipitación).
Precipitación: procedimiento químico que consiste en insolubilizar una
sustancia tratándola con un reactivo adecuado. Mediante reacciones de
sustitución simple o doble, podemos obtener un compuesto insoluble.
Por ejemplo los iones Cl
-
presentes en un líquido biológico pueden ser
precipitados con Ag
+
contenidos en una solución de AgNO
3
.
Cl
-
+ AgNO
3
AgCl + NO
-
3
Por simple decantación o centrifugación se puede separar el precipitado formado.
Este archivo fue descargado de https://filadd.com
FILADD.COM
Este documento contiene más páginas...
Descargar Completo
Material de laboratorio - Operaciones elementales.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.