ALQUENOS
Los alquenos son hidrocarburos que contienen enlaces dobles carbono-carbono. Se emplea
frecuentemente la palabra olefina como sinónimo.
Los alquenos abundan en la naturaleza. El eteno, es un compuesto que controla el crecimiento de
las plantas, la germinación de las semillas y la maduración de los frutos.
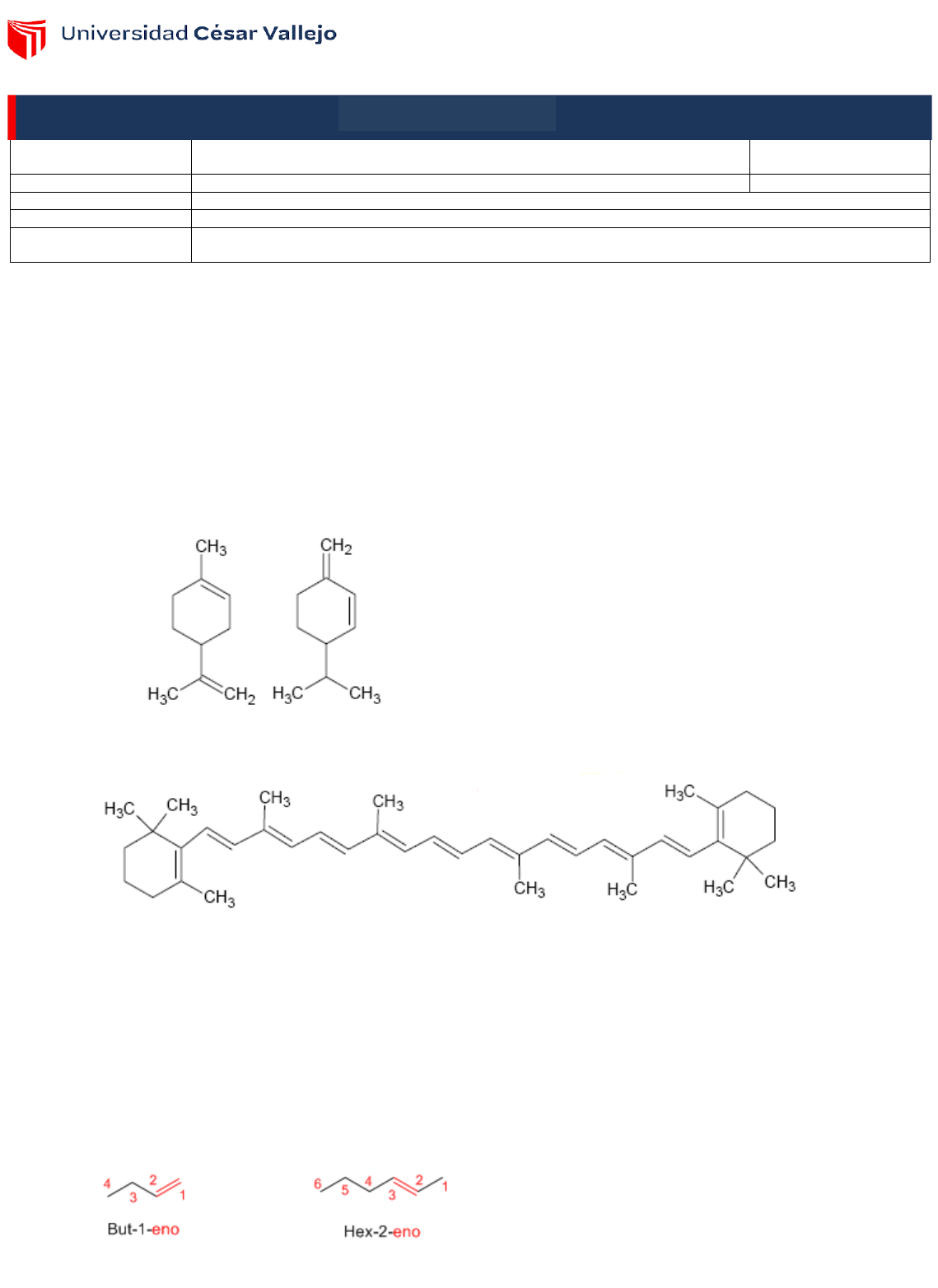
El α−Pineno es una fragancia obtenida a partir de los pinos. β-Caroteno es un compuesto que
contiene 11 dobles enlaces y es precursor de la vitamina A.
Nomenclatura de Alquenos
Los alquenos se nombran reemplazando la terminación -ano del correspondiente alcano por -
eno. Los alquenos más simples son el eteno y el propeno, también llamados etileno y propileno a
nivel industrial.
Regla 1.- Se elige como cadena principal la de mayor longitud que contenga el doble enlace. La
numeración comienza en el extremo que otorga al doble enlace el menor localizador.
Programa de
Estudios/Programa
MEDICINA
Sesión N° 8
Experiencia Curricular:
QUÍMICA
Semestre 2022
Contenido temático:
ALQUENOS, ALQUINOS Y AROMÁTICOS
Docente:
EQUIPO DOCENTE
Tipo de Material
Informativo
LECTURA
MATERIAL
INFORMATIVO
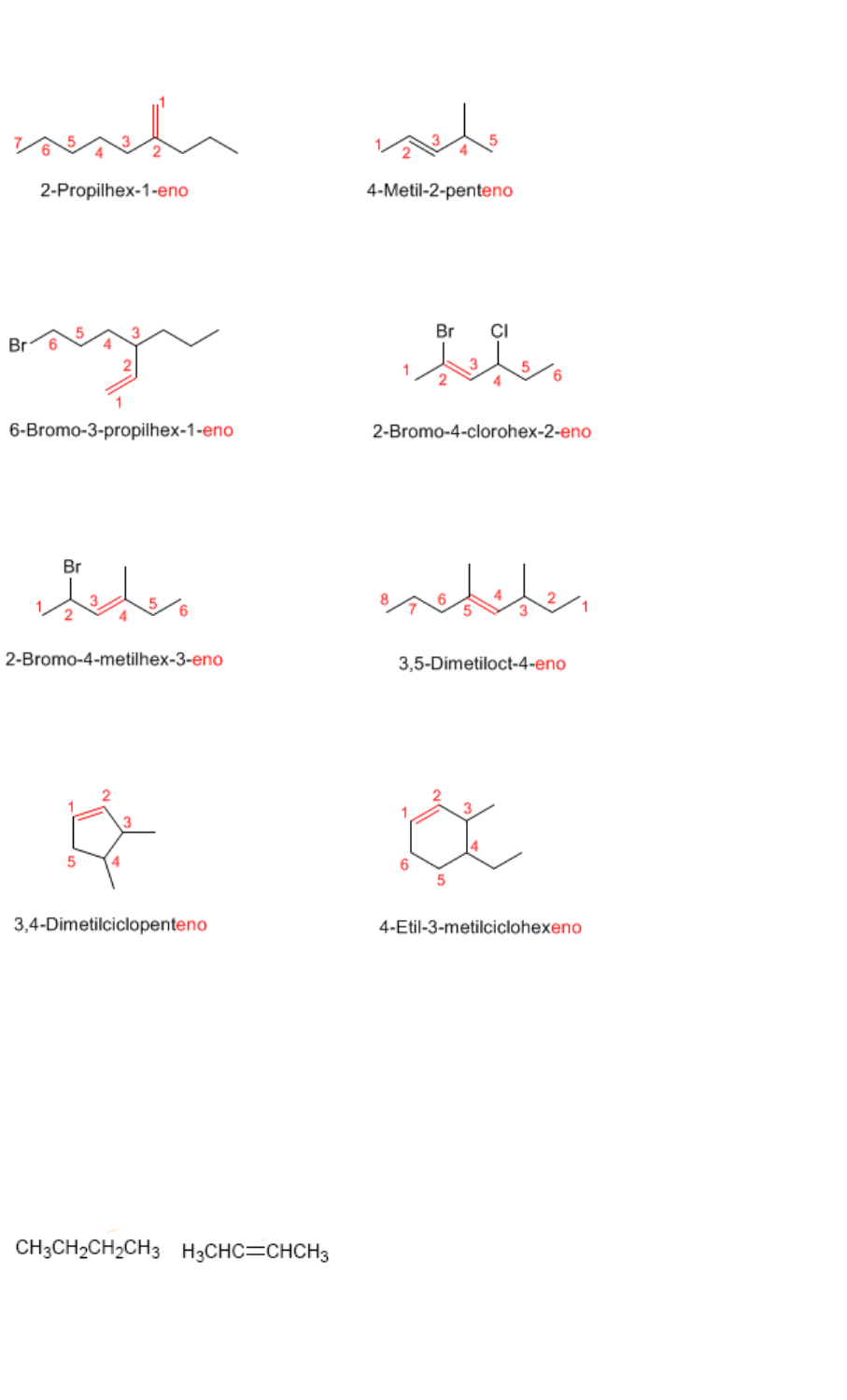
Regla 2.- El nombre de los sustituyentes precede al de la cadena principal y se acompaña de un
localizador que indica su posición en la molécula. La molécula se numera de modo que el doble
enlace tome el localizador más bajo.
Regla 3.- Cuando hay varios sustituyentes se ordenan alfabéticamente y se acompañan de sus
respectivos localizadores
Regla 4.- Cuando el doble enlace está a la misma distancia de ambos extremos, se numera para que
los sustituyentes tomen los menores localizadores.
Regla 5.- En compuestos cíclicos resulta innecesario indicar la posición del doble enlace, puesto
que siempre se encuentra entre las posiciones 1 y 2.
Grado de insaturación
Cada anillo o ciclo de una molécula implica la pérdida de dos hidrógenos respecto a un alcano de
fórmula C
n
H
2n+2
. Se denomina grado de insaturación al número de ciclos y dobles enlaces presentes
en una molécula.
Debido a que los alcanos contienen el máximo número posible de enlaces carbono-hidrógeno, se
dice de ellos que son hidrocarburos saturados. Alquenos y compuestos cíclicos son hidrocarburos
insaturados.
El número total de enlaces π y ciclos en una molécula se denomina grado de insaturación.
Grado de insaturación en compuestos que contienen halógenos, oxígenos y nitrógenos:
Halógenos: Sumar el número de halógenos al número de hidrógenos.
Oxígenos: Ignorar los oxígenos.
Nitrógenos: Restar el número de nitrógenos del número de hidrógenos.
Ejemplo 1: Calcular el grado de insaturación en las siguientes fórmulas:
a) C
4
H
8
Solución: Un alcano saturado de 4 carbonos tiene de fórmula C
4
H
10
. El compuesto tiene un par de
hidrógenos menos, así que, su grado de insaturación es uno.
b) C
9
H
16
Br
2
Solución: Sumamos los halógenos a los hidrógenos obteniéndose la fórmula C
9
H
18
. Un alcano
saturado de 9 carbonos tiene de fórmula C
9
H
20
. El compuesto tiene una insaturación.
Propiedades físicas de Alquenos
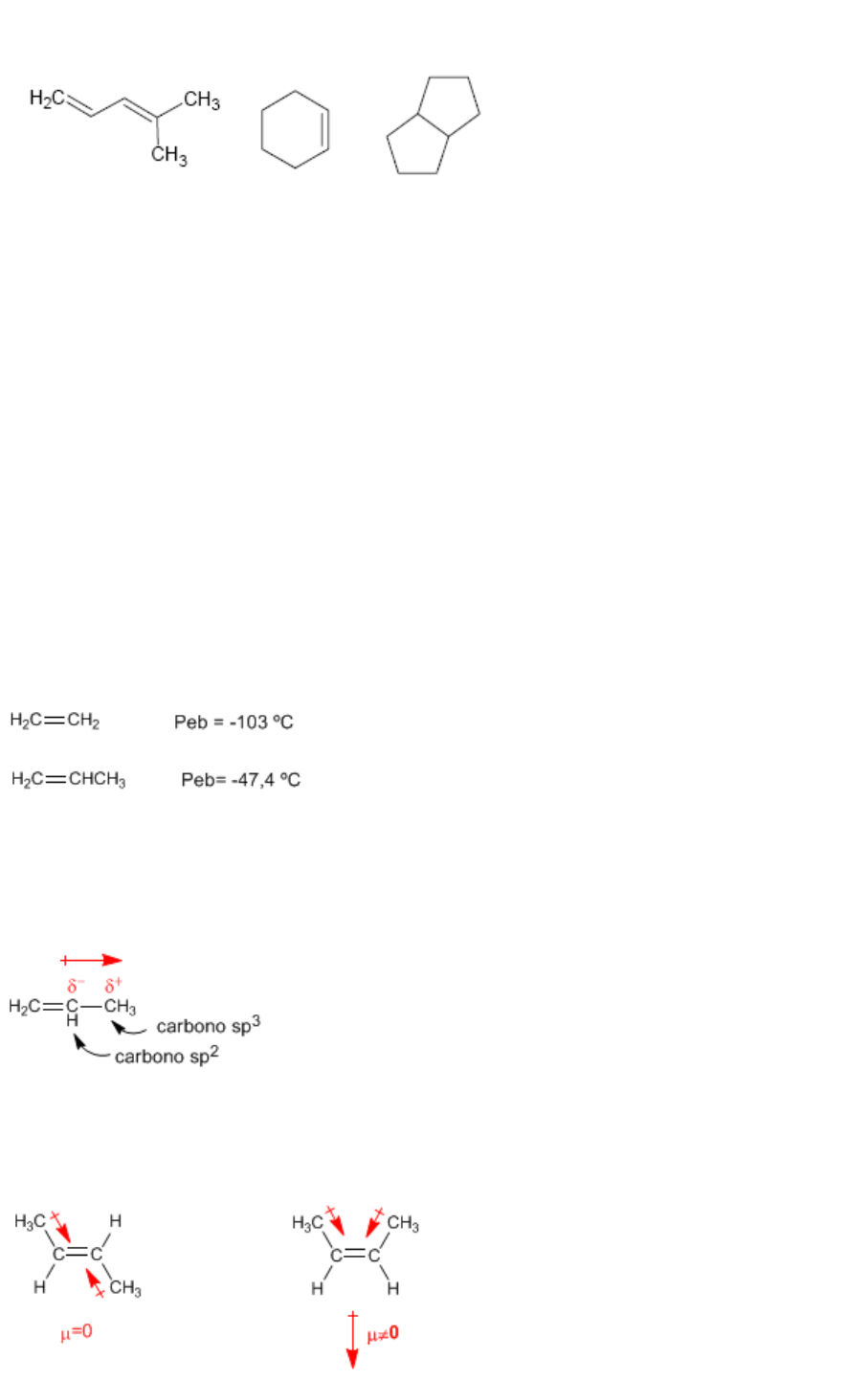
Los alquenos presentan puntos de fusión y ebullición próximos a los alcanos correspondientes.
Momento dipolar en alquenos.
El carbono sp
2
tiene más carácter s que el carbono sp
3
, los electrones en el orbital s están más
próximos al núcleo y son atraídos fuertemente por éste, de modo que un carbono sp
2
tiene tendencia
a atraer hacia si electrones, lo que genera momentos dipolares.
En alquenos trans los momentos dipolares se restan, llegando a anularse en el caso de que ambos
carbonos tengan cadenas iguales. En los alquenos cis los momentos dipolares se suman dando
lugar a un momento dipolar total distinto de cero (molécula polar)
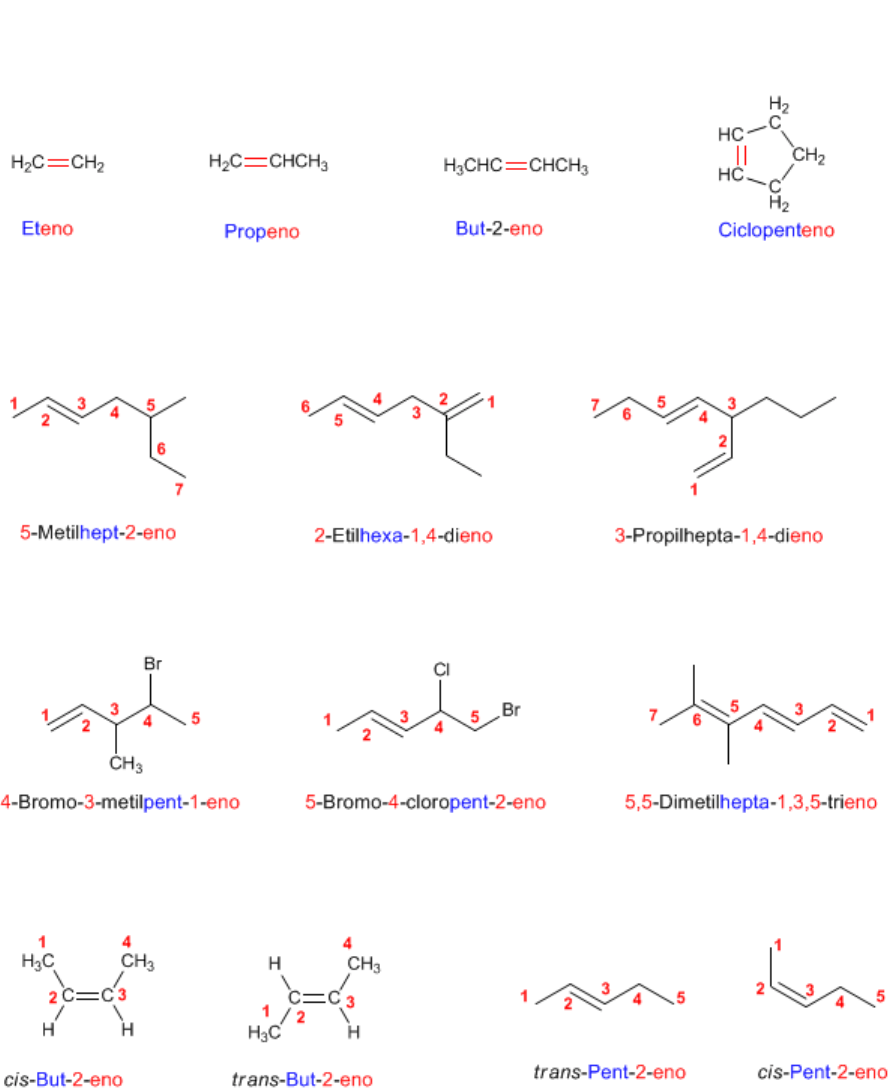
Nomenclatura de Alquenos - Reglas IUPAC
Regla 1. Los alquenos son hidrocarburos que responden a la fórmula C
n
H
2n
. Se nombran
utilizando el mismo prefijo que para los alcanos (met-, et-, prop-, but-....) pero cambiando el
sufijo -ano por -eno.
Regla 2. Se toma como cadena principal la más larga que contenga el doble enlace. En caso de
tener varios dobles enlaces se toma como cadena principal la que contiene el mayor número de
dobles enlaces (aunque no sea la más larga)
Regla 3. La numeración comienza por el extremo de la cadena que otorga al doble enlace el
localizador más bajo posible. Los dobles enlaces tienen preferencia sobre los sustituyentes
Regla 4. Los alquenos pueden existir en forma de isómeros espaciales que se distinguen con la
notación cis/trans.
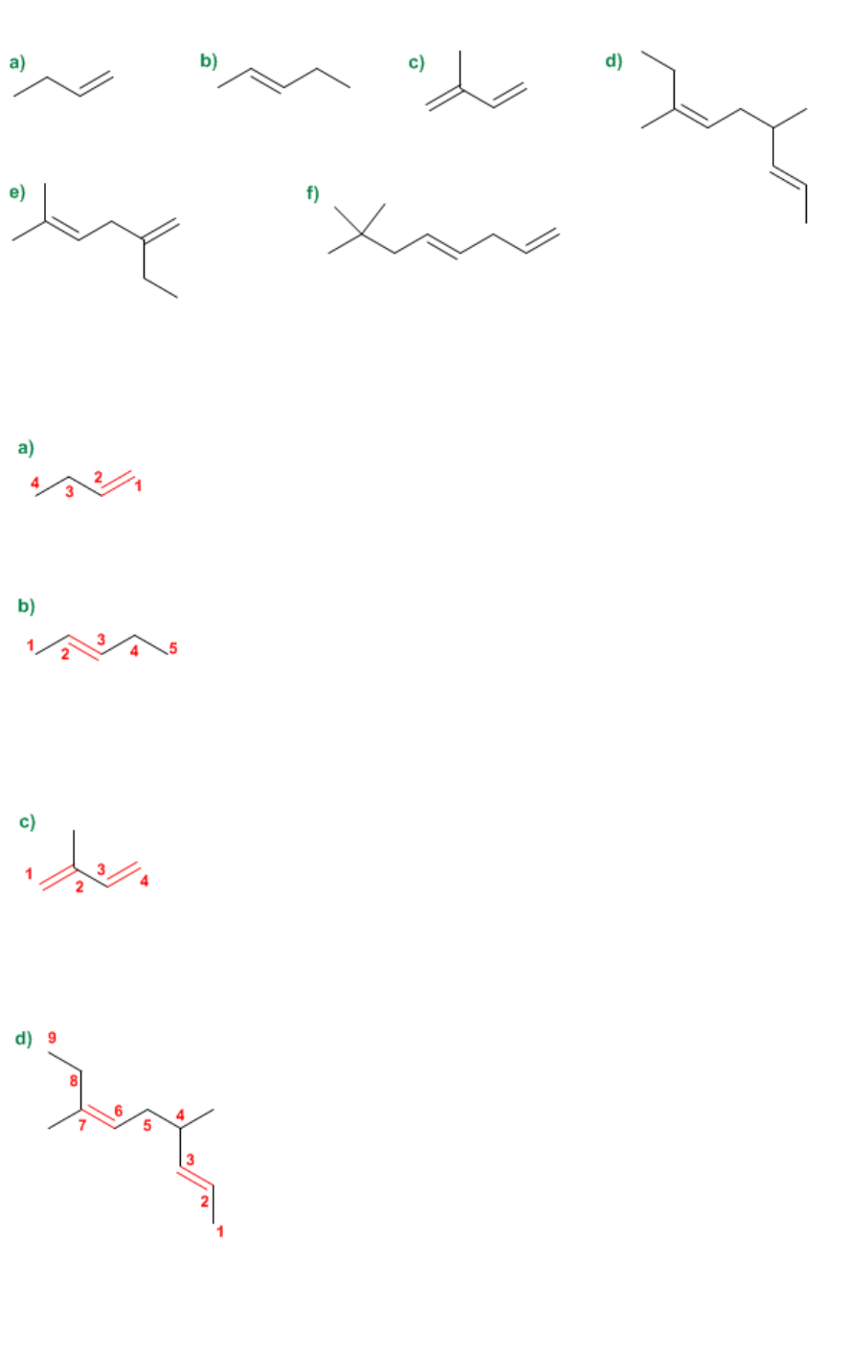
Problema 4.1
Nombrar los siguientes alquenos:
Solución
a)
1. Cadena principal: 4 carbonos con doble enlace (buteno)
2. Numeración: localizador más bajo al doble enlace.
3. Sustituyentes: no
4. Nombre: But-1-eno
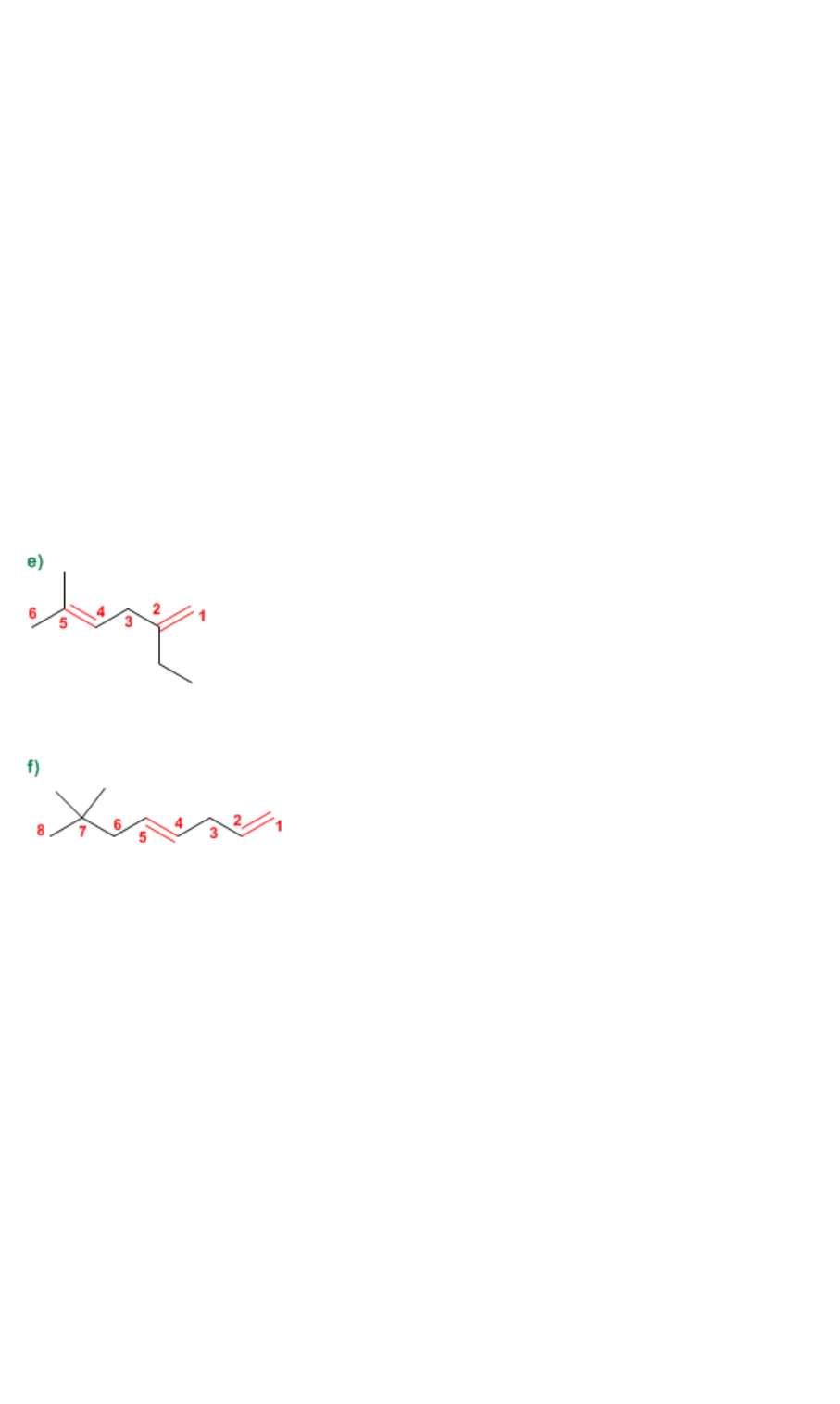
b)
1. Cadena principal: 5 carbonos con doble enlace (penteno)
2. Numeración: localizador más bajo al doble enlace.
3. Sustituyentes: no
4. Nombre: Pent-2-eno
c)
1. Cadena principal: 4 carbonos con dos dobles enlaces (butadieno)
2. Numeración: dobles enlaces a igual distancia de los extremos, numeramos para que el metilo
tome el menor localizador.
3. Sustituyentes: metilo en posición 2.
4. Nombre: 2-Metilbuta-1,3-dieno
d)
1. Cadena principal: 9 carbonos con dos dobles enlaces (nonadieno)
2. Numeración: localizador más bajo a los dobles enlaces (2,6).
3. Sustituyentes: metilos en posición 4,7.
4. Nombre: 4,7-Dimetilnona-2,6-dieno
Se elige como cadena principal la de mayor longitud, que contenga el mayor número de dobles
enlaces
e)
1. Cadena principal: 6 carbonos con dos dobles enlaces (hexadieno). Obsérvese que no es la más
larga.
2. Numeración: localizador más bajo a los dobles enlaces (1,4).
3. Sustituyentes: etilo en posición 2 y metilo en 5.
4. Nombre: 2-Etil-5-metilhexa-1,4-dieno
f)
1. Cadena principal: 8 carbonos con dos dobles enlaces (octadieno)
2. Numeración: localizador más bajo a los dobles enlaces (1,4).
3. Sustituyentes: metilos en posición 7,7.
4. Nombre: 7,7-Dimetilocta-1,4-dieno
Se numera la cadena principal para que los dobles enlaces tomen los menores localizadores
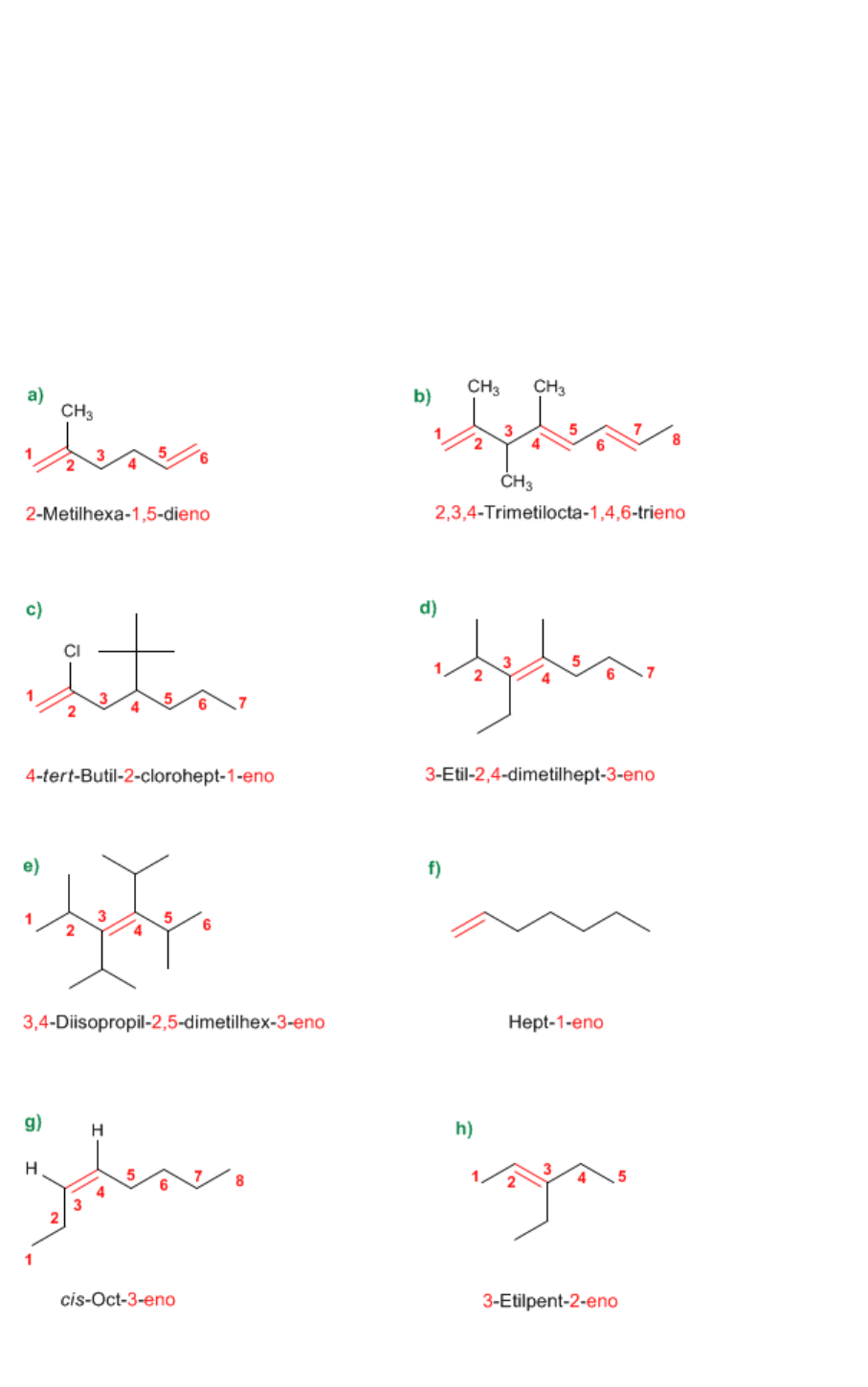
Problema 4.2
Dibuja las fórmulas de los siguientes compuestos:
a) 2-Metilhexa-1,5-dieno
b) 2,3,4-Trimetilocta-1,4,6-trieno
c) 4-tert-Butil-2-clorohept-1-eno
d) 3-Etil-2,4-dimetilhept-3-eno
e) 3,4-Diisopropil-2,5-dimetilhex-3-eno
f) Hept-1-eno
g) cis-Oct-3-eno
h) 3-Etilpent-2-eno
i) trans-1,4-Dibromobut-2-eno
j) 3-Clorohex-2-eno
k) Buta-1,3-dieno
l) Hexa-1,4-dieno
m) 5-Metil-3-propilocta-1,4,6-trieno
n) 6-Metil-6-propilnona-2,4,7-trieno
o) 2,3,5-Trimetilocta-1,4-dieno
p) 3-Propilhepta-1,5-dieno.
Solución
La notación cis, indica que los grupos iguales (hidrógenos) de las posiciones 3,4 van orientados
al mismo lado del alqueno.
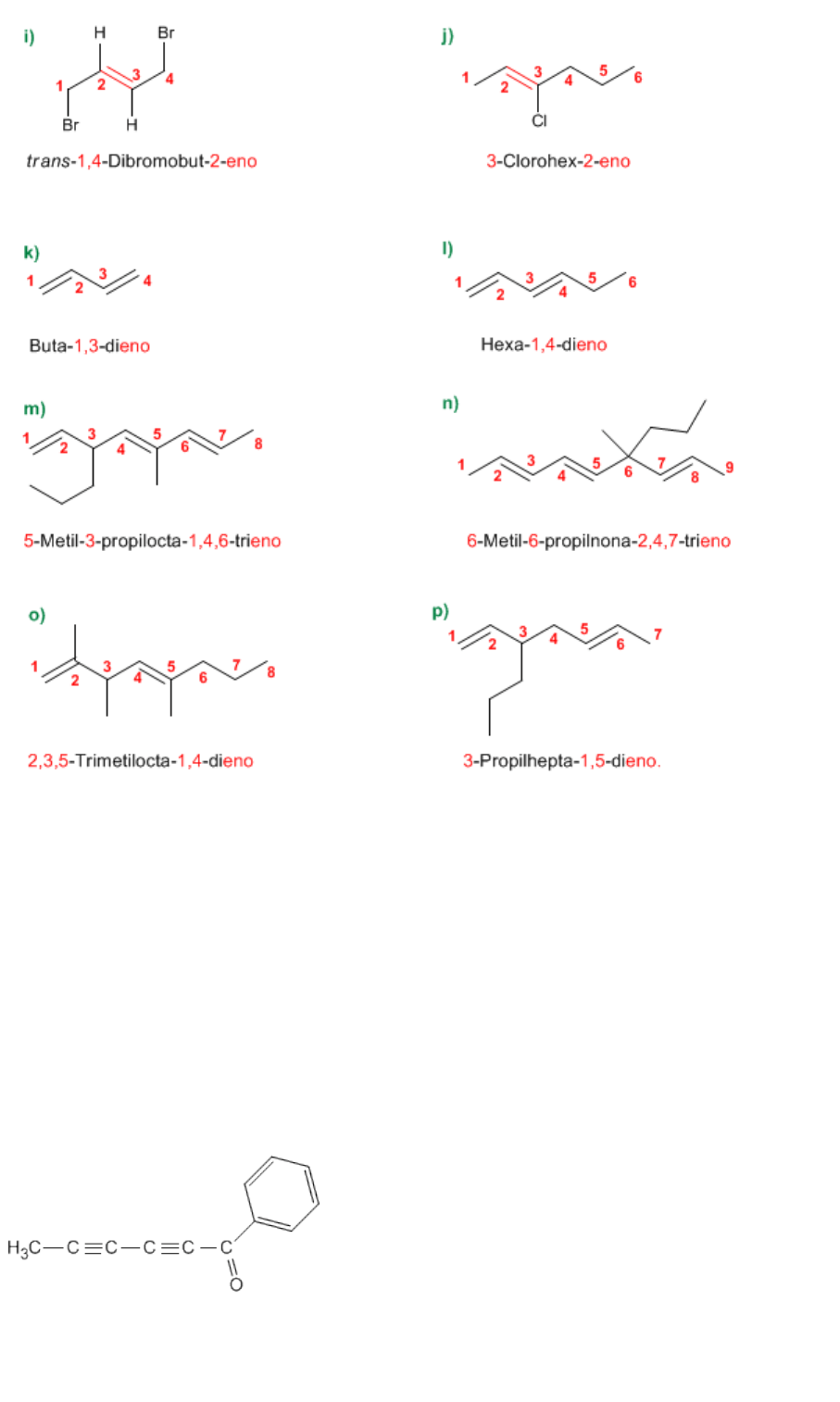
La notación trans, indica que los grupos iguales del doble enlace (hidrógenos) van orientados a
lados opuestos.
Alquinos
Los alquinos son hidrocarburos que contienen enlaces triples carbono-carbono. La fórmula molecular
general para alquinos acíclicos es C
n
H
2n-2
y su grado de insaturación es dos. El acetileno o etino es el
alquino más simple, fue descubierto por Berthelot en 1862.
El acetileno puede obtenerse a partir de óxido de calcio y coke. En una primera etapa son calentados
en horno eléctrico para formar carburo de calcio.
CaO+3C ------> CaC
2
+ CO
2
En la segunda etapa el carburo de calcio reacciona con agua para formar acetileno.
CaC
2
+ 2H
2
O ------>Ca(OH)
2
+ C
2
H
2
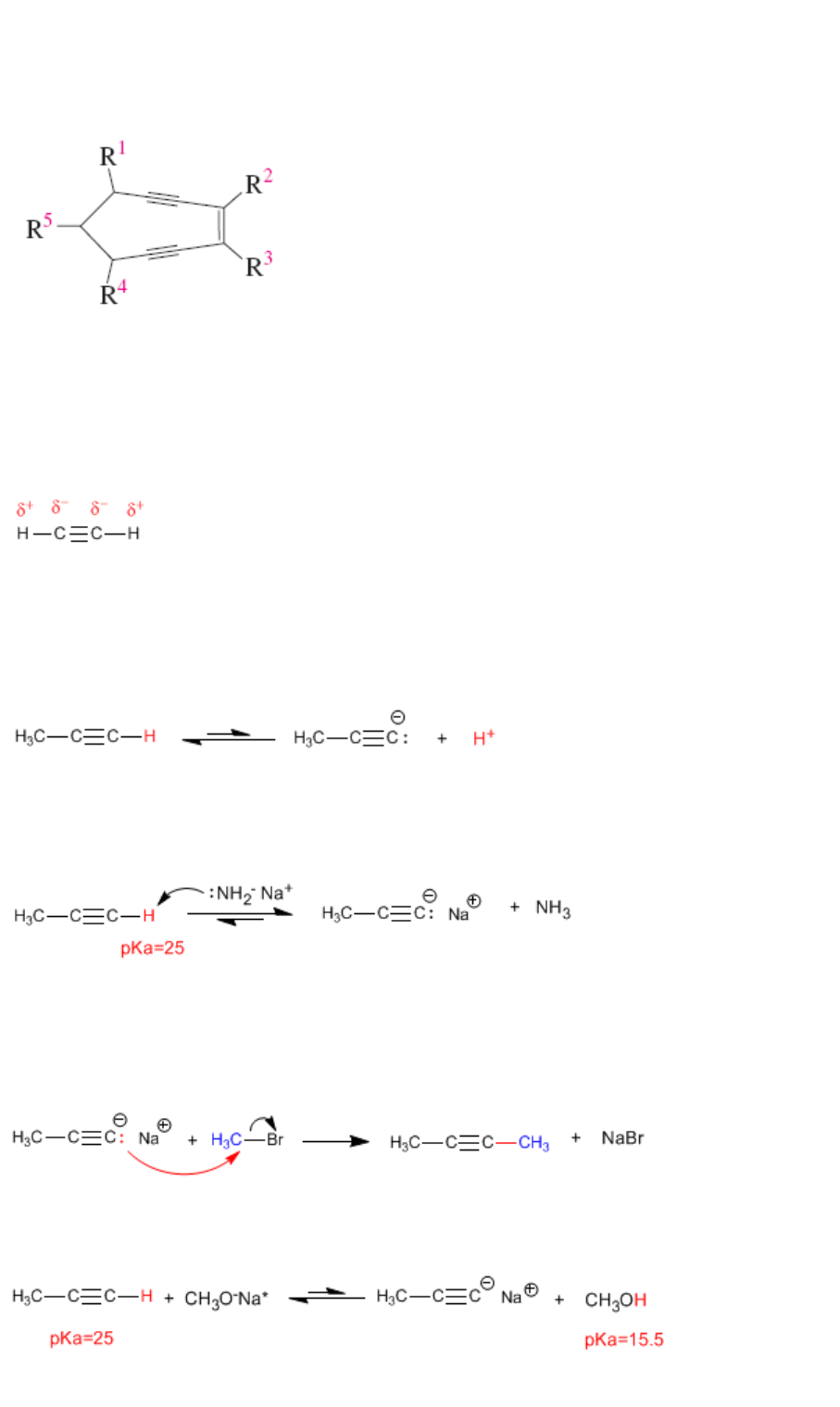
El acetileno fue usado en la industria para preparar acetaldehído, ácido acético, cloruro de vinilo y
polímeros acrílicos.
Existen numerosos ejemplos de productos naturales que contienen triples enlaces. Capillin, el cual
tiene actividad fungicida. Enodiinos, los cuales tienen propiedades anticancerígenas.
Propiedades físicas de Alquinos
Los alquinos tienen unas propiedades físicas similares a los alcanos y alquenos. Son poco solubles
en agua, tienen una baja densidad y presentan bajos puntos de ebullición. Sin embargo, los alquinos
son más polares debido a la mayor atracción que ejerce un carbono sp sobre los electrones,
comparado con un carbono sp
3
o sp
2
.
Acidez de Alquinos
El enlace carbono - hidrógeno de alquinos terminales está polarizado y muestra una ligera tendencia
a ionizarse.
El Hidrógeno del propino es débilmente ácido, con un pKa = 25. Utilizando bases fuertes (NaH,
LDA, NH
2
-
) se puede desprotonar, obteniéndose su base conjugada -propinil sodio- una especie muy
básica y nucleófila.
El propinil sodio generado en la reacción anterior puede actuar como nucleófilo atacando a
haloalcanos primarios mediante mecanismo SN2.
Las bases derivadas de alcoholes y agua son demasiado débiles para desprotonar los alquinos,
estando los equilibrios ácido-base muy desplazados a la izquierda.
Un equilibrio ácido-base se desplaza hacia el ácido conjugado de mayor valor de pKa.
Ejemplo: completar los siguientes equilbrios ácido-base
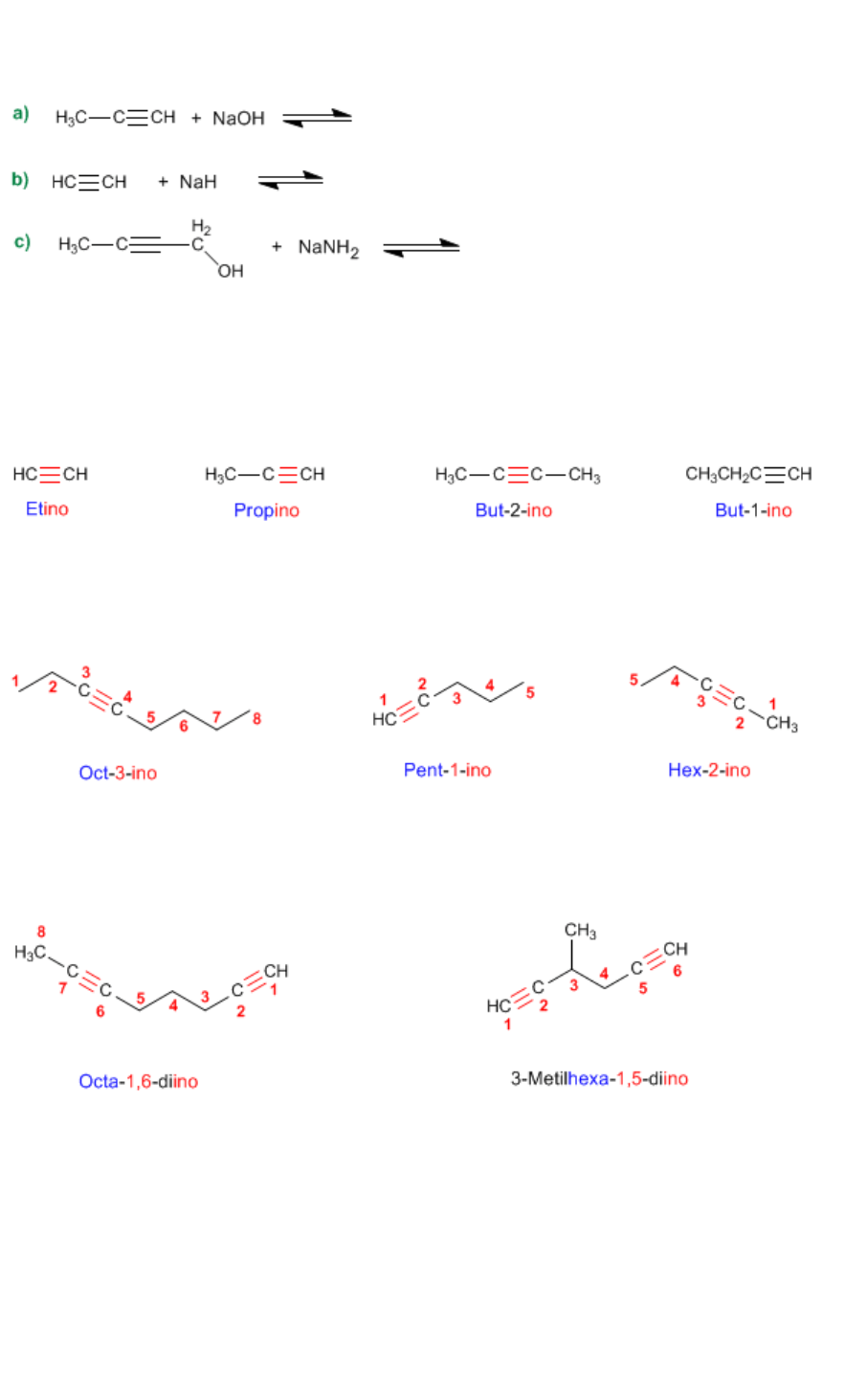
Nomenclatura de Alquinos
Regla 1. Los alquinos responden a la fórmula C
n
H
2n-2
y se nombran sustituyendo el sufijo -ano del
alca-no con igual número de carbonos por -ino.
Regla 2. Se elige como cadena principal la de mayor longitud que contiene el triple enlace. La
numera-ción debe otorgar los menores localizadores al triple enlace.
Regla 3. Cuando la molécula tiene más de un triple enlace, se toma como principal la cadena que
contie-ne el mayor número de enlaces triples y se numera desde el extremo más cercano a uno de
los enlaces múltiples, terminando el nombre en -diino, triino, etc.
Regla 4. Si el hidrocarburo contiene dobles y triples enlaces, se procede del modo siguiente:
1. Se toma como cadena principal la que contiene al mayor número posible de enlaces múltiples,
prescindiendo de si son dobles o triples.
2. Se numera para que los enlaces en conjunto tomen los localizadores más bajos. Si hay un doble
enlace y un triple a la misma distancia de los extremos tiene preferencia el doble.
3. Si el compuesto tiene un doble enlace y un triple se termina el nombre en -eno-ino; si tiene dos
dobles y un triple, -dieno-ino; con dos triples y un doble la terminación es, -eno-diino
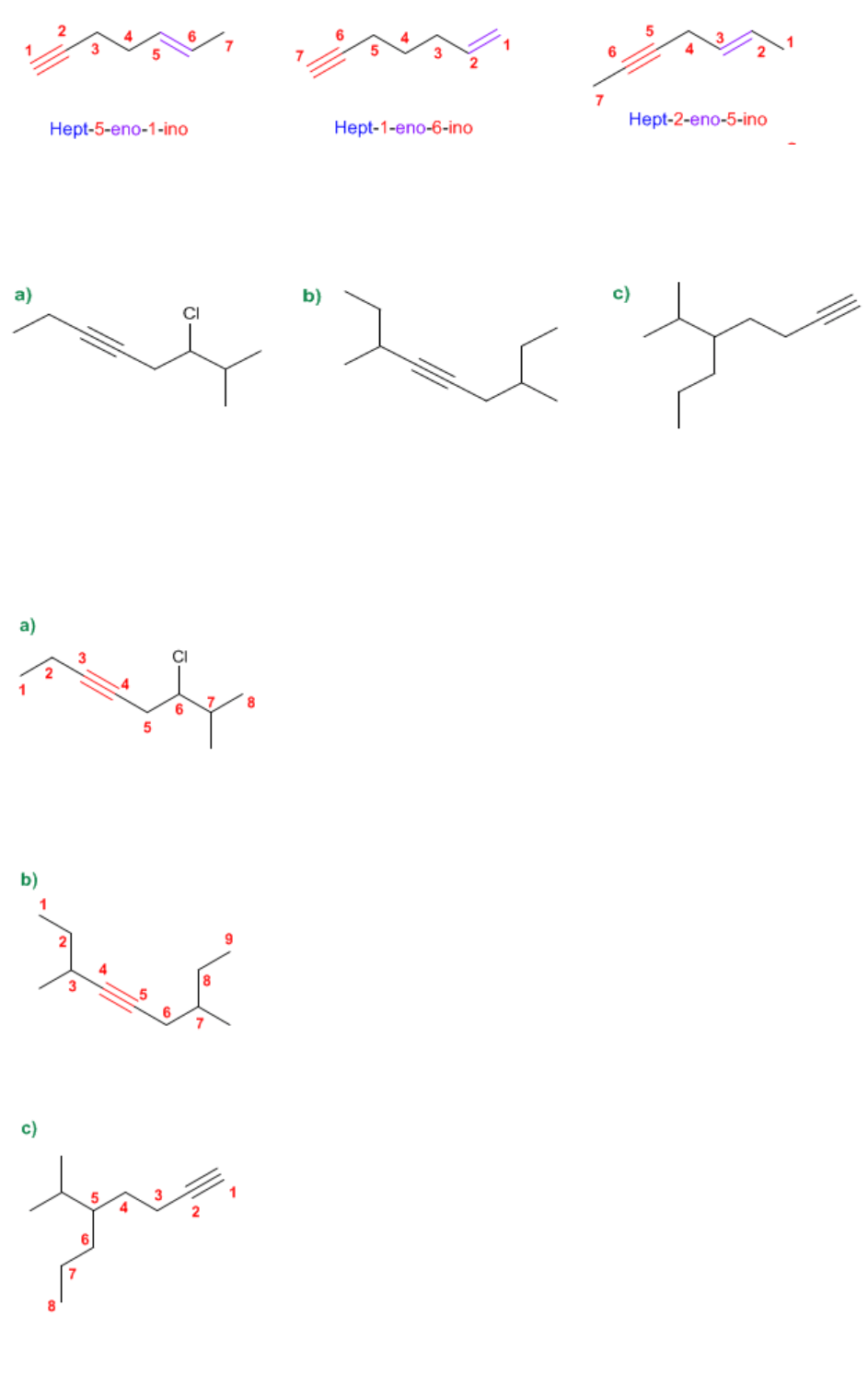
Problema 5.1
Nombra los siguientes alquinos según las reglas IUPAC.
SOLUCIÓN
1. Cadena principal: Cadena de 8 carbonos (octino)
2. Numeración: se empieza por el extremo izquierdo para que el triple enlace tome el localizador más
6-Cloro-7-metiloct-3-ino
6-Cloro-7-metiloct-3-ino
bajo
3. Sustituyentes: cloro en posición 6 y metilo en 7.
4. Nombre: 6-Cloro-7-metiloct-3-ino
1. Cadena principal: la cadena de mayor longitud que contiene el triple enlace tiene 9 carbonos
(nonino)
2. Numeración: empieza por el extremo izquierdo para otorgar al triple enlace localizador 4. Si
numeramos desde la derecha el localizador es 5.
3. Sustituyentes: metilos en posición 3,7
4. Nombre: 3,7-Dimetilnon-4-ino
1. Cadena principal: cadena de 8 carbonos (octino)
2. Numeración: localizador más bajo al triple enlace.
3. Sustituyentes: isopropilo en posición 5
4. Nombre: 5-Isopropiloct-1-ino
El triple enlace tiene prioridad sobre los sustituyentes, por ello, debe estar contenido en la cadena
principal y debe numerarse desde el extremo de la cadena que le otorgue el menor localizador
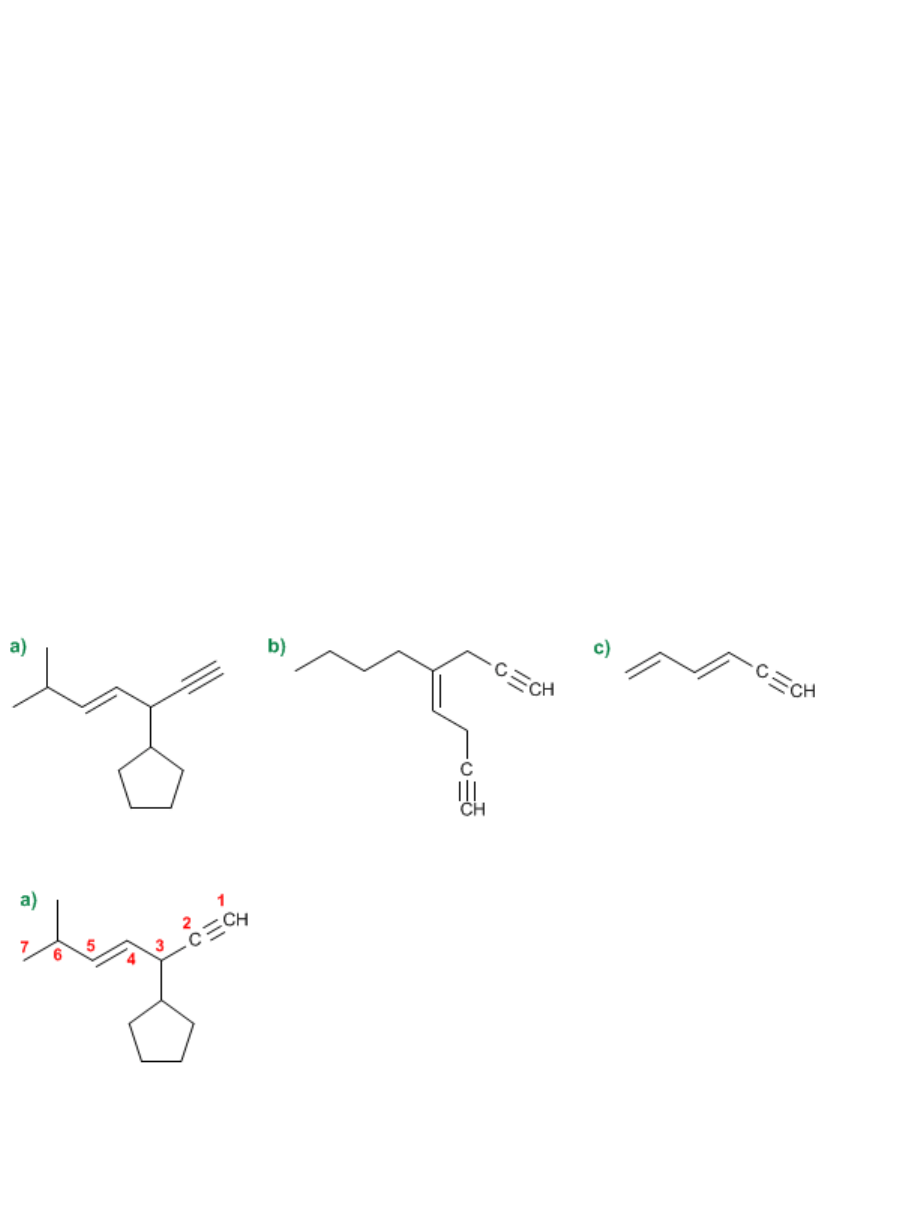
Problema 5.2
Nombra los siguientes hidrocarburos con dobles y triples enlaces.
SOLUCIÓN
1. Cadena principal: de mayor longitud que contenga el doble y triple enlace (hept-4-eno-1-ino).
2. Numeración: doble y triple enlace con los menores localizadores.
3. Sustituyentes: ciclopentilo en 3 y metilo en 6.
4. Nombre: 3-Ciclopentil-6-metilhep-4-eno-1-ino
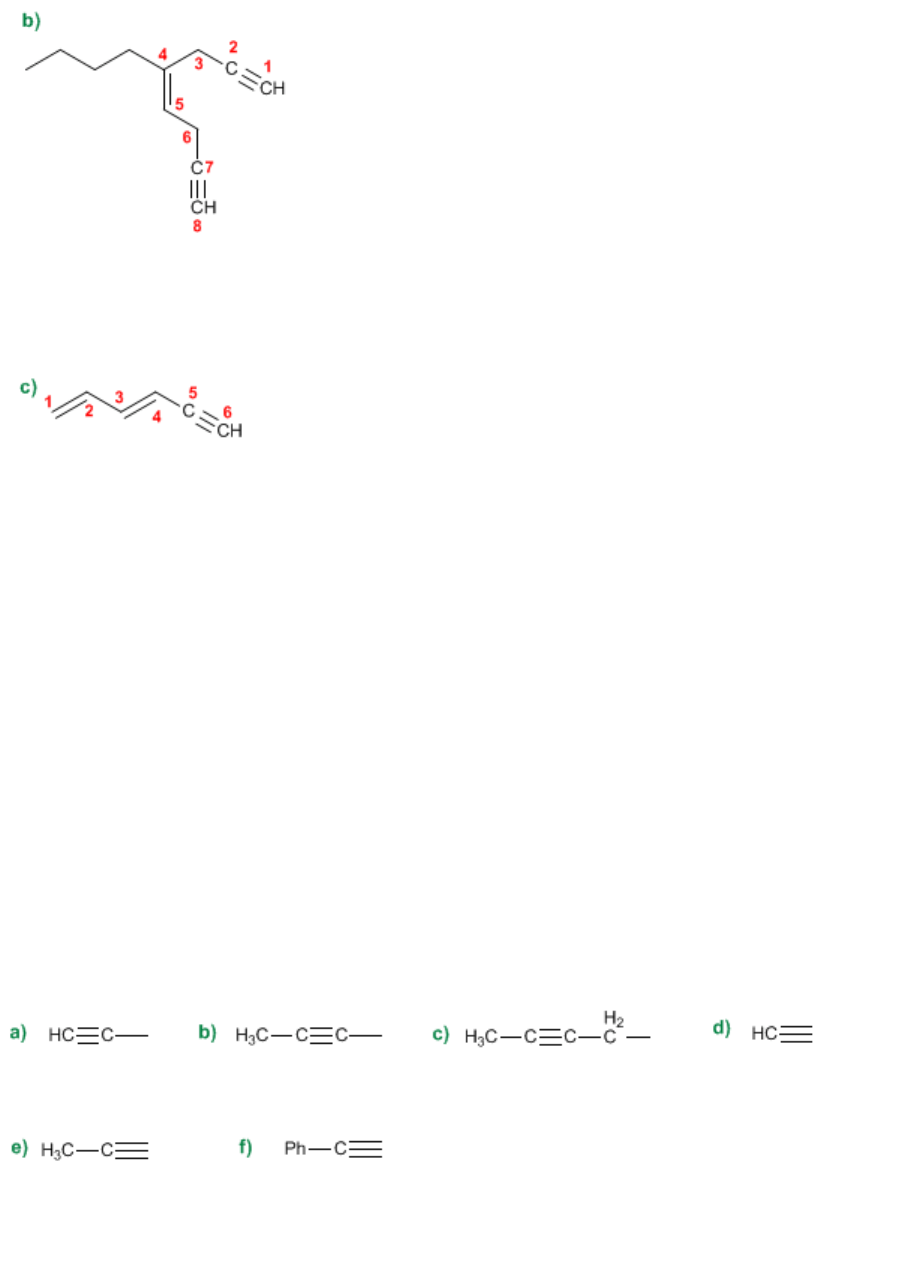
1. Cadena principal: la cadena que contiene el doble y los triples enlaces (oct-4-eno-1,7-diino).
2. Numeración: como los enlaces múltiples están a la misma distancia de ambos extremos (1,4,7),
numeramos para que el butilo tome el menor localizador (4).
3. Sustituyentes: butilo en posición 4.
4. Nombre: 4-Butiloct-4-eno-1,7-diino
1. Cadena principal: de 6 carbonos con dos dobles enlaces y un triple. (hexa-1,3-dieno-5-ino)
2. Numeración: el doble enlace tiene preferencia frente al triple al numerar.
3. Sustituyentes: no tiene.
4. Nombre: Hexa-1,3-dieno-5-ino
Problema 5.3
Los alquinos también pueden nombrarse como sustituyentes. Nombra los siguientes radicales que
contienen triples enlaces.
SOLUCIÓN
Los radicales con triple enlace se nombran terminando en -inilo el prefijo que indica el número de
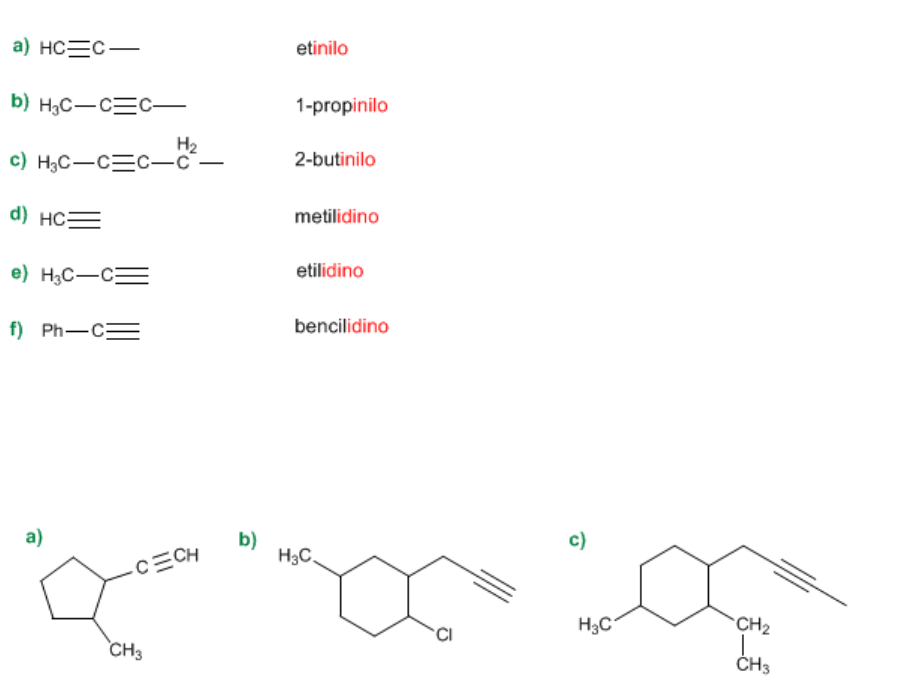
carbonos. Cuando un radical tiene 3 valencias libres se termina en -idino.
Problema 5.4
Nombra los siguientes alquinos tomando el ciclo como cadena principal.
Aromáticos
Los hidrocarburos aromáticos son aquellos hidrocarburos que poseen las propiedades
especiales asociadas con el núcleo o anillo del benceno, en el cual hay seis grupos de
carbono-hidrógeno unidos a cada uno de los vértices de un hexágono. Los enlaces que unen
estos seis grupos al anillo presentan características intermedias, respecto a su
comportamiento, entre los enlaces simples y los dobles. Así, aunque el benceno puede
reaccionar para formar productos de adición, como el ciclohexano, la reacción característica
del benceno no es una reacción de adición, sino de sustitución, en la cual el hidrógeno es
reemplazado por otro sustituto, ya sea un elemento univalente o un grupo.
Los hidrocarburos aromáticos y sus derivados son compuestos cuyas moléculas están
formadas por una o más estructuras de anillo estables del tipo antes descrito y pueden
considerarse derivados del benceno de acuerdo con tres procesos básicos:
1. por sustitución de los átomos de hidrógeno por radicales de hidrocarburos alifáticos,
2. por la unión de dos o más anillos de benceno, ya sea directamente o mediante cadenas
alifáticas u otros radicales intermedios,
3. por condensación de los anillos de benceno.
Cada una de las estructuras anulares puede constituir la base de series homólogas de
hidrocarburos, en las que una sucesión de grupos alquilo, saturados o no saturados, sustituye
a uno o más átomos de hidrógeno de los grupos de carbono-hidrógeno.
Las principales fuentes de hidrocarburos aromáticos son la destilación de la hulla y una
serie de procesos petroquímicos, en particular la destilación catalítica, la destilación del
petróleo crudo y la alquilación de hidrocarburos aromáticos de las series más bajas. Los
aceites esenciales, que contienen terpenos y p-cimeno, también pueden obtenerse de los
pinos, los eucaliptos y las plantas aromáticas y son un subproducto de las industrias
papeleras que utilizan pulpa de pino. Los hidrocarburos policíclicos se encuentran en las
atmósferas urbanas
Usos
La importancia económica de los hidrocarburos aromáticos ha aumentado progresivamente
desde que a principios del siglo XIX se utilizaba la nafta de alquitrán de hulla como
disolvente del caucho. En la actualidad, los principales usos de los compuestos aromáticos
como productos puros son: la síntesis química de plásticos, caucho sintético, pinturas,
pigmentos, explosivos, pesticidas, detergentes, perfumes y fármacos. También se utilizan,
principalmente en forma de mezclas, como disolventes y como constituyentes, en
proporción variable, de la gasolina.
El cumeno se utiliza como componente de alto octanaje en los combustibles de los aviones,
como disolvente de pinturas y lacas de celulosa, como materia prima para la síntesis de
fenol y acetona y para la producción de estireno por pirólisis. También se encuentra en
muchos disolventes comerciales derivados del petróleo, con puntos de ebullición que
oscilan entre 150 y 160 °C. Es un buen disolvente de grasas y resinas y, por este motivo, se
ha utilizado como sustituto del benceno en muchos de sus usos industriales. El p-cimeno se
encuentra en muchos aceites esenciales y se puede obtener porhidrogenación de los
terpenos monocíclicos. Es un subproducto del proceso de fabricación de pasta de papel al
sulfito y se utiliza principalmente, junto con otros disolventes e hidrocarburos aromáticos,
como diluyente de lacas y barnices.
La cumarina se utiliza como desodorante o como potenciador del olor en jabones, tabaco,
productos de caucho y perfumes.
También se utiliza en preparados farmacéuticos.
El benceno se ha prohibido como componente de productos destinados al uso doméstico y
en muchos países también se ha prohibido su uso como disolvente y componente de los
líquidos de limpieza en seco. El benceno se ha utilizado ampliamente en la fabricación de
estireno, fenoles, anhídrido maleico, detergentes, explosivos, productos farmacéuticos y
colorantes.
También se ha empleado como combustible, reactivo químico y agente de extracción para
semillas y frutos secos. Los derivados mono, di y trialquilados del benceno se utilizan
principalmente como disolventes y diluyentes y en la fabricación de perfumes y productos
intermedios en la producción de colorantes. Estas sustancias se encuentran en algunos
petróleos y en los destilados del alquitrán de hulla. El pseudocumeno se utiliza en la
fabricación de perfumes y el 1,3,5-trimetilbenceno y el pseudocumeno se emplean también
como productos intermedios en la producción de colorantes, aunque el uso industrial más
importante de estas sustancias es como disolventes y diluyentes de pinturas.
El tolueno es un disolvente de aceites, resinas, caucho natural (mezclado con ciclohexano)
y sintético, alquitrán de hulla, asfalto, brea y acetilcelulosas (en caliente, mezclado con
etanol).
También se utiliza como disolvente y diluyente de pinturas y barnices de celulosa y como
diluyente de las tintas de fotograbado. Al mezclarse con el agua, forma mezclas
azeotrópicas que tienen un efecto deslustrante. El tolueno se encuentra en mezclas que se
utilizan como productos de limpieza en distintas industrias y en artesanía. También se
utiliza en la fabricación de detergentes y cuero artificial y es una importante materia prima
para síntesis orgánicas, como las de cloruro de benzoilo y bencilideno, sacarina, cloramina
T, trinitrotolueno y un gran número de colorantes. El tolueno es un componente del
combustible para aviones y de la gasolina para automóviles. El Reglamento 594/91/CE del
Consejo ha prohibido el uso de esta sustancia en la Unión Europea.
El naftaleno se utiliza como material de partida para la síntesis orgánica de una amplia gama
de sustancias químicas, como antipolillas, y en conservantes de madera. También se emplea
en la fabricación de índigo y se aplica externamente al ganado o las aves para controlar los
insectos parásitos.
Este documento contiene más páginas...
Descargar Completo
Lectura 8 - Alquenos alquinos y aromaticos.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.