INFLAMACION Y REPARACION DE LOS TEJIDOS
La
lesión
de los
tejidos vascularizados provoca una
serie
de
acontecimientos
coordinados, complejos
y
dinámicos a
los que se
denomina
de
forma global como
inflamación y
reparación. Aunque
se
han observado variaciones entre la respuesta
de los
diferentes tipos
de
tejido,
los
procesos glo
bales son
muy similares.
Las
secuelas dependen
del
origen
y la
zona
de la
lesión,
del
estado
de la
homeostasis
local
y
de si la
lesión
es
aguda
o
crónica.
El
objetivo último
de
la
inflamación
es
reparar
y
restaurar
la
función,
eliminando
el
agente
físico o
patológico, sustituyendo
los
tejidos lesio
nados
o
destruidos
y
promoviendo
la
regeneración
de
la
estructura tisular normal.
Los
profesionales
de la
rehabilitación tratan una
gran variedad
de
procesos
inflamatorios resultantes
de
traumatismos, procedimientos quirúrgicos
o
cicatrizaciones
con
flictivas.
El
facultativo requerido
para
tratar
este
tipo
de lesiones necesita
comprender
la
fisiología
de la
inflamación
y de la
cicatrización
y
cómo
se
pueden
modificar.
El
médico puede mejorar
la
cicatrización mediante
la
aplicación ade
cuada
de
diversos agentes
físicos,
ejercicios
terapéuticos o
técnicas manuales.
Un
programa
de
rehabilitación exitoso
precisa
del
conocimiento
de la
biomecánica,
de las fases
de
la
cicatrización
de
tejidos
y de los
efectos
de la
inmovilización
y las
intervenciones
terapéuticas
sobre los
procesos
de
curación.
FASES
DE LA I
NFLAMACIÓN
Y LA
CICA
TRIZACIÓN
El
proceso
de
inflamación
y
reparación consta
de
tres
fases:
inflamación,
proliferación
y
maduración.
La fase
de
inflamación prepara
a la
herida
para la
curación;
la
fase
de
proliferación reconstruye
las
estructuras
y
fortalece la
herida;
y la
fase de
maduración modifica
el
tejido
cicat
ricial hacia
su
forma madura
(fig. 3-1). La
duración de
cada fase varía en
cierto grado,
y las fases
generalmente se
solapan.
Por
tanto,
los
esquemas
de las
diversas
fases de
la
curación
que se
muestran
en este
capítulo
son sólo
pautas
generales,
no
definiciones precisas
(fig.
3-2
).
FASE DE INFLAMACIÓN (DÍAS 1 A 6)
La
inflamación,
del
latín inflamer,
que
significa «prender»,
comienza cuando
la
fisiología
normal
del
tejido
se ve
alterada
por
una enfermedad
o
un traumatismo.
Esta
respuesta
pro
tectora inmediata intenta destruir, diluir
o aislar las
células
o
los
agentes
que
pueden
ser
lesivos.
Es
un prerrequisito nor
mal y
necesario
para la
curación.
Si no se
produce
inflama
ción,
no se
puede producir
la
cicatrización.
La
inflamación
puede
ser
también
peligrosa,
sobre
todo cuando
se
dirige
al
tejido erróneo
o es
excesiva.
Por
ejemplo,
las
reacciones
inflamatorias dirigidas
de
forma inadecuada
que
subyacen
en
las
enfermedades
autoinmunes, como
la
artritis
reumatoide,
pueden provocar una cicatriz excesiva
que
puede lesionar y
destruir articulaciones. Aunque
el
proceso inflamatorio
sigue
la
misma
secuencia independientemente
de la causa de
la
lesión, algunas
de las
causas provocan
la
prolongación o
la
exageración
de
determinados acontecimientos.
Hace casi
2.000 años Cornelio
Celso
caracterizó
la
fase
inflamatoria
por los
cuatro
signos cardinales
de calor,
r
ubor
,
tumor y dolor
(términos latinos). Virchow añadió
posterior
mente un quinto signo cardinal,
functio laesa
(pérdida de función) (tabla
3-1
).
En
primer lugar,
hay
un aumento
de la
llegada
de
sangre
a la
zona, denominada
hiperemia,
con
un aumento
de
la
temperatura
y
enrojecimiento
de la
zona
de
inflamación
aguda.
El
inicio
de la
hiperemia
al
principio
de la
respuesta inflamatoria
está
controlado
por
mediadores químicos y
neurogénicos.
El
edema
local es el
resultado
de
un
aumento
de la
permeabilidad
y de la
vasodilatación
de los
vasos
sanguíneos locales y de
la infiltración de líquido en los espacios intersticiales de la zona lesionada. El dolor es el resultado de
la presión del edema y de la irritación de las estructuras sensibles al dolor por las sustancias químicas
liberadas por las células lesionadas. Tanto el dolor como el edema pueden producir pérdida de función.
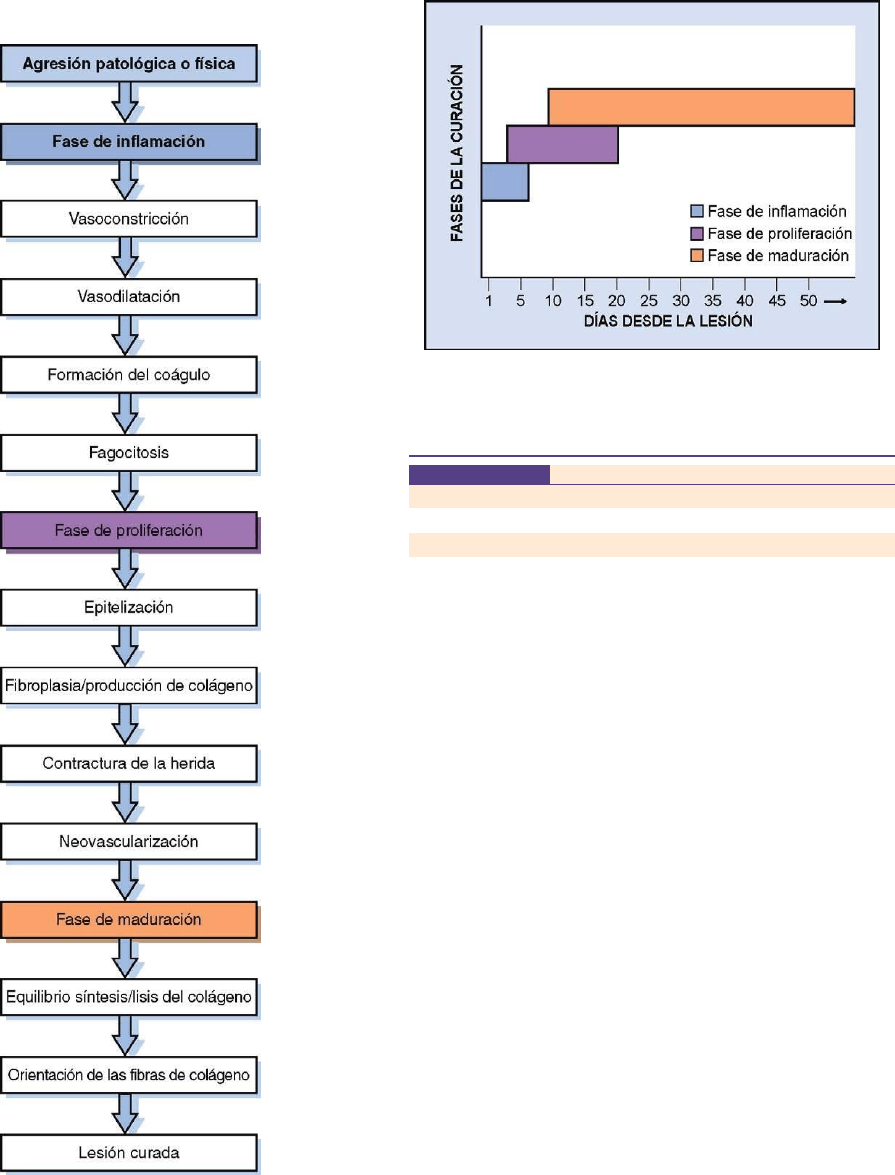
FIG 3-2
Cronograma
de las fases de la
inflamación
y la
reparación.
TABLA
3-1
Signos cardinales
de la
inflamación
Signo (español)
Signo (latín)
Causa
Calor
Calor
Aumento
de la
vascularización
Enrojecimiento
Rubor
Aumento
de la
vascularización
Edema
T
umor
Bloqueo del
drenaje linfático
Dolor
Dolor
Presión física o
irritación
química de las
estructuras
sensibles al
dolor
Pérdida de la Functio laesa Dolor y
edema
Función
Se ve
cierta discrepancia
en la
literatura acerca
de
la
duración
del
proceso
de
la fase de
inflamación.
Algunos
investigadores establecen
que es
relativamente
breve,
con
una duración inferior
a
cuatro días,
y
otros piensan que
puede durar
hasta
seis
días.
Esta
discrepancia puede
ser
el
resultado
de
variaciones
individuales
y
específicas
de
la
lesión
o
puede reflejar
la
característica
de
solapamiento de
las fases de la
inflamación
y la
curación
de los
tejidos.
La fase
inflamatoria consiste
en
una compleja secuencia
de
acontecimientos
interactivos
que se
solapan
y que
in
cluye
procesos vasculares, celulares,
hemostáticos
e
inmu
nológicos.
Los
mediadores humorales
y
nerviosos actúan
para
controlar
la fase
inflamatoria.
Se ha
demostrado
que
inmediatamente
después
de la
lesión predominan
las
pla
quetas
y los
neutrófilos,
y
liberan una
serie de
factores
que
aumentan
la
respuesta
de
agregación plaquetaria, inician
la
cascada
de
coagulación
o
actúan como quimiotácticos
para
las
células implicadas
en la fase
inflamatoria.
La
infiltración
por
neutrófilos
cesa
después
de
unos pocos
días, y éstos
van
siendo sustituidos
por
macrófagos
a
partir
de los dos
días
después
de la
lesión.
Este
cambio
en el
tipo celular
en
la
zona
de la
lesión
se
correlaciona
con el
cambio
de la
fase
de
inflamación
a la de
proliferación.
Las
alteraciones
en la
anatomía
y la
función
de la
microvascularización,
incluyendo capilares, vénulas poscapilares
y vasos
linfáticos,
se
encuentran
entre
las
respuestas
más
precoces
que se
han observado
en la fase de
inflamación
.
Respuesta vascular
Los
traumatismos,
tales
como
la
laceración,
la
distensión o
la
contusión, rompen
físicamente
estas
estructuras
y
pueden
provocar hemorragia, pérdida
de
líquido,
lesión celular y
exposición
de los
tejidos
a
materiales
extraños, incluyendo
bacterias.
Los vasos
lesionados responden
rápidamente
con
una constricción
transitoria
en
un intento
de
reducir
al
mínimo
la
pérdida
de
sangre.
Esta
respuesta,
que
está
mediada
por
noradrenalina, dura generalmente entre
5
y
10
minutos, pero
se
puede prolongar
en los
pequeños
vasos
por
acción
de la
serotonina
liberada
por los
mastocitos y
las
plaquetas.
Después
de la
vasoconstricción transitoria
de los
vasos
lesionados,
los
capilares
próximos
a la
zona
de
lesión
se
dilatan.
La
permeabilidad capilar también aumenta
al
lesio
narse
la
pared
de los
capilares
y en
respuesta
a las
sustancias
químicas
liberadas
por los
tejidos lesionados
(fig. 3-3). La
vasodilatación
y el
aumento
de la
permeabilidad capilar se
inician
por
acción
de la
histamina,
el
factor Hageman, la
bradicinina,
las
prostaglandinas
y las
fracciones
del
comple
mento.
La
vasodilatación
y
el
aumento
de la
permeabilidad capilar duran hasta una hora después
de
haberse
producido
la
lesión.
La
histamina
es
liberada principalmente
por los
mastocitos,
así
como
por las
plaquetas
y los
basófilos
en
la
zona
de la
lesión.
La
histamina provoca
vasodilatación
y
aumento
de la
permeabilidad vascular
en las
vénulas,
lo cual
contribuye
al
edema
local. La
histamina
también
atrae
a los
leucocitos (células
blancas
de la
sangre) hacia la
zona lesionada.
La
capacidad
de
una sustancia
química
para
atraer células
se
conoce como
quimiotaxis.
La
his
tamina
es
uno
de los
primeros mediadores inflamatorios
liberado
después
de la
lesión tisular
y está
activa
durante
aproximadamente una hora
después
de la
lesión
(fig.
3-4
)
.
El
factor Hageman (conocido también como factor
XII
de
la
coagulación), una
enzima
que se
encuentra
en la
sangre,
se
activa
por el
contacto
con
superficies
cargadas
negativamente
en la
cubierta endotelial
que
quedan expuestas
al
lesionarse los vasos. El papel del factor Hageman es doble. En primer lugar,
activa el sistema de coagulación para detener la hemorragia local. En segundo
lugar, provoca vasoconstricción y aumento de la permeabilidad vascular mediante
la activación de otras proteínas de plasma. Convierte el plasminógeno en plasmina
y la precalicreína en calicreína, y activa la vía alternativa del complemento (fig. 3-
5).
La plasmina aumenta la permeabilidad vascular tanto en la piel como en los
pulmones al inducir la rotura de la fibrina y rompiendo componentes del sistema
de complemento. La plasmina también activa el factor Hageman, el cual inicia la
cascada que genera bradicinina.
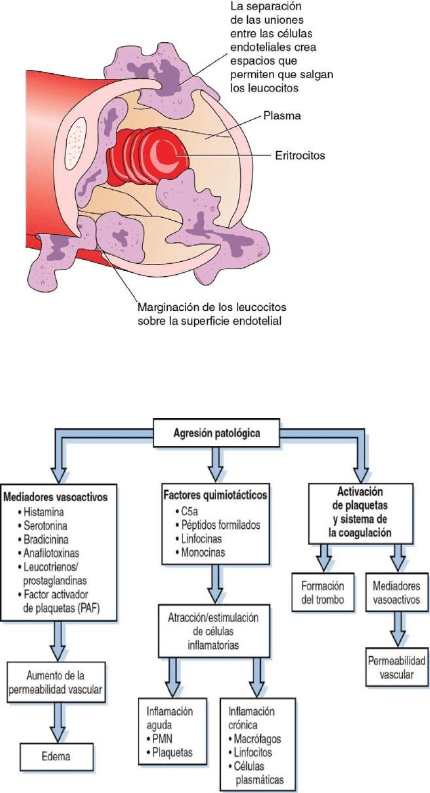
FIG 3-3 Respuesta vascular para la
curación
de una
herida.
FIG 3-4 Mediadores de la respuesta inflamatoria. PMN, polimorfonucleares
Respuesta Hemostatica
La
respuesta hemostática
a la
lesión controla
la
pérdida de sangre cuando
se
lesionan
o se
rompen
los vasos.
Inmediata- mente después
de la
lesión,
las
plaquetas llegan
a la
zona
y
se
unen
al
colágeno expuesto, liberando fibrina
para
estimular
la
coagulación.
Las
plaquetas liberan también una proteína
re
guladora
conocida como factor
de
crecimiento derivado
de
plaquetas
(FCDP), que es
quimiotáctico
y
mitogénico
para
los
fibroblastos
y
puede
ser
también
quimiotáctico
para los
ma
-
crófagos,
monocitos
y
neutrófilos.
Por
tanto,
las
plaquetas
intervienen
no sólo en la
hemostasia,
sino que
también con
-
tribuyen
al
control
del
depósito
de
fibrina,
a la
proliferación
de
fibroblastos
y a la
angiogénesis.
Cuando
la
fibrina
y la
fibronectina llegan
a la
zona de
lesión, forman puentes
de
unión
con el
colágeno
para
crear
una
red de
fibrina.
Esta débil
estructura
proporciona un
tapón
temporal
en los vasos
sanguíneos
y
linfáticos, limitando
la
hemorragia
local y el
drenaje
de
líquido.
El
entramado
sella
los
vasos
lesionados
y
delimita
la
reacción inflamatoria
a la
zona inmediatamente alrededor
de la
lesión.
Los vasos
lesionados
taponados
no se
abren hasta
que está
muy avanzado
el
pro
ceso de
curación.
La red de
fibrina
sirve
como
la
única fuente
de
consistencia
durante
la fase
inflamatoria
de la
curación
.
Respuesta celular
La
sangre circulante
está
compuesta
por
células especiali
zadas
suspendidas
en
un líquido conocido como
plasma.
Estas
células
son los
hematíes
(glóbulos
rojos),
los
leucocitos
(glóbulos blancos)
y las
plaquetas.
Los
glóbulos
rojos
tienen
una relevancia menor
en el
proceso
inflamatorio, aunque
pueden migrar
a los
espacios tisulares
si la
reacción
inflama
-
toria
es
intensa.
La
función principal
de
los
glóbulos rojos,
el
transporte
de
oxígeno,
se
desarrolla
en el
interior
de
los
vasos. Un
exudado inflamatorio
que
contiene sangre indica
normalmente una
lesión
grave de la
microcirculación.
La
acumulación
de
sangre
en
un tejido
o en
un órgano
se
cono
- ce
como hematoma;
la
salida
de
sangre
a
una articulación
se
denomina hemartrosis.
El
hematoma
en el
músculo puede provocar dolor
y
limitación
de la
función
y de la
movilidad;
también puede aumentar
la
formación
de
tejido
cicatricial.
Los
hematomas musculares pueden provocar dolor,
li
mitación
de la
movilidad
y
un aumento
de la
formación
de
tejido cicatricial.
Una
función fundamental
de la
inflamación
es
proporcionar leucocitos
a la
zona
de la
lesión
a
través
del
sistema
circulatorio.
Los
leucocitos
se
clasifican
según
su
estructura
en
polimorfonucleares
(PMN) y en
células
mononucleares
(fig. 3-8). Los PMN
presentan núcleos
con
varios lóbulos y contienen gránulos
citoplasmáticos. Además,
se
subclasifi
can en
neutrófilos, basófilos
y
eosinófilos
en
función
de
sus
preferencias
por
diferentes tinciones histológicas
específi
- cas. Los
monocitos
son más
grandes
que los PMN y
tienen un único núcleo.
En el
proceso inflamatorio,
los
leucocitos
tienen
la
función muy importante
de
limpiar
la
zona
de
la
lesión
de
restos
y
microorganismos
para
preparar
la
zona
para la
reparación
del
tejido.
La
migración
de los
leucocitos
a la
zona
de
lesión
se
produce
en las
horas próximas
a la
lesión. Cada leucocito
se
especializa
y
tiene un objetivo específico. Algunos
leucocitos
predominan
más en la fase
precoz
de la
inflamación, mientras
que
otros
adquieren
más
importancia durante
las fases más
tardías.
Al
principio,
el
número
de
leucocitos
en la
zona
de
lesión es
proporcional
a su
concentración
en la
sangre
cir
culante.
Como
los
neutrófilos
son los que
presentan una mayor concentración
en
sangre, predominan
en las fases
precoces
de la
inflamación.
Los
agentes
quimiotácticos liberados
por
otras células, como
los
mastocitos
y las
plaquetas,
atraen
a
los
leucocitos
en el
momento
de la
lesión.
Los
neutrófilos limpian
la
zona
de
lesión
de
bacterias
y
restos mediante
fagocito
sis.
Cuando
se
lisan,
los
lisosomas
de los
neutrófilos liberan
enzimas proteolíticas (proteasas)
y
enzimas
colagenolíticas
(colagenasas),
que
comienzan
el
proceso
de
desbridamiento.
Los
neutrófilos permanecen
en la
zona
de
lesión
sólo
durante
24
horas,
y al
transcurrir
dicho tiempo
se
desintegran.
Sin
em
bargo, ayudan
a
perpetuar
la
respuesta
inflamatoria liberando agentes quimiotácticos
para
atraer
a
otros leucocitos
a la
zona.
Los
basófilos liberan histamina después
de la
lesión
y
contribuyen
al
aumento
de
permeabilidad vascular inicial.
Los
eosinófilos
se
pueden implicar
en la
fagocitosis
en
cierto grado.
Durante
las 24-48
horas siguientes
a
una lesión
aguda
predominan
los
monocitos.
Los
monocitos
constituyen entre
el 4% y el 8% del
total
del
recuento
de
glóbulos
blancos. Se piensa que el predominio de dichas
células en esta fase de la inflamación se debe en parte a su vida media
más larga. Los linfocitos fabrican anticuerpos para me- diar la respuesta
inmune del organismo. Prevalecen en las situaciones de inflamación crónica.
Los monocitos se convierten en macrófagos cuando salen de los capilares y pasan a los
espacios tisulares. Se considera que el macrófago es la célula más importante en la fase de
inflamación y es fundamental para la curación de la lesión. Los macrófagos son importantes
porque producen un amplio rango de sustancias químicas (cuadro 3-1). Tienen una función
fundamental en la fagocitosis, al producir enzimas como la colagenasa (fig. 3-9). Estas
enzimas facilitan la retirada de tejido necrótico y bacterias. Los macrófagos producen,
además, factores que son quimiotácticos para otros leucocitos y factores de crecimiento que
inducen la proliferación celular y la síntesis de moléculas de la matriz extracelular por
células residentes en la piel.
Probablemente los macrófagos desempeñen un papel en la localización del proceso
inflamatorio y en la atracción de fibroblastos a la zona lesionada liberando factores
quimiotácticos como la fibronectina. Los macrófagos influyen a través de mediadores
químicos en el número de fibroblastos de reparación activados; por tanto, en ausencia de
macrófagos hay menos fibroblastos maduros que se desplazan a la zona de lesión. Los
macrófagos también liberan el FCDP liberado por las plaquetas durante la coagulación y
pueden activar a los fibroblastos. En las fases más avanzadas de fibroplasia, los
macrófagos pueden potenciar el depósito de colágeno haciendo que los fibroblastos se
adhieran a la fibrina.
Como los macrófagos fagocitan organismos, liberan diversas sustancias, como peróxido
de hidrógeno, ácido ascórbico y ácido láctico, que favorecen la muerte de dichos
organismos. El peróxido de hidrógeno inhibe el crecimiento microbiano anaeróbico. Los
otros dos productos indican el nivel de la lesión en la zona, y su concentración se interpreta
por el organismo como el grado de necesidad de más macrófagos en la zona. Esta
interpretación, a su vez, provoca un aumento de la producción de estas sustancias, lo cual
resulta en un aumento de la población de macrófagos y una respuesta inflamatoria más
intensa y más prolongada.
Los macrófagos son más eficaces cuando hay oxígeno en los tejidos lesionados. Sin
embargo, pueden tolerar condiciones de bajas concentraciones de oxígeno, como se
demuestra por su presencia en los estados inflamatorios crónicos. También es necesaria una
tensión de oxígeno adecuada en la zona de la lesión para reducir el riesgo de infección. La
tensión de oxígeno tisular depende de la concentración atmosférica de oxígeno que está
disponible para la respiración, de la cantidad de oxígeno absorbido por los sistemas
respiratorios y circulatorios y del volumen de sangre disponible para el transporte, así como
del estado de los tejidos. La aplicación tópica de oxígeno a una zona lesionada no influye
tanto en la tensión de oxígeno tisular como el nivel de oxígeno que llega a dicha zona a
través de la sangre circulante
Respuesta inmunitaria
La respuesta inmunitaria está mediada por factores celulares y humorales. A nivel celular,
los macrófagos presentan antígenos extraños a los linfocitos T para activarlos. Los linfocitos
T acti- vados elaboran un gran número de mediadores inflamatorios y activan a las células B,
haciendo que éstas evolucionen a células plasmáticas, las cuales fabrican anticuerpos que se
unen de forma específica a los antígenos extraños. Estos anticuerpos pueden cubrir a las
bacterias y a los virus inhibiendo su función y opsonizarlos de forma que puedan ser
rápidamente ingeridos y eliminados del sistema por las células fagocíticas. Los anticuerpos
también se unen a los antígenos, bacterias y virus mediante la activación del sistema del
complemento, una fuente importante de mediadores vasoactivos. El sistema del
complemento es uno de los sistemas de proteínas plasmáticas más importante en la
inflamación, ya que sus componentes participan teóricamente en todas las respuestas
inflamatorias.
El sistema del complemento es una serie de proteínas plasmáticas enzimáticas que se
activan por dos vías diferentes, la clásica y la alternativa. La activación del primer
componente de cada vía de la cascada produce la activación enzimática secuencial de los
componentes de la cascada (fig. 3-10). La vía clásica se activa por una asociación antígeno-
anticuerpo, y la vía alternativa se activa mediante sustancias microbianas y celulares. El
producto final de la cascada, por cualquiera de las vías, es un complejo de C6, C7, C8 y C9
que forma el complejo de ataque de membrana (CAM). El CAM origina poros en las
membranas plasmáticas, permitiendo de esta manera la entrada de agua y de iones al interior
de la célula, provocando la lisis y la muerte celular.
Los subcomponentes generados en las primeras fases de la cascada también presentan
funciones importantes. La activación de los componentes de C1 a C5 produce subunidades
que potencian la inflamación haciendo a las bacterias más vulnerables a la fagocitosis
(conocido como opsonización), atrayendo leucocitos por quimiotaxis y actuando como
anafilotoxinas. Las anafilotoxinas inducen la desgranulación de los mastocitos y los
basófilos, provocando la liberación de histamina, factor activador de plaquetas y
leucotrienos. Todas estas sustancias potencian aún más el aumento de permeabilidad
vascular.
En resumen, la fase inflamatoria tiene tres consecuencias principales. Primero, la fibrina,
la fibronectina y el colágeno establecen puentes de unión para formar una malla de fibrina
que limita la pérdida de sangre y le proporciona a la herida cierta consistencia inicial.
Luego, los neutrófilos, seguidos por los macrófagos, comienzan a eliminar el tejido
lesionado. Finalmente, se reclutan células endoteliales y fibroblastos y se estimula su
división. Todo esto prepara al proceso para la fase de proliferación de la curación. La tabla
3-3 resume los acontecimientos de la fase inflamatoria de la curación.
FASE DE PROLIFERACIÓN (DÍAS 3 A 20)
La segunda fase de la reparación de un tejido se conoce como fase de proliferación.
Esta fase dura generalmente hasta 20 días, e implica tanto a las células epiteliales como a los
tejidos conjuntivos.
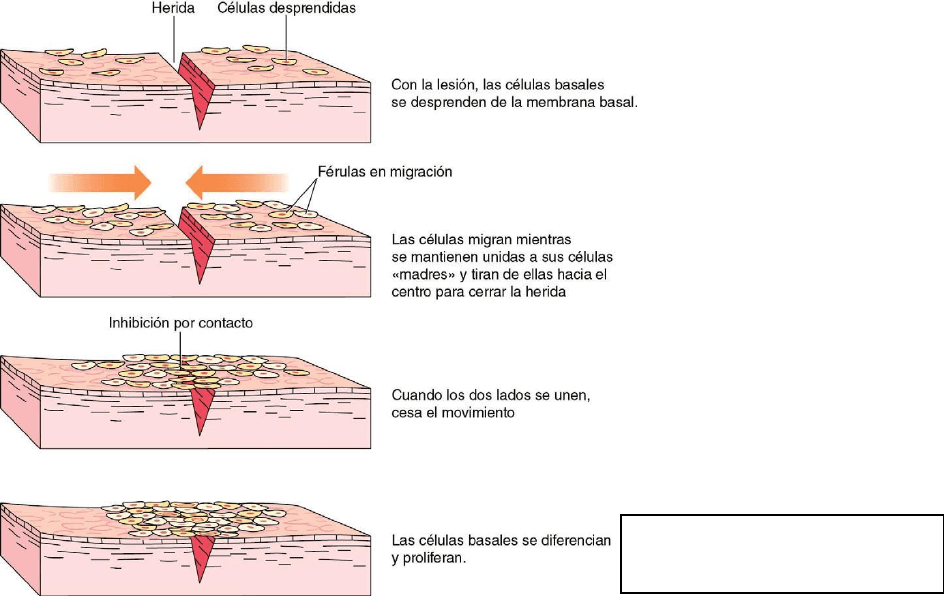
FIG 3-11 Diagrama esquemático de la
epitelización.
Su objetivo es cubrir la herida y proporcionar consistencia a la zona de lesión. Las células
epiteliales forman la cubierta de las membranas mucosas y serosas y de la epidermis de la
piel. El tejido conjuntivo contiene fibroblastos, sustancia fundamental y fibras, y
proporciona el andamiaje para el resto de los tejidos. La estructura, la consistencia y la
elasticidad del tejido conjuntivo varían, dependiendo del tipo de tejido que incluya. Se
producen simultáneamente cuatro procesos en la fase de proliferación para conseguir la
coalescencia y el cierre de la zona lesionada: epitelización, producción de colágeno,
contracción de la herida y neovascularización.
Epitelización
La epitelización, el restablecimiento de la epidermis, se inicia precozmente en la
proliferación cuando una herida es superficial, normalmente en las primeras horas de
producirse la lesión. Cuando una herida es profunda, la epitelización es más tardía, tras la
producción de colágeno y de la neovascularización. La epitelización proporciona una barrera
protectora para prevenir la pérdida de agua y electrólitos y para reducir el riesgo de
infección. La curación de la superficie de una herida sólo mediante epitelización no
proporciona la consistencia adecuada para satisfacer las demandas mecánicas a las que se
someten la mayoría de los tejidos. Dicha consistencia la proporciona el colágeno producido
mediante fibroplasia.
Durante la epitelización, las células epiteliales no lesionadas de los bordes de la zona
lesionada, se reproducen y migran sobre la zona lesionada, cubriendo la superficie de la
herida y cerrando el defecto. Se cree que el estímulo para dicha actividad es la pérdida de
inhibición por contacto que se produce cuando las células epiteliales están normalmente en
contacto entre ellas, pero es una hipótesis. Las células epiteliales que migran permanecen
conectadas a sus células «progenitoras» tirando de la epidermis intacta hacia el borde de la
herida. Cuando las células epiteliales de un borde se encuentran con las del otro borde, dejan
de moverse por la inhibición por contacto (fig. 3-11). Aunque estén limpias, las heridas que
se han aproximado pueden quedar recubiertas clínicamente aproximadamente en 48 horas;
las heridas abiertas más grandes tardan más tiempo. En ese caso tardan varias semanas para
que esta delgada capa se multiplique y se diferencie en los diversos estratos de la
epidermis normal.
Producción de colágeno
Los fibroblastos fabrican colágeno. El crecimiento de los fibroblastos, conocido como
fibroplasia, tiene lugar en el tejido conjuntivo. Los fibroblastos se diferencian a partir de
células mesenquimales indiferenciadas localizadas alrededor de los vasos sanguíneos y en la
grasa. Estas células migran a la zona de la lesión a lo largo de tiras de fibrina, en respuesta a
influencias quimiotácticas, y están presentes en toda la zona lesionada. Para que se produzca
la fibroplasia, es necesario un aporte adecuado de oxígeno, ácido ascórbico y otros
cofactores como el zinc, el hierro, el manganeso y el cobre. Según aumenta el número de
fibroblastos, comienzan a alinearse entre ellos perpendicularmente a los capilares. Los
fibroblastos sintetizan procolágeno, el cual está compuesto por tres cadenas polipeptídicas
enrolladas que se mantienen unidas entre sí por enlaces electrostáticos débiles en una triple
hélice. Estas cadenas sufren fracturas por la acción de la colagenasa para formar
tropocolágeno. A continuación, múltiples cadenas del tropocolágeno se agrupan
conjuntamente para formar microfibrillas de colágeno, las cuales a su vez forman fibrillas de
colágeno que en última instancia se combinan para formar fibras de colágeno (fig. 3-12). Los
puentes de unión entre las moléculas de colágeno proporcionan aún más consistencia a la

zona lesionada. El colágeno cumple dos objetivos en la curación de las heridas: proporciona
consistencia y facilita el desplazamiento de otras células, tales como las células endoteliales
y los macrófagos, mientras están participando en la curación de la herida. Este tejido que
contiene los capilares, los fibroblastos y los miofibroblastos de nueva formación se conoce
como tejido de granulación. Según va aumentando la cantidad de tejido de granulación se va
produciendo una reducción concomitante del tamaño del coágulo de fibrina, permitiendo la
formación de una estructura de soporte más permanente. Estos acontecimientos están
mediados por factores quimiotácticos, que estimulan un aumento de la actividad de los
fibroblastos, y por la fibronectina, que potencia la migración y la adhesión de los
fibroblastos. Inicialmente, los fibroblastos producen un colágeno delgado, de estructura débil
con una organización no consistente, conocido como colágeno tipo III. Este período es la
fase más delicada durante el proceso de curación, debido a que el tejido tiene muy poca
consistencia. Durante la fase de proliferación, una zona lesionada presenta la mayor cantidad
de colágeno, aunque su consistencia o tensión puede llegar a ser tan baja como del 15% de la
consistencia de un tejido normal.
Apunte clínico
Durante la fase de proliferación, una zona lesionada presenta la mayor cantidad de
colágeno, aunque su consistencia o tensión puede llegar a ser tan baja como del 15% de
la consistencia de un tejido normal.
Los fibroblastos producen también ácido hialurónico, un glucosaminoglucano (GAG) que
aporta agua a la zona, aumenta la cantidad de matriz intracelular y facilita la migración
celular. Se postula que la composición de esta sustancia está relacionada con el número y la
localización de los puentes de unión, lo cual implica que la relación entre los GAG y el
colágeno es la que dicta la arquitectura de la cicatriz.
La formación de enlaces cruzados permite que el tejido recién formado tolere
movimientos precoces, controlados, sin romperse. Sin embargo, la aparición de infección,
edema o una tensión excesiva en la zona de la lesión puede provocar más inflamación y un
depósito adicional de colágeno. El depósito excesivo de colágeno origina una cicatriz
excesiva que puede limitar el pronóstico funcional.
Hacia el séptimo día después de la lesión se produce un aumento significativo de la
cantidad de colágeno, que hace que la consistencia de la zona lesionada aumente de forma
constante. En el día 12, el colágeno tipo III inmaduro inicial comienza a ser sustituido por
colágeno tipo I, una forma más madura y más resistente. La proporción entre colágeno tipo
I y tipo III aumenta de forma constante desde este momento. La producción de colágeno es
máxima hacia el día 21 de la curación, pero la consistencia de la herida en este momento es
sólo el 20% de la de la dermis normal. Aproximadamente a las 6 semanas de la lesión,
cuando una herida está cicatrizando bien, presenta una consistencia que corresponde al 80%
de la definitiva.
Contracción de la herida
La contracción de la herida es el mecanismo final para la reparación de una zona
lesionada. Al contrario de lo que ocurre con la epitelización, que recubre la superficie de la
herida, la contracción tira de los bordes de la herida para juntarlos, encogiendo, de hecho, la
herida. La contracción satisfactoria deja una pequeña zona que será reparada con la
formación de una cicatriz. La contracción de la herida comienza aproximadamente 5 días
después de la lesión y tiene su pico más alto después de unas 2 semanas. Las principales
células responsables de la contracción de una herida son los miofi- broblastos. Los
miofibroblastos, identificados por Gabbiani y cols. en 1971, derivan de las mismas células
mesenquimales que los fibroblastos. Los miofibroblastos son parecidos a los fibroblastos
excepto en que, además, poseen las propiedades contráctiles del músculo liso. Los
miofibroblastos se insertan en los bordes de piel intacta y tiran de toda la capa epitelial hacia
dentro. La tasa de contracción es proporcional al número de miofibroblastos que hay en y
por debajo de los márgenes celulares, y es inversamente proporcional a la estructura en
malla del colágeno.
Según la teoría del «marco de fotos», el margen de la herida por debajo de la epidermis es
donde se localiza la actividad de los miofibroblastos. Un anillo de miofibroblastos se
desplaza hacia dentro desde los bordes de la herida. Aunque las fuerzas contráctiles al
principio son iguales, la forma del marco es la que predice la velocidad del cierre de la
herida (fig. 3-13). Las heridas longitudinales estrechas se contraen rápidamente; las heridas
cuadradas o rectangulares, cuyos bordes no están próximos, progresan de forma más
moderada; y las heridas circulares se contraen más lentamente.
Si la contracción de la herida es incontrolada, puede provocar la formación de
contracturas. Las contracturas son situaciones en las que hay una gran resistencia al
estiramiento pasivo y pueden ser el resultado de una fibrosis en los tejidos que rodean una
articulación. Las contracturas también pueden producirse por adherencias, acortamiento
muscular o lesión tisular.
Cuando la lesión inicial provoca una pérdida mínima de tejido y una mínima
contaminación bacteriana, la herida se puede cerrar con suturas y, por tanto, puede curar sin
contracción de la misma. Esto se conoce como curación por primera intención (también
denominada unión primaria) (fig. 3-14). Cuando la lesión inicial provoca una pérdida
significativa de tejido o contaminación bacteriana, la herida tiene que experimentar
previamente el proceso de contracción para cerrarse; esto se conoce como curación por
segunda intención (o unión indirecta). La aproximación más tardía de los bordes de una
herida con suturas o con la aplicación de grapas cutáneas puede reducir la contracción de la
herida y se denomina curación por primera intención retardada. Para reducir al mínimo la
contracción, se pueden aplicar injertos en la fase inflamatoria inicial, antes de que comience
el proceso de contracción.
Cuando el tejido cicatricial madura, desarrolla terminaciones nerviosas sensibles a la
presión y a la tensión para proteger al sistema inmaduro de vasos, el cual es muy débil y
puede sangrar fácilmente ante cualquier lesión. Durante la fase de proliferación, la cicatriz es
roja y abultada por el aumento de vascularización y de líquido, por la inervación de la zona
lesionada y por la relativa inmadurez del tejido. Este tejido puede lesionarse fácilmente y es
muy sensible a la tensión y a la presión.
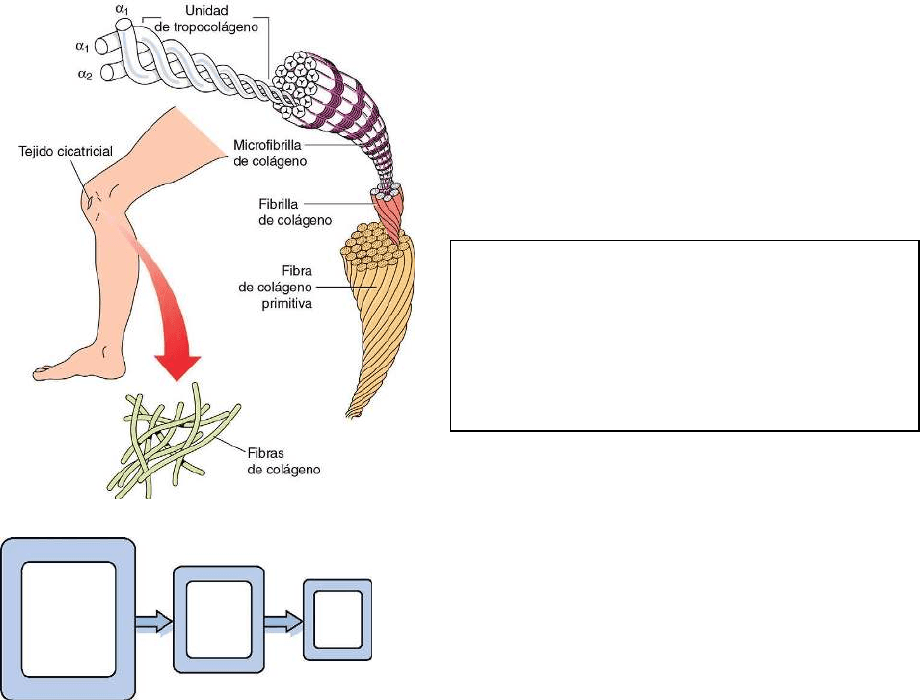
FIG 3-13 Ilustración de la teoría del «marco de fotos» para la contracción de la herida.
Neovascularización
La neovascularización, desarrollo de un nuevo sistema de aporte sanguíneo a la zona
lesionada, se produce como resultado de la angiogénesis, el crecimiento de nuevos vasos
sanguíneos. No se puede producir curación sin angiogénesis. Estos vasos nuevos son
necesarios para aportar oxígeno y nutrientes a la zona lesionada. Se piensa que los
macrófagos son los que dan la señal para iniciar la neovascularización mediante la
liberación de factores de crecimiento. La angiogénesis puede producirse por uno de tres
mecanismos diferentes: generación de una nueva red vascular, anastomosis de los vasos
preexistentes o acoplamiento de los vasos en la zona lesionada.
Los vasos de la periferia de la herida desarrollan pequeñas yemas que crecen hacia el
interior de la herida. Estos crecimientos externos finalmente entran en contacto y se unen
con otras yemas arteriales o venulares para formar un anillo capilar. Estos vasos rellenan la
zona lesionada confiriéndole un aspecto de rosa a rojo brillante. Cuando la herida se cura,
muchos de estos anillos capilares dejan de funcionar y se retraen, dando a la cicatriz un
aspecto más blanquecino que el de los tejidos adyacentes. Al principio, las paredes de estos
capilares son delgadas, haciéndolos susceptibles a las lesiones. Por tanto, en esta fase la
inmovilización puede ayudar a proteger estos vasos y permite un mayor crecimiento,
mientras que una excesiva movilización precoz puede producir microhemorragias y
aumentar la probabilidad de infección.
FIG 3-12 Diagrama que representa una unidad
de tropocolágeno uniéndose con otras para
formar filamentos de colágeno y finalmente
fibras de colágeno
FASE DE MADURACIÓN (DÍA 9 EN ADELANTE)
Cuando ya se ha realizado la transición de la fase de proliferación a la de maduración, se
producen cambios en la forma, el tamaño y la consistencia del tejido cicatricial. La fase de
maduración es la fase más larga en el proceso de curación. Puede persistir incluso hasta un
año después de haberse producido la lesión inicial. Durante este tiempo, el número de
fibroblastos, macrófagos, miofibroblastos y capilares desciende, así como también se reduce
el con- tenido de agua. La cicatriz adquiere una apariencia más blanquecina según el
colágeno va madurando y la vascularización va disminuyendo. El objetivo final de esta fase
es la restauración de la principal función del tejido lesionado.
Hay varios factores que determinan la tasa de maduración y de las características físicas
definitivas de la cicatriz. Éstas incluyen la orientación de las fibras y el equilibrio entre la
síntesis y la lisis de colágeno.
A lo largo de la fase de maduración, la síntesis y la lisis del colágeno se va produciendo
de forma equilibrada. La estimulación hormonal que se produce como resultado de la
inflamación produce un aumento de la destrucción del colá- geno por acción de la
colagenasa. La colagenasa procede de los leucocitos polimorfonucleares, del epitelio
migratorio y del lecho de tejido de granulación. La colagenasa es capaz de romper las
fuertes uniones de las moléculas de tropocolágeno, haciéndolo soluble. A continuación, se
excreta como un producto de desecho. Aunque la colagenasa es más activa en la zona de
lesión propiamente dicha, su efecto también puede notarse, en mayor grado, en zonas
adyacentes a la lesión. Por tanto, se produce una remodelación mediante un proceso de
renovación de colágeno.
El colágeno, una glucoproteína, proporciona el entramado extracelular para todos los
microorganismos multicelulares. Aunque se han identificado más de 27 tipos de colágeno, la
siguiente discusión se limita a los tipos I, II y III (tabla 3-4). Todas las moléculas de
colágeno están constituidas por tres cadenas polipeptídicas separadas enlazadas fuertemente
entre ellas en una triple hélice trenzada a la izquierda. El colágeno tipo I es el principal tipo
de colágeno que encontramos en el hueso, la piel y el tendón, y es el que predomina en las
cicatrices maduras. El colágeno tipo II es el que predomina en el cartílago. El colágeno tipo
III se encuentra en el tracto gastrointestinal, el útero y los vasos sanguíneos en el adulto.
También es el primer colágeno que se deposita durante el proceso de curación Durante la
fase de maduración, el colágeno que se sintetiza y se deposita es fundamentalmente tipo I. El
equilibrio entre la síntesis y la lisis generalmente es ligeramente favorable a la síntesis.
Como el colágeno tipo I es más resistente que el colágeno tipo III que se ha depositado en
la fase de proliferación, la consistencia aumenta más que la masa. Si la tasa de producción
de colágeno es mucho mayor que la tasa de lisis, se puede producir un queloide o cicatriz
hipertrófica. Los queloides y las cicatrices hipertróficas son el resultado de un depósito
excesivo de colágeno causado por una inhibición de la lisis. Se piensa que esta inhibición de
la lisis está provocada por un defecto genético. Los queloides se extienden más allá de los
límites de una lesión e invaden tejido circundante, mientras que las cicatrices hipertróficas,
aunque estén abultadas, se limitan al interior de los márgenes de la herida original. El
tratamiento de las cicatrices queloides con cirugía, fármacos, presión y radiación ofrece sólo
resultados limitados.
TABLA 3-4
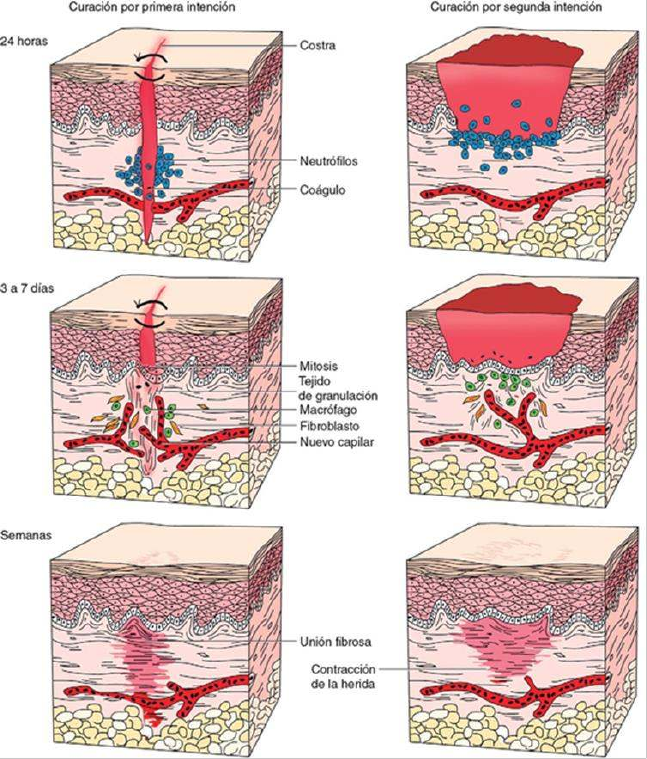
TABLA 3-4 Tipos de colágeno
Tipo Distribución
I Forma más abundante de colágeno: piel, hueso, tendones y la mayoría de los
órganos
II Principal colágeno del cartílago y del humor vítreo
III Abunda en vasos sanguíneos, útero y piel
IV Todas las membranas basales
V Componente secundario de la mayoría de los tejidos intersticiales
VI Abunda en la mayoría de los tejidos intersticiales
VII Unión dermoepidérmica
VIII Endotelio
IX Cartílago
X Cartílago
La síntesis de colágeno es dependiente del oxígeno, mientras que la lisis no lo es. Por
tanto, cuando los niveles de oxígeno son bajos, el proceso de maduración se inclina hacia la
lisis, lo que provoca una cicatriz más blanda y menos consistente. Las cicatrices
hipertróficas pueden tratarse con presión prolongada, lo que provoca una reducción del
oxígeno, induciendo a su vez un descenso en la síntesis neta de colágeno, mientras que se
mantiene la tasa de lisis. Esta es una de las bases para el empleo de prendas de presión en el
tratamiento de pacientes que padecen quemaduras y para la utilización de elastómeros en el
tratamiento de cicatrices en la terapia manual. Finalmente, el equilibrio se alcanza cuando la
cicatriz se aplana y se
aproxima al tejido normal.
La síntesis y la lisis del
colágeno pueden durar
desde 12 hasta 24 meses
después de una lesión. La
elevada tasa de reposición
de colágeno durante este
período puede considerarse
tanto beneficiosa como
perjudicial. Mientras que el
tejido cicatricial aparece de
un color más rojizo que los
tejidos de alrededor, la
remodelación se está
produciendo todavía.
Aunque durante esta fase
una articulación o un tejido
pueden perder movilidad de
forma rápida, dicha pérdida
de movilidad puede todavía
ser reversible con una
intervención adecuada.
La estructura física de las
fibras de colágeno es, en
gran parte, responsable de la
Este documento contiene más páginas...
Descargar Completo
INFLAMACION Y REPARACION DE LOS TEJIDOS (IMPRESO).pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.