
1
GENERALIDADES DE LAS TÉCNICAS
UTILIZADAS EN HISTOLOGÍA / 1
PREPARACIÓN DEL TEJIDO / 2
Tinción con hemaxotilina y eosina con fijación
en formalina / 2
Otros fijadores / 2
Otras técnicas de tinción / 3
HISTOQUÍMICA Y CITOQUÍMICA / 3
Composición química de las muestras
histológicas / 3
Fundamentos químicos de la tinción / 5
Digestión enzimática / 7
Histoquímica enzimática / 7
Inmunocitoquímica / 8
Técnicas de hibridación / 10
Autorradiografía / 12
MICROSCOPÍA / 12
Microscopía óptica / 12
Examen de un preparado histológico en el
microscopio óptico / 13
Otros sistemas ópticos / 16
Microscopía electrónica / 18
Microscopía de fuerza atómica / 21
Microscopía virtual / 22
Cuadro 1-1 Correlación clínica: biopsias por
congelación / 4
Cuadro 1-2 Consideraciones funcionales:
microespectrofotometría de Feulgen / 7
Cuadro 1-3 Correlación clínica: anticuerpos
monoclonales en medicina / 9
Cuadro 1-4 Consideraciones funcionales: uso
correcto del microscopio óptico / 15
HISTOLOGÍA 101. Puntos esenciales / 23
GENERALIDADES DE LAS
TÉCNICAS UTILIZADAS EN
HISTOLOGÍA
El objetivo de un curso de histología es conducir al estu-
diante a comprender la microanatomía de las células, teji-
dos y órganos y a correlacionar la estructura con la función.
Histología [Gr., ἱστός, histos = tejidos; λογíα, logía = ciencia],
también llamada
anatomía microscópica, es el estudio cientí-
co de las estructuras microscópicas de los tejidos y órganos del
cuerpo. La histología moderna no es sólo una ciencia descrip-
tiva sino que también incluye muchos aspectos de la biología
molecular y celular, que ayudan a describir la organización y
función celular. Las técnicas utilizadas por los histólogos son
diversas en extremo. La mayor parte de los contenidos de un
curso de histología se puede formular en términos de la mi-
croscopia óptica. En la actualidad, los estudiantes en los labo-
ratorios de histología utilizan ya sea
microscopios ópticos o,
con mayor frecuencia,
microscopía virtual, que representa
métodos para examinar muestras microscópicas en la pantalla
de un ordenador o dispositivo móvil. Anteriormente, se reali-
zaba una interpretación más detallada de la microanatomía con
un microscopio electrónico (ME) – tanto con el microscopio
electrónico de transmisión (MET)
como con el microsco-
pio electrónico de barrido (MEB)
. Hoy, el microscopio de
fuerza atómica (MFA)
también puede proporcionar imágenes
de alta resolución que son comparables o incluso mejores que
las obtenidas a través del MET. Tanto el ME como el MFA,
debido a su mayor resolución y más útil aumento, suelen ser el
último paso en la adquisición de datos a partir de muchas téc-
nicas auxiliares de la biología celular y molecular. Estas técnicas
auxiliares incluyen:
•
histoquímica y citoquímica,
•
inmunoquímica y técnicas de hibridación,
•
autorradiografía,
•
cultivo de tejido y órganos,
•
separación de células y orgánulos por centrifugación di-
ferencial,
•
microscopios y técnicas microscópicas especializadas.
Es posible que los estudiantes se sientan distantes de estas
técnicas y procedimientos experimentales debido a que no
suele estar contemplada una experiencia directa con ellos en
los programas actuales de la asignatura. Sin embargo, es im-
1
Técnicas

2
CAPÍTULO 1 Técnicas PREPARACIÓN DEL TEJIDO
portante saber algo acerca de los procedimientos y los datos
que proveen. Este capítulo proporciona un estudio de técnicas
y una explicación de cómo los datos aportados por éstas pueden
ayudar al estudiante a comprender mejor la función de las célu-
las, tejidos y órganos.
Un problema que enfrentan los estudiantes de histología
es comprender la índole de la imagen bidimensional de un
preparado histológico de una micrografía electrónica y cómo
la imagen se relaciona con la estructura tridimensional de la
cual proviene. Para salvar esta brecha conceptual, primero de-
bemos presentar una descripción de las técnicas mediante las
cuales se producen los preparados y las muestras de la micros-
copia electrónica.
PREPARACIÓN DEL TEJIDO
Tinción con hematoxilina y eosina con fijación
en formalina
El corte de rutina teñido con hematoxilina y eosina es la
muestra que se utiliza con mayor frecuencia.
El grupo de preparados que se entrega a cada estudiante junto
con el microscopio óptico contiene por lo general muestras
jadas en formalina, incluidas en parana y coloreadas con
hematoxilina y eosina (H&E). Cas todas las fotomicrografías
ópticas en las secciones del atlas de esta obra son de prepara-
dos de estos mismos grupos. Además, la mayor parte de las
fotomicrografías utilizadas para ilustrar tejidos y órganos en
la cátedra de histología y en conferencias se obtienen de estos
preparados. A veces se utilizan otras técnicas de tinción para
mostrar componentes especícos de las células y los tejidos;
varias de estas técnicas se describen más adelante.
El primer paso en la preparación de una muestra de tejido
u órgano es la jación para conservar la estructura.
La fijación, obtenida en general mediante una sustancia quí-
mica o una mezcla de sustancias químicas, conserva de forma
permanente la estructura del tejido para tratamientos poste-
riores. Las muestras deben sumergirse en el jador inmedia-
tamente después de extraerse del organismo. La jación se
utiliza para:
•
abolir el metabolismo celular,
•
impedir la degradación enzimática de las células y tejidos
por la autólisis (autodigestión),
•
destruir microorganismos patógenos tales como bacterias,
hongos o virus y
•
endurecer el tejido como resultado de la formación de
enlaces cruzados o de la desnaturalización de moléculas
proteicas.
El jador de uso más común es la
formalina, una solución
acuosa de formaldehído al 37 %, en diluciones variadas y en
combinación con otras sustancias químicas y amortiguadores
(buers). El formaldehído conserva la estructura general de la
célula y de los componentes extracelulares al reaccionar con
los grupos amino de las proteínas (con frecuencia los enlaces
cruzados de residuos de lisina). Debido a que el formalde-
hído no altera su estructura tridimensional de forma signi-
cativa, las proteínas mantienen su capacidad de reaccionar
con anticuerpos especícos. Esta propiedad es importante en
las técnicas de inmunocitoquímica (v. pág. 8). La solución co-
mercial estándar de formaldehído amortiguado con fosfatos
(pH 7) actúa con lentitud pero penetra bien en el tejido. Sin
embargo, dado que no reacciona con los lípidos, es un mal
jador de las membranas celulares.
En el segundo paso, la muestra se dispone para su inclu-
sión en parana con el n de permitir su corte.
Para examinar una muestra se requiere de su inltración con
un
medio de inclusión que permita realizar corte muy del-
gados, por lo general en el rango de 5 mm a 15 mm (1 micrón
[mm] equivale a una milésima parte de un milímetro [mm];
v. tabla 1-1). Después de la jación la muestra se
lava y se
deshidrata en una serie de soluciones alcohólicas de concen-
tración creciente hasta alcanzar alcohol al 100 %. En el paso
siguiente, el
aclarado, se utilizan solventes orgánicos tales
como el xileno o tolueno que son miscibles tanto en alcohol
como en
parafinas, para extraer el alcohol antes de la inltra-
ción de la muestra con la parana fundida.
Cuando la parana fundida se ha enfriado y endurecido,
se empareja para formar un bloque de tamaño adecuado. Este
bloque se coloca en una máquina cortadora especial, el
mi-
crótomo
que lo corta en rebanadas nas con una cuchilla de
acero. Los cortes obtenidos se montan sobre portaobjetos de
vidrio utilizando un
medio de montaje (pineno o resinas de
acrílico) como adhesivo.
En el tercer paso, la muestra se tiñe para permitir su examen.
Debido a que los cortes en parana son incoloros, la muestra
todavía no está lista para su examen bajo el microscopio óp-
tico. Para colorear o teñir los cortes histológicos, la parana
debe disolverse y extraerse, con xileno o tolueno y los tejidos
deben rehidratarse mediante el uso de una serie de soluciones
de alcohol de concentración decreciente. Después, el tejido
sobre el portaobjetos se tiñe con
hematoxilina en agua. De-
bido a que el colorante de contraste, la eosina, es más soluble
en alcohol que en agua, se vuelve a deshidratar la muestra a
través de una serie de soluciones alcohólicas de concentración
creciente y después se tiñe con
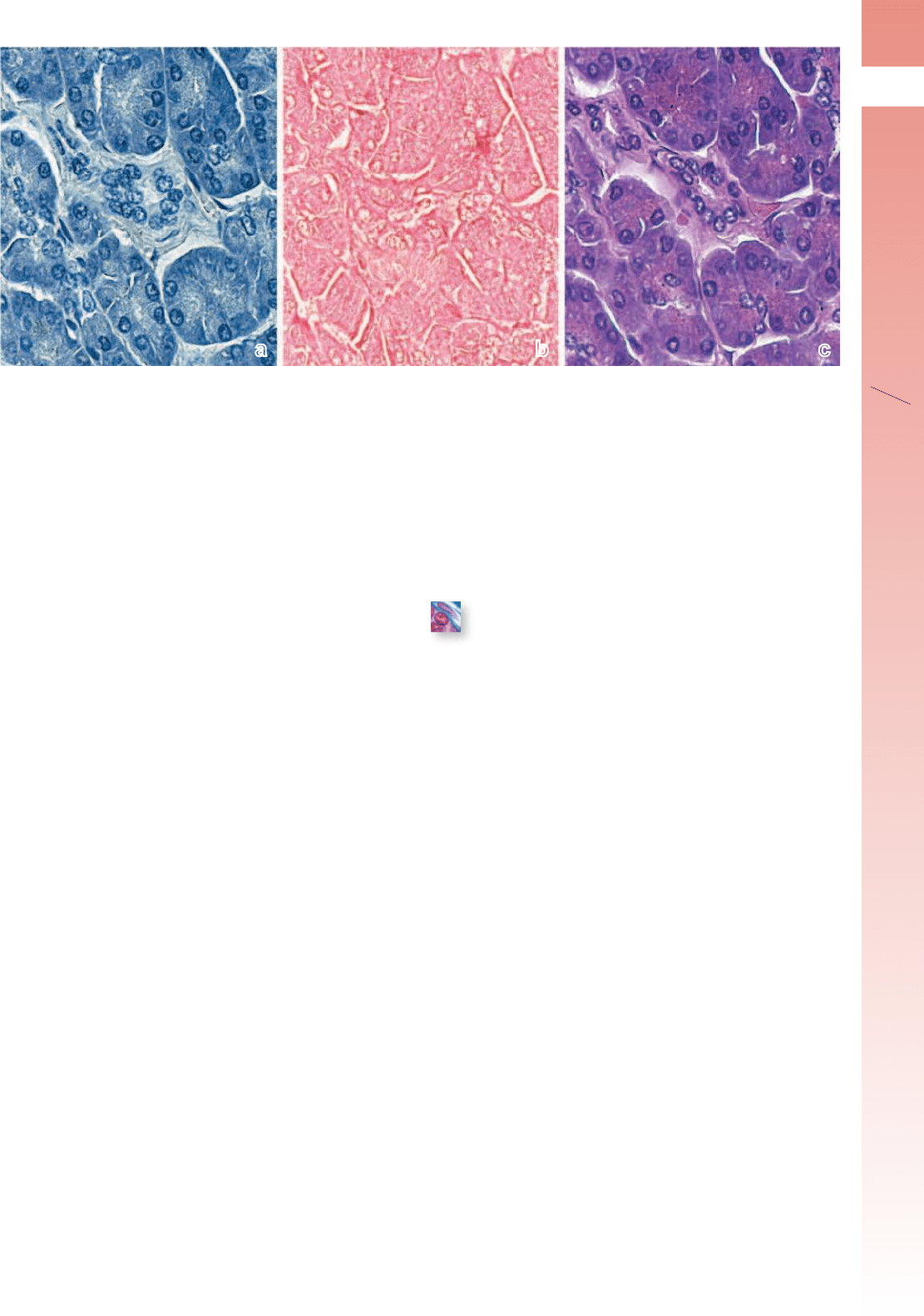
eosina en alcohol. En la gura
1-1 se muestran los resultados de la tinción con hematoxilina
sola, con eosina sola y con ambos colorantes. Después de la
tinción, la muestra se pasa por xileno o tolueno y se le coloca
un medio de montaje no acuoso antes de cubrirla con un cu-
breobjetos para obtener un preparado permanente.
Otros fijadores
La formalina no preserva todos los componentes de las cé-
lulas y los tejidos.
1 picómetro (pm)
5
0,01 angstroms (A)
1 angstrom
5
0,1 nanómetro (nm)
10 angstrom
5
1,0 nanómetro
1 nanómetro
5
1 000 picómetros
1 000 nanómetros
5 1,0 micrómetro (mm)
1 000 micrómetros
5
1,0 milímetro (mm)
TABLA 1-1 Equivalencias en las medidas de longitud
3
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
Si bien los corte teñidos con H&E de muestras jadas en
formalina son convenientes ya que muestran adecuadamente
las características estructurales generales, no son especícos
para dilucidar la composición química de los elementos ce-
lulares. Además, muchos componentes se pierden durante la
preparación de la muestra. Para retener estos componentes y
estructuras, se deben utilizar otras técnicas de jación. Por lo
general, estas técnicas se fundamentan en un conocimiento
sólido de la química involucrada. Por ejemplo, los alcoholes y
solventes orgánicos que se usan en preparados de rutina dilu-
yen los lípidos neutros.
Para conservar los lípidos neutros, como los de las células
adiposas, se deben utilizar cortes por congelación de tejido -
jado en formalina y colorantes que se disuelvan en grasa; para
conservar las estructuras de la membrana, se utilizan jadores
especiales con metales pesados, como permanganato y osmio,
que se unan a los fosfolípidos. El empleo de rutina de
te-
tróxido de osmio
como jador en la microscopia electrónica
es la razón principal del excelente estado de conservación de
las membranas en las fotomicrografías electrónicas.
Otras técnicas de tinción
La hematoxilina y la eosina se utilizan principalmente para
poner en evidencia las características estructurales.
A pesar de los méritos de la tinción con H&E, el procedi-
miento no permite ver de forma adecuada ciertos componen-
tes estructurales de los cortes histológicos tales como elastina,
bras reticulares, membranas basales y lípidos. Cuando se
desea estudiar estos componentes, se pueden utilizar otros
procedimientos de tinción, en su mayoría selectivos. Estos
procedimientos incluyen el uso de orceína y fucsina- resor-
cina para el material elástico y la impregnación argéntica para
bras reticulares y las membranas basales. Pese a que no siem-
pre se comprende el fundamento químico de muchas técnicas
de tinción, estos procedimientos sirven. Es más importante
saber lo que el método permite observar que conocer su fun-
cionamiento.
HISTOQUÍMICA Y CITOQUÍMICA
Los procedimientos químicos especícos pueden proveer
información acerca de la función de las células y de los
componentes extracelulares de los tejidos.
Los procedimientos histoquímicos y citoquímicos pueden
tener su fundamento en la
unión específica de un colorante,
en el uso de
anticuerpos marcados con un colorante fluo-
rescente
con un componente celular en particular o en la
actividad enzimática inherente de un elemento constitutivo
de la célula.
Además, muchas macromoléculas presentes en las células
pueden detectarse mediante la
autorradiografía, en la cual
precursores moleculares marcados radiactivamente se incor-
poran en las células y en los tejidos antes de la jación. Mu-
chos de estos procedimientos pueden utilizarse en preparados
tanto para la microscopia óptica como para la microscopia
electrónica.
Antes de comentar sobre la química de las tinciones de ru-
tina y de las técnicas histoquímicas y citoquímicas, es conve-
niente describir brevemente la índole de un corte histológico
de rutina.
Composición química de las muestras
histológicas
La composición química de un tejido listo para una tinción
de rutina diere de la del tejido vivo.
Los componentes que perduran después de la jación son prin-
cipalmente moléculas grandes que no se disuelven con facili-
dad, en especial después de aplicar el jador. Estas moléculas,
en particular las que reaccionan con otras moléculas semejantes
abc
FIGURA 1-1 ▲ Coloración con Hematoxilina y eosina (H&E). Esta serie de muestras de cortes de páncreas seriados (contiguos) demues-
tran el efecto de la hematoxilina y la eosina utilizadas solas o combinadas.
a. En esta fotomicrografía se ve una tinción con hematoxilina sola. Si bien hay
una tinción general de la muestra, aquellos componentes y estructuras con gran afinidad por el colorante se tiñen con una intensidad mucho mayor,
por ejemplo, el ADN nuclear y el ARN citoplasmático.
b. En esta fotomicrografía, la eosina, colorante de contraste, consigue una tinción general de los
tejidos al usarse sola. Sin embargo, debe notarse que los núcleos son menos conspicuos que en la muestra teñida sólo con hematoxilina. Después de
que la muestra se colorea con hematoxilina y que se le prepara para la tinción con eosina en solución alcohólica, la hematoxilina que no estaba unida
con firmeza se pierde, y entonces la eosina tiñe esos componentes para los que tiene gran afinidad.
c. Esta fotomicrografía muestra el efecto de la
tinción con ambos colorantes (H&E). 480 Χ.
4
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
CUADRO 1-1
Correlación clínica: biopsias por congelación
A veces, el patólogo necesita valorar de inmediato el tejido
obtenido durante la cirugía, sobre todo cuando el diagnóstico
patológico instantáneo puede determinar el paso siguiente
en la cirugía. Hay varias indicaciones para realizar dicha valo-
ración, que se conoce como biopsia por congelación. Por
lo general, un cirujano en el quirófano solicita una biopsia por
congelación cuando se carece de un diagnóstico preopera-
torio o cuando hay que identificar hallazgos intraoperatorios
inesperados. Además, el cirujano puede querer saber si se
ha extirpado toda la masa patológica dentro del límite de los
tejidos sanos y si el borde de la resección quirúrgica está libre
de tejido enfermo. Las biopsias por congelación también se
realizan en combinación con otros procedimientos como la
endoscopia o la biopsia con aguja fina para confirmar si el ma-
terial obtenido se podrá utilizar en otros estudios patológicos.
Para realizar una biopsia por congelación se siguen tres
pasos principales:
• Congelación del tejido. Se congelan muestras de tejido de
tamaño pequeño mediante el uso de dióxido de carbono
sólido o mediante inmersión en un líquido frío (isopen-
tano) a una temperatura de –50 °C. El enfriamiento puede
lograrse en una cámara refrigeradora muy eficiente. La
congelación endurece el tejido y permite el corte con un
micrótomo.
• Corte del tejido congelado. El corte suele realizarse dentro
de un criostato, una cámara refrigerada que contiene un
micrótomo. Dado que el tejido está congelado, se puede
cortar en rebanadas muy finas (5 nm a 10 mm). Después
los cortes se montan sobre portaobjetos de vidrio.
• Tinción de los cortes. La tinción se realiza para diferenciar
los núcleos celulares del resto del tejido. Las tinciones de
uso más frecuente para las biopsias por congelación son
H&E, el azul de metileno (fig. C1-1.1) y tinción de PAS.
Todo el proceso de preparación y valoración de las biopsias
por congelación puede tardar en completarse en un mínimo
de 10 m. El tiempo total para obtener resultados depende en
gran medida del tiempo de transporte del tejido desde el qui-
rófano hasta el laboratorio de patología, de la técnica patoló-
gica utilizada y de la experiencia del patólogo. Los resultados
se comunican directamente al cirujano que está esperando en
el quirófano.
a
b
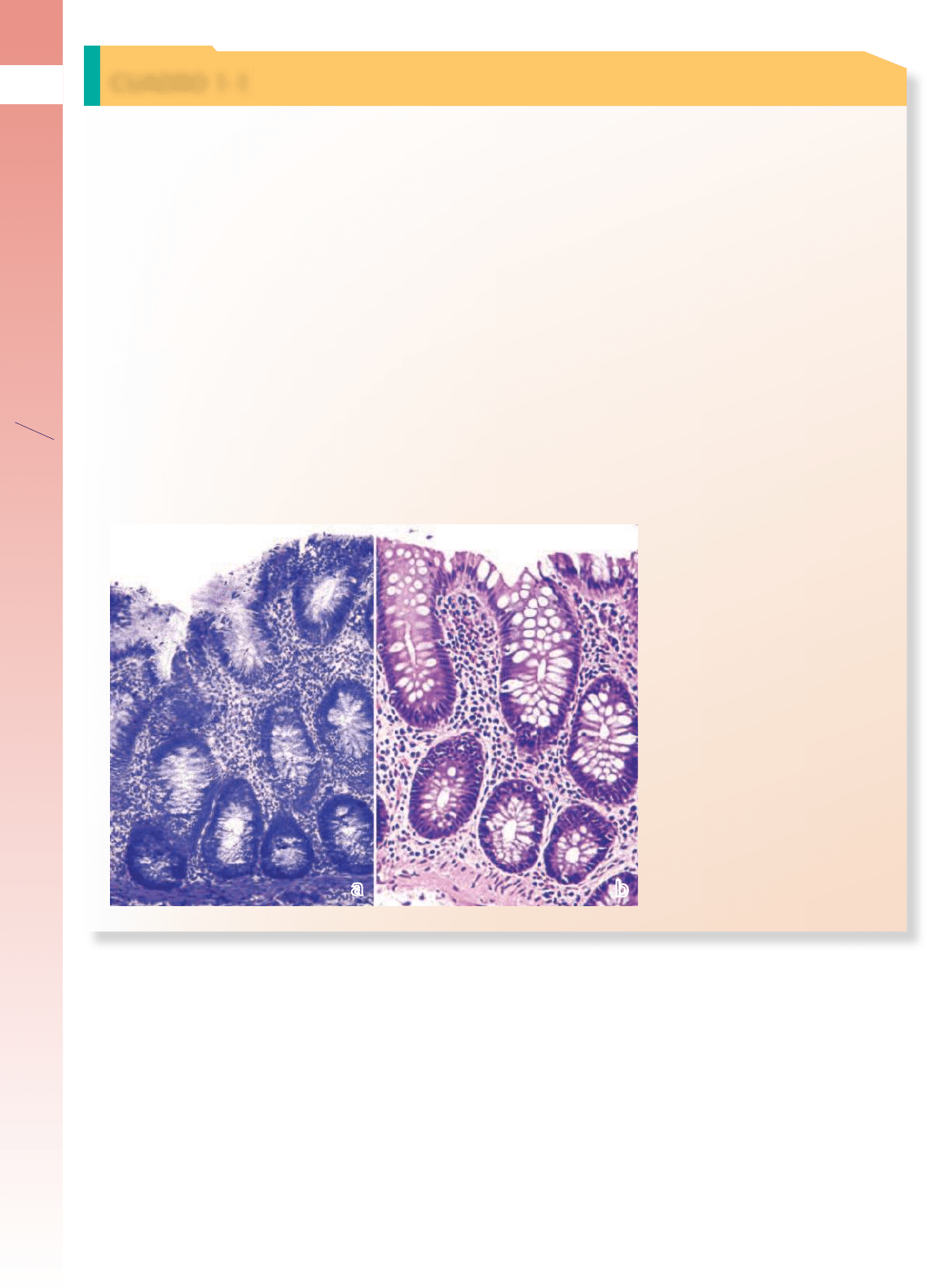
FIGURA F1-1.1 ▲ Valoración
de una muestra obtenida durante
la cirugía y preparada mediante la
técnica de congelación
. a. En esta fo-
tomicrografía se ve una muestra obtenida
del intestino grueso que se preparó me-
diante la técnica de congelación y se tiñó
con azul de metileno. 160 Χ. b. Parte de la
muestra se fijó en formalina y se procesó
con una técnica de rutina que comprende
la coloración con H&E. El examen de la
biopsia por congelación permitió com-
probar que el tejido era normal. El diag-
nóstico se confirmó más tarde mediante
el examen del preparado de rutina teñido
con H&E. 180 Χ. (Gentileza del Dr. Daniel
W. Visscher).
para formar complejos macromoleculares, son las que suelen
conservarse en un corte histológico. Los siguientes son ejem-
plos de complejos macromoleculares grandes:
•
nucleoproteínas, formadas a partir de ácidos nucleicos
unidos a proteínas;
•
proteínas intracelulares del citoesqueleto, en complejo
con proteínas asociadas;
•
proteínas extracelulares en grandes aglomeraciones inso-
lubles, unidas a moléculas similares mediante enlaces cru-
zados de moléculas vecinas, como ocurre en las formación
de las bras de colágeno;
•
complejos de fosfolípidos y proteínas (o hidratos de
carbono) en las membranas.
Estas moléculas constituyen la estructura de las células y los
tejidos; es decir, son los elementos morfógenos hísticos. Son
la base de la organización del tejido que se observa con el
microscopio.
En muchos casos, un elemento estructural es al mismo
tiempo una unidad funcional. Por ejemplo, en el caso de las
proteínas que forman los lamentos contráctiles de las células
musculares, ellos son los componentes estructurales visibles y
además participan en el proceso de contracción. El ARN del
citoplasma aparece como parte de un componente estructural
(p. ej., el ergastoplasma de las células secretoras, sustancia de
Nissl de las neuronas) y es también el participante activo en
las síntesis de proteínas.
5
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
Muchos de los componentes de los tejidos se pierden du-
rante la preparación de rutina de los cortes teñidos con
H&E.
A pesar de que los ácidos nucleicos, proteínas y fosfolípidos
en su mayoría se conservan en los cortes de tejidos, también
muchos se pierden. Las proteínas pequeñas y los ácidos nu-
cleicos pequeños, como los ARN de transferencia, en general
se pierden durante la preparación del tejido. Como se men-
cionó antes, los lípidos neutros suelen disolverse mediante
el uso de solventes orgánicos utilizados en la preparación de
tejidos. También pueden perderse otras moléculas grandes,
por ejemplo, al ser hidrolizadas como consecuencia del pH
desfavorable de las soluciones jadoras. Algunos ejemplos de
moléculas que se pierden durante la jación de rutina en ja-
dores acuosos son:
•
glucógeno (hidrato de carbono intracelular común en el
hígado y las células musculares)
•
proteoglucanos y glucosaminoglucanos (hidratos de
carbono complejos extracelulares que se encuentran en el
tejido conjuntivo).
Sin embargo, estas moléculas pueden conservarse utili-
zando jadores no acuosos para el glucógeno o añadiendo
agentes ligadores especiales a la solución jadora que preser-
ven las moléculas extracelulares que contienen hidratos de
carbono.
Los componentes solubles, iones y moléculas pequeñas
también se pierden durante la preparación de muestras de
parana.
Metabolitos intermedios, glucosa, sodio, cloro y sustancias
similares se pierden durante la preparación de muestras de ru-
tina en parana teñidas con H&E. Muchas de estas sustancias
pueden estudiarse en preparados especiales, en ocasiones con
una pérdida considerable de la integridad estructural. Estos
iones y pequeñas moléculas solubles no constituyen los ele-
mentos morfógenos de un tejido; participan en procesos de
síntesis o reacciones celulares. Cuando pueden conservarse y
detectarse mediante técnicas especícas, aportan información
muy valiosa sobre el metabolismo celular, transporte activo
y otros procesos vitales de las células. El agua, una molécula
muy versátil, participa en estas reacciones y procesos y con-
tribuye a estabilizar la estructura macromolecular a través de
enlaces de hidrógeno.
Fundamentos químicos de la tinción
Colorantes ácidos y básicos
La hematoxilina y la eosina (H&E) son los colorantes de uso
más frecuente en la histología.
Un
colorante ácido, como la eosina, tiene una carga neta
negativa en su parte coloreada y se la describe con la fórmula
general [Na
+
anilina
–
].
Un
colorante básico tiene una carga neta positiva en
su parte coloreada y se lo describe con la fórmula general
[anilina
+
Cl
–
].
La
hematoxilina no es exactamente un colorante básico
pero tiene propiedades muy semejantes a las de los coloran-
tes básicos. El color de una anilina no está relacionado con
el hecho de que sea ácida o básica, como lo demuestran los
ejemplos de colorantes ácidos o básico que se presentan en la
tabla 1-2.
Los colorantes básicos reaccionan con los componentes
aniónicos de las células y de los tejidos (componentes que
tienen una carga neta negativa).
Los
componentes aniónicos incluyen los grupos fosfato de
los ácidos nucleicos, los grupos sulfato de los glucosamino-
glucanos y los grupos carboxilo de las proteínas. La capaci-
dad de estos grupos aniónicos de reaccionar con una anilina
o colorante básico se denomina
basofilia [gr., anidad por
lo básico]. Los componentes del tejido que se tiñen con la
hematoxilina también exhiben basolia.
La reacción de los grupos aniónicos varía según el pH. Así:
•
Con un pH alto (cerca de 10) los tres grupos se ionizan y
quedan disponibles para la reacción con el colorante bá-
sico mediante uniones electroestáticas.
•
Con un pH ligeramente ácido a neutro (5 a 7) se ionizan los
grupos fosfato y sulfato y quedan disponibles para reac-
cionar con la anilina básica a través de uniones electroes-
táticas.
•
Con un pH bajo (inferior a 4) solo se mantienen ionizados
los grupos sulfato y reaccionan con colorantes básicos.
En consecuencia, la tinción con colorantes básicos en un
pH determinado se puede utilizar para centrar el estudio en
grupos aniónicos especícos; debido a que estos grupos pre-
dominan en ciertas macromoléculas, la tinción sirve, enton-
ces, como un indicador de estas macromoléculas.
Como ya se mencionó, la
hematoxilina no es un colorante
básico en sentido estricto. Se usa con un
mordiente (es decir,
un intermediario entre el componente del tejido y la anilina).
El mordiente hace que la tinción se parezca a un colorante
básico. La unión en el complejo
tejido-mordiente-hematoxi-
lina
no es un simple enlace electrostático; cuando los cortes se
colocan en agua, la hematoxilina no se disocia del tejido. La
hematoxilina se presta para aquellos procedimientos tintoria-
les en los que a ella le siguen soluciones acuosas de coloran-
tes ácidos. Los colorantes básicos verdaderos, a diferencia de
la hematoxilina, no suelen usarse en secuencias en las que la
Colorante Color
Colorantes básicos
Verde de metilo Verde
Azul de metileno Azul
Pironina G Rojo
Azul de toluidina Azul
Colorantes ácidos
Fuscina ácida Rojo
Azul de anilina Azul
Eosina Rojo
Naranja G Naranja
TABLA 1-2 Algunos colorantes ácidos y básicos

6
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
Metacromasia
Ciertos colorantes básicos reaccionan con los componen-
tes del tejido que cambian su color normal de azul a rojo
o púrpura; este cambio de la absorbancia se llama meta-
cromasia.
El mecanismo subyacente para la
metacromasia es la pre-
sencia de
polianiones en el tejido. Cuando estos tejidos se
tiñen con una solución colorante básica concentrada, como
el
azul de toluidina, las moléculas de colorante están lo su-
cientemente cerca como para formar aglomerados diméricos
y poliméricos. Las propiedades de absorción de estas aglome-
raciones dieren de las de las moléculas de colorante indivi-
duales no aglomeradas.
Las estructuras celulares y tisulares que tienen altas con-
centraciones de grupos sulfato y fosfato ionizados, como la
sustancia fundamental del cartílago ionizado, los gránulos
de heparina de los mastocitos y el retículo endoplasmático
rugoso de los plasmocitos, exhiben metacromasia. Por tanto,
el azul de toluidina aparecerá de púrpura a rojo cuando tiña
estos componentes.
Grupos aldehído y el reactivo de Schiff
La capacidad de la fucsina básica decolorada (reactivo de
Schi) para reaccionar con los grupos aldehído trae como
resultado la aparición de un color rojo distintivo y es la base
de las reacciones de ácido peryódico-reactivo de Schi y de
Feulgen.
La reacción de
ácido peryódico-reactivo de Schiff (PAS) tiñe
hidratos de carbono y macromoléculas con abundancia de
ellos. Se utiliza para demostrar glucógeno en las células, moco
en diversas células y tejidos, la membrana basal subyacente
epitelios y bras reticulares en el tejido conjuntivo. El reactivo
de Schi también se utiliza en la
reacción de Feulgen, que se
basa en una hidrólisis débil con ácido clorhídrico para teñir
el ADN.
anilina básica es seguida por una anilina ácida. Entonces, la
anilina básica tiende a disociarse del tejido durante los lavados
en soluciones acuosas entre las dos soluciones de anilina.
Los colorantes ácidos reaccionan con los grupos catiónicos
en las células y los tejidos; en particular, con los grupos
amino ionizados de las proteínas.
La reacción de los
grupos catiónicos con un colorante ácido
recibe el nombre de
acidofilia [gr., anidad por lo ácido]. Las
reacciones de los componentes celulares y tisulares con los
colorantes acídicos no son tan especícas ni tan precisas como
las reacciones con los colorantes básicos.
Si bien el enlace electrostático es el factor principal en la
unión primaria de un colorante ácido con el tejido, no es el
único; debido a ello, los colorantes ácidos a veces se utilizan
combinados para teñir selectivamente distintos componentes
de los teñidos. Por ejemplo, en la
técnica de teñido de Ma-
llory
, se utilizan tres colorantes ácidos: anilina azul, fuscina
ácida y naranja G. Estos colorantes tiñen en forma selectiva el
colágeno, el citoplasma en general y los eritrocitos, respectiva-
mente. La fuscina ácida también tiñe los núcleos.
En otras técnicas con anilinas ácidas múltiples, la hema-
toxilina se utiliza para teñir primero los núcleos y luego se
aplican los colorantes ácidos para teñir selectivamente el ci-
toplasma y las bras extracelulares. La tinción selectiva de los
componentes del tejido por los colorantes ácidos es atribui-
ble a factores relativos, como el tamaño y el grado de acu-
mulación de las moléculas del colorante y la permeabilidad y
“densidad” del tejido.
Los colorantes básicos también se pueden utilizar en com-
binación o secuencialmente (p. ej., verde de metilo y pironina
para estudiar la síntesis y secreción de proteínas), pero estas
combinaciones no son de uso tan difundido como las de los
colorantes ácidos.
Una cantidad limitada de sustancias dentro de las células y
en la matriz extracelular presenta basolia.
Entre estas sustancias se incluyen:
•
heterocromatina y nucléolos del núcleo (principalmente
por los grupos fosfato ionizados en los ácidos nucleicos de
ambos),
•
componentes citoplasmáticos como el ergastoplasma
(también por los grupos fosfato ionizados en el ARN ri-
bosómico) y
•
materiales extracelulares como los hidratos de carbono
complejos de la matriz del cartílago (por los grupos sulfato
ionizados).
La tinción con colorantes ácidos es menos especíca, pero
más sustancias dentro de las células y en la matriz extrace-
lular presentan acidolia.
Entre estas sustancias se incluyen::
•
la mayor parte de los
filamentos citoplasmáticos, en es-
pecial los de las células musculares,
•
la mayoría de los
componentes membranosos intrace-
lulares
y la mayor parte del citoplasma no especializado, y
•
la mayor parte de las fibras extracelulares (principal-
mente a causa de grupos amino ionizados).
T
T
T
T
T
T
T
C
C
BC
BC
FIGURA 1-2 ▲ Fotomicrografía de tejido renal teñido con
la técnica de PAS.
Esta técnica histoquímica sirve para demostrar y lo-
calizar hidratos de carbono y macromoléculas ricas en hidratos de car-
bono. Las membranas basales son PAS positivas como lo demuestra la
tinción púrpura de estos sitios. Los túbulos renales (T) se encuentran bien
delineados por la membrana basal teñida que los rodea. Los capilares glo-
merulares (C) y el epitelio de la cápsula de Bowman (BC) también poseen
membranas basales de PAS positivas. La muestra se contratiñó con hema-
toxilina para visualizar los núcleos celulares. 320 X.

7
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
El material intracelular que se tiñe con la reacción de PAS se
puede identicar como glucógeno por el tratamiento previo
de los cortes con diastasa o amilasa. La falta de tinción des-
pués de este tratamiento identica positivamente el material
teñido como glucógeno.
Del mismo modo, el pretratamiento de los cortes histo-
lógicos con desoxirribonucleasa (ADNasa) evitará la tinción
de Feulgen en esos cortes y el tratamiento de las muestras
de epitelios secretores de proteínas con ribonucleasa (RNasa)
suprimirá la tinción del ergastoplasma con colorantes básicos
Histoquímica enzimática
Las técnicas histoquímicas también se utilizan para identi-
car y localizar enzimas en células y tejidos.
Para localizar las enzimas en los cortes histológicos, debe te-
nerse un cuidado especial en la jación para preservar la ac-
tividad enzimática. Por lo general, la jación aldehídica leve
es el método preferido. En estos procedimientos se detecta
el producto de reacción de la actividad enzimática y no la
enzima propiamente dicha. En general, se usa un
reactivo de
captura,
ya sea un colorante o un metal pesado, para atrapar
o jar el producto de reacción de la enzima mediante preci-
pitación en el sitio de reacción. En una reacción típica para
detectar una enzima hidrolítica, el corte histológico se coloca
en una solución que contiene un sustrato (AB) y un agente
de captura (T) que precipitará uno de los productos de la
siguiente manera:
AB 1 T
enzima
AT 1 B
donde AT es el producto nal capturado y B es el sustrato
hidrolizado.
Mediante el uso de tales técnicas, se pudo correlacionar el
lisosoma, identicado por primera vez en estudios celulares
de centrifugación diferencial, con un componente vacuolar
visible en fotomicrografías electrónicas. En los tejidos some-
La reacción de PAS tiene como fundamento lo siguiente:
•
Los anillos hexosa de hidratos de carbono contienen car-
bonos contiguos, cada uno de los cuales lleva un grupo
hidroxilo (–OH).
•
Las hexosaminas de glucosaminoglucanos contienen car-
bonos contiguos, uno de las cuales lleva un grupo –OH,
mientras que el otro lleva un grupo amino (–NH2).
•
El ácido peryódico escinde la unión entre estos átomos de
carbono contiguos y forma grupos aldehído.
•
Estos grupos aldehído reaccionan con el reactivo de Schi
para dar un color púrpura distintivo.
La tinción PAS de la membrana basal (g. 1-2) y las bras
reticulares se basa en el contenido o asociación de proteo-
glucanos (hidratos de carbono complejos asociados con un
núcleo de proteína). Esta tinción es una alternativa a los mé-
todos de impregnación argéntica, que también se basan en la
reacción con las moléculas de sacáridos en los proteoglucanos.
La reacción de Feulgen se basa en la separación de purinas
de la desoxirribosa del ADN mediante una hidrólisis ácida
débil; el anillo de los sacáridos se abre a continuación y se
forman grupos aldehído. Una vez más, los grupos aldehído
recién formados reaccionan con el reactivo de Schi para dar
el color púrpura característico. La reacción del reactivo de
Schi con el ADN es
estequiométrica, lo que signica que
el producto de esta reacción es medible y es proporcional a la
cantidad de ADN. Por consiguiente, se puede utilizar en los
métodos espectrofotométricos para cuanticar la cantidad de
ADN en el núcleo de una célula. El ARN no se tiñe con el
reactivo de Schi porque carece de desoxirribosa.
Digestión enzimática
La digestión enzimática para un componente especíco
(como glucógeno, ADN o ARN), se puede utilizar para con-
rmar la identidad del material que se tiñe.
CUADRO 1-2
Consideraciones funcionales:
microespectrofotometría de Feulgen
La microespectrofotometría de Feulgen es una técnica
ideada para el estudio de los aumentos del ADN en las células
en desarrollo y para analizar la ploidía, es decir, la cantidad de
veces que está multiplicado el contenido normal del ADN en
una célula (se dice que una célula somática normal que no se
está dividiendo, es diploide; en cambio, los espermatozoides
o los óvulos son haploides). Dos técnicas, citometría está-
tica para cortes de tejidos y citometría de flujo para células
aisladas, se utilizan para cuantificar el ADN nuclear. La técnica
de citometría estática de cortes de tumores teñidos con el
método de Feulgen se vale de la microespectrofotometría
acoplada a un sistema de visualización digital para cuantificar
la absorción de la luz con una longitud de onda de 560 nm
por parte de las células y de las aglomeraciones celulares. En
cambio, la técnica de citometría de flujo utiliza instrumentos
capaces de rastrear sólo células individuales que fluyen ante
un detector en un medio líquido. Esta técnica permite el aná-
lisis cuantitativo rápido de una célula individual sobre la base
de la medición de la luz fluorescente emitida.
En la actualidad, la microespectrofotometría de Feulgen se
utiliza para estudiar cambios en el contenido del ADN de las
células en división que se están diferenciando. También se uti-
liza en clínica para analizar la cantidad cromosómica anómala
(es decir, patrones de ploidía) en las células malignas. Se dice
que algunas células malignas que tienen un patrón mayorita-
riamente diploide, están bien diferenciadas; los tumores con
este tipo de células tienen un pronóstico mejor que los tumo-
res aneuploides (con múltiplos no enteros de la cantidad ha-
ploide de ADN) o tetraploides. La microespectrofotometría de
Feulgen ha sido de particular utilidad en los estudios de ade-
nocarcinomas (cánceres epiteliales), cáncer de mama, cáncer
de riñón, cáncer de colon y de otras partes del tubo digestivo,
cáncer de endometrio (mucosa del útero) y cáncer ovárico.
Es una de las herramientas más valiosas que los patólogos
utilizan para valorar el potencial metastásico de estos tumo-
res y para tomar decisiones de pronóstico o terapéuticas.

8
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
de la fosfatasa ácida). Entonces, el producto reactivo precipi-
tado puede observarse tanto con un microscopio óptico como
electrónico. Se han desarrollado procedimientos histoquími-
cos similares para demostrar la fosfatasa alcalina, la adenosina
trifosfatasa (ATPasa) de varios tipos (incluyendo el Na+ / K+
ATPasa que es la base enzimática de la bomba de sodio en
células y tejidos), diversas esterasas y muchas enzimas respira-
torias (g. 1-3a).
Uno de los métodos histoquímicos más comunes (a me-
nudo utilizado en combinación con la inmunocitoquímica)
emplea peroxidasa de rábano para la detección de antígenos
mediada por enzimas. Un sustrato ampliamente utilizado
para la peroxidasa de rábano es la 3,3’ diaminobenzidina
(DAB), un compuesto orgánico incoloro que genera un pro-
ducto insoluble de color pardo en el sitio de la reacción enzi-
mática (g. 1-3b). El producto de esta reacción enzimática se
puede localizar en las células de forma simple, produciendo
imágenes de alta resolución, tanto en un microscopio óptico
como electrónico.
Inmunocitoquímica
La especicidad de la reacción entre el antígeno y el anticu-
erpo es el fundamento de la inmunocitoquímica
Los
anticuerpos, también llamados inmunoglobulinas, son
glucoproteínas que se producen por las células especícas del
sistema inmunitario en respuesta a una proteína extraña o
antígeno. En el laboratorio, los anticuerpos pueden puri-
carse de la sangre y conjugarse (asociarse) con un colorante
uorescente. En general, los
colorantes fluorescentes (fluo-
rocromos)
son productos químicos que absorben la luz de
longitudes de onda diferente (p. ej., luz ultravioleta) y luego
emiten luz visible de una longitud de onda especíca (p.
ej., verde, amarillo, rojo). La
fluoresceína, el colorante más
utilizado, absorbe la luz ultravioleta y emite luz verde. Los
anticuerpos conjugados con uoresceína se pueden aplicar a
FIGURA 1-4 ▲ Imagen de microscopía confocal de una
célula muscular cardíaca de rata.
Esta imagen se obtuvo con el mi-
croscopio confocal mediante el uso de la técnica de inmunofluorescen-
cia indirecta. Se utilizaron dos anticuerpos primarios. El primer anticuerpo
primario reconoce un transportador específico de lactato (MCT1) y se
detecta con un anticuerpo secundario conjugado con rodamina (rojo).
El segundo anticuerpo primario está dirigido contra la proteína trans-
membrana CD147, que está estrechamente asociada con MCT1. Este
anticuerpo se detectó mediante un anticuerpo secundario marcado con
fluoresceína (verde). El color amarillo aparece en el sitio en el que los dos
anticuerpos secundarios marcados tienen exactamente la misma locali-
zación (colocalizan) dentro de la célula muscular cardíaca. Esta imagen
tridimensional muestra que ambas proteínas están distribuidas en la su-
perficie de la célula muscular, mientras que el transportador de lactato
solo, aparece profundo con respecto a la membrana plasmática. (Genti-
leza de los Dres. Andrew P. Halestrap y Catherine Heddle).
ba
FIGURA 1-3 ▲ Técnicas histoquímicas ópticas y electrónicas a. Esta micrografía electrónica muestra la ubicación de ATPasa en la membrana
de las células epiteliales de la vesícula biliar de un conejo. Las áreas oscuras visibles en la micrografía electrónica corresponden a la ubicación de la enzima ATPasa.
Esta enzima se detecta en la membrana plasmática en los dominios laterales de las células epiteliales, que corresponden a la ubicación de las bombas de sodio.
Estas células epiteliales están involucradas en el transporte activo de moléculas a lo largo de la membrana plasmática. 26 000 X. b. Esta fotomicrografía muestra
macrófagos teñidos con una técnica histoquímica utilizando anticuerpos marcados con peroxidasa y reactivo DAB. Un corte en parafina de un riñón de ratón con
hipertensión vascular renal se tiñó para detectar la presencia del marcador proteico específico F4/80+ expresada sólo en la superficie de los macrófagos. Primera-
mente, las secciones fueron incubadas con los anticuerpos primarios de rata contra F4/80+ seguido de la incubación con anticuerpos secundarios de cabra anti-
IgG de rata marcados con peroxidasa de rábano. La muestra se lavó y se trató con un amortiguador (buffer) que contenía DAB. Se observa un precipitado de color
pardo (producto de la oxidación DAB por peroxidasa de rábano) en las áreas donde los macrófagos están presentes. Se hizo tinción de contraste a esta muestra
con hematoxilina para visualizar los núcleos celulares. 400 X. (Gentileza del Dr. Joseph P. Grande).
tidos a una jación débil, las hidrolasas ácidas y las esterasas
contenidas en los lisosomas reaccionan con un sustrato ade-
cuado. La mezcla reactiva también contiene iones de plomo
para precipitar (p. ej., fosfato de plomo derivado de la acción

9
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
CUADRO1-3
Correlación clínica: anticuerpos monoclonales en medicina
En la actualidad, los anticuerpos monoclonales son de
uso muy difundido en técnicas inmunocitoquímicas y tam-
bién tienen muchas aplicaciones clínicas. Los anticuerpos
monoclonales conjugados con compuestos radiactivos se
utilizan para detectar y diagnosticar metástasis tumorales
en patología, diferenciar los subtipos de tumores y sus
etapas de su diferenciación y en el diagnóstico de enferme-
dades infecciosas para identificar microorganismos en la
sangre y en los líquidos de los tejidos. En estudios clínicos
recientes, se han usado los anticuerpos monoclonales con-
jugados con inmunotoxinas, fármacos de quimioterapia o
radioisótopos para administrar agentes terapéuticos a las
células tumorales específicas en el cuerpo.
INMUNOFLUORESCENCIA DIRECTA
Antígeno
A
nticuerpo
Anticuerpo
primario
Anticuerpo secundario
fluorescente
INMUNOFLUORESCENCIA INDIRECTA
a
b
FIGURA 1-5 ▲ Inmunouorescencia directa e indirecta. a. En la inmunofluorescencia directa, un anticuerpo primario marcado con fluoro-
cromo reacciona con un antígeno específico dentro de la muestra de tejido. A continuación, las estructuras marcadas, se examinan con el microscopio
de fluorescencia en el que una longitud de onda excitadora (por lo general luz ultravioleta) desencadena la emisión de otra longitud de onda. La
longitud de esta emisión depende de la índole del fluorocromo utilizado para marcar el anticuerpo. b. El método indirecto comprende dos procesos.
Primero, los anticuerpos primarios específicos reaccionan con el antígeno de interés. Segundo, los anticuerpos secundarios, que están marcados con
fluorocromo, reaccionan con los anticuerpos primarios. La apariencia de las estructuras marcadas dentro del tejido es la misma en ambos métodos y
para verlas se necesita un microscopio de fluorescencia.
cortes de tejidos congelados o jados levemente en portaobje-
tos de vidrio para localizar un antígeno en células y tejidos. La
reacción del anticuerpo con el antígeno puede entonces exa-
minarse y fotograarse con un microscopio de uorescencia
o un microscopio confocal que produce una reconstrucción
tridimensional de los tejidos examinados (g. 1-4).
En la inmunocitoquímica se utilizan dos tipos de anticu-
erpos: anticuerpos policlonales producidos por animales
inmunizados y anticuerpos monoclonales producidos por
líneas celulares inmortalizadas (duplicación continua).
En un procedimiento típico, una proteína especíca, como
la actina, se aísla a partir de una célula muscular de una
especie, p. ej. una rata, y se inyecta en la circulación de otra
especie, p. ej. un conejo. En el conejo inmunizado, el sis-
tema inmunitario reconoce las moléculas de actina de la rata
como un antígeno extraño. Este reconocimiento desenca-
dena una cascada de reacciones inmunitarias que activan las
células inmunitarias llamadas
linfocitos B. Diferentes clones
de linfocitos B se activan y eventualmente conducen a la
producción y secreción de anticuerpos anti-actina. En con-
junto, estos
anticuerpos policlonales representan mezclas
de diferentes anticuerpos producidos por muchos clones de
linfocitos B donde cada clon reconoce diferentes regiones de
la molécula de actina. Los anticuerpos se retiran de la san-
gre, se purican y conjugan con un colorante uorescente.
Éstos ahora sí se pueden utilizar para localizar moléculas de
actina en tejidos o células de rata. Si la actina está presente
en una célula o tejido, como un broblasto en el tejido con-
juntivo, el anticuerpo marcado con uoresceína se une a
la misma y la reacción puede verse con el microscopio de
uorescencia.
Los anticuerpos monoclonales (cuadro 1-3) son los pro-
ducidos por una
línea celular productora de anticuerpos
que se derivó de un solo clon de linfocitos B. Para producir
anticuerpos monoclonales contra un antígeno especíco, se
inmuniza un ratón o rata con ese antígeno. Los linfocitos B
activados, que son de diferentes clonas, son aislados del tejido
linfático (bazo o ganglios linfáticos) del animal y se fusionan
con células de mieloma (células tumorales inmortales) para
generar
hibridomas. Esta fusión produce diferentes hibrido-

10
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
se conjuga con un anticuerpo secundario dirigido contra el
anticuerpo primario de rata (es decir, p. ej., anticuerpo de
cabra dirigido contra el anticuerpo de rata; g. 1-5b). Por lo
tanto, cuando la uoresceína se conjuga directamente con el
anticuerpo primario especíco, el método es directo; cuando
la uoresceína se conjuga con un anticuerpo secundario, el
método es indirecto. El método indirecto aumenta en forma
considerable la emisión de la señal de uorescencia del tejido.
Una ventaja adicional del método de marcaje indirecto
Es que un solo anticuerpo secundario se puede utilizar
para localizar la unión especíca de tejido de diferentes anti-
cuerpos primarios (g. 1-6). Para los estudios microscópicos,
el anticuerpo secundario puede conjugarse con diferentes co-
lorantes uorescentes de modo que se vean múltiples marcas
en el mismo corte de tejido (v. g. 1-4). Las desventajas de la
inmunouorescencia indirecta son que es cara, requiere de
mucho trabajo y no se adapta con facilidad a los procedimien-
tos automatizados.
También es posible conjugar anticuerpos policlonales o
monoclonales con otras sustancias, como enzimas (p. ej., pe-
roxidasa de rábano), que convierten sustratos incoloros (p.
ej., DAB) en un producto insoluble de un color especíco
que precipita en el sitio de la reacción enzimática. La tin-
ción que resulta de este
método de inmunoperoxidasa se
puede observar en el microscopio óptico (v. g. 1-3b), ya sea
con técnicas inmunocitoquímicas directas o indirectas. En
otra variante, el oro coloidal o ferritina (una molécula que
contiene hierro) se pueden unir a la molécula de anticuerpo.
Estos marcadores densos en electrones pueden verse directa-
mente con el microscopio electrónico.
Técnicas de hibridación
La hibridación es un método de localización de ARN men-
sajero (ARNm) o ADN mediante la hibridación de la secuen-
cia de interés con una sonda de nucleótidos de secuencia
complementaria.
mas, uno por cada clon de linfocito B activado fusionado a la
célula del mieloma, que conserva su capacidad de secretar un
solo tipo de anticuerpo (monoclonal) y que al mismo tiempo
es una célula inmortal. Por ejemplo, para obtener anticuerpos
monoclonales contra moléculas de actina humana, los linfo-
citos B de los órganos linfáticos de conejos inmunizados con
esta actina deben fusionarse con células de mieloma, y pos-
teriormente identicar los hibridomas que secreten un anti-
cuerpo monoclonal que reconozca a dicha actina.
Para localizar un antígeno diana (o blanco) en células y teji-
dos, se utilizan técnicas inmunocitoquímicas tanto directas
como indirectas.
La técnica de inmunocitoquímica más antigua utilizada para
la identicación de la distribución de un antígeno dentro
de las células y tejidos se conoce como
inmunofluorescen-
cia directa.
Esta técnica utiliza un anticuerpo primario (ya
sea policlonal o monoclonal) marcado con uorocromo que
reacciona con el antígeno dentro de la muestra (g. 1-5a).
Como procedimiento de un solo paso, este método involucra
un único anticuerpo marcado. La visualización de las estruc-
turas no es ideal debido a la baja intensidad de la emisión de
la señal. Debido a la sensibilidad subóptima, los métodos de
inmunouorescencia directa están siendo reemplazados cada
vez más por los métodos indirectos.
La inmunofluorescencia indirecta proporciona una sen-
sibilidad mucho mayor que los métodos directos y a menudo
recibe el nombre de “técnica del emparedado” o “de la capa
doble”. En lugar de conjugar un uorocromo con un anti-
cuerpo (primario) especíco dirigido contra el antígeno de
interés (p. ej., una molécula de actina de rata), el uorocromo
FIGURA 1-6 Microtúbulos vistos con técnicas inmunoci-
toquímicas. El comportamiento de los microtúbulos (elementos del
citoesqueleto) obtenidos de células de tumores de mamarios humanos
puede estudiarse in vitro mediante la cuantificación de su actividad de
nucleación, que es iniciada por el centrosoma. Esta imagen se obtuvo con
el microscopio de fluorescencia. Mediante el uso de técnicas de inmuno-
fluorescencia indirecta, los microtúbulos se marcaron con una mezcla de
anticuerpos monoclonales antitubulina a y antitubulina b (anticuerpos
primarios) y éstos se visualizaron con anticuerpos secundarios conjuga-
dos con fluoresceína (inmunoglobulina G de cabra anti-ratón unida a
isotiocianato de fluoresceína). La reacción antígeno-anticuerpo, realizada
directamente sobre el cubreobjetos de vidrio, permitió ver las moléculas
de tubulina responsables de la formación de más de 120 microtúbulos
que aparecen en esta imagen. Estos se originan en el centriolo y se ex-
tienden desde él unos 20 a 25 mm para adquirir una distribución radial
uniforme. 1 400 X. (Fotomicrografía gentileza de las Dras. Wilma L. Lingle
y Vivian A. Negron).
FIGURA 1-7 ▲ Ejemplo de la técnica FISH utilizada en una
prueba de detección prenatal. Núcleos en interfase de células obte-
nidas de muestras de líquido amniótico se hibridaron con dos sondas de
ADN específicas. La sonda naranja (LSI 21) es específica para un locus del
cromosoma 21, y la sonda verde (LSI 13) es específica para un locus del
cromosoma 13. El núcleo a la derecha proviene de una muestra de líquido
amniótico normal y exhibe dos señales verdes y dos naranjas, lo que in-
dica que hay dos copias de los cromosomas 13 y 21, respectivamente. El
núcleo de la izquierda tiene tres señales naranjas, que indican una triso-
mía del cromosoma 21 (síndrome de Down). El ADN se ha teñido de azul
con un colorante de contraste no específico (DAPI) para tornar visible el
núcleo. 1 250 X. (Gentileza del Dr. Robert B. Jenkins).
11
CAPÍTULO 1 Técnicas HISTOQUÍMICA Y CITOQUÍMICA
ca del ARNm, se utilizan sondas de ARN complementarias.
Estas sondas se marcan con isótopos radioactivos (p. ej.,
32
P,
35
S,
3
H), un nucleótido modicado especícamente (digoxi-
genina), o biotina (un marcador multipropósito covalente
utilizado con frecuencia). Las sondas radioactivas se pueden
detectar y visualizar mediante la autorradiografía. La digoxi-
genina y la biotina se detectan por métodos inmunocitoquí-
micos y citoquímicos, respectivamente.
La fuerza de los enlaces entre la sonda y la secuencia com-
plementaria depende del tipo de ácido nucleico en las dos
cadenas. Un enlace más fuerte se forma entre una sonda de
ADN y una cadena de ADN complementaria y el más débil
lo hace entre una sonda de ARN y cadena de ARN comple-
mentaria. Si se espera que una muestra de tejido contenga
una cantidad muy pequeña de ARNm o un transcrito vírico,
puede utilizarse la amplicación de la
reacción en cadena de
la polimerasa (PCR)
para el ADN o la PCR con transcriptasa
inversa (RT-PCR)
para el ARN. Las transcripciones amplica-
das obtenidas durante estos procedimientos suelen detectarse
mediante el uso de sondas de nucleótidos complementarias
marcadas en técnicas de hibridación in situ estándares.
En general, el término
hibridación describe la capacidad de
las moléculas monocatenarias de ARN o ADN para interac-
tuar (hibridar) con secuencias complementarias. En el labora-
torio, la hibridación requiere el aislamiento del ADN o ARN,
que se mezcla a continuación con una secuencia de nucleó-
tidos complementaria (denominada
sonda de nucleótidos).
Los híbridos se detectan más a menudo usando un marcador
radiactivo unido a un componente del híbrido.
La unión de la sonda y la secuencia puede tener lugar en
una solución o en una membrana de nitrocelulosa. En la
hibridación in situ,
la localización del ARNm o ADN es-
pecíco (p.ej., ARNm para insulina) se realiza directamente
dentro de las células o tejidos, como células de cultivo o em-
briones enteros, adicionando la sonda de nucléotidos mar-
cada radiactivamente. Esta técnica permite la localización de
secuencias de nucleótidos especícas tan pequeñas como 10 o
20 copias de ARNm o ADN por célula.
En la hibridación in situ se utilizan diversas
sondas de
nucleótidos.
Las sondas de oligonucleótidos pueden conte-
ner un mínimo de 20 a 40 nucleótidos. Las sondas de ADN
monocatenario o bicatenario son mucho más largas y pueden
contener hasta 1 000 nucleótidos. Para la localización especí-
a b
inv
tub
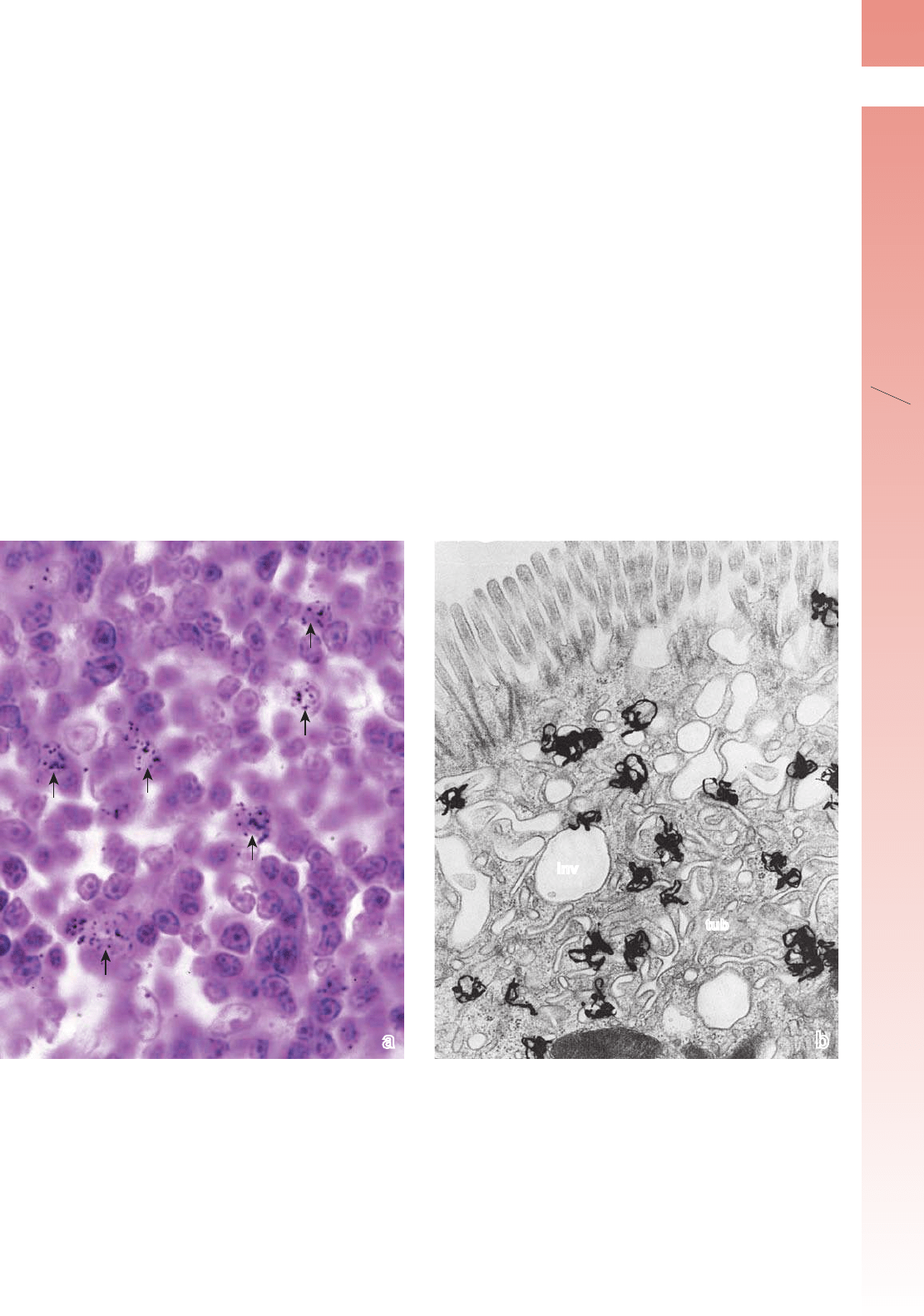
FIGURA 1-8 ▲ Ejemplos de autorradiografía óptica y electrónica. a. Fotomicrografía de un corte de ganglio linfático de un animal al que se
le administró timidina tritiada [3H]. Algunas de las células exhiben aglomeraciones de gránulos de plata metálica con el aspecto de pequeñas partículas
negras (flechas). Estas células han sintetizado ADN en preparación para la división celular y han incorporado la [
3
H] timidina en el ADN recién formado.
Con el tiempo, las partículas radiactivas de baja energía emitidas por la [
3
H] timidina chocan contra los cristales de haluro de plata de una emulsión
fotográfica que cubre la muestra (exposición) y crea una imagen latente (como hace la luz al incidir sobre la película de una cámara de fotos). Durante
el revelado del portaobjetos cubierto con la emulsión, la imagen latente, en realidad el haluro de plata activado, se reduce a plata metálica, que aparece
como gránulos negros en el microscopio. 1 200 X. (Preparado original gentileza del Dr. Ernst Kallenbach). b. Autorradiografía microscópica electrónica de
la región apical de una célula absortiva intestinal. Se le inyectó a un animal
125
I unido a factor de crecimiento nervioso (NGF) y la muestra de tejido se
retiró 1 hora más tarde. Después se preparó de una manera similar a la de la microscopía óptica. El tamaño relativamente pequeño de los gránulos de
plata contribuye a la localización precisa de los complejos
125
I -NGF. Debe observarse que los gránulos de plata se concentran en la de invaginaciones
apicales (inv) y en las siluetas tubulares endosómicas tempranas (tub). 32 000 X. (Fotomicrografía electrónica gentileza de la Dra. Marian R. Neutra).

12
CAPÍTULO 1 Técnicas MICROSCOPÍA
cuada en una cámara oscura, por lo general durante días a
semanas, la emulsión expuesta se revela con las técnicas fo-
tográcas comunes y el portaobjetos con la muestra se man-
tiene siempre sellado con un cubreobjetos. Los preparados se
pueden teñir antes o después de la exposición y revelado. Por
medio de este procedimiento, se exponen y se revelan los grá-
nulos de plata en la emulsión sobre las moléculas marcadas ra-
diactivamente y aparecen como puntos oscuros que recubren
el sitio de la emisión radiactiva cuando la muestra se examina
con el microscopio óptico (g. 1-8a).
Estos gránulos pueden utilizarse simplemente para indicar
la ubicación de una sustancia o pueden contarse para propor-
cionar información semicuantitativa sobre la cantidad de una
sustancia dada en un sitio especíco. Por ejemplo, después
de inyectar timidina tritiada a un animal, las células que han
incorporado este nucleótido en su ADN antes de dividirse
tendrán aproximadamente el doble de gránulos de plata sobre
sus núcleos que las células que se han dividido después de la
incorporación del nucleótido marcado.
La autorradiografía también puede practicarse sobre cortes
delgados de material incluido en plástico para su observación
con el ME. En esencia, se utilizan los mismos procedimien-
tos, pero como ocurre con todas las técnicas de preparación
de MET, los procesos son mucho más delicados y difíciles; sin
embargo, también producen una resolución mucho mayor y
una detección más precisa (g. 1-8b).
MICROSCOPÍA
Microscopía óptica
Un microscopio, ya sea simple (una sola lente) o compuesto
(lentes múltiples), es un instrumento que amplica una ima-
gen y permite ver más detalles de lo que es posible a simple
vista. El microscopio más simple es una lupa o un par de gafas
o anteojos para leer.
El poder de resolución del ojo humano, es decir, la dis-
tancia a la que deben estar dos objetos para que se vean por
separado (0,2 mm), está determinado por el espacio que hay
entre las células fotorreceptoras contiguas de la retina. La fun-
ción de un microscopio es la de ampliar una imagen a un
nivel en el que la retina pueda resolver la información que,
de otro modo, estaría por debajo de su límite de resolución.
La tabla 1-3 compara la resolución del ojo con la de diversos
microscopios.
El poder de resolución es la capacidad de una lente de mi-
croscopio o sistema óptico para obtener imágenes separa-
das de objetos que están muy cerca unos de otros.
La resolución depende no sólo del sistema óptico, sino
también de la longitud de onda de luz y de otros factores
como el espesor de la muestra, la calidad de la jación y la
intensidad de la tinción. Con una luz de longitud de onda
de 540 nm (v. tabla 1-1), luz proveniente de un ltro verde
para la cual el ojo es muy sensible, y con lentes objetivo
y condensador apropiados, la máxima resolución posible
con un microscopio de campo claro sería de alrededor de
0,2
μm (v. cuadro 1-4, pág. 15 para una descripción del
método de cálculo). Ésta es la resolución teórica y, como
se ha mencionado, depende de que todas las condiciones
Recientemente, los colorantes uorescentes se han com-
binado con sondas de nucleótidos, por lo que es posible vi-
sualizar múltiples sondas al mismo tiempo (g. 1-7). Esta
técnica, llamada
técnica de hibridación in situ con fluores-
cencia (FISH)
, tiene un uso muy difundido en clínica para
las pruebas genéticas. Por ejemplo, una sonda hibridada con
cromosomas en metafase se puede usar para identicar la po-
sición cromosómica de un gen.
La técnica FISH se utiliza
para examinar simultáneamente los cromosomas, la expresión
génica y la distribución de los productos génicos como las
proteínas patológicas o anómalas. En la actualidad, muchas
sondas fluorescentes especícas están disponibles co-
mercialmente y se utilizan en clínica para los procedimien-
tos de cribado para el cáncer cervical o para la detección
de células infectadas con el VIH. La técnica FISH también se
puede utilizar para examinar los cromosomas de los linfocitos
de los astronautas para estimar la dosis de radiación absorbida
por ellos durante su estadía en el espacio. La frecuencia de
translocaciones cromosómicas en linfocitos es proporcional a
la dosis de radiación absorbida.
Autorradiografía
La autorradiografía utiliza una emulsión fotográca que
se coloca sobre un corte histológico para localizar material
radiactivo en los tejidos.
Muchos precursores moleculares pequeños de moléculas más
grandes, como los aminoácidos que integran las proteínas y
los nucleótidos que forman los ácidos nucleicos, se pueden
marcar mediante la incorporación de un átomo radiactivo o
de varios en su estructura molecular. A continuación, se in-
vestiga la radiactividad para detectar las moléculas más gran-
des en células y tejidos. Las moléculas precursoras marcadas
pueden inyectarse en los animales o introducirse en células
u órganos de cultivo. De esta manera, se han estudiado la
síntesis de ADN y la posterior división celular, la síntesis y
la secreción de proteínas por las células y la localización de
los productos sintetizados dentro de las células y en la matriz
extracelular.
Los cortes de las muestras que han incorporado material
radiactivo se montan en portaobjetos. En la oscuridad, el
portaobjetos suele sumergirse en una emulsión fotográca
fundida, produciendo de este modo una película fotográca
delgada sobre su supercie. Después de la exposición ade-
Distancia entre los puntos que se resuelven
Ojo humano 0,2 mm
Microscopio óptico de campo claro
0,2 mm
MEB 2,5 nm
MET
En la teoría
En la práctica
0,05 nm
1,0 nm
Microscopio de fuerza atómica 50,0 pm
MEB, microscopio electrónico de barrido; MET, microscopio electrónico
de transmisión.
TABLA 1-3 Resolución del ojo en comparación
con la de los microscopios
13
CAPÍTULO 1 Técnicas MICROSCOPÍA
Fuente luminosa
(lámpara)
Lente condensador
Fuente
de electrones
(cátodo)
Ánodo
Lente condensador
Solenoide de barrido
Haz de barrido
Detector
de electrones
retrodispersos
Detector de
electrones
secundarios
Vacío
Muestra
Imagen en la
pantalla de visión
Detector de
electrones con
cámara de CCD
MICROSCOPIO
ÓPTICO
MICROSCOPIO ELECTRÓNICO
DE TRANSMISIÓN (MET)
MICROSCOPIO ELECTRÓNICO
DE BARRIDO (MEB)
Imagen
de MEB
Imagen de MET
Lente objetivo
Lente de proyección
Lente ocular
Imagen
en la retina
del ojo
Muestra
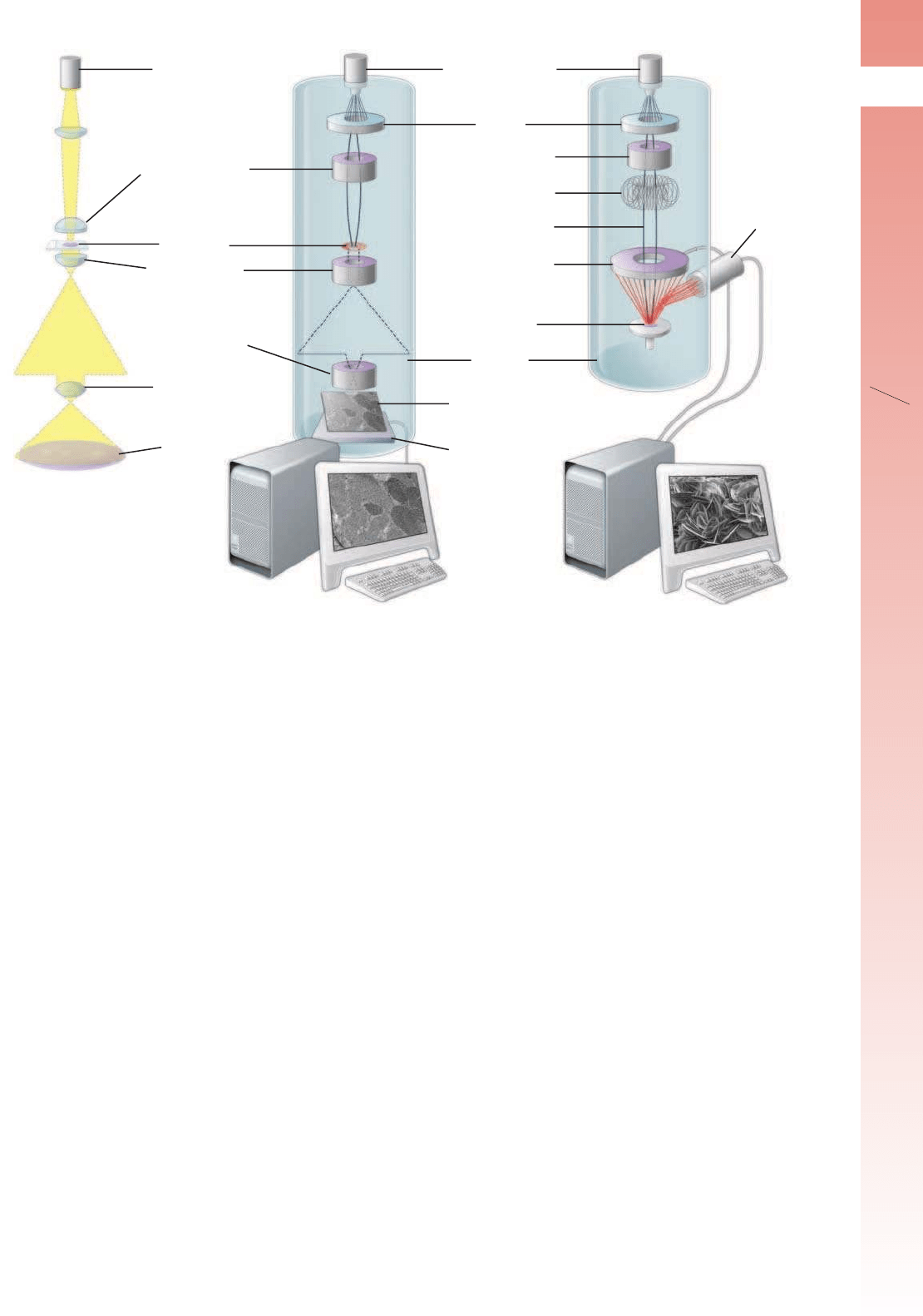
FIGURA 1-9 ▲ Diagramas comparativos de la formación de la imagen en diferentes tipos de microscopios Para una mejor compara-
ción entre los tres tipos de microscopios, se muestra el microscopio óptico (izquierda) como si estuviera invertido, el MET (medio) y el MEB (derecha).
Debe tenerse en cuenta que tanto en el MET como el MEB, las muestras deben mantenerse en un medio de gran vacío (10
–4
a 10
–7
Pa).
sean óptimas. La lente ocular aumenta la imagen producida
por la lente objetivo, pero no puede aumentar la resolución.
En la investigación biológica moderna se dispone de va-
rios microscopios ópticos para el uso general y especializado.
Sus diferencias radican, en gran medida, en factores como la
longitud de onda con la que se ilumina la muestra, en la al-
teración física de la luz que entra o sale de la muestra y en
los procesos analíticos especícos que se pueden aplicar a la
imagen nal. En esta sección se describen brevemente estos
instrumentos y sus aplicaciones.
El microscopio utilizado por la mayor parte de los estudian-
tes e investigadores es el microscopio de campo claro.
El microscopio de campo claro es el descendiente directo de
los microscopios de uso muy difundido en el siglo XIX e ini-
ciaron la primera gran era de la investigación histológica. Bá-
sicamente, los componentes del microscopio de campo claro
(g. 1-9) son los siguientes:
•
fuente luminosa para la iluminación de la muestra (p. ej.,
una lámpara en la base del microscopio),
•
lente condensador para enfocar el haz de luz a la altura
de la muestra,
•
platina sobre la que se coloca el portaobjetos,
•
lente objetivo para recoger la luz que ha atravesado la
muestra y
•
lente ocular (o un par de lentes oculares en los microsco-
pios binoculares, de uso más común) a través de la cual se
puede examinar directamente la imagen formada por la
lente de objetivo.
Para que una muestra pueda examinarse con el micros-
copio de campo claro, debe ser lo sucientemente na para
que la luz pase a través de ella. Si bien algo de luz es absor-
bida al atravesar la muestra, el sistema óptico del microscopio
de campo claro no produce un grado útil de contraste en la
muestra no teñida. Por esta razón, se utilizan los diversos mé-
todos de tinción que se comentaron antes.
Examen de un preparado histológico con el
microscopio óptico
Los órganos son tridimensionales, mientras que los
cortes histológicos tan sólo tienen dos dimensiones.
Como se comentó en la sección anterior “Preparación de los
tejidos”, toda muestra de tejido preparado para su examen
por microscopía óptica debe cortarse en rebanadas muy nas.
Por tanto, de una muestra tridimensional de tejido se obtie-
nen cortes bidimensionales. Uno de los mayores desafíos que
enfrentan los estudiantes que utilizan el microscopio para es-
tudiar la histología, es tratar de reconstruir mentalmente la
tercera dimensión “faltante”.
14
CAPÍTULO 1 Técnicas MICROSCOPÍA
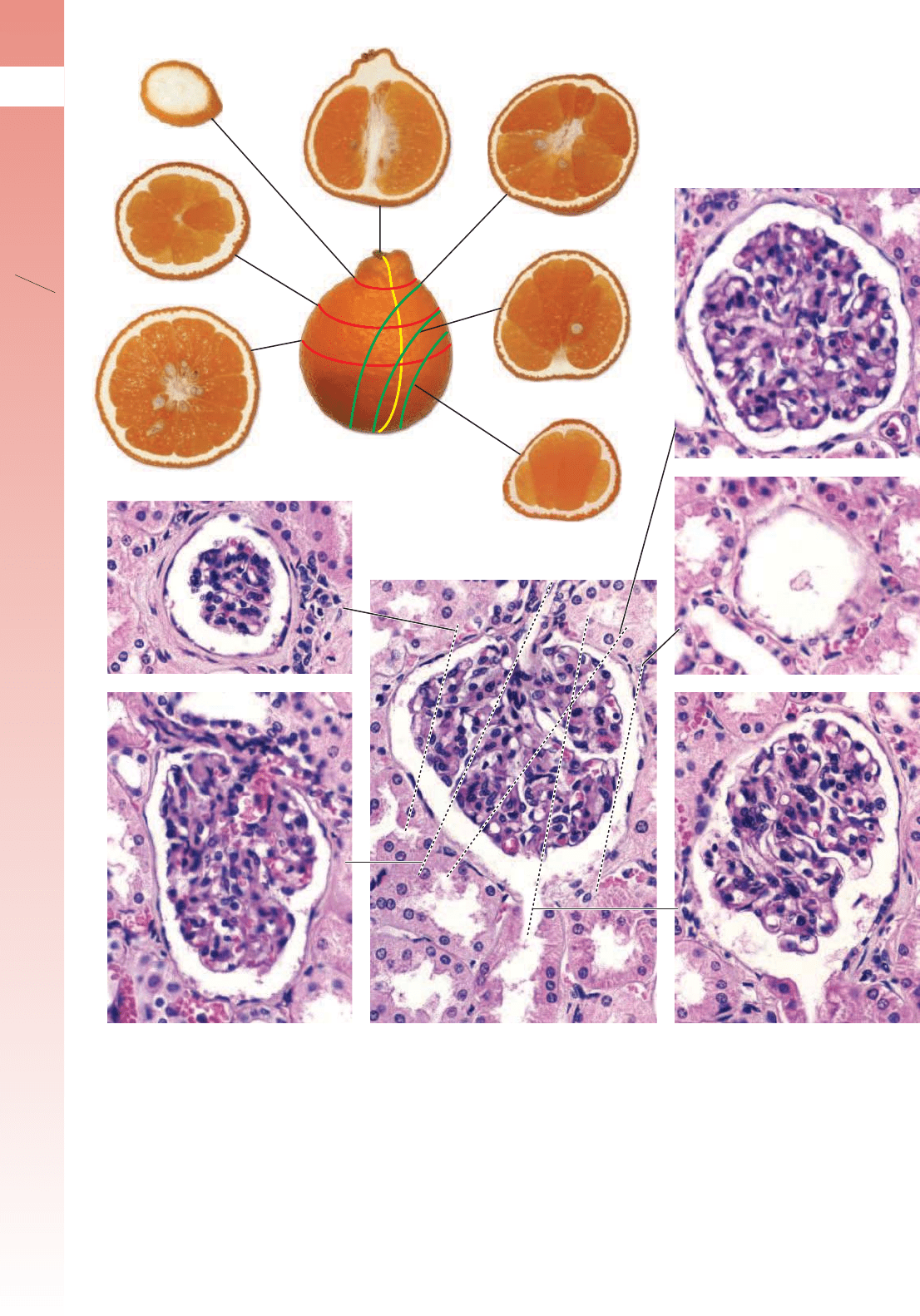
Por ejemplo, en la gura 1-10 se ilustran cortes en diferen-
tes planos a través de una naranja. Téngase en cuenta que cada
supercie de corte (indicada por la línea de puntos) de la na-
ranja entera exhibe diversos tamaños y patrones de supercie,
según la orientación del corte. Por consiguiente, al examinar
un corte dado a través de la naranja, es importante ser capaz
de reconstruir mentalmente la organización de la estructura
y de sus componentes. Un ejemplo de una estructura histo-
lógica, en este caso, un corpúsculo renal, se muestra como
aparecería en diferentes planos de corte (v. g. 1-10). Nótese
la marcada diferencia en cada corte del corpúsculo renal. Me-
diante el examen de una serie de estos cortes bidimensionales,
es posible imaginar la conguración tridimensional de la es-
tructura examinada.
FIGURA 1-10 ▲ Ejemplo de cortes de una naranja y un corpúsculo renal. Las líneas de puntos dibujadas sobre la naranja entera indican
el plano de corte que se correlaciona con cada superficie seccionada. Del mismo modo, los cortes diferentes a través de un corpúsculo renal, que
también es una estructura esférica, exhiben diferencias en su aspecto. El tamaño y el aspecto de la estructura interna son un reflejo del plano de corte.
15
CAPÍTULO 1 Técnicas MICROSCOPÍA
CUADRO 1-4
Consideraciones funcionales: Uso correcto
del microscopio óptico
Esta breve introducción al uso correcto del microscopio óptico
se dirige a aquellos estudiantes que usarán el microscopio
para el examen de rutina de los tejidos. Si los comentarios
siguientes parecen elementales, sólo se debe a que la mayo-
ría de los usuarios del microscopio no lo hacen aprovechando
todas sus ventaja. A pesar del equipo sofisticado del que
disponemos en la actualidad, en muchos casos se carece
de instrucción formal necesaria sobre el uso correcto del mi-
croscopio óptico.
Los sistemas ópticos costosos y muy corregidos sólo
pueden funcionar de forma óptima cuando los trayectos de
los haces de iluminación y de observación están centrados y
tienen un ajuste correcto. El uso de ajustes y alineamientos
adecuados contribuirá sustancialmente al reconocimiento de
detalles muy diminutos de la muestra y a la manifestación
fidedigna de los colores para la visión directa o mediante la
fotomicrografía.
La iluminación Köhler es una de las claves de la buena
microscopía y está incorporada en el diseño de prácticamente
todos los microscopios modernos que se usan en laboratorios
o para la investigación. En la figura C1-4.1 se ilustran los dos
trayectos de los rayos luminosos y todos los controles de
ajustes de un microscopio moderno; es necesario seguir las
instrucciones que se dan a continuación para obtener una ilu-
minación adecuada en el microscopio.
Los pasos del ajuste necesarios para conseguir una
buena iluminación Köhler son pocos y sencillos:
• Se enfoca la muestra
• Se cierra el diafragma de campo
• Se enfoca el condensador moviéndolo hacia arriba o hacia
abajo hasta que el contorno de su diafragma de campo
aparezca bien nítido (en foco).
• Se centra el diafragma de campo con los controles de
centrado de la subplatina (donde está el condensador).
Después se abre el diafragma de campo hasta que el haz
luminoso cubra todo el campo observado.
• Se retira el ocular (o se usa un telescopio de centrado o
un accesorio telescópico de fase si se dispone de ellos)
y se observa la pupila de salida del objetivo. Así se verá
un campo circular iluminado cuyo radio es directamente
proporcional a la abertura numérica del objetivo. A medida
que se cierra el diafragma del condensador, su contorno
aparecerá dentro de este campo circular. Para la mayor
parte de los preparados teñidos, el diafragma del conden-
sador debe cerrarse hasta cubrir aproximadamente dos
terceras partes de la abertura del objetivo. El resultado de
este ajuste es el mejor equilibrio entre la resolución y el
contraste (que no es más que la diferencia de intensidades
entre las regiones claras y oscuras de la muestra).
Si se ponen en práctica estos cinco consejos simples, la
imagen obtenida será la mejor que permita la óptica del mi-
croscopio. Ahora veamos por qué.
Primero, ¿por qué ajustamos el diafragma de un campo
para cubrir sólo el campo observado? El iluminar un campo
más grande que el sistema óptico puede “ver” sólo conduce
a reflexiones internas o una pérdida de luz lo cual trae como
consecuencia más “ruido” o una disminución del contraste de
la imagen.
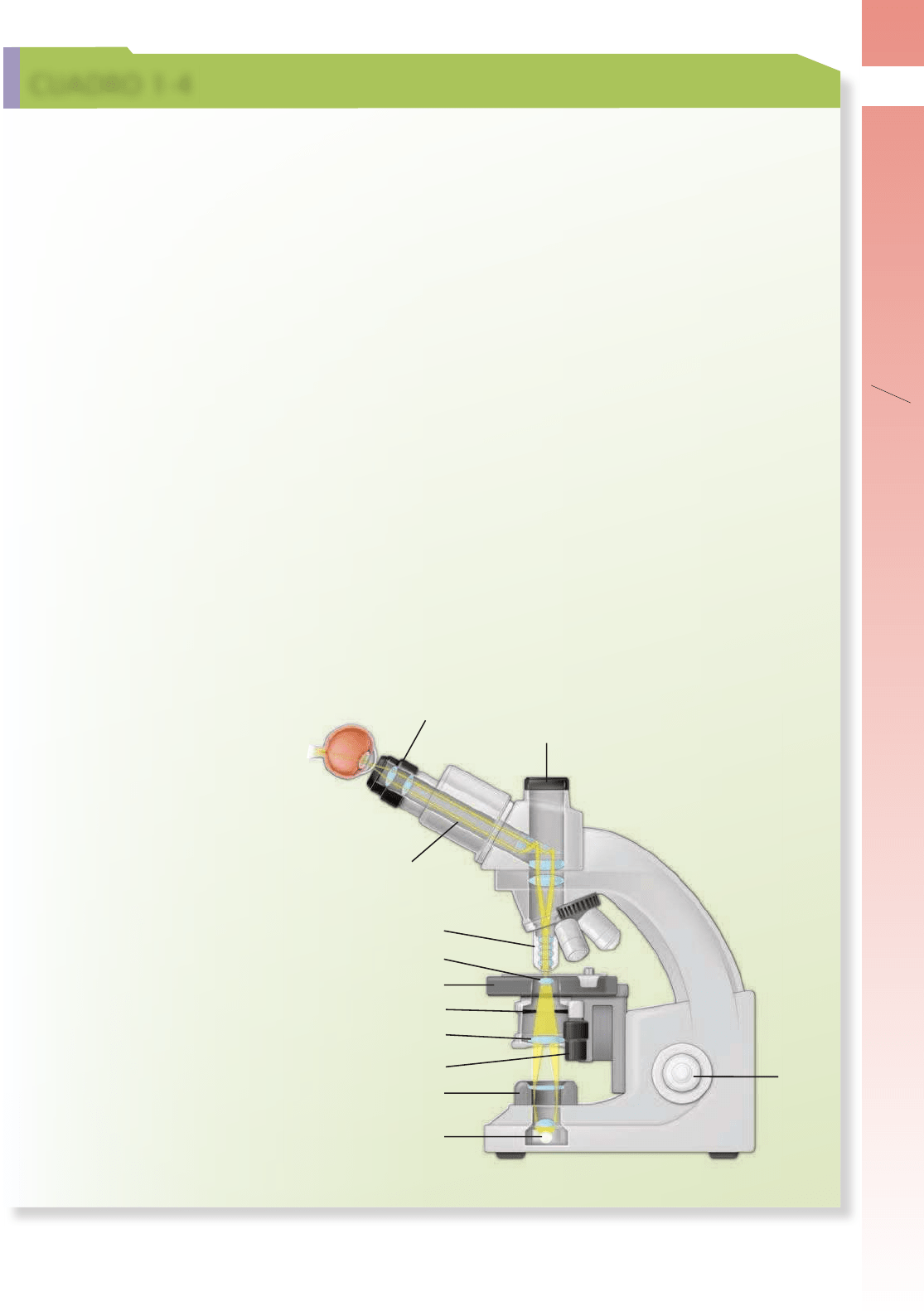
FIGURA C1-4.1 ▲ Diagrama
de un microscopio óptico típico.
Este dibujo muestra un corte transversal
del microscopio, sus componentes ope-
racionales y el trayecto de la luz.
(Continúa en página 16)
Diafragma de campo
Fuente luminosa
Condensador
Ajuste de la platina
Objetivo
Tubo
Cámara tubular
opcional
Ocular
Ajuste
de foco
Diafragma del condensador
Lente condensador auxiliar
Platina
Este documento contiene más páginas...
Descargar Completo
Histologia_Ross_7_edicion.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.