Glúcidos
1
HIDRATOS DE CARBONO
Los hidratos de carbono también llamados glúcidos, se encuentran tanto en vegetales como
animales, los primeros tienen la capacidad de sintetizar H de C a partir de CO
2
y H
2
O, mediante el
proceso de fotosíntesis, de esta manera, los glúcidos producidos por los vegetales son ingeridos
por los animales, y así, los animales utilizan éstos H de C como materia prima para síntesis de otros
compuestos o como fuente de energía para el cumplimiento de sus funciones.
• COMPOSICIÓN QUÍMICA:
Los glúcidos están compuestos químicamente por C, H, O, debido a estos pueden definirse
como: Polihidroxialdheídos o polihidroxicetonas, es decir, que están constituidos por un
grupo aldehído R-C-H o un grupo cetona R-C-R ya varios grupos alcohólicos o funciones
alcohólicas. OH O
• CLASIFICACIÓN:
Según la complejidad de la molécula se clasifican en:
→ MONOSACÁRIDOS: también llamados azúcares simples, están constituídos por un
solo polihidroxialdheído o polihidroxicetona. El más importante de este grupo es
la glucosa, pero también veremos a la galactosa, manosa y fructosa.
→ OLIGOPOLISACÁRIDOS: están compuestos por la unión de 2 a 10 unidades de
monosacáridos. Se nombran de acuerdo a la cantidad de monosacáridos, suelen
ser lineales o ramificados, homopolisacáridos o heteropolisacáridos, es decir,
formados por un solo tipo de glúcido o distinto respectivamente.
→ POLISACARIDOS: son moléculas de gran tamaño, poseen más de 10
monosacáridos, pueden ser lineales o ramificados, homopolisacáridos o
heteropolisacáridos.
A su vez los glúcidos se clasifican en no hidrolizables (monosacáridos) e hidrolizables
(oligosacáridos y polisacáridos).
MONOSACÁRIDOS:
Como dijimos anteriormente son polihidroxialdehídos o polihidroxicetonas. A los primeros se los
llama también aldosas y a los segundos cetosas. Es decir que para denominarlos se utiliza el sufijo -
--osa, ejemplo triosas, tetrosas, etc, según el número de carbono que posean.
Si combinamos la función con el número de carbonos tendríamos por ejemplo que una aldohexosa
es un glúcido de 6 carbonos que posee una función aldehído.
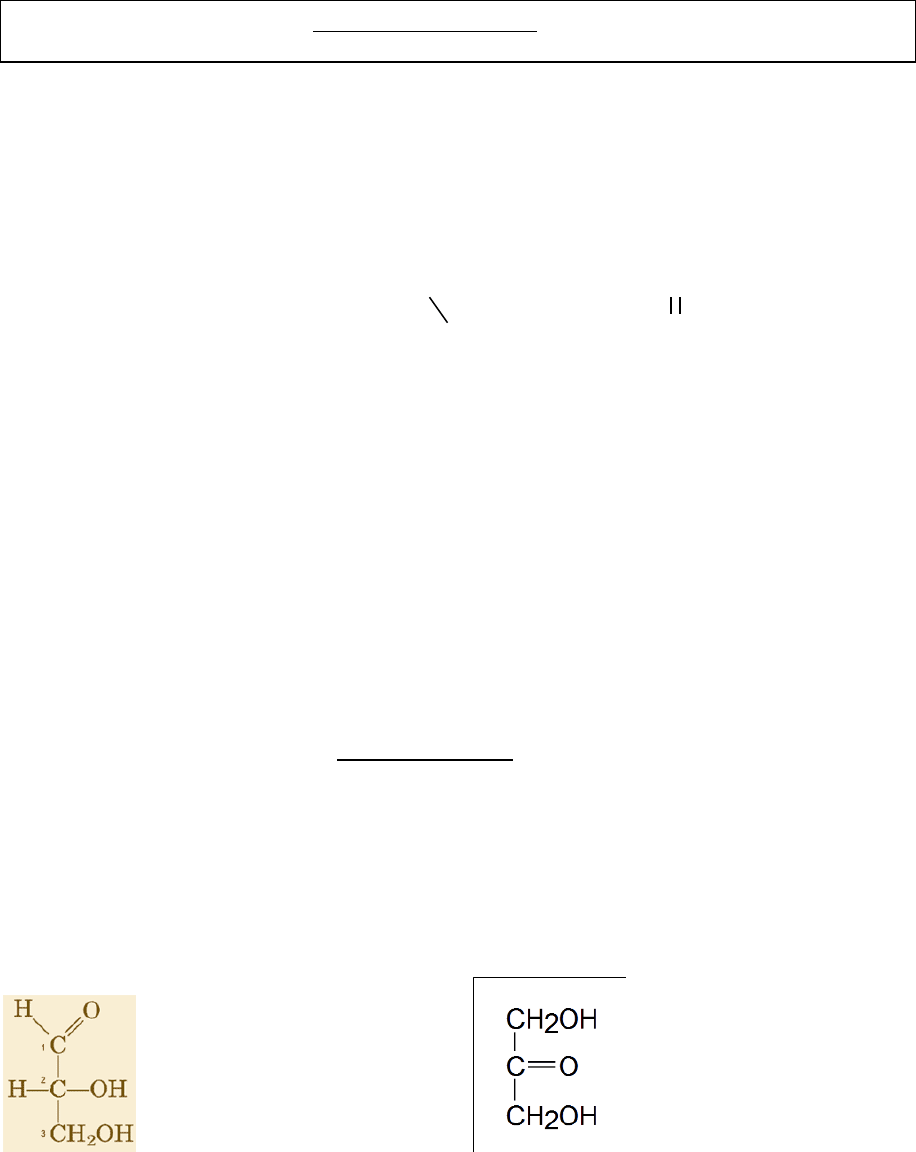
Los monosacárdidos más simples son las triosas. De allí nace el gliceraldehído que es una
aldotriosa y la cetotriosa o dihidroxiacetona.
Gliceraldheído Dihidroxiacetona
O Aldosa o Cetotriosa.
Todos los glúcidos de más de 4 carbonos son derivados de estas triosas que se originan agregando
el grupo H-C-OH en cadena lineal, como carbono 2º, es decir, contiguo al grupo aldehído.

Glúcidos
2
ISOMERIA:
Podemos tomar como ejemplo al gliceraldehído, éste posee el 2º carbono asimétirco o quiral, es
decir, que posee cuatro grupos funcionales diferentes, de esta manera, tendremos 2 isómeros del
gliceraldehído con diferentes propiedades ópticas.
Uno desvía la luz polarizada en sentido horario, será dextrógiro o dextro-rotatorio y se lo designa
anteponiendo la letra D a su nombre. El otro será levógiro o levo-rotativo (desvía la luz polarizada
en sentido antihorario) y se lo designa anteponiendo la letra L a su nombre.
Ambos cokmpuestos son ENANTIOMEROS, es decir, que uno es la imagen especular del otro,
también son llamados ANTÍPODAS ÓPTICOS.
D(+) Gliceraldehído L(-) gliceraldehído.
El carbono quiral suele indicarse con un asterisco y por convención, el dextrógiro tendrá el grupo
OH a la derecha y el levógiro a la izquierda.
A medida que vamos agregando grupos C-OH como 2º carbono originamos un nuevo carbono
quiral, así una aldotetrosa tendrá 2 carbonos quirales o asimétricos, y así sucesivamente.
El número de isómeros posibles para cada compuesto se calcula como 2
n
, siendo “n” el número
de carbonos asimétricos, por ejemplo:
Las aldotetrosas poseen dos carbonos quirales, entonces existen 2
2
aldotetrosas, 2 dextrógiras y
2 levógiras.
Aldotetrosas fila L aldotetrosas fila D
Como podemos tener 2 tipos de gliceraldehídos y las aldosas derivan de él, se pueden tener 2
familias de estos monosacáridos, una derivada del D-gliceraldehído y la otra del L-gliceraldehído.
Cada familia posee la misma configuración en el carbono 2º más próximo a la función alcohol
primario, es decir, en el carbono 2º más alejado del grupo aldehído. De aquí la fila D o serie D
posee el grupo OH ala derecha en ese carbono.
La actividad óptica de los compuestos formados por varios carbonos será la resultante de la
interacción de todos ellos, es por eso que la letra D sólo indicará la fila a la cual pertenece y la
actividad óptica de ese compuesto se indicará con un signo (+) o (-) a continuación de D o L. asó
por ejemplo, la D (+) glucosa, es una aldohexosa de la familia D con capacidad dextrógira.

Glúcidos
3
Las orientaciones en el grupo agregado originan isómero que no son antípodos ópticos, sino
DIASTEROISÓMEROS.
Para cada compuesto de la serie D, existe un ENENTIÓMERO correspondiente de la serie L.
ALDOSAS SERIE D indica la serie.

Glúcidos
4
CETOSAS SERIE D:
La diferenciación de series o filas tiene importancia biológica, los organismos
superiores (humano) utilizan prácticamente los glúcidos de la serie D.

Glúcidos
5
MONOSACÁRIDOS DE INTERÉS EN BIOQUÍMICA HUMANA:
Dentro del grupo de las aldopentosas consideramos a la ribosa, de las aldohexosas, la
glucosa, la galactosa y la manosa. De las cetosas, las más importantes es la fructosa.
→ Glucosa: es la más abundante, fisiológicamente más importante de los
monosacáridos. También se la llama dextrosa debido a sus propiedades
dextrógiras, es el principal combustible usado por las células. Se la puede
encontrar libre o unida a otros monosacáridos formando disacáridos o
polisacáridos.
LIBRE EN FRUTOS MADUROS, EN SANGRE Y HUMORES ORGÁNICOS DE
VERTEBRADOS.
UNIDA DISACÁRIDO: FORMA PARTE DE LA LACTOSA Y LA SACAROSA.
POLISACÁRIDO: ALMIDÓN, GLUCÓGENO, CELULOSA.
Estructura cíclica:
No todos los glúcidos presentan inmediatamente reacciones características de la función aldehído
o cetona, esta es debido a que pueden encontrarse mediante formas cíclicas. La glucosa presenta
dos formas cristalinas, una y la otra que difieren en su índice de rotación específica, el de la -
D- glucosa es de + 112,2º y el de la -D- glucosa es de +18,7º, als dos formas muestran el
fenómeno de MUTORROTACIÓN que consiste en lo siguiente:
Si se prepara una solución de -D- glucosa en agua y se mide inmediatamente el índice de
rotación específica se obtiene el valor de +112,2º, pero con el tiempo ese índice crece hasta un
valor constante de +52,7º.
La -D- glucosa, también presenta un índice de rotación específico de +18,7º que va aumentando
con el tiempo hasta un valor de +52,7º.
La existencia de estas formas de y y de las modificaciones antes vistas se debe a la formación
de estructuras cíclicas. Estas se forman por acercamiento de la función aldehído del 1º C a la
función oxhidrilo del carbono 5, de esta manera se forma una unión HEMIACETAL.

Glúcidos
6
HEMIACETAL: compuesto por un aldehído o cetona con en alcohol y se representan:
De aquí que existen azúcares con formas piranosas y furanosas. Mediante la ciclación, el carbono 1
no posee la función aldehído es por esto que las reacciones típicas de las funciones aldehído se
dan de manera más lenta.
La estructura cíclica de las aldosas, poseen en el C1 una función aldehído potencial responsable de
la capacidad reductora de éstos azúcares.
PROCESO DE CICLACION DE LA GLUCOSA:
FORMA FURANOSA
Aquí la unión es entre el carbono 1 y el carbono 4.

Glúcidos
7
FORMA PIRANOSA
Aquí la unión es entre el carbono 1 y el carbono 5.
El carbono 1 es asimétrico o quiral a partir del cual existen dos configuraciones posibles. A este
tipo de isómeros se los denomina ANÓMEROS. Por convención se representa la forma con el OH
hacia abajo y la con el OH hacia arriba.
En solución, si se coloca la -D-glucosa, una cierta cantidad de moléculas se convertirán en , de
esta manera cambia el índice de rotación específica, hasta llegar al equilibrio donde obtenemos el
índice estable de +52,7.
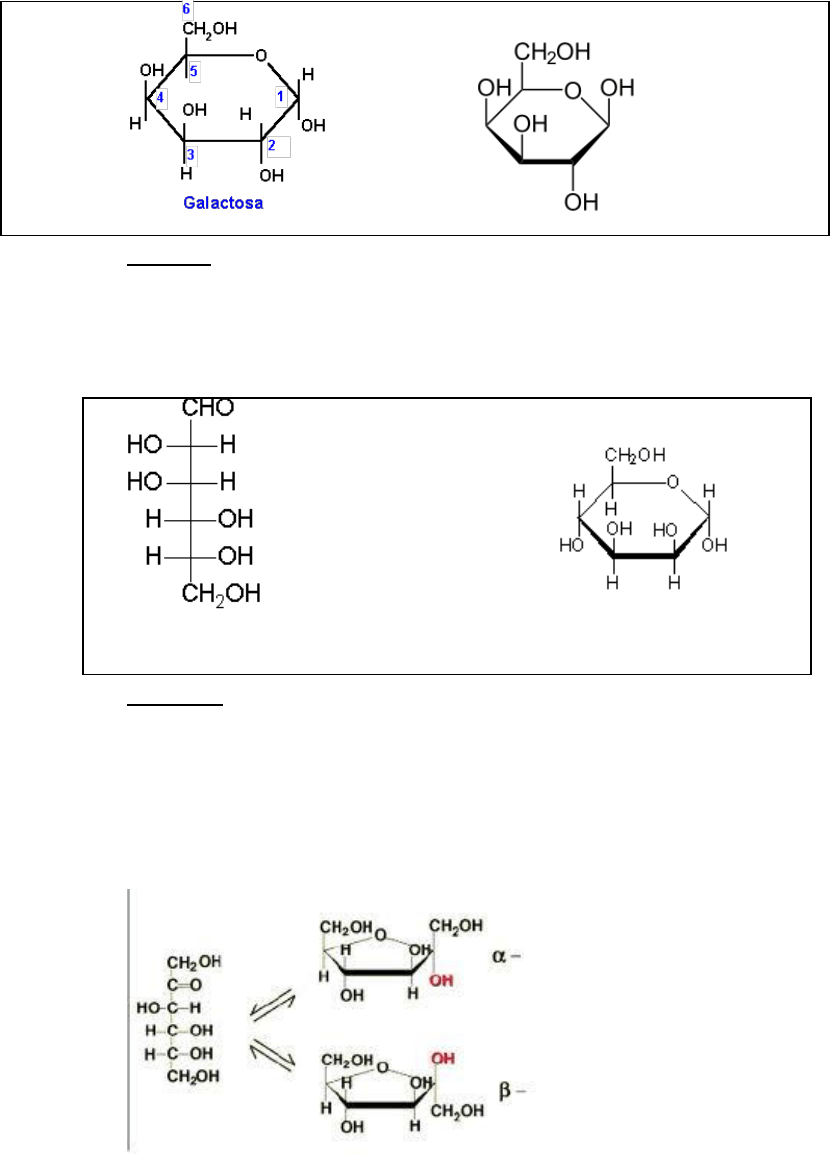
→ Galactosa: es una aldohexosa que no se encunetra generalmente libre, sino
asociada a otras, por ejemplo la galactosa se une a la glucosa para formar un
disacárido llamado lactosa (azúcar de la leche). La galactosa es un epímero de
glucosa, es decir, un isómero que difiere en la configuración del carbono 4. La
galactosa se encuentra bajo 3 formas, 2 de ellas cíclicas piranosas (y) y la
forma lineal.
forma lineal D-galactosa
Glúcidos
8
-D-galactosa β-D-galactosa
→ Manosa: es una aldohexosa que se encuentra formando parte de
oligosacáridos. En organismos animales constituye parte glucídica de
glicoproteínas. En organismos vegetales se encuentra en polidisacáridos como
los mananos. Es un epímero de la glucosa, difiere en al configuración del C2.
Se encuentra en las siguientes formas:
Forma lineal D-manosa Forma pìranosa -manosa.
→ Fructosa: es una cetohexosa llamada levulosa, debido a sus propiedades
levorotatorias. Se encuentra libre en frutos maduros, en la miel. Combinada
con la glucosa, forman la sacarosa o azúcar de caña. La fructosa posee la
función cetona en el carbono 2, puede formar ciclos del furano debido a la
formación de la unión hemiacetálica del c2 y el C5. La función cetona del C2 en
la estructura cíclica es considerada “potencial”, y es la responsable de las
propiedades reductoras de la fructosa.

Glúcidos
9
Dentro del grupo de las pentosas, la de mayor importancia es la D-ribosa que
veremos a continuación:
→ Ribosa: es una aldopentosa que forma parte del ARN y otras sustancias de
importancia biológica. En la naturaleza se la encunetra bajo la forma cíclica
tipo furanosa, es por eso que presentará (al igual que las anteriores) los
anómeros y .
D-Ribosa -D-ribosa
FORMULAS DE HAWORTH
Haworth propuso representar a los anillos furano y pirano en un plano y a los grupos funcionales
por encima y debajo de ese plano.

Glúcidos
10
Esta forma no es del todo correcta, debido a que los átomos que integran el anillo se encuentran
en un mismo plano. La molécula tiende adoptar conformaciones de menor energía, que para el
anillo piranósico corresponde dos formas: una de silla y la otra de bote.
Las conformaciones C1 y 1C con conformaciones de SILLAS y las B conformación de BOTE. De
todas, la más favorable termodinámicamente, es la conformación C1 que posee los grupos OH en
planos ecuatoriales.
La forma furanosa de monosacáridos se encuentra bajo la conformación llamada de SOBRE, donde
uno de los carbonos del ciclo se aparta del plano en el que se encuentran los otros 4.
(Llamada así porque el C3 es el que está fuera del plano).
En la desoxirribosa, (constituyente del ADN), el C2 es el que está fuera del plano.
C1
1C
B

Glúcidos
11
DERIVADOS DE MONOSACÁRIDOS:
→ Glicósidos: son obtenidos cuando el carbono heiacetálico de las aldosas o
cetosas reacciona con otra molécula.
Por ejemplo:
Α-D-glucosa + matanol α-D-metilglucósido.
El carbono hemiacetálico C1 de la α D-glucosa reacciona con el metanol dando
un glicósido más agua.
Como esta reacción se puede dar con α-O y la β- D-glucósa, puedo obtener
dos tipos de glicósidos y la unión entre el monosacárido y el radical agregado
será el tipo α o β-gicosídica.
Una vez formado el glicósido, las formas α o β NO se interconvierten, es decir,
que no presentan el fenómeno de mutorrotación, y no son reductores.
Si el glúcido que reacciona es la glucosa, el compuesto obtenido se
denomina se denomina glucósido, si por el contrario, es la galactosa, se
forma galactósido, si fuera fructosa sería fructósido.
+
OH-CH
3
O-CH
3
+ H
2
O

Glúcidos
12
PRODUCTOS DE REDUCCIÓN DE ALDOSAS:
La reducción se lleva a cabo en el grupo aldehído o cetona del glúcido, dando origen a un
polialcohol. Por ejemplo, la reducción de la D-glucosa da origen al sorbitol (hexa-alcohol). Este tipo
de compuestos no pueden adquirir la forma cíclica ya que han perdido la función capaz de formar
la unión hemiacetálica.
DEOXIAZÚCARES:
Son derivados de los monosacáridos, obtenidos por pérdida del oxígeno de uno de los grupos
alcohólicos.
El más abundante es la 2-desoxirribosa, la cual es obtenida por la sustracción del oxígeno unida al
C2 de la aldopentosa ribosa.
+ H
2
D-glucosa
sorbitol

Glúcidos
13
Otro deoxiazúcar es la L-fucosa, obtenida por la pérdida del oxígeno en el carbono 6 (6-desoxi-L-
galactosa), ésta participa en la formación de glicoproteínas de animales superiores y paredes de
células bacterianas.
PRODUCTOS DE OXIDACIÓN DE LAS ALDOSAS.
Bajo la acción de oxidantes suaves, la función aldehído se oxida a carboxilo, originando ÁCIDOS
ALDÓNICOS: es formado por la oxidación del C1 de la glucosa y se denomina ácido glucónico.
Una oxidación más energética afecta a ambos carbonos terminales de la aldosa (C1 y C2)
originando ÁCIDOS DICARBOXÍLICOS, éstos díacidos reciben el nombre de ácidos sacáricos o
aldáricos.
D-glucosa
Oxidación C1

Glúcidos
14
En condiciones controladas donde se oxidan únicamente el C6 se originan ÁCIDOS URÓNICOS.
Se oxida solamente el C6
LOS ÁCIDOS URÓNICOS PUEDEN ADOPTAR ESTRUCTURAS CÍCLICAS YA QUE LA REACCIÓN NO
AFECTA LA UNIÓN HEMIACETÁLICA.
Oxidación C6
OOH
H
OOH
Ácido glucárico

Glúcidos
15
ÉSTERES FOSFÓRICOS:
Son obtenidos al reaccionar el monosacárido con el ácido fosfórico en un proceso denominado
fosforilación. Se produce como el 1º paso en la utilización de monosacáridos en el organismo. Los
más importantes son:
Dihidroxiacetona-fosfato.
OH
O
OH
α-D-glucosa-6-fosfato
α-D-fructosa-1,6-bifosfato.
α-D-glucosa-1-fosfato
Este documento contiene más páginas...
Descargar Completo
proteinas mio.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.