HEMOGLOBINA
Proteína conjugada cuyo grupo prostético es el hemo, al cual debe su intenso color rojo.
Pertenece a las llamadas hemoproteínas.
Tanto la mioglobina como la hemoglobina están constituidas por una proteína de carácter
básico llamada globina.
La mioglobina posee una cadena polipeptídica unida a un grupo hemo, mientras que la
hemoglobina es una molécula tetramérica integrada por cadenas de globina, cada una
asociada a un grupo hemo.
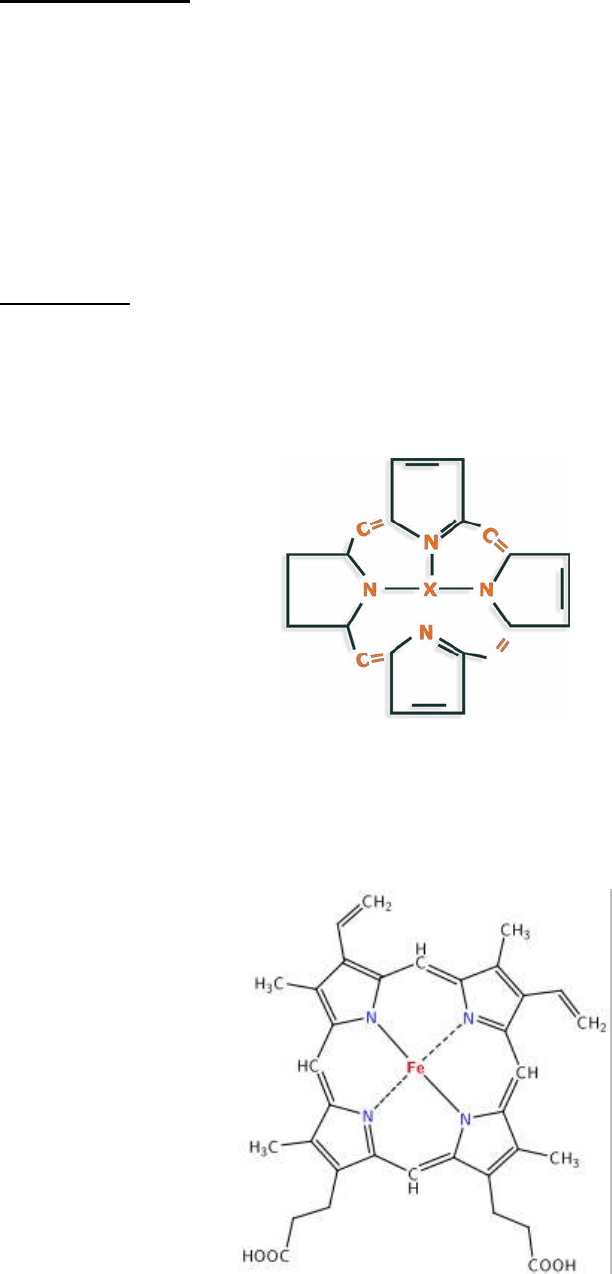
Grupo Hemo
Derivado del núcleo porfina, anillo macrocíclico formado por 4 grupos pirrol unidos por
puentes metino. Los pirroles se enumeran de I a IV, y los puentes metino de α a δ. Los
átomos de hidrógeno unidos a carbonos de los grupos pirrol se enumeran del 1 al 8. Esta
estructura presenta resonancia.
Cuando los hidrógenos se encuentran sustituidos por restos carbonados, la porfina se
convierte en porfirina.
Protoporfirina III: grupos metilo en 1, 3, 5, 8, grupos vinilo (-CH=CH2) en 2 y 4, y
propionilo en 6 y 7.
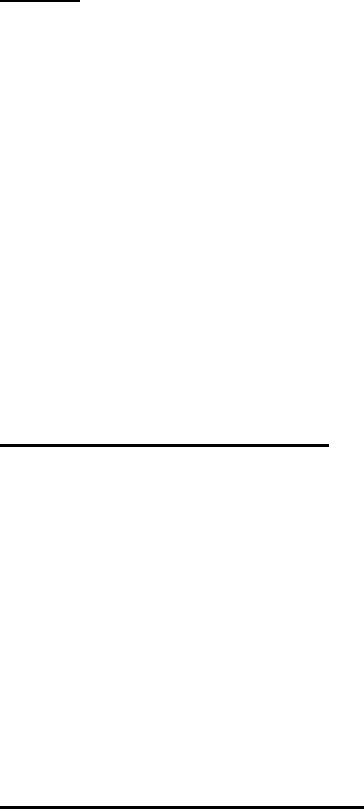
El hierro del hemo es bivalente, forma 6 enlaces coordinados, aceptando pares de
electrones no compartidos. Esos electrones se ubican en 6 orbitales híbrido, cuando la
hemoglobina fija oxígeno tienen una configuración octaédrica. Cuatro de los enlaces
coordinados unen el Fe a los átomos de N de los pirroles, el quinto a un N del núcleo
imidazol de un resto de histidina, y en la sexta posición se unen las moléculas de oxígeno.
Cuando el hierro del hemo está en estado ferroso la hemoglobina puede formar
oxihemoglobina. Si el hierro se oxida a férrico, el hemo se convierte en hematina y la
hemoglobina se transforma en metahemoglobina, incapaz de transformar oxígeno. El
ambiente apolar alrededor del hemo es fundamental para mantener el Fe en estado ferroso.
Globina
La hemoglobina es una molécula tetramérica, constituida por la asociación de dos cadenas
polipeptídicas (α o ζ) y otras dos cadenas (β, γ, δ o ε).
Hemoglobina A
1
(Hb A
1
): formada por 2 α y 2 β. Es la más abundante (95%).
Hemoglobina A
2
(Hb A
2
): 2 cadenas α y 2 δ. Representa el 3%.
Hemoglobina F (Hb F): 2 cadenas α y 2 γ. Es la predominante en el feto durante los 6
meses de vida intrauterina.
Hemoglobinas embrionarias:
Gower 1: 2 ζ y 2 ε. Las cadenas ζ son reemplazadas por α y se forma gower 2
Gower 2: 2 α y 2 ε.
Portland: 2 ζ y 2 γ.
Estructura secundaria y terciaria
El 80% de la molécula posee estructura helicoidal. Cada subunidad está formada por
segmentos hélice α conectados por trozos de disposición al azar.
La cadena β está formada por 8 hélices α (A a H a partir del extremo N-terminal). La
cadena α posee 7 trozos de hélice α. Los aminoácidos se numeran según la posición en la
cadena o también en el segmento del cual forman parte.
Los residuos polares se disponen hacia la superficie, en contacto con el medio acuoso, y
los hidrófobos hacia el interior, contribuyendo a estabilizar el ensamble de las 4
subunidades y a formar el nicho o bolsillo. La cavidad destinada al hemo se encuentra en
el espacio entre las hélices E y F de cada cadena.
Estructura cuaternaria hemoglobina
Las 4 cadenas se ensamblan para formar un conjunto compacto, casi esférico, con una
cavidad a lo largo del eje central de la molécula.
Cada una de las cadenas forma un nicho en el cual se aloja el hemo, que se coloca con
sus dos restos propionilo dirigidos hacia afuera. Los grupos hemo quedan bien separados
entre sí.
Las uniones de las 4 cadenas son más firmes para las subunidades diferentes, unidas por
puentes de hidrógeno o interacciones hidrofóbicas, que para las iguales, unidas por
puentes salinos (atracciones electrostáticas).
Funciones
La hemoglobina se une reversiblemente al oxígeno para formar oxihemoglobina. Una
molécula de Hb reacciona con 4 de oxígeno.
El curso de la reacción depende de la presión parcial de oxígeno en el medio. Unn
aumento de presión desplaza la reacción hacia la derecha. A una presión de 100 mm de
Hg la hemoglobina se satura casi completamente con oxígeno.
Curva de disociación del oxígeno de hemoglobina
La relación entre tensión de oxígeno y proporción de oxihemoglobina formada se describe
en la curva de disociación. El eje de las x nos marca los valores de la presión de oxígeno,
y el eje de las y el porcentaje de hemoglobina formado.
Se obtiene una curva de tipo sigmoidea, a bajas presiones de oxígeno es muy pobre el
ascenso, pero por encima de los 10 Torrs la curva se eleva bruscamente. A partir de 60
Torrs se alcanza cerca del 90% de saturación y la curva tiende a horizontal.
Con mioglobina la curva tiene un aspecto muy diferente. Su curva es hiperbólica, asciende
muy rápidamente a presiones reducidas de O
2
.
Estas curvas muestran la mayor afinidad por el O
2
de la mioglobina respecto a la
hemoglobina. A 10 Torrs más del 85% de la mioglobina está saturada, mientras que el
5% de la Hb se convirtió en oxihemoglobina. La mioglobina no sería útil como
transportador de oxígeno ya que a la presión de los capilares no cedería su oxígeno.
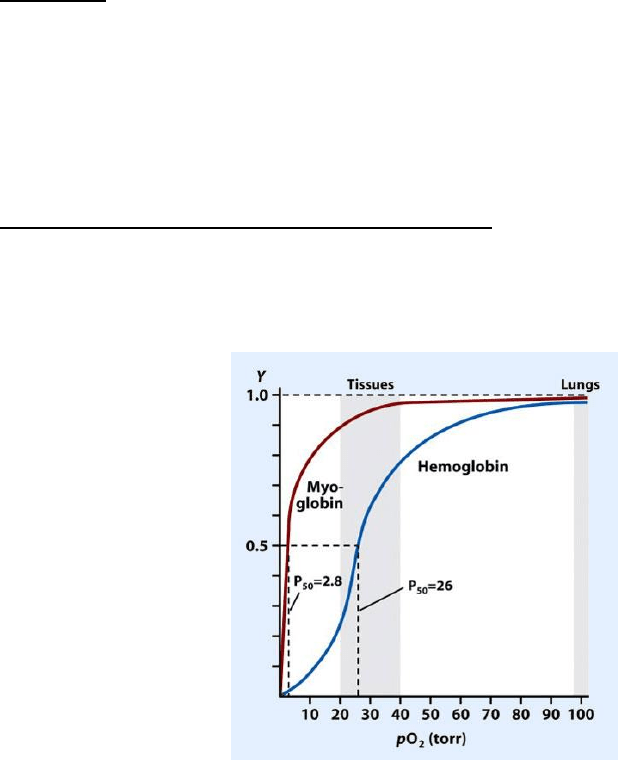
Hemoglobina Fetal
En la hemoglobina fetal, el efecto que toma el oxígeno se lo saca de la sangre materna,
que circula por la placenta, por donde el feto puede oxigenarse, tomando por la alta
afinidad que presenta la hemoglobina fetal, esta gran afinidad se da por la cadena γ.
Representa la cantidad de concentraciones de cadenas polipeptídicas a lo largo del
desarrollo del niño. En la línea central representa el nacimiento. Las primeras semanas de
gestación vemos que están presentes otras cadenas polipeptídicas (ε y ζ), aumentan la α
y la γ. Llegado el 3er trimestre comienza la síntesis de cadena polipeptídica β, que se
correlaciona con una degradación de las cadenas γ; y en el momento del nacimiento se
intercambian estas dos cadenas, esto por el contacto de los pulmones del bebé con el aire
atmosférico.
Después de la concepción, aparece la síntesis de las globinas ζ, ε y α. Al poco tiempo de
la concepción comienza a sintetizarse la globina de tipo γ, y cerca del nacimiento esta
disminuye su concentración. Mientras esta disminuye aumenta la globina β, que al nacer
aumenta y forma la hemoglobina característica en el ser humano α2β2. Al momento del
nacimiento comienza a desarrollarse la globina δ, que es la que perdurará todo el tiempo
para formar la hemoglobina α2δ2, que corresponde a la Hb A2.
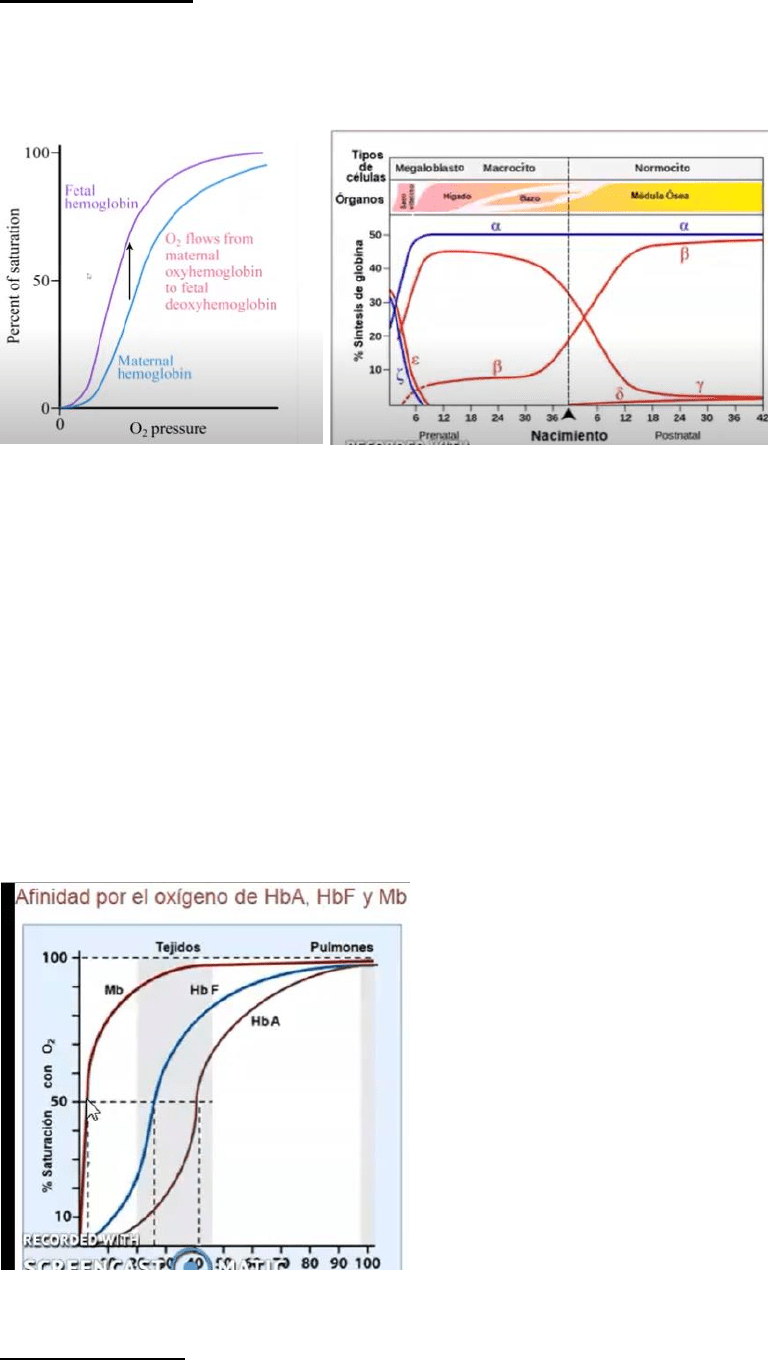
Efecto cooperativo
La mioglobina tiene la función de almacenar
el oxígeno en el músculo. Este tipo de
globina no presenta forma sigmoidea, sino
hiperbólica, debido a que solamente está
formada por una cadena, y su afinidad es
mayor que la Hb F y la Hb A; esto le da la
propiedad a la Hb A de transferirle el
oxígeno a la Hb F o a la mioglobina
fácilmente.

En la forma desoxigenada, las 4 cadenas de la Hb se mantienen estrechamente asociadas:
las 2 cadenas α y las 2 β se unen entre sí mediante enlaces salinos, dando una
conformación tensa, que dificulta el acceso de oxígeno a la cavidad ocupada por el hemo.
En esta forma el ion Fe+2 está unido por su 5ta posición a la histidina de las cadenas de
globina y se encuentra ligeramente desplazado del plano hemo. Cuando llega una
molécula de oxígeno y se une al Fe+2 por su 6to enlace se produce una tracción que lleva
al átomo de Fe+2 al centro del anillo del hemo. Esto produce un acercamiento de las
hélices E y F, y un cambio conformacional en toda la subunidad polipeptídica (se
transfiere a las demás), se altera la disposición de las subunidades y se rompen puentes
salinos intercatenarios, terminando en una conformación relajada. Este fenómeno en el
que una de las subunidades modifica su forma y transmite el cambio a las demás,
tornándolas receptivas para el O
2
recibe el nombre de interacción hemo-hemo o efecto
cooperativo. También se cumple a la inversa.
Este efecto cooperativo también se ha observado en enzimas, ocurriendo sólo en
moléculas oligoméricas.la mioglobina NO muestra efecto cooperativo.
Causas que favorecen la disociación de la Hb con el O2 (desviación hacia la derecha
de la curva): aumento de presión de CO2, de temperatura o de 2,3 BPG (2,3
bifosfoglicerato), o bajada de pH.
La acción de pH y CO
2
sobre la unión de O
2
y Hb se denomina efecto Bohr. A él se debe
que la oxihemoglobina libere su ocígeno con más facilidad a nivel de los tejidos, donde
la presión CO
2
es elevada y el pH más bajo.
2,3 bifosfoglicerato
Sustancia presente en glóbulos rojos. Se introduce en la cavidad central de la molécula de
Hb, establece enlaces con las 2 cadenas β y contribuye a estabilizar la molécula en la
forma T. Esto resulta en disminución de afinidad por el oxígeno a bajas presiones de este
gas.
La presencia de 2,3 BPG en los hematíes, al disminuir la afinidad de la Hb por O
2
,
favorece la liberación de éste a nivel de los tejidos. A nivel clínico:
Hipoxia: uno de los mecanismos de adaptación a condiciones de hipoxia consiste
en una disminución de la afinidad de la Hb por el O
2
para que este sea más
fácilmente liberado en los tejidos. Esto se logra aumentando la concentración de
BPG.
Transfusiones: se le agrega solución anticoagulante. En estas condiciones, la
concentración de BPG disminuye progresivamente. Debido al bajo tenor de BPG
la Hb de los hematíes inyectados no liberan oxígeno en los tejidos con la eficiencia
necesaria.
Hb F: la hemoglobina fetal tiene mayor afinidad por oxígeno que la HbA1. La
diferencia entre HbA y HbF se debe a la menor tendencia de ésta a unirse al BPG
y, en consecuencia, no experimenta disminución marcada de la afinidad por el O
2
a presiones relativamente bajas del gas.

Estas acciones, en las que la unión de una sustancia produce cambios conformacionales
que afectan el funcionamiento de la molécula, reciben el nombre de efectos alostéricos y
resultan de acciones cooperativas.
Transporte de anhídrido carbónico
La hemoglobina participa en el transporte de CO2. El 5% del total de CO2 vehiculizado
por sangre y liberado en el pulmón se transporta en forma de carbamino (Hb-NH-COOH).
Cuando la sangre llega a los pulmones la formación de oxihemoglobina favorece la
liberación del CO2 del Carbamino, acción inversa al efecto Bohr
DERIVADOS DE HEMOGLOBINA
Carboxihemoglobina
Compuesto resultante de la unión de hemoglobina con monóxido de carbono. La
hemoglobina tiene mayor afinidad por monóxido de carbono que por oxígeno, ya que este
primero es tóxico para el organismo. La carboxihemoglobina tiene color rojo cereza.
Metahemoglobina
Grupo prostético hematina o ferrihemo. La conversión del Fe+2 en Fe+3 inhabilita a la
hemoglobina para el transporte de oxígeno. Tiene color marrón oscuro.
El hierro del hemo se mantiene en estado ferroso por:
Residuos de aminoácidos no polares en nichos de la molécula de Hb.
Sistemas reductores en el glóbulo rojo que impiden la elevación de los niveles de
metahemoglobina.
Defectos genéticos determinan cambios en el entorno hidrofóbico del hemo o afectar
enzimas del sistema reductor y producir metahemoglobinemia. También puede darse por
nitrofenoles, anilina o fármacos sulfonamidas.
Hemoglobina A
1c
Se produce por glicosilación. Se genera lentamente dentro de los glóbulos rojos por
reacción entre la Hb y glucosa-6-fosfato, cuyo resultado es la formación de cetoamina
(amino-1-desoxifructosa) en el extremo N-terminal. En pacientes diabéticos se
encuentran cantidades elevadas de HbA1c.
HEMOGLOBINAS ANORMALES O HEMOGLOBINOPATÍAS
Se dan por mutaciones de los genes que sintetizan las cadenas. Se la designa con letras,
países, nombre del paciente portador, o del grupo étnico donde se las descubrió.
Se observaron distintos tipos de alteraciones:
Sustitución de 1 ó 2 aminoácidos por otro/s.
Falta de uno o más aminoácidos en la cadena.
Presencia de cadenas híbridas, formadas por trozos de dos subunidades
polipeptídicas distintas.
Presencia de cadenas más larga de lo normal.
Síntesis disminuida o nula de un determinado tipo de cadena (talasemias).
El simple reemplazo de un solo aminoácido por otro puede ocasionar un comportamiento
anómalo de la Hb. Cuando el cambio altera la secuencia en posiciones críticas para la
conformación y funcionamiento de la molécula se puede producir:
1. Inestabilidad de la hemoglobina: con tendencia a precipitar dentro de los
eritrocitos. Promueve la destrucción precoz de los glóbulos rojos, con un cuadro
de anemia hemolítica. Ejemplo: Hemoglobina S o anemia falciforme.
Anemia Falciforme
Es de origen genético, se hereda de forma autosómica recesiva. Se modifica el gen
de la cadena β de la Hb A que tiene una secuencia CTT, que se va a transcribir a
GAA, y traducir a glutamato; a CAT, que cuando se transcribe forma GUA, y se
traduce como valina. Esta última es la Hb S.
Esta hemoglobina va a tener 2 cadenas α y 2 β, pero en la β, en su posición 6 va a
estar la valina en vez del glutamato, adquiriendo el eritrocito forma de hoz o
falciforme.
2. Modificación de aminoácidos en el entorno del hemo. Se facilita la oxidación del
Fe+2 a Fe+3 generando metahemoglobinemia. Por ejemplo: hemoglobina M.
3. Cambios de residuos aminoacídicos en zonas de contacto entre subunidades
pueden anular los efectos cooperativos o alostéricos. La hemoglobina muestra
mayor afinidad por el O
2
o no responde al efecto Bohr. Afecta la capacidad para
liberar el oxígeno en los tejidos.
4. Sustitución de residuos involucrados en la unión de BPG e imposibilidad de fijar
este compuesto. Produce aumento de la afinidad de la Hb por el O
2
y la liberación
de este gas en los tejidos está dificultada.
Talosemias: enfermedad genética donde la síntesis de una cadena está reducida o falta
totalmente. Comprende anomalías en la forma de eritrocitos o presencia en ellos de
cuerpos de inclusión, destrucción prematura de hematíes y anemia muy severa. Las
cadenas polipeptídicas de la Hb tienen una estructura primaria idéntica a las normales, la
anomalía consiste en la aparición de homotetrámeros o alteración de la proporción de los
tipos de Hb.
Talasemias α: afecta la síntesis de la cadena α en estos casos se puede encontrar HbH
(β4) y Hb Bart (γ4). Estos tienen mayor afinidad por el O2, no presentan efecto Bohr ni
responden a BPG.
Talasemias β: producen un aumento en la producción de otras subunidades, como las
cadenas δ, con aumento de la proporción de HbA2. EN otros casos puede persistir la
síntesis de cadenas γ y, con ello, Hb F. Los pacientes homocigotos padecen talasemia β
mayor, y heterocigotos la menor.

PROTEÍNAS DEL PLASMA SANGUÍNEO
Plasma sanguíneo es el medio líquido en el cual están suspendidos los elementos formes
de la sangre. Los primeros métodos de fraccionamiento de proteínas permitieron separar
albúminas y globulinas.
Entre las globulinas se aisló el fibrinógeno, de menor solubilidad, que participa en la
coagulación de la sangre. En la coagulación de la sangre el fibrinógeno se convierte en
fibrina, que forma la red que aprisiona los elementos formes.
El hígado es el órgano exclusivo de la producción de albúmina, fibrinógeno, protrombina
y mayor parte de las globulinas α y β. Las globulinas γ se forman en células plasmáticas
derivadas de linfocitos B. Todo trastorno en el hígado se manifiesta por alteraciones de
la composición proteica del plasma. Dichas alteraciones se llaman disproteinemias. La
síntesis de estas proteínas requiere de aminoácidos provistos normalmente por la dieta.
Las funciones generales de lsa proteínas plasmáticas son el mantenimiento de la volemia
y función amortiguadora, ya que ejercen una acción buffer. Esta propiedad depende de la
presencia de restos de histidina.
Electroforesis de proteínas del suero
A determinado Ph las proteínas pueden manifestar cargas eléctricas de distinto signo y
magnitud, gracias a esto migran a diferente velocidad hacia uno u otro electrodo cuando
se establece un campo eléctrico en el medio.
Fundamento del fraccionamiento electroforético: Si 2 o más proteínas cuyos pHi son
diferentes se disuelven en un medio de determinado pH y las diferencias entre este pH y
el pHi de cada proteína son distintas, el valor de sus cargas netas y sus velocidades de
migración en el campo eléctrico serán también distintos.
Los métodos más difundidos utilizan un papel de filtro, acetato de celulosa o gel de agar
como medio soporte sobre el que se realiza la migración. En general, en estos medios se
separan 5 fracciones proteínicas en el suero sanguíneo. Estas fracciones se denotan como
bandas cuando se tiñe, mediante un colorante, el material sobre el que se realizó la
migración. La intensidad de coloración y la amplitud de cada banda son proporcionales a
la cantidad de prteínas contenida en cada fracción. Por densitometría, procedimiento que
registra la intensidad de la tinción en los distintos sectores del material de soporte, se
obtiene un trazado que dibuja una serie de ondas correspondencia con cada una de las
bandas. La superficie de cada onda es proporcional a la intensidad de color y el tamaño
de las bandas. A este trazado se le llama proteinograma electroforético.
Generalmente se realiza a Ph 8.6, ya que todas las proteínas séricas poseen carga
electronegativa y migran hacia el ánodo en estas condiciones. La fracción más rápida es
la albúmina y detrás de ellas marchan α1, α2, β y γ.
En las técnicas de electroforesis, el único factor determinante de la separación de las
proteínas es su carga eléctrica.
En resumen: Se ponen 2 cubatas con solución buffer de pH 8.6, con un cátodo y un ánodo.
Hay un puente donde se coloca el soporte, acetato de celulosa, y los bordes van a estar
sumergidos en el buffer. En un punto del soporte se aplicará la muestra, las proteínas que
tengan pHi por debajo se cargan negativamente y van a migrar hacia el ánodo, y las que
tengan uno mayor hacia el cátodo. Las proteínas que migran más rápido son aquellas que
van hacia el ánodo. Retiramos el soporte de las cubatas y lo ponemos en otras cubatas con
colorante, lo dejamos colorear, lo retiramos y lo decoloramos.
Una vez obtenida la tira decolorada se la va a transparentizar, de modo que pueda pasar
un haz de luz y nos pueda dar en el densitómetro un gráfico con la concentración de cada
proteína
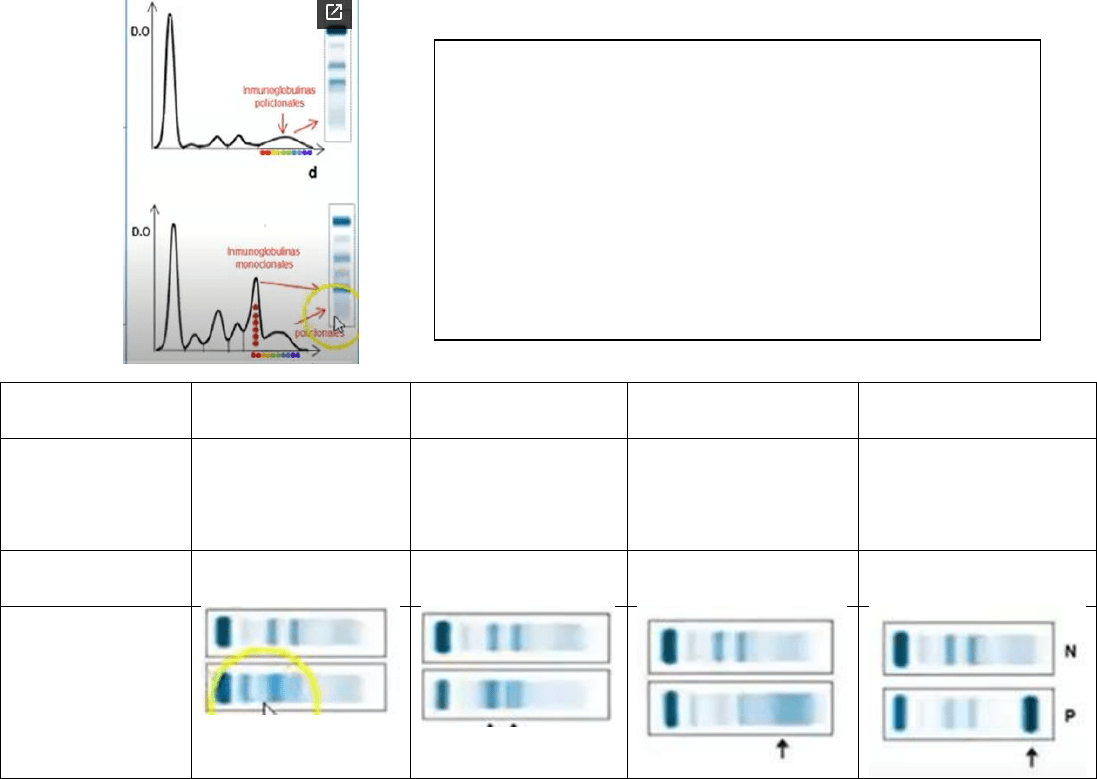
Proteinograma
Inflamación aguda
Síndrome
nefrótico
Inflamación/
cirrosis/ infecciones
Mieloma
AUMENTO
.α1 y α2 globulinas
por aumento de α1
antitripsina y
haptoglobina.
α2 globulinas y β
Inmunoglobulinas
policlonales en zona γ
Inmunoglobulinas
monoclonales en zona
γ
DISMINUCIÓN
Albúmina
Albúmina y α11
globulina.
Albúmina
Albúmina y α
globulinas
IMÁGEN
Principales proteínas del plasma sanguíneo
ALBÚMINA
o Más abundante.
o Proteína globular formada por una cadena polipeptídica.
o Presencia de muchos grupos reactivos, lo que congiere capacidad para
unirse a gran variedad de sustancias.
o Funciona como activo transportador de distintos compuestos.
GLOBULINAS
o Contiene proteínas conjugadas de 2 tipos: glicoproteínas y lipoproteínas.
Fracción o banda monoclonal de Ig:
Forman un pico alto de base estrecha y gran densidad
En el proteingrama se identifican con actividad
electroforética homogénea
Fracción o banda policlonal de Ig:
Forman una curva de base ancha y baja densidad
En el proteinograma se identifican con actividad
electroforética heterogénea.

GLOBULINAS
Globulinas α1
Globulinas α2
Globulinas β
Globulinas γ o inmunoglobulinas
Α1-antiproteinasa: o antitripsina, es
la más abundante. Uno de los
principales inhibidores de serina
proteasa. Protege los tejidos de la
acción de proteasas. El hábito de
fumar favorece la oxidación de un
resto metionina y la inactiva.
Orosomucoide: o glicoproteína ácida
α1. Aumenta en procesos
inflamatorios junto con la proteína C-
reactiva.
Protorombina: precursor de la
trombina, la cual cataliza la
conversión de fibrinógeno en fibrina.
Transcortina: encargada del
transporte de cortisol.
Ceruloplasmina: Contiene 6 átomos
de cobre por molécula. Tiene
actividad enzimática de ferroxidasa.
Haptoglobina: se une eventualmente
a la hemoglobina. Este complejo
impide que la pequeña cantidad de Hb
liberada por hemólisis intravascular
sea secretada por orina.
Α2-macroglobulina: homotetrámero.
Transporta parte del zinc del plasma.
Eritropoyetina: hormona que controla
la producción de glóbulos rojos.
Transferrina o siderofilina: cada
molécula fija dos átomos de hierro, es
transportadora del metal del plasma.
Β2-microglobulina:
Histocompatibilidad. Se encuentra en
membranas celulares.
Ig G: comprenden alrededor del 75%
de Ig. Presenta 4 subclases
ennumeradas del 1 al 4. Coef.
Sedimentación 7S.
Ig A: representan del 12 al 15%.
Presentan 2 subclases 1 y 2.
Coeficiente de sedimentación de 7 a
11S.
Ig M: 8% de las Ig. Se las designa
macroglobulinas.
Ig D: 1% de Ig.
Ig E: menos del 0.3%.
Por defecto genético se puede ser
incapaz de sintetizarlas formando
agamaglobulinemia o
hipogamaglobulinemia. En los
mielomas suelen aumentar las
inmunoglobulinas.
LIPOPROTEÍNAS
Encargadas del transporte de sustancias hidrófobas en el plasma. Son proteínas globulares donde los componentes lipídicos apolares se disponen en el interior
del complejo, rodeados por fosfolípidos, colesterol libre y proteínas, y las funciones polares al exterior. Las porciones proteica son heterogéneas y se las designa
con las letras A, B, C, D y E.
De acuerdo a su densidad se pueden reconocer 4 grupos de lipoproteínas plasmáticas:
Quilomicrones: no migran en el campo eléctrico. Transportan principalmente triacilgliceroles del intestino al sistema linfático. Las proteínas forman una
delgada película polar en su superficie.
Lipoproteínas de muy baja densidad (VLDL): se desplazan delante de las β, se las designa lipoproteínas pre-β. Ricas en triacilgliceroles.
Liporpoteínas de baja densidad (LDL): tiene movilidad de globulinas β, por lo que se las llama lipoproteínas β. Mayor proporción en colesterol.
Lipoproteínas de alta densidad (HDL): en electroforesis migran con la velocidad de globulinas α, por lo que se las llama lipoproteínas α.

APOPROTEÍNAS LIPÍDICAS
APO A
APO B
APO C
APO D
APO E
Apo AI: principal componente
de las HDL, menor en
quilomicrones y VLDL.
Activadora de la lectina-
colesterol aciltransferasa.
Apo AII: parte de las HDL.
Apo IV: sintetizada en mucosa
intestinal y está asociada a
quilomicrones.
Apo B-100: Sintetiazda en el
hígado. Abundante en LDL y
VLDL
Apo B-48: forma parte de los
quilomicrones. Sintetiza en el
intestino.
Apo CI a Apo CIII
Apo CII: activador de la
lipasa que hidrolisa
triacilgliceroles de
quilomicrones y VLDL.
En HDL. Favorece el
intercambio de ésteres de
colesterol y triacilgliceroles
entre VLDL y HDL.
componente menor en
quilomicrones, VLDL y
HDL. 4 subtipos de I a IV.
Participa en metabolismo,
especialmente ctabolismo, del
colesterol. También en
reconocimiento y captación
de lipoproteiínas.

HEMOGLOBINA.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.