
7/2/2020 Final A | Química (2019) | UBA XXI
https://www.altillo.com/examenes/uba/ubaxxi/quimica/quim_2019_fina.asp 1/6
Final A | Química (2019) | UBA XXI

7/2/2020 Final A | Química (2019) | UBA XXI
https://www.altillo.com/examenes/uba/ubaxxi/quimica/quim_2019_fina.asp 2/6
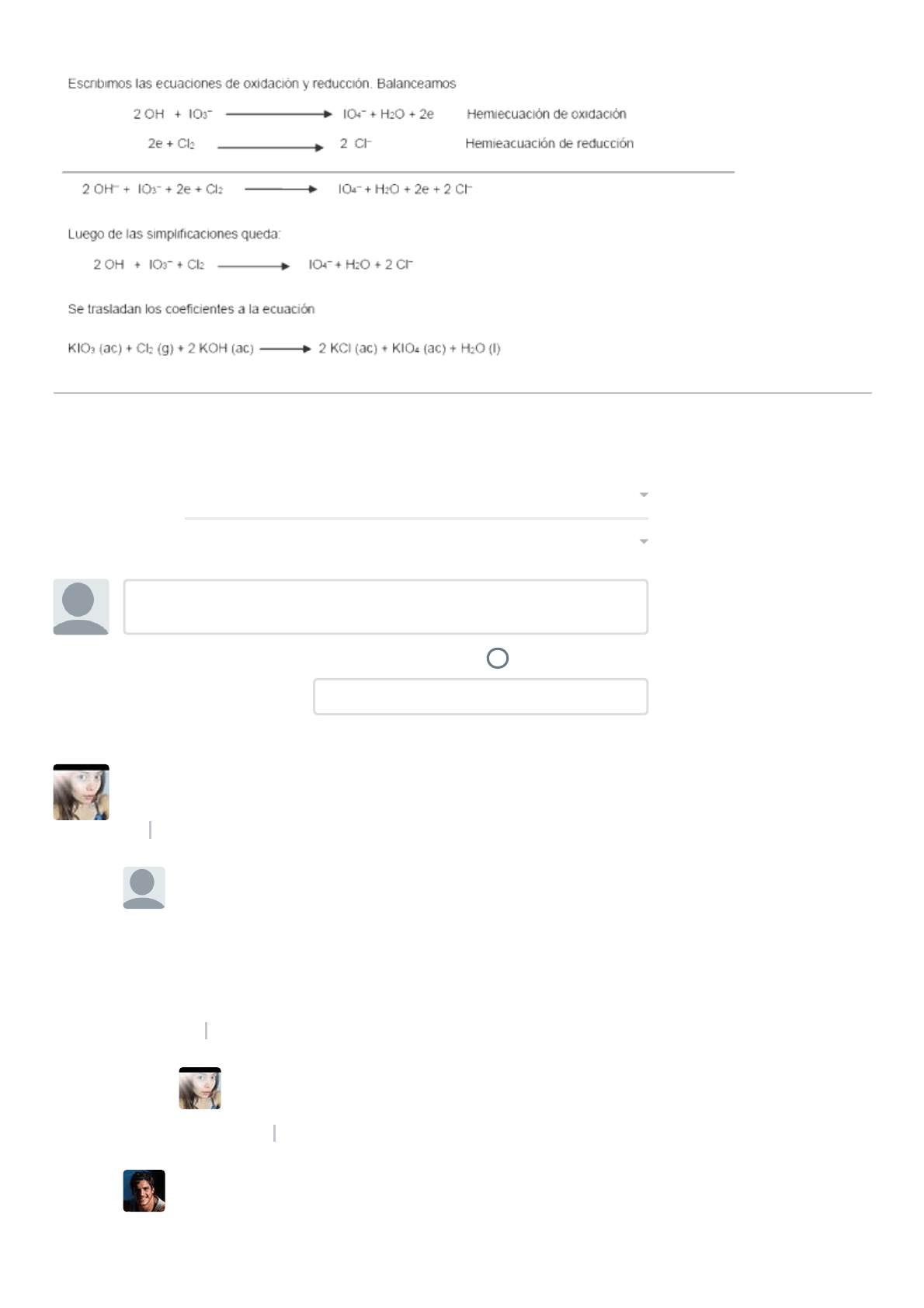
7/2/2020 Final A | Química (2019) | UBA XXI
https://www.altillo.com/examenes/uba/ubaxxi/quimica/quim_2019_fina.asp 3/6
Preguntas y Respuestas entre Usuarios:
20 Comentarios Altillo.com
Iniciar sesión
1
t Tweet f Compartir
Más antiguos primero
INICIA SESIÓN CON
O REGISTRATE EN DISQUS
Nombre
Unite a la discusión...
?
Jime Britos • hace 7 meses
• Responder •
Cómo se resuelve el 4b?
△
▽
Pilar • hace 7 meses
• Responder •
> Jime Britos
• (2× 6,02x10^23)= 1,20x10^24 catión Na => 78 g Na2S
En 2,80x10^23 -> X= 18,2 g Na2S
• 12 g sto => 100 cm3 sc
18, 2 sto => X= 151 cm3
Yo lo hice de esta manera y me dio la respuesta
△
▽
Jime Britos • hace 7 meses
• Responder •
> Pilar
Graciad
1
△
▽
Rodrigo Pithon • hace 7 meses> Jime Britos
Se hay 2,8.10^23 cátiones de Na en Na2S, es porque hay
1,4.10^23 en el compuesto (2,8.10^23 dividido por 2 ya que
son 2 Na).
Recomendar
5
Compartir ›
Compartir ›
Compartir ›

7/2/2020 Final A | Química (2019) | UBA XXI
https://www.altillo.com/examenes/uba/ubaxxi/quimica/quim_2019_fina.asp 4/6
• Responder •
)
Hace entonces la regla de 3 para hallar la cantidad de moles
de la molecula, que queda 0,233 moles. (1 mol = 6,02.10^23,
1,4.10^23 = 0.233 moles)
Despues halla la cantidad de moles por la concentracion 12%
m/V (12g----100ml) de Na2S. -> 1 mol ----- 78g (Na2S), x
mol ------- 12g = 0,154 mol de Na2S.
Al final hace la regla de 3 con los moles hallados en la
concentracion m/v para hallar el volumen necesario.
0,154 mol --- 100ml
0,233 mol --- x ml = 151 ml o cm^3.
Espero que entienda! Saludos y suerte
1
△
▽
Jime Britos • hace 7 meses
• Responder •
> Rodrigo Pithon
👍 muchas gracias!
△
▽
Barbara • hace 7 meses
• Responder •
Cómo se resuelve el 1a?
△
▽
kato kastro • hace 7 meses
• Responder •
> Barbara
Si, esta fácil: solo tienes que asociar el 2+ al X, con esto ya
sabes que tiene 2 e- adicionales osea que le restas a su
isoelectrón te dará el Sr y para el R es el Bromo puesto que
los halógenos son el el grupo VIIA y te dice q es mono-anión
por tanto solo gano 1. Y ahí ya tienes tu respuesta.
△
▽
laura valentina barragan
• hace 2 meses
• Responder •
> kato kastro
pero no entiendo como sabes que es Sr si no se nada
del elemento solo se que es isoelectronico con un
elemento que es isobarico con otro que tampoco dan
mas datos
1
△
▽
ceci • hace 2 meses
• Responder •
> laura valentina barragan
creo que cuando te da el isótopo se refiere al
más estable y en la tabla periódica abajo del
nombre de cada elemento dice cuánto es el
número del isótopo más estable
△
▽
Agustín Visini • hace 2 meses> ceci
Del elemento R se dan dos datos: es halógeno
con número másico A=79. Te fijas en la tabla
el grupo halógeno y buscás el elemento cuyo
Compartir ›
Compartir ›
Compartir ›
Compartir ›
Compartir ›
Compartir ›
7/2/2020 Final A | Química (2019) | UBA XXI
https://www.altillo.com/examenes/uba/ubaxxi/quimica/quim_2019_fina.asp 5/6
• Responder •
átomo pesa 79 uma: el Bromo. Sabemos que
el Bromo posee por número atómico Z=35 y
siendo estable posee igualmente 35
electrones. Sin embargo, el ejercicio plantea
que R (es decir, Bromo) no posee carga neutra
sino que es un anión (si no aclara divalente, se
presume monovalente) por lo cual nuestro
átomo de Bromo tendrá 36 electrones. Aquel
elemento cuyo catión divalente posee 36
electrones (ya que se lo busca isoeléctronico a
R, lo cual significa que posee igualdad de
electrones) es el elemento Estroncio.
△
▽
Celeste • hace 7 meses
• Responder •
Alguien sabe como se hace el 4 a ??
△
▽
kato kastro • hace 7 meses
• Responder •
> Celeste
Si mira, es fácil te dicen 9% m/m osea 9g de soluto cada
100g de solución. luego te dicen que se extrajeron 220 de
solución, eso te da 19.8 (220g sc x 9g st / 100g sc).
Entonces te dicen que se diluyeron hasta obtener 720ml de
solución. Como tu quieres saber el la molaridad (osea en
1000ml) entonces haces una nueva regla: [1000ml sc x 19.8g
st / 720ml sc]= 27,5g de soluto. Este es el valor de la
molaridad, que solo resta pasarlo a moles: {n=m/M}
entonces [27,5g st / 111g.mol ]=0,247M y este es el
resultado. (los 111 los da el ejercicio es el peso molar de
CaCl2; otro modo de hacerlo es convertir directamente a
moles los 19.8g para cuando lo multipliques por 1000ml y lo
dividas por 720ml te debería dar igual.
1
△
▽
ami • hace 7 meses
• Responder •
alguien pudo resolver el 4 a
△
▽
ami • hace 7 meses
• Responder •
alguien `pudo resover el 4a
△
▽
July Bianco • hace 2 meses
• Responder •
Es el mismo examen para el final del 2do cuatrimestre?
△
▽
Marti • hace 2 meses
• Responder •
Hola alguien me explicaria el 2.b) ?
△
▽
Compartir ›
Compartir ›
Compartir ›
Compartir ›
Compartir ›
Compartir ›
Compartir ›

7/2/2020 Final A | Química (2019) | UBA XXI
https://www.altillo.com/examenes/uba/ubaxxi/quimica/quim_2019_fina.asp 6/6
espo de Co pa t
Final C _ Quimica (2018) _ UBA XXI.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.