1
EP 9 – TEMA 6: REACCIONES DE COMPUESTOS CARBONÍLICOS I
PROBLEMA 1
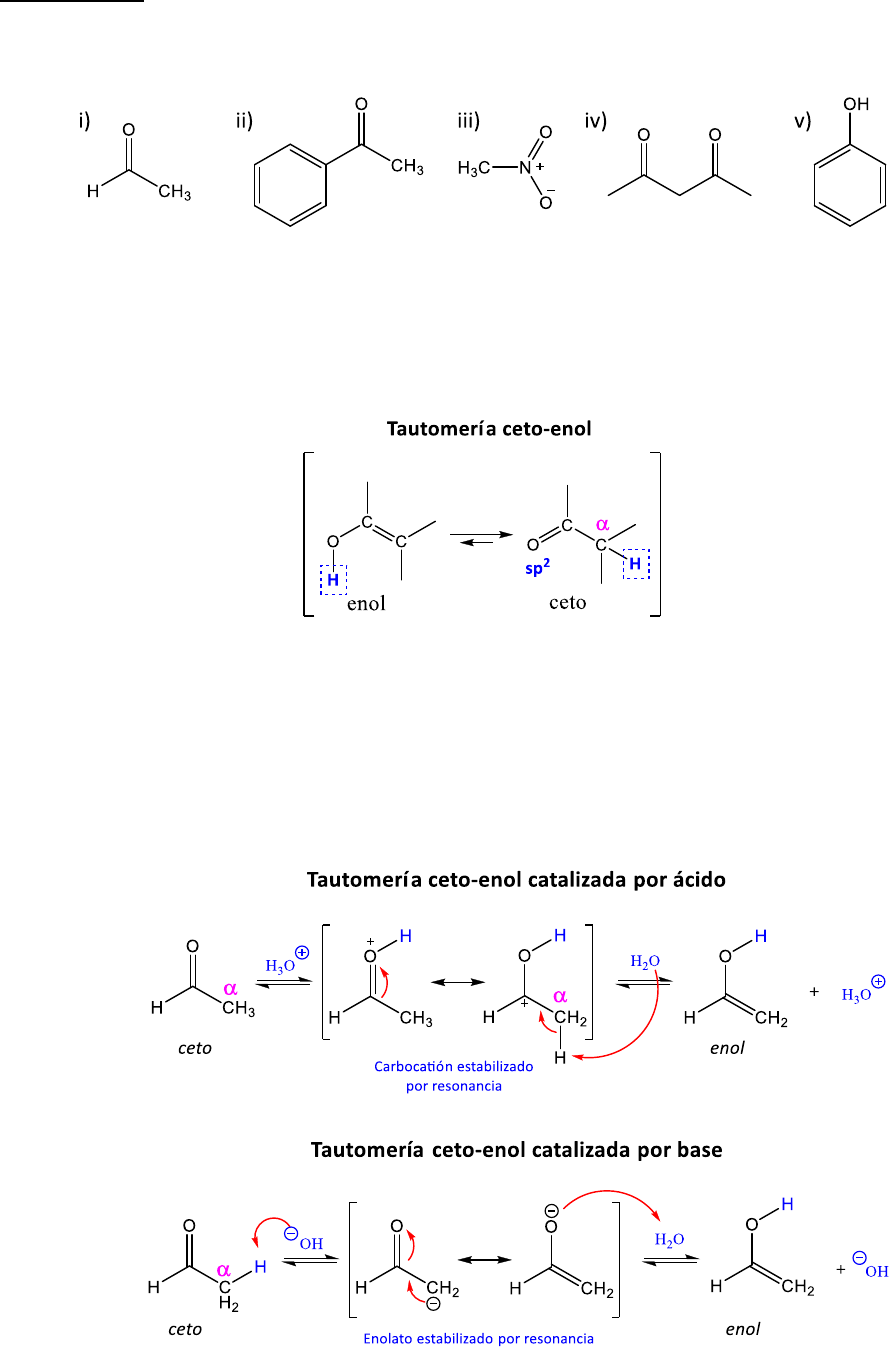
a) Escriba las ecuaciones de tautomería de los siguientes compuestos e indique cuál es el
tautómero más estable:
Un equilibrio de tautomería es un equilibrio de isomerización en el cual los tautómeros ceto y enol (ambos
isómeros estructurales) se interconvierten debido a la transferencia de un H entre el C
𝛼
a un carbonilo y un
O sp
2
, a la vez que ocurre la relocalización del doble enlace. En general, este equilibrio está desplazado hacia
el isómero ceto más estable. La tautomería ceto-enol puede estar catalizada tanto por ácidos como por
bases.
En los siguientes ejercicios se muestran los equilibrios de tautomería en medio ácido y básico.
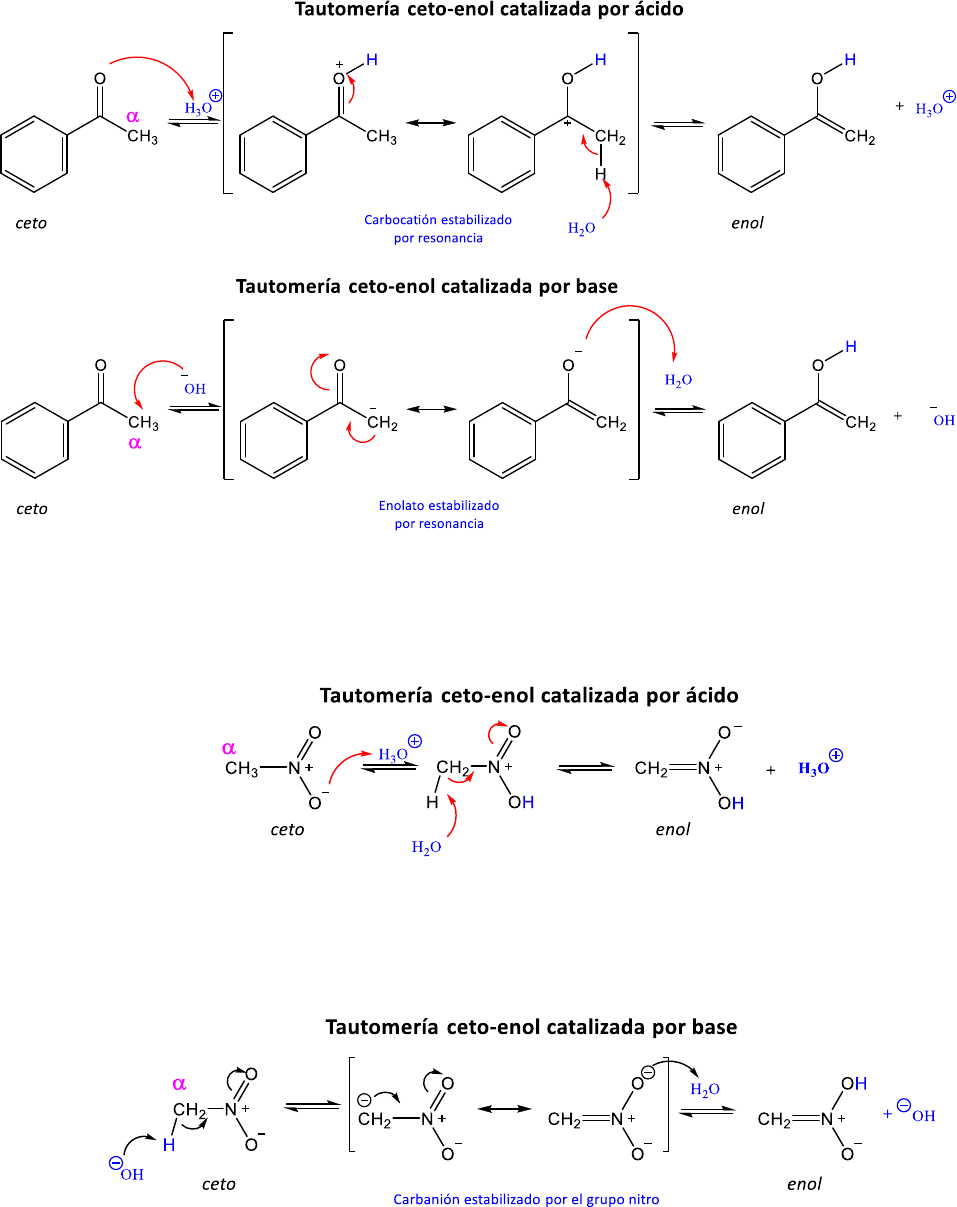
i) En el acetaldehído sólo hay un C
𝛼
vecino al carbonilo con H enolizables, es decir, protones que pueden
ser transferidos al O sp
2
del carbonilo. Las tautómeros ceto y enol del acetaldehído están en equilibrio tanto
en condiciones ácidas como básicas y predomina el tautómero ceto. Sin embargo, los intermediarios son
diferentes según las condiciones de reacción. En medio ácido se forma un carbocatión estabilizado por
resonancia, mientras que en medio básico se forma el anión enolato, un carbanión estabilizado por
resonancia. El enolato es un intermediario importante porque es nucleofílico.
2
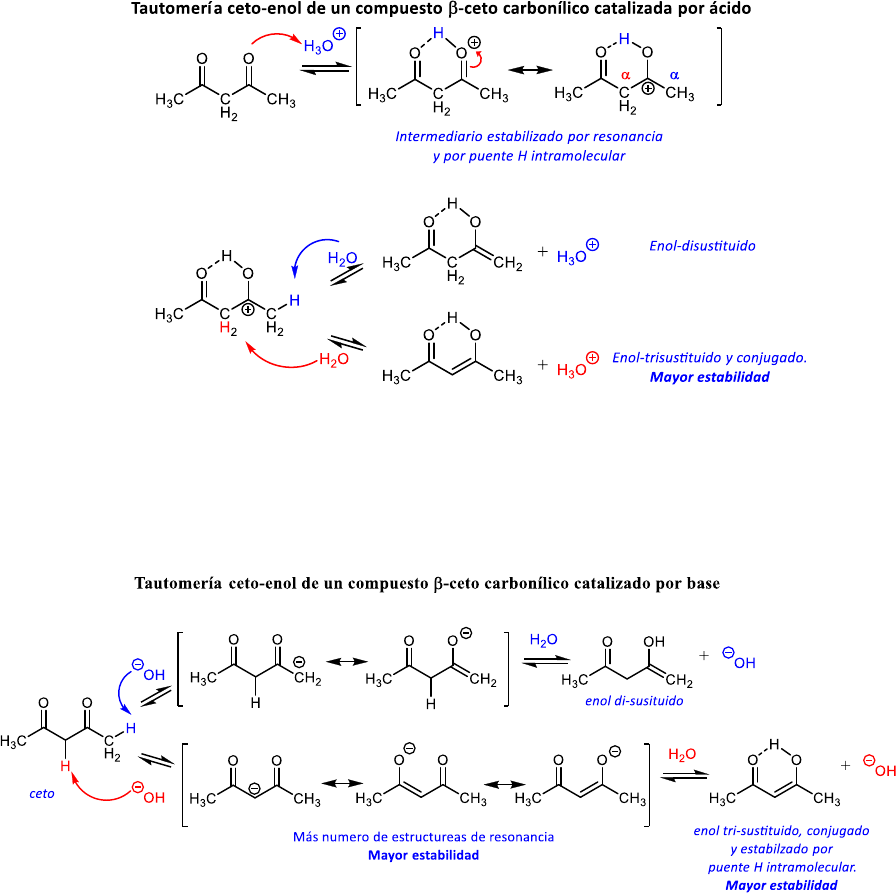
ii) En la acetofenona sólo hay un C
𝛼
vecino al carbonilo con H enolizables. Las tautómeros ceto y enol
de la acetofenona están en equilibrio tanto condiciones ácidas como básicas mediante un mecanismo igual
al descripto en el inciso (i). En ambos medios predomina el tautómero ceto más estable
.
iii) El nitrometano, aunque no sea un compuesto carbonílico, también presenta tautomería ceto-enol
catalizada tanto por ácidos como por bases. Uno de los H del metilo puede ser transferido a un O del grupo
nitro. En ambos medios predomina el tautómero “ceto” (con +N=O) más estable.
El grupo metilo presenta H enolizables que pueden ser abstraídos por una base dado que se forma un
carbanión estabilizado por el grupo nitro vecino fuertemente tomador de e
−
. En medio básico, el
nitrometano es nucleofílico porque está en equilibrio con su carbanión.
3
iv) En el caso de este compuesto
𝛽
-ceto carbonílico, todos los C
𝛼
a los grupos carbonilo presentan H
enolizables. Como la molécula es simétrica, los CH
3
terminales son equivalentes y generan un mismo enol.
En soluciones ácidas, los compuestos
𝛽
-ceto carbonílicos están en equilibrio con su forma protonada, la cual
predomina porque, además de estar estabilizada por resonancia, presenta estabilización adicional por la
formación de un puente de hidrógeno intramolecular entre los grupos carbonilo cercanos. En el equilibrio de
tautomería, se observa que la pérdida de dos H diferentes es posible (marcados en rojo y azul), lo cual
genera dos enoles isoméricos de diferente estabilidad. El equilibrio de tautomería del compuesto di-
carbonílico está desplazado hacia el enol tri-sustituido porque tiene un doble enlace interno, el cual se
encuentra conjugado con el grupo carbonilo, y además presenta estabilidad adicional debido al puente de
hidrógeno intramolecular.
En medio básico, los protones del metileno son más ácidos y se enolizan primero porque el enolato que se
forma es más estable, ya que se encuentra estabilizado por resonancia con los dos grupos carbonilo. Este
tipo de estabilización no es posible si se desprotona uno de los grupos metilo terminales. Tal como ocurre en
medio ácido, en medio básico el equilibrio de tautomería del compuesto di-carbonílico también está
desplazado hacia el enol tri-sustituido más estable.
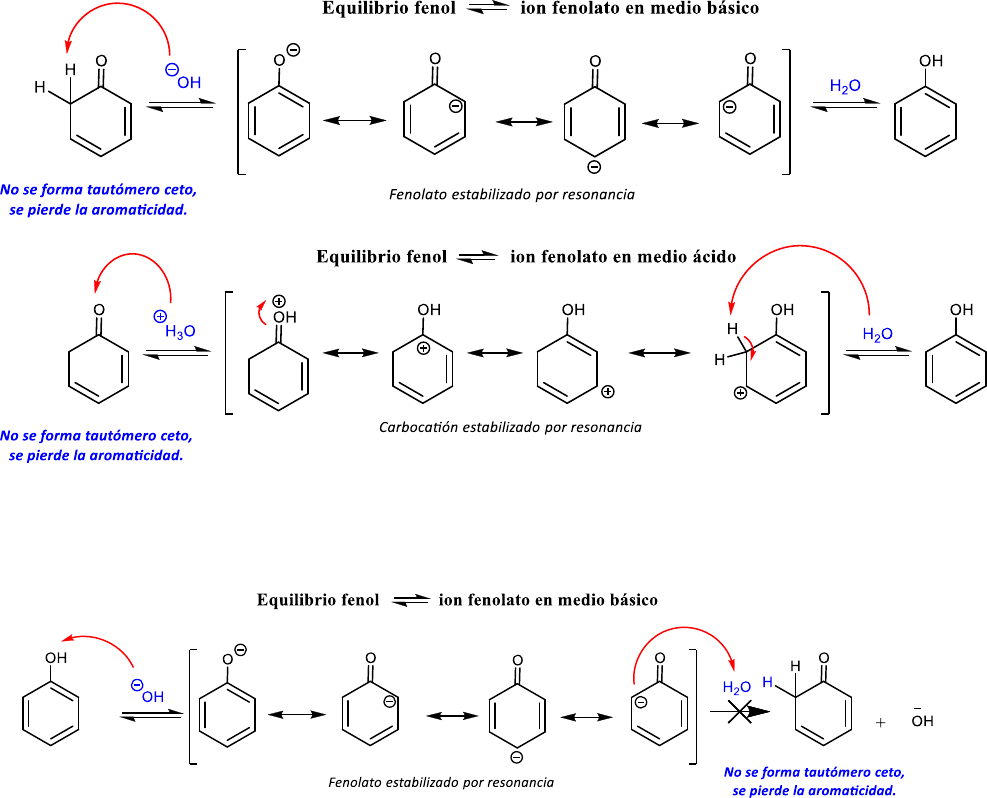
v) En medio básico el fenol está en equilibrio con su base conjugada fenolato, la cual se encuentra
estabilizada por resonancia. La protonación del C2 del fenolato para generar el tautómero ceto implicaría la
formación de un C sp
3
y la pérdida de la aromaticidad del anillo benceno. Se concluye que el equilibrio de
tautomería del fenol está totalmente desplazado hacia los tautómeros aromáticos enol (fenol) en medio
ácido y enolato (fenolato) en medio básico y la formación del tautómero ceto no aromático es despreciable.
4
Con la finalidad de continuar con el análisis de los equilibios ceto-enol, en el caso del fenol (enol) podríamos
partir de su forma ceto (inexistente). Los equilibrios correspondientes en medio básico y ácido serían los
siguientes:
Debido a la estabilidad del fenol dada por conjugación, este equilibrio se encuentra desplazado hacia el
tautómero enol, y esto resulta ser una evidencia por la que la forma ceto no existe.
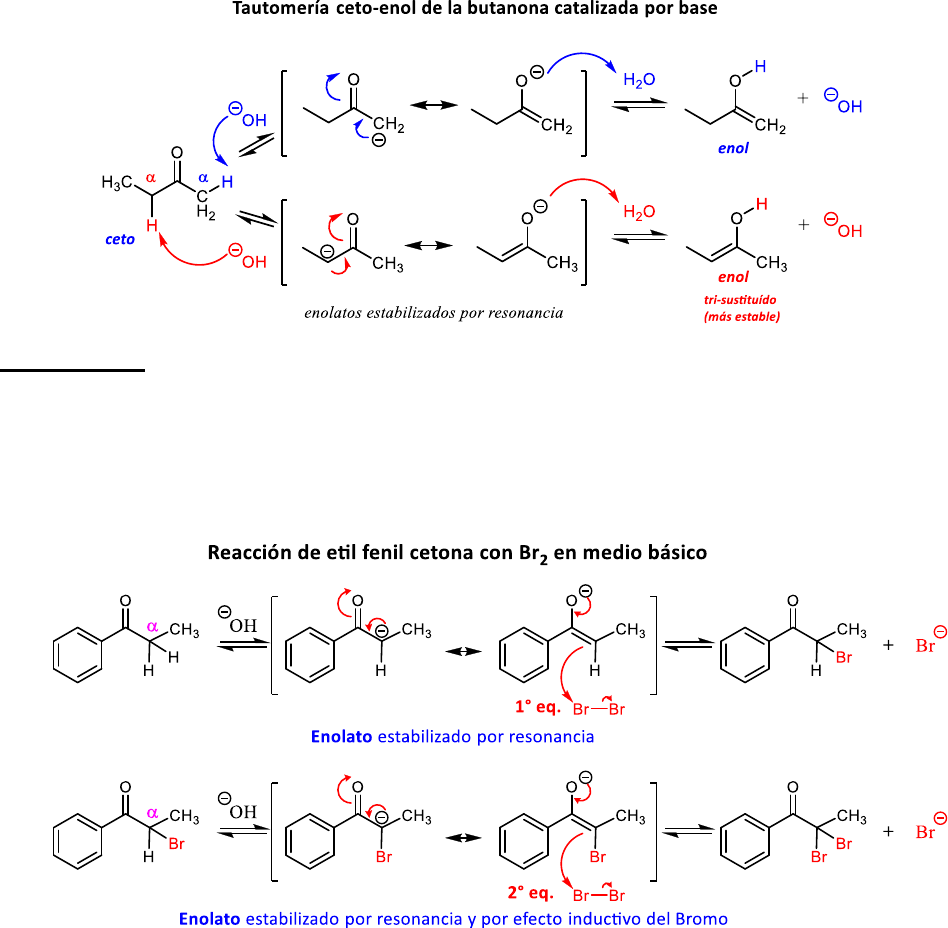
b) ¿Cuáles son los dos enoles posibles que se encuentran en equilibrio con la butanona? ¿Cuál es
más estable?
Los C en posiciones
𝛼
al carbonilo de la butanona tienen H enolizables. En el equilibrio de tautomería
catalizado por base (que se muestra en la figura de abajo), se observa que es posible la pérdida de dos
protones diferentes (marcados en rojo y azul), lo cual genera dos enoles con diferentes grados de
sustitución. Entre estos dos enoles, el tri-sustituido es más estable.
5
PROBLEMA 2
a) Explique por qué un mol de Br
2
y un mol de C
6
H
5
COCH
2
CH
3
en medio básico, producen 0,5
mol de C
6
H
5
COCBr
2
CH
3
y 0,5 mol de C
6
H
5
COCH
2
CH
3
.
Los enolatos son intermediarios importantes porque se comportan como nucleófilos pudiendo reaccionar
con halógenos electrofílicos X
2
.
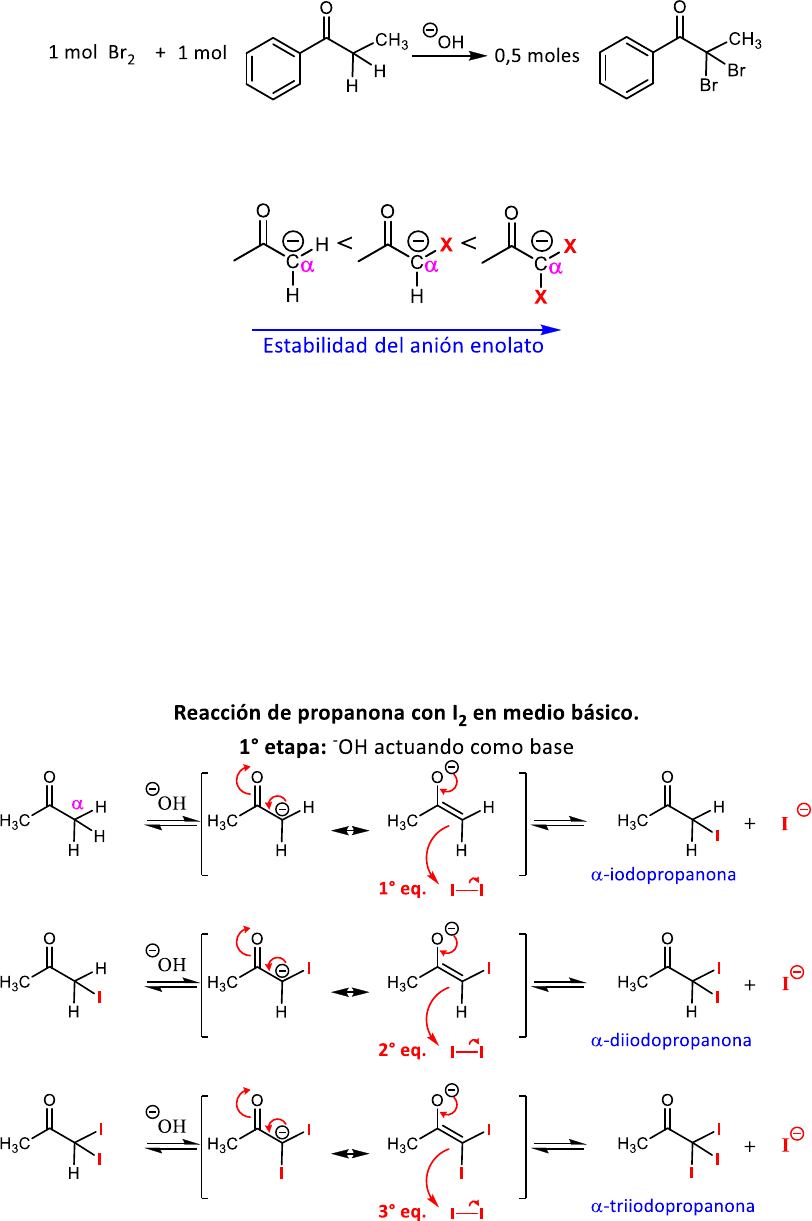
En medio básico, la base abstrae uno de los H enolizables unidos al C
𝛼
al carbonilo de etil fenil cetona y se
forma el enolato estabilizado por resonancia.
El enolato es nucleofílico y reacciona con el primer mol de Br
2
formándose el producto de sustitución
𝛼
mono-bromado.
El producto mono-bromado sigue teniendo un H enolizable unido al C
𝛼
y en las condiciones básicas este
protón es abstraído por la base. Este segundo enolato se forma más rápido que el primero ya que el C
tiene un nuevo sustituyente que es tomador de electrones y el anión presenta una estabilización adicional
por efecto inductivo del Br unido al carbanión.
Finalmente, la reacción del enolato con el segundo mol de Br
2
genera el producto de sustitución en
𝛼
di-
bromado.
Notar que para obtener el producto dibromado, 1 mol de la cetona reacciona con 2 moles de Br
2
. Por lo
tanto, a partir de la estequiometría de la reacción, 1 mol de Br
2
reaccionará con 0,5 moles de la cetona
generando 0,5 moles del producto di-bromado y 0,5 moles de la cetona quedan sin reaccionar dado que Br
2
es el reactivo limitante.
6
La razón por la cual no se obtiene como único producto a la cetona mono-bromada se debe a que en medio
básico la reactividad de un enolato aumenta mientras más halógenos tiene en su estructura.
b) Proponga un mecanismo para la adición de I
2
a propanona, en medio ácido y básico.
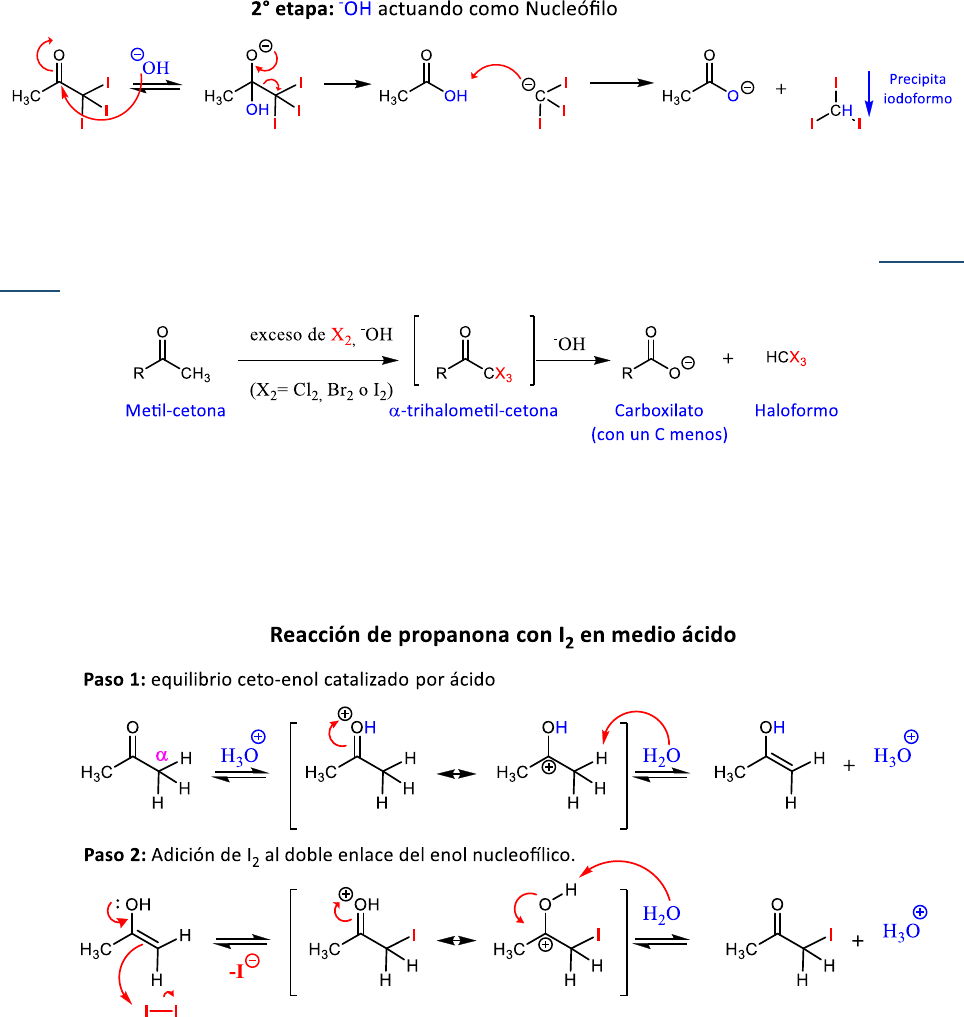
La propanona posee dos grupos metilo con tres H enolizables cada uno. En medio básico, la base abstrae el
primer H enolizable de uno de los C
𝛼
y se establece el equilibrio con su enolato y su tautómero enol.
El enolato de la propanona es nucleofílico y en exceso de I
2
ocurre un ataque nucleofílico y se forma el
producto de sustitución
𝛼
-iodopropanona. Dado que
𝛼
-iodopropanona aún presenta dos H enolizables en el
grupo —CH
2
I y que su enolato es más reactivo que el enolato sin iodo (por efecto inductivo debido al enlace
C—I), de manera consecutiva ocurren dos veces más la formación del enolato estabilizado por resonancia y
el ataque nucleofílico del enolato al electrófilo I
2
. Luego de tres reacciones de sustitución consecutivas de los
H enolizables por I se forma la
𝛼
-triiodopropanona.
La
𝛼
-triiodopropanona es inestable en condiciones básicas porque el grupo —CI
3
(triiodometilo) es un muy
buen grupo saliente en la sustitución nucleofílica de acilo catalizada por base. La adición de
−
OH al grupo
carbonilo y la salida de
−
CI
3
(carbanión triiodometano) seguido de una transferencia rápida del protón del
grupo carboxilo a
−
CI
3
, genera iodoformo (HCl
3
), el cual decanta como un precipitado amarillo y desplaza el
equilibrio de la reacción hacia la formación del carboxilato
.
7
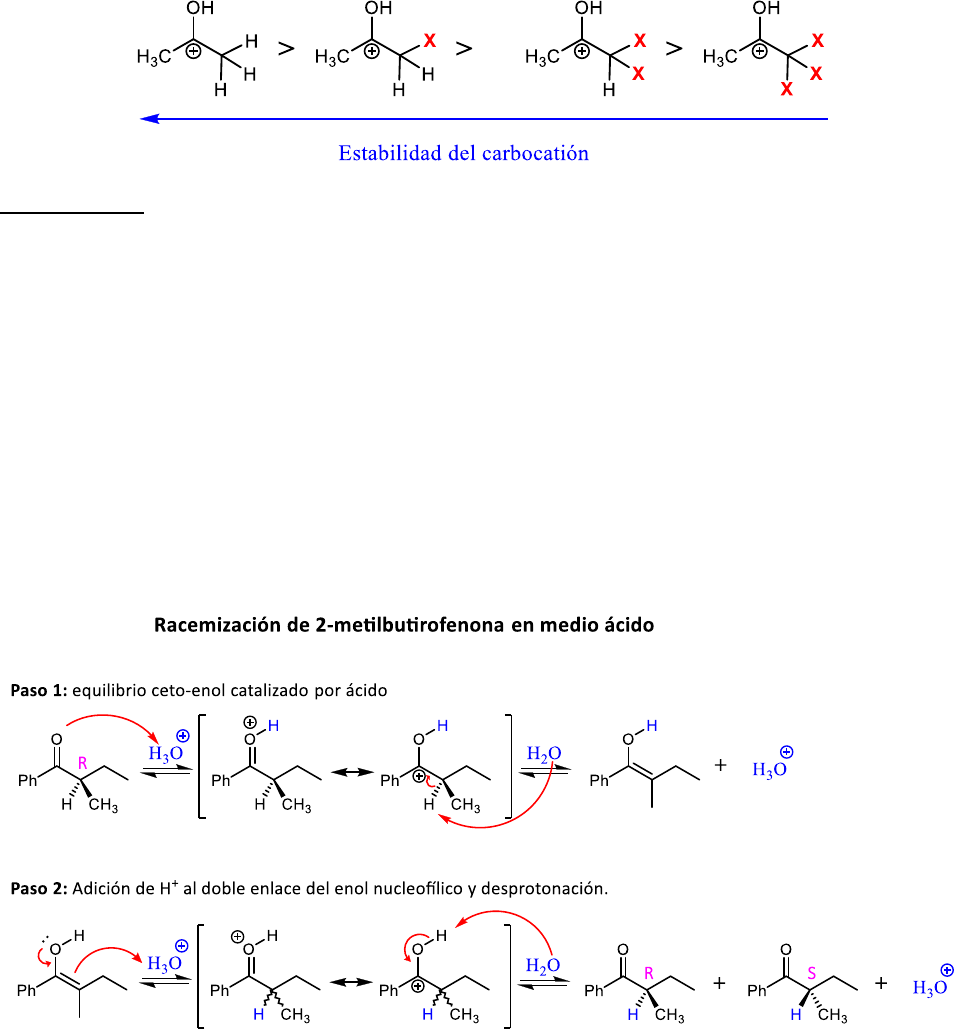
Las metil-cetonas reaccionan de manera cuantitativa con exceso de X
2
en condiciones básicas generando el
carboxilato correspondiente y HCX
3
. Sólo HCl
3
(iodoformo) precipita, mientras que HCCl
3
y HCBr
3
poco
polares se separan como una segunda fase inmiscible al final de la reacción. La reacción del haloformo es
útil para identificar metil-cetonas y para oxidar metil-cetonas al carboxilato correspondiente con un C
menos.
En medio ácido, el agua actúa como base débil abstrayendo un protón de un C
𝛼
del intermediario
estabilizado por resonancia y se establece el equilibrio con su tautómero enol.
El enol de la propanona es un nucleófilo débil que reacciona con el electrófilo I
2
. La adición de I
2
al doble
enlace del enol seguido por una desprotonación genera la
𝛼
-iodopropanona.
Mientras que en medio básico ocurre la tri-sustitución de los 3 H enolizables de uno de los grupos metilo de
la propanona, en medio ácido sólo ocurre una sola sustitución de uno de los H
𝛼
. La razón de esta diferencia
se debe a la capacidad que tiene los halógenos para estabilizar un carbanión. Sin embargo, en medio ácido
el intermediario es un catión y la presencia de halógenos tomadores de e- lo desestabilizan. En particular,
mientras mayor número de halógenos se encuentren unidos al C
𝛼
, mayor es su
𝛿
+
, y mayor es la repulsión
con el carbocatión vecino. Además, el primer paso en la catálisis ácida es la protonación del O del carbonilo,
el cual tiene sus electrones no enlazantes cada vez menos disponibles a medida que aumenta el número de
átomos de halógeno en C
𝛼
.
A partir de esta explicación se concluye que en medio ácido la estabilidad del intermediario catiónico
disminuye a medida que tiene más halógenos en su estructura.
8
PROBLEMA 3
La racemización, el intercambio de D (deuterio) y la bromación de los compuestos con un grupo
carbonilo también son catalizados por ácido. Usando como ejemplo 2-metilbutirofenona, sugiera
un mecanismo razonable en el cual el enol sea un intermediario.
La racemización, el intercambio de deuterio y la bromación son reacciones que les ocurren a los carbonilos
con H enolizables como consecuencia de su equilibrio de tautomería ceto-enol catalizada por ácidos. Por
ejemplo, los tautómeros ceto y enol de la 2-metilbutirofenona están en equilibrio en medio ácido. Si la (R)-2-
metilbutirofenona se disuelve en medio ácido, la solución resultante no es ópticamente activa. Este
resultado es indicativo de que ha ocurrido la racemización del enantiómero puro de partida. El C
𝛼
con
configuración inicial R se convierte en un C sp
2
en el enol. La posterior re-hibridación de este C sp
2
a sp
3
ocurre cuando se adiciona H
+
al doble enlace del enol. Dado que esta adición puede ocurrir por encima o por
debajo del plano del doble enlace del enol, los enantiómeros R y S se forman en iguales proporciones
generando una mezcla racémica.
Otro experimento que es usualmente empleado para identificar y estudiar los equilibrios de tautomería es el
intercambio de deuterio (D) empleando RMN-
1
H. Para ello, la 2-metilbutirofenona se disuelve en una
solución ácida deuterada preparada con DCl y D
2
O. Al tomar el espectro de
1
H, se observa la desaparición de
una única señal correspondiente al protón unido al C
𝛼
de la 2-metilbutirofenona, mientras las señales de los
protones restantes permanecen iguales. La desaparición de la señal se debe al intercambio de H por D en la
posición del C
𝛼
, lo cual es posible a través de la formación del intermediario enol. Si luego se agrega H
2
O a
la solución deuterada, se observará que la señal de H
𝛼
reaparece porque D se intercambia por H
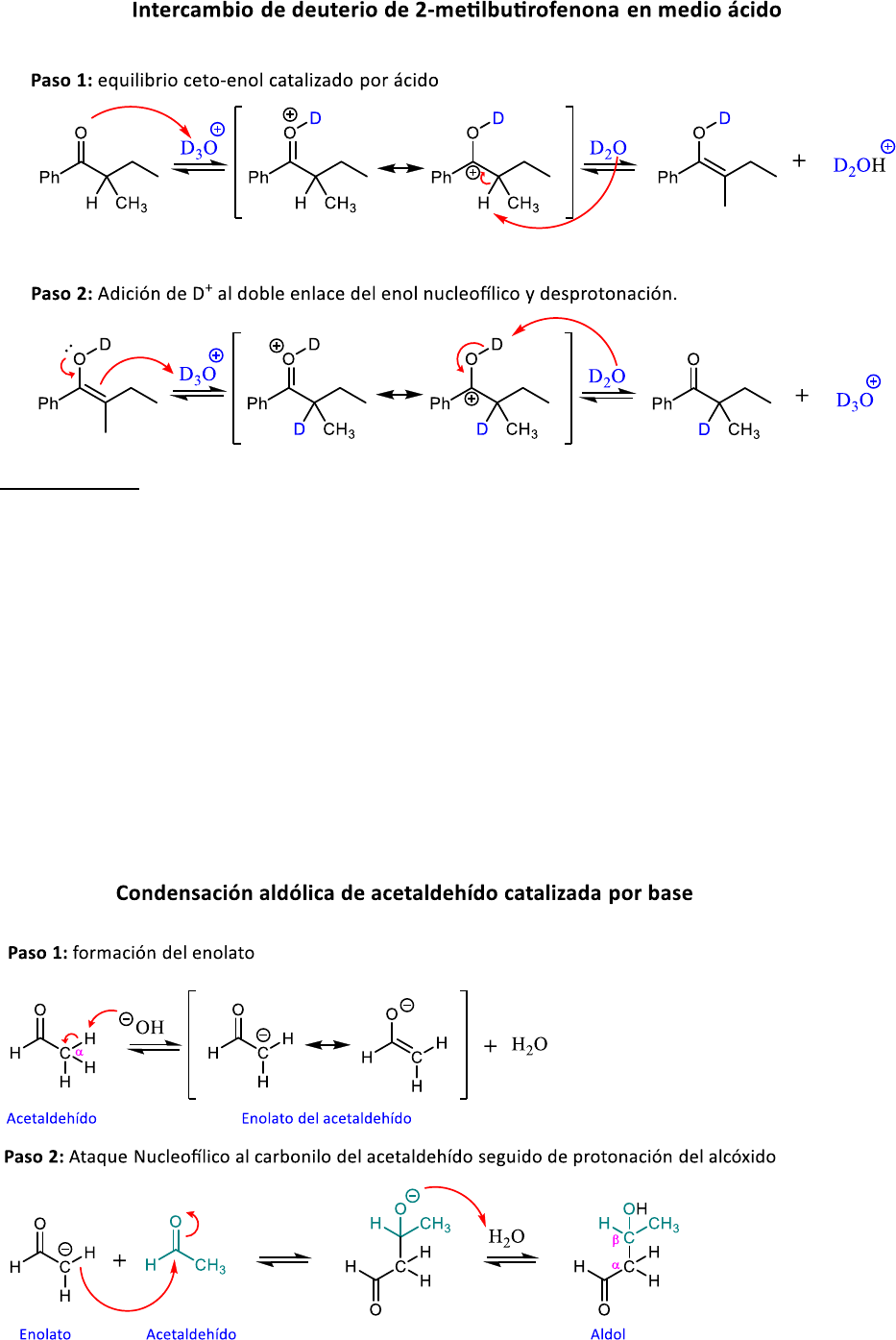
nuevamente, lo que confirma que se trata de un equilibrio químico. El siguiente mecanismo explica cómo
ocurre el intercambio de H
𝛼
por D en la 2-metilbutirofenona.
9
PROBLEMA 4
a) Sugiera un mecanismo para la condensación aldólica del acetaldehído catalizada por
−
OH y
H
+
.
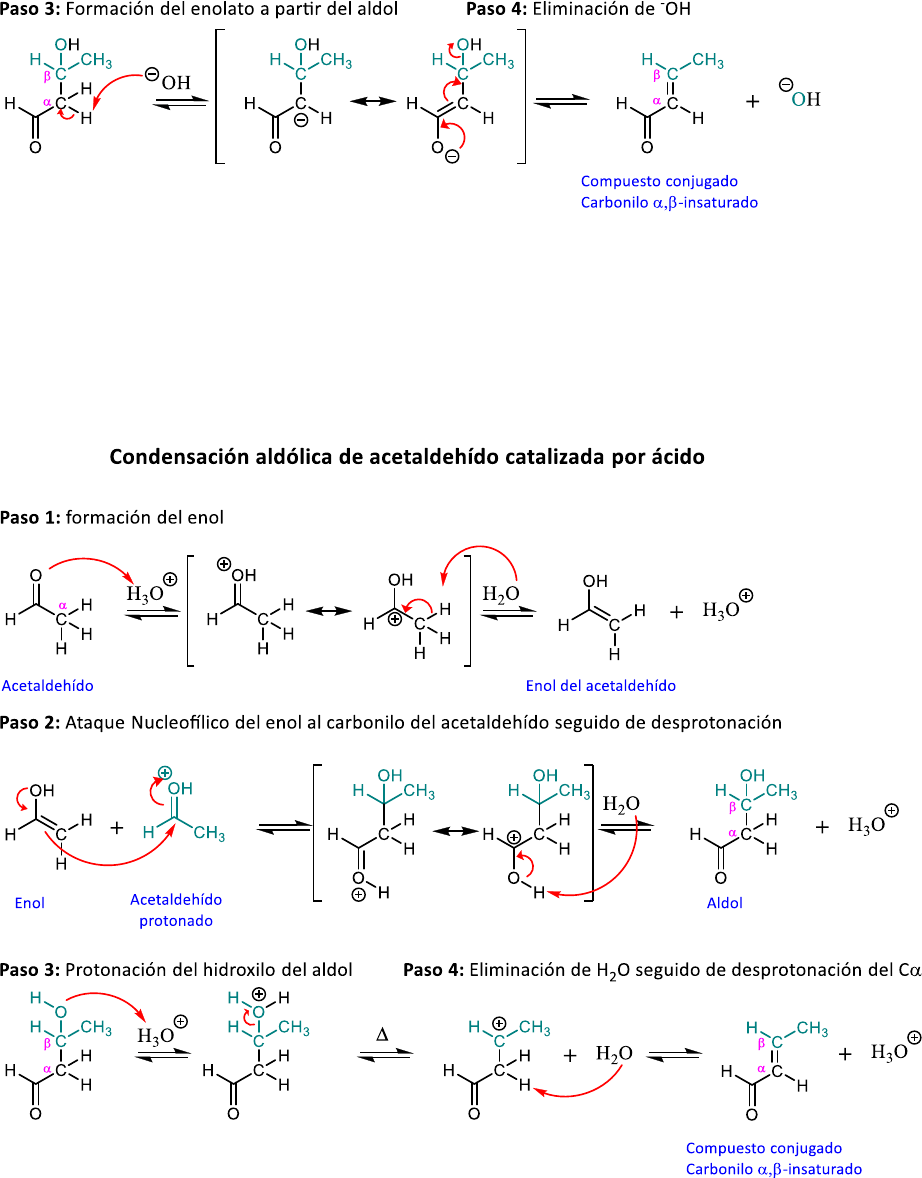
En medio básico, el acetaldehído está en equilibrio con su enolato (PASO 1). La condensación aldólica del
acetaldehído consiste en la adición nucleofílica del enolato al carbonilo de otro acetaldehído, seguido por
una protonación del alcóxido formado (PASO 2). El producto posee dos grupos funcionales, un carbonilo y
un hidroxilo en posición
𝛽
. Este
𝛽
-hidroxi-aldehído se denomina aldol.
El producto formado sigue teniendo un C
𝛼
con H enolizables. Por lo tanto, en medio básico, la base puede
abstraer uno de estos protones para formar nuevamente un enolato estabilizado por resonancia (PASO 3).
Finalmente, con calentamiento se puede favorecer la eliminación del
−
OH que, como vimos en temas
anteriores, es posible si esta reacción ocurre en una etapa que no sea determinante de la velocidad. La
pérdida de
−
OH ocurre en una etapa exotérmica que conduce a la formación de un compuesto conjugado
𝛼
,
𝛽
insaturado (PASO 4).
10
En medio ácido, el acetaldehído está en equilibrio con su enol (PASO 1). El enol es un nucleófilo débil que
ataca al carbonilo activado de otro aldehído y se genera el
𝛽
-hidroxi-aldehído protonado, el cual luego se
desprotona para dar lugar al aldol neutro (PASO 2). Posteriormente, una base débil abstrae un protón del
carbocatión intermediario estabilizado por resonancia y se forma el producto neutro. En condiciones ácidas
y con calentamiento, se favorece la reacción de deshidratación del alcohol (PASOS 3 y 4). El grupo
−
OH se
protona y se pierde como H
2
O, formándose un carbocatión. Luego H
2
O abstrae un protón del C
𝛼
y se forma
un doble enlace conjugado con el grupo carbonilo, un compuesto conjugado
𝛼
,
𝛽
insaturado.
Los aldehídos y/o cetonas están en equilibrio químico con sus aldoles tanto en medio ácido como básico,
pero el carbonilo de los aldehídos es más reactivo que el de las cetonas por lo que los
𝛽
-hidroxi-aldehídos se
forman en mayor proporción que las
𝛽
-hidroxi-cetonas. La formación del compuesto insaturado
generalmente requiere calor.
b) Indique el/los producto/s correspondientes a la reacción en medio básico de:
11
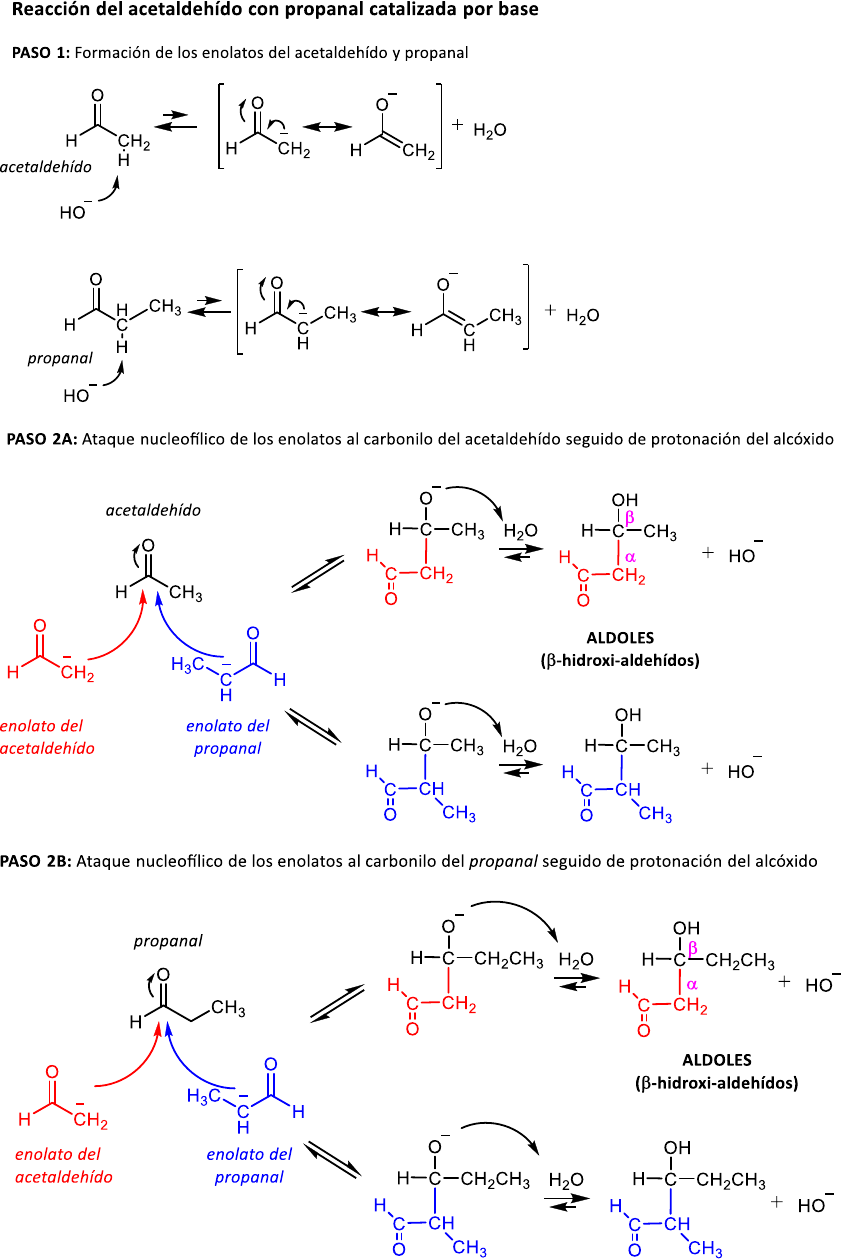
i) acetaldehído y propanal
ii) butanona
12
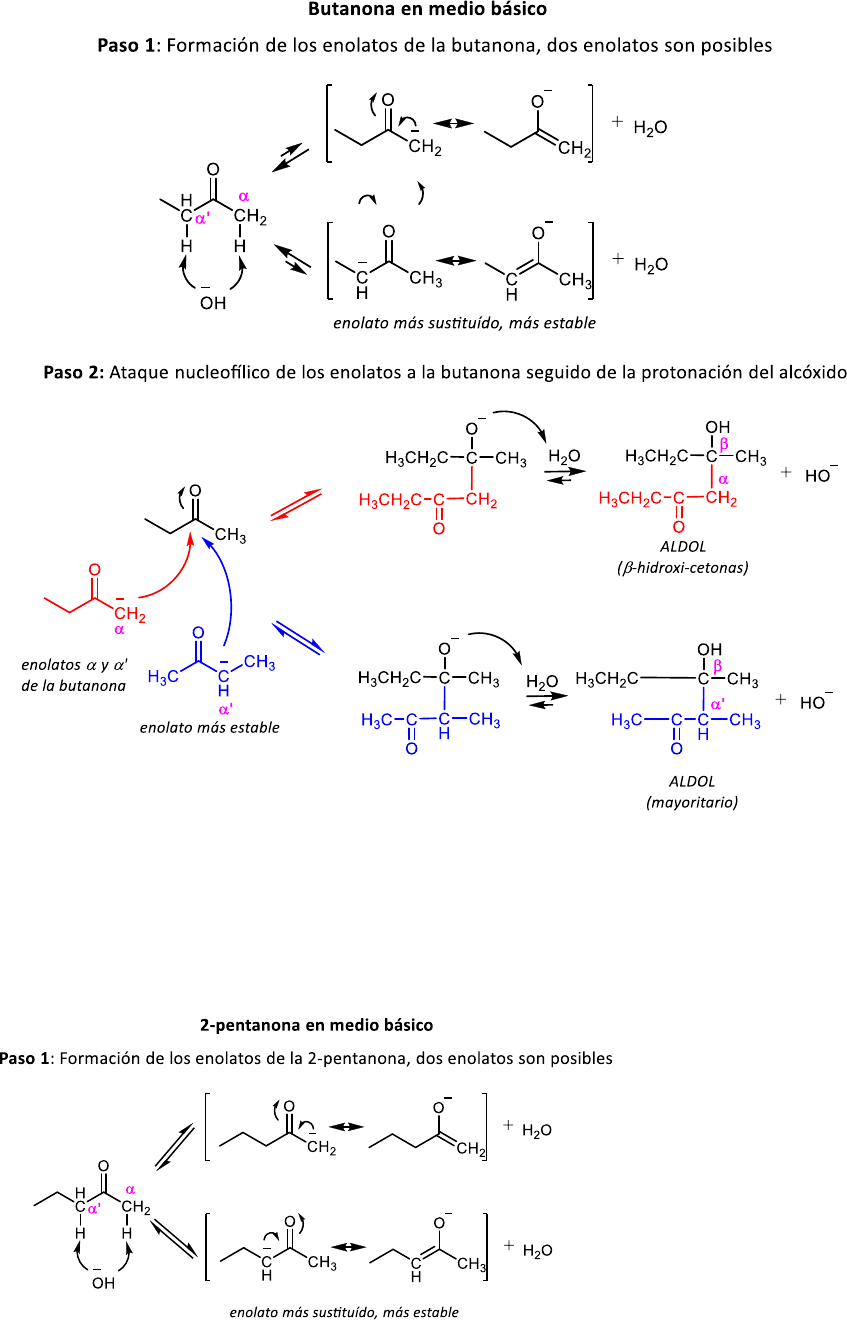
La butanona tiene H enolizables en el grupo metilo y metileno. En medio básico, la formación del enolato
más sustituido está favorecida. La adición de ambos enolatos al carbonilo de la butanona genera dos
aldoles posibles en equilibrio con la butanona, pero el aldol procedente del ataque nucleofílico por el
enolato más estable será mayoritario.
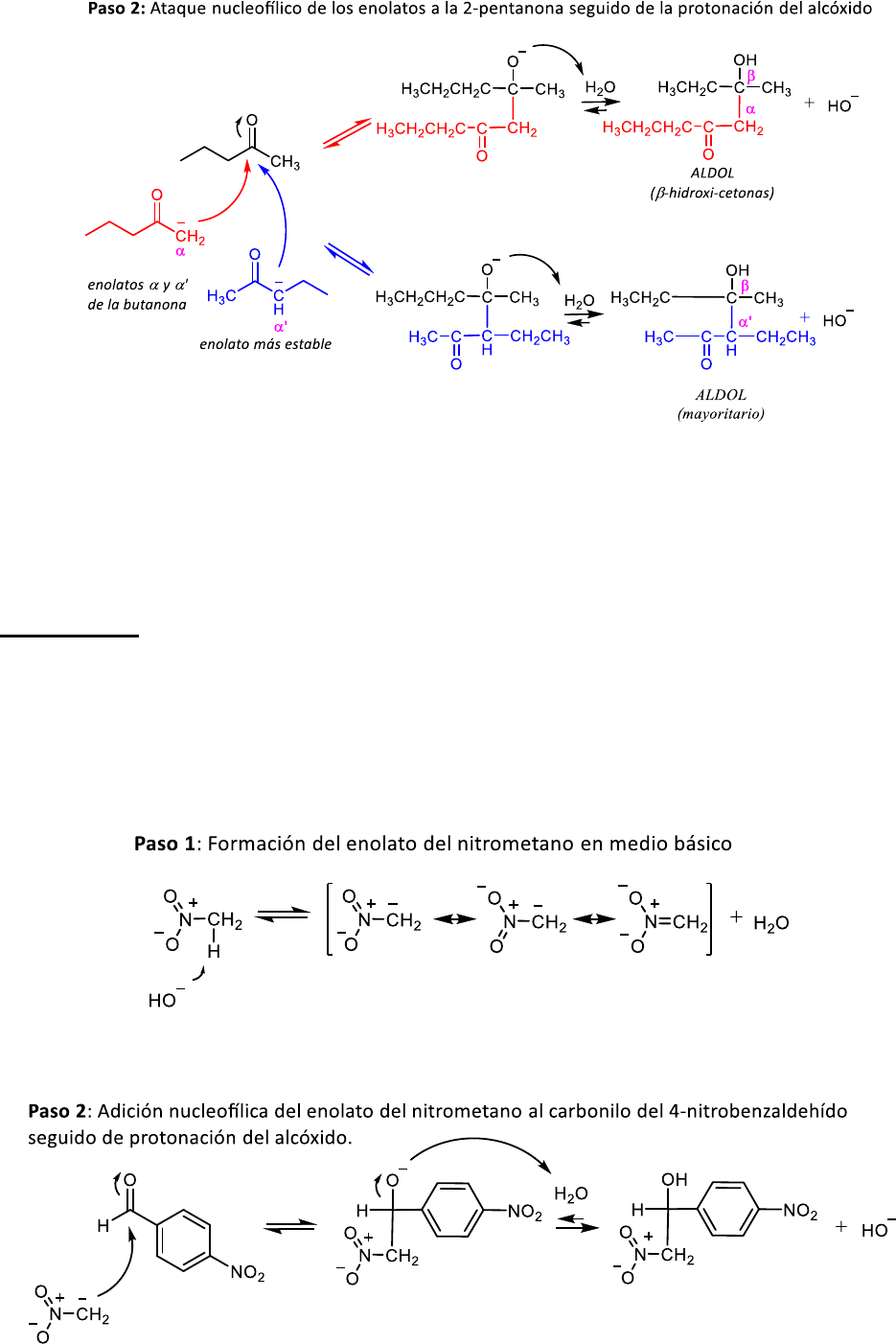
iii) 2-pentanona
13
Similar a lo que ocurre con la butanona, la 2-pentanona también tiene H enolizables en el grupo metilo y
metileno. En medio básico, la formación del enolato más sustituido está favorecida. La adición de ambos
enolatos al carbonilo de la butanona genera dos aldoles posibles en equilibrio con la 2-pentanona, pero el
aldol procedente del ataque nucleofílico por el enolato más estable será mayoritario.
PROBLEMA 5
Formule la reacción de adición entre 4-nitrobenzaldehído y nitrometano en medio básico. ¿Cómo
haría para obtener el producto insaturado?
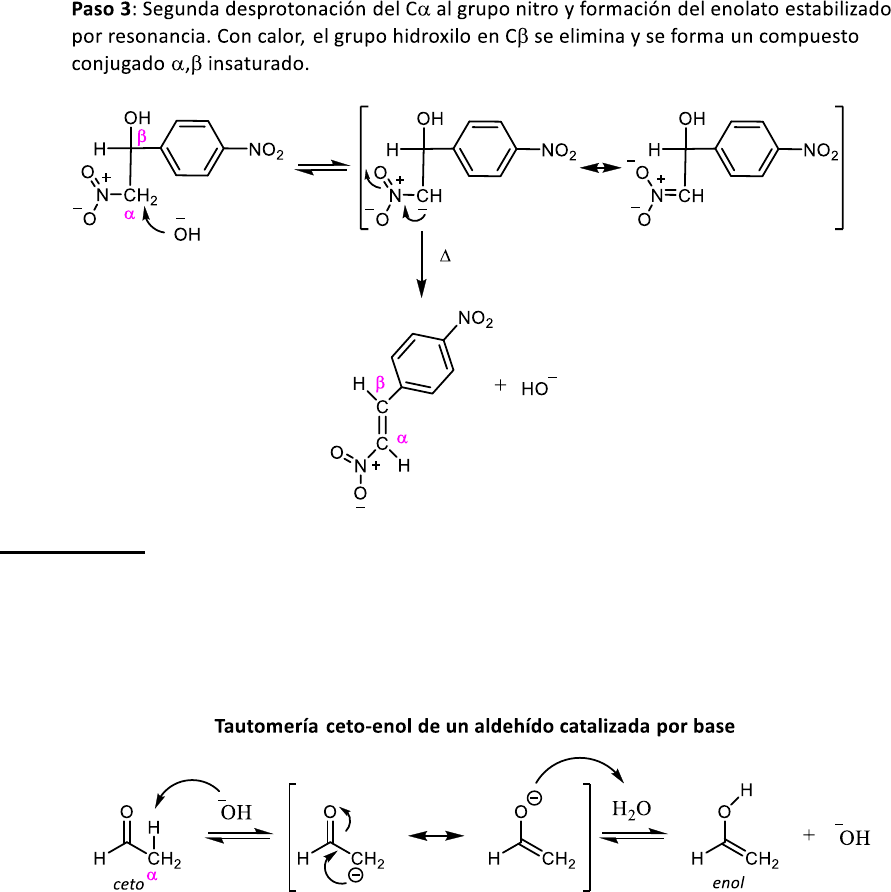
En el problema 1 se vió que el nitrometano, aunque no se trata de un compuesto carbonílico, también
presenta un equilibro de tautomería catalizado tanto por ácidos como por bases. En medio básico se forma
un carbanión estabilizado por resonancia con el grupo nitro.
Este enolato nucleofílico puede atacar al C electrofílico de un carbonilo, tal como sucede en la reacción de
adición con 4-nitrobenzaldehído
.
14
El producto formado sigue teniendo un C
𝛼
con H enolizables. Por lo tanto, en medio básico, la base puede
abstraer uno de estos protones para formar un enolato estabilizado por resonancia. Finalmente, con
calentamiento se puede favorecer la eliminación del
−
OH que, como vimos en temas anteriores, es posible si
esta reacción ocurre en una etapa que no sea determinante de la velocidad. La pérdida de
−
OH ocurre en
una etapa exotérmica que conduce a la formación del compuesto
𝛼
,
𝛽
insaturado conjugado.
PROBLEMA 6
¿Por qué los compuestos con H en posición 𝛼 no tienen reacción de Cannizzaro en medio básico?
La abstracción por una base de los H enolizables de un C
𝛼
de un aldehído es una reacción ácido-base. El
comportamiento ácido de los H enolizables en presencia de una base se debe a la estabilización por
resonancia del intermediario enolato formado.
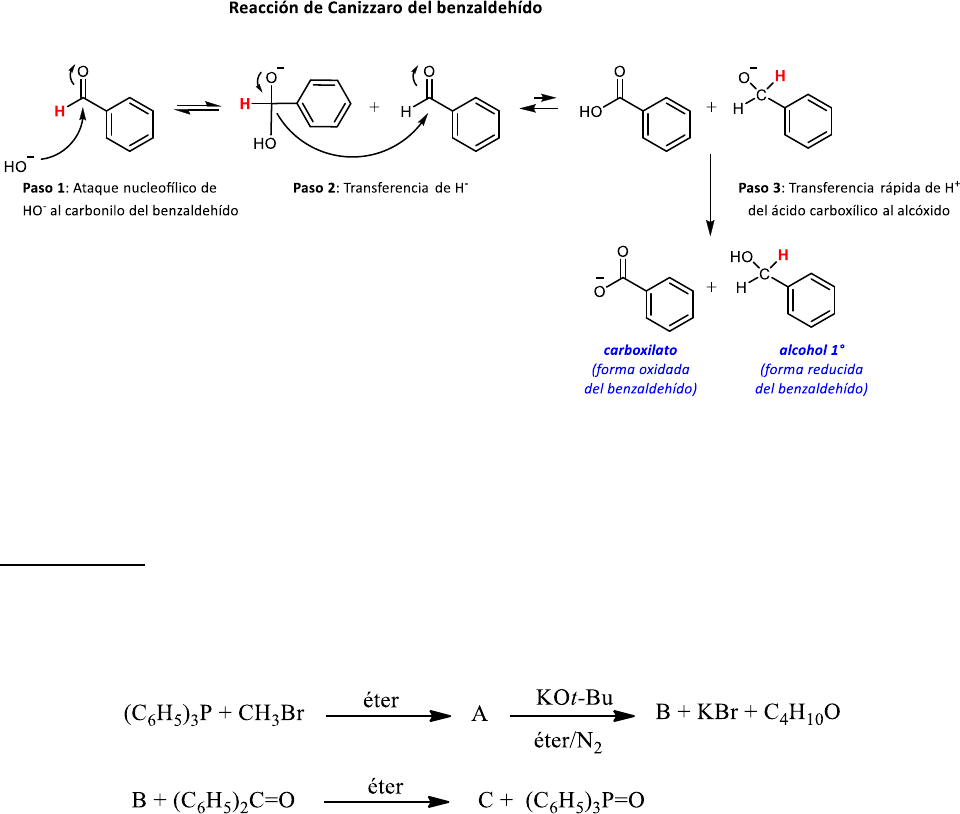
Un aldehído que no posee H enolizables en su C
𝛼
como por ejemplo el benzaldehído, en condiciones
fuertemente básicas puede sufrir otro tipo de reacción llamada reacción de Cannizzaro (reacción redox de
desproporción). La base (el medio), en ausencia de H enolizables, se comporta como un nucleófilo que se
adicionará al carbonilo del benzaldehído. Posteriormente ocurre una transferencia rápida de H (coloreado
en rojo) como hidruro (H
−
) al carbonilo de otra molécula del aldehído. Finalmente, la transferencia rápida de
un protón del ácido carboxílico al alcóxido genera un carboxilato y un alcohol, las formas oxidada y reducida
de un aldehído, respectivamente. En conclusión, la reacción de Cannizzaro es una reacción redox que en
condiciones muy básicas oxida y reduce un aldehído que no tienen H en C
𝛼
a su carboxilato y alcohol 1°.
15
La razón por la cual un aldehído con H enolizables en medio básico presenta tautomerismo en lugar de
reacción de Cannizzaro se debe a que el equilibrio de tautomería está más favorecido dado que se forma un
intermediario enolato estabilizado por resonancia, mientras que la adición de
−
OH al carbonilo genera un
intermediario tetraédrico de mayor energía que no está estabilizado.
PROBLEMA 7
La reacción de Wittig (en honor a Georg Wittig, premio Nobel de química en 1979, quien la
descubrió) es una reacción muy importante en síntesis de alquenos. Complete la siguiente
reacción.
Se ha discutido que un enolato es un carbanión estabilizado por resonancia con un carbonilo. En la reacción
de condensación aldólica, el enolato es el nucleófilo que se adiciona al carbonilo de otro compuesto
carbonílico para generar un aldol.
Otra manera de conseguir la adición de un carbanión estabilizado por resonancia a un grupo carbonilo es
mediante la reacción de Wittig. En esta reacción, un grupo carbonilo se convierte en un alqueno. Para llevar
a cabo la reacción de Wittig es necesario generar inicialmente el carbanión, que será el nucleófilo que
atacará al grupo carbonilo de un aldehído o cetona. Para esto, se parte de trifenilfosfina que reacciona con
un halogenuro de alquilo 1° vía S
N
2. La sal de trifenilfosfonio formada se desprotona en presencia de una
base o un reactivo organometálico y genera un carbanión estabilizado por resonancia con fósforo conocido
como iluro de fósforo.
Este carbanión es un nucleófilo fuerte que se puede adicionar al carbonilo. Posteriormente se forma un
enlace P—O y un intermediario cíclico que colapsa eliminando óxido de trifenilfosfina muy estable y se
forma el alqueno, el cual posee los sustituyentes del grupo carbonilo y del halogenuro de alquilo originales.
A continuación, se muestra la reacción a completar y se detalla el mecanismo para la síntesis de 1,1-
difenileteno a partir de trifenilfosfina y bromometano.
Este documento contiene más páginas...
Descargar Completo
EP13 Acidos Nucleicos.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.