
lOMoARc PSD|20637235
Encuentro 14: <Presentación Antigénica y generación de efectores=
Introducción
Los linfocitos T y B son los efectores fundamentales de la inmunidad adaptativa, mediante el uso de receptores de membrana
generados en forma aleatoria para reconocer el antígeno. El reconocimiento del antígeno produce la expansión clonal de los
linfocitos, lo que aumenta el número de células disponibles para montar una respuesta y asegura que el encuentro posterior con
el mismo antígeno se alcance con mayor fuerza desde el comienzo (memoria inmunitaria).
Mientras que los receptores de las células B (lgM e lgD de superficie) pueden interactuar directamente con el antígeno, los
linfocitos T requieren que el antígeno les sea presentado en el contexto de las moléculas del CMH. La presentación del antígeno
a las células T vírgenes (es decir, no estimuladas con anterioridad) tiene lugar en los tejidos linfoides y normalmente se lleva a
cabo por las células dendríticasmaduras que habrán migrado desde los tejidos periféricos debido a la exposición a un estímulo
de maduración, como un patrón molecular derivado del patógeno (PAMP). Las células dendríticas maduras presentan los
antígenos procesados a las células T que exponen los péptidos derivados de esos antígenos sobre las moléculas del CMH. Las
células dendríticas también proporcionan co estimulación a las células esencial para su activación.
La activación de la célula B también se produce dentro de los ganglios linfáticos y otros tejidos linfoides y es facilitada por
células dendríticas foliculares especializadas que, de manera eficiente, capturan y concentran el antígeno que proviene de los
tejidos circundantes. Con algunas excepciones, las células B activadas también necesitan la estimulación de las células T helper,
para permitir la proliferación y diferenciación. Además de la expansión clonal, laactivación de una célula B o T también produce
la maduración de células efectoras especializadas que producen anticuerpos (en el caso de las células B) o combinaciones
particulares de citocinas o moléculas citotóxicas (en el caso de las células T).
Las células B pueden también presentar el antígeno y estimular a una célula T activada previamente, con el fin de recibir
colaboración de la célula T para la expansión clonal y la diferenciación a una célula B efectora (colaboración T-B), pero las células
dendríticas son típicamente las principales células presentadoras de antígenos (CPA) para la activación de las células T vírgenes.
Los macrófagos también pueden actuar como CPA pero, debido a que su comportamiento es relativamente no migratorio,
tienen una participación importante en re−estimular las células T previamente activadas en los sitios de infección en lugar de
producir el cebado de las células T vírgenes en los tejidos linfoides secundarios.
El objetivo de la activación de los linfocitos dirigida por el antígeno es desencadenar laexpansión clonal de las células correctas
para que estas células puedan ponerse a trabajar para montar una respuesta inmunitaria adaptativa específica para ese
antígeno. Esta última actúa en tándem con una respuesta inmunitaria innata en curso y, amplifica y refuerza la respuesta
inmunitaria innata a través de la provisión de citocinas, anticuerpos y moléculas citotóxicas. Las células T activadas se
diferencian en células efectoras (ej. Th1, Th2, Th17) capaces de secretar diversos patrones de citocinas; del mismo modo, las
células B activadas se diferencian en plasmocitos capaces de secretar diferentes clases de anticuerpos.
Capitulo 8 Fainboim: <Regulación de la expresión génica en el sistema
inmunitario=
Los organismos multicelulares complejos están formados por diferentes tejidos cuyas características individuales dependen de la
expresión de proteínasespecíficas. La diferenciación, el desarrollo y la funcionalidad de estos tejidos dependen del conjunto de
proteínas expresadas selectivamente por cada célula. Estas proteínas pueden funcionar como:
Componentes extracelulares de las células
Receptores celulares
Enzimas
Casais María Luz
Augusto Mailen

lOMoARc PSD|20637235
Agentes, Mecanismos de Defensa y Nutrición
Componentes intracelulares de señalización
Citocinas
Factores quimiotacticos
Moléculas de adhesión celular
La expresión defectuosa de estas proteínas, su expresión espaciotemporal alterada o la producción en cantidades anormales de
proteínasespecíficas subyacen a diversas patología inmunitarias.
Niveles de regulación de la expresión génica en las células eucariontes
¿De qué manera las células regulan procesos de gran complejidad, como la proliferación, diferenciación y apoptosis?
Con dicho objetivo, una célula debe captar señales del ambiente extracelular, transmitirlas al núcleo y traducirlas en un
programa de expresión de genes.
La expresión génica puede controlarse mediante:
La exposición de un determinado locus a la maquinaria transcripcional. La transcripción del RNA se inicia por factores
de transcripción que atraen al complejo de la RNA polimerasa ll.
Los niveles de compactación de la cromatina
La acetilación de histonas del DNA nucleosomico
Las modificacionespostranscripcionales
El transporte de transcritos desde el núcleo celular
La estabilidad del RNA mensajero
De todas estas etapas, la iniciación de la transcripción es probablemente el mecanismo regulador de mayor relevancia en el
control específico de la expresión génica.
La regulación transcripcionalcomprende un conjunto coordinado de interacciones entre proteínasespecíficas que actúan sobre
secuencias promotoras de determinados genes.
En las etapas iníciales de la transcripciónespecífica de genes determinados, desempeñan un papel patogénico los factores de
transcripción. Estos factores son proteínas que se unen a secuencias específicas de DNA situadas en elementos reguladores
denominados promotores de genes.
En el sistema inmunitario, los factores de transcripción controlan procesos biológicos esenciales, como:
La maduración de los linfocitos T y B
La activación linfocitaria
La diferenciación de las células T CD4+ en un perfil efector de tipo Th1, Th2, Th17 o Treg
La actividad citotoxica de los linfocitos T y las células NK
La diferenciación de los linfocitos B en células plasmáticas productoras de anticuerpos o células B de memoria
La inducción de fenómenos inflamatorios propios de la inmunidad innata
Los genomenos de homeostasis y tolerancia, en particular, selección negativa, anergia clonal, generación de células T
regulados y apoptosis de células T efectoras
Factores involucrados en la diferenciación de las células T efectoras y reguladoras
DlFERENClAClON DE LAS CELULAS T CD4+ EFECTORAS
Las células T CD4+ pueden diferenciarse en diversos perfiles efectores, como Th1, Th2 y Th17.
La inmunidad de tipo 1 se basa en la diferenciación de los linfocitos T CD4+ hacia células Th1 capaces de inducir respuestas
inflamatorias y citotoxicas, esenciales para la destrucción de patógenos intracelulares.
Las célulasTh1 secretan las citocinaslL-2, lNF-y y TNF-a. Son capaces de:
Casais María Luz
Augusto Mailen

lOMoARc PSD|20637235
Agentes, Mecanismos de Defensa y Nutrición
Activar macrófagos y células NK
Generar reacciones de hipersensibilidad retardada
Promover la función de linfocitos T CD8+ citotoxicos
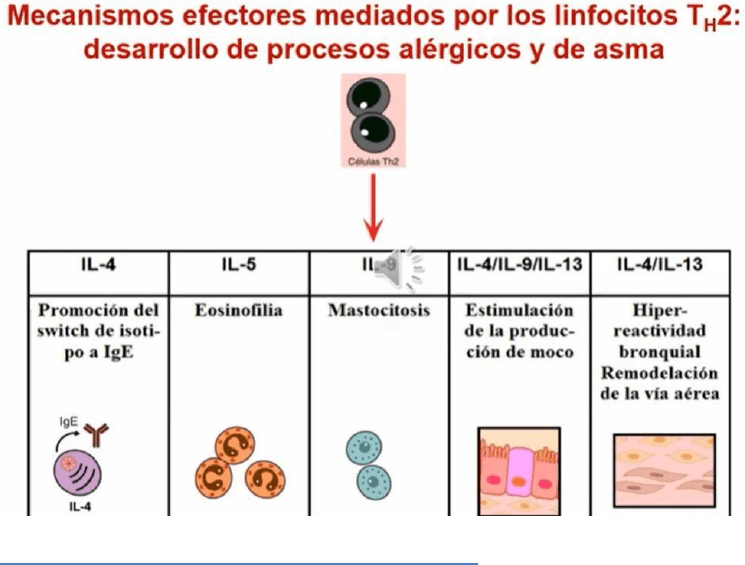
Las célulasTh2 sintetizan altos niveles de citocinas como lL-4, lL-5 e lL-13, que promueven la activación de eosinofilos y
mastocitos y la producción de anticuerpos lgE. Cumplen un papel fundamental en la inmunidad frente a los helmintos y en el
desarrollo de los fenómenos alérgicos.
Las célulasTh17 producen las citocinaslL-17 e lL-22 y promueven la producción, movilización y activación de los granulocitos
neutrofilos. Desempeñan una función relevante en la inmunidad antibacteriana y antimicótica.
Las citocinaslL-12 e lL-18 determinan la polarización de los linfocitos T CD4+ vírgenes en un perfil Th1
La presencia de lL-4 producida por células NKT y mastocitos, en ausencia de lL−12, promueve la diferenciación de los
linfocitos T CD4+ en un perfil Th2.
Por último, la presencia de las citocinaslL-1, lL-6 e lL-23 favorece la polarización de las células T CD4+ en un perfil Th17.
Factores de transcripción involucrados en la activación y diferenciación de las células B
Los linfocitos B maduros, luego de reconocer el antígeno en su forma nativa en el ganglio linfático, a través de su BCR,
interactúan con linfocitos T CD4+ a fin de poder activarse.
Una fracción minoritaria de los linfocitos B activados se dirigirá a los cordones medulares, en el propio ganglio linfático, se
diferenciaran a plasmocitos y producirán, centralmente, anticuerpos de isotipolgM.La mayorías de los linfocitos B activados
migraran al folículo primario para formar el centro germinal. En el centro germinal, las células B sufrirán el cambio de clase de lg
y la hipermutacion somática. Serán luego seleccionadas, en función de su afinidad por el antígeno, y se diferenciaran en
plasmocitos productores de anticuerpos o en linfocitos B de memoria.
Capitulo 9 Fainboim: <Inmunidad mediada por linfocitos T=
Los linfocitos T que emigran del timo son células maduras que expresan un único tipo de TCR: la moléculaCD4 o CD8, y circulan
por la sangre en estado de reposo. Estos linfocitos se denominanlinfocitos vírgenes (naive), ya que no han encontrado aun su
antígeno especifico.
Los linfocitos T vírgenes se extravasan en los órganos linfáticos secundarios a fin de encontrar el antígeno. Este proceso de
extravasación depende, en una primera etapa, de la expresión de las moléculas L−selectina y CCR7 en el linfocito T, que
interactuaran con sus ligandos expresados en las vénulas del endotelio alto.
Una vez ingresadas en el área T de los órganos linfáticos secundarios, las células T vírgenes interactúan con las células
dendríticas convencionales a fin de captar en su superficie los péptidos antigénicos presentados por las moléculas del CMH. Si
reconocen estos péptidos de modo adecuado, los linfocitos T se activan, se expanden y se diferencian en linfocitos T efectores.
Los linfocitos T CD4+ se activan al reconocer péptido antigénicos presentados por las moléculas de clase ll del CMH, mientras
que los linfocitos T CD8+ se activan por el reconocimiento de péptidos presentados por las moléculas de clase l.
Los linfocitos T vírgenes son células de vida media larga y pueden vivir muchos años. Por el contrario, los linfocitos T efectores
son células de vida media corta que viven pocas semanas.
Activación de los linfocitos T vírgenes
ENCUENTRO DE LOS LlNFOClTOS T VlRGENES CON LAS CELULAS DENDRlTlCAS
La respuestas adaptativa no se inicia en el foco de infección sino en los órganos linfáticos secundarios. Aquí, el antígeno es
llevado por las células dendríticas que los capturaron en la periferia, o es traído directamente por la linfa, en forma libre. Las
Casais María Luz
Augusto Mailen
lOMoARc PSD|20637235
Agentes, Mecanismos de Defensa y Nutrición
células T vírgenes que abandonan la sangre e ingresan en los ganglios linfáticos a través de las vénulas del endotelio alto (HEV),
se ubican en el áreaparacortical del ganglio, también denominada área T. Allí son reclutadas además las células dendríticas.
El desplazamiento de las células T vírgenes y las células dendríticas en el áreaparacortical se ordena sobre la base de los
conductos fibroblasticos reticulares (CFR), que guían el trafico de ambos tipos celulares a fin de maximizar sus posibilidades de
encuentro.
Las células dendríticas que han ingresado en el ganglio linfático, tienden a permanecer inmóviles en el áreaparacortical. No
obstante, barren constantemente su entorno inmediato extendiendo y contrayendo prolongaciones celulares denominadas
dendritas, lo que favorece su encuentro con los linfocitos T.
LOS NOTABLES DESAFlOS QUE ENFRENTA LA ACTlVAClON DE LOS LlNFOClTOS T VlRGENES
Existen dos desafíos adicionales:
1.
Un péptido particular será presentado sobre una célula dendrítica con una frecuencia relativamentebaja.
2.
Las interacciones establecidas entre el TCR y los péptidos presentados por las moléculas del CMH son de baja afinidad.
En otras palabras, aun cuando se establezca el contacto entre la célula T virgen y la célula dendrítica, la efectiva activación de la
célula T deberá superar el obstáculo que impone la baja densidad de epitopos antigénicos por reconocer y la baja afinidad del
TCR hacia ellos.
¿Cómo se superan?
En primer lugar, las células dendríticas tienen una gran capacidad para interactuar con las células T vírgenes gracias a
interacciones establecidas entre las moléculas de adhesión expresadas por ambos tipos celulares. Estas interacciones son de
naturaleza inespecífica, es decir, no guardan relación con la especificidad del TCR ni con la particular naturaleza de los péptidos
antigénicos presentados por la célula dendrítica. Sin embargo, el reconocimiento del péptido antigénico por el TCR pone en
marcha vías transduccionales en la célula T.
Esta interacción junto con la interacciónTCR-péptido/CMH, tiende a estabilizar por horas la unión establecida entre la célula
dendrítica y el linfocito T, a fin de que este pueda reconocer efectivamente el péptido presentado.
En segundo lugar, las moléculas correceptoras CD4 y CD8 facilitaran el reconocimiento antigénico. Al interactuar con las
moléculas de clases l y ll del CMH, los correceptores CD8 y CD4 contribuirántambién a estabilizar la unión del TCR con el péptido
reconocido.
En tercer lugar, las moléculas que participan en el reconocimiento antigénico se distribuyen en la superficie celular de un modo
muy particular, a efectos de lograr una máxima eficacia. Al analizar la zona de contacto establecida entre la célula T y la célula
dendrítica se observa que los TCR, junto con las moléculas CD4 o CD8 y los péptidos antigénicos asociados con las moléculas del
CMH, definen un círculo central, mientras que las moléculas de adhesión definen un circulo periférico, definiendo así los
llamados complejos supramoleculares de activación centrales y periféricos.
Esta organización supramolecular constituye lo que denominamos sinapsis inmunitaria. ¿Cuál es su importancia? Al concentrar
las proteínas intracelulares que participan en el proceso de señalización, la formación de la sinapsis inmunitaria potencia las
señales de activación inducidas a través del TCR.
LA ACTlVAClON DEL LlNFOClTO T VlRGEN Y SU EXPANSlON CLONAL REQUlEREN LA PERCEPClON DE DOS SEÑALES
DlFERENTES
Señal 1: es impartida por el reconocimiento del péptido antigénicopresentado por las moléculas del CMH, a través del TCR
Señal 2: es impartida por el reconocimiento de las moléculas coestimuladoras expresadas por la célula dendrítica (CD80 y CD86,
también llamadas moléculas B7) por la moléculaCD28 expresada por el linfocito T.
Casais María Luz
Augusto Mailen

lOMoARc PSD|20637235
Agentes, Mecanismos de Defensa y Nutrición
Aquellos linfocitos T vírgenes que reconozcan el péptido antigénico pero no perciban la señal 2 sufrirán un proceso de anergia
irreversible que conducirá a su muerte.
¿Cuál es la lógica de requerir dos señales a fin de activar al linfocito T virgen? No es otra que imponer un control estricto a la
activación <no deseada= de los linfocitos T, en primer lugar, a aquellos que muestren autorreactividad.
Los clones T aurreactivos se encuentran presentes presentes en la periferia en todos los individuos. Deberemos silenciarlos a fin
de evitar el desarrollo de enfermedades autoinmunes. El requerimiento de una segunda señal de activación hace que, aun
cuando un clon autorreactivo contacte, en un órgano linfático secundario, con una célula dendrítica que exprese péptidos
propios, este encuentro no determinara generalmente la activación del clon autorreactivo.
¿Por qué? En ausencia de señales infecciosas (PAMP) o señales indicativas de daño tisular (DAMP) en los tejidos periféricos, las
células dendríticas que logren arribar al OLS expresaran muy bajos niveles de moléculas coestimuladoras; por lo tanto, la
presentación de péptidos propios dará lugar, casi siempre, al silenciamiento (anergia y muerte) y no a la activación del clon T.
¿Cómo progresa el proceso que conducirá a la expansión clonal de las células T activadas? Los linfocitos T vírgenes expresan
constitutivamente un receptor de baja afinidad para la lL−2. Este receptor se compone de dos cadenas denominadas B y Y. La
activación de la célula T conduce, en primer lugar, a la producción de la cadena a (CD25) del receptor para lL−2. El heterodimero
a, b y Y representa el receptor de alta afinidad para la lL−2, que le permite a la célula T expandirse clonalmente en respuesta a
concentraciones fisiológicas de lL−2.
¿Cómo se regula la expansión clonal T? La expansión clonal T es un fenómeno estrictamente regulado. La moléculaCTLA-4
cumple, en este sentido, un papel fundamental. Mediara su acción inhibitoria no solo transduciendo señales inhibitorias sino
también <secuestrando= a CD80 y CD86, de modo de impedir su interacción con la molécula estimuladora CD28.
Generación de linfocitos T CD4+ efectores: células Th1, Th2, Th17, Tfh y T REGULADORAS
Casais María Luz
Augusto Mailen
La molécula CD8 es expresa en forma constitutiva por las células T vírgenes. Su entrecruzamiento
o agregación inducida por CD80 o CD86 provee la señal 2 de activación al linfocito T y le permite a
este sintetizar la cadena a del receptor de la lL−2, citocina encargada de inducir la expansión clonal
T.
El proceso de expansión clonal permitirá disponer rápidamente de un ejército compuesto por
millones de células T efectoras con el objeto de erradicar o contener el proceso infeccioso.
lOMoARc PSD|20637235
Casais María Luz
Augusto Mailen
Una propiedad esencial de la respuesta T CD4+ es su plasticidad. En otras palabras, una misma célula T CD4+ virgen, al
activarse, podía diferenciarse en distintos perfiles efectores.
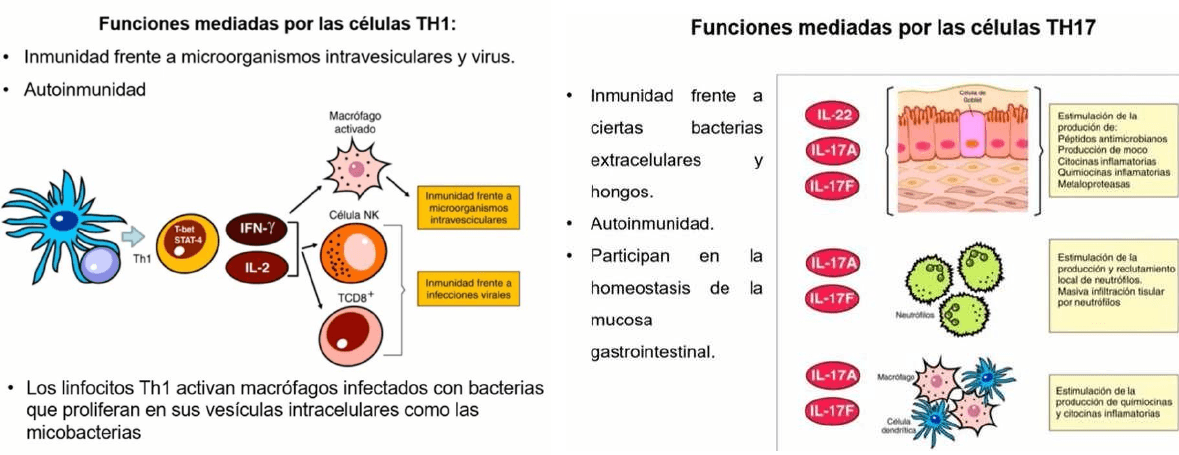
Células Th1: producen interferon−y e inducen la activación del macrófago en los tejidos periféricos
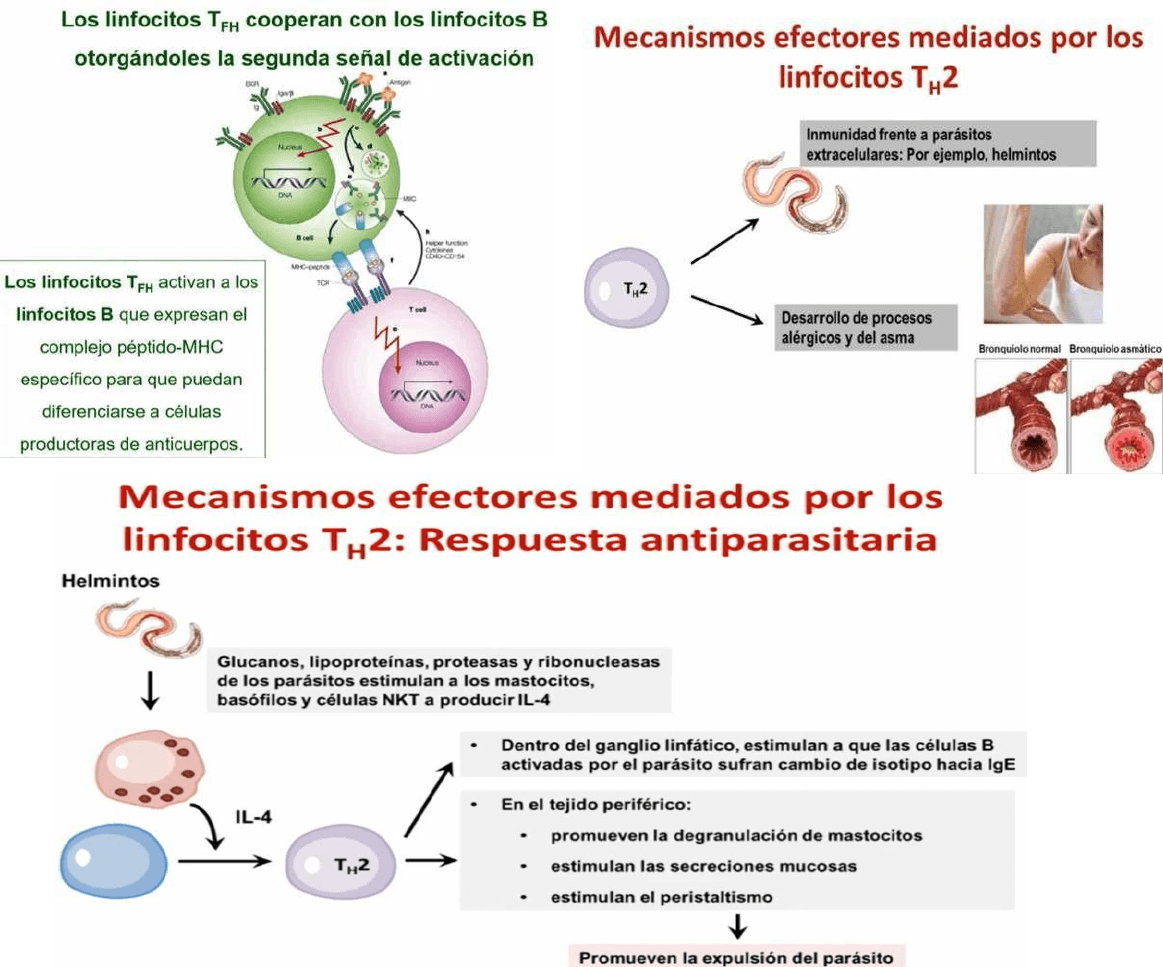
Células Th2: producen lL−4, lL−5 e lL−13, e inducen la movilización y activación de eosinofilos y mastocitos, favoreciendo
además la producción de anticuerpos lgE por las células B
Células Th17: producen lL−17 y promueven la producción, movilización e infiltración por neutrofilos del tejido afectado
Células Tfh: median la colaboración con los linfocitos B y les permite diferenciarse en plasmocitos productores de
anticuerpos
Las célulasTh1 y Th17 median el desarrollo de patologías autoinmunes, mientras que las célulasTh2 cumplen un papel clave en
el desarrollo de los fenómenos alérgicos.
a.
Linfocitos T reguladores: por su parte, median un efecto supresor sobre la activación de las diferentes poblaciones de
linfocitos T y sobre los linfocitos B, a fin de controlar la actividad de los clones T y B autorreactivos, presentes en la
periferia y modulan, además, el desarrollo de la respuesta inmunitaria antiinfecciosa.
A diferencia de los linfocitos CD4+ vírgenes, los linfocitos T CD4 efectores pueden activarse sin reconocer moléculas
coestimuladoras.
Las células T CD8+ suelen mostrar menor plasticidad que las células T CD4+. La activación de las células T CD8+ vírgenes conduce
a la producción de célulasT CD8+ efectoras capaces de mediar dos funciones:
a.
Citotoxicidad
b.
Producción de citocinas inflamatorias, en primer lugar, lFN−y
¿Cómo decide el linfocito T CD4+ virgen el perfil en el que se diferenciara tras reconocer el antígeno?
El particular conjunto de receptores que se active en la célula dendrítica, expuesta en el tejido periféricos al proceso infeccioso,
determinara el patrón de citocinas que producirá esta célula dendrítica en el ganglio linfático y, por ende, el perfil en el que se
diferenciaran los linfocitos T CD4+ activados.
¿Es excluyente la activación en uno u otro perfil? Un linfocito T CD4+ virgen que ingresa en el ganglio linfático y reconoce el
antígeno se diferenciara en un único perfil. No obstante, al población de células T vírgenes activadas durante el curso de un
proceso infeccioso puede no activarse en un único perfil. Aunque, la respuesta inmunitaria antiinfecciosa, como también la
inmunidad antitumoral y la autoinmunidad, suelen mostrar perfiles <predominantes=. Esto puede entenderse considerando dos
variables:
a.
La inducción de los distintos perfiles T CD4+ es promovida por diferentes citocinas
b.
Ciertas citocinas, propias de un perfil, inhiben la diferenciación de los linfocitos T CD4+ en un perfil diferente
lOMoARc PSD|20637235
Casais María Luz
Augusto Mailen
lOMoARc PSD|20637235
Generación de linfocitos T CD8+ efectores
ACTlVAClON DE LOS LlNFOClTOS T CD8+
Los linfocitos T CD8+ vírgenes, al igual que los linfocitos T CD4+ vírgenes, se extravasan en los órganos linfáticos secundarios a
fin de encontrar el antígeno. Una vez que ingresan en el área T, interactúan con las células dendríticas para detectar, en su
superficie, la presencia de péptidos antigénicos presentados por moléculas de clase l del CMH. A fin de facilitar el
reconocimiento antigénico, se establecen interacciones entre las moléculas de adhesión expresadas por las células T CD8+ y las
células dendríticas.
Si reconocen los péptidos antigénicos, los linfocitos T CD8+ se activan, se expanden y se diferencian en linfocitos efectores
citotoxicos. Si no encuentran a su antígeno especifico, retornan a la circulación sanguínea a través de los vasos linfáticos
eferentes y el conducto torácico. Rápidamente, volverán a extravarse a los órganos linfáticos secundarios y recomenzaran la
búsqueda de su antígeno específico, en forma similar a lo que sucede con los linfocitos T CD4+ vírgenes.
La activación de los linfocitos T CD8+ vírgenes requiere también la percepción de dos señales:
1.
La primera deviene del reconocimiento antigénico por el TCR
2.
La segunda, de la percepción de señales coestimuladoras
En relación con la señal 2, es importante destacar que el tenor de coestimulacion requerido por una célula T CD8+ virgen para
activarse es mayor que el requerido por una célula T CD4+ virgen.
Aun cuando el tenor de coestimulacion aportado por las células dendríticas resulte suficiente para inducir la activación y
expansión clonal de los linfocitos T CD8+, se requiere la colaboración de las células T CD4+ para la generación y el
mantenimiento de las células T CD8+ de memoria.
PAPEL DE LAS CELULAS T CD8+ EN LA lNMUNlDAD ANTllNFECClOSA
Las células T CD8+ desempeñan un papel central en la inmunidad antiviral y participan, además, en la respuesta inmune
generada contra ciertas bacterias y parasitos. Por ejemplo virus de la gripe y virus del herpes.
Luego de la infección por el virus de la gripe, las células T CD8+ eliminan el patógeno, generan memoria y proveen inmunidad
frente a reinfecciones por el mismo virus. En las infecciones por virus pertenecientes a la familia Herpesviridae, las células T
Casais María Luz
Augusto Mailen

lOMoARc PSD|20637235
CD8+ ejercen una actividad protectora permanente, mediante el control cotidiano de la infección establecida, que no es posible
erradicar.
En todos los casos, la inmunidad conferida por las células T CD8+ se ejerce por dos mecanismos:
Destrucción de las células infectadas (citotoxicidad)
Producción de citocinas inflamatorias, en primer lugar, lFN−y
Cabe destacar que las células T CD8+ no solo participan en la inmunidad antiviral. Desempeñan también un papel importante
frente a las infecciones bacterianas producidas por agentes que se alojan tanto en el citosol celular como en el compartimiento
vacuolar del macrófago.
ClTOTOXlClDAD MEDlADA POR CELULAS T CD8+
El proceso de activación, expansión clonal y diferenciación en linfocitos T citotoxicos se completa aproximadamente 5 días
después del encuentro con el antígeno.
Durante este periodo, las células T CD8+ sintetizan los componentes presentes en sus gránulos secretorios: granzimas y
perforinas. Los linfocitos T CD8+ efectores abandonan luego el OLF y se dirigen a los tejidos inflamatorios, en busca de células
infectadas por el mismo patógeno que dio lugar a su activación. Durante su diferenciación en células T CD8+ efectoras, los
linfocitos T CD8+ cambian el patrón de expresión de diversas moléculas de adhesión de forma tal que puedan reconocer el
endotelio activado y extravasarse hacia el sitio de infección.
Los linfocitos T citotoxicos que han arribado al sitio de infección contactan con las células del tejido, infectadas o no, a través de
interacciones no especificas.
Las células T CD8 citotoxicas pueden destruir a las células diana por dos mecanismos, conducentes ambos a su apoptosis:
Mediante la liberación de granzimas perforinas (mecanismo secretorio)
A través del sistema FasL/Fas
Una vez que el linfocito T citotoxico descargo el contenido de sus gránulos sobre la membrana de la célula diana se separa de
esta y puede volver a reconocer y matar otras células infectadas.
En consecuencia, la citotoxicidad T es muy eficaz, ya que una sola célula efectora puede inducir la apoptosis de muchas células
infectadas.
PRODUCClON DE ClTOClNAS POR LAS CELULAS T CD8+
Los linfocitos T CD8+ contribuyen a la inmunidad no solo en función de su extraordinaria capacidad de mediar respuestas
citotoxicas, sino también a través de la liberación de citocinas inflamatorias, en primer lugar lFN-y y TNF-a
El lFN-y cumple un papel crucial en la activación de los macrófagos y en la promoción de la diferenciación de los linfocitos T CD4
vírgenes en un perfil Th1. Por su parte, el TNF-a media una actividad inflamatoria por diferentes mecanismos.
Las células T CD8+ activadas producen también quimiocinas inflamatorias, que contribuyen al reclutamiento de diferentes
células inmunitarias en el tejido afectado.
Células Tyδ y células NK
Casais María Luz
Augusto Mailen
Los linfocitos T CD8+ efectores a diferencia de los vírgenes, no requieren señal 2 para
activarse. Ello les permite destruir células parenquimatosas infectadas, propias de los
diferentes tejidos, que no suelen expresar moléculas coestimuladoras.

lOMoARc PSD|20637235
Estas células constituyen dos poblaciones de células T no convencionales. Cumplen una función importante en la inmunidad
antimicrobiana actuando en la fase temprana de los procesos infecciosos. Son células T; sin embargo, comparten propiedades
con las células de la inmunidad innata, ubicándose en la interfaz de los mecanismos propios de las inmunidades innata y
adaptativa.
Casais María Luz
Augusto Mailen

lOMoARc PSD|20637235
Fainboim Capitulo 12: Tolerancia Inmunologica y celulas T reguladoras
Las celulas B y T autorreactivas presentes en la periferia deben ser sielnciadas a fin de evitar el desarrollo de autoinmunidad. En
esta funcion el papel protagonico es de las celulas T reguladoras.
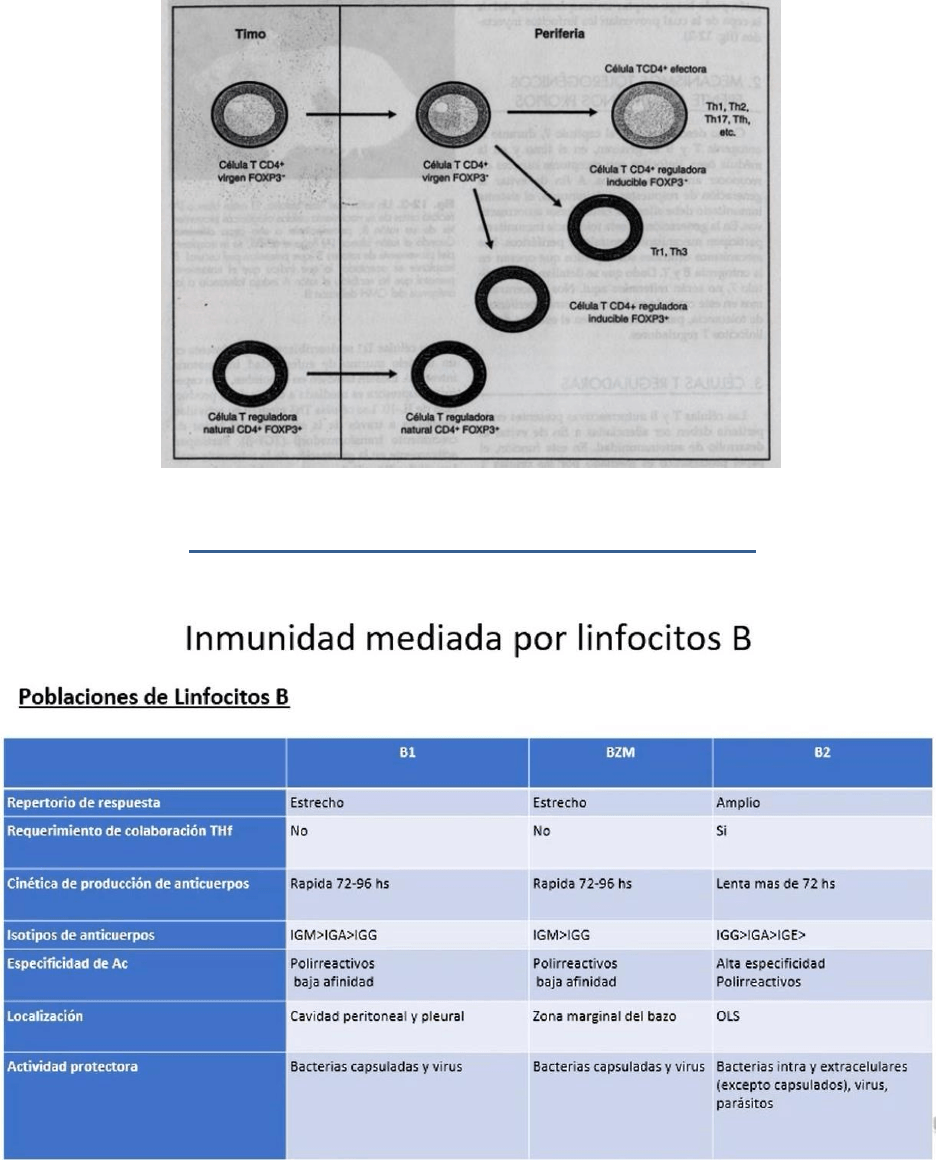
De acuerdo con su fenotipo, su tejido de orgien, las citocinas que secretan y su mecanismo de accion se pueden distinguir 3
subtipos de celulas T CD4+ reguladoras:
Celulas T reguladoras de tipo l (Tr1)
Celulas Th3: median su actividad supresora a tarves de la secrecion del factor de crecimiento transformador B (TGF−B) y
participan activamente en la generacion de la tolerancia oral.
Celulas T-reguladoras CD4+CD25+FOXP3+ (Treg): constituyen al poblacion de celulas reguladoras mejor caracterizadas
y el linaje celualr con mas potente actividad suspensora. Se encunetran distribuidas en el organismo. Estas celulas
cumplen el papel central en la regulacion de la respuesta hacia los antigenos propios.
La eliminacion de las celulas Treg no solo conduce a la autoinmunidad, sino ademas a la exacerbacion de la respuesta
inmunitaria dirigida hacia antigenos tumorales y microbianos. Ello indica que las celulas Treg modulan tambien a la respuesta
inmunitaria antitumoral y antiinfecciosa
Diferentes poblaciones de las celulas T reguladoras
Casais María Luz
Augusto Mailen
lOMoARc PSD|20637235
Fainboim Capitulo 13: Memoria Inmunitaria
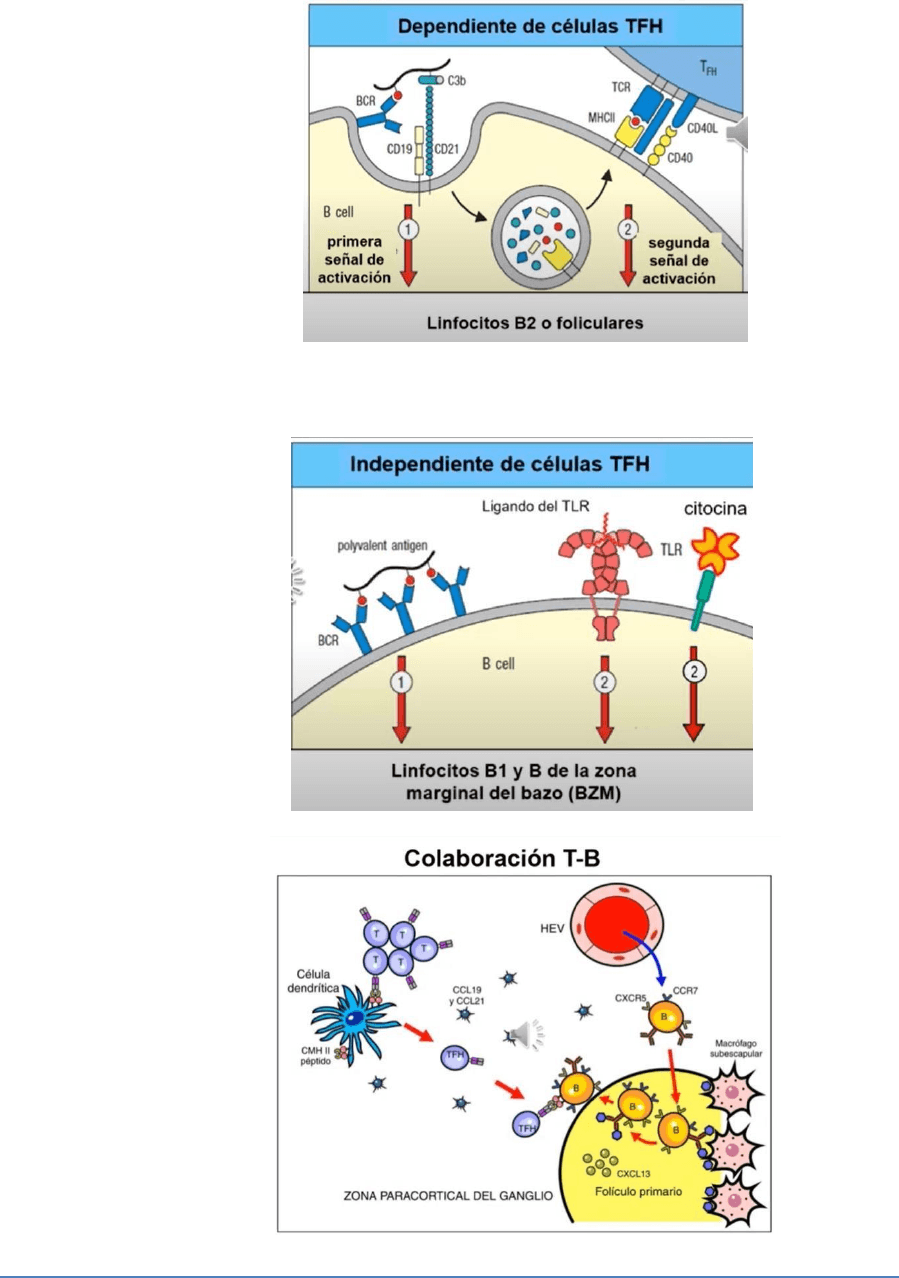
La mayoría de las respuestas inmune del linfocito B están activadas a través de la colaboración de los linfocitos T helper
(fundamentalmente los B2 o foliculares) quienes reconocen a un antígeno presentado en el contexto de MHC y se lo presenta al
linfocito b para que este pueda generar las inmunoglobulinas q corresponda
Casais María Luz
Augusto Mailen
lOMoARc PSD|20637235
Hay otras respuestas que son independientes de las células TFH que están dadas por los linfocitos B1 y B2 de la zona marginal
del bazo
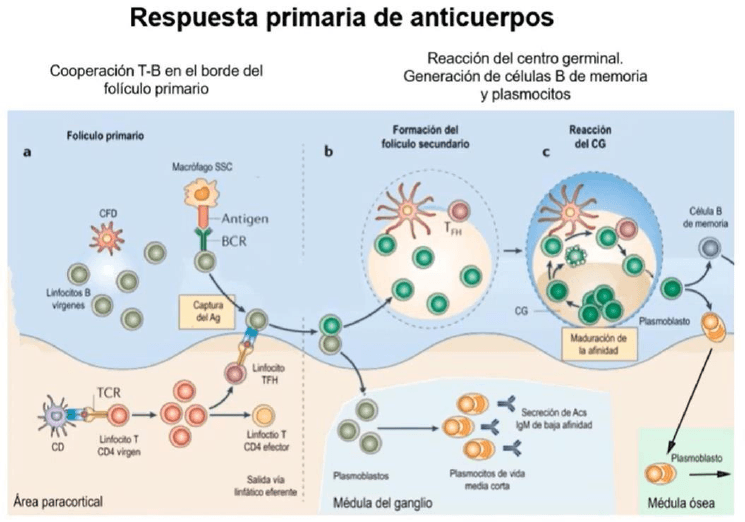
Respuesta primaria de un anticuerpo frente a un antígeno t-dependiente
Los linfocitos B vírgenes que ingresan en el ganglio atravesando las vénulas del endotelio alto (HEV) son atraídos hacia los
folículos primarios por la quimiocina CXCL13.
Los linfocitos T vírgenes ingresan en la zona paracortical de los ganglios atravesando las HEV, donde están las células dendríticas
que han capturado al antígeno, lo han procesado y presentado a los péptidos antigénicos sobre moléculas declase ll.
Casais María Luz
Augusto Mailen
lOMoARc PSD|20637235
Los linfocitos TCD4+ que reconocen el péptido antigénico presentado son detenidos yactivados, produciéndose su expansión
clonal y diferenciación en perfiles efectores, entre ellos, el perfil tfh. Estos linfocitos T CD4+ q se activaron se diferencian en
linfocitos tfh y migran hacia el folículo primario.
Los linfocitos B vírgenes reconocen el antígeno, se van a activar, aumenta la expresión de CCR7 y migra hacia la zona
paracortical. La colaboración tfh−linfocito B se produce en el borde del folículo primario, donde ambas poblaciones celulares se
expanden.
En el folículo primario hay una presentación antigénica desde el macrófago hacia el receptor del linfocito b y la captura
antigénica.
Y por otro lado, a traves del receptor del linfocito T y las células dendríticas le es presentado un poli péptido a LT cd4+ virgen, el
cual hace una expansión clonal y se dirige a esa zona folicular, donde realiza la misma presentación hacia el linfocito B. El
linfocito b puede tomar dos caminos:
1.
Hacia la formación de plasmoblastos (células inmaduras) que van a terminar en plasmocitos con la secreción de
anticuerpos de lgM de baja afinidad y son de vida media corta
2.
Puede dirigirse a la formación de un folículo secundario, donde va a haber mas presentación y más presencia del
linfocito t helper foliculares, con los cuales se produce la maduración con la afinidad y la producción de células b de
memoria. Por otro lado la formación de plasmoblasto que actúan como memoria dirigiéndose a la Mo, y en una
reacción subsiguiente tendremos una respuesta más intensa y más especifica
Casais María Luz
Augusto Mailen
lOMoARc PSD|20637235
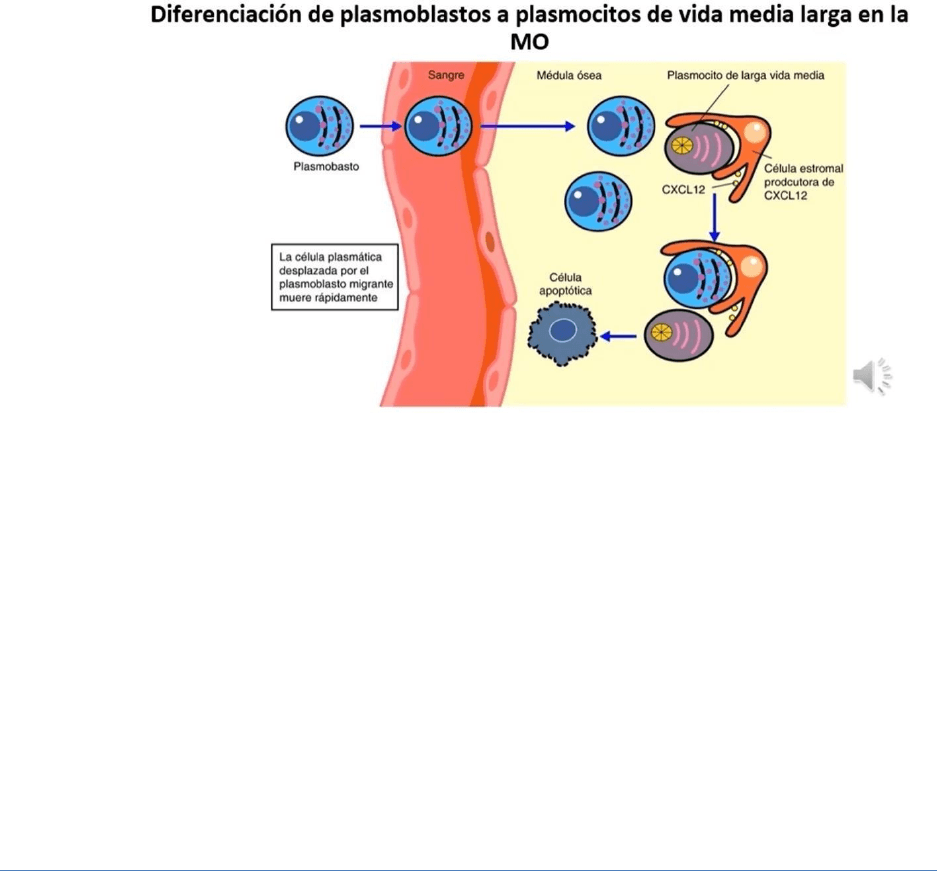
Los plasmoblastos que abandonan el centro germinal, migran a la medula ósea y dan lugar a plasmocitos de corta vida (días) o
larga vida (meses o años).
Los plasmoblastos son células proliferantes que expresan moléculas de clase ll del CHM y tienen capacidad migratoria. La
maduración a esta célula plasmática se asocia con la pérdida de 3 condiciones, los plasmoblastos dejan de expresar CXCR5 y
CCR7. Esto les permite abandonar el centro germinal, expresan CXCR4, el receptor para la quimiocina CXCL12. Esta citosina atrae
a los plasmoblastos a la MO para su diferenciación final en plasmocitos, en microambientes (nichos) que les permitirán
continuar secretando anticuerpos por tiempos prolongados y mantener asi niveles protectores de anticuerpos en el suero, por
meses o años. CXCL12 no actúa solo como quimioatractante, sino también estimula la supervivencia de los plasmocitos en sus
nichos en la MO
La fase migratoria de los plasmoblastos se extiende por una semana. Si no encuentran un nicho apropiado, mueren por
apoptosis. El número de nichos capaces de albergar plasmocitos de vida media larga es limitado. Cada plasmoblasto que llega a
la medula ósea deberá desplazar a una célula plasmática ya establecida, de lo contrario morirá.
Diferencias entre Linfocitos B virgenes, plasmocitos y celulas B de memoria
Linfoctios B virgenes: presenta un receptor de celula B con lgM o lgD
Plasmocitos: Es la celula madura y productora de anticuerpos que pueden ser secretados a la circulacion.
Como la lgG, lgA, lgM, lgE. Se encuentra en tejidos linfatucos secundarios y MO
Celulas B de memoria: presentan receprotes con lgM, lgA, lgG, lgE. Puede estar en la circulacion o en tejidos
linfaticos secundarios
Casais María Luz
Augusto Mailen
Este documento contiene más páginas...
Descargar Completo
encuentro-14-inmunidad-adaptativa-celulas-y-mediadore-mecanismos-de-evasion (1)_organized.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.