M. R. – Facultad de Medicina 2020
• Cuando me piden enzima libre, complejo ES o total de enzima:
Et: concentración total de enzima
E: concentración de enzima libre
ES: concentración de enzima formando el complejo enzima-sustrato
• Cuando me piden complejo ES, K
cat
, V
0
:
• Cuando me piden total de enzima, K
cat
, V
máx
:
o Despejo si me dan V
máx
y [Et]:
o Kcat es lo mismo que decir K2 en enzimas MM. Es el número de
recambio de la enzima.
o La unidad de kcat es la inversa de la unidad de tiempo (s
-1
, min
-1
,
etc).
o Ejemplo: kcat = 500 s-1 , quiere decir que esa enzima cataliza la
transformación de 500 moléculas de sustrato por segundo en su sitio
activo.
• Definición de K
m
:

M. R. – Facultad de Medicina 2020
• Ecuación Michaelis-Menten:
o Si me piden Vmáx:
• Ciclo catalítico (recíproco de Kcat):
Equivalencias:
1M – 1x10
9
nM
1M – 1x10
3
mM
M. R. – Facultad de Medicina 2020
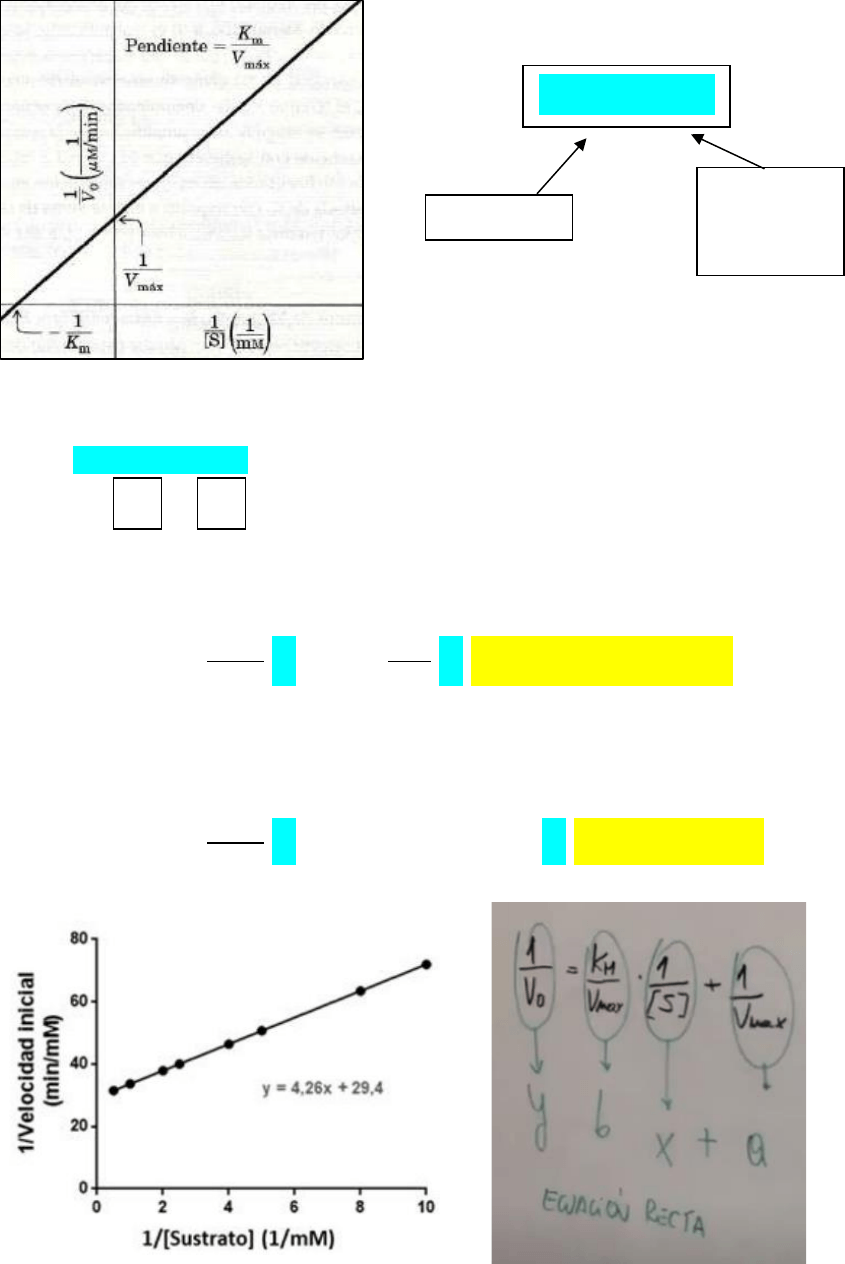
¿Cómo determinar K
m
y V
máx
a partir de un gráfico de doble recíproco?
● Tengo la ecuación de la recta:
1. Me dan:
y = 4,26x + 29,4
2. Primero despejamos V
máx
de la ordenada en el origen:
b = 29,4 =
V
máx
=
V
máx
= 0,034 mM/min
3. Y luego KM de la pendiente:
a = 4,26 =
K
m
= 4, 26 · 0, 034 K
m
= 0,145 mM
y = mx + n
Ordenada
en el
origen
Pendiente
a
b
M. R. – Facultad de Medicina 2020
• Constantes y unidades utilizadas frecuentemente en termodinámica:
o Constante de Boltzmann, k = 1,381 x 10
-23
J/K
o Número de Avogadro, N = 6,022 x 10
23
mol
-1
o Constante de Faraday, F = 96.480 J/V.mol o 96,480 kJ/V.mol
o Constante de los gases, R = 8,315 J/mol.K
Las unidades de temperatura absoluta, T, son grados Kelvin (K).
25°C = 298 K
A 25°C, RT = 8,315 x 298 = 2479 J/mol o 2,479 kJ/mol
• Sistemas:
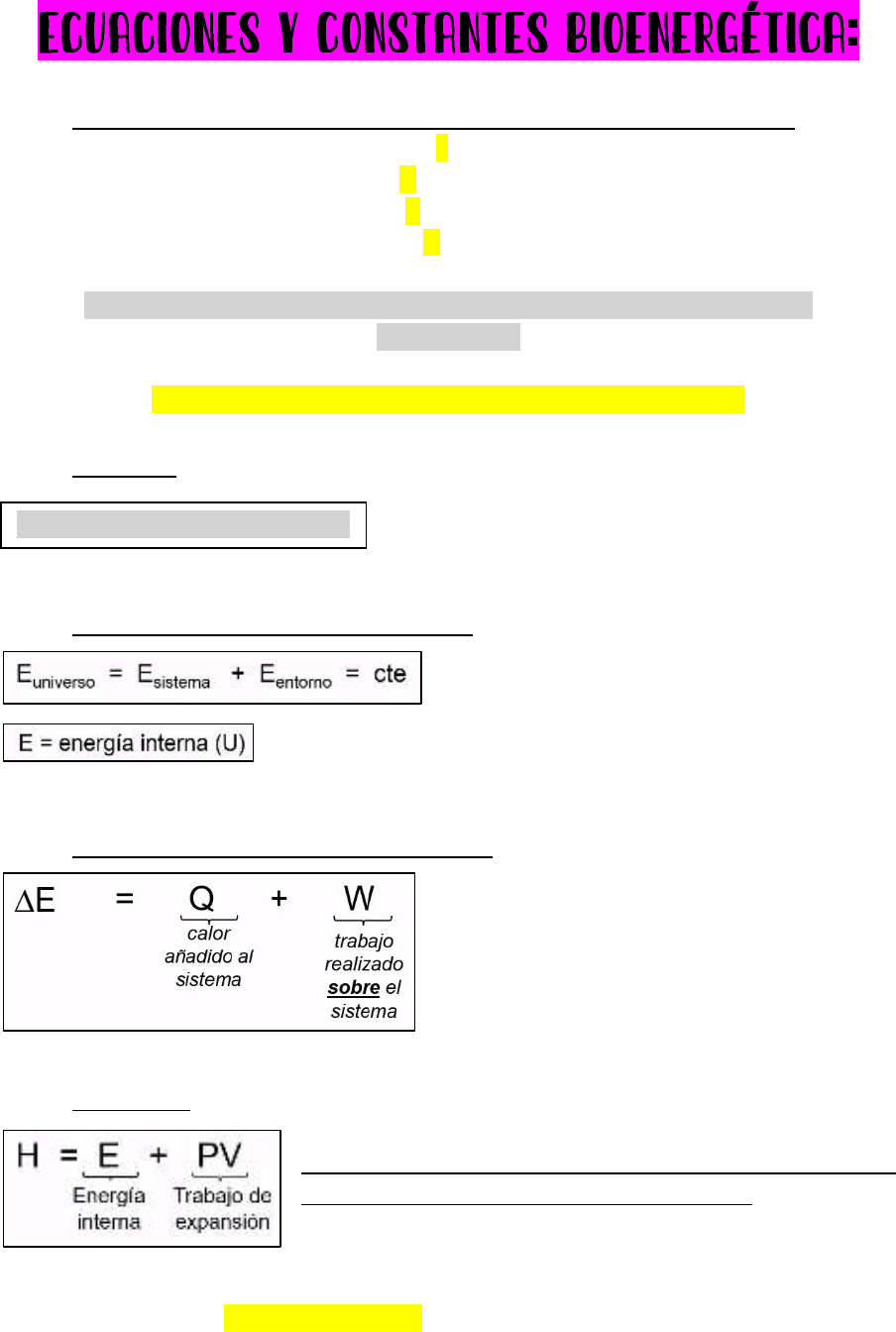
• Energía del universo/sistema/entorno:
• Calcular la variación de energía interna:
• Entalpía H:
La uso para calcular la energía interna (no la variación),
porque E no se puede medir directamente.
o Signo: + (ENDO) – (EXO)
o Unidad: energía/mol
Sistema + entorno = universo
M. R. – Facultad de Medicina 2020
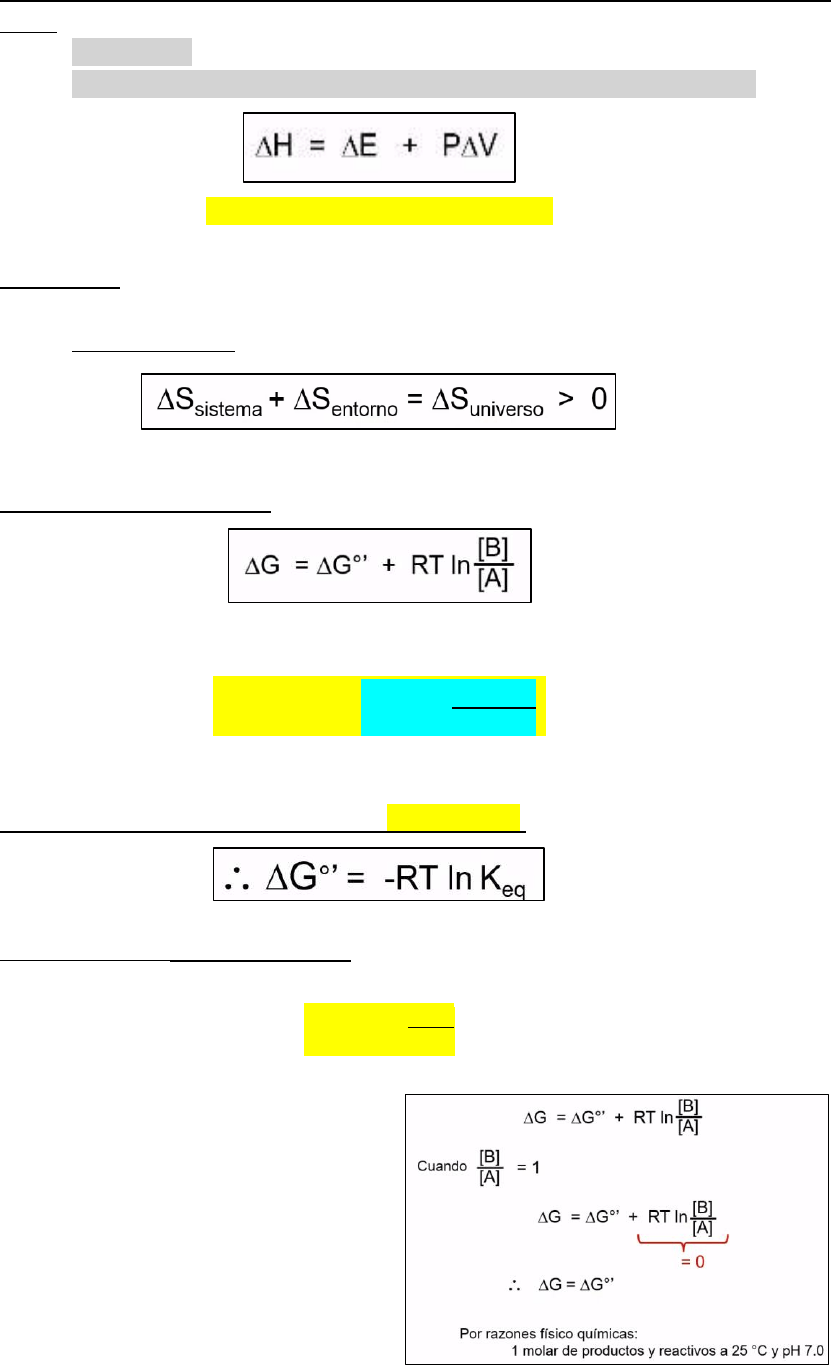
• La entalpía H tampoco se puede medir directamente, para eso uso la variación
de H:
o H = E + PV (ecuación anterior) NO
o ΔH = ΔE (si lo puedo obtener, q+w) + PΔV (si lo puedo obtener)
A T constante: ΔH = ΔG + TΔS
• Entropía S:
o Variación de S:
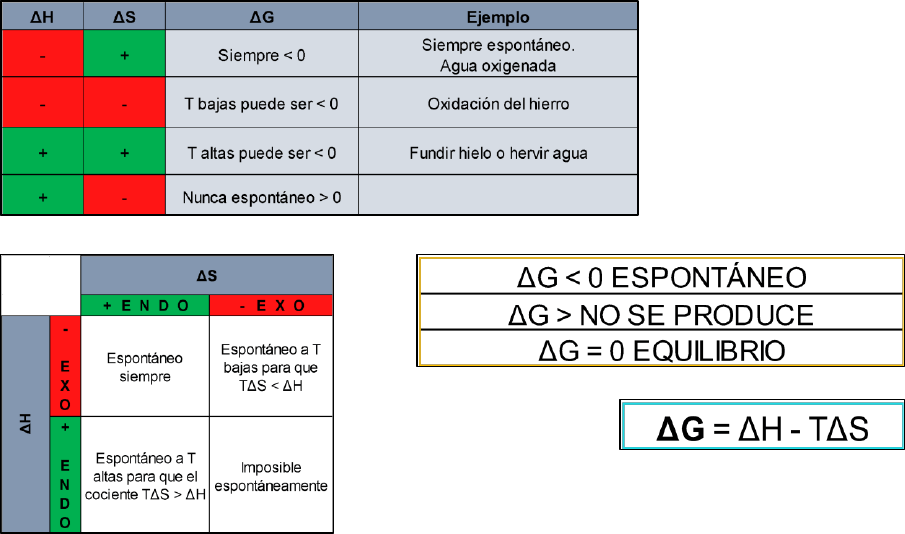
• Energía libre de Gibbs G:
Hago todo de corrido con paréntesis en la división, cuando arranca y cuando termina.
• Variación de energía libre estándar: 25°C y pH 7.
• Si me piden K
eq
a partir de ΔG°’:
• Cuando concentraciones de
reactivos y productos son iguales:
M. R. – Facultad de Medicina 2020
Funciones de estado:
• Energía cinética
• Energía potencial
• Volumen
• Temperatura
• Entalpía ΔH
• Energía libre ΔG
• Entropía ΔS
Funciones de trayectoria:
• Trabajo (W)
• Calor (q)

M. R. – Facultad de Medicina 2020
● Uso esta para determinar el E de cada semirreacción (generalmente uso
directamente y me lo dan):
● Cuando tengo los dos valores, los resto y obtengo ∆E.
● Cuando tengo ese valor puedo calcular ∆G en esta ecuación:
● n: número de electrones que se transfieren
● f: constante de Faraday = F = 96.480 J/V.mol o 96,480 kJ/V.mol
● ∆E⁰’: diferencia entre el E⁰’ de reducción del aceptor menos el E⁰’ del dador.
● ΔG es siempre < 0 en las redox
Semirreacciones
Captan electrones
(Ganan)
E°’ positivo
agentes oxidantes
Ceden electrones
(Pierden)
E°’ negativo
agentes reductores
M. R. – Facultad de Medicina 2020

M. R. – Facultad de Medicina 2020
● : constante de Faraday = F = 96.480 J/V.mol o 96,480 kJ/V.mol
● ∆Ψ: potencial de membrana
● ΔpH = [H
+
ext
] / [H
+
int
]

Ecuaciones.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.