DISOCIACIÓN DEL AGUA Y CONCEPTO DE pH
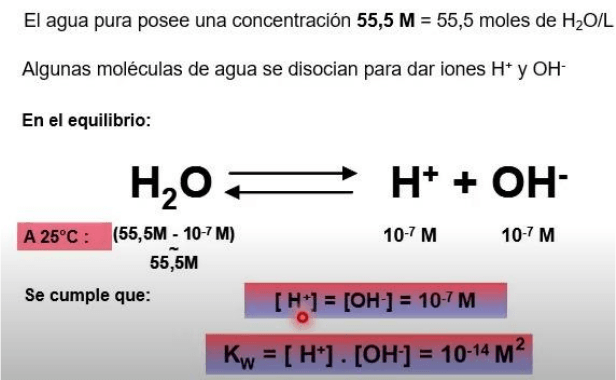
El agua pura posee una concentración 55,5 M = 55,5 moles de H2O/L.
Algunas de esas moléculas de agua se disocian para dar iones, protones y oxidrilos, de H+
Y OH-.
El proceso es reversible de modo tal que cuando alcancemos el equilibrio, la velocidad de
disociación de agua para generar protones y oxidrilos, va a ser igual a la velocidad, de Re
asociación de estos protones y oxidrilos, para volver a generar agua, de modo tal que, las
concentraciones de iones, protones, las concentraciones de los iones, oxidrilos, y la
concentración del agua, alcanzado el equilibrio va a ser constante.
En el equilibrio y a 25 grados centígrados, la molécula de agua se disocia muy poco, de
modo tal que, la concentración de protones, y las concentraciones de oxidrilos son iguales
y pequeñas igual a 10 a la menos 7(10/7) mientras que la concentración de agua se
mantiene aproximadamente en 55,5 molar.
Siempre se cumple estas condiciones, que la concentración de protones entonces es igual
a la concentración de oxidrilos e igual a 10 a la menos 7 molar y que el producto de las
concentraciones molares de protones y oxidrilos es igual a 10 a la menos 14 es lo que se
conoce como constante de disociación del agua o Kw.
¿Qué sucede con las concentraciones de protones de protones (H+) y oxidrilos (OH-)
cuando adicionamos pequeñas cantidades de un ácido o en una base fuerte para generar
soluciones diluidas del ácido o de la base correspondiente?
¿Qué es un ácido y una base? Hay 2 tipos de definiciones.
ARRHENIUS: un ácido es una sustancia que contiene un exceso de protones (H+)
mientras que una base es una sustancia que contiene un exceso de oxidrilos (OH-).
BRONSTED-LOWRY: un acido es una sustancia capaz de ceder protones (donor de
protones) y una base es una sustancia capaz de tomar protones (aceptor de protones).
• Los ácidos y bases fuertes se disocian completamente en agua.
• Los ácidos y bases débiles se disocian parcialmente en agua.
Ahora si vamos a ver que sucederá, con la concentración de protones y de oxidrilos
cuando adicionemos al agua pura, pequeñas cantidades de un acido fuerte para generar
una solución acida diluida.
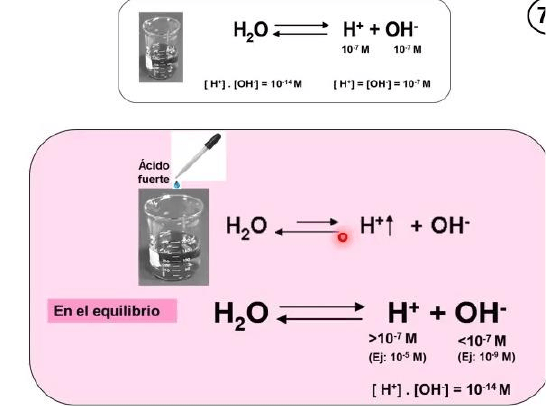
Cuando agreguemos el ácido, la concentración de protones va a aumentar , de modo tal
que, la situación de equilibrio que teníamos se rompe, el sistema va a reaccionar tratando
de recompensar, esa perturbación que a sufrido y va a aumentar la Re asociación de
protones y oxidrilos para regenerar agua, en ese proceso, la concentración de oxidrilos
claramente va a disminuir, va a ser menor que 10 a la menos 7, mientras que la
concentración de protones va a ser mayor que 10 a la menos 7, siempre se va a seguir
cumpliendo con la concentración de protones por la concentración de oxidrilos va a ser 10
a la menos 14, entonces en una solución acida, la concentración de protones es mayor
que 10 a la menos 7 y la concentración de oxidrilos va a ser menor que 10 a la menos 7.
Que va suceder con esa concentración de protones y oxidrilos, cundo lo que
adicionaremos al agua pura, sea pequeñas cantidades de una base fuerte para generar
una solución alcalina diluida, en esa situación, lo que va a suceder , es que lo que va a
aumentar en el sistema es la concentración de oxidrilo, nuevamente el equilibrio se va a
romper, el sistema va a reaccionar tratando de contra restarlo y en ese proceso lo que va
a suceder es que la concentración de protones va a ser menor que 10 a la menos 7, la
concentración de oxidrilos va a ser mayor que 10 a la menos 7, se sigue manteniendo que
la concentración de protones por la concentración de oxidrilos una vez regenerando el
equilibrio va a ser 10 a la menos 14 , en una solución básica o alcalina diluida, la
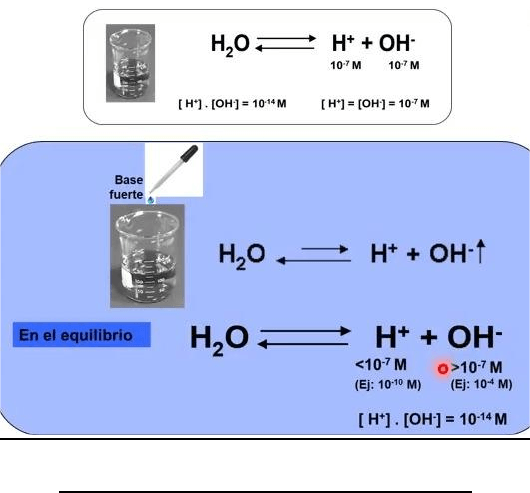
concentración de protones va a ser menor que 10 a la menos 7, y la concentración de
oxidrilo va a ser mayor que 10 a la menos 7.
Soluciones neutras, acidas y básicas.
En las soluciones neutras es aquella que la concentración de protones es
igual a los oxidrilos e igual a 10 a la menos 7 molar en ambos casos.
Las soluciones acidas, son aquellas en que las concentraciones de protones
superan a la concentración de oxidrilo, de modo, que la concentración de
protones es mayor que 10 a la menos 7, y la de oxidrilos es menor que 10 a la
menos 7.
En una solución básica, la concentración de protones es inferior a la
concentración de oxidrilos es menor que 10 a la menos 7, y la concentración
de oxidrilos es mayor que 10 a la menos 7.
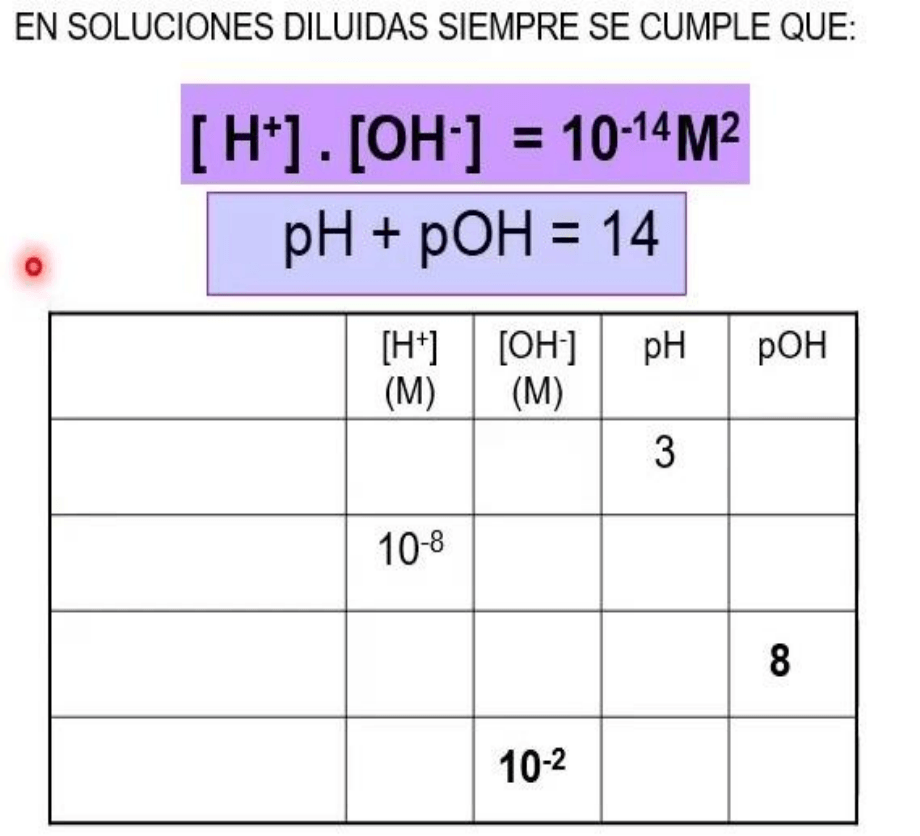
Siempre se cumple que, en el equilibrio, la concentración de protones por la
concentración de oxidrilos es igual a 10 a la menos 14.
Como podemos observar las concentraciones de protones y oxidrilos, en el agua pura, en
las soluciones acidas y soluciones básicas diluidas son muy bajas.

Se define como “P” a un operador matemático que implica aplicar la función: -log 10 de
modo que: si tenemos pX es igual a menos logaritmo de X. pX=-logX.
Siempre que aparezca el operador P, nos esta diciendo que aplique la función menos
logaritmo.
Por lo tanto, cuando hablamos de pH, estamos hablando de menos logaritmo de la
concentración de protones.
pOH es menos logaritmo de la concentración de oxidrilo.
pK es menos de logaritmo de la constante de equilibrio.
Aplicando este concepto del operador P y partiendo de la constante disociación del agua,
que recordemos que la concentración de protones por la concentración de oxidrilos igual
siempre a 10 a la menos 14.
Si aplicamos logaritmo a ambos miembros de esta ecuación pasaríamos a tener esta
ecuación que tenemos aquí; log([H+]. ([OH-]) =log (10-14).
Aplicando las propiedades de los logaritmos que dicen que el logaritmo de una
multiplicación es igual a la suma de los logaritmos y teniendo en cuenta que el logaritmos
en base 10 de 10 a la menos 14, va a ser igual a menos 14, pasaríamos a tener esta
ecuación que tenemos aquí; log[H+]+log [OH-]=-14.
Si multiplicamos ambos términos por menos 1, pasaríamos a tener esta ecuación; -
log[H+]-log [OH-]=14.
En la que nos parece menos logaritmo de la concentración de protones que es el pH,
menos el logaritmo de la concentración de oxidrilos que es pOh, de modo tal que,
podemos decir que pH mas pOH es igual a 14.
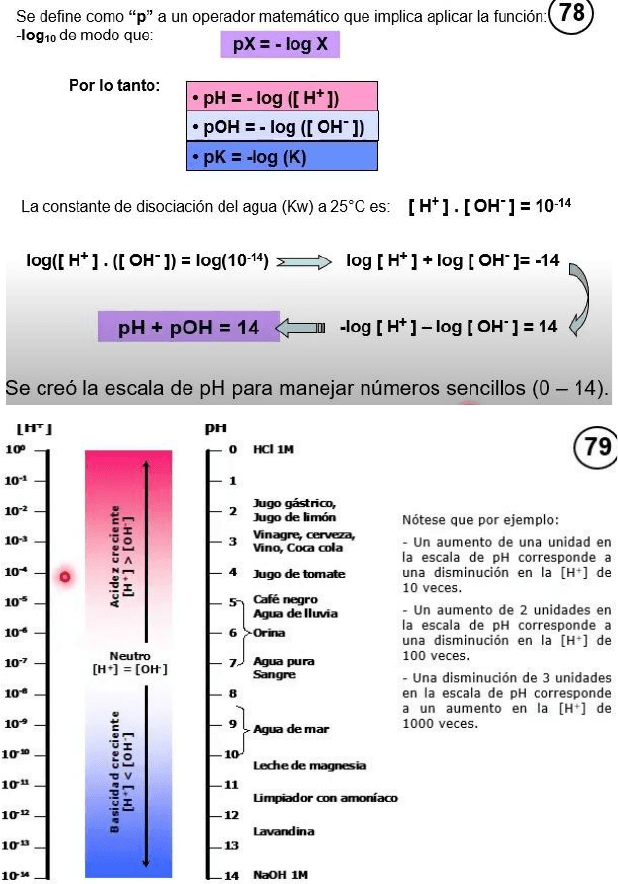
Esta manera se creo la escala del pH para manejar números sencillos (0-14).
Si la concentración de protones aumenta 10 veces, el pH disminuye en una unidad, si el
pH aumenta en una unidad la concentración de protones disminuye 10 veces, si el pH
aumenta en dos unidades la concentración de protones disminuye 100 veces.

DISOCIACIÓN DEL AGUA Y CONCEPTO DE pH.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.