
UNIVERSIDAD NACIONAL DEL CALLAO 1
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”

UNIVERSIDAD NACIONAL DEL CALLAO 2
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
Tabla de contenido
I. INTRODUCCION ......................................................................................................... 3
II. OBJETIVOS ................................................................................................................ 4
III. JUSTIFICACIÓN ......................................................................................................... 5
IV. MARCO TEORICO ...................................................................................................... 6
V. DETALLES EXPERIMENTALES ............................................................................... 7
5.1. Equipos y materiales ....................................................................................................7
5.2. Procedimiento experimental .....................................................................................11
VI. RESULTADOS Y DISCUSIÓN ................................................................................. 12
VII. CONCLUSIONES ...................................................................................................... 17
VIII. REFERENCIAS BIBLIOGRÁFICAS ........................................................................ 18
IX. ANEXOS .................................................................................................................... 19

UNIVERSIDAD NACIONAL DEL CALLAO 3
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
I. INTRODUCCION
El hierro o fierro, es un metal de transición es el cuarto elemento más abundante en
la corteza terrestre, representando un 5% y, entre los metales, sólo el aluminio es
más abundante. Es un metal maleable, de color gris plateado y presenta
propiedades magnéticas; es ferromagnético a temperatura ambiente y presión
atmosférica. Es extremadamente duro y pesado. Se encuentra en la naturaleza
formando parte de numerosos minerales, entre ellos muchos óxidos, y raramente
se encuentra libre. Para obtener hierro en estado elemental, los óxidos se reducen
con carbono y luego es sometido a un proceso de refinado para eliminar las
impurezas presentes. El hierro es el metal más usado, con el 95%en peso de la
producción mundial de metal. El hierro puro (pureza a partir de 99,5%) no tiene
demasiadas aplicaciones, salvo excepciones para utilizar su potencial magnético.
El hierro tiene su gran aplicación para formar los productos siderúrgicos, utilizando
éste como elemento matriz para alojar otros elementos aleantes tanto metálicos
como no metálicos, que confieren distintas propiedades al material. Se considera
que una aleación de hierro es acero si contiene menos de un 2,1% de carbono; si
el porcentaje es mayor, recibe el nombre de fundición. El acero es indispensable
debido a su bajo precio y tenacidad, especialmente en automóviles, barcos y
componentes estructurales de edificios. Las aleaciones férreas presentan una gran
variedad de propiedades mecánicas dependiendo de su composición o el
tratamiento que se haya llevado a cabo. El dicromato de potasio (K2Cr2O7) es una
sal del hipotético ácido di crómico (este ácido en sustancia no es estable)
H2Cr2O7.Se trata de una sustancia de color intenso anaranjado. Es un oxidante
fuerte. Se usa para la determinación de hierro por la oxidación de hierro (II) a hierro
(III), en volumetría de oxido-reducción.

UNIVERSIDAD NACIONAL DEL CALLAO 4
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
II. OBJETIVOS
Determinar el porcentaje de hierro en la muestra.
Aplicar los principios básicos de las volumetrías redox en las titulaciones.
Aplicar el concepto estadístico de desviación estándar para evaluar la
precisión de los resultados obtenidos.

UNIVERSIDAD NACIONAL DEL CALLAO 5
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
III. JUSTIFICACIÓN
La valoración o titulación es un método de análisis químico cuantitativo en el
laboratorio que se utiliza para determinar la concentración desconocida de un
reactivo a partir de un reactivo con concentración conocida. Debido a que las
medidas de volumen desempeñan un papel fundamental en las titulaciones, se le
conoce también como análisis volumétrico
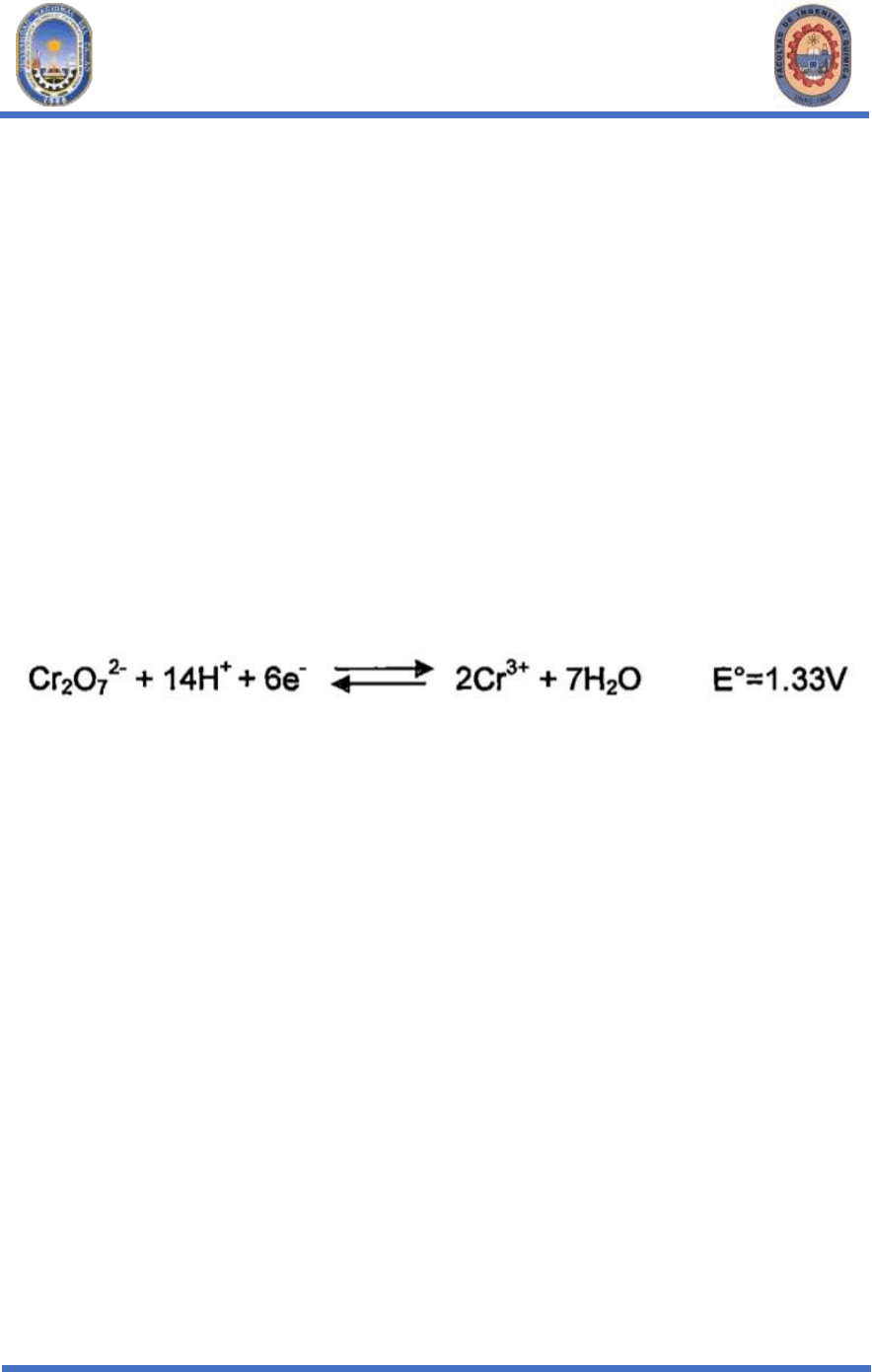
UNIVERSIDAD NACIONAL DEL CALLAO 6
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
IV. MARCO TEORICO
El Hierro se disuelve en ácidos minerales diluidos. Con ácidos. no oxidantes y en
ausencia de aire, se obtiene el Fe +2. Cuando está presente el aire, o cuando se
usa ácido nítrico diluido no muy caliente, parte del hierro pasa a Fe+3. En medios
fuertemente oxidantes como el ácido nítrico concentrado hacen pasivo al hierro.
METODO DE DICROMATOMETRIA
La dicromatometría se basa en la reacción de oxidación con el ion dicromato. Su
acción se debe a la transformación de aniones Cr207(2-) que contienen como en el
grado de oxidación +6, en cationes Cr3 +
La reducción de iones Cr2O7(2-) aCr3 + se produce con la participación de iones
H+, la titulación dicromatométrica se realiza en medio acido, donde, el ion dicromato,
es un oxidante fuerte que reduce al ion crómico.
Puesto que el Cr2O7(2-) es de color naranja y los complejos de Cr3 + viran del verde
al violeta, se deben utilizar indicadores redox para detectar el punto final de las
valoraciones, en la dicromatometria se utiliza generalmente la difenilamina.
Técnica del método
Luego de recoger las muestras que contienen hierro titulamos con solución de
dicromato de potasio, al inicio de la titulación la solución tomará un color verduzco,
luego irá cambiando a verde azulado y por último aun color azul-violáceo que se
mantiene invariable, el cual indica el punto final de la titulación.

UNIVERSIDAD NACIONAL DEL CALLAO 7
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
V. DETALLES EXPERIMENTALES
5.1. Equipos y materiales
Materiales
Imagen
Probeta de 10 mL
MATRACES AFORADOS
DE 250mL y 100mL
BURETA DE 50mL

UNIVERSIDAD NACIONAL DEL CALLAO 8
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
PIPETAS DE 10 a 25mL
VIDRIOS DE RELOJ
VARILLA AGITADORA

UNIVERSIDAD NACIONAL DEL CALLAO 9
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
VASOS PRECIPITADOS
DE 250 mL
AGITADOR
MAGNETICO
DICROMATO DE
POTASIO K2Cr2O7
UNIVERSIDAD NACIONAL DEL CALLAO 10
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
ACIDO SULFURICO AL
5% H2SO4
DIFENILAMINA

UNIVERSIDAD NACIONAL DEL CALLAO 11
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
5.2. Procedimiento experimental
A. Estandarización de la disolución de K2Cr2O7
La estandarización de la solución K2Cr2O7 0,1 N es por pesada directa;
instale una bureta de 50 mL con la disolución de K2Cr2O7 0,1 N preparada.
Realice los cálculos para determinar la masa a pesar de K2Cr2O7 0, 1 N.
B. Determinación de hierro
Pesar muestra entre 0,2 a 0,3 gramos y disolver en un erlenmeyer de 250ml.
Añadir 30mL de agua, 100ml de ácido sulfúrico H2SO4 5% y 10 gotas de
indicador difenilamina.
Colocar un agitador magnético.
Titular (hasta cambio a color azul).
Repetir la valoración dos veces.
Calcular % de hierro en la muestra

UNIVERSIDAD NACIONAL DEL CALLAO 12
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
VI. RESULTADOS Y DISCUSIÓN
Datos: K
2
Cr
2
O
7
0,1 N
Valor teórico=Fe (SO
4
)
2
(NH
4
)
2
.6H
2
O
ppm
I
II
III
IV
Peso muestra (g.)
0,2015
0,2060
0,2005
0,2020
Volumen gastado K
2
Cr
2
O
7
(mL)
5,2
5,3
5,1
5,2
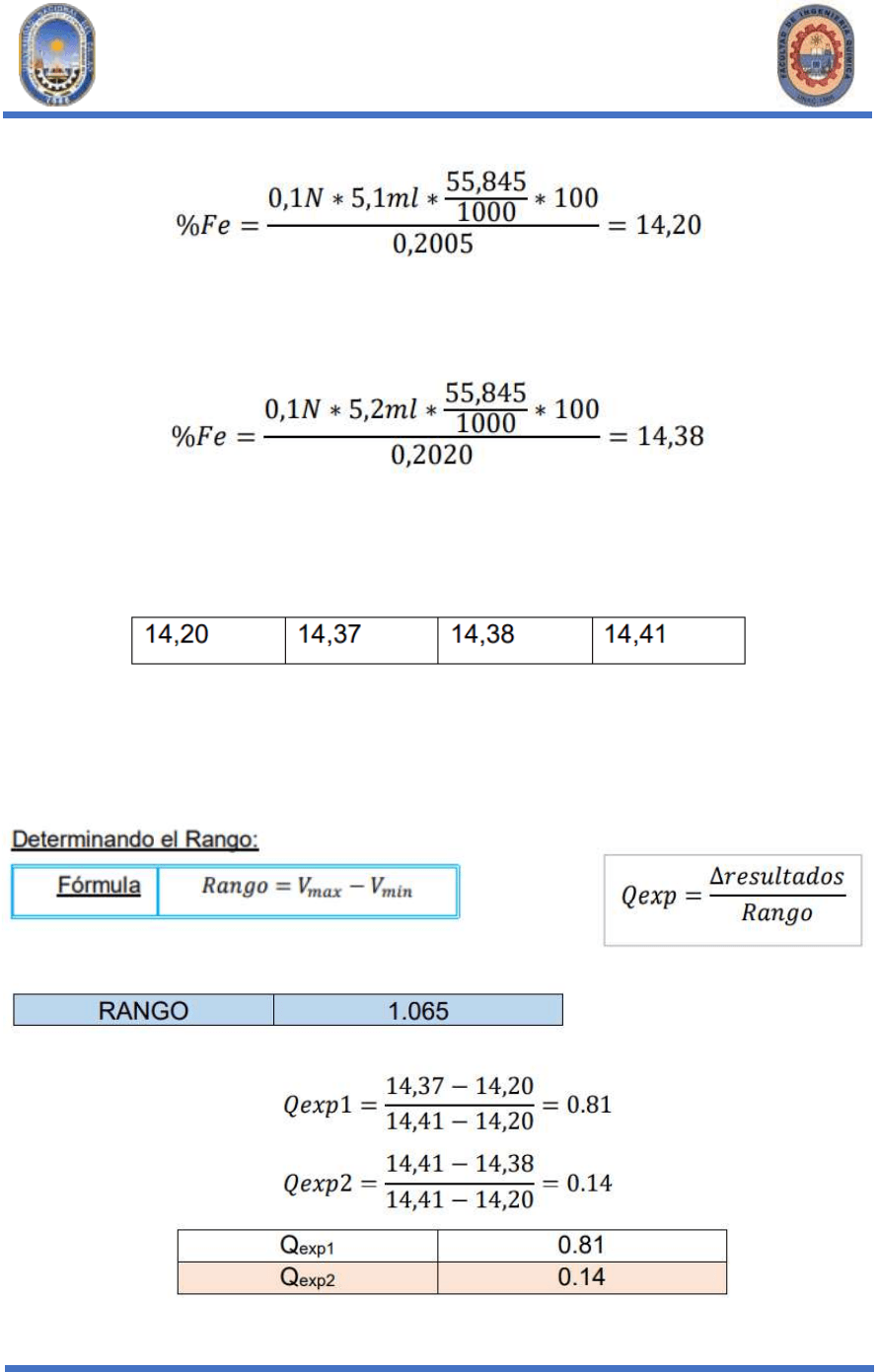
Calcular: a) % Fe, b) % C.V., c) % valor recuperación y d) valor reportar.
CALCULO:
Grupo 1:
Grupo 2:
UNIVERSIDAD NACIONAL DEL CALLAO 13
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
Grupo 3:
Grupo 4:
Ordenando los datos:
✓ Analizamos los resultados (Rechazo de datos), ya que existen resultados
dudosos.
UNIVERSIDAD NACIONAL DEL CALLAO 14
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
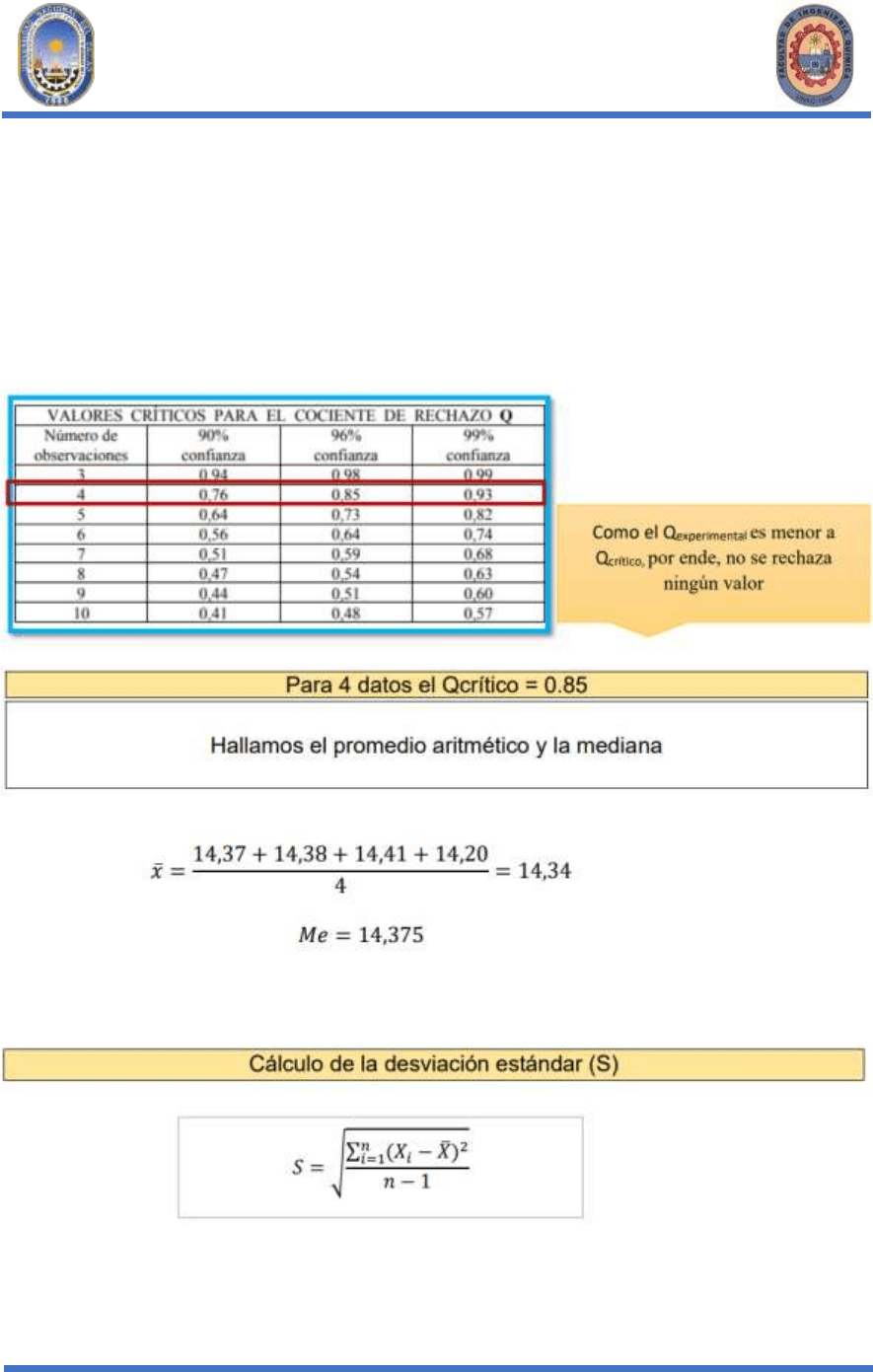
➢ Rechazo de datos:
Para rechazar alguno de los datos (Valor máximo o mínimo) debe cumplirse la
siguiente condición: Qexperimental ≥ Qcrítico. El valor del Q critico se encuentra en
tabla, obteniéndose el siguiente dato: Qcrítico = 0.85
Hallamos el Qcrítico de tablas
➢ Calculando la desviación estándar (PRECISIÓN) y el coeficiente de variación.

UNIVERSIDAD NACIONAL DEL CALLAO 15
Facultad de Ingeniería Química
Química Analítica Cuantitativa
Informe 11 - “Determinación de hierro”
OBSERVACIÒN:
Como el coeficiente de variación es menor a 1.3 se aceptan esos 4 valores, esto
nos indica que hay buena precisión entre estos 4 valores aceptados.
Este documento contiene más páginas...
Descargar Completo
Determinacion-Del-Hierro 549232713-Informe-Nº11.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.