DESARROLLO DEL SISTEMA GENITAL
El sexo cromosómico de un embrión queda determinado en el momento de la fecundación por el tipo de espermatozoide (X o Y) que
se introduce en el ovocito. Las características morfológicas propias de los sexos masculino y femenino no empiezan a desarrollarse
hasta la séptima semana.
Los sistemas genitales iniciales son similares en ambos sexos, por lo que el período inicial del desarrollo genital se denomina fase
indiferente del desarrollo sexual.
DESARROLLO DE LAS GÓNADAS
Las gónadas son los órganos que producen las células sexuales, y tienen 3 orígenes:
o El mesotelio (epitelio mesodérmico) que reviste la pared abdominal posterior.
o El mesénquima (tejido conjuntivo embrionario) subyacente, de origen mesodérmico.
o Las células germinales primordiales (las células sexuales indiferenciadas iniciales).
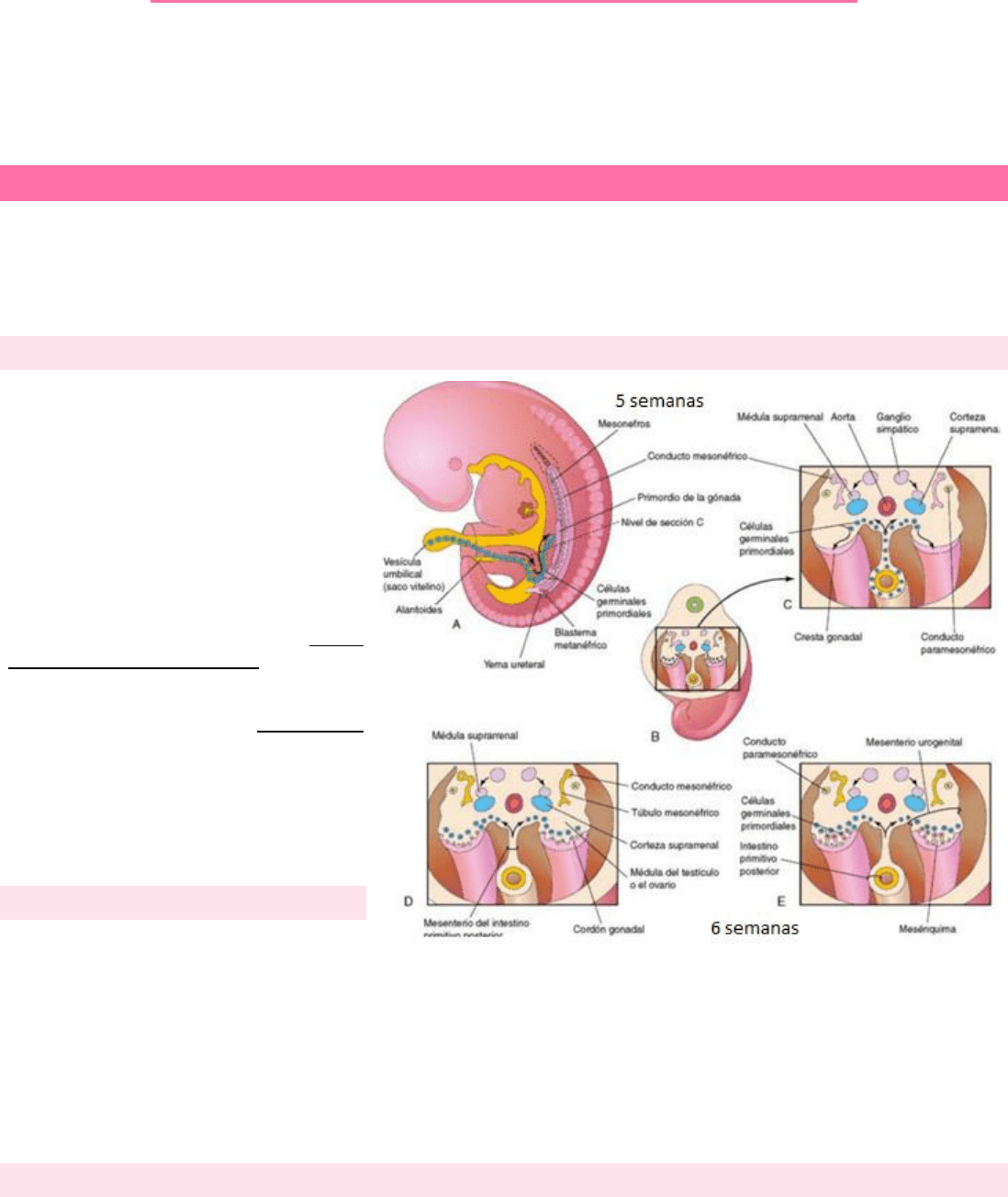
GÓNADAS INDIFERENCIADAS
Las fases iniciales del desarrollo gonadal
ocurren durante la quinta semana, cuando se
desarrolla una zona engrosada de mesotelio en
la parte medial del mesonefros (riñón
primitivo). La proliferación de este epitelio y del
mesénquima subyacente da lugar a una
protrusión en el lado medial del mesonefros, la
cresta gonadal. Al poco tiempo aparecen los
cordones gonadales (cordones epiteliales en
forma de dedo), que crecen en el mesénquima
subyacente. En este momento la gónada
indiferenciada está constituida por una corteza
externa y por una médula interna.
En los embriones con la dotación cromosómica
sexual XX, la corteza de la gónada indiferenciada
se diferencia hacia la formación de un ovario
mientras que la médula experimenta una
regresión. En los embriones con la dotación
cromosómica sexual XY, la médula se diferencia
hacia la formación de un testículo, mientras que
la corteza involuciona.
CÉLULAS GERMINALES PRIMORDIALES
Las células sexuales grandes y esféricas pueden
identificarse inicialmente a los 24 días de la fecundación entre las células endodérmicas de la vesícula umbilical (cerca del origen de
la alantoides).
Durante el plegamiento del embrión, la parte dorsal de la vesícula umbilical queda incorporada en el embrión. Mientras esto sucede,
las células germinales primordiales migran a lo largo del mesenterio dorsal del intestino primitivo posterior hasta alcanzar las crestas
gonadales. En el transcurso de la sexta semana, las células germinales primordiales se introducen en el mesénquima subyacente y se
incorporan en los cordones gonadales.
La migración de las células germinales primordiales está regulada por los genes Stella, Fragilis y BMP-4.
FUNDAMENTO CROMOSÓMICO DE LA DETERMINACIÓN SEXUAL
Antes de la séptima semana, las gónadas de ambos sexos se denominan gónadas indiferenciadas.

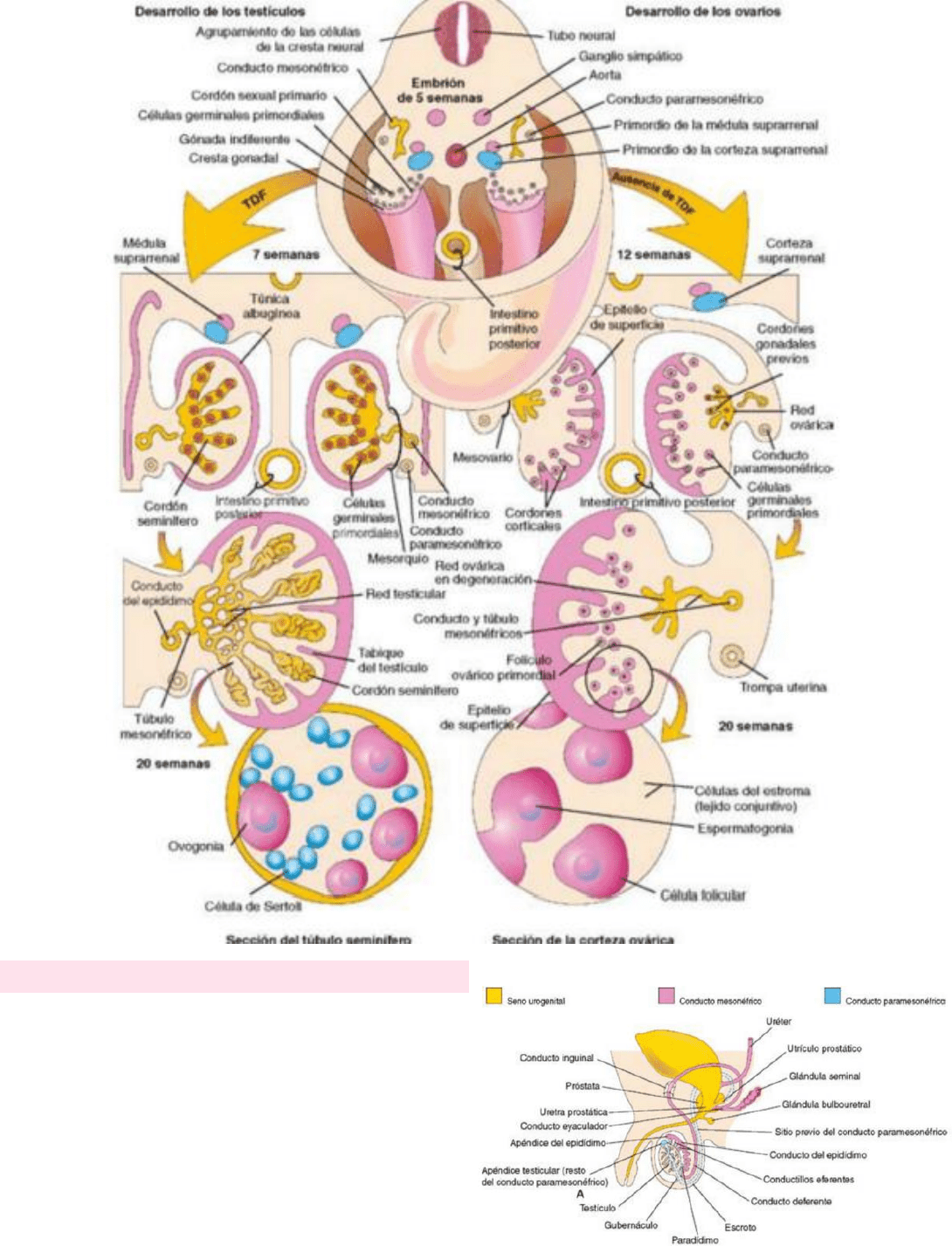
El desarrollo del fenotipo masculino requiere la presencia de un cromosoma Y. El gen SRY (región de la determinación del sexo en el
cromosoma Y), que codifica un factor determinante de los testículos (TDF) y se encuentra localizado en la región del brazo corto del
cromosoma Y, es el factor que determina la diferenciación testicular. Bajo la influencia de éste, los cordones gonadales se diferencian
hacia la formación de cordones seminíferos (primordios de los túbulos seminíferos). La testosterona (producida por los testículos
fetales), la dihidrotestosterona y la hormona antimülleriana determinan la diferenciación sexual masculina normal, que se inicia
durante la séptima semana.
Para que se desarrolle el fenotipo femenino se necesita la presencia de dos cromosomas X. Diversos genes y regiones del cromosoma
X desempeñan funciones especiales en la determinación sexual. El desarrollo ovárico se produce cuando no hay cromosoma Y y se
inicia aproximadamente en la semana 12. La diferenciación sexual femenina primaria no depende de las hormonas y ocurre incluso
en ausencia de los ovarios.
DESARROLLO DE LOS TESTÍCULOS
El TDF induce la condensación y extensión de los cordones seminíferos hacia la médula de la gónada indiferenciada, donde se ramifican
y anastomosan formando la red testicular. La conexión de los cordones seminíferos con el epitelio de superficie desaparece al
desarrollarse una cápsula fibrosa gruesa: la túnica albugínea. El desarrollo de ésta es el rasgo distintivo del desarrollo testicular. De
manera gradual, el testículo que está aumentando de tamaño se separa del mesonefros en degeneración y queda suspendido por el
mesorquio (su propio mesenterio). Los cordones seminíferos se transforman en los túbulos seminíferos, los túbulos rectos y la red
testicular.
Los túbulos seminíferos están separados por el mesénquima que origina las células intersticiales (de Leydig). Hacia la octava semana,
éstas células comienzan a secretar hormonas androgénicas (testosterona y androstenediona), que inducen la diferenciación masculina
de los conductos mesonéfricos y de los genitales externos.
La producción de testosterona está estimulada por la GCH, que alcanza sus concentraciones máximas durante el período entre la 8ª
y 12ª semana. Las células de Sertoli producen la AMH o MIS (sustancia inhibidora mülleriana - una hormona glucoproteica) hasta la
pubertad, donde luego se reducen sus concentraciones. Esta hormona suprime el desarrollo de los conductos paramesonéfricos, que
forman el útero y las trompas uterinas.
Los túbulos seminíferos no muestran una luz en su interior hasta la pubertad. Las paredes de éstos se componen de dos tipos de
células:
1. Las células de Sertoli, que desempeñan una función de soporte y que proceden del epitelio de superficie de los testículos.
2. Las espermatogonias, células espermáticas primordiales derivadas de las células germinales primordiales (CGP).
Durante el desarrollo fetal tardío, el epitelio de superficie de los testículos se aplana y forma el mesotelio en la superficie externa de
los testículos. La red testicular se continúa con 15-20 túbulos mesonéfricos que se convierten en los conductillos eferentes; que están
conectados con el conducto mesonéfrico, que luego se convierte en el conducto del epidídimo.
DESARROLLO DE LOS OVARIOS
El desarrollo gonadal tiene lugar de manera lenta en los embriones de sexo femenino. El ovario no puede identificarse
histológicamente hasta + o – la semana 10. Los cordones gonadales no son prominentes en un ovario en desarrollo, pero se extienden
hacia la médula y forman una red ovárica rudimentaria, que luego degeneran y desaparecen.
Los cordones corticales se extienden desde el epitelio de superficie del ovario en desarrollo hasta el mesénquima subyacente (procede
del mesotelio peritoneal) a lo largo del período fetal temprano. A medida que los cordones corticales aumentan de tamaño las CGP
quedan incorporadas en su interior. Aproximadamente a las 16 semanas estos cordones comienzan a fragmentarse y aparecen grupos
celulares aislados (folículos primordiales); cada uno contiene una ovogonia que procede de una CGP. Los folículos están rodeados por
una capa única de células foliculares aplanadas que proceden del epitelio de superficie. Durante la vida fetal, las ovogonias muestran
mitosis activas y esto da lugar a los folículos primordiales.
Tras el nacimiento, el epitelio de superficie del ovario se aplana y forma una capa de células que se continúa con el mesotelio peritoneal
en el hilio ovárico. El epitelio de superficie se separa de los folículos de la corteza con la interposición de la túnica albugínea (fina
cápsula fibrosa). A medida que el ovario se separa del mesonefros en regresión, queda suspendido por el mesoovario.
DESARROLLO DE LOS CONDUCTOS GENITALES
Durante la 5ª y 6ª semana, el sistema genital permanece
indiferenciado y están presentes dos pares de conductos
genitales. Los conductos mesonéfricos (de Wolff) desempeñan
una función importante en el desarrollo del sistema reproductor
masculino, mientras que los conductos paramesonéfricos
(müllerianos) desempeñan una función importante en el
desarrollo del femenino.
Los conductos paramesonéfricos se desarrollan lateralmente
respecto a las gónadas y a los conductos mesonéfricos, a cada
lago, a partir de invaginaciones del mesotelio en las partes
laterales del mesonefros. Los bordes de estas invaginaciones se
Recién nacido
aproximan entre sí y se fusionan para formar los
conductos paramesonéfricos. Los extremos craneales
se éstos se abren hacia la cavidad peritoneal.
Caudalmente, estos conductos discurren paralelos a los
conductos mesonéfricos hasta que alcanzan la futura
región pélvica del embrión. Aquí, cruzan ventralmente a
los conductos mesonéfricos, se aproximan entre sí en el
plano medio y se fusionan formando un primordio
uterovaginal con forma de Y. Esta estructura se
proyecta hacia la pared dorsal del seno urogenital y
produce una elevación: el tubérculo del seno.
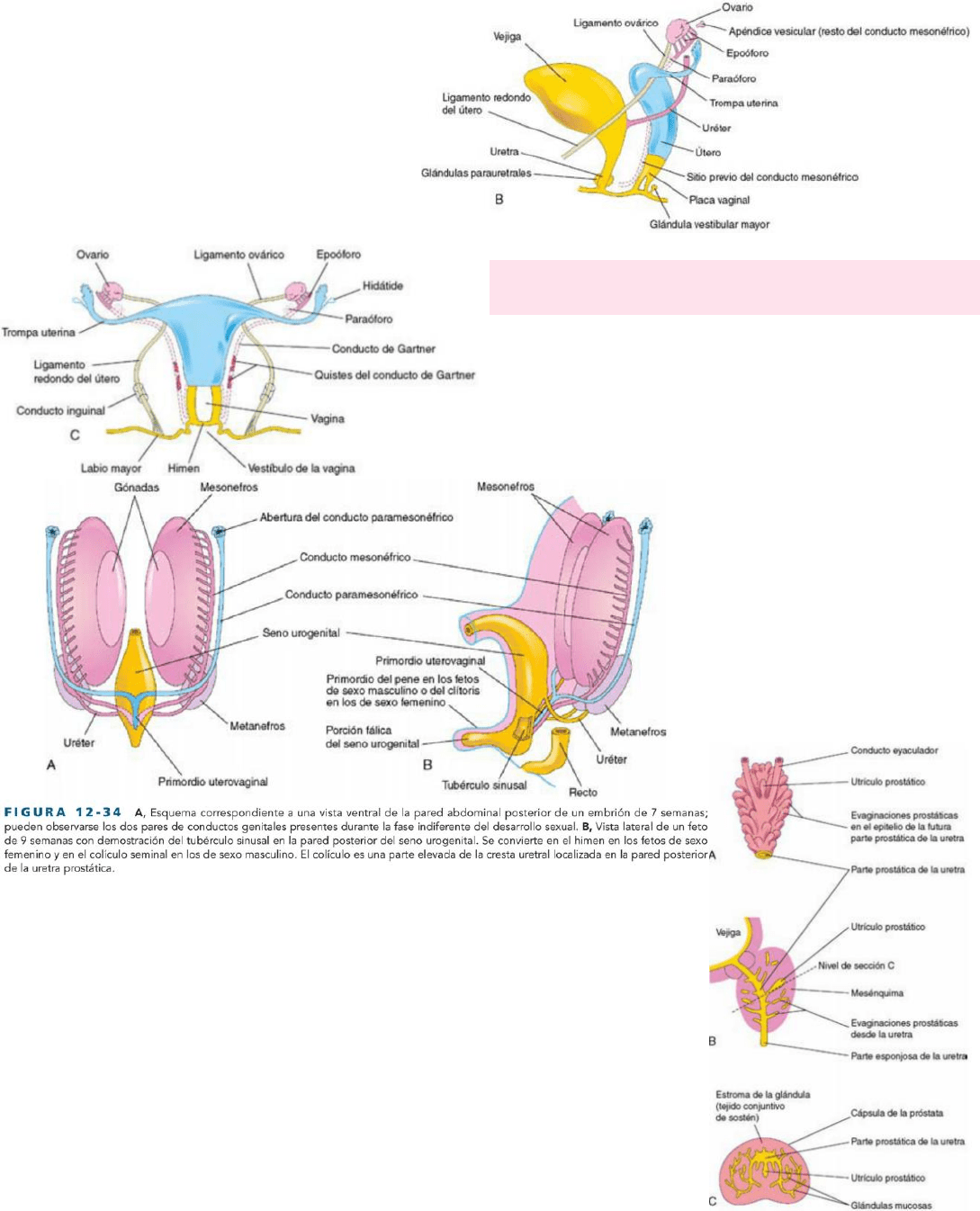
DESARROLLO DE LOS CONDUCTOS Y LAS GLÁNDULAS DEL
TRACTO GENITAL MASCULINO
Los testículos fetales producen hormonas masculinizantes (como
la testosterona) y MIS (AMH). Las células intersticiales comienzan
a producir testosterona durante la octava semana; ésta estimula
los conductos mesonéfricos para la formación de los conductos
genitales masculinos, mientras que la MIS suprime el desarrollo de
los conductos paramesonéfricos. Bajo la influencia de la
testosterona, la parte proximal de cada conducto mesonéfrico se
enrolla para formar el epidídimo.
A medida que degenera el
mesonefros persisten algunos
túbulos mesonéfricos y se
transforman en los conductillos
eferentes, que se abren en el
conducto del epidídimo en esta
región. Distalmente al epidídimo,
el conducto mesonéfrico
adquiere una gruesa capa de
músculo liso y se convierte en
conducto deferente.
GLÁNDULAS SEMINALES
En el extremo caudal de cada conducto mesonéfrico aparecen evaginaciones laterales que se
convierten en vesículas seminales (glándulas), que producen la secreción que constituye la
mayor parte del líquido del eyaculado y nutre a los espermatozoides. La parte del conducto
mesonéfrico que queda entre el conducto de esta glándula y la uretra se convierte en el
conducto eyaculador.
PRÓSTATA
En la parte prostática de la uretra aparecen muchas evaginaciones endodérmicas que crecen
hacia el mesénquima adyacente. El epitelio glandular de la próstata se diferencia a partir de
estas células endodérmicas y e mesénquima asociado se diferencia hacia la formación del
estroma denso y el músculo liso de la próstata.
GLÁNDULAS BULBOURETRALES
Se desarrollan a partir de evaginaciones bilaterales en la parte esponjosa de la uretra. Las fibras musculares lisas y el estroma proceden
de la diferenciación del mesénquima adyacente. Las secreciones de estas glándulas contribuyen al semen.
12 semanas
Recién
nacida
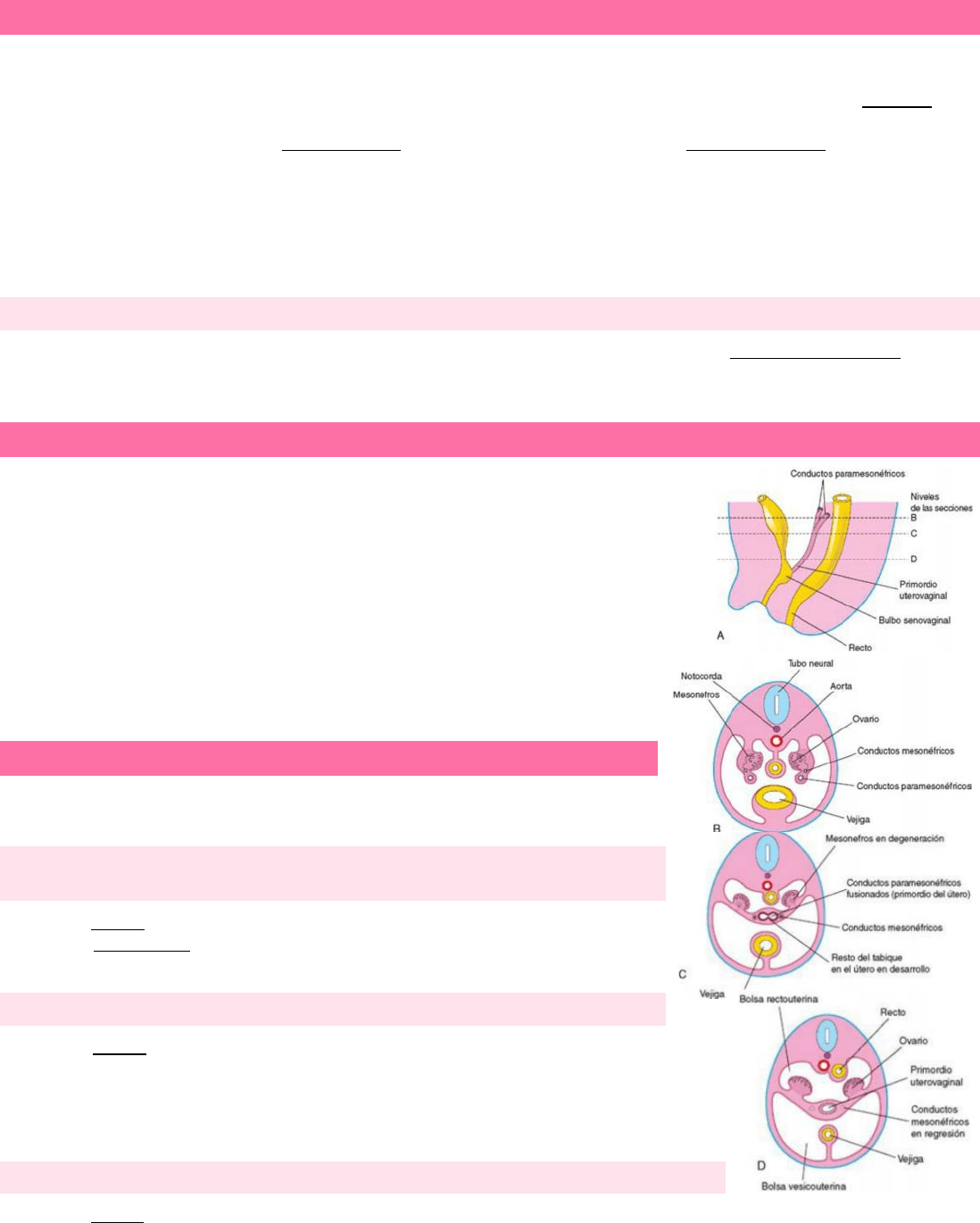
DESARROLLO DE LOS CONDUCTOS Y LAS GLÁNDULAS DEL TRACTO GENITAL FEMENINO
Los conductos mesonéfricos de los embriones femeninos experimentan una regresión debido a la ausencia de testosterona; los
conductos paramesonéfricos se desarrollan gracias a la ausencia de MIS. El desarrollo sexual femenino durante el período fetal no
depende de la presencia de ovarios o de hormonas, sino que, más adelante, los estrógenos producidos por los ovarios maternos y por
la placenta estimulan el desarrollo de las trompas uterinas, el útero y la parte superior del tracto genital femenino. Las trompas
uterinas se desarrollan a partir de las partes craneales no fusionadas de estos conductos. Las porciones caudales fusionadas de estos
conductos forman el primordio uterovaginal, que origina el útero y la parte superior de la vagina.
La fusión de los conductos paramesonéfricos también genera un pliegue peritoneal que se convierte en el ligamento ancho y que
define dos espacios peritoneales: la bolsa o saco rectouterino y la bolsa o saco vesicouterino. A lo largo de las partes laterales del
útero (entre las capas del ligamento ancho) el mesénquima prolifera y se diferencia hacia un tejido celular: el parametrio, constituido
por tejido conjuntivo laxo y músculo liso.
GLÁNDULAS AUXILIARES DEL TRACTO GENITAL FEMENINO
Varias evaginaciones de la uretra en el mesénquima adyacente forman las glándulas uretrales y las glándulas parauretrales (secretan
moco). Otras evaginaciones aparecen en el seno urogenital y forman las glándulas vestibulares mayores en el 1/3 inferior de los labios
mayores, que secretan moco y son análogas a las glándulas bulbouretrales masculinas.
DESARROLLO DE LA VAGINA
La pared fibromuscular de la vagina se desarrolla a partir del mesénquima adyacente. El contacto
del primordio uterovaginal con el seno urogenital da lugar a que se forme el tubérculo sinusal
e induce la formación de evaginaciones endodérmicas bilaterales, los bulbos senovaginales, que
se extienden desde el seno urogenital hasta el extremo caudal del primordio uterovaginal. Los
bulbos senovaginales forman una placa vaginal, donde luego se formará la luz de la vagina. El
epitelio vaginal procede de las células periféricas de la placa vaginal.
Hasta etapas avanzadas de la vida fetal, la luz de la vagina está separada de la cavidad del seno
urogenital por el himen, membrana formada por la invaginación de la pared posterior del
seno urogenital, que resulta de la expansión del extremo caudal de la vagina. El himen se
suele romper durante el período perinatal y permanece como un fino pliegue constituido
por una membrana mucosa localizado en el interior del orificio vaginal.
RESTOS VESTIGIALES DE LOS CONDUCTOS GENITALES EMBRIONARIOS
Durante la conversión de los conductos mesonéfricos y paramesonéfricos en las
estructuras del adulto, una parte de éstos permanece en forma de estructuras vestigiales.
RESTOS DEL CONDUCTO MESONÉFRICO EN LOS LACTANTES DE SEXO
MASCULINO
El extremo craneal del conducto mesonéfrico puede persistir en forma de un apéndice del
epidídimo. Caudalmente a los conductillos eferentes pueden persistir algunos túbulos
mesonéfricos en forma del paradídimo.
RESTOS EL CONDUCTO MESONÉFRICO EN LOS LACTANTES DE SEXO FEMENINO
El extremo craneal del conducto mesonéfrico puede persistir en forma de un apéndice vesicular,
que puede permanecer en el mesoovario, entre el ovario y la trompa uterina. Partes del conducto
mesonéfrico (correspondientes al conducto deferente y al conducto eyaculador, pueden persistir
en forma de quistes entre las capas del ligamento ancho o a lo largo de la pared lateral del útero o
la vaginal.
RESTOS DEL CONDUCTO PARAMESONÉFRICO EN L OS LACTANTES DE SEXO MASCULINO
El extremo craneal de este conducto puede persistir en forma de un apéndice testicular que permanece unido al testículo. El utrículo
prostático es una pequeña estructura que se origina a partir de este conducto y que se abre en la uretra prostática.
8 semanas
RESTOS DEL CONDUCTO PARAMESONÉFRICO EN L OS LACTANTES DE SEXO FEMENINO
Parte del extremo craneal del conducto paramesonéfrico que no contribuye al infundíbulo de la trompa uterina puede persistir en
forma de un apéndice vesicular, denominado hiátide.
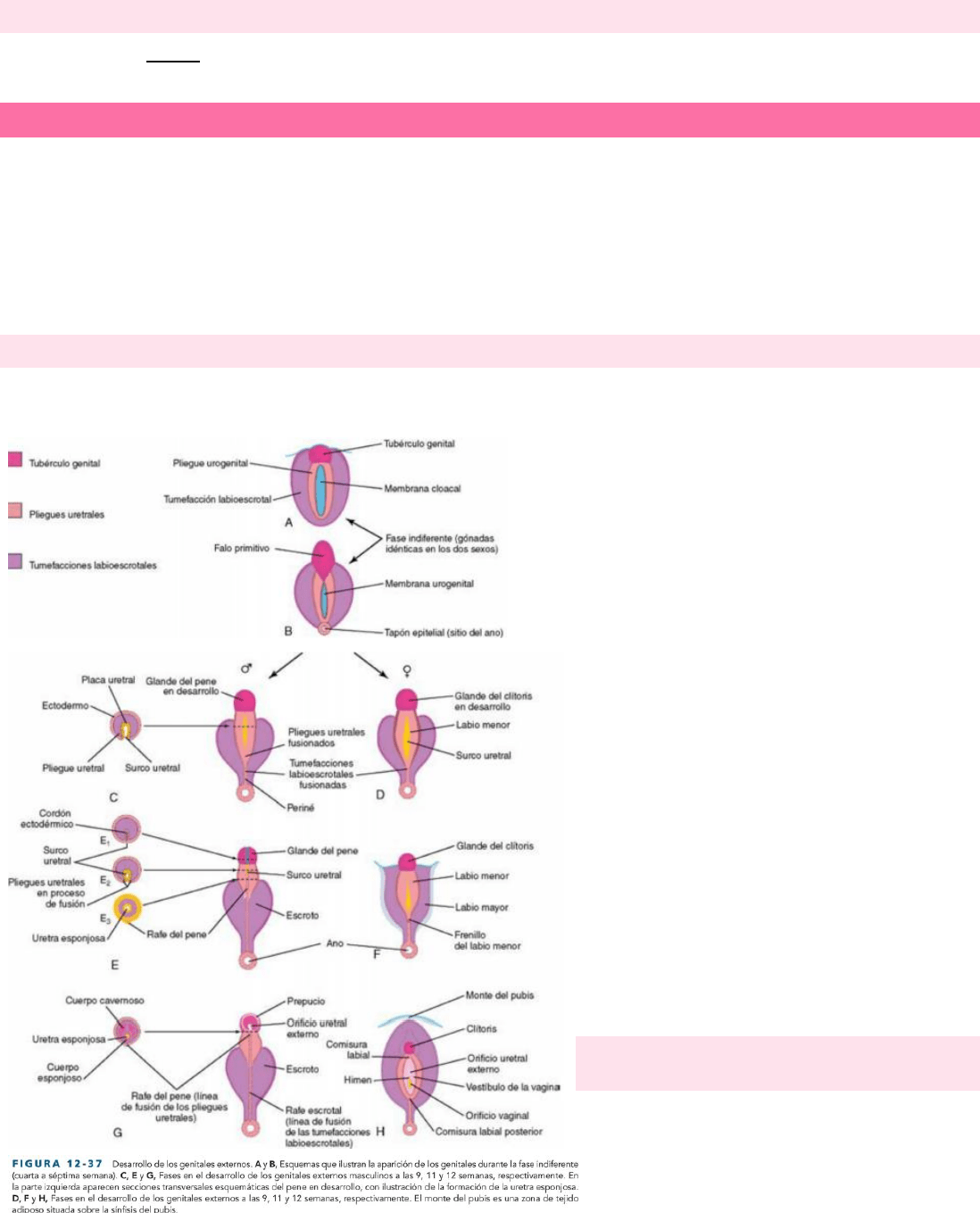
DESARROLLO DE LOS GENITALES EXTERNOS
Hasta la séptima semana los genitales externos son similares en ambos sexos. Los caracteres sexuales comienzan a distinguirse durante
la novena semana, pero no están completamente diferenciados hasta la semana 12.
Al inicio del cuarto mes, la proliferación del mesénquima produce un tubérculo genital (primordio del pene o del clítoris) en ambos
sexos, en el extremo craneal de la membrana cloacal. Al poco tiempo se desarrollan a cada lado de ésta membrana las tumefacciones
labioescrotales y los pliegues urogenitales. El tubérculo genital aumenta de longitud y forma el falo primitivo. La membrana
urogenital se localiza en el suelo del surco uretral (hendidura), limitada por los pliegues uretrales. En los fetos femeninos, la uretra y
la vagina se abren en una cavidad común denominada vestíbulo de la vagina.
DESARROLLO DE LOS GENITALES EXTERNOS MASCULINOS
La masculinización de los genitales externos indiferenciados está inducida por la testosterona que producen las células intersticiales
de los testículos fetales.
A medida que el falo aumenta en tamaño y longitud para
formar el pene, los pliegues uretrales constituyen las paredes
laterales del surco uretral en la superficie ventral del pene.
Este surco está revestido por células endodérmicas: la placa
uretral. Los pliegues uretrales se fusionan entre sí a lo largo de
la superficie ventral del pene, formando la uretra esponjosa.
El ectodermo de superficie se fusiona en el plano medio del
pene, formando el rafe del pene y así deja incluida la uretra
esponjosa en el interior del pene.
En el extremo del glande del pene una invaginación del
ectodermo forma un cordón celular que crece hacia la
raíz del pene hasta alcanzar la uretra esponjosa. Su luz
se une a la uretra esponjosa y de este modo se
completa la parte terminal de la uretra y el orificio
uretral externo se desplaza hasta el extremo del
glande.
Durante la 12ª semana aparece una invaginación
circular en el ectodermo de la periferia del glande, que
luego se desestructura y forma el prepucio, pliegue de
piel que desempeña una función de cobertura. Los
cuerpos cavernosos y el cuerpo esponjoso se
desarrollan a partir del mesénquima en el falo. Las
tumefacciones labioescrotales se aproximan entre sí y
se fusionan formando el escroto. La línea de fusión de
estos pliegues forma el rafe escrotal.
DESARROLLO DE LOS GE NITALES EXTERNOS
FEMENINOS
En el feto femenino, el falo primordial se convierte
gradualmente en el clítoris. Los pliegues uretrales no
se fusionan, excepto en su parte posterior, en la cual
se unen formando el frenillo de los labios menores.
Las partes no fusionadas de los pliegues urogenitales
forman los labios menores. Los pliegues
labioescrotales se fusionan en la parte posterior y generan la comisura labial posterior, y en la parte anterior, la comisura labial
anterior y el monte del pubis. Los pliegues labioescrotales en su mayoría no se fusionan, pero se convierten en dos grandes pliegues
cutáneos, los labios mayores.
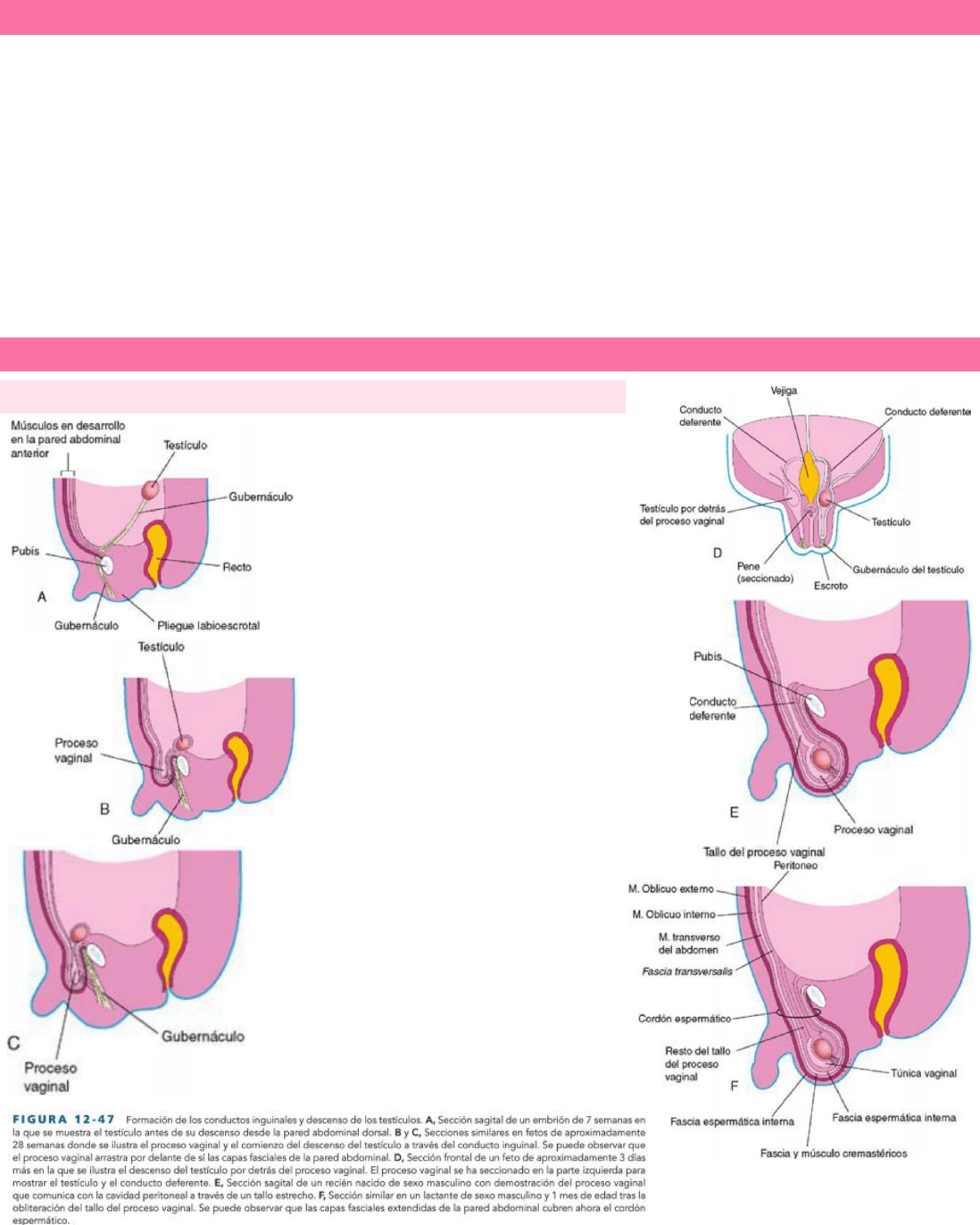
DESARROLLO DE LOS CONDUCTOS INGUINALES
Los conductos inguinales representan el trayecto que siguen los testículos en su descenso desde la pared abdominal dorsal a través
de la pared abdominal anterior y hasta el escroto. Estos conductos se desarrollan en ambos sexos debido a la existencia del período
indiferente del desarrollo sexual. A medida que degenera el mesonefros, a cada lado del abdomen se desarrolla un ligamento (el
gubernáculo) a partir del polo caudal de la gónada. El gubernáculo discurre a través de la pared abdominal anterior en desarrollo en
la zona del futuro conducto inguinal y acaba uniéndose caudalmente a la superficie interna de las tumefacciones labioescrotales
(futuras mitades del escroto o de los labios mayores).
El proceso vaginal (evaginación del peritoneo), se desarrolla por delante del gubernáculo y se hernia a través de la pared abdominal
y a lo largo del trayecto constituido por el gubernáculo. El proceso vaginal arrastra extensiones de las capas de la pared abdominal por
delante que forman las paredes del conducto inguinal. Estas capas también forman las cubiertas del cordón espermático y el testículo.
La abertura existente en la fascia transversalis y que se ha originado por el proceso vaginal se convierte en el anillo inguinal profundo,
mientras que la abertura creada en la aponeurosis oblicua externa forma el anillo inguinal superficial.
REUBICACIÓN DE LOS TESTÍCULOS Y LOS OVARIOS
DESCENSO TESTICULAR
Se asocia a:
Aumento de tamaño de los testículos y
atrofia del mesonefros, permitiendo el
movimiento caudal de los testículos a lo
largo de la pared abdominal posterior.
Atrofia de los conductos
paramesonéfricos inducida por la MIS,
permitiendo que los testículos se desplacen a
través del abdomen hasta los anillos inguinales
profundos.
Aumento de tamaño del proceso vaginal que
guía al testículo a través del conducto inguinal
hasta el escroto.
Hacia la semana 26 los testículos ya han
descendido hasta el retroperitoneo (por fuera del
peritoneo), desde la región lumbar superior hasta
la pared abdominal posterior y hasta los anillos
inguinales profundos. Esto sucede a medida que la
pelvis fetal aumenta de tamaño y se alargan el
cuerpo y tronco del embrión.
El descenso testicular a través de los conductos
inguinales está controlado por los andrógenos (x
ej. Testosterona) producidos por los testículos
fetales. El gubernáculo origina el anclaje del
testículo en el escroto y guía su descenso hacia
él. El paso del testículo a través del conducto
inguinal puede verse facilitado por el incremento
de la presión intraabdominal por el crecimiento
de los órganos abdominales.

El descenso testicular a través de los conductos inguinales y hasta el escroto suele iniciarse durante la semana 26 y dura entre 2 a 3
días. Normalmente para la semana 32 los testículos ya se ubican en el escroto. Tras esto, el conducto inguinal se contrae alrededor
del cordón espermático.
Cuando descienden, los testículos arrastran con ellos los conductos deferentes y los vasos testiculares. A medida que esto sucede,
quedan rodeados por extensiones fasciales de la pared abdominal: la fascia espermática interna, el músculo y la fascia cremastéricos
y la fascia espermática externa.
Dentro del escroto, el testículo se proyecta hacia el extremo distal del proceso vaginal. Durante el período perinatal, el tallo de
conexión del proceso vaginal suele “desecharse” y formar una membrana serosa, la túnica vaginal, que cubre las partes anterior y
laterales de los testículos.
DESCENSO OVÁRICO
Los ovarios también descienden desde la región lumbar de la pared abdominal posterior y se reubican en la pared lateral de la pelvis,
sin embargo, no pasan de la pelvis ni se introducen en los conductos inguinales. El gubernáculo está unido al útero cerca de la zona
de unión de la trompa uterina. La parte craneal del gubernáculo se convierte en el ligamento ovárico mientras que su parte caudal
forma el ligamento redondo del útero. Los ligamentos redondos pasan a través de los conductos inguinales y finalizan en los labios
mayores. El proceso vaginal, pequeño en el feto femenino, suele obliterarse y desaparece mucho antes del parto.

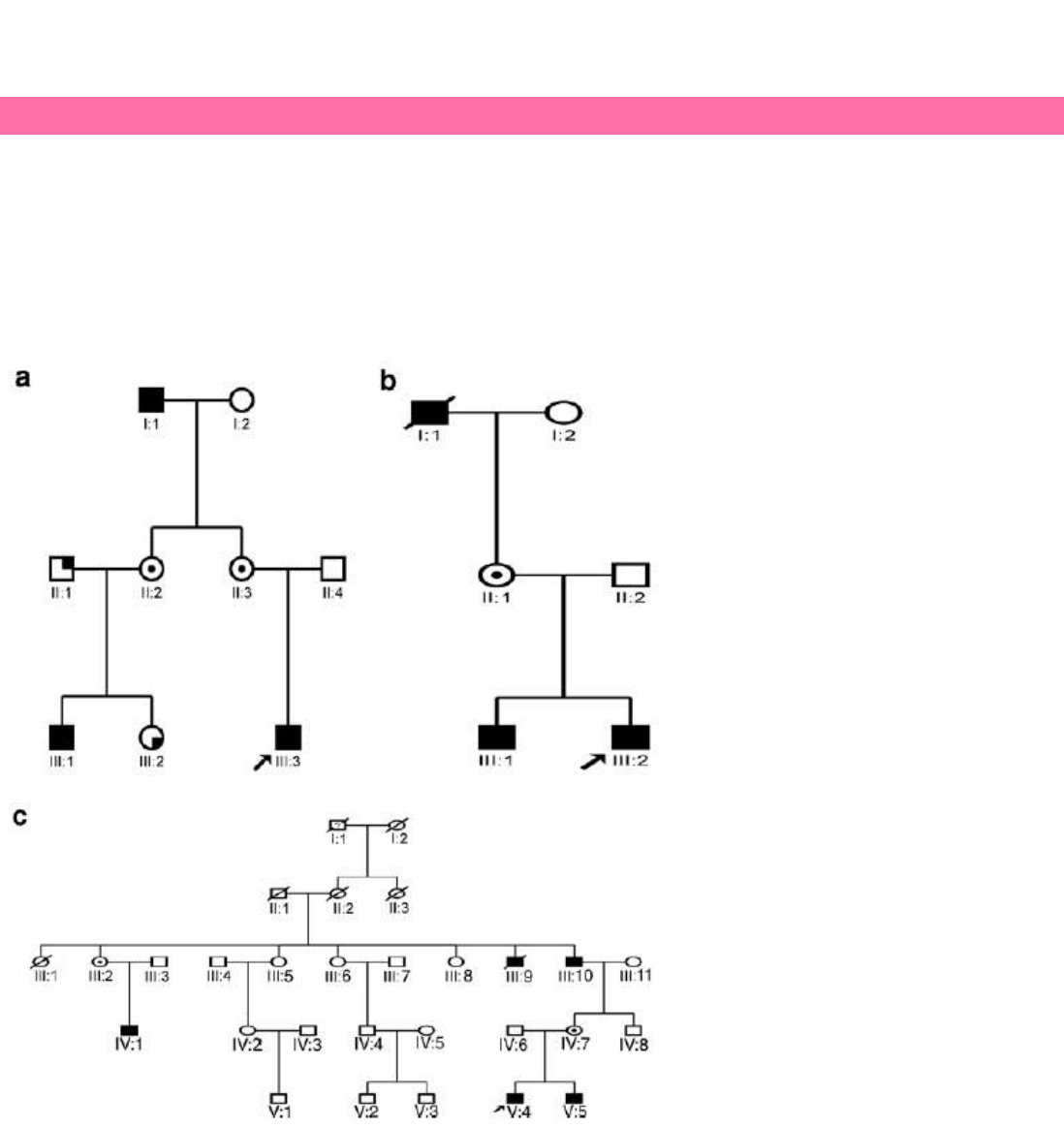
HERENCIA RECESIVA LIGADA AL CROMOSOMA X
El patrón de herencia recesiva ligada al cromosoma X se da cuando el alelo alterado es recesivo sobre el normal, por lo
que con una sola copia del alelo alterado no se expresa la enfermedad, y el gen se encuentra en el cromosoma X.
Normalmente se da con más frecuencia en hombres dado que tienen un solo cromosoma X, por lo que si heredan el alelo
mutado desarrollarán la enfermedad, sin embargo, las mujeres al tener dos cromosomas X si solo heredan un alelo mutado
serán portadoras, pero no desarrollaran la enfermedad, para esto tendrían que heredar dos alelos mutados.
Una mujer afectada por una enfermedad recesiva ligada al cromosoma X trasmitirá el alelo mutado a todos sus
descendientes, todas las hijas serán portadoras (pero no afectadas) y todos los hijos afectados por la enfermedad. Un
hombre afectado trasmitirá el alelo mutado a todas sus hijas que serán portadoras, pero a ninguno de sus hijos. Una mujer
portadora tiene una probabilidad del 50% con cada hijo o hija (independientemente de su sexo) de que este herede el alelo
mutado, si lo hereda un niño desarrollará la enfermedad y si lo hereda una niña será portadora de la enfermedad.
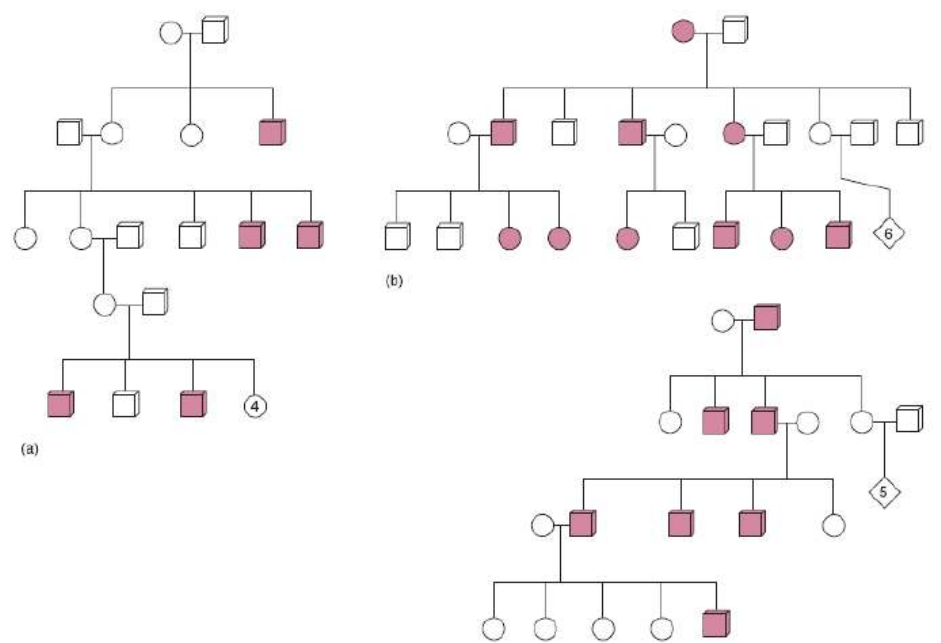
HERENCIA DOMINANTE LIGADA AL CROMOSOMA X
El patrón de herencia dominante ligada al cromosoma X se da cuando el alelo alterado es dominante sobre el normal, basta
una sola copia para que se exprese la enfermedad, y el gen se encuentra en el cromosoma X. Normalmente se da con más
frecuencia en mujeres dado que pueden heredar el alelo mutado tanto de un padre como de una madre afectada. Una mujer
afectada tiene una probabilidad del 50% con cada hijo o hija (independientemente de su sexo) de que este herede el alelo
mutado y desarrolle la enfermedad dominante ligada al cromosoma X, mientras que un hombre afectado trasmitirá el alelo
mutado y por tanto la enfermedad a todas sus hijas pero a ninguno de sus hijos.
COMPENSACIÓN DE DOSIS GÉNICA
En los organismos en donde las hembras y los machos difieren en el número de cromosomas sexuales (cromosomas X), se
ha desarrollado un proceso que elimina la diferencia en el número de dosis de los genes ligados a dicho cromosoma, de
forma tal que los productos de los genes ligados al sexo están representados en cantidades equivalentes en hembras y
machos. Este proceso recibe el nombre de compensación de dosis génica.
En los mamíferos, la compensación de dosis génica se consigue por inactivación al azar en el embrión de uno de los dos
cromosomas X de las hembras; mientras que en los tejidos extraembrionarios el cromosoma X que se inactiva es siempre el
que proviene del padre. Esto implica que el cromosoma X sufre un proceso de impronta genómica. Se ha identificado el
gen Xist como gen clave en el proceso de inactivación del cromosoma X. Este gen se encuentra localizado en el cromosoma
X y su expresión determina la inactivación del cromosoma que lo porta (efecto de inactivación en "cis"). El modelo actual
que explica la inactivación del cromosoma X es el siguiente. Existiría un factor de transcripción específico del gen Xist, el
cual estaría en cantidades limitantes, lo que determinaría que se inactivase un solo cromosoma X de las hembras. El gen
Xist del cromosoma X materno sufriría una impronta genómica durante la meiosis en la hembra. Esta impronta puede tomar
la forma de metilación. Cuando se produce la inactivación del cromosoma X en los tejidos extraembrionarios de la hembra,
el gen Xist materno no podría expresarse como consecuencia de su impronta, de modo que el factor de transcripción
actuaría sobre el gen Xist del cromosoma X paterno activándolo, lo que determinaría la inactivación selectiva de este
cromosoma. A medida que avanza el desarrollo, la impronta del gen Xist materno va desapareciendo, y en el momento de
la inactivación del cromosoma X en el embrión ambos genes Xist, el de procedencia materna y paterna, tienen la misma
posibilidad de ser activado por el factor de transcripción, pero dada la cantidad limitante de este, al final sólo uno de los
dos cromosomas X activaría su gen Xist. Aquel cromosoma que lo activase sería inactivado. El gen Xist no codifica una
proteína sino un ARN. El papel de este sería fijarse al cromosoma X y actuar como señal para la fijación de proteínas que
determinarían un cambio cromatínico que conduce a la inactivación génica. Posteriormente, la metilación del ADN del
cromosoma inactivado supone el mantenimiento de ese estado de inactivación.
HERENCIA HOLÁNDRICA
Es un término utilizado para definir el tipo de herencia en el cual los genes, encontrados en el cromosoma Y, son
directamente traspasados a los descendientes masculinos. Esto sucede puesto que el cromosoma Y solo puede provenir del
macho, ya que la hembra carece de éste, dentro de su genotipo. Un caso típico de la herencia holándrica es la enfermedad
hipertricosis auricular, la cual es heredada desde el padre hacia todos los varones de las generaciones posteriores.
DISGENESIA GONADAL
Es un trastorno del desarrollo embrionario que impide la maduración completa del tejido gonadal en su diferenciación hacia
testículo u ovario. En la disgenesia gonadal no hay ovocitos, y los ovarios aparecen como gónadas lineales. Los individuos
son fenotípicamente del sexo femenino, pero pueden tener una variedad de complementos cromosómicos, entre ellos XY.
La disgenesia gonadal femenina XY (síndrome de Swyer) se debe a mutaciones o deleciones puntuales del gen SRY. Los
individuos tienen aspecto de mujeres normales, pero no menstrúan y no desarrollan rasgos sexuales secundarios durante
la pubertad. Los pacientes con síndrome de Turner también sufren disgenesia gonadal. Tienen cariotipo 45, X y son de
estatura baja, presentan paladar arqueado y alto, cuello ancho y alado, tórax de tipo escudo, alteraciones cardiacas y renales,
y pezones invertidos.

desarrollo del sistema genital.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.