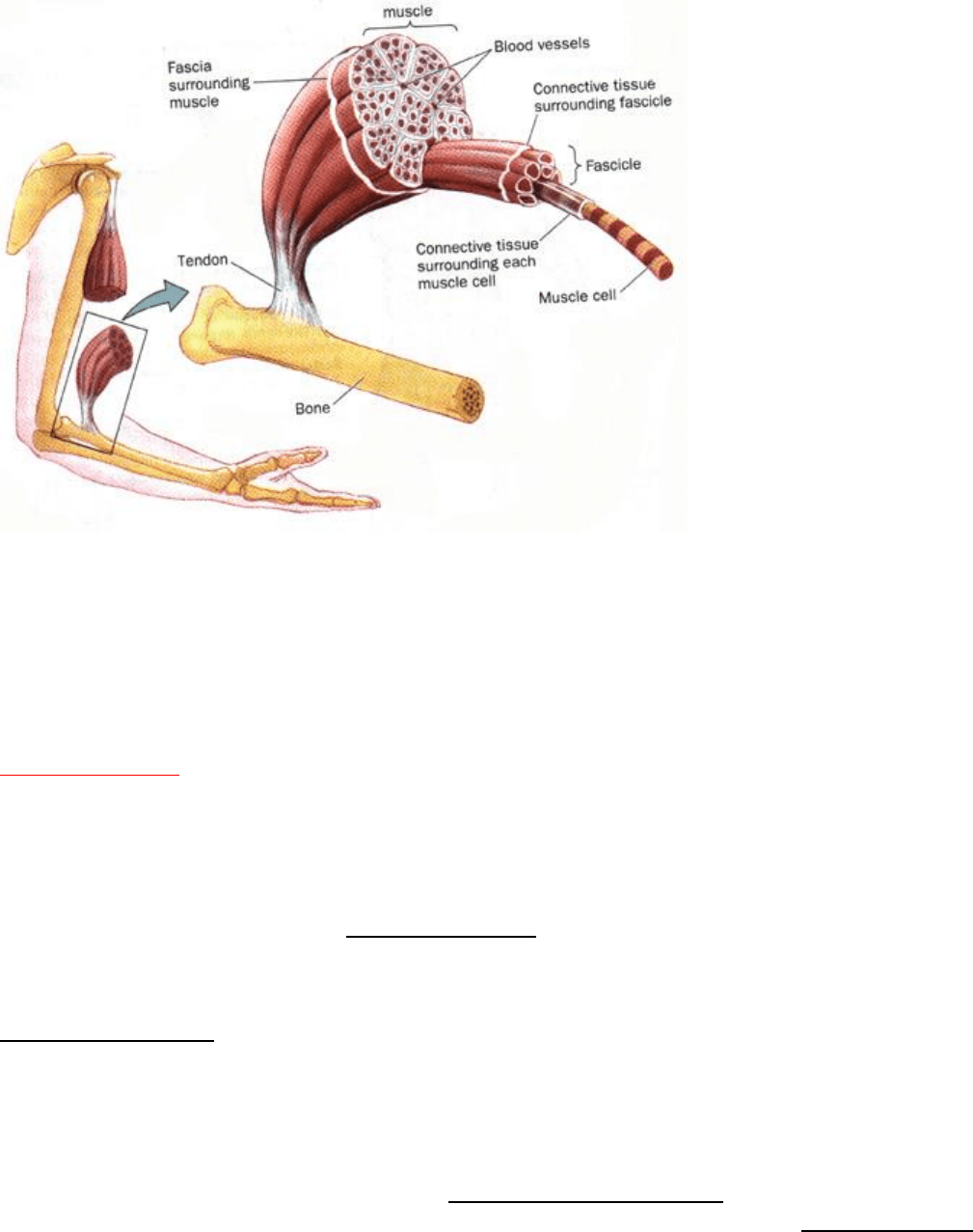
CONTRACCIÓN DEL MÚSCULO ESQUELÉTICO
El músculo esquelético es responsable del movimiento voluntario de los huesos que forman la base del
movimiento y de la producción de trabajo. También controla el ciclo respiratorio de los pulmones a
través de la contracción del diafragma y actúa como una bomba para facilitar el retorno de la sangre
venosa al corazón.
Fibra muscular → unidad
contráctil más pequeña del
músculo esquelético. Es una
alargada célula multinucleada.
Fascículo → haz de fibras
musculares.
Músculo → haces de fascículos
- Epimisio: vaina externa
que envuelve a la totalidad del
músculo.
- Perimisio: vaina que
envuelve a cada fascículo (o a
cada conjunto de fibras
musculares).
- Endomisio: vaina que
envuelve a cada fibra muscular
dentro de cada fascículo.
Por debajo del endomisio, y rodeando a cada fibra muscular, está la membrana plasmática de la célula
muscular denominada sarcolema. Una célula muscular aislada contiene una serie densa de elementos
cilíndricos dispuestos en paralelo llamados miofibrillas. Cada miofibrilla es una cadena termino
terminal de unidades que se repiten con regularidad, o sarcómeros, que constan de filamentos
interdigitalizados más pequeños llamados miofilamentos, los cuales contienen filamentos gruesos y
finos.
MOTONEURONAS: son las neuronas que controlan voluntariamente al músculo esquelético. Las
motoneuronas somáticas son neuronas eferentes cuyos cuerpos celulares están localizados en el SNC.
Una célula muscular aislada responde a una única motoneurona cuyo cuerpo celular, salvo en el caso
de los pares craneales, reside en el asta ventral de la médula espinal.
El grupo de fibras musculares inervadas por la totalidad de las ramificaciones colaterales de una sola
motoneurona recibe el nombre de UNIDAD MOTORA. Un músculo íntegro puede generar una amplia
gama de fuerzas y un rango de acortamiento escalonado variando el número de unidades motoras
excitadas dentro del músculo.
Tasa de inervación: es el número de fibras musculares inervadas por una sola motoneurona. Los
músculos con una tasa de inervación pequeña controlan los movimientos finos de gran precisión e
implican fuerzas pequeñas. Los músculos con una tasa de inervación grande controlan los movimientos
groseros que se requieren para el desarrollo de fuerzas notables.
Un axón de un nervio motor contacta con cada fibra muscular aproximadamente hacia la mitad de dicha
fibra para formar una sinapsis denominada UNIÓN NEUROMUSCULAR. La región especializada del
sarcolema en íntimo contacto con el terminal nervioso presináptico se denomina PLACA MOTORA.
La excitación fisiológica del músculo esquelético siempre supone una activación química mediante la
liberación de ACh desde el terminal nervioso motor. La unión de la ACh al receptor nicotínico da lugar
a un POTENCIAL DE PLACA MOTORA despolarizador escalonado. Un potencial de placa motora de la
magnitud suficiente, eleva el potencial de membrana hasta el umbral de disparo y activa a los canales
de Na+ voltajes dependientes en la vecindad de la placa motora, desencadenando un PA que se
propagará a lo largo de la membrana superficial.
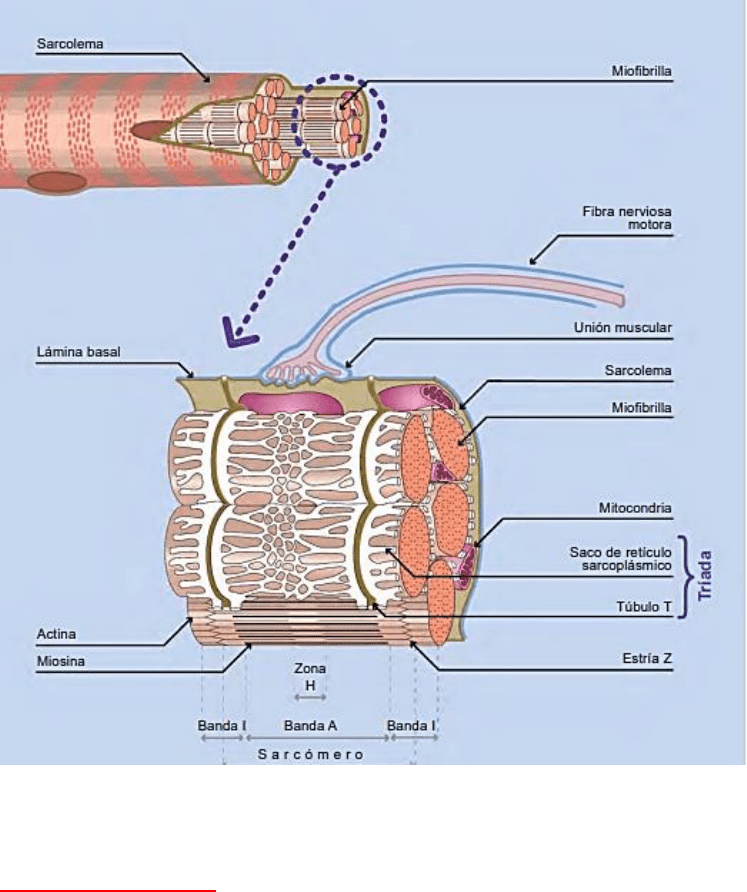
Cuando los PA van
propagándose a lo largo de
la membrana de las fibras
del músculo esquelético y
cardíaco, penetran en el
interior celular a través de
los TÚBULOS T. Los
túbulos T son
invaginaciones cilíndricas
de la membrana plasmática
orientadas radialmente, se
sumergen en la fibra
muscular y rodean a las
miofibrillas en dos puntos
en cada sarcómero: en las
uniones de las bandas A e I.
A lo largo de su longitud, el
túbulo se asocia a dos
cisternas terminales, que
son regiones
especializadas del RS. El
RS de las células
musculares es una versión
especializada de RE de las
células no contráctiles y
sirve como
almacenamiento intracelular para el Ca2+. La combinación de la membrana del túbulo T y sus dos
cisternas vecinas se denomina UNIÓN EN TRÍADA.
ACOPLAMIENTO EC
→
proceso mediante el cual la excitación eléctrica de la membrana superficial
desencadena una elevación de la [Ca2+] intracelular en el músculo.
➔ La propagación del PA en los túbulos T de la miofibrilla despolariza a la región de la tríada de los
túbulos T, activando de este modo a los canales de Ca2+ de tipo L. A estos canales también se
los llama receptor DHP, ya que son inhibidos por una clase de fármacos antihipertensivos y
antiarrítmicos conocidos como dihidropiridinas o antagonistas de los canales del calcio.
➔ La despolarización de la membrana del túbulo T produce cambios conformacionales en los
canales que abren el poro, lo que permite la entrada de Ca2+ mediante electrodifusión. A su
vez, los cambios conformacionales provocados por el voltaje, activan mecánicamente a cada
una de las subunidades acopladas directamente de otro canal, el canal de liberación de
Ca2+ localizado en la porción de la cisterna terminal de la membrana del RS que está frente al
túbulo T. Este canal también es conocido como receptor de rianodina (RYR1), ya que es
inhibido por el alcaloide vegetal rianodina.
➔ Las interacciones mecánicas entre estos dos canales de Ca2+ diferentes son importantes en el
acoplamiento EC en el músculo esquelético. Pueden producirse muchos ciclos de excitación y
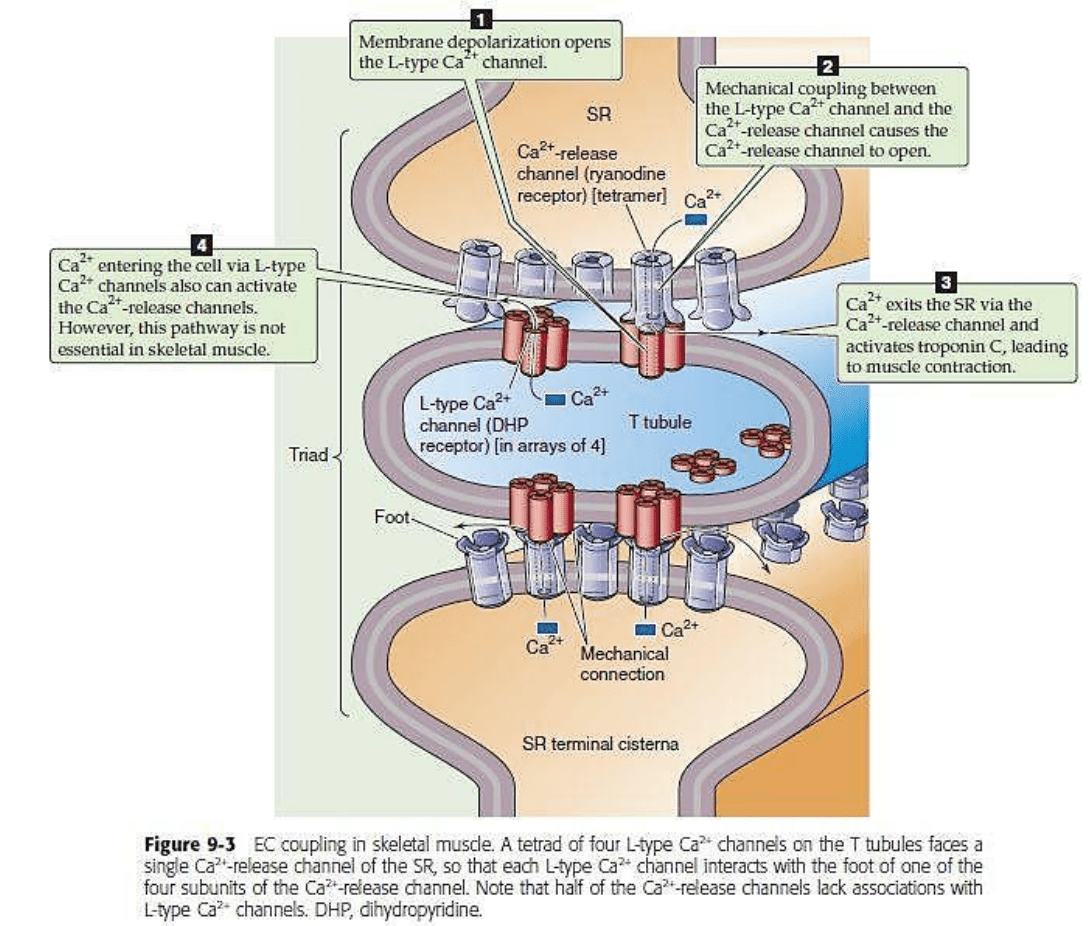
contracción en ausencia completa de Ca2+ extracelular. Además, los canales de Ca2+ de tipo L
en un estado cerrado, inhiben físicamente la apertura de los canales RYR1 e impiden por tanto
la liberación espontánea de Ca2+ del RS en el estado de reposo o no activado. Así pues, el
acoplamiento EC en el músculo esquelético es un proceso electromecánico que supone un
mecanismo de liberación de Ca2+ inducido por el voltaje.
➔ Después de la despolarización del canal de Ca2+ de tipo L y de la activación mecánica del canal
de liberación del Ca2+, el Ca2+ almacenado en el RS sale rápidamente a través del canal de
liberación de Ca2+. El aumento rápido y transitorio de la [Ca2+] intracelular local a partir de
grupos de canales RYR aparece como un chispazo o centello. Este incremento de la [Ca2+]
intracelular activa a la troponina C, iniciando la formación de puentes cruzados entre los
miofilamentos.
Hay otros mecanismos que modulan la actividad del RYR1. Por ejemplo, el RYR1 está sujeto a regulación
por el Ca2+, el Mg2+, el ATP y la calmodulina (CaM) del plasma, así como por quinasas como la PKA y la
quinasa dependiente de Ca2+-calmodulina II (CaMKII). En respuesta de lucha o huida, el SNA simpático
activa a receptores adrenérgicos β provocando la fosforilación del RYR1 y otras proteínas musculares
por la PKA; esto da lugar a incrementos mayores y más rápidos en el Ca2+ citoplasmático, y por tanto a
una contracción muscular más fuerte.
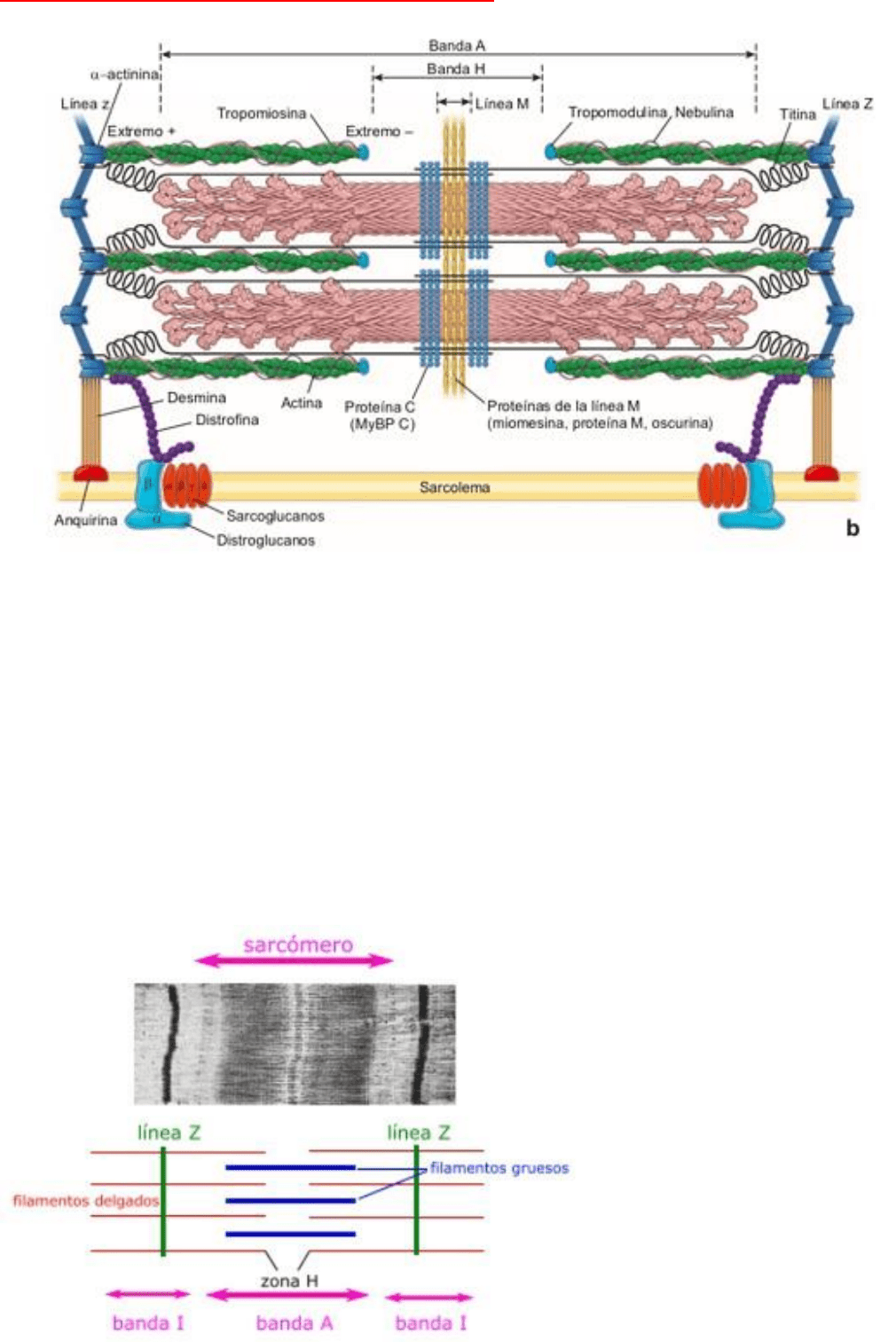
ESTRUCTURA MOLECULAR DEL MÚSCULO ESTRIADO
Miofilamentos → 2 tipos:
- Filamentos gruesos compuestos fundamentalmente de una proteína llamada MIOSINA.
- Filamentos finos compuestos principalmente de una proteína llamada ACTINA.
Sarcómero → unidad repetitiva entre dos discos Z.
Una miofibrilla es una serie lineal de sarcómeros apilados extremo contra extremo. Los sarcómeros
son responsables del aspecto a rayas o estriado de las fibras musculares de estos tejidos. Tanto el
músculo esquelético como el músculo cardíaco son músculos estriados. Por el contrario, el músculo liso
carece de estriaciones, ya que la actina y la miosina muestran un patrón menos regular de organización
en estos miocitos.
El extremo positivo de los filamentos finos se une a las caras opuestas de un disco Z. Entrecruzando
los filamentos finos en el disco Z están las proteínas de α-actinina. Dos proteínas grandes, la titina y la
nebulina, también están unidas
a los discos Z, al igual que otras
proteínas que al parecer están
implicadas en la detección del
estiramiento y en la
comunicación de señales al
núcleo.
Los filamentos gruesos,
compuestos de miosina, se
colocan entre los filamentos
finos y se interdigitan
parcialmente con ellos, lo que da
lugar a una alternancia de
bandas claras y oscuras a lo
largo del eje de la miofibrilla.
Bandas claras o bandas I→ representan regiones del filamento fino que no se solapan con los filamentos
gruesos. Son isotrópicas a la luz polarizada. El disco Z se aprecia como una línea oscura perpendicular
en el centro de la banda I.
Bandas oscuras o bandas A → representan a los filamentos de miosina. Son anisotrópicas a la luz
polarizada.
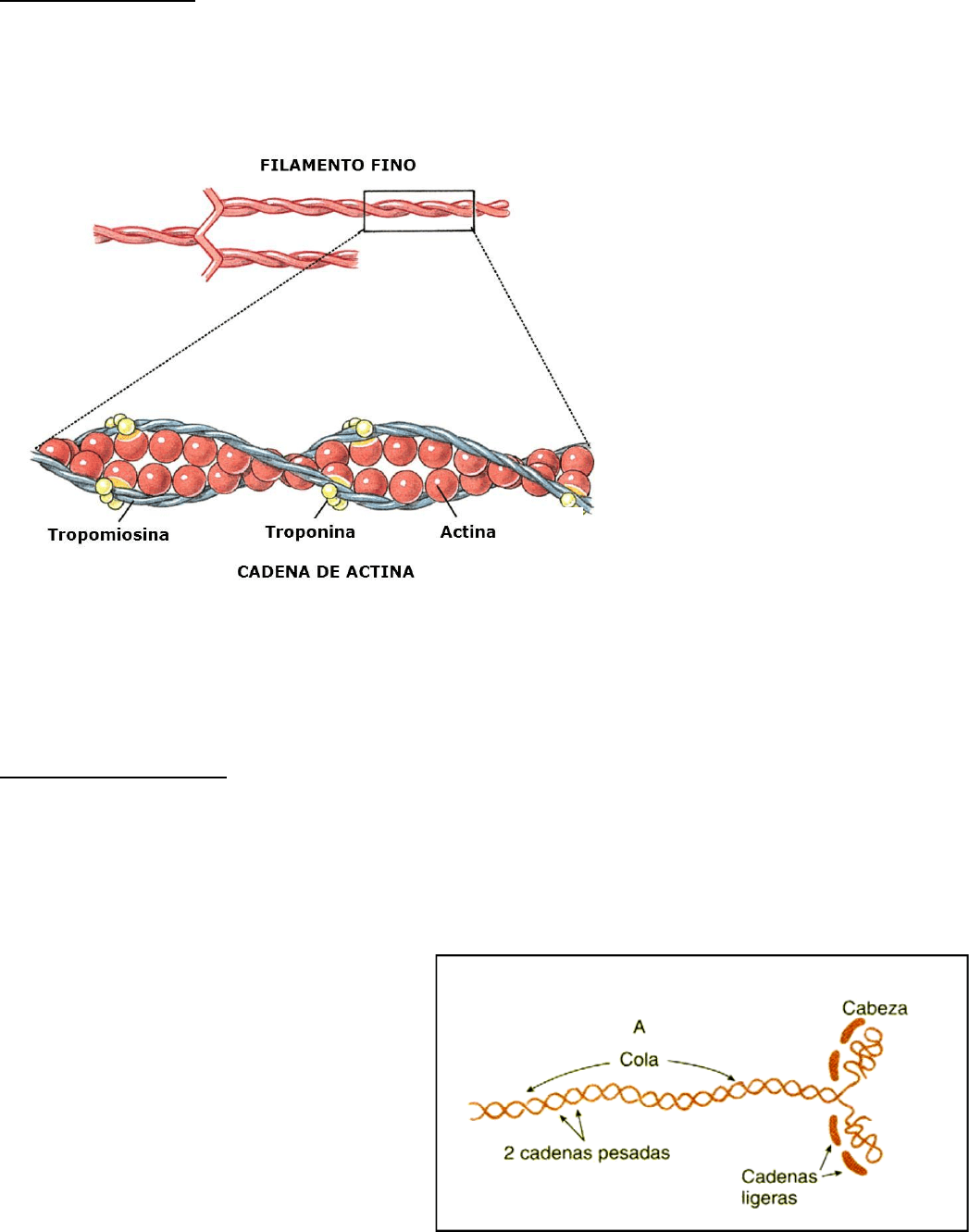
FILAMENTOS FINOS
El esqueleto es una hélice de doble hebra de moléculas de actina polimerizadas no covalentemente, que
forman la actina filamentosa o actina F. El filamento fino muscular resulta de la asociación de la actina
F y dos proteínas de unión a actina reguladoras importantes: la tropomiosina y el complejo de la
troponina.
Dos monómeros de
tropomiosina forman un dímero
alineado en paralelo y enrollado
entre sí creando una estructura
de bobina enrollada. Dos de estos
dímeros de tropomiosina
flanquean a cada hélice
supramolecular de actina. La
tropomiosina actúa como una
barrera en la regulación de la
unión de las cabezas de la
miosina a la actina.
La troponina es un
heterodímero que consta de:
- Troponina T (TnT): se
une a una molécula de
tropomiosina.
- Troponina C (TnC): se une al Ca2+. Está íntimamente relacionada con otra proteína de unión al
Ca2+, la calmodulina.
- Troponina I (TnI): se une a la actina e inhibe la contracción.
FILAMENTOS GRUESOS
En el músculo esquelético de contracción rápida, el filamento grueso es una supraestructura bipolar de
varios cientos de moléculas de miosina II que forman parte de una familia más amplia de miosinas. La
miosina II es responsable de la generación de fuerza dependiente de ATP en todos los tipos de miocitos.
La molécula de miosina II es una pareja de heterotrímeros idénticos, cada uno compuesto de una
CADENA PESADA DE MIOSINA (MHC) y DOS CADENAS LIGERAS DE MIOSINA (MLC). Una de las MLC
es una cadena ligera esencial (ELC) y la
otra es una cadena ligera reguladora
(RLC).
En las regiones de los cuellos, las dos MHC se
separan dando lugar a dos cabezas
globulares. Cada cabeza de la MHC tiene en
su extremo varios bucles que se unen a la
actina, y en su zona intermedia una región de
unión a nucleótidos para la unión y la
hidrólisis del ATP.

La cadena ligera esencial y la cadena ligera reguladora, ambas relacionadas estructuralmente con la
superfamilia CaM, se unen a la región helicoidal del cuello y la estabilizan mecánicamente. La
fosforilación de la RLC por quinasas de la cadena ligera de la miosina (MLCK), miembros de la familia
CaMK, favorecen las interacciones de los puentes cruzados de miosina. Las fosfatasas ejercen el efecto
contrario. En el músculo esquelético esta fosforilación constituye un mecanismo importante para la
potenciación de la fuerza.
CICLO DE ENTRECRUZAMIENTO – FORMACIÓN DE PUENTES CRUZADOS
Empezamos el ciclo en ausencia de ATP y ADP, con la porción cefálica de la miosina unida rígidamente
a un filamento de actina.
Paso 1: UNIÓN DEL ATP. La unión del ATP a la porción cefálica de la MHC reduce la afinidad de la
miosina por la actina, lo que hace que la cabeza de la miosina se libere del filamento de actina.
Paso 2: HIDRÓLISIS DEL ATP. La degradación del ATP a ADP y Pi ocurre en la cabeza de la miosina;
los productos de la hidrólisis son retenidos en el interior de la zona activa de la miosina. Como resultado,
la cabeza de la miosina gira en una posición erguida en la que la cabeza se alinea más con el vástago.
Este giro provoca que la punta de la miosina se mueva a lo largo del filamento de actina, de modo que
se alinea con un nuevo monómero de actina, dos monómeros más allá en el filamento de actina.
Paso 3: FORMACIÓN DE ENTRECRUZAMIENTOS DÉBILES. La miosina erguida se une entonces
débilmente a una nueva posición en el filamento de actina, buscando una zona de unión idónea.
Paso 4: LIBERACIÓN DE Pi DE LA MIOSINA. La disociación del Pi de la cabeza de la miosina provoca
un aumento de la afinidad del complejo miosina-ADP por la actina, dando lugar al estado de
entrecruzamiento fuerte. La transición de una unión débil a una fuerte constituye el paso limitante del
ciclo de entrecruzamiento.
Paso 5: GOLPE DE FUERZA. Un cambio conformacional provoca que el cuello de la miosina rote
alrededor de su cabeza, la cual permanece fuertemente fijada a la actina. Este giro tracciona del vástago
de la miosina, tirando de los filamentos de actina y miosina y deslizando uno sobre el otro. Esta actividad
tracciona de las líneas Z y las aproxima, acortando el sarcómero y generando fuerza.
Paso 6: LIBERACIÓN DE ADP. La disociación del ADP de la miosina completa el ciclo y el complejo
queda en un estado acoplado rígido. Las posiciones no varían hasta que se une otra molécula de ATP y
vuelve a iniciarse otro ciclo.
El complejo de miosina libre de ADP debería unirse rápidamente al ATP a las concentraciones en las
que normalmente está el ATP en el interior de las células. Cada ronda de ciclo de entrecruzamiento
consume una molécula de ATP.
AUMENTO EN LA [Ca2+] INTRACELULAR
El Ca2+ ejerce su efecto uniéndose a proteínas reguladoras en lugar de interaccionar directamente con
las proteínas contráctiles. En ausencia de Ca2+, estas proteínas reguladoras actúan coordinadamente
para inhibir las interacciones de la actina y la miosina, inhibiendo de este modo el proceso contráctil.
Cuando el Ca2+ se una a una o más de estas proteínas se produce un cambio conformacional en el
complejo regulador que libera la inhibición de la contracción. Las proteínas reguladoras forman el
COMPLEJO DE LA TROPONINA, que está compuesto de troponina C, troponina I y troponina T. La
troponina T se une a la tropomiosina, estableciendo el nexo entre el complejo de la troponina y la
tropomiosina.
El Ca2+ debe eliminarse del sarcoplasma para que la contracción cese y el músculo se relaje → ocurre
mediante dos mecanismos: el Ca2+ puede expulsarse a través de la membrana plasmática celular
o bien secuestrarse en el interior de los compartimentos intracelulares.

La célula puede expulsar Ca2+ mediante un NCX o INTERCAMBIADOR DE NA-CA, o un PMCA (ATPasa
o bomba de Ca de la membrana plasmática). Pero la expulsión a través de la membrana acabaría por
consumir completamente el Ca2+ de la célula y por tanto es un mecanismo menor para su eliminación
desde el citoplasma. En lugar de esto, la recaptación de Ca2+ hacia el RS es el mecanismo más
importante mediante el cual la célula regresa a los valores de [Ca2+] intracelular de reposo. Esta
mediado por un SERCA (ATPasa o bomba de Ca sarcoplasmática o del RE).
Una [Ca2+] alta dentro de la luz del RS, INHIBE la actividad de SERCA, un efecto que se ve atenuado por
la presencia de proteínas de unión al Ca2+ en la luz del RS. Estas proteínas de unión amortiguan el
incremento de la [Ca2+] en el RS durante la recaptación y de este modo aumenta notablemente la
capacidad de almacenamiento del RS. La principal proteína de unión al Ca2+ en el músculo esquelético
es la CALSECUESTRINA (CSQ).
CONTRACCIONES ISOMÉTRICAS Y CONTRACCIONES ISOTÓNICAS
Fuerza total generada por un músculo → suma de las fuerzas generadas por numerosos
entrecruzamientos de actina y miosina que ciclan independientemente. Este número de
entrecruzamientos depende en gran medida de la longitud inicial de la fibra muscular y de la frecuencia
de estimulación de la célula muscular. Esta fuerza determina la tensión desarrollada por el músculo.
Contracciones isométricas: se producen cuando la estimulación de la fibra provoca un aumento de la
tensión, pero no acortamiento. Como estas contracciones se producen a una longitud constante se
denominan isométricas.
Contracciones isotónicas: se producen cuando la estimulación de la fibra provoca acortamiento,
siempre que la tensión desarrollada por el músculo sea mayor que la carga de oposición. Como dichos
acortamientos tienen lugar a una carga constante se denominan isotónicos.
Un músculo no estimulado puede elongarse hasta cierta medida aplicándola tensión y estirándolo. La
tensión medida antes de la contracción muscular se denomina TENSIÓN PASIVA. Como la rigidez del
músculo aumenta a medida que se distiende, se necesitan cantidades crecientes de tensión pasiva para
elongar a la célula muscular. A cualquier longitud fija (en condiciones isométricas), cuando se estimula
el músculo para que se contraiga, se desarrolla una TENSIÓN ACTIVA adicional debido al ciclo de
entrecruzamientos. La TENSIÓN TOTAL es la suma de la tensión pasiva y la tensión activa. La tensión
activa es máxima a una LONGITUD ÓPTIMA, que está cercana a la longitud muscular normal.
Esta relación entre longitud y tensión es el resultado directo de la anatomía de los filamentos gruesos y
finos en los sarcómeros individuales.
➔ Cuando el músculo aumenta su longitud, los extremos de los filamentos se actina se alejan de los
discos Z opuestos. Cuando la longitud supera el 150% de la longitud del sarcómero en reposo,
los extremos de los filamentos de actina están más allá de los extremos de los filamentos de
miosina. En dichas condiciones no se produce ninguna interacción entre los filamentos de actina
y los de miosina y por tanto no se desarrolla tensión activa.
➔ A medida que se acorta la longitud del músculo desde este punto, los filamentos de actina y
miosina comienzan a solaparse y puede desarrollarse tensión.
El grado máximo de solapamiento entre los filamentos de actina y de miosina, y por tanto de la tensión
activa máxima, se corresponde con una longitud del sarcómero cercana a la longitud normal en reposo.
SUMACIÓN TEMPORAL O DE FRECUENCIA
Las contracciones musculares esqueléticas aisladas duran entre 25 y 200 ms. Si bien cada contracción
es desencadenada por un solo potencial de acción, su duración es larga comparada con la del PA
excitador, que dura solamente unos milisegundos. Como la duración de la contracción muscular excede

con mucho a la duración del PA, es posible iniciar un segundo PA antes de que haya cedido por completo
la primera contracción. Cuando ocurre esta situación, el segundo PA estimula una contracción que se
superpone sobre la tensión residual de la primera y por tanto alcanza una tensión isométrica mayor
que la primera → EFECTO DE SUMACIÓN.
Entonces, la tensión es mayor cuando los PA se suceden a frecuencias más altas.
Cuando se aumenta lo suficiente la frecuencia de la estimulación, cada contracción individual aparece
tan próxima en el tiempo con la siguiente que se fusionan, de modo que la tensión muscular se mantiene
en una meseta estable. El estado en el que las contracciones individuales dejan de distinguirse entre sí
se conoce como TETANIA. La tetania surge cuando el tiempo entre PA sucesivos es insuficiente para
lograr que regrese suficiente cantidad de Ca2+ al RS con el fin de disminuir la [Ca2+] intracelular por
debajo del valor al que se inicia la relajación. De hecho, persiste un incremento sostenido de la [Ca2+]
hasta que cesa el estímulo tetánico. La tensión de la fibra aumenta muy poco a frecuencias de
estimulación por encima de la frecuencia de fusión que causa la tetania.
SUMACIÓN ESPACIAL
También puede controlarse la fuerza muscular fijando el número de fibras musculares individuales a
las que se estimula en un momento concreto. Cuando se excita una motoneurona adicional, las fibras
musculares que forman parte de su unidad motora se añaden al conjunto de fibras que se contraen,
efecto llamado SUMACIÓN ESPACIAL.
En general, las motoneuronas más pequeñas actúan sobre unidades motoras con menos fibras
musculares individuales. Como un estímulo excitador concreto generará un potencial postsináptico
excitador más grande en las motoneuronas con cuerpos celulares más pequeños, las unidades motoras
pequeñas son reclutadas incluso con una estimulación neuronal mínima. A medida que se intensifica la
estimulación neuronal, también van reclutándose motoneuronas más grandes que inervan a unidades
motoras de mayor tamaño → PRINCIPIO DEL TAMAÑO (reclutamiento progresivo de unidades
motoras, primero pequeñas y luego más grandes).

CONTRACCIÓN MÚSCULO ESQUELÉTICO.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.