
1
CONFIGURACIÓN ELECTRÓNICA
La Configuración o Distribución electrónica nos dice como están ordenados los electrones en los
distintos niveles de energía (órbitas), o lo que es lo mismo como están distribuidos los electrones
alrededor del núcleo de su átomo.
¿Para qué queremos saber esto? Es imprescindible para realizar los enlaces y conocer los llamados
electrones de valencia, que son el número de electrones que tiene el átomo de un elemento en su
última capa u orbita.
Lo primero que debes saber es que cuanto más alejado del núcleo esté girando el electrón mayor es
su nivel de energía. Los electrones de un átomo, que tengan la misma energía se dice que están en el
mismo nivel de energía. Estos niveles de energía también se llaman orbitales de energía.
Orbitales de Energía
En la actualidad, la periferia del núcleo se divide en 7 niveles de energía diferente, numerados del 1
al 7 y en los que están distribuidos los electrones.
Además, cada nivel se divide en subniveles. Estos subniveles pueden llegar a ser hasta 4: s, p, d, f.
En resumen: niveles de energía hay del 1 al 7 y subniveles hay 4 el s, p, d, f
Ojo, hay átomos que no tienen los 4 subniveles, como veremos más adelante y átomos que no tiene
los 7 niveles de energía, pueden tener menos. Esto es precisamente lo que queremos averiguar,
cuantos niveles y subniveles de energía tiene un átomo concreto y cuantos electrones tiene en
cada uno de estos subniveles y niveles, es decir su Configuración Electrónica.
Además, en cada subnivel solo podemos tener un número máximo de electrones.
SUBNIVEL
CANTIDAD MAXIMA DE e
-
s
2
p
6
d
10
F
14
En cada nivel hay 4 más que en el nivel anterior
Fíjate en la imagen que en el nivel 1 (no se
aprecia el círculo en la imagen, pero está ahí)
solo se permiten 2 electrones y además solo
tiene un subnivel, el s. No hay ningún átomo que
tenga más de 2 electrones girando en el primer
nivel de energía (puede tener 1 o 2 electrones).
Si ahora pasamos al nivel 2, vemos que tiene 2
subniveles, lógicamente el s y el p.
En el nivel s solo habrá como máximo 2
electrones y en el p como máximo 6.
Si seguimos viendo la imagen nos daremos
cuenta de lo siguiente.
Si hay un subnivel siempre será el s, si hay 2
serán el s y el p, si hay 3 serán el s, el p y el d, y
si hay 4 subniveles serán el s, el p, el d y el f.
2
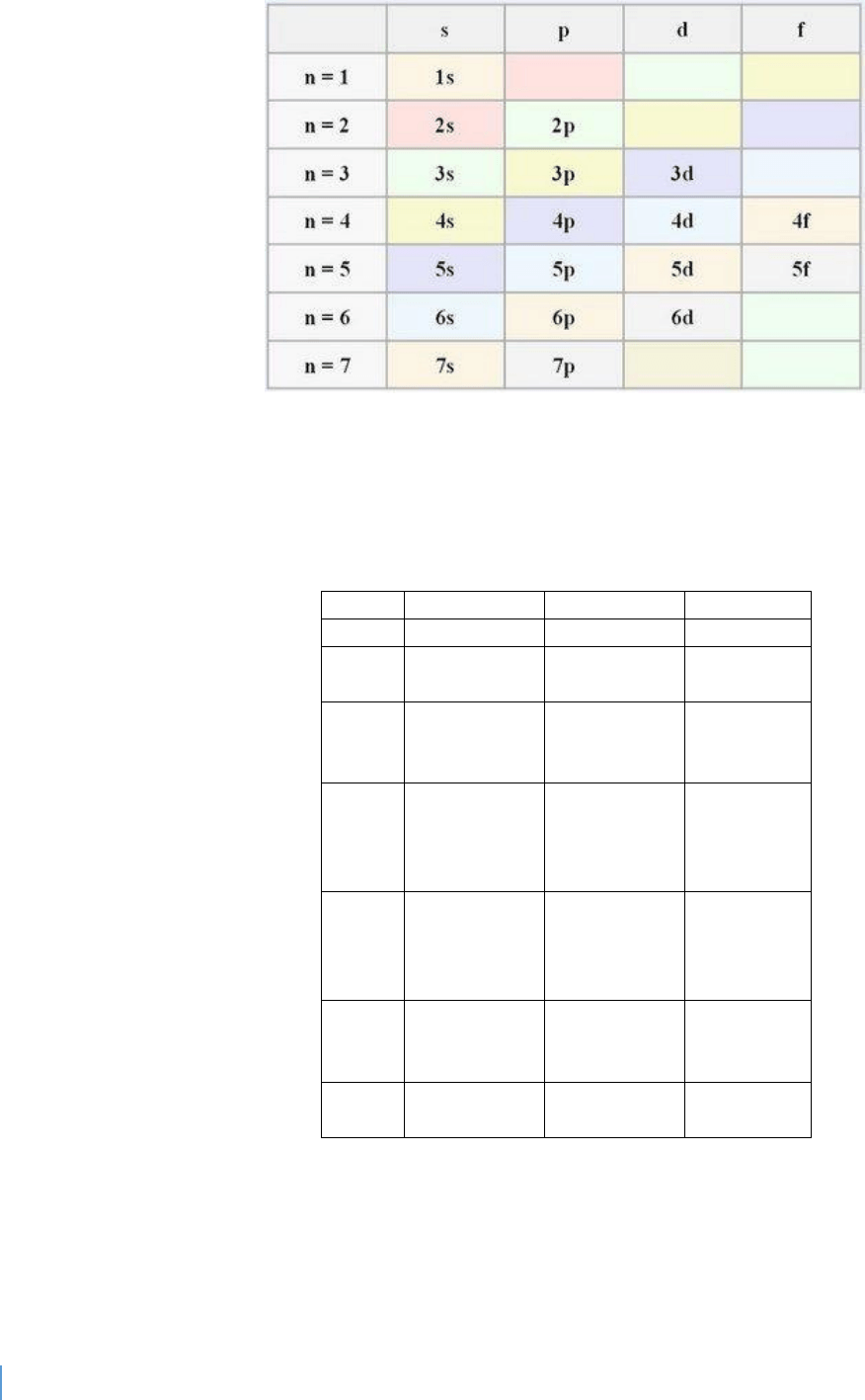
Antes de llegar a un nivel superior tendremos que rellenar los niveles más bajo de energía de
electrones.
Para llegar al nivel 2p, primero tenemos que llenar de electrones el 1s (con 2 electrones), el 2s (con
otros 2) y luego ya llenaríamos el 2p con un máximo de hasta 6, como ya sabemos.
Según esta tabla podríamos saber….
Nivel
Orbitales
Max e
-
TOTAL
1
s
2
2
2
s
p
2
6
8
3
s
p
d
2
6
10
18
4
s
p
d
f
2
6
10
14
32
5
s
p
d
f
2
6
10
14
32
6
s
p
d
2
6
10
18
7
s
p
2
6
8
Bien pues ahora si supiéramos cuantos electrones tiene un elemento concreto de la tabla periódica, ya
podríamos saber cómo se distribuyen esos electrones alrededor de su núcleo.
El número de electrones que tiene el átomo de cada una de los elementos diferentes que conocemos
viene en la tabla periódica de los elementos, es su número atómico o Z.
Veamos algunos ejemplos. Imaginemos el Helio. Sabemos que tiene 2 electrones.
¿Cómo estarán distribuidos? Sencillo. El primer nivel permite 2 electrones, pues ahí estarán.

3
Además, el primer nivel solo permite un subnivel, el s, y en este subnivel puede tener un máximo de 2
electrones.
Conclusión estarán girando alrededor del nivel 1 y sus dos electrones estarán en el subnivel s, del nivel
de energía 1.
Cuando queremos hacer la configuración electrónica de un elemento concreto, por ejemplo, la del Helio
del caso anterior, tendremos que tener una forma de expresarlo y que todo el mundo utilice la misma
forma.
Veamos de qué forma se hace.
Si te fijas en la imagen, se pone un número que nos dice de qué nivel de energía estamos hablando,
detrás y en minúscula, la letra del subnivel de ese nivel del que estamos hablando, y un exponente
sobre la letra del subnivel que nos dice el número de electrones que hay en ese subnivel.
En este caso como es el subnivel s nunca podría tener un exponente mayor de 2, ya que son los
máximos electrones que puede tener este subnivel.
¡¡¡Ya tenemos la configuración electrónica del Helio!!!.
La más fácil será la del Hidrógeno, que tiene un electrón.
Será 1s
1
. ¿Fácil NO?
¿Y si tiene 3 electrones? Por ejemplo, el caso del Litio (Li).
Tendrá 2 electrones en el primer nivel (son los máximos), y uno en el segundo.
¿Cómo lo expresamos? 1s
2
2s
1
En el nivel de energía 1 y subnivel s = 2 electrones, ya estaría llena por lo que pasamos al nivel 2.
En este nivel estará el electrón que nos falta por acomodar.
Lo acomodamos en el primer subnivel del nivel 2.
El primer subnivel de un nivel es siempre el s, el segundo el p, el tercero el d y el cuarto el f.
Luego 2s
1
significa nivel 2 subnivel s con un electrón.
Ya tenemos los 3 electrones del Litio en su sitio y expresada correctamente su configuración
electrónica.
Si tuviéramos más electrones iríamos poniendo el cuarto en el nivel 2 y en el subnivel s (que ya sabemos
que entran 2), pero si tuviéramos 5 tendríamos que poner el quinto en el nivel 2 pero en la capa p.
Así sucesivamente.
Pero para esto es mejor utilizar un esquema muy sencillo, ya que algunas veces, antes del llenar algún
subnivel posible de un nivel, se llena un subnivel de otro nivel superior.
El orden en el que se van llenando los niveles de energía es: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p.
OJO Fíjate que antes de llenarse el nivel 3 por completo, se empieza a llenar el nivel 4 (pasa del 3s, 3p
al 4s y no al 3d).

4
Pero tranquilo para esto hay un esquema muy sencillo Regla de la Diagonal
El esquema de llenado de los orbitales atómicos, lo
podemos tener utilizando la regla de la diagonal.
Deberás seguir atentamente la flecha del esquema
comenzando en 1s; siguiendo la flecha podrás ir
completando los orbitales con los electrones en forma
correcta.
Es importante recordar que los orbitales se van llenando
en el orden en que aparecen, siguiendo esas diagonales,
empezando siempre por el 1s.
Con esta simple regla, sabiéndose la imagen anterior es
muy fácil sacar la configuración electrónica de cualquier
elemento.
Veamos cómo se hace definitivamente.
Si hacemos la configuración electrónica de un átomo de un elemento con 10 electrones (Neón)
siguiendo la regla de la diagonal su configuración quedaría así: 1s
2
2s
2
2p
6
¿Y si tuviera 9 electrones?
Pues muy sencillo igual, pero al llegar al nivel 2p solo pondríamos 5 electrones en ese nivel, 2p
5
y
quedaría 1s
2
2s
2
2p
5
. el nivel 2p no se llena por completo. ¿Fácil no?
¿Cuantos electrones tiene un átomo en su última capa? Pues en el caso del Neón en su última capa
tendrá 6 electrones y el en el caso del Flúor, en su última capa tendrá 5.
Veamos algunos ejemplos más:
Configuración electrónica del Nitrógeno: Lo primero miramos en la tabla periódica y tiene un número
atómico = 7. Con esto sacamos su configuración: Nitrógeno: 1s
2
2s
2
2p
3
Hay algunos elementos que no cumplen exactamente esta configuración: Cu, Cr, Au, Ag. Todos ellos
no completan su último orbital s (tienen 1 electrón en él).
Mira por ejemplo la CE del cobre: CE (
29
Cu): 1s
2
2s
2
2p
6
3s
2
3p
6
4s
1
3d
10
ISOELECTRONICOS
Los átomos isoelectrónicos son aquellos que presentan igual cantidad de electrones
Por ejemplo, el anión flúor, el neón y el catión sodio son isoelectrónicos entre ellos.
Anión flúor (F¯ ): El flúor en su estado neutro posee Z=9 (9 electrones). No obstante, cuando forma
un anión este gana un electrón, quedando ahora 10 e
-
.
Su configuración electrónica es la siguiente: 1s
2
2s
2
2p
6
Neón (Ne): Este elemento presenta Z= 10 (10 electrones), como está en su estado neutro, no hay
perdida ni ganancias de electrones.
Quedando su configuración electrónica: 1s
2
2s
2
2p
6

5
Catión Sodio (Na+): El sodio en su estado neutro presenta Z=11 (11 electrones). Sin embargo, este
forma un catión cuando pierde un electrón, quedando ahora en 10 e
-
Su configuración electrónica es la siguiente: 1s
2
2s
2
2p
6
Como te habrás dado cuenta, todas las especies presentan 10 electrones por lo tanto, se dice
que estas son isoelectrónicas.
Escriba las configuraciones electrónicas de las especies siguientes: N
3-
Mg
2+
Cl
–
K
+
Ar y además
indique las entidades que son isoelectrónicas.
N
3-
Nitrógeno Z= 7 + 3 (gana 3 electrones) = 10; CE: 1s
2
2s
2
2p
6
Mg
2+
Magnesio Z = 12 – 2 (pierde 2 electrones) = 10; CE: 1s
2
2s
2
2p
6
Cl
–
Cloro Z= 17 + 1 (gana 1 electrón) = 18 electrones; CE: 1s
2
2s
2
2p
6
3s
2
3p
6
K+ Potasio Z= 19 – 1 (pierde 1 electrón) = 18 electrones; CE: 1s
2
2s
2
2p
6
3s
2
3p
6
Ar Argón Z= 18; CE: 1s
2
2s
2
2p
6
3s
2
3p
6
Resultado: El N3- y Mg2+ son especies isoelectrónicas entre ellas, debido a que presentan 10
electrones en su distribución electrónica.
Por su parte, las especies Cl–, K+, Ar son isoelectrónicas entre ellas ya que todas poseen 18 electrones
en su configuración electrónica.
CONFIGURACIÓN ELECTRÓNICA EXTERNA (CEE)
La configuración electrónica de los electrones que pertenecen a los niveles más externos forma la
configuración electrónica externa (CEE). Consiste en escribir cómo se encuentran distribuidos los
electrones en la parte más externa de un átomo (estos electrones son los que participan en las
reacciones químicas). Normalmente son los del último nivel. Tenés que tener cuidado cuando tienen
orbitales d en un nivel anterior: si la CE termina en el nivel, por ejemplo, 5 y el átomo tiene ocupado un
orbital d del nivel 4 entonces pueden ocurrir dos cosas:
1 - Los orbitales d están completos, es decir, tiene 10 electrones. En este caso
i) si ese subnivel es el último que aparece en la CEE entonces sí se escribe;
ii) si le sigue un orbital p en la configuración, no se lo escribe en la CEE.
2 - Los orbitales d están incompletos, tiene menos de 10 electrones. En este caso sí se escribe en la
CEE.
Ejemplos:
7
N CE: 1s
2
2s
2
2p
3
CEE: 2s
2
2p
3
48
Cd CE: 1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
6
5s
2
4d
10
CEE: 5s
2
4d
10
35
Br CE: 1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
5
CEE: 4s
2
4p
5
26
Fe CE: 1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
6
CEE: 4s
2
3d
6

6
Actividades
1) Escribir la configuración electrónica de X
2-
sabiendo que X tiene número másico 32 y 16
neutrones en su núcleo. ¿De qué elemento se trata? Usa tabla periódica.
2) Escribí las configuraciones electrónicas de los siguientes átomos e iones, indicar en cada caso
el numero atómico que corresponde.
N O Na Na
+
Sr
2+
Sn
4+
Br
3) Determinar el número de neutrones que tiene el núcleo de X cuyo A = 128, si su configuración
electrónica termina en 5p4 . Indicar el nombre y símbolo de X.
4) Indica el símbolo, el grupo y el período en que se encuentran los elementos cuyas
configuraciones electrónicas se indican a continuación:
1s
2
2s
2
2p
6
3s
2
3p
4
1s
2
2s
2
2p
6
3s
2
3p
6
1s
1
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
5
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
8
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
5
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
6
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d2
2
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
3
1s
2
2s
2
1s
2
2s
2
2p
6
3s
2
3p
6
4s
1
5) Un átomo de un elemento X produce un anión divalente negativo que es isoelectrónico con el
segundo gas noble. Determina del elemento X; CE, CEE, G, P, y su símbolo químico
6) Cuál es el número másico del elemento X sabiendo que tiene 45 neutrones y que su
configuración electrónica finaliza en 4p
5
.
7) Un elemento cuyo número másico es 127 pertenece al periodo 5 y grupo 7. ¿Cuántos protones,
neutrones y electrones tienen? Indica el Z
8) Los iones X
3-
y R
1–
son isoelectrónicos con el ión dipositivo de
40
G.
a) Indicar el símbolo de X y el grupo al que pertenece un isótopo de él de A = 82
b) Escribir la CE y CEE de R y la de su ión.
c) Sabiendo que el número de neutrones de X
3-
es 45, indicar el número másico del átomo
y el número de partículas con carga positiva que posee el mismo.
9) Dados los átomos
88
Q (que tiene 50 neutrones en su núcleo) y R (que forma un anión divalente
con CEE 5s
2
4d
10
5p
6
), Indicar:
a) La CEE de Q.
b) El número de protones que tiene el catión Q
2+
.
c) El número de partículas eléctricamente neutras del átomo
127
R.
10) Escribe el símbolo y número másico para cada uno de los siguientes casos:
a) Un átomo con 4 protones y 5 neutrones.
b) Un átomo con 12 protones y 14 neutrones.
c) Un átomo de calcio con un número de masa 46.
d) Un átomo con 30 electrones y 40 neutrones.
e) Un átomo de cobre con 34 neutrones.

7
11) Considera los siguientes átomos en los que el símbolo químico del elemento se representa
mediante X:
a) ¿Cuáles átomos tienen el mismo número de protones?
b) ¿Cuáles átomos son isótopos? ¿De cuál elemento?
c) ¿Cuáles átomos son isóbaros?
d) ¿Cuáles átomos son isótonos?
12) Un átomo de un elemento E produce un anión divalente negativo que es isoelectrónico con el
tercer gas noble. Indicar su C.E.E:
13) Un átomo tiene 12 protones y 12 neutrones en su núcleo. Indicar en qué grupo y periodo se
encuentra
14) Cuál es el número másico del elemento X sabiendo que tiene 45 neutrones y que su
configuración electrónica termina en 4p
5
TABLA PERIÓDICA
Todos los elementos químicos que se conocen están ordenados en la tabla periódica según su número
atómico (Z) formando filas y columnas.
Las filas (horizontales) se llaman períodos (P). Los elementos que forman un mismo período tienen la
misma cantidad de capas.
Las columnas (verticales) se llaman grupos (G); cada grupo está formado por elementos con iguales
propiedades químicas, algunos tienen algún nombre en particular:
Grupo 1 son los Metales alcalinos, con 1 electrón de valencia
Grupo 2 son los Metales acalinotérreos, con 2 electrones de valencia.
Grupos del 3 al 12 son los Metales de transición – Pueden tener diferentes electrones de
valencia, depende de su estado.
Grupo 13 son los Térreos, con 3 electrones de valencia
Grupo 14 son los Carbonoides con 4 electrones de valencia
Grupo 15 son los Nitrogenoides con 5 electrones de valencia
Grupo 16 son los Calcógenos con 6 electrones de valencia
Grupo 17 son los Halógenos con 7 electrones de valencia
Grupo 18 son los Gases nobles con 8 electrones de valencia
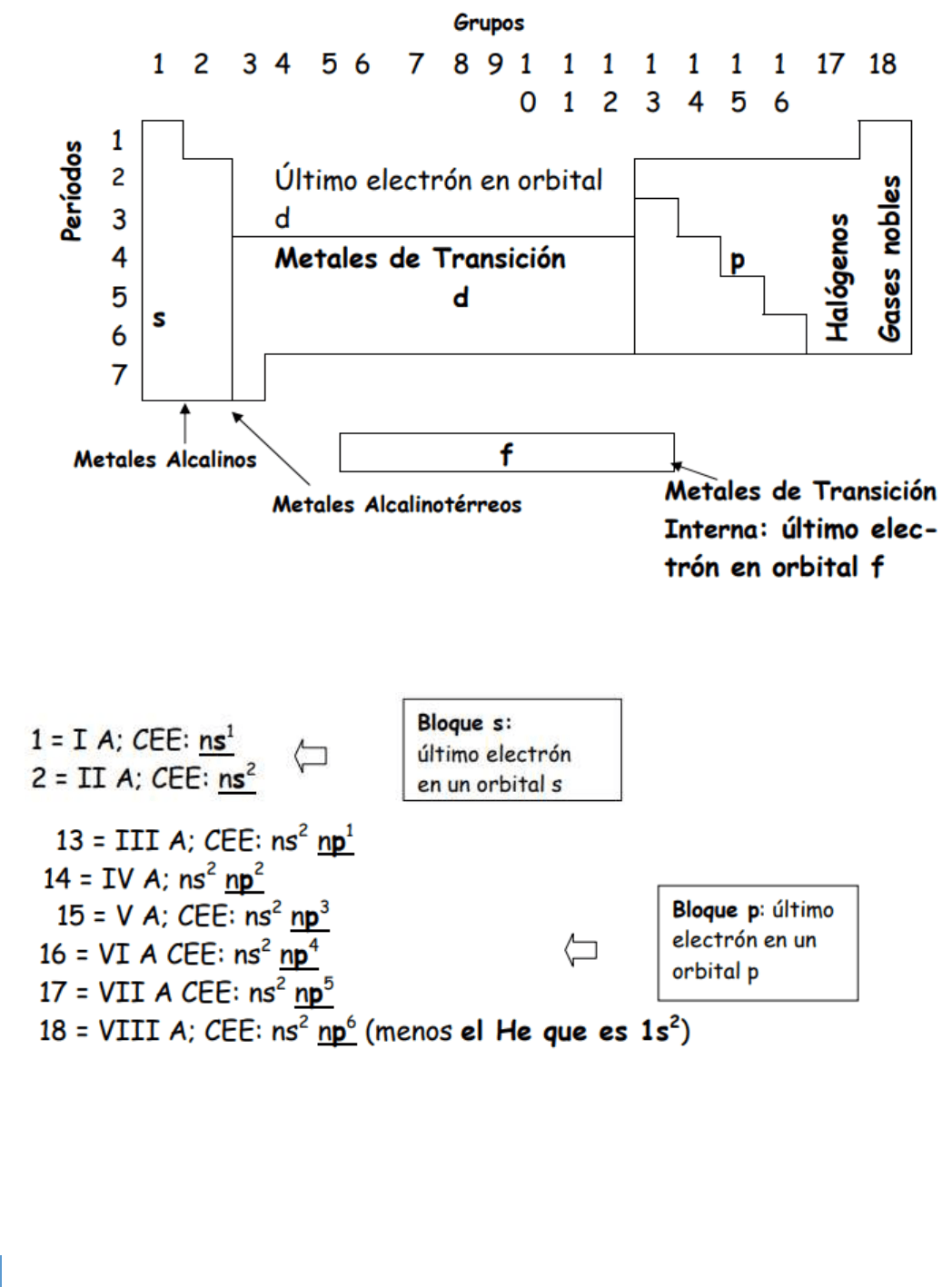
La ubicación de los elementos en la tabla también se relaciona con la CE de cada uno: se ubican según
cuál es el tipo de orbital (s, p, d o f) en el que termina su CE. En el siguiente esquema de la tabla podés
ver todo lo que acabo de decir
8
Los elementos de los bloques s y p se llaman representativos. Los elementos que están a la izquierda
y debajo de la "escalerita" son metales. Los que están a la derecha y arriba son no metales. Además
de numerar lo grupos, éstos tienen otro nombre y tienen una CEE característica:
Otra forma de escribir la CE de un elemento es poniendo entre corchetes el gas noble que está antes
en la tabla y completando lo que falta. Por ejemplo, la CE el
20
Ca se escribe como [Ar] 4s2 .
¡Podes escribir la CE del argón (Ar) y la del calcio (Ca) y compararlas!

9
¿Cómo ubicar un elemento en la tabla?
Hay 3 formas de ubicarlo:
1) Sabiendo cuál es su período y cuál es su grupo. Entonces si te digo que un elemento tiene P 3 y G
IIA, vas a la tabla, te fijás a lo largo del período 3 (segunda fila horizontal) y te parás en la casilla del
grupo 2: es el magnesio (Mg).
2) Sabiendo cuál es el número atómico (Z) del elemento. Podés identificar cuál es el valor de Z que
tiene cada elemento haciendo esto: el primer elemento es el hidrógeno ( H: P 1 y G 1 ) con Z=1, arriba
a la izquierda, y siguiendo hacia la derecha a lo largo de una fila sumás 1 al Z cuando pasás al elemento
de al lado; al acabar la fila seguís sumando de igual manera en la fila de abajo (también empezando en
la izquierda).
3) Sabiendo cómo termina su configuración electrónica: según cuál sea el último orbital ocupado en
seguida sabés a qué bloque perteneces (s, p, d o f), y según cuántos electrones tenga ese orbital,
sabrás en qué grupo.
Actividades
1) Indica si los elemento: Z = 26; Z = 60; Z = 86 y Z = 31 son representativos, de transición o de
transición interna. Escribe sus C.E
2) La CEE de un átomo de un elemento es 5s
2
4d
10
. Indicar a que grupo y periodo pertenece dicho
elemento
3) La C.E:E. de un átomo de un elemento es 5s
2
4d
10
5p
3
. Indicar a qué grupo y período pertenece
dicho elemento
4) Un elemento cuyo número másico es 122 pertenece al periodo 5 y grupo 5A. ¿Cuántos protones,
neutrones y electrones tiene? Indica el Z del elemento
5) Un elemento pertenece al grupo VII A, periodo 4. Indica el número de protones, neutrones y
electrones que presenta el elemento
6) Detalla para cada uno de los iones siguientes: número de protones, número de neutrones,
número de electrones; escribe el símbolo del átomo que posee igual número de electrones que
el ión.
a) F
–
b) Al
3+
c) S
2-
7) Escribe la configuración electrónica de los átomos de los elementos con Z=9, 15 y 34 e indica
en cada caso cuántos electrones serían necesarios para tener la configuración electrónica del
gas noble con Z más cercano
8) Escribe la configuración electrónica de los iones siguientes:
a) Mg
2+
b) Li
+
c) Cl
-
d) P
3-
e) Al
3+
f) O
2-
g) S
2-
.
Identificar cuáles de ellos son isoelectrónicos entre sí. Indica además si son isoelectrónicos con
algún gas noble

Configuración electrónica.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.