
COMPONENTES QUÍMICOS
DE LA CÉLULA
En los seres vivos todo obedece a las leyes de la química y la física. La química de la vida es
especial.
En primer lugar, se basa casi por completo en los compuestos de carbono, cuyo estudio se
conoce como química orgánica. En segundo lugar, depende de reacciones químicas que
tienen lugar en soluciones acuosas y en el rango de temperaturas estrecho que hay en a
tierra. En tercer lugar, es enormemente compleja, incluso la química de la célula más simple
es mucho más complicada que cualquier otro sistema químico. En cuarto lugar, está
dominada y coordinada por enormes moléculas poliméricas (cadenas de subunidades
químicas unidas en sus extremos), cuyas propiedades permiten que las células y los
organismos crezcan y se reproduzcan, y realicen todas las funciones características de la
vida. Por último, tiene una regulación estricta: las células despliegan una variedad de
mecanismos que garantizan que todas sus reacciones químicas se realicen en el lugar y
tiempo adecuados. La química, dictamina toda la biología.
La materia está compuesta por una combinación de elementos, sustancias con el
hidrógeno o el carbono que no se pueden descomponer o convertir en otras sustancias por
medios químicos.
La partícula más pequeña de un elemento, que mantiene sus propiedades químicas, es el
átomo. Las características de las sustancias que no son elementos puros dependen de los
átomos que contienen y del modo en que estos átomos se combinan entre sí para formar
moléculas. Por lo tanto, para entender cómo están constituidos los organismos vivos es
importante conocer cómo se forman los enlaces químicos que mantienen unidos a los
átomos de una molécula.
Los tipos de átomos que forman las células son
relativamente pocos
Cada átomo tiene en su centro un núcleo con carga positiva, rodeado a cierta distancia por
una nube de electrones con carga negativa que se mantienen en órbita alrededor del núcleo
por atracción electrostática. El núcleo está formado por dos tipos de partículas subatómicas:
los protones, con carga eléctrica positiva, y los neutrones, con son neutros. El numero de
protones presentes en el núcleo del átomo determina su número atómico. Por ejemplo, un
átomo de Carbono tiene seis protones en su núcleo y su NA es 6. La carga eléctrica de un
protón es exactamente igual y opuesta a la carga de un solo electrón.
El átomo es eléctricamente neutro; el número de electrones con carga negativa que rodean
al núcleo es igual al número de protones con carga positiva que contiene el núcleo, por lo
tanto, el número de electrones de un átomo también es igual al número atómico.
Los neutrones son partículas subatómicas sin carga que tienen la misma masa que los
protones. Éstos, contribuyen a la estabilidad estructural del núcleo, pero no alteran las
propiedades químicas del átomo. Así, un elemento puede existir en diversas formas físicas
distinguibles pero idénticas, denominadas isótopos. Cada isótopo tiene diferente número
de neutrones, pero el mismo número de protones.
El peso atómico de un átomo o el peso molecular de una molécula, es su masa en relación
con la masa del átomo de hidrógeno. Esto es igual al número de protones más el número de
neutrones que contiene el átomo o molécula. La masa de un átomo o molécula se suele
especificar en
daltons
. Un
dalton
es una unidad de masa atómica, aproximadamente igual
a la masa de un átomo de hidrógeno.
En la naturaleza existen 92 elementos que se diferencian entre sí por el número de protones
y electrones de sus átomos. Sin embargo, los organismos vivos sólo tienen una pequeña
selección de todos estos elementos: Carbono (C), Hidrógeno (H), Nitrógeno (N) y
Oxígeno (O).
Los electrones más externos determinan cómo interactúan
los átomos
Para entender cómo se unen los átomos para formar las moléculas que componen a los seres
vivos, debemos prestar atención a sus electrones.
En el núcleo, los protones y neutrones están fuertemente unidos entre sí y sólo se
intercambian en condiciones extremas, por ejemplo, durante la desintegración radiactiva. En
los tejidos vivos, solo los electrones de los átomos sufren reordenamientos. Constituyen las
partes accesibles de los átomos y determinan las leyes de la química por las que se combinan
los átomos formando las moléculas.
En esta escala submicroscópica, los movimientos de los electrones obedecen a leyes que
establecen que, los electrones de un átomo sólo pueden existir en determinadas regiones de
movimiento definidas, es decir, en órbitas separadas, y hay un límite del número de
electrones que pueden ocupar una órbita de un tipo determinado, llamado orbital
electrónico.
Los electrones que están más cerca del núcleo positivo son atraídos con más fuerza hacia él,
y ocupan el orbital más interno y estrechamente unido. Tal orbital puede contener un máximo
de dos electrones.
El segundo orbital está más alejado del núcleo, y sus electrones están unidos con menor
fuerza. En este orbital, puede haber hasta ocho electrones.
El tercer orbital, en el que la fuerza de unión es menor aún, también puede contener hasta
ocho electrones. Los orbitales cuarto y quinto pueden contener hasta 18 electrones cada
uno. En las moléculas biológicas son muy poco frecuentes los átomos con más de cuatro
orbitales.
La disposición de electrones de un átomo más estable es aquella en la que todos los
electrones se encuentran en los estados de unión más fuertes posibles, cuando ocupan los
orbitales más internos y cercanos al núcleo de carga positiva. Por ende, los electrones de un
átomo ocupan los orbitales en orden: el primero antes del segundo, el segundo antes del
tercero, etc. Un átomo cuyo orbital más externo está ocupado por electrones, es muy estable
y no reactivo.
Los átomos presentes en los tejidos vivos tienen orbitales electrónicos externos incompletos
y pueden reaccionar entre sí y formar moléculas.
Un orbital electrónico incompleto es menos estable que un orbital completo, por eso, los
átomos cuyos orbitales extremos están incompletos tienen una tendencia a interactuar con
otros átomos, ganando o perdiendo los electrones necesarios a fin de lograr un orbital
externo completo. Tal intercambio de electrones se puede producir transfiriendo electrones
de un átomo a otro o compartiendo electrones entre dos átomos.
Estas dos estrategias generan dos tipos de enlaces químicos entre los átomos: un
enlace
iónico
que es cuando un átomo cede electrones a otro, y un
enlace covalente
que es
cuando dos átomos comparten un par de electrones, a menudo compartiéndose de manera
desigual, y un átomo atrae a los electrones compartidos con mayor fuerza que el otro, dando
lugar a un
enlace covalente polar
.
Un átomo de H que sólo necesita un electrón más para completar su orbital en general lo
adquiere compartiéndolo, o sea, formando un enlace covalente con otro átomo, en muchos
casos, este enlace es polar. Los otros elementos más comunes en los organismos vivos, tales
como el C, N, y O tienen incompleto su segundo orbital, y el P y S que tienen su tercer orbital
incompleto suelen compartir electrones y completan su orbital externo de ocho electrones
mediante la formación de varios enlaces covalentes.
El número de electrones que un átomo debe adquirir o perder determina la cantidad de
enlaces que puede formar el átomo.
Los enlaces iónicos se forman por ganancia o pérdida de
electrones
Cuando un electrón salta de un elemento a otro, ambos átomos se convierten en iones con
carga eléctrica. Un átomo que ha perdido un electrón tiene ahora un electrón menos que la
cantidad de protones que tiene el núcleo, y por lo tanto tiene una carga neta positiva.
Estos iones positivos se denominan cationes.
El átomo que ha ganado un electrón, tiene ahora un electrón más que la cantidad de
protones y por consiguiente su carga es negativa. Éstas iones negativos se llaman
aniones. Por lo tanto, los iones se pueden clasificar según la cantidad de electrones que
ceden o adquieren.
Cuando dos elementos, uno con carga positiva y otro con carga negativa, se atraen entre
sí, se mantienen unidos por medio de un enlace iónico. Los enlaces iónicos son un tipo
de atracción electrostática: una fuerza de atracción que se produce entre dos átomos con
cargas opuestas.
Los enlaces covalentes se forman cuando dos átomos
comparten electrones.
Todas las características de una célula dependen de las moléculas que contiene.
Una molécula es una agrupación de átomos que se mantienen unidos por enlaces
covalentes en los que los átomos comparten electrones en lugar de transferirlos entre sí. Los
electrones compartidos completan los orbitales externos de ambos átomos.
Cuando los núcleos están separados por cierta distancia (longitud de enlace), las fuerzas
de atracción y rechazo se encuentran en equilibrio.
El átomo de H puede formar un solo enlace covalente pero los otros átomos que forman
enlaces covalentes en las células (O, N, S, P y C) pueden formar más de uno. Los orbitales
más externos de estos átomos pueden contener hasta ocho electrones y forman enlaces
covalentes con tantos átomos como sea necesario para alcanzar ese número.
Cuando un átomo forma enlaces covalentes con varios otros, estos enlaces múltiples tienen
una orientación espacial definida unos respecto de otros, reflejando las orientaciones de las
órbitas de los electrones compartidos.
Los enlaces covalentes entre múltiples átomos se caracterizan por ángulos de enlaces
específicos, así como por longitudes y energías de enlace también específicos.
Los enlaces covalentes pueden tener distinta fuerza
Otra propiedad importante de todo enlace (covalente o no covalente) es su fuerza.
La fuerza del enlace se mide por la cantidad de energía que se debe usar para romper el
enlace, que por lo general se expresa en unidades de kilocalorías por mol (kcal/mol).
Una kilocaloría es la cantidad de energía necesaria para elevar la temperatura de un litro de
agua en un grado centígrado. Una kilocaloría equivale a alrededor de 4,2 kilo Jules.
Los enlaces covalentes típicos son 100 veces más fuertes que la energía térmica o calórica y
por ende no se separan por movimientos térmicos sino solo durante reacciones químicas
específicas con otros átomos y moléculas.
La formación y rotura de los enlaces covalentes son eventos violentos, y en las células vivas,
estos eventos son controlados cuidadosamente por catalizadores específicos, denominados
enzimas.
Existen distintos tipos de enlaces covalentes
En la mayoría de los enlaces covalentes se comparten dos electrones, cada uno cedido por
cada átomo participante, tales enlaces se llaman enlaces simples. Sin embargo, en algunos
enlaces covalentes, se comparte más de un par de electrones. Por ejemplo, cada átomo
puede ceder dos electrones, este tipo de enlace se llama enlace doble. Estos enlaces son
más cortos y fuertes que los simples y tienen un efecto característico sobre la geometría
tridimensional de las moléculas.
Generalmente, un enlace covalente simple entre dos átomos permite la rotación de una parte
de la molécula en relación con la otra alrededor del eje del enlace. Un enlace doble impide
esa rotación, generando una disposición más rígida y menos flexible de los átomos.
Algunas moléculas contienen átomos que comparten electrones de una manera que produce
enlaces intermedios entre el enlace simple y doble. Cuando los átomos unidos por un enlace
simple perteneces a elementos diferentes, el grado de atracción que ejerce cada átomo sobre
los electrones compartidos suele ser distinto, por ejemplo, en comparación con el átomo de
C, la atracción que ejerce los átomos de O y N sobre los electrones es más fuerte, mientras
que la que ejerce el átomo de H es más débil.
Una estructura polar es aquella en la que la carga positiva se concentra en un extremo de la
molécula (el polo positivo), y la carga negativa, en el otro (el polo negativo). Por lo tanto,
los enlaces covalentes en los que se comparten electrones de esta manera desigual se
denominan enlaces covalentes polares.
Las atracciones electrostáticas ayudan a unir las moléculas
de las células
En las soluciones acuosas, los enlaces covalentes son de 10 a 100 veces más fuertes que las
otras fuerzas de atracción entre átomos, lo que permite que sus conexiones definan los
límites entre una molécula y otra. Pero gran parte de la biología depende de la unión de
diferentes moléculas entre sí. Tal unión es mediada por un grupo de atracciones no
covalentes que son, individualmente, bastante débiles, pero cuyas energías se pueden sumar
y crear una fuerza eficaz entre dos moléculas distintas. Las atracciones electrostáticas
alcanzan su máxima fuerza cuando los átomos involucrados están totalmente cargados, pero
también hay una atracción electrostática más débil entre las moléculas que tienen enlaces
covalentes polares. Así, los enlaces covalentes polares son muy importantes en biología,
porque permiten la interacción entre las moléculas a través de fuerzas eléctricas. Cualquier
molécula grande con muchos grupos polares tendrá un patrón de cargas parciales positivas
y negativas en su superficie. Cuando esta molécula encuentre a otra con cargas
complementarias, ambas experimentarán atracción electrostática, que se asemeja a los
enlaces iónicos que mantienen unidas a las sales. Cuando se forman suficientes enlaces no
covalentes débiles de este tipo entre dos moléculas grandes, sus superficies se adherirán
entre sí de forma específica. Sin embargo, el agua reduce mucho la atracción de estas cargas
entre sí, en la mayor parte de los contextos biológicos.
El agua se mantiene unida por enlaces de hidrógeno
El agua representa cerca del 70% del peso de la célula, y la mayor parte de las reacciones
químicas intracelulares ocurren en un medio acuoso. La química de la vida ha sido modelada
por las propiedades del agua.
En cada molécula de agua (H2O), los dos átomos de H están unidos al átomo de O por
enlaces covalentes. Los dos enlaces son altamente polares porque el O atrae con mayor
fuerza a los electrones, mientras que el H los atrae sólo débilmente. En consecuencia, los
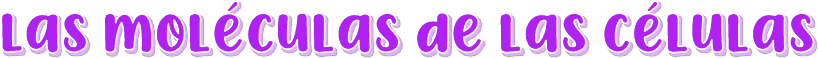
electrones se distribuyen en forma desigual en la molécula de agua, con preponderancia de
carga positiva en los dos átomos de H y carga negativa en el átomo de O.
Cuando una región con carga positiva de una molécula de agua se acerca a una región con
carga negativa de una segunda molécula de agua, la atracción eléctrica entre ellas puede
establecer un enlace débil denominado enlace de hidrógeno. Estos enlaces son más débiles
que los covalentes, y se rompen con facilidad por acción de los movimientos térmicos
aleatorios debido a la energía calórica de las moléculas, de manera que cada enlace persiste
solo durante un tiempo breve.
Cada molécula de agua puede formar enlaces de hidrógeno a través de sus dos átomos de
H con otras dos moléculas de agua, produciendo una red en la que los enlaces de H se
forman y se rompen en forma continua. Estos enlaces de H entrelazados son los que
mantienen al agua en estado líquido a temperatura ambiente, con un punto de ebullición
alto y una alta tensión superficial, y no en estado gaseoso. La vida no podría existir sin
enlaces de hidrógeno.
Sin embargo, no todos los átomos de H forman enlaces de hidrógeno. Los enlaces de H se
forman cuando un H con carga positiva, mantenido en una molécula mediante un enlace
covalente polar se acerca a un átomo con carga negativa (típicamente un átomo de O o N)
perteneciente a otra molécula. También se pueden formar enlaces de H entre distintas partes
de una misma molécula grande, en la que con frecuencia ayudan a crear formas especiales.
El enlace de H es sólo un miembro de una familia de enlaces no covalentes débiles que
desempeñan un papel crucial en permitir que las grandes moléculas se plieguen de maneras
singulares y se unan en forma selectiva a otras moléculas.
Las moléculas, como los alcoholes, que tienen enlaces polares y que pueden formar enlaces
de H, se mezclan bien con el agua. Las moléculas que tienen carga positiva o negativa
también se disuelven con facilidad en el agua. Estas moléculas se denominan hidrófilas, lo
que significa que tienen afinidad por el agua. Una gran cantidad de moléculas del medio
acuoso de la célula pertenecen a esta categoría, como por ejemplo los azúcares, ADN, ARN,
y la mayor parte de las proteínas.
Las moléculas hidrófobas no tienen carga y forman pocos enlaces de H o directamente
ninguno, por lo tanto no se disuelven en agua, como por ejemplo los hidrocarburos,
moléculas cuyos átomos de H se unen a los átomos de C por medio de enlaces covalentes,
mayormente no polares. Los átomos de H casi no tienen carga positiva neta, por lo tanto,
no pueden formar enlaces de H eficaces con otras moléculas. Por este motivo los
hidrocarburos son hidrófobos, una propiedad aprovechada por las células cuyas membranas
están compuestas por moléculas con largas colas de hidrocarburos. Como no se disuelven
en agua, los hidrocarburos hidrófobos pueden formar las delgadas barreras de membrana
que separan el interior acuoso de la célula con el medio externo, también acuoso.
La mayor parte de un organismo es agua. Si el agua se evapora, la mayor parte del peso
seco restante consiste en moléculas que contienen átomos de carbono.
Los compuestos producidos por organismos vivos se llaman bioquímicos. La química de la
vida se centra en la química del átomo de carbono. La calidad esencial del carbono que le
ha permitido desempeñar este papel es la increíble cantidad de moléculas que puede formar.
Al tener cuatro electrones de capa externa, un átomo de Carbono puede unirse con hasta
cuatro átomos más. Cada átomo de carbono puede unirse con otros átomos de carbono para
construir moléculas con cadenas principales que contienen largas cadenas de átomos de
carbono. Tanto el tamaño como la estructura electrónica del carbono lo hacen especialmente
adecuado para generar grandes cantidades de moléculas, de las cuales se conocen varios
cientos de miles.
Las cadenas principales que contienen carbono pueden ser lineales, ramificadas o cíclicas.
Podemos comprender mejor la naturaleza de las moléculas biológicas comenzando con el
grupo más simple de moléculas orgánicas, los hidrocarburos, que contienen solo átomos de
carbono e hidrógeno. La molécula etano (C2H6) es un hidrocarburo simple que consta de
dos átomos de carbono en el que cada carbono está unido al otro carbono, así como a tres
átomos de hidrógeno.
A medida que se agregan más carbonos, los esqueletos de las moléculas orgánicas aumentan
de longitud y su estructura se vuelve más compleja.
Grupos funcionales
Los hidrocarburos no se producen en cantidades significativas en la mayoría de las células
vivas (aunque constituyen la mayor parte de los combustibles fósiles formados a partir de
los restos de plantas y animales antiguos). Muchas de las moléculas orgánicas que son
importantes en biología contienen cadenas de átomos de carbono, como los hidrocarburos,
pero ciertos átomos de hidrógeno son reemplazados por varios grupos funcionales. Los
grupos funcionales son agrupaciones particulares de átomos que a menudo se comportan
como una unidad y dan a las moléculas orgánicas sus propiedades físicas, reactividad química
y solubilidad en solución acuosa.
Dos de los enlaces más comunes entre los grupos funcionales son los
enlaces éster
, que
se forman entre los ácidos carboxílicos y los alcoholes, y los
enlaces amida
, que se
forman entre los ácidos carboxílicos y las aminas. Varios de estos grupos pueden
ionizarse y cargarse positiva o negativamente.
Clasificación de moléculas biológicas según función
Las moléculas orgánicas que se encuentran comúnmente en las células vivas se pueden
dividir en varias categorías según su función en el metabolismo:
Macromoléculas: Las moléculas que forman la estructura y llevan a cabo las
actividades de las células son moléculas enormes y altamente organizadas llamadas
macromoléculas, que contienen de docenas a millones de átomos de carbono. Debido a su
tamaño y a las formas intrincadas que pueden asumir las macromoléculas, algunos de estos
gigantes moleculares pueden realizar tareas complejas con gran precisión y eficiencia. La
presencia de macromoléculas dota a los organismos de las propiedades de la vida y los
separa químicamente del mundo inanimado. Las macromoléculas se pueden dividir en cuatro
categorías principales: proteínas, ácidos nucleicos, polisacáridos y ciertos lípidos. Los
tres primeros tipos son polímeros compuestos de un gran número de bloques de construcción
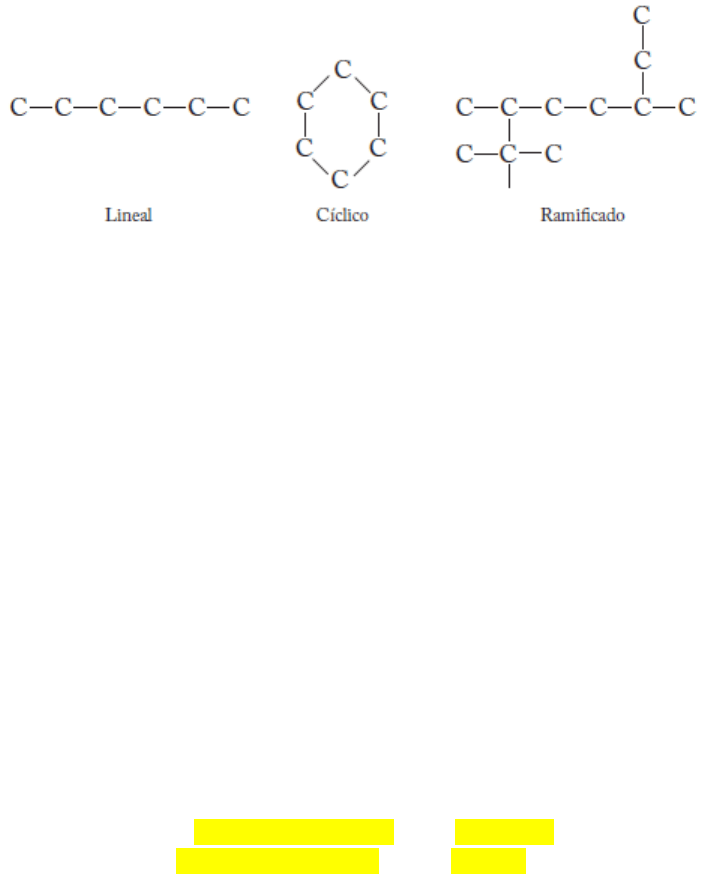
de bajo peso molecular o monómeros. Estas macromoléculas están construidas a partir de
monómeros mediante un proceso de polimerización que se asemeja a la unión de vagones
de ferrocarril en un tren. La estructura básica y la función de cada tipo de macromolécula
son similares en todos los organismos. No es hasta que se observan las secuencias
específicas de los monómeros que componen las macromoléculas individuales que se hace
evidente la diversidad entre los organismos.
Los bloques de construcción de las macromoléculas:
La mayoría de las macromoléculas dentro de una célula tienen una vida útil corta en
comparación con la propia célula; con la excepción del DNA de la célula, estos se degradan
continuamente y son reemplazados por nuevas macromoléculas. En consecuencia, la
mayoría de las células contienen un suministro (o conjunto) de precursores de bajo peso
molecular que están listos para incorporarse en las macromoléculas. Estos incluyen
azucares, que son los precursores de
polisacáridos
; aminoácidos, que son los
precursores de las
proteínas
;
nucleótidos
, que son los precursores de
ácidos nucleicos
,
y ácidos grasos, que se incorporan a los
lípidos
.
Intermediarios metabólicos (metabolitos).
Las moleculas en una celula tienen estructuras quimicas complejas y deben sintetizarse en
una secuencia paso a paso que comienza con materiales de partida especificos. En la celula,
cada serie de reacciones quimicas se denomina vía metabólica. La celula comienza con el
compuesto A y lo convierte en el compuesto B, luego en el compuesto C, y asi sucesivamente,
hasta que se produce algun producto final funcional (como un bloque de construccion de
aminoacidos de una proteina). Los compuestos formados a lo largo de las vias que conducen
a los productos finales pueden no tener funcion per se y se denominan intermedios
metabólicos.
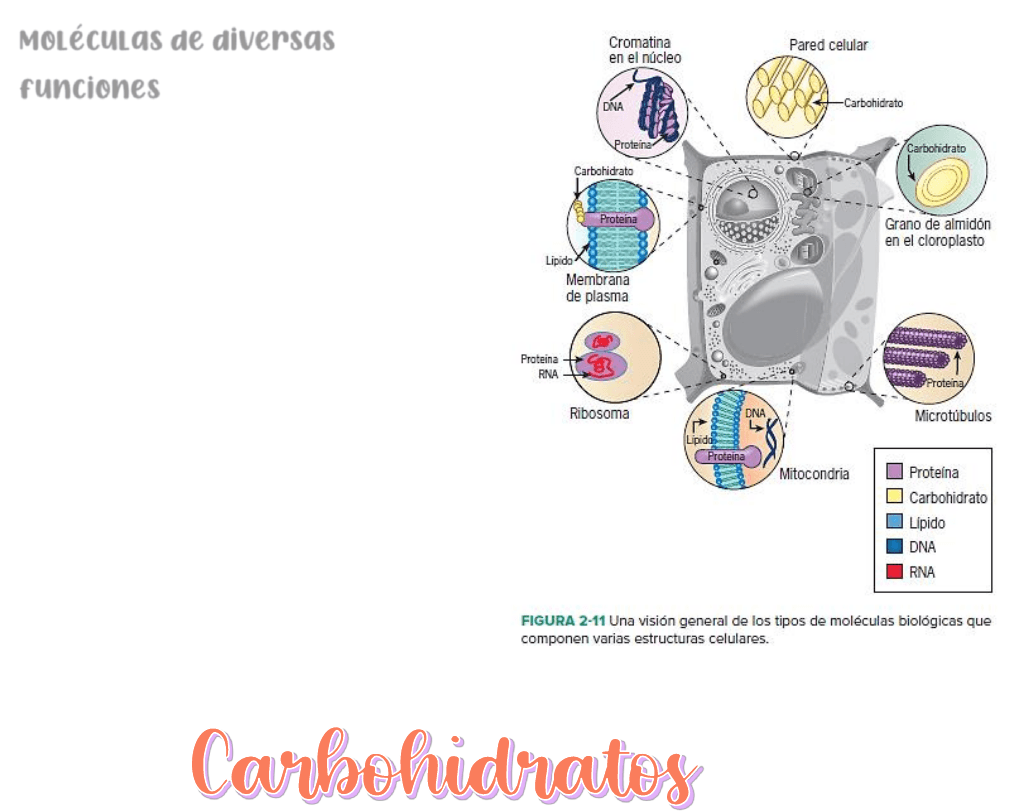
Moléculas de diversas
funciones
Obviamente esta es una amplia categoria de
moleculas, pero no tan grande como se
podria esperar; el grueso del peso seco de
una celula esta formado por
macromoleculas y sus precursores
directos. Las moléculas de diversas funciones
incluyen sustancias como vitaminas, que
funcionan principalmente como adyuvantes
de las proteinas; ciertas hormonas
esteroides o de aminoacidos; moléculas
involucradas en el almacenamiento de
energia, como ATP; moleculas
reguladoras como el monofosfato de
adenosina (AMP, monophosphate adenosine)
ciclico, y productos de desecho
metabolicos como la urea.
Los carbohidratos (o glucanos, como se les llama a menudo) incluyen azucares simples (o
monosacaridos) y todas las moléculas mas grandes construidas con bloques de azucar.
Los carbohidratos funcionan principalmente como depositos de energia química y como
materiales de construccion duraderos para la construcción biologica. La mayoria de los
azucares tienen la formula general (CH2O). Los azucares de importancia en el metabolismo
celular tienen valores de
n
que van de 3 a 7.
Los azucares que contienen tres carbonos se conocen como
triosas
, los que tienen cuatro
carbonos como
tetrosas
, los que tienen cinco carbonos como
pentosas
, los que tienen
seis carbonos como
hexosas
y aquellos con siete carbonos como
heptosas
.
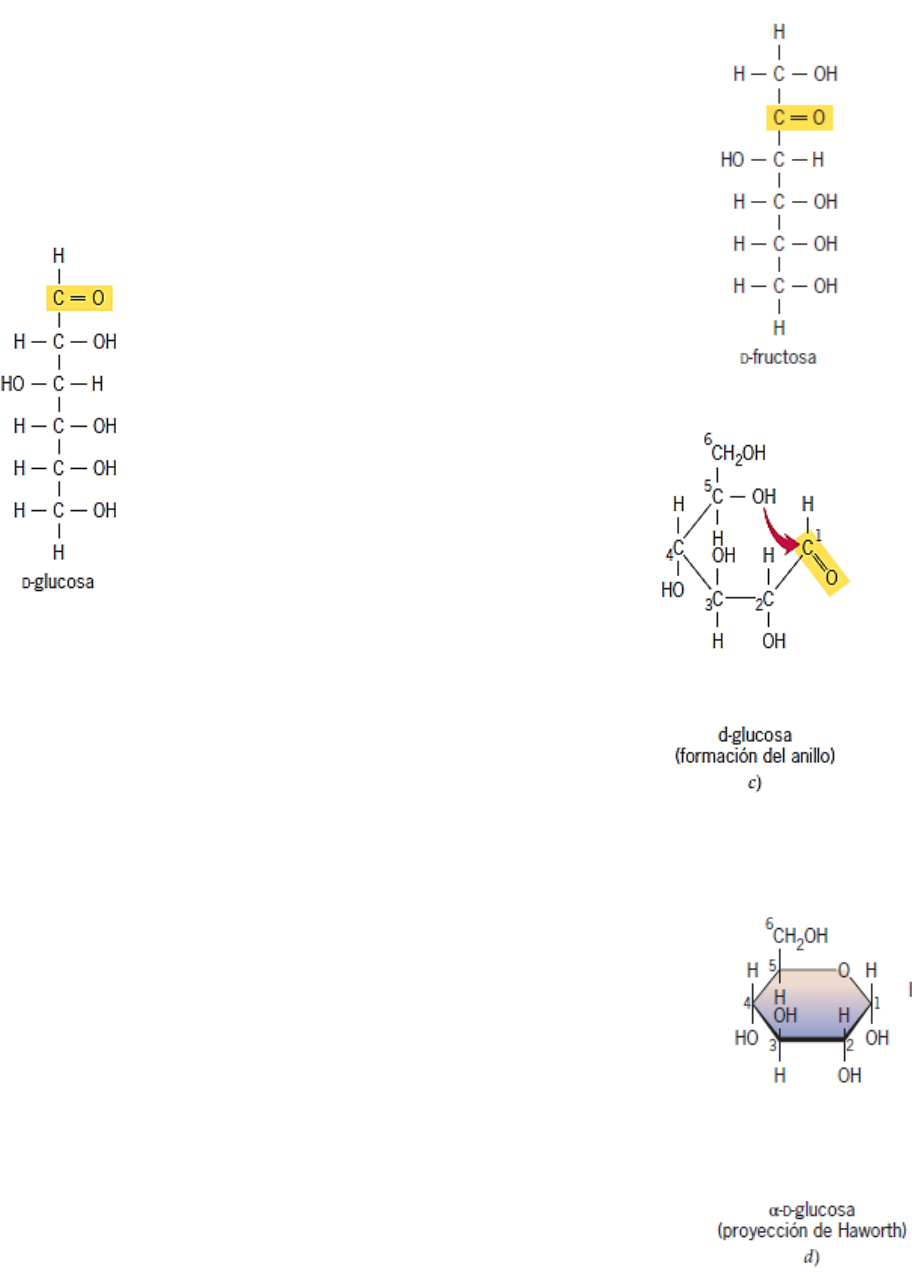
Estructura de azúcares simples
Cada molecula de azucar consiste en una columna central de atomos de
carbono unidos entre si en una serie lineal por enlaces simples. Cada uno
de los atomos de carbono de la cadena principal esta unido a un unico grupo
hidroxilo, a excepcion de uno que porta un grupo carbonilo (C=O). Si el
grupo carbonilo esta ubicado en una posicion interna (para formar un grupo
cetona), el azucar es una cetosa, como la fructosa
Si el carbonilo se encuentra en un extremo del azucar, forma
un grupo aldehido y la molecula se conoce como aldosa,
como se ejemplifica con la glucosa.
Debido a su gran cantidad de grupos hidroxilo, los azucares
tienden a ser altamente solubles en agua.
Los azucares que tienen cinco o mas carbonos
reaccionan espontáneamente para producir una
molecula cerrada o que contiene un anillo. Solo una
pequena fraccion de las moleculas de azucar en
solucion se encuentran en la forma lineal de cadena
abierta; el resto esta en forma de anillo. La forma
lineal es bioquimicamente importante porque el
grupo aldehído al final de la cadena es reactivo y puede reaccionar
con las proteinas, especialmente con la hemoglobina. Los pacientes
con diabetes tienen niveles mas altos de azucar en la sangre y este
azucar en su forma de cadena abierta reacciona con la hemoglobina
para producir una hemoglobina modificada llamada hemoglobina
A1c, que a menudo se usa en analisis de sangre para rastrear el
progreso de la diabetes. Reacciones similares de azúcar en forma
lineal con proteínas involucradas en el metabolismo del colesterol son una de las razones por
las que la diabetes causa enfermedades cardiacas.
La forma de cadena abierta de los azucares es, por tanto, muy importante
en medicina, pero la gran mayoria de los azucares se encuentran en forma
de anillo, y es en esta forma que se usan como bloques de construccion
para construir otros tipos de carbohidratos. Las formas de anillo de los
azucares generalmente se representan como estructuras planas que se
encuentran perpendiculares al plano del papel con la linea engrosada
situada mas cerca del lector.
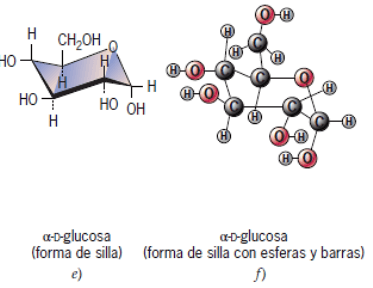
Los grupos H y OH se encuentran paralelos al
plano del papel, sobresaliendo por encima o por
debajo del anillo del azucar. De hecho, el anillo de
azucar no es una estructura plana, sino que
generalmente existe en una conformacion
tridimensional que se asemeja a una silla.
Unión de los azúcares
Los azucares se pueden unir entre si mediante
enlaces glucosídicos covalentes para formar moleculas mas grandes. Los enlaces glucosidicos
se forman por reaccion entre el atomo de carbono C1 de un azucar y el grupo hidroxilo de
otro azucar, generando un enlace —C—O—C entre los dos azucares. Los azucares se pueden
unir mediante una gran variedad de enlaces glucosídicos diferentes.
Las moleculas compuestas de solo dos unidades de azucar son disacaridos (figura 2-16).
Los disacaridos sirven principalmente como reservas de energia de facil acceso. La sacarosa,
o azucar de mesa, es un componente principal de la savia de la planta, que transporta energia
quimica de una parte de la planta a otra. La lactosa, presente en la leche de la mayoria de
los mamiferos, suministra a los mamiferos recien nacidos combustible para el crecimiento y
desarrollo temprano. La lactosa en la dieta es hidrolizada por la enzima lactasa, que esta
presente en las membranas plasmaticas de las celulas que recubren el intestino. Muchas
personas pierden esta enzima despues de la infancia y descubren que comer productos
lacteos causa molestias digestivas.
Los azucares tambien se pueden unir para formar pequeñas cadenas llamadas
oligosacaridos (oligo = poco). Con mucha frecuencia, tales cadenas se encuentran
covalentemente unidas a lipidos y proteinas, convirtiendolas en glucolipidos y
glucoproteinas, respectivamente. Los oligosacaridos son particularmente importantes en
los glucolipidos y glucoproteinas de la membrana plasmatica, donde se proyectan desde la
superficie de la celula. Debido a que los oligosacaridos pueden estar compuestos por muchas
combinaciones diferentes de unidades de azucar, estos carbohidratos pueden desempenar
un papel informativo; es decir, pueden servir para distinguir un tipo de celula de otro y
ayudar a mediar interacciones especificas de una celula con su entorno.
Polisacáridos
A mediados del siglo XIX, se sabia que la sangre de las personas que padecian diabetes tenia
un sabor dulce debido a un nivel elevado de glucosa, el azucar clave en el metabolismo
energetico.
Claude Bernard, un prominente fisiologo frances de la epoca, estaba buscando la causa de
la diabetes investigando la fuente de azucar en la sangre. Se supuso en ese momento que
cualquier azucar presente en un ser humano o un animal tenia que haberse Bernard
descubrio que, incluso si los animales se colocaban en una dieta totalmente carente de
carbohidratos, su sangre aun contenia una cantidad normal de glucosa. Claramente, la
glucosa podría formarse en el cuerpo a partir de otros tipos de compuestos.
Despues de mas investigaciones, Bernard descubrio que la glucosa ingresa a la sangre a
traves del higado. El descubrio que el tejido hepatico contiene un polimero insoluble de
glucosa que llamo glucógeno. Bernard concluyo que varios materiales alimenticios (como
proteinas) se llevaban al higado, donde se convertian quimicamente en glucosa y se
almacenaban como glucogeno.
Luego, como el cuerpo necesitaba azucar como combustible, el glucogeno del higado se
transformo en glucosa, que se libero al torrente sanguineo para satisfacer los tejidos sin
glucosa.
En la hipotesis de Bernard, el equilibrio entre la formacion de glucogeno y la degradacion del
glucogeno en el higado fue el principal determinante para mantener el nivel relativamente
constante (homeostatico) de glucosa en la sangre.
La hipotesis de Bernard resulto ser correcta. La molecula que denominó glucogeno es un
tipo de polisacárido, un polimero de unidades de azucar unidas por enlaces glucosídicos
consumido previamente en la dieta.
Glucógeno y almidón: polisacáridos nutricionales
El glucogeno es un polimero ramificado que contiene solo un tipo de monomero: glucosa. La
mayoria de las unidades de azucar de una molecula de glucogeno se unen entre si por
enlaces glucosidicos α.
Los puntos de ramificacion contienen un azucar unido a tres unidades vecinas en lugar de a
dos, como en los segmentos no ramificados del polimero. El vecino adicional, que forma la
rama, esta unido por un enlace glucosídico α(1 y 6) (
El glucogeno sirve como almacen de excedentes de energía quimica en la mayoria de los
animales. Los musculos esqueléticos humanos, por ejemplo, tipicamente contienen suficiente
glucogeno para alimentar alrededor de 30 minutos de actividad moderada. Cuando se
almacena en las celulas, el glucogeno esta altamente concentrado en lo que parecen ser
granulos irregulares y con tinción oscura en las micrografias electronicas. La mayoria de las
plantas depositan su excedente de energía quimica en forma de almidón, que al igual que
el glucogeno es tambien
un polimero de glucosa
. Las papas y los cereales, por ejemplo,
consisten principalmente en almidon. El almidon es en realidad una mezcla de dos polimeros
diferentes, amilosa y amilopectina. La amilosa es una molecula helicoidal no ramificada
cuyos azucares estan unidos por enlaces α(1 → 4) , mientras que la amilopectina es
ramificada. La amilopectina difiere del glucogeno por ser mucho menos ramificada y tener
un patron de ramificacion irregular. El almidon se almacena como granulos densamente
empaquetados, o granos de almidon, que están encerrados en organelos unidos a la
membrana (plastidos) dentro de la celula de la planta. Aunque los animales no sintetizan el
almidon, poseen una enzima (amilasa) que lo hidroliza facilmente.
Celulosa, quitina y glucosaminaglucanos: polisacáridos
estructurales
Considerando que algunos polisacaridos constituyen depósitos de energia facilmente
digeribles, otros forman materiales estructurales resistentes y duraderos. El algodon y el lino,
por ejemplo, consisten principalmente en celulosa, que es el componente principal de las
paredes celulares de las plantas. Las telas de algodón deben su durabilidad a las moleculas
de celulosa largas, no ramificadas, que se ordenan en agregados uno al lado del otro para
formar cables moleculares que estan construidos idealmente para resistir las fuerzas de
tracción (o tension).

Al igual que el glucogeno y el almidon, la celulosa consiste unicamente en monomeros de
glucosa; sus propiedades difieren drasticamente de estos otros polisacaridos porque las
unidades de glucosa estan unidas por enlaces β(1 y 4) en lugar de enlaces α(1 y 4).
Los animales multicelulares (con raras excepciones) carecen de la enzima necesaria para
degradar la celulosa, que resulta ser la materia organica mas abundante en la Tierra y rica
en energia quimica. Los animales que “sobreviven” al digerir la celulosa, como las termitas
y las ovejas, lo hacen al albergar bacterias y protozoos que sintetizan la enzima necesaria,
la celulasa.
La celulosa es un componente importante de la fibra dietetica, un termino amplio que incluye
todos los polisacaridos que comemos que no pueden ser digeridos por las enzimas humanas.
No todos los polisacaridos biologicos consisten en monómeros de glucosa. La quitina es un
polimero no ramificado del azúcar N-acetilglucosamina, que es similar en estructura a la
glucosa pero tiene un grupo acetil amino en lugar de un grupo hidroxilo unido al segundo
atomo de carbono del anillo.
La quitina se presenta ampliamente como material estructural entre los invertebrados,
particularmente en la cubierta exterior de insectos, arañas y crustaceos. La quitina es un
material resistente, elastico y flexible, a diferencia de ciertos plasticos. Los insectos deben
gran parte de su exito a este polisacarido altamente adaptativo.
Otro grupo de polisacaridos que tiene una estructura mas compleja son los
glucosaminoglucanos (o los GAG). A diferencia de otros polisacaridos, tienen la estructura
—A—B—A—B—, donde A y B representan dos azucares diferentes. El GAG mejor estudiado
es la heparina, que es secretada por las celulas en los pulmones y otros tejidos en respuesta
a la lesion tisular. La heparina inhibe la coagulacion de la sangre, evitando asi la formación
de coagulos que pueden bloquear el flujo de sangre al corazon o los pulmones. La heparina
logra esta hazaña al activar un inhibidor (antitrombina) de una enzima clave (trombina)
que se requiere para la coagulacion de la sangre. La heparina, que normalmente se extrae
del tejido del cerdo, se ha usado durante décadas para prevenir los coagulos de sangre en
pacientes despues de una cirugia mayor. A diferencia de la heparina, la mayoria de los GAG
se encuentran en los espacios que rodean a las celulas. Los polisacáridos mas complejos se
encuentran en las paredes celulares de las plantas.
Los lipidos son un grupo diverso de moleculas biologicas no polares cuyas propiedades
comunes son su capacidad para disolverse en solventes organicos, como el cloroformo o el
benceno, y su incapacidad para disolverse en el agua, una propiedad que explica muchas de
sus variadas funciones biologicas. Los lipidos de importancia en la funcion celular incluyen
grasas, esteroides y fosfolipidos.
Grasas
Las grasas consisten en una molecula de glicerol unida por enlaces ester a tres acidos
grasos; la molecula compuesta se denomina triacilglicerol, tambien conocida como
triglicerido.
Los acidos grasos son cadenas de hidrocarburos largas, no ramificadas con un unico grupo
carboxilo en un extremo. Debido a que los dos extremos de una molecula de acido graso
tienen una estructura muy diferente, tambien tienen distintas propiedades.
La cadena de hidrocarburo es hidrofobica, mientras que el grupo carboxilo (—COOH), que
tiene una carga negativa a pH fisiologico, es hidrofilico.
Se dice que las moleculas que tienen ambas regiones hidrofobica e hidrofilica son
anfipáticas
; tales moleculas tienen propiedades inusuales y biológicamente importantes.
Las propiedades de los acidos grasos se pueden apreciar considerando el uso de un producto
familiar: el jabon, que consiste en acidos grasos.
Los acidos grasos difieren entre si en la longitud de su cadena de hidrocarburos y la presencia
o ausencia de dobles enlaces. Los acidos grasos presentes en las celulas generalmente varian
en longitud de 14 a 20 carbonos. Los acidos grasos que carecen de dobles enlaces, como el
acido esteárico, se describen como saturados; aquellos que poseen dobles enlaces son
insaturados. Los acidos grasos naturales tienen dobles enlaces en la configuración cis. Los
dobles enlaces (de la configuracion cis) producen dobleces en una cadena de acido graso.
En consecuencia, cuantos mas enlaces dobles poseen las cadenas de acidos grasos, menos
eficazmente pueden encapsularse estas cadenas largas. Esto reduce la temperatura a la que
se licua un lípido que contiene acidos grasos. El triestearato, cuyos acidos grasos carecen
de dobles enlaces, es un componente comun de las grasas animales y permanece en estado
solido muy por encima de la temperatura ambiente. Por el contrario, la profusion de dobles
enlaces en las grasas vegetales explica su estado liquido, tanto en la celula de la planta como
en el estante del supermercado, y por ser etiquetados como “poliinsaturados”.
Las grasas que son liquidas a temperatura ambiente se denominan aceites.
Las grasas solidas, como la margarina, se forman a partir de aceites vegetales insaturados
mediante la reduccion quimica de los dobles enlaces con atomos de hidrogeno (un proceso
denominado hidrogenacion). El proceso de hidrogenacion tambien convierte algunos de
los dobles enlaces cis en dobles enlaces trans, que son rectos en lugar de torcidos. Este
proceso genera grasas parcialmente hidrogenadas o trans. Comer grasas trans aumenta
el riesgo de enfermedades del corazon, y las grasas trans artificiales ahora estan prohibidas
en varios paises, con otras grasas se esta considerando tomar medidas similares.
Una molecula de grasa puede contener tres acidos grasos identicos o puede ser una grasa
mixta, que contiene mas de una especie de acido graso.
La mayoria de las grasas naturales, como el aceite de oliva o la grasa lactea, son mezclas de
moleculas que tienen diferentes especies de acidos grasos.
Las grasas son muy ricas en energia quimica; un gramo de grasa contiene mas del doble del
contenido de energia de un gramo de carbohidratos. Los carbohidratos funcionan
principalmente como una fuente de energia disponible a corto plazo, mientras que las
reservas de grasa almacenan energia a largo plazo.
Debido a que carecen de grupos polares, las grasas son extremadamente insolubles en agua
y se almacenan en las celulas en forma de gotas de lipidos secos. Debido a que las gotas de
lípidos no contienen agua como lo hacen los granulos de glucogeno, representan un
combustible de almacenamiento extremadamente concentrado. En muchos animales, las
grasas se almacenan en celulas especiales (adipocitos) cuyo citoplasma esta lleno de una

o unas pocas gotas de lipidos grandes. Los adipocitos exhiben una capacidad notable de
cambiar su volumen para acomodar cantidades variables de grasa.
Esteroides
Los esteroides se construyen alrededor de un caracteristico esqueleto de hidrocarburo de
cuatro anillos. Uno de los esteroides mas importantes es el colesterol, un componente de
las membranas de las celulas animales y un precursor para la sintesis de varias hormonas
esteroides, como la testosterona, la progesterona y el estrógeno. El colesterol esta ausente
en gran parte de las celulas vegetales, por lo que los aceites vegetales se consideran “libres
de colesterol”, pero las celulas vegetales pueden contener grandes cantidades de
compuestos relacionados.
Fosfolípidos
La molecula de un fosfolípido común se asemeja a una grasa (triacilglicerol), pero tiene solo
dos cadenas de acidos grasos en lugar de tres; es un diacilglicerol. El tercer hidroxilo de
la cadena principal de glicerol se une covalentemente a un grupo fosfato, que a su vez se
une covalentemente a un pequeño grupo polar, como la colina.
A diferencia de las moléculas de grasa, los fosfolipidos contienen dos extremos que
tienen propiedades muy diferentes: el extremo que contiene el grupo fosfato tiene un
caracter claramente hidrofilico; el otro extremo compuesto por las dos colas de acidos
grasos tiene un carácter claramente hidrofobico.
Las proteinas son las macromoleculas que llevan a cabo prácticamente todas las actividades
de una celula; son las herramientas moleculares y las maquinas que hacen que las cosas
sucedan.
Como enzimas, las proteinas aceleran enormemente la tasa de reacciones metabolicas;
como cables estructurales, las proteinas proporcionan soporte mecanico tanto dentro de
las celulas como fuera de sus perímetros; como hormonas, factores de crecimiento y
activadores de genes, las proteinas realizan una amplia variedad de funciones
reguladoras; como receptores de membrana y transportadores, las proteinas
determinan a que reacciona una celula y que tipos de sustancias entran o salen de la celula;
como filamentos contractiles y motores moleculares, las proteinas constituyen la
maquinaria para los movimientos biologicos.
Entre sus muchas otras funciones, las proteinas actuan como anticuerpos, sirven como
toxinas, forman coagulos de sangre, absorben o refractan la luz y transportan
sustancias de una parte del cuerpo a otra. ¿Como puede un tipo de molecula tener
Este documento contiene más páginas...
Descargar Completo
componentes químicos de la célula.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.