
Cicatrización dirigida
M. Revol, J.-M. Servant
La cicatrización dirigida es un método quirúrgico propiamente dicho, que puede estar
indicado siempre que una pérdida de sustancia no sea suturable pero su lecho esté
correctamente vascularizado, sin que queden expuestos órganos nobles. La cicatrización
espontánea se denomina «dirigida» por el cirujano, quien debe vigilarla con regularidad
para asegurarse de la ausencia de infección, puede acelerarla mediante una escisión
quirúrgica en el estadio de detersión, puede resecar una zona de granulación hipertrófica
y puede acortar la evolución en el estadio de epidermización mediante un injerto
cutáneo. Algunas regiones del cuerpo se prestan mejor que otras a la cicatrización
espontánea. La cicatrización dirigida tiene como ventaja el limitar la superficie de la
pérdida de sustancia cutánea inicial y repararla sin cicatrices adicionales. Puede utilizarse
de forma exclusiva o como preparación para un injerto o un colgajo. Si el paciente está
sano, la cicatrización se logra en todos los casos, con independencia del tipo de apósito,
que en última instancia importa muy poco en cirugía.
© 2010 Elsevier Masson SAS. Todos los derechos reservados.
Palabras Clave: Cicatrización; Heridas; Apósitos
Plan
¶ Introducción 1
¶ Principios 1
Detersión supurada 2
Granulación 2
Epidermización 2
¶ Métodos 3
Material necesario y suficiente 3
Material opcional: apósitos modernos 3
Presión negativa 4
¶ Indicaciones 4
Indicaciones de la cicatrización dirigida 4
Indicaciones de los apósitos 8
Casos especiales de los apósitos con presión negativa 9
■ Introducción
La cicatrización dirigida es un método quirúrgico de
pleno derecho, al igual que las suturas, los injertos y los
colgajos. Al contrario de lo que su sencillez aparente
podría hacer pensar, requiere también una cierta expe-
riencia, tanto para plantear su indicación como para
seguir su evolución. Para ser realmente dirigida, la
cicatrización debe ser vigilada por el propio cirujano que
la prescribe, al menos una vez a la semana.
■ Principios
Cuando un ser humano sano no muere por sus
heridas, cicatriza de forma natural y espontánea como
cualquier animal o vegetal, sin ayuda de nadie. El arte
del terapeuta moderno consiste en acompañar esta
cicatrización sin perjudicarla y/o disminuyendo la
duración de la evolución o la magnitud de las secuelas
mediante un injerto o un colgajo. Se deben conocer los
mecanismos de la cicatrización espontánea de las
heridas. Aunque el nivel de los conocimientos en
materia de cicatrización aumenta de forma exponencial
y en la actualidad se ha llegado a la escala molecular y
genética
[1-3]
, es totalmente inútil entrar en este artículo
en los detalles moleculares, porque estos conocimientos
carecen de aplicaciones prácticas eficaces. El cirujano
plástico, que es el único especialista de las heridas que
cicatrizan de verdad, puede presumir sin rubor de
conocer las fases clínicas de la cicatrización que perma-
necen a nivel de la visión humana o del simple micros-
copio. Este proceso es un viaje apasionante en el tiempo
y/o en el espacio. A pesar de que contamos con un
entorno material excepcionalmente favorable, cicatriza-
mos del mismo modo que nuestros ancestros más
lejanos en sus cavernas o que la mayor parte de la
humanidad, que aún está desprovista de medicinas,
enfermeras y apósitos especiales.
Por tanto, el punto de partida es la herida o la
pérdida de sustancia, con independencia de su origen,
pero que se produce en un paciente sano. Cuando su
¶ E – 45-050
1Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.

lecho tiene una vascularización adecuada, la cicatriza-
ción espontánea evoluciona en tres fases sucesivas: la
detersión supurada, la granulación y la epidermización.
La duración relativa de cada una de estas fases es muy
variable según la causa de la necrosis (traumática,
isquémica, térmica, etc.), según su localización y según
su extensión.
Detersión supurada
La detersión supurada tiene como objetivo la elimi-
nación de los tejidos necrosados. Esta eliminación
natural se realiza por separación enzimática entre las
células muertas y las células vivas. Las enzimas proteo-
líticas provienen tanto del organismo (leucocitos y
macrófagos que llegan a la herida por la reacción
inflamatoria) como de los microorganismos de la piel
del paciente. Sin microorganismos, no hay detersión
supurada y, por tanto, no se produce la eliminación
espontánea de la necrosis. Según cuál sea la naturaleza
de los tejidos necrosados, la detersión espontánea es
más o menos prolongada: rápida en el tejido adiposo,
lenta en la dermis e interminable en las aponeurosis y
los tendones.
Desde el punto de vista celular y molecular, los
primeros elementos que llegan a la herida con el coá-
gulo son las plaquetas, que liberan citocinas y factores
de crecimiento (factor de crecimiento derivado de
plaquetas [PDGF], factor de crecimiento transformante
[TGF], etc.), que atraen hacia la zona de necrosis a los
polimorfonucleares y a los macrófagos durante la
reacción inflamatoria. Además de su papel en la fagoci-
tosis de los restos celulares, estos últimos liberan en la
herida otras citocinas y otros factores de crecimiento
que favorecen la reacción inflamatoria y la formación
del tejido de granulación. Entre los principales factores
de crecimiento conocidos que participan en la cicatriza-
ción, se pueden citar el PDGF, el TGF alfa y beta, el
factor de crecimiento endotelial vascular (VEGF), y el
factor de crecimiento fibroblástico (FGF). Por el
momento, basta con saber que existen.
Desde el punto de vista clínico, la detersión «supu-
rada» se acompaña de pus, como su nombre indica. No
hay que preocuparse, sino limpiar la herida a diario
mediante lavado con agua. Aunque los antisépticos
líquidos se han convertido en un ritual, son inútiles.
Dado que la detersión se debe a la reacción inflamatoria
y a los microorganismos, se deben prohibir los antiin-
flamatorios o los antisépticos e, incluso, los antibióticos.
Por último, hay que verificar cada día la ausencia de
eritema periférico intenso alrededor de la herida, la
ausencia de linfangitis, de dolor o de fiebre, que obliga-
rían a tomar una muestra para su estudio bacteriológico
y plantear un tratamiento antibiótico adecuado.
Por último, basta con comprender bien la diferencia
entre la situación bacteriológica y los signos clínicos.
Los microorganismos están por todas partes, tanto en la
piel sana como en las heridas. Esto puede ser inquie-
tante cuando aparecen los signos clínicos (eritema,
linfangitis, dolor, fiebre), lo que es infrecuente en la
práctica.
Granulación
Una vez que se eliminan los tejidos necrosados, el
tejido de granulación rellena la pérdida de sustancia
para reemplazar a la dermis desaparecida. Siempre que
el lecho tenga una vascularización correcta, granulará.
En el fondo de la pérdida de sustancia aparecen neova-
sos y su crecimiento se acompaña de la migración de
fibroblastos, que sintetizan a su vez colágeno, que es la
base de una nueva matriz extracelular a cuyo seno
migran los fibroblastos y las células de la inflamación.
Desde el punto de vista macroscópico, la altura de la
pérdida de sustancia se rellena poco a poco por un
«tejido de granulación» de color rojo intenso. De forma
simultánea, la superficie de la pérdida de sustancia se
reduce de forma considerable bajo el efecto de los
miofibroblastos, que son un tipo especial de diferencia-
ción de los fibroblastos, parecidos a las fibras musculares
lisas. Esta retracción que acompaña a la granulación de
una cicatrización espontánea es constante y siempre es
muy extensa, superior al 50% de la pérdida de sustancia
inicial. Esta retracción, que suele ser útil, en ocasiones
puede ser perjudicial cuando se localiza cerca de una
articulación, donde conlleva el riesgo de limitar su
amplitud, o cerca de un orificio natural, al que puede
deformar.
Desde el punto de vista clínico, se debe verificar la
aparición del tejido de granulación y después su progre-
sión, con el llenado progresivo del fondo de la herida.
En especial, hay que vigilar su evolución, que conlleva
el riesgo de dar lugar a una hipertrofiaoaungranu-
loma inflamatorio. La granulación hipertrófica, que se
reconoce por su aspecto exudativo, blando, friable,
edematoso y hemorrágico, sobrepasa el nivel de la piel
sana vecina, lo que impide la epidermización. Por tanto,
se trata de un callejón sin salida de la cicatrización, que
se debe tratar mediante corticoides locales. El tejido de
granulación se aplana, tras lo que puede epidermizarse,
bien de forma espontánea o quirúrgicamente con un
injerto dermoepidérmico. La prescripción de una corti-
coterapia se realiza siempre a demanda, en el caso en el
que la granulación sobrepase el nivel de la piel vecina.
Su duración máxima será de 24 horas. No debe utili-
zarse de forma sistemática (en días alternos) ni
prolongada.
Epidermización
Cuando el tejido de granulación cubre la totalidad de
la pérdida de sustancia, la epidermización termina el
proceso de cicatrización recubriéndolo con una nueva
epidermis. Esta epidermización sólo tiene lugar cuando
el tejido de granulación ha alcanzado el nivel de los
bordes de la pérdida de sustancia, pues proviene de la
epidermis de los bordes y se realiza de forma centrípeta.
Los queratinocitos forman una capa unicelular que
progresa desde la periferia, donde tienen lugar las
mitosis, hasta el centro del tejido de granulación. Este
“ Punto importante
Infección de una herida
[4, 5]
Al igual que la piel sana, todas las heridas están
contaminadas con microorganismos. Según su
cantidad, en la actualidad se distinguen cuatro
niveles de contaminación cuyas definiciones son
relativamente difusas:
• heridas «contaminadas», donde las bacterias
están presentes, pero no proliferan;
• heridas «colonizadas», donde las bacterias
proliferan sin consecuencias sobre la cicatrización;
• heridas «colonizadas de forma crítica», sin
signos clínicos, pero con una alteración de la
cicatrización;
• heridas «infectadas», con signos clínicos
manifiestos (eritema, linfangitis, fiebre). Desde el
punto de vista bacteriológico, esto corresponde a
másde10
5
bacterias/mm
3
de tejido.
La cicatrización se produce de forma espontánea
en los dos primeros niveles y está inhibida en los
dos últimos, donde necesita un desbridamiento
y/o una antibioticoterapia adaptada según los
casos. Por último, la naturaleza de los
microorganismos implicados importa al menos
tanto como su cantidad.
E – 45-050
¶
Cicatrización dirigida
2 Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
fino ribete epitelial que se desliza por la superficie del
tejido de granulación es muy frágil. Este fenómeno
extraordinario de epitelización, que es visible a simple
vista, se basa en mecanismos ultraestructurales de una
complejidad enorme.
Cuando todo el tejido de granulación está recubierto
por la epidermis, la migración de los queratinocitos se
detiene. A continuación, se diferencian de forma pro-
gresiva como una dermis normal y se reconstituye una
membrana basal de forma progresiva, fijando la epider-
mis a su lecho conjuntivo. En este momento la cicatri-
zación ha terminado, pero comienza la vida de la
cicatriz y su maduración dura1o2años antes de que
la remodelación progresiva de la matriz de colágeno la
permita presentar propiedades mecánicas definitivas
parecidas a la de la dermis normal.
En todos los casos, el tejido cicatrizal carece de
anexos epidérmicos (pelos, glándulas sebáceas o sudorí-
paras). Los melanocitos colonizan de forma secundaria
la nueva epidermis y en ocasiones pueden causar fenó-
menos discrómicos, que se agravan por una exposición
solar intempestiva.
Desde el punto de vista clínico, el ribete epitelial es
visible en la periferia de la herida retraída, en la super-
ficie del tejido de granulación. No está adherido a este
último, es muy frágil y puede arrancarse con los cam-
bios de apósitos. Por tanto, éstos deben ser grasos o
húmedos, no adhesivos y no requieren que se cambien
a diario.
■ Métodos
La cicatrización es un mercado para la industria de los
apósitos. Se trata de un mercado en plena expansión,
pues cada vez más personas sobreviven más tiempo. Sin
embargo, en personas sanas la cicatrización se produce
de forma espontánea, con independencia del tipo de
apósito. El cirujano plástico es el responsable de este
tipo de heridas, en las que puede acortar su evolución
o disminuir las secuelas retráctiles. En pacientes con
algún tipo de enfermedad, la herida se cronifica y, si no
es operable o si no tiene tratamiento etiológico, no
tendrá ninguna posibilidad de cicatrizar de forma
espontánea, con independencia del tipo de apósito. Una
herida «crónica» es una herida inoperable debido a las
características del paciente en el que se produce. Por
tanto, en todos los casos, se debe relativizar la relevan-
cia del apósito, cuya elección corresponde mucho más
al médico que al cirujano plástico. Los apósitos actuales,
que carecen de beneficios reales para las heridas agudas
(en las que no acortan la evolución), sólo son un factor
de gasto adicional en el que hay que sopesar cuidado-
samente las indicaciones. Nunca se debe perder de vista
que, con independencia del apósito prescrito, la herida
cicatrizará en pacientes sanos y que la velocidad de
cicatrización no tiene ninguna relación con el precio del
apósito.
Material necesario y suficiente
En los tres estadios de la cicatrización, basta tan sólo
con la vaselina, en pomada bajo una compresa y/o en
tul, asociada a la limpieza con agua del grifo y con
jabón de Marsella. Es un producto barato y sólo es
perjudicial a largo plazo, porque irrita la piel sana
vecina.
• En el estadio de detersión supurada, su mecanismo de
acción sería doble: estimulación de la reacción infla-
matoria del organismo por una parte y estimulación
de la proliferación microbiana local por otra, al
mantener un ambiente cálido y húmedo sobre la
herida. El apósito debe cambiarse a diario, tanto para
la eliminación del pus (agua del grifo mediante ducha
o, en su defecto, suero fisiológico con jeringa o con
un frasco de plástico para lograr un efecto mecánico)
como para vigilar la evolución. La técnica terapéutica
adecuada consiste en acelerar la velocidad de deter-
sión espontánea mediante la escisión mecánica de los
tejidos necrosados
[6]
, con bisturí o tijeras. Esto se
realiza sin anestesia, es totalmente indoloro y no
provoca hemorragia, pues la escisión adecuada se
lleva a cabo entre los tejidos necrosados y los tejidos
vivos. No obstante, sólo es posible después de un
cierto período de evolución de la detersión espontá-
nea, que es variable según la localización y la inten-
sidad de la necrosis.
• En el estadio de granulación, la vaselina actúa por su
acción proinflamatoria. Por desgracia, las pomadas de
corticoides han sustituido al tul de corticoides. Están
indicadas cuando el nivel del tejido de granulación
sobrepasa al de la piel vecina. Se extienden sobre
compresas grasas (tules o interfases) y se dejan apli-
cadas menos de 24 horas.
• En el estadio de epitelización, la vaselina sólo debe
aplicarse en una capa fina, en forma de tul, todos los
díasocada2o3días, vigilando de forma regular el
aspecto del tejido de granulación.
Tanto si la cicatriz es secundaria a una cicatriz diri-
gida o a una sutura (simple o de un injerto o colgajo),
el único consejo indispensable es que debe protegerse
del sol mientras tenga un color rojo, es decir, durante
un período variable de 6 meses a 2 años. El riesgo de
una exposición solar prematura es la aparición de una
discromía definitiva. Esta protección solar puede efec-
tuarse de forma muy eficaz con una crema solar de tipo
«pantalla total» de índice máximo, que se aplica cada
2 horas. También existen protecciones en forma de
barra. Todos los demás métodos de protección son
complementos útiles, y varían según la localización de
la cicatriz (sombrero, camiseta, pantalón, etc.).
Todos los demás métodos recomendados para tratar
las cicatrices recientes sólo tienen una utilidad de ritual,
cuya eficacia no se ha demostrado, pero no se debe
pasar por alto su beneficio psicológico, que puede ser
muy significativo en muchos pacientes.
Material opcional: apósitos modernos
El esquema clásico precedente admite múltiples
variantes, en ocasiones bastante originales (azúcar en
polvo o miel), pero a menudo caras, sin un beneficio
demostrado en las heridas que experimentan una verda-
dera cicatrización. Por tanto, esta lista, que corresponde
más al médico que al cirujano, se presenta en este
artículo como elemento de cultura general de este
último y para proporcionarle argumentos en las conver-
saciones con sus enfermeras o farmacéuticos. Al contra-
rio que los médicos, que son los especialistas de las
heridas crónicas que no cicatrizan, el cirujano plástico
es el especialista de las heridas que sí lo hacen. Esto
debe proclamarlo con claridad y no dejar su puesto
vacío en las reuniones dedicadas a tomar decisiones
sobre los apósitos.
Se puede utilizar el siguiente material
[5]
.
Tules e interfases
Según si su mallado es grande o pequeño, se distin-
guen los «tules» clásicos (compresas) y las «interfases»
(fibras sintéticas). Todos ellos están impregnados por un
elemento graso, que suele ser vaselina. A las mallas
grandes se les reprocha el que favorecen el arranca-
miento del tejido de granulación y que su retirada es
dolorosa en ocasiones, aunque ésta es una crítica
realizada por personas que no realizan una prescripción
adecuada. Si el tul arranca el tejido de granulación, es
porque se ha dejado colocado varios días sin vigilar la
herida, lo que es muy criticable. Por otra parte, al igual
que un grosor de una sola compresa desplegada no
basta para realizar un apósito seco, un único grosor de
tul no es suficiente para un apósito graso. Siempre hay
que colocar varias capas e incluso añadir vaselina si no
hay bastante. Incluso con muchas capas y con mucha
Cicatrización dirigida
¶
E – 45-050
3Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
vaselina, un apósito graso clásico sigue siendo mucho
más barato que las otras variedades de apósitos e igual
de eficaz que ellos.
Hidrocoloides
Son polímeros de carboxi-metil-celulosa (CMC) sobre
una película o una espuma de poliuretano, de poliéster
o de poliamida oclusiva o semioclusiva. Son adhesivos
y deben dejarse colocados varios días, hasta que la
ampolla llegue a sus bordes, momento en el que deben
cambiarse. Son simples de utilizar, impermeables al agua
y absorben las secreciones. No obstante, huelen mal y
tienen un color desagradable en el momento del cam-
bio, porque se disuelven en la herida como el pus.
Pueden provocar maceración y eccema. Por último, el
hecho de no cambiarlos durante varios días hace que
sean más adecuados para la fase de epidermización que
a la de detersión o de granulación, que se deben vigilar
a diario. Existen numerosas presentaciones comerciales
(cremas, placas más o menos delgadas, anatómicas u
opacas).
Hidrocelulares
Se trata de una espuma de poliuretano o de poliacri-
lato recubierta por una película de poliuretano semiper-
meable, adhesiva o no. Son apósitos opacos, no
adherentes y tienen un alto poder absorbente (10 veces
su peso). Al contrario que los anteriores, no se disuelven
en contacto con la herida y no emiten un olor desagra-
dable. No obstante, son mucho más caros. Existen
numerosas presentaciones comerciales.
Hidrogeles
Son polímeros insolubles de hidrocoloides (CMC) que
contienen al menos un 75% de agua. Liberan el agua
que contienen a la herida y requieren un apósito
secundario poco absorbente (película).
Alginatos
Los alginatos son extractos de algas marinas y contie-
nen ácido gulurónico o manurónico asociado o no a
CMC. Son hemostáticos, tienen un alto poder de reab-
sorción (10-15 veces) y no se disuelven en la herida.
Pueden ser útiles en cirugía plástica, bien en las heridas
hemorrágicas o bien en las heridas infectadas y
exudativas.
Hidrofibras
Las hidrofibras son fibras de CMC con un alto poder
de absorción (30 veces su peso). La capacidad de absor-
ción es superior a la de los alginatos. En contacto con
los exudados, el producto se transforma en un gel
húmedo cohesivo.
Carbones
Se trata de carbón activado envuelto en una lámina
no tejida y no adherente, asociada o no a plata (anti-
bacteriana). Este apósito tiene una capacidad de absor-
ción moderada de las secreciones y su propiedad
principal es la absorción de los malos olores.
Apósitos argénticos
La plata tiene una actividad antibacteriana de amplio
espectro. En la actualidad están muy desarrollados, pero,
por desgracia, no se ha demostrado ningún beneficio. O
bien tienen una actividad antiséptica, en cuyo caso no
hay más motivos para utilizarlos que los antisépticos
líquidos o los antibióticos, o bien carecen de ella, de
modo que su sobrecosto no está justificado. No se
deben confundir con la pomada de sulfadiazina argén-
tica, que se muy útil, sobre todo en los pacientes
quemados.
Películas semipermeables
Son películas adhesivas de poliuretano transparente,
no absorbente y semipermeable (permeable al oxígeno y
al vapor de agua e impermeable al agua y a las bacte-
rias). Se utilizan más como apósito secundario que
como apósito primario.
Presión negativa
Aunque el principio de los apósitos usados bajo
presión negativa (APN) data del siglo XIX
[7, 8]
, fueron
los equipos rusos quienes publicaron por primera vez las
aplicaciones clínicas de esta técnica a partir de la década
de 1970. En 1989, Chariker y Jeter
[9]
publicaron una
técnica de APN utilizando el vacío mural con un dre-
naje de silicona adyacente a las compresas de gasa
simples y con una membrana semipermeable cubriendo
la herida. A partir de la publicación de Morykwas y
Argenta en 1997
[10]
el procedimiento se difundió y se
utilizó de forma comercial a escala mundial
[7, 11]
.
Los APN se basan en el principio de la equimosis por
succión: además de la aspiración de los exudados
abundantes, la aplicación continua o discontinua de
vacío aumenta el flujo sanguíneo a nivel de dicha
aplicación, tanto en la piel sana como en una herida. Al
mejorar la vascularización, favorece la granulación de
una pérdida de sustancia cutánea, siempre que el lecho
esté bien vascularizado. Es inútil esperar la granulación
de un lecho desvascularizado tanto aplicando vacío
como recubriéndola con un apósito graso.
Además de la inducción de la formación de un tejido
de granulación por el estrés mecánico que estimula las
mitosis y que aumenta la neovascularización, se atri-
buye también a esta técnica una reducción del edema y
del exudado, así como una reducción de la colonización
bacteriana.
Las APN, que tienen como objetivo estimular la
granulación, están contraindicadas en el estadio de
detersión supurada. Por último, no deben considerarse
como un procedimiento de cobertura, sino como una
variedad de apósito que puede servir de preparación a
ésta.
■ Indicaciones
Una cuestión destacada es determinar el momento de
proponer una cicatrización dirigida y qué materiales
utilizar para ello.
Indicaciones de la cicatrización
dirigida
La cicatrización dirigida es tan sencilla y eficaz que
merece ser propuesta por el cirujano siempre que sea
posible, es decir, siempre que una pérdida de sustancia
no sea suturable pero que su lecho esté correctamente
vascularizado, sin una exposición de órganos nobles.
Topografía
Algunas localizaciones son excelentes indicaciones
para la cicatrización dirigida.
• Cuero cabelludo.
• Cráneo desperiostizado, siempre que sea el propio
cirujano el que haya eliminado el periostio del hueso
y que haya impedido de inmediato que éste se seque
en contacto con el aire (paños húmedos durante la
intervención y vaselina después de la misma). Los
cuidados de enfermería diarios consisten a continua-
ción en evitar esta desecación más allá de 1 minuto
y en hacer macerar el hueso bajo un apósito hiper-
graso oclusivo (abundante vaselina y lámina de
envoltorio del tul graso). El hueso desperiostizado
granulará y se epidermizará de forma espontánea o se
injertará, dependiendo de sus dimensiones (
Fig. 1).
E – 45-050
¶
Cicatrización dirigida
4 Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
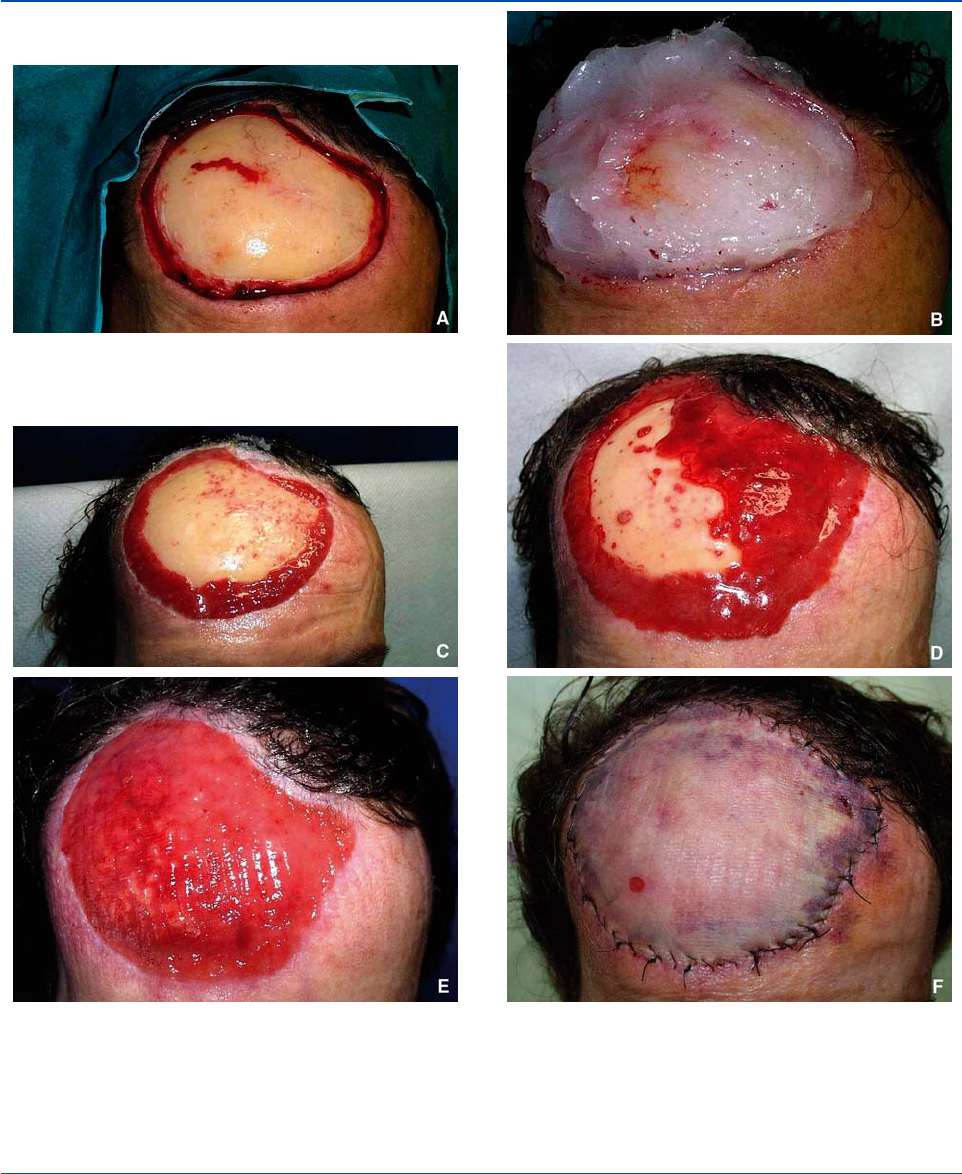
Figura 1. Un hueso desperiostizado puede granular y someterse a un injerto. La cicatrización dirigida permite preparar el lecho de un
injerto.
A. Exéresis de un carcinoma basocelular esclerodermiforme de la región frontal. La exéresis engloba el periostio en profundidad.
B. El hueso desperiostizado se recubre de inmediato con vaselina para evitar su desecación.
C. El hueso desperiostizado comienza a granular.
D. El tejido de granulación progresa.
E. A los tres meses del desbridamiento, todo el hueso está recubierto de tejido de granulación.
F. De este modo, se puede colocar un injerto y resolver con gran sencillez el problema de la cobertura cutánea.
Cicatrización dirigida
¶
E – 45-050
5Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
• Frente: en especial, las zonas donantes de un colgajo
frontal con pedículo inferior pueden dejarse curar por
cicatrización dirigida en su parte distal no suturable,
con un resultado estético muy bueno.
• Sienes (
Fig. 2).
• Región cantal interna, sobre todo si la pérdida de
sustancia se sitúa de un modo casi simétrico respecto
a la línea horizontal que pasa por el ángulo del ojo.
• Nariz. La punta es una indicación excelente de
cicatrización dirigida, siempre que la pérdida de
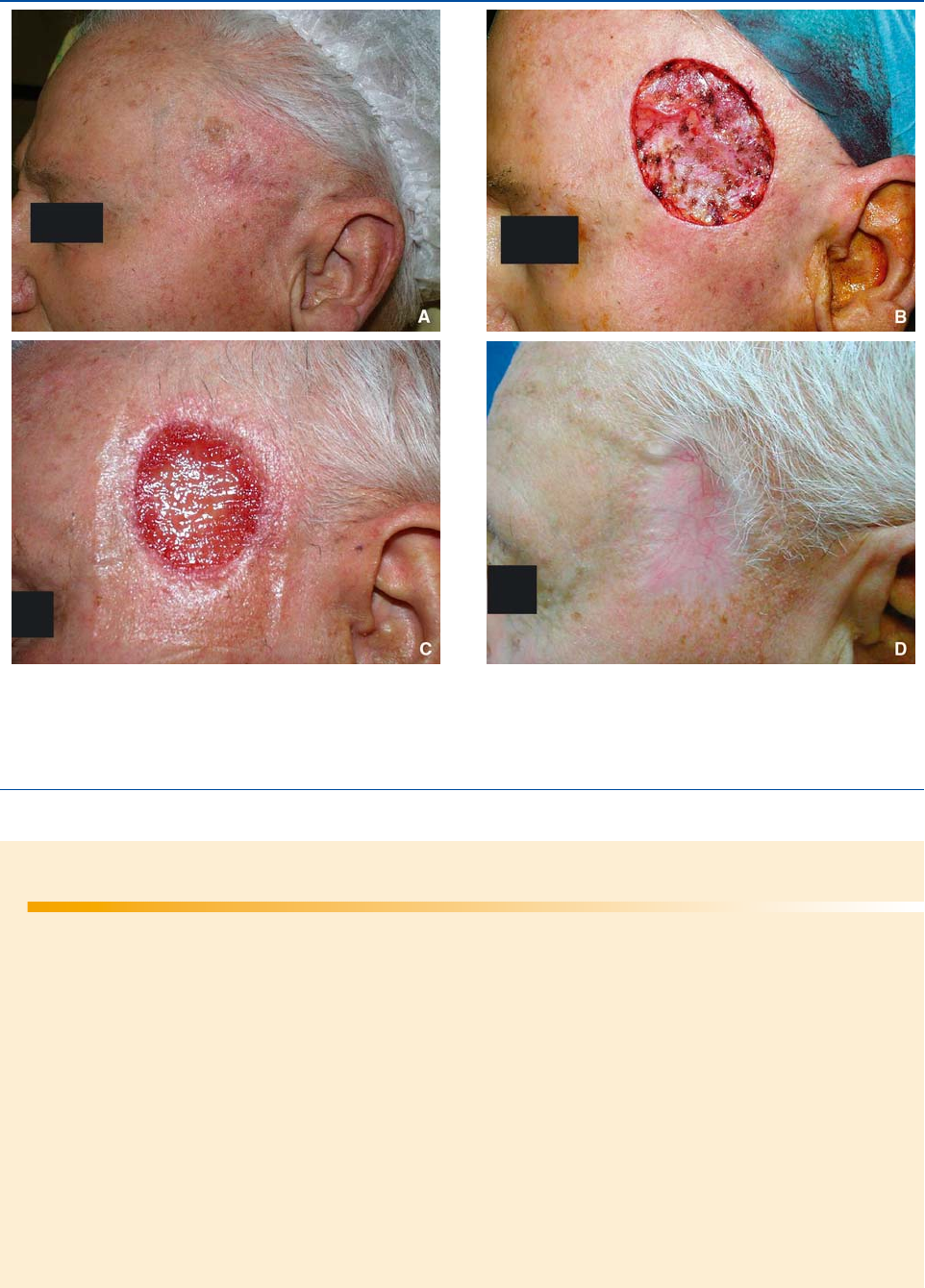
Figura 2.
A. Carcinoma de la sien izquierda. Una vez informado de la duración previsible de la cicatrización espontánea (2 meses), el paciente no
deseaba someterse a un injerto cutáneo.
B. Exéresis bajo anestesia local y apósito graso.
C. Aspecto a los 29 días.
D. Resultado después de 1 año.
“ Punto importante
Apósito de medio húmedo
Todos los fabricantes de apósitos modernos se refieren desde el punto de vista comercial al «medio húmedo», cuya
superioridad sobre la cicatrización al aire libre («medio seco») se ha demostrado de forma definitiva desde la década
de 1960 por los estudios de Winter en cerdos y de Hinman y Maibach en el ser humano
[12]
. No se pretende aquí
refutar esta afirmación, sino matizarla. Basta para ello conseguir el artículo original de Hinman, publicado en la
prestigiosa revista Nature, y leerlo para convencerse de su fragilidad extrema. Es indudable que no tendría la más
mínima posibilidad de ser publicado en la actualidad en cualquier revista. Este artículo de dos páginas expone los
resultados de una serie de siete casos, realizada con siete voluntarios de la prisión de San Quintín en California. Cada
caso era su propio control. Se realizaron dos heridas superficiales de 0,5 cm
2
bajo anestesia local en la cara interna del
brazo, respetando la dermis profunda. Una herida se dejó al aire y la otra se recubrió con una película de polietileno
estéril. Después, se realizó una biopsia en sacabocados a los 3, 5,7y9días. Al 7.° día, todas las heridas estaban
epitelizadas, tanto si habían estado expuestas al aire como si no. La diferencia entre los dos modos de tratamiento era
de orden cualitativo y no cuantitativo.
En conclusión, es incontestable que la cicatrización se produce en un medio húmedo, pero también puede tener
lugar en un medio seco, lo que es una posibilidad natural que debe tenerse en cuenta sin sectarismo, en algunos
casos bien seleccionados de pérdidas de sustancia superficiales de la dermis. Basta para ello dejar que se forme la
costra en la herida expuesta al aire y vigilar a continuación la ausencia de supuración bajo la misma.
E – 45-050
¶
Cicatrización dirigida
6 Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
sustancia no afecte a la base (triángulos blandos,
columela, alas) y que los cartílagos alares no estén
expuestos (
Fig. 3). La región del pie del ala de la nariz
y de su confluencia con la mejilla y el surco nasoge-
niano también constituye una buena indicación
(
Fig. 4).
• El pulpejo de los dedos es una indicación excelente
para la cicatrización dirigida, que evita el dolor de la
anestesia local y las cicatrices suplementarias de los
clásicos colgajos locales descritos en esta región. La
palma de las manos también es una indicación muy
buena de cicatrización dirigida (cf el método de
McCash denominado «de la palma abierta» en el
tratamiento de la enfermedad de Dupuytren).
• Periné. Tanto si es de forma deliberada o si es preciso
tras la pérdida más o menos extensa de un injerto
cutáneo, la cicatrización dirigida es un buen método
a nivel perineal, incluida la región lateroanal, a
condición de que la pérdida de sustancia sea de
tamaño moderado. Si la pérdida de sustancia es
extensa, la cicatrización dirigida permite preparar el
lecho para un injerto.
• Axilas. Después de la exéresis de la zona pilosa de la
axila por una hidrosadenitis supurada, la cicatrización
dirigida permite una curación sin secuelas, a condi-
ción de vigilar que no se produzca una limitación de
la abducción del brazo durante toda su duración, que
es prolongada (alrededor de 2,5 meses).
• Sacro. La cicatrización dirigida es una indicación
excelente tras la exéresis de un sinus pilonidal.
Patología
En todas las enfermedades tegumentarias habituales
puede emplearse la cicatrización dirigida.
• Traumatismos.
• Tumores (después de la exéresis quirúrgica).
• Infecciones (después del desbridamiento), en especial
las infecciones postoperatorias.
Características del paciente
Algunas personas, una vez informadas adecuada-
mente de sus ventajas e inconvenientes, prefieren evitar
de forma deliberada un injerto o un colgajo cuando es
posible realizar una cicatrización dirigida.
Método definitivo o preparatorio
La cicatrización dirigida puede utilizarse a modo de
método de cobertura definitiva cuando la pérdida de
sustancia no tiene una superficie demasiado grande o
cuando no se localiza en una zona funcional (pliegue de
flexión, orificio). Esto es especialmente útil en la cirugía
dermatológica del rostro (
Figs.2a4). También se puede
utilizar de forma provisional antes de un injerto cutáneo
o de un colgajo:
• o bien a la espera de un resultado histológico defini-
tivo después de haber extirpado un tumor o para
esperar una consulta especializada después de la
estabilización de una fractura abierta de la pierna;
• o para permitir que el lecho granule y pueda injer-
tarse (Fig. 1);
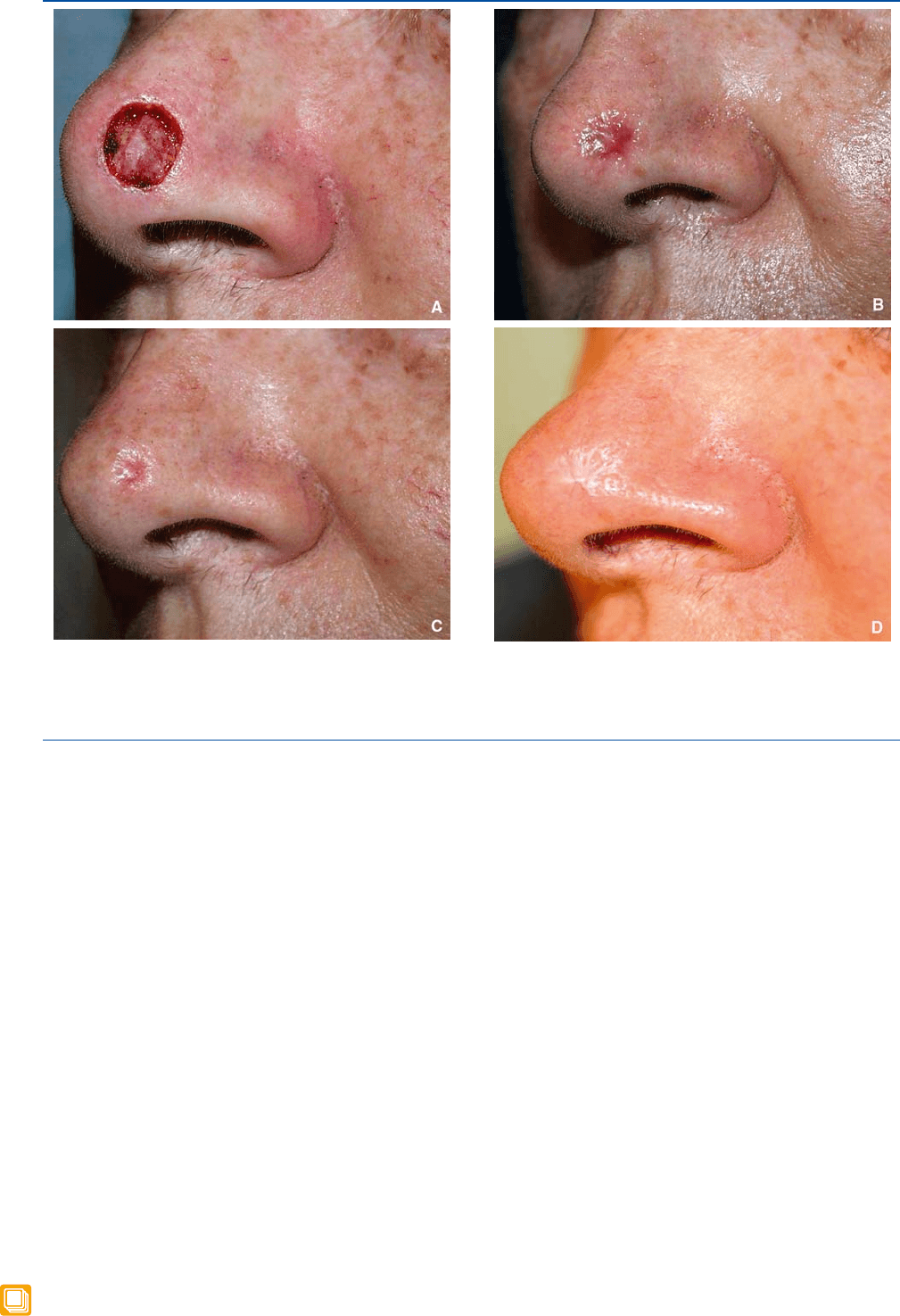
Figura 3. Carcinoma basocelular de la punta nasal.
A. Desbridamiento.
B. 17.° día.
C. 29.° día.
D. Resultado después de 1 año.
.
Cicatrización dirigida
¶
E – 45-050
7Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
• o bien para aprovechar la retracción del tejido de
granulación y reducir así la superficie de la herida
antes de cubrirla (
Fig. 5).
Límites
Los límites esenciales de la cicatrización dirigida
derivan tanto de la localización como de la superficie de
la pérdida de sustancia.
Localización
La cicatrización dirigida debe evitarse de forma
deliberada en algunas zonas del cuerpo, donde la
retracción no es deseable.
• Párpados y región periorbitaria, a excepción de la
región cantal interna, en la cara lateral de la raíz
nasal.
• Base de la nariz: alas, columela y triángulos blandos.
• Mentón, labios, mejillas (salvo cerca del pie del ala
nasal).
• Orejas.
• Cuello.
• Pliegues de flexión (pilares de la axila, pliegue del
codo, muñeca, región poplítea, tobillo).
• Mamas.
• Dorso de las manos (por motivos estéticos), dorso de
los pies (por motivos funcionales).
Superficie
Para no crear retracciones cicatrizales excesivas, la
superficie de la pérdida de sustancia debe ser «mode-
rada». Este concepto depende de cada localización. Sin
embargo para fijar los conceptos y además de en las
zonas precedentes, se puede decir que una pérdida de
sustancia no suturable de 2-3 cm de diámetro puede
dejarse casi siempre que cure por cicatrización dirigida
sola y que el período de epidermización será de
6-8 semanas a partir de la creación quirúrgica de la
pérdida de sustancia.
Características del paciente
El paciente, una vez informado adecuadamente de las
ventajas e inconvenientes del método, puede preferir un
injerto o un colgajo.
Indicaciones de los apósitos
Si por cualquier motivo los apósitos grasos tradicio-
nales no bastan al cirujano o al personal de enfermería,
también se pueden utilizar los siguientes apósitos,
dentro de los límites económicos del centro:
• en el estadio de detersión supurada: alginatos e
hidrofibras, carbón, hidrocoloides, hidrogeles;
• en el estadio de granulación: interfases, hidrocoloides
delgadas o hidrocelulares, hidrogeles, hidrofibras o
alginatos en caso de exudados abundantes;
• en el estadio de epidermización: hidrocelulares o
hidrocoloides en placas delgadas, dejando el apósito
durante varios días, películas semipermeables e
interfases.
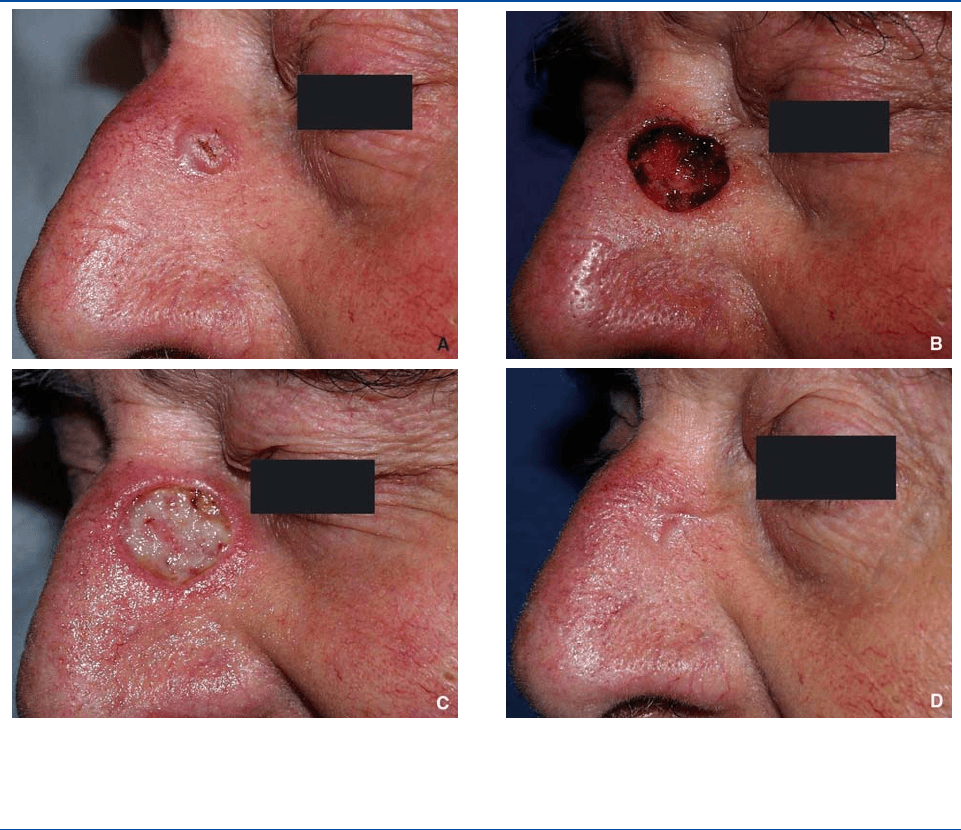
Figura 4.
A. Carcinoma de la cara izquierda de la raíz nasal.
B. Exéresis bajo anestesia local y apósito graso.
C. Aspecto a los 9 días.
D. Resultado después de 1 año.
E – 45-050
¶
Cicatrización dirigida
8 Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
Casos especiales de los apósitos
con presión negativa
La indicación principal de los APN corresponde a las
pérdidas de sustancia no suturables y mal vasculariza-
das, para favorecer su granulación final y permitir de ese
modo su epidermización espontánea, o bien injertarlos
de forma secundaria o realizar un colgajo. Este método
parece tener una utilidad cierta en las mediastinitis
después de la cirugía cardíaca, sobre todo cuando las
arterias torácicas internas se han utilizado para la
revascularización coronaria. Además del drenaje, mejora
de forma indudable la revascularización de la región y
permite realizar los posibles desbridamientos óseos
secundarios necesarios en mejores condiciones antes o
durante una reparación con un colgajo local, que
siempre es indispensable.
Por tanto, las indicaciones de los APN en el contexto de
la cicatrización son exactamente las mismas que las de los
apósitos grasos tradicionales. Sin embargo, las ventajas e
inconvenientes no se conocen aún con precisión y
objetividad. Al igual que en los otros tipos de apósitos,
se trata de un ámbito en el que los intereses comerciales
de los fabricantes interfieren sin duda alguna de forma
considerable con la independencia científica de los
médicos que los prescriben.
En cualquier caso, al igual que sucede con los apósi-
tos, los APN sólo son un procedimiento complementa-
rio en el método de la cicatrización dirigida, por lo que
no deben confundirse con un procedimiento suplemen-
tario de cobertura de las pérdidas de sustancia.
■ Bibliografía
[1] Monaco JL, Lawrence WT. Acute wound healing. An
overview. Clin Plast Surg 2003;30:1-2.
[2] Robson MC. Cytokine manipulation of the wound. Clin Plast
Surg 2003;30:57-65.
[3] Leahy PJ, Lawrence WT. Biologic enhancement of wound
healing. Clin Plast Surg 2007;34:659-71.
[4] Heggers JP. Assessing and controlling wound infection. Clin
Plast Surg 2003;30:25-35.
[5] Morin RJ, Tomaselli NL. Interactive dressings and topical
agents. Clin Plast Surg 2007;34:643-58.
[6] Knox KR, Datiashvili RO, Granick MS. Surgical wound bed
preparation of chronic and acute wounds. Clin Plast Surg
2007;34:633-41.
[7] Danino A. Pansement à pression négative : plaidoyer pour un
pluralisme nécessaire à la réflexion scientifique. J Chir (Paris)
2007;144:464-6.
[8] Glicenstein J. Jules Guérin (1801-1885) et l’occlusion
pneumatique des plaies. Ann Chir Plast Esthet 2008;53:
378-82.
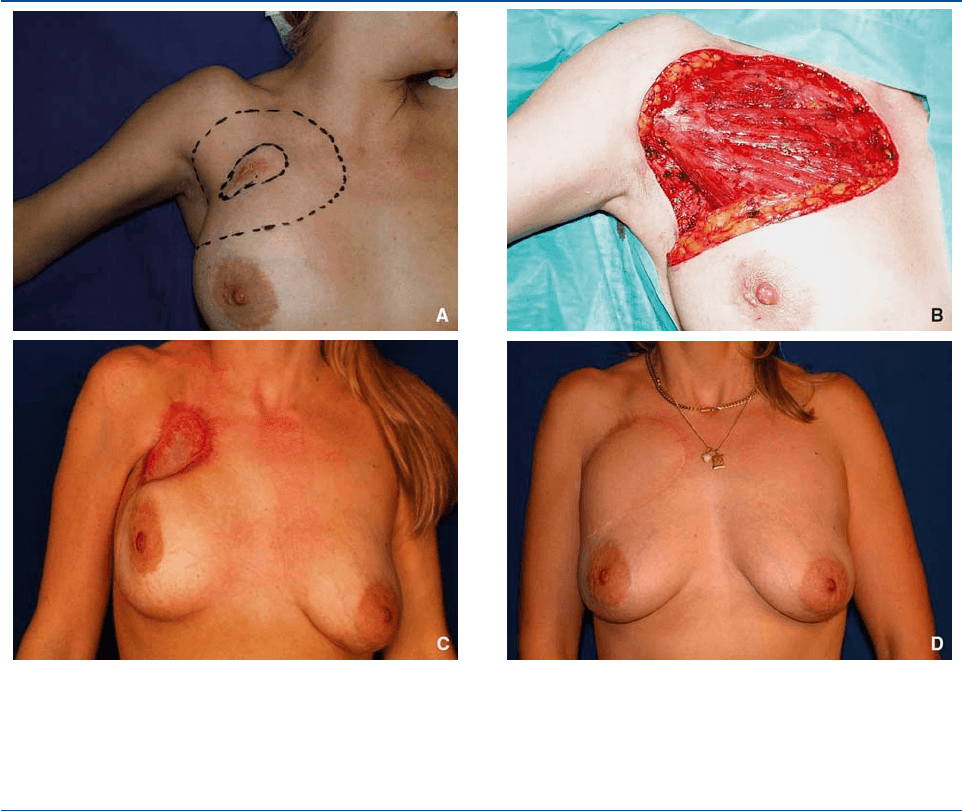
Figura 5. La cicatrización dirigida previa permite reducir la superficie que debe cubrirse con un injerto.
A. Dermatofibrosarcoma de Darier y Ferrand del surco inframamario derecho.
B. Exéresis amplia del tumor que pasaa5cmenlasuperficieyengloba la aponeurosis pectoral en profundidad.
C. La pérdida de sustancia se deja cicatrizar de forma dirigida, primero para lograr el resultado histológico y después para aprovechar la
retracción.
D. Un colgajo de dorsal ancho (cuya zona donante puede cerrarse de forma directa) puede resolver con sencillez el problema de la
cobertura cutánea.
Cicatrización dirigida
¶
E – 45-050
9Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.

[9] Chariker ME, Jeter KF, Tintle TE, Bottsford Jr. JE. Effective
management of incisional and cutaneous fistulae with closed
suction wound drainage. Contemp Surg 1989;34:59-63.
[10] Morykwas MJ, Argenta LC, Shelton-Brown EI, McGuirt W.
Vacuum-assisted closure: a new method for wound control
and treatment: animal studies and basic foundation. Ann Plast
Surg 1997;38:553-6.
[11] Miller MS, Lowery CA. Negative pressure wound therapy: ″a
rose by any other name″. Ostomy Wound Manage 2005;51:
44-9.
[12] Hinman CD, Maibach H. Effect of air exposure and occlusion
on experimental human skin wounds. Nature 1963;200:
377-8.
Para saber más
Kremlin Papers. Traduits en anglais et regroupés sur le site Internet
de BlueSky Medical : www.blueskymedical.com/Portals/0/
LBL-00221-01-
AA%20Reprint,%20Kremlin%20Papers.pdf.
www.o-wm.com/article/3815.
J.-M. Servant, Professeur des Universités.
Service de chirurgie plastique, Hôpital Saint-Louis, 75475 Paris cedex 10, France.
Cualquier referencia a este artículo debe incluir la mención del artículo original: Revol M., Servant J.-M. Cicatrisation dirigée. EMC (Elsevier
Masson SAS, Paris), Techniques chirurgicales - Chirurgie plastique reconstructrice et esthétique, 45-050, 2010.
Disponible en www.em-consulte.com/es
Algoritmos Ilustraciones
complementarias
Vídeos /
Animaciones
Aspectos
legales
Información
al paciente
Informaciones
complementarias
Autoevaluación Caso
clínico
E – 45-050
¶
Cicatrización dirigida
10 Cirugía plástica reparadora y estética
Descargado de ClinicalKey.es desde Universidad Nacional Autonoma de Mexico agosto 09, 2016.
Para uso personal exclusivamente. No se permiten otros usos sin autorización. Copyright ©2016. Elsevier Inc. Todos los derechos reservados.
Cicatrización-dirigida.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.