

Índice
Coordinación:
Jorge Baldoni
Autores:
Guillermo Alonso
Jorge Baldoni
Carlos Belluscio
Claudio Jensen
Mónica Rodríguez
3
Diseño y compaginación: Julio Mendez
© Editorial CCC Educando
Av. Warnes 2361/5 (1417)
Capital Federal
Con una tirada 500 ejemplares
Impreso en Argentina
Queda hecho el deposito que previene
la ley 11.723
ISBN: 978-987-3665-33-2
No se permite la reproduccion total o parcial
de este libro, ni su almacenamiento en un
sistema informatico, ni su transmision en
cualquier forma o por cualquier medio,
electronico, mecanico, fotocopia, u otros
metodos, sin el permiso previo del editor.
Biología celular : bionergética y enzimas / Jorge Baldoni ... [et al.] ;
coordinación general de Jorge Baldoni. - 1a edición para el alumno. -
Ciudad Autónoma de Buenos Aires : C.C.C. Educando, 2017.
44 p. ; 20 x 15 cm.
ISBN 978-987-3665-33-2
1. Biología Celular. I. Baldoni, Jorge II. Baldoni, Jorge, coord.
CDD 571.6
Presentación
La presente colección de “Introducción a la Biología celular y molecular” ha sido elaborada
por cada uno de los profesores coordinadores del Departamento de Ciencias Biológicas, con
sus respectivos equipos docentes.
Sobre la base de un grupo de trabajo interdisciplinario, con amplia experiencia en la ense-
ñanza, en la investigación cientíca y educativa y, en la particular intersección entre la Escuela
Secundaria y la Universidad, se genera la necesidad de brindar un material de lectura adaptado
al perfil de los estudiantes que ingresan al CBC, con una mirada puesta en los conocimientos y
habilidades intelectuales, necesarios para afrontar la demanda de las futuras carreras, en cada
una de las facultades.
La Biología celular y molecular contemporánea se caracteriza por atravesar un período de
enorme crecimiento tanto en los métodos, como en las técnicas y resultados que requieren de
una actualización adecuada, que permita ese tránsito entre la formación recibida en la escuela
secundaria y los primeros tramos del ciclo profesional.
Por ello, presentamos esta segunda edición que recoge la experiencia obtenida con la edi-
ción anterior, las sugerencias de alumnos y colegas, y que ofrece la posibilidad de despertar en
el alumno el interés por saber y de impulsarlo a esforzarse para lograr un aprendizaje profundo.
En esta oportunidad, contamos con la invalorable colaboración de la Lic. Adriana Schnek
que con mucha habilidad y profesionalismo asumió el rol de revisora y editora. También
nuestro agradecimiento a Adriana García que coordinó las ilustraciones efectuadas por
Eduardo de Navarrete y David Gonzalez Marquez, que tanto ayudan a la comprensión de los
distintos temas.
Índice
Bioenergética y Enzimas
Energía 3
1. El concepto de energía 3
1.1 La energía no puede ser creada ni destruida 4
1.2 Cambio de estado de un sistema y variación de energía 4
1.3 ¿Cómo puede ganar o perder energía un sistema? Trabajo (W) y Calor (Q) 5
1.4 Energía, calor y trabajo: Entalpía (H) 5
1.5 La energía es la capacidad de realizar trabajo 7
1.6. ¿Qué ocurre con la porción de energía “inútil”? Entropía (S) 7
1.7. ¿Cómo relaciona la termodinámica estos cambios de energía? 7
1.8 ¿Es posible revertir un proceso espontáneo? 8
El individuo como sistema termodinámico- leyes de la termodinámica 9
2. Bioenergética 9
2.1 La célula y la energía química 10
2.2 El ATP es un intermediario energético 10
3. Metabolismo celular 12
3.1 Catabolismo y anabolismo 13
3.2 El ATP como molécula integradora 13
4.Enzimas 15
17
19
19
21
21
22
25
4.1 Características de las enzimas
4.2 Clasificación de las enzimas
4.3 Reconocimiento del sustrato
4.4 Cinética enzimática
4.4.1. Factores que afectan la cinética enzimática
4.4.2. Efecto de la concentración de sustrato sobre la cinética enzimática
4.4.3. Efecto de la temperatura sobre la cinética enzimática
4.4.4. Efecto del pH sobre la cinética enzimática 26
5. Inhibición de la actividad enzimática 28
5.1 Inhibición reversible 28
5.2 Inhibición competitiva 29
5.3. Inhibición no competitiva 30
5.4 Inhibición irreversible 31
6. Regulación de la actividad enzimática 33
6. 1. Regulación de la actividad catalítica 34
6.2. Regulación de la síntesis de enzimas 40
6.3. Regulación de la degradación de enzimas 40
6.4 Multimodulación 41

Biología Celular
3
ENERGÍA
Al caracterizar a un ser vivo tenemos en cuenta sus funciones vitales básicas: autoconservación,
autorregulación y autoperpetuación. La autoconservación se lleva a cabo mediante un conjunto de pro-
cesos complejos en los que se obtiene y transforma energía. En este fascículo analizaremos las bases de
estos procesos y cómo se regulan, lo que permite la continuidad de la vida. De este modo, analizaremos
los conceptos fundamentales sobre energía, las leyes que permiten interpretar sus transformaciones y
cómo éstas operan en los seres vivos.
1. El concepto de energía
El concepto de energía es fundamental en las ciencias naturales. Sin embargo, no es de fácil defin -
ción. Es de uso frecuente, no sólo en las distintas ramas de la ciencia, sino en los distintos aspectos de la
sociedad humana. Por ejemplo, todos tenemos “conciencia” de la necesidad de la energía: un automóvil
requiere energía para circular, requerimos energía para caminar, etc. También sabemos que la nafta sumi-
nistra la energía para que el automóvil funcione o que los alimentos son indispensables pues proporcionan
la energía necesaria para mantener nuestras funciones; o que el sol nos da energía en forma de luz y calor.
La física define a la energía como la causa capaz de producir un trabajo. Esta energía puede ser poten-
cial, cuando un objeto almacena energía por su posición (un coche parado, una célula nerviosa en reposo);
cinética, cuando existe movimiento (el automóvil en movimiento, el espermatozoide en movimiento),
calórica (por ejemplo, desprendimiento de calor durante el trabajo muscular), eléctrica (por ejemplo, el
pasaje de iones a través de una membrana) o química (por ejemplo, la existente en las uniones de átomos
y moléculas).
La rama de la ciencia que estudia los cambios energéticos del universo es la termodinámica, término
griego que significa “movimiento del calor”. Este campo de estudio se ocupa solo de los aspectos macros-
cópicos de un sistema: temperatura, presión, volumen, trabajo, calor, desorden, etc. A partir de este marco,
se analizan fundamentalmente los cambios de energía que acompañan a un proceso en particular, en un
sistema determinado. No requiere del conocimiento acerca del contenido de energía del sistema sino de la
variación que se produce entre un estado inicial, antes del cambio, y un estado final, luego del cambio; lo
que se designa mediante la letra griega Δ (delta). Debe considerarse, además, que la termodinámica puede
suponer que un sistema es todo el universo o bien una parte de él, que se separa en forma teórica para
su estudio del entorno que lo rodea.
En relación con el entorno, el sistema en estudio puede ser:
aislado, si no permite intercambio alguno con ese entorno (por ej. un termo)
cerrado, permite el intercambio de energía pero no de materia (por ej. una pila electroquímica)
abierto, si permite el intercambio energía y materia (por ej. el cuerpo humano)

Bioenergética y Enzimas
4
1.1 La energía no puede ser creada ni destruida
La Ley de Conservación de la Energía, conocida como 1ª Ley de la Termodinámica, establece que
la energía no puede ser creada ni destruida. Si bien puede convertirse de una forma a otra, (es decir,
cualquiera sea el proceso considerado, la energía podrá cambiar de forma o transferirse de un lugar a
otro), la energía total (energía del sistema + energía del entorno) permanece constante.
Los ejemplos de transformaciones de energía son tantos como los procesos que existen en el univer-
so. No hay proceso de cambio sin transformación energética. Así, al quemar gas, la energía química que
contienen las moléculas que lo componen se transforma en energía térmica produciendo calor, capaz de
calentar agua.
De forma análoga, la energía química presente en las moléculas de los hidratos de carbono y lípidos
almacenados en las células es utilizada en reacciones químicas permitiendo que se lleven a cabo sus fun-
ciones vitales. En dichos procesos también se libera energía térmica. Los átomos mismos son paquetes de
energía transformable. La fusión de los núcleos de átomos de hidrógeno forma átomos de helio, produci-
dos en el interior de ese gran reactor nuclear que es el sol. Este proceso genera energía radiante, la que al
llegar a la Tierra es, en parte, absorbida por las plantas mediante el proceso de fotosíntesis, convertida en
energía eléctrica y posteriormente en energía química, como se verá más adelante.
1.2 Cambio de estado de un sistema y variación de energía
Cualquiera sea el sistema que se considere –gaseoso, líquido o sólido– la cantidad total de energía que
gana o pierde al cambiar de un estado definido a otro estado definidoes la misma, independientemente del
camino seguido. Si por ejemplo se considera un sistema y se produce un cambio del estado A al estado B,
al invertirse el cambio del estado B al A, independientemente del camino seguido, la variación de
energía debe ser la misma. Si llamamos E
A
y E
B
a los respectivos valores de la energía del sistema en
los dos estados considerados, la variación de energía cuando se pasa del estado A al B será:
Δ E = E
B
– E
A
De acuerdo con lo expresado, si una piedra cae de la cima de una montaña desde una cierta altura,
liberando energía,
se requerirá de una cantidad de energía equivalente para volverla a poner en la cima,
lo que será independiente de si se la lleva rodando por un camino o se la levanta mediante una grúa.
Análogamente, si se quema glucosa mediante una llama hasta convertirla en dióxido de carbono y agua,
liberará la misma cantidad de energía que cuando el proceso se realiza en una célula. De igual manera, la
cantidad de energía necesaria para formar glucosa por medios químicos, será idéntica a la que requiere
una célula vegetal para fabricarla. Esto último es una ventaja para el experimentador, pues permitirá, por
ejemplo, medir la energía que se produce al quemar glucosa, externamente, mediante el uso de un dispo-
sitivo adecuado, y ésta será la misma que se libera cuando la célula la degrada. Por supuesto, no será lo
mismo quemar o fabricar una sola molécula de glucosa que muchas; la energía del sistema dependerá de
la cantidad de sustancia que contiene y si la cantidad de sustancia cambia, la energía del sistema variará
también proporcionalmente.

Biología Celular
5
1.3 ¿Cómo puede ganar o perder energía un sistema? Trabajo (W) y Calor (Q)
Cuando un sistema cambia de un estado a otro puede perder o ganar energía bajo dos formas: calor
y trabajo. Esa ganancia o pérdida de energía la hará a expensas del entorno. La física define el trabajo
mecánico, simbolizado por la letra W, como una magnitud (con unidades de energía) resultante de la apli-
cación de una fuerza a través de una distancia dada. Matemáticamente, esto se expresa como el producto
de la fuerza por el desplazamiento.
A su vez, este producto tiene un signo (positivo o negativo) dependiendo de la coincidencia o no entre
el sentido de aplicación de la fuerza y el sentido del desplazamiento. Por ejemplo, cuando empujamos
un objeto pesado el sentido de aplicación de la fuerza coincide con el sentido del movimiento del objeto.
Más generalmente, en un sistema determinado el trabajo, por convención, se considera positivo si es
realizado por el sistema y negativo si es realizado por el entorno sobre el sistema.
El calor, una de las formas de energía, se transmite de un cuerpo a otro cuando existe una diferencia de
temperaturas entre ambos. El calor se designa con la letra Q, siendo positivo cuando es absorbido desde
entorno y negativo (-Q), si se desprende del sistema hacia el entorno.
¿Qué ocurre con la energía total de un sistema (también llamada energía interna del sistema) cuando
éste sufre un cambio de estado?
Una consecuencia natural de la Primera Ley de la Termodinámica es que, si el sistema está aislado,
la energía interna que contiene debe permanecer constante. Si por el contrario el sistema no está aislado,
y puede intercambiar energía con su entorno, deberá cumplirse que la variación de energía del sistema al
pasar de un estado a otro sea idénticamente igual al intercambio de energía entre el sistema y su entorno.
Aceptando que las únicas formas de producir ese intercambio son el calor y el trabajo, resulta:
Δ E = Q - W
de manera tal que la energía total del sistema más su entorno permanezca sin variación alguna. La
expresión anterior suele presentarse como la formulación matemática de la Primera Ley de la Termodi-
námica.
1.4 Energía, calor y trabajo: Entalpía (H)
Los sistemas materiales en cualquiera de sus estados (gaseoso, líquido o sólido) están constituidos por
átomos y moléculas en continuo movimiento. Según el estado en que se encuentren los átomos y molécu-
las el movimiento será mayor o menor; es decir tendrán distinta energía cinética, la que podemos sentir de
una forma que llamamos calor. Es necesario destacar que la materia no contiene calor propiamente dicho
sino que tiene energía en distintas formas, y esta energía puede transferirse de un sistema a otro en forma
de calor. La transferencia de calor será de un cuerpo a otro y se realizará siempre en forma espontánea del
cuerpo más caliente al más frío.
Si se entrega calor, los átomos y moléculas que constituyen el sistema en estudio tienden a separarse
produciendo una expansión, es decir, un aumento de volumen. Esto ocurre con la mayoría de los sistemas
materiales los que al calentarse tienden a expandirse y al enfriarse se contraen. En la construcción de
viviendas, por ejemplo, al realizarse una estructura de concreto, se deja un espacio libre para permitir la
expansión, de lo contrario se produce un resquebrajamiento o rajadura.

Bioenergética y Enzimas
6
Cuando la expansión (es decir, el aumento de volumen) se realiza contra una fuerza exterior que se
opone a la misma (como por ejemplo la presión exterior), y si consideramos que la presión exterior es
constante, el sistema, al recibir calor y expandirse, efectuará un trabajo que será igual al producto de la
fuerza (que, expresada por unidad de superficie, es la presión P) multiplicada por la distancia (la variación
de volumen ΔV) y según la Primera Ley de la Termodinámica:
ΔE = Q
P
- W ó ΔE = Q
P
- P ΔV
Estas expresiones indican que la variación de energía producida en el sistema al absorber una deter-
minada cantidad de calor del entorno estará equilibrada por el trabajo efectuado por el sistema el entorno.
Otra forma de expresarlo es que la cantidad de calor absorbido por el sistema es:
Q
P
= ΔE + P ΔV (1)
Si por otro lado el sistema absorbe calor, pero sin que exista variación de volumen, no efectuará
trabajo alguno.
ΔV = 0 y por lo tanto Δ E = Q
V
Es decir que el sistema incrementará su energía en una magnitud proporcional al calor que absorba.
Si por el contrario el sistema perdiera calor hacia el entorno, disminuiría la energía del mismo en forma
proporcional.
Cuando un sistema absorbe calor se dice que el proceso es endotérmico y si por el contrario libera
calor es exotérmico.
La variación de energía de un sistema depende, segn vimos, del estado inicial y final del mismo y no
de la condición previa ni del camino por el cual se realizó el proceso; si reemplazamos en la ecuación
(1) ΔE por E
2
– E
1
y ΔV por V
2
–V
1
(donde 1 y 2 indican los estados inicial y final, respectivamente,
de nuestro sistema, siempre considerando la presión como constante):
Q
P
= ΔE + P ΔV Q
P
= (E
2
– E
1
) + P (V
2
–V1) y Q
P
= (E
2
+ PV
2
) – (E
1
+ PV
1
)
donde el término E + PV representa el contenido calorífico, o entalpía, del sistema y se designa con
la letra H; de ello se desprende que:
Q
P
= H
2
– H
1
= ΔH
Esto significa que el aumento o disminución del contenido calorífico de un sistema será igual al calor
absorbido a presión constante: ΔH = ΔE + P ΔV y si no se efectúa trabajo alguno ΔH = ΔE
El término ΔH se utiliza generalmente para expresar la variación de calor en las transformaciones
de energía. Así una ΔH positiva (+) indicaría un cambio exotérmico y una ΔH negativa (–) un cambio
endotérmico.

Biología Celular
7
1.5 La energía es la capacidad de realizar trabajo: ¿toda la energía puede convertirse en
trabajo? Energía libre (G)
Retomando un ejemplo anterior, en un automóvil, al quemar un combustible como el gas, la presencia
de un dispositivo mecánico como un motor permite que se mueva. Parte de la energía del combustible,
mediante el calor que se genera en la combustión dentro del cilindro, se transforma en energía mecánica
pero una porción de energía es expulsada por el caño de escape. Parte de la energía que contenía el com-
bustible produjo un trabajo pero existe una cantidad no recuperable que es expulsada.
Se ha determinado que esto no solo ocurre con un motor de combustión interna sino con cualquier
tipo de maquina térmica. Es decir que solo una parte de la energía producida por el combustible es “útil” o
capaz de realizar trabajo. Esta cantidad de energía “útil” se llama energía libre y se designa con la letra G
.
Así como cuando nos referimos a los intercambios de calor, expresamos que si un sistema absorbe
calor el proceso es endotérmico y si libera calor es exotérmico, en forma análoga, diremos que el proceso
es endergónico si requiere el aporte de energía útil desde el entorno y es exergónico si libera energía útil
al entorno.
1.6 ¿Qué ocurre con la porción de energía “inútil”? Entropía (S)
De acuerdo con la teoría del big-bang, el universo está en constante expansión. Al expandirse, aumen-
ta el desorden y tiende, en miles de millones de años, al caos. Toda organización, desde la estructura inter-
na de un átomo, la asociación de los mismos en moléculas, y de allí a las estructuras celulares, requerirá
de energía pues deberá de alguna manera oponerse a la tendencia al desorden.
Como la energía total del universo es constante, es la porción de energía disipada como calor (“in-
útil”) la que aumenta el desorden. Ese desorden se conoce con el nombre de entropía y se designa con la
letra S.
1.7 ¿Cómo relaciona la termodinámica estos cambios de energía?
La Segunda Ley de la Termodinámica explica la relación entre energía libre y entropía.
Se ha observado que siempre que se produce una transformación de energía capaz de generar trabajo,
parte de la misma se pierde en forma irrecuperable aumentando el desorden del entorno.
La termodinámica expresa en su segunda ley: “todo cambio energético se produce desde estados
de mayor energía a menor energía”. Esto trae como consecuencia que durante los cambios energéticos
la tendencia natural, que llamaremos espontánea, será la que permita la realización de un trabajo pero
aumentando la entropía, el desorden del universo. Es necesario aclarar que la característica de esponta-
neidad estará dada para todo proceso que no requiere energía externa, por lo que se dice que está termo-
dinámicamente favorecido. Como consecuencia de esto, todo proceso espontáneo sin aporte de energía
externa será irreversible.
Si, por ejemplo, consideramos un gas, éste tendrá la tendencia natural, espontánea, de expandirse en
el vacío. En toda reacción química espontánea, los productos tendrán un contenido energético menor que
el de las sustancias que reaccionan.

Bioenergética y Enzimas
8
1.8 ¿Es posible revertir un proceso espontáneo?
En los ejemplos anteriores, para revertir la situación del gas, será necesario el aporte de energía ex-
terna, es decir del entorno, de manera tal que mediante la ejecución de un trabajo se pueda comprimir el
gas. Al mismo tiempo, se producirá una cantidad equivalente de calor, con el consiguiente aumento de
temperatura.
Todo sistema tiende a aumentar su entropía, es decir su desorden.
Cuanto más ordenado es un sistema mayor cantidad de energía requiere para mantener dicho
orden. En consecuencia, la entropía disminuye en los estados desde el gaseso, al líquido, al
sólido.
Se ha podido determinar que en el cero absoluto, que corresponde a 0 grados Kelvin, aproxima-
damente 273,16 ºC, se está en presencia de lo que se llama el “cristal perfecto”, temperatura por
debajo de la cual no puede existir un orden mayor.
Sobre esta base, se ha enunciado la Tercera Ley de la Termodinámica que expresa que la
entropía de una sustancia disminuye al descender la temperatura llegando a tener valor 0 en el 0
absoluto.
Esta cantidad de calor no podrá ser convertida en trabajo, sino que será liberada al entorno y con-
tribuirá a aumentar el desorden. Durante mucho tiempo se intentó convertir este excedente de energía
calórica en trabajo construyendo una máquina adecuada a tal fin, con lo cual se tendría una máquina per-
fecta. Ahora se sabe que es imposible; el primer intento fue la máquina a vapor, en la que una parte de la
energía térmica obtenida a partir de un combustible adecuado se transformaba en energía mecánica capaz
de mover unas paletas en el agua, pero parte de dicha energía se perdía irremediablemente como calor.
En toda máquina construida, ya sea a vapor, térmica, eléctrica, etc., siempre existe una porción de calor
irrecuperable que se pierde en el entorno.
Los conceptos termodinámicos expresados hasta aquí (energía, entropía, entalpía, endotérmico, exotér-
mico, endergónico, exergónico) permitirán al lector comprender con mayor claridad su aplicación a
los procesos biológicos que se desarrollarán a lo largo del curso.
______________________________________________________________________
Tercera Ley de la Termodinámica

Biología Celular
9
EL INDIVIDUO COMO SISTEMA TERMODINÁMICO- LEYES DE
LA TERMODINÁMICA
2. Bioenergética
Los seres vivos tienen un elevado grado de orden molecular que se sostiene por un necesario aporte
de energía cuya fuente primordial es el Sol. Las transformaciones y cambios que sufre esa energía en los
organismos vivos son estudiados por una rama de la Biología que se denomina Bioenergética. Ésta se basa
en lo establecido por las Leyes de la Termodinámica.
Las Leyes de la Termodinámica se aplican a todos los sistemas, incluidos los sistemas vivientes.
Según la 1º Ley de la Termodinámica, la energía total del sistema (por ej. una célula) y de su
entorno permanecen constantes. Esto signi ica que el sistema no puede crear energía, sino que
solamente puede transformarla de un tipo a otro. Es decir que los seres vivos absorben de su entorno
un tipo de energía, parte de la cual resulta “útil”, y devuelven al entorno una cantidad equivalente de
energía en una forma menos utilizable para el sistema. El tipo de energía útil para la célula se
denomina energía libre, como de inimos anteriormente, y será aquella capaz de realizar un trabajo en la
célula (por ejemplo, transportar moléculas, contraer músculos o sintetizar proteínas), mientras que la
energía no utilizable para la célula consiste principalmente en energía calórica, que devuelve a su
entorno y que en él se distribuye azarosa-mente.
La 2º Ley de la Termodinámica permite explicar qué ocurre con la energía devuelta por la célula a su
entorno. Esta ley establece que los procesos químicos y físicos tienden a aumentar la entropía del sistema
más su entorno. Es decir que en todo proceso aumenta el desorden del universo, tendiendo a alcanzar un
valor máximo. Pero anteriormente caracterizamos a la célula como un sistema que posee un elevado gra-
do de orden molecular ¿y entonces? Lo que ocurre es que la energía disipada hacia el entorno, aumentan
la entropía o desorden del mismo. Dicho de otro modo, las células mantienen su orden a expensas de
aumentar el desorden o caos de su entorno.
¿Podemos considerar a la célula como un sistema que extrae energía libre del medio? Sí, y además
es un sistema muy eficaz, ya que la eficacia con que convierte esa energía en trabajo es superior al de las
máquinas construidas por los humanos. Las estructuras de transformación de la energía que posee la cé-
lula están constituida por moléculas orgánicas relativamente frágiles e incapaces de resistir temperaturas
elevadas o corrientes eléctricas intensas.
La energía que la célula toma de su entorno se acumula en forma de energía química (energía con-
tenida en los enlaces químicos entre los átomos que constituyen las moléculas), o un trabajo osmótico
como ocurre en el transporte de materiales hacia el interior de la célula, o un trabajo mecánico como
ocurre en la contracción muscular o en la locomoción.
Estos conceptos nos permiten afirmar que la célula es un sistema químico isotérmico y constituye un
sistema abierto.
Bioenergética y Enzimas
10
2.1 La célula y la energía química
La energía libre que utiliza la célula para los distintos tipos de trabajo celular, independientemente
de la forma en que la obtiene, se almacena en forma de energía química. Como vimos antes, la energía
química es aquella contenida en los enlaces que unen a los átomos al constituir moléculas. Al romperse
un enlace químico, la forma de energía que se libera es también energía química.
¿Todas las células obtienen del entorno el mismo tipo de energía?
La respuesta es no. Teniendo en cuenta el tipo de energía que las células obtienen de su entorno, las
podemos clasificar básicamente en dos grandes grupos.
El primer grupo lo constituyen las células autotrócas fotosintéticas, que fabrican compuestos
químicos (su alimento) a partir de la energía lumínica. Estas células se caracterizan por utilizar como
principal fuente de energía a la luz solar. La energía lumínica es absorbida por un pigmento denominado
clorofila y es transformada en energía química, que es utilizada en distintos trabajos dentro de la célula.
El segundo grupo lo conforman las células heterotrócas (aquellas que no sintetizan directamente sus
alimentos), que aprovechan del entorno la energía química contenida en diferentes moléculas orgánicas
ricas en energía, como la glucosa. La energía contenida en estas moléculas es utilizada posteriormente en
diversos tipos de trabajo celular.
Si bien estos dos grupos celulares difieren en la forma de energía tomada del entorno, ambos la acu-
mulan en forma de energía química en un compuesto químico denominado ATP.
El ATP actúa como el transportador de energía química más importante en las células de todas las es-
pecies vivientes.
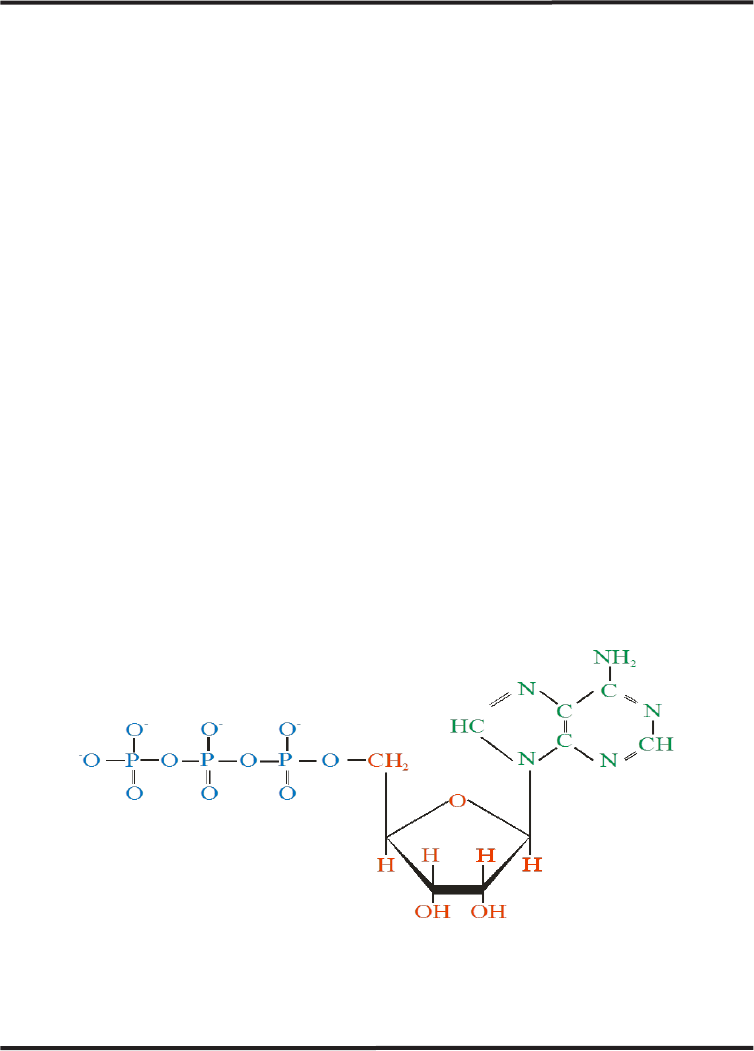
2.2 El ATP es un intermediario energético
El ATP tiene un papel central en el metabolismo de las células. Su estructura y características se han
desarrollado en el fascículo 2.
GRUPOS FOSFATO RIBOSA PURINA
Fig. 1. Representación esquemática de la estructura de una molécula de ATP.
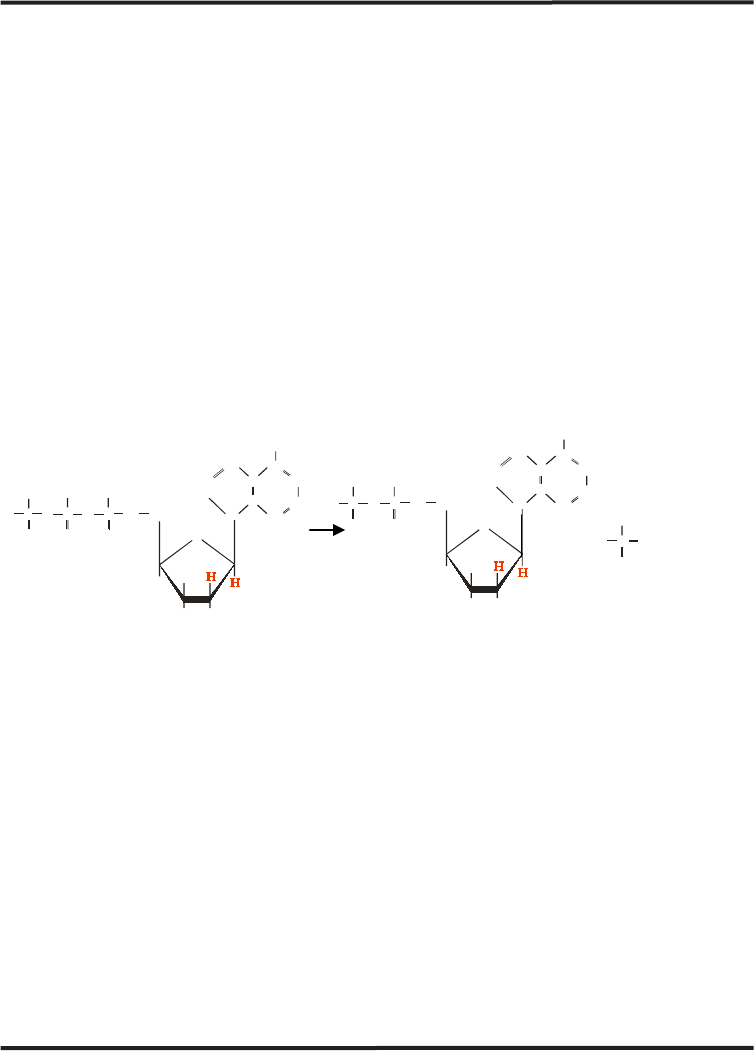
Biología Celular
11
Como vimos, el enlace entre el segundo y el tercer grupo fosfato es un enlace rico en energía, lo que
significa que necesita el aporte de mucha energía para establecerse y que al romperse libera a su vez gran
cantidad de energía. El aporte energético para la formación del ATP proviene de la energía libre obtenida
por la célula de su entorno, la que entonces queda recuperada como energía química en este tercer enlace
fosfato del ATP. La energía liberada al producirse la ruptura de este enlace se utiliza en los distintos tipos
de trabajos celulares. Esto explica el concepto de intermediario energético del ATP, ya que lo podemos
considerar como un transportador de energía hacia los distintos puntos celulares en donde es requerida
para realizar algún tipo de trabajo celular.
¿Qué ocurre con el ATP cuando se rompe su tercer enlace fosfato?
Lo primero que debemos recordar es que se libera una buena cantidad de energía que será utilizada
convenientemente por la célula en distintos trabajos. El otro producto de esta ruptura química es el ADP
(adenosina difosfato), que es la molécula en que se convierte el ATP al perder su tercer grupo fosfato. La
regeneración del ATP se consigue con la fosforilación del ADP, la que requiere una molécula de ácido
fosfórico y energía suficiente para formar el enlace.
Se ha demostrado que dentro de todas las células existe una concentración relativamente constante
de ATP, ADP y AMP (adenosina monofosfato). Asimismo se observa que en una célula con un
metabolismo muy activo, la concentración de ATP supera ampliamente la de ADP.
Si repasamos lo explicado anteriormente, nos daremos cuenta que cuando la célula consume ATP, se
genera ADP, y que al tomar del entorno energía libre, ese ADP es fosforilado a ATP, y así sucesivamente.
Es decir que se genera un ciclo, denominado ciclo del ATP, en donde se entiende claramente su papel de
intermediario energético.
Fig. 2. Esquema de la ruptura del ATP y su conversión en ADP más fosfato, con la consecuente liberación
de energía. La doble flecha indica la bidireccionalidad de esta reacción química.
-
O
O
-
O
-
O
-
P
P P
O O O
O
O O O CH
2
H
H
N
N
N
N
C
C
C
CH
HC
NH
2
P
O
O
-
O
-
P P
O
O
O
O
O O CH
2
H
H
OH OH
N
N
N
N
C
C
C
CH
HC
NH
2
+
-
O
O
-
O
+
ENERGÍA
OH OH
Bioenergética y Enzimas
12
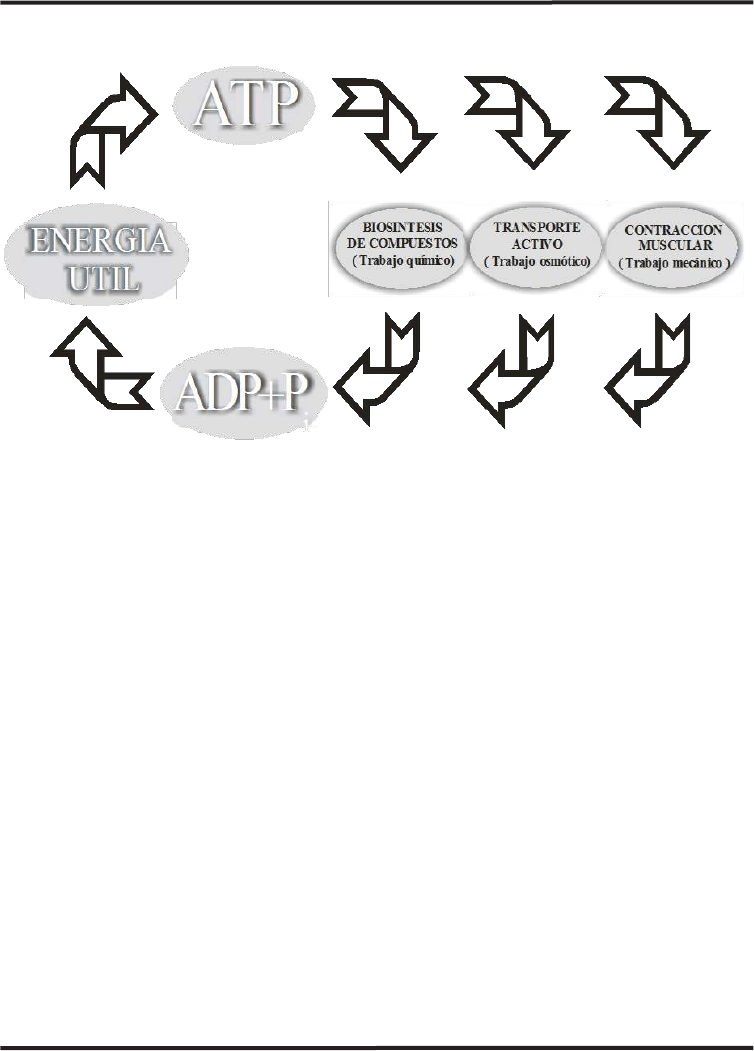
Fig. 3. Esquema que representa el ciclo del ATP. La energía contenida en el ATP es utilizada para dis-
tintos trabajos celulares como los indicados en la figura, generándose ADP. Este es fosforilado y forma
ATP a partir de la energía útil obtenida por la célula del entorno.
3. Metabolismo celular
El metabolismo intermediario, o metabolismo celular, puede definirse como el conjunto de reacciones
bioquímicas que ocurren en el interior de una célula. Estas reacciones ocurren de manera ordenada, eficaz
y específica debido a que cada una de ellas está catalizada por enzimas
El metabolismo celular se puede resumir en los siguientes procesos:
a) obtención de energía química a partir de moléculas orgánicas combustibles o de la luz solar, en
ambos casos provenientes del entorno (exógenos),
b) conversión de los principios nutritivos exógenos en precursores de las macromoléculas de la célula,
c) ensamblaje de estos precursores en proteínas, ácidos nucleicos, lípidos y otros componentes de la
célula, y
d) formación y degradación de las biomoléculas que cumplen funciones especializadas de la célula.
Como vimos anteriormente, las reacciones endergónicas son aquellas que necesitan el aporte de
energía química, mientras que las reacciones exergónicas son aquellas que liberan energía química.
¿De dónde proviene la energía necesaria para que ocurran procesos endergónicos en las células?:
Proviene del ATP, transformándose en ADP.
¿Qué compuesto capta la energía libre producida en una reacción exergónica?:
El ADP, transformándose en ATP.
´
´
´
´
Este documento contiene más páginas...
Descargar Completo
CBC cuadernillo 3 .pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.