
SC 7.1. La composición celular compleja del esbozo renal y la
regulación del balance proliferación/sobrevida/muerte celular
programada. Factores de crecimiento y proteínas
proapoptóticas y antiapoptóticas. V. Flores, R. Rey
El desarrollo normal de cualquier esbozo requiere un equilibrio entre
la proliferación celular, la diferenciación celular y la apoptosis. En
general las células del esbozo cumplen esos comportamientos
celulares con una dinámica que caracteriza a toda la población. La
sincronización en la dinámica de comportamientos celulares que
caracteriza a cada esbozo en particular es fácil explicar en los casos
en los que las células del esbozo tienen un origen embrionario
común. Sin embargo, en la constitución de los esbozos de la mayoría
de los órganos, las células no poseen un origen embrionario común.
En muchos casos provienen de varias poblaciones celulares que, en
alguna etapa del desarrollo previo, se segregaron y determinaron
diferentemente. Por ejemplo, durante la gastrulación se segregan y
determinan diferentemente las tres capas germinativas, cada una de
ellas posee dinámicas de proliferación, procesos morfogenéticos y de
apoptosis diferentes. Sin embargo, muchos esbozos se forman más
tarde como consecuencia de la integración de subpoblaciones
celulares provenientes de diferentes capas germinativas, y los CCD
mencionados se sincronizan una vez constituido el esbozo.
El ejemplo del riñón es muy notable en este aspecto debido a que en
la formación del esbozo renal participan al menos 4 categorías o
subpoblaciones celulares diferentes, cada una con sus respectivas
programaciones: a) células del brote ureteral. Estas células tienen su
origen en el mesodermo intermedio. Las células de la región
mesonéfrica del cordón nefrógeno tempranamente originan el
conducto mesonéfrico y éste, a su vez, origina el brote
ureteral; b) células de la regiónmetanéfrica del cordón nefrógeno.
Estas células se determinan en sentido metanéfrico como
consecuencia de interacciones locales, probablemente con la cloaca
y tienen la capacidad de originar, entre otras cosas,
nefrones; c) células de niveles caudales del mesodermo
paraxil que se interacalan con células del metanefros; al parecer
carecen de la capacidad para formar nefrones; d) células de la cresta
neural que también integran el mesénquima del metanefros. De no
ser por el uso de marcadores específicos y del uso de mapas de
destinos modernos sería muy difícil distinguir estos tres últimos tipos
celulares. Sin embargo, parecen exhibir tasas de proliferación y
apoptosis similares, lo que sugiere que ambos CCD se regulan
interactivamente.

Las células que integran el mesénquima metanéfrico tienen al
principio una tasa de proliferación. Luego, durante la morfogénesis y
la histogénesis renal aparecen diferencias regionales significativas
que también se regulan interactivamente (SC 7.5. El brote ureteral
promueve la formación de las células troncales del blastema
metanefrogénico).
No todas las células del mesénquima metanéfrico inicial aportan
descendientes al riñón definitivo. De las células que nacen en el
mesénquima metanéfrico, una cantidad importante se eliminanpor
apoptosis. Las que sobreviven siguen proliferando, se diferencian y
forman parte del parénquima o del estroma renal.
En el balance proliferación/apoptosis del mesénquima metanéfrico
participan por un lado ciertos factores de crecimiento, las proteínas
que integran el control central del ciclo celular y también las que
regulan la apoptosis.
Entre los factores de crecimiento, las proteínas señal factor de
crecimiento fibroblástico 2 (Fgf2), la proteína morfogenética del
hueso 7 (Bmp7) y, probablemente también, la proteína señal factor
neurotrófico derivado de la glía o Gdnf (Gdnf: Glial cell line-
derived neurotrophic factor) parecen cumplir en forma directa un
papel central en la regulación de la proliferación. Por otro lado, se
considera que los factores de crecimiento Fgf2 y Bmp7 también
influyen en el balance proliferación/apoptosis manteniendo activa la
expresión de la proteína factor de transcripción Wt1 (WT: de
tumor de Wilms). Este factor de transcripción se expresa
específicamente en el mesodermo intermedio y contrarresta el
ingreso a la vía de la apoptosis inhibiendo a algunas proteínas
proapotóticas.
Con respecto a la expresión de las proteínas que intervienen en la
apoptosis renal, se asigna un papel importante a una combinatoria
de factores de transcripción entre los cuales parece poseer papel
crucial la proteína factor de transcripción Pax2. Este factor regula
el balance proliferación/apoptosis debido a que reprime la expresión
de la proteína proapoptótica p53 que facilita el ingreso de las
células en la vía de la apoptosis. Las células mesonéfricas y
metanéfricas que expresan Pax2 no entran en apoptosis. Por el
contrario, la deficiencia en la expresión o la función de esta proteína
ocasiona el aumento de la muerte celular y fallas en el desarrollo de
los derivados mesonéfricos y metanéfricos (agenesia renal y
gonadal). En esta situación también se afecta el desarrollo de los
derivados de los conductos de Wolff y de Müller.

Otro factor con función antiapoptótica expresado en el blastema
metanéfrico y en el brote ureteral es la proteína de la membrana
mitocondrial bcl2.
También participa en el desarrollo del mesodermo intermedio
la proteína factor de transcripción Lim-1; su deficiencia genera
una anomalía de la formación del mesonefros y del metanefros (algo
similar a lo que ocurre con la deficiencia de Pax2).
Los factores mencionados no participan sólo en el desarrollo del
riñón, sino también en el de muchas otras estructuras del organismo.
Debido a ello, las mutaciones en dichos genes pueden generar
malformaciones múltiples y diversas en varios órganos.
Señalamos que en el blastema metanefrogénico se expresa el factor
de transcripción Wt1, codificado por el gen supresor de tumores del
mismo nombre. La proteína Wt1 tiene varias funciones: por un lado
es una proteína antiapoptótica ya que se une a la proteína
proapoptótica p53 y la inactiva. El gen Wt-1 se expresa
específicamente en derivados del mesodermo intermedio, por lo cual
sus mutaciones afectan solamente el desarrollo de estructuras
urogenitales.
Otros datos que indican que la muerte celular en el riñón está
regulada por interacciones entre tipos celulares está ejemplificado
por el hecho de que la metaloproteasa de la matriz 9 o Mmp9, que
participa en las Int e-m en el desarrollo del riñón, también influye
sobre la tasa de apoptosis en las etapas tempranas del desarrollo.
Los embriones deficientes en Mmp9 sufren un gran aumento en la
apoptosis renal que se traduce en una disminución del 20% del peso
del órgano y una disminución del 30% del número de nefrones. En
los riñones de embriones deficientes en Mmp9 se detecta una
disminución de la forma activada del receptor c-kit, receptor de
la proteína factor de célula troncal o Scf (Stem cell factor)
acompañada de un aumento de la Scf unida a membrana. Este
resultado es compatible con resultados de cultivos organotípicos de
riñones de estos embriones en los que se detecta un déficit en la
secreción de Scf. Estos datos indican que el Mmp9, además de
estimular el desarrollo de ramificaciones del brote ureteral, también
protege a las células del mesénquima metanefrogénico, las que
tienen capacidad de formar nefrones, de la apoptosis.
SC 7.2. Factores de transcripción, factores de crecimiento y
sus receptores y proteínas de la matriz extracelular regulan
dinámicamente el patrón de ramificaciones del brote ureteral.
V. Flores, R. Rey

Las células mesenquimáticas de la región metanéfrica expresan
la proteína factor de transcripción Wt-1 codificada por el gen
supresor de tumores homónimo. El factor Wt1 cumple varias
funciones. Una de ellas es posibilitar las interacciones recíprocas que
ocurren entre las poblaciones celulares que forman el esbozo renal.
Su expresión le permite, por un lado, la generación de señales que
tienen como población competente el brote ureteral y, por otro,
responder a señales provenientes del brote ureteral. También,
indirectamente, inhibiendo a proteínas proapoptóticas, participa del
balance sobrevida/muerte celular durante el desarrollo renal.
Una de las funciones de la proteína Wt-1 es la regulación de la
síntesis de dos proteínas señal que genera el blastema
metanéfrico: el factor neurotrófico derivado de la glía (Gdnf) y
el factor de crecimiento del hepatocito (Hgf).
Las células epiteliales del brote ureteral, a su vez, expresan en sus
membranas plasmáticas las proteínas receptor de estas señales:
el receptor Ret, al que se une el Gdnf, y el receptor c-Met, cuyo
ligando es el Hgf.
Los dos factores de crecimiento liberados por el mesénquima
metanéfrico actúan sobre las células epiteliales del brote ureteral;
estimulan la proliferación celular, el crecimiento en longitud de los
brotes y su ramificación dicotómica. En este último proceso también
participan las proteínas señal denominadas factores de
crecimiento transformantes beta (Tgfβ), que poseen efectos
contrapuestos a los anteriormente mencionados.
El crecimiento, morfogénesis y patrón de ramificaciones del brote
ureteral también depende de las características de la matriz
extracelular del blastema metanétrico (Véase SC El papel
morfogenético del mesénquima. La remodelación regulada de la
matriz extracelular como mecanismo de control del patrón de
ramificaciones de un órgano epitelial). Por ejemplo, la síntesis,
secreción y deposición de proteínas de matriz extracelular como la
laminina es esencial, pues, cuando el brote ureteral se ramifica y da
origen a los tubos colectores, éstos expresan la proteína integral
de membrana fibroquistina. Las moléculas de fibroquistina que se
insertan en la región basal de la membrana plasmática poseen la
función de realizar interacciones con la laminina y otras proteínas de
la matriz extracelular e iniciar vías de señalización intracelulares que
controlan muchos de los CCD involucrados en todos los aspectos de
la morfogénesis y diferenciación de los túbulos renales. Las que se
insertan en las regiones laterales y apical de la membrana poseen
otra función (SC Proteínas complejas polifuncionales y sus

alteraciones como bases moleculares de la enfermedad renal
poliquística).
La importancia de los componentes de la matriz extracelular en el
desarrollo de los derivados del brote ureteral se pone de manifiesto
con claridad cuando se analiza el efecto de los factores arriba
mencionados en medios de cultivo. Por ejemplo, el factor Hgf
promueve la formación de estructuras tubulares ramificadas
(similares a ramas del brote ureteral) en los cultivos celulares de riñón
(línea celular MDKC: Madin-Darby canine kidney). Este efecto se
observa cuando los cultivos se realizan sobre un sustrato con
colágeno tipo I. Cuando son cultivadas sobre un extracto de
membrana basal de composición compleja (Matrigel) no se produce
este efecto.
La extracción sucesiva de distintos compuestos del Matrigel y su
adición ulterior al sustrato de colágeno tipo I permitió detectar qué
sustancia del primero inhibe la tubulogénesis inducida por Hgf en el
segundo. Este procedimiento permite constatar
que: a) algunas proteínas de la matriz extracelular
tales como laminina, fibronectina y entactina facilitan la formación
de ramificaciones y, en consecuencia, aumentan la complejidad del
patrón de ramas; b) otros componentes, como por
ejemplo, colágeno tipo IV, proteoglucanos de heparán
sulfato, vitronectina y otros, producen una marcada inhibición de
las ramificaciones y c) la proteína señal factor transformante β
(Tgf-β), por un lado, reduce el crecimiento de las ramas y, por otro,
en el caso de las ramas que sí se forman, tienen menos
ramificaciones.
Todos estos resultados sugieren que el proceso de crecimiento y
ramificación del conducto ureteral y sus ramas está regulado
dinámicamente por un conjunto de factores que operan
positivamente (lo estimulan) y negativamente (lo inhiben) (Fig. SC 7-
2-1).
Habría algunos morfógenos tubulogénicos, o señales positivas,
como Gdnf y Hgf, y factores anti-tubulogénicos, o señales negativas,
como el Tgf β que, actuando dentro de contexto de una matriz
extracelular de composición cambiante, como el que rige durante los
procesos de desarrollo de estructuras epiteliales, modularían
dinámicamente las características que definen el patrón de
ramificaciones: formación de túbulos, longitud de éstos, la frecuencia
de ramificaciones y la extensión global de la arborización.
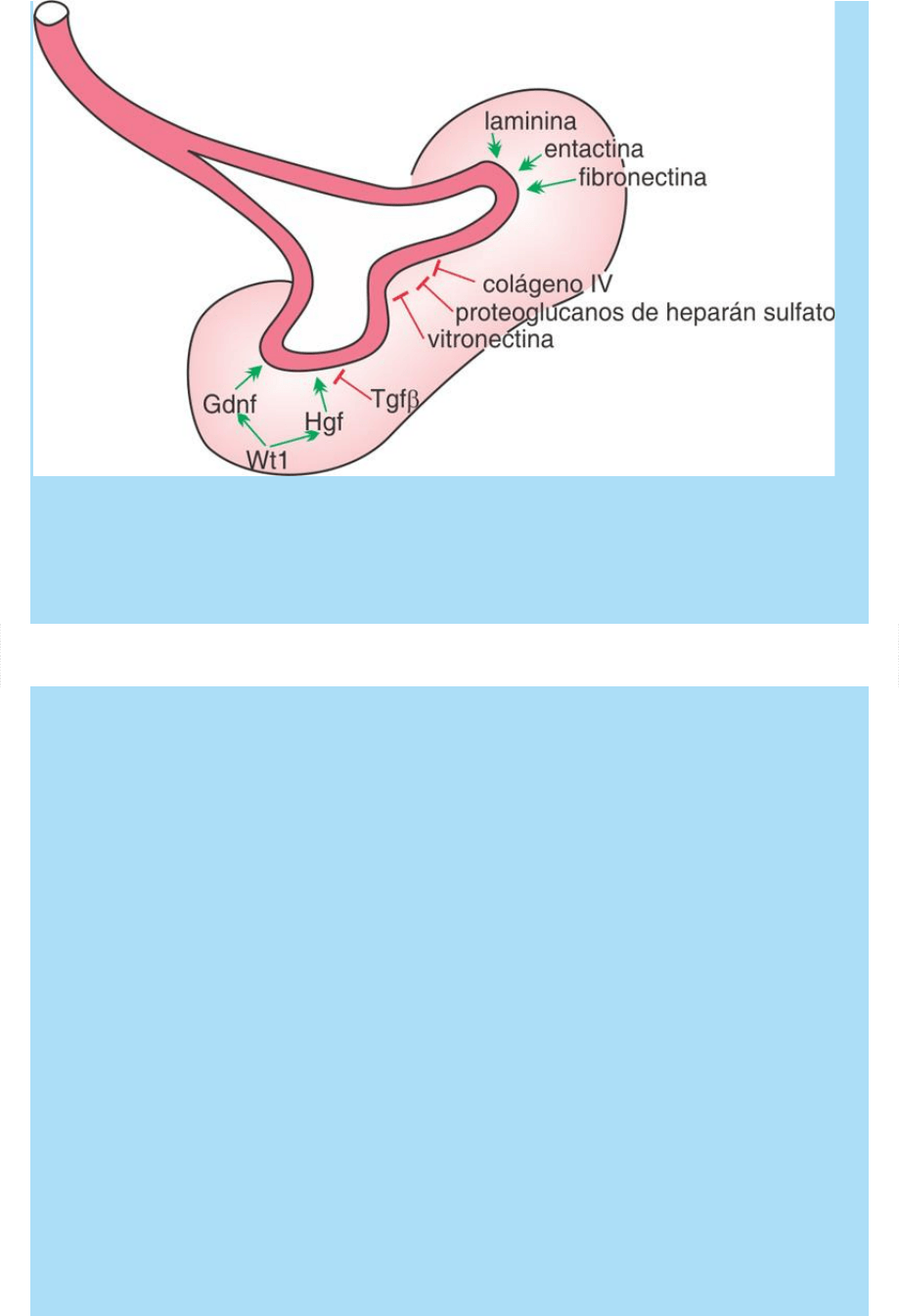
Fig. SC 7-2-1. Representación esquemática del modelo que plantea
que el desarrollo del brote ureteral y sus ramas es el resultado
regulado de fenómenos estimulantes e inhibitorios del desarrollo.
SC 7.3. La constitución del esbozo renal requiere una sucesión
de interacciones celulares. V. Flores
En la constitución del esbozo renal participan al menos dos
poblaciones celulares, el blastema metanéfrico y el brote ureteral.
La primera de ellas, sin embargo, de acuerdo con estudios modernos
de marcación y seguimiento de linajes celulares, es una población
heterogénea de células mesenquimáticas de diverso origen: las
propias del mesénquima metanéfrico con el agregado de otras
provenientes del mesodermo paraxil y de la cresta neural.
La constitución del mesénquima metanéfrico. El cordón
nefrógeno del mesodermo intermedio se extiende a lo largo de casi
toda la extensión del embrión. Su extremo caudal se ubica a ambos
lados de la cloaca. Sólo el mesodermo intermedio del extremo caudal
del cordón nefrógeno posee la capacidad de formar nefrones
metanéfricos cuando es puesto a interactuar con el brote ureteral.
Trabajos clásicos de disociación y reasociación de tejidos
embrionarios sugieren que tal capacidad del mesodermo intermedio
es adquirida sólo en el entorno de la cloaca, por lo cual el mesodermo
intermedio sería determinado en sentido metanéfrico por el epitelio
cloacal u otra población celular de la región. A esta región del
mesodermo intermedio se agregan luego células originadas en los
segmentos caudales de la cresta neural y del mesodermo paraxil.

La incorporación de células de la cresta neural al mesénquima
metanéfrico es considerada por algunos investigadores como
fenómeno asociado al hecho de que el uréter que deriva del conducto
mesonéfrico posee en sus capas musculares plexos nerviosos y
neuronas parasimpáticas derivadas de la cresta neural.
La formación del brote ureteral. El siguiente paso es la
determinación del brote ureteral en el epitelio del conducto
mesonéfrico y su ulterior crecimiento hacia el mesénquima
metanefrénico. En este proceso, el mesénquima metanéfrico actuaría
como población determinante y el brote ureteral como población
competente.
Una vez constituidos el brote ureteral y el blastema metanefrogénico,
el proceso de formación del riñón implica una sucesión de
interacciones entre ambas poblaciones. Si bien es imposible conocer
la secuencia completa de eventos interactivos, con fines didácticos
algunos proponen cuatro categorías de eventos sucesivos:
a) El primero de ellos, probablemente mediado por señales de
relativamente largo alcance, está mediado por señales generadas en
el blastema que llevan a la formación del brote ureteral a partir del
conducto mesonéfrico. Este fenómeno implicaría, por un lado, un
efecto determinante y, por otro, un efecto estimulante de la
proliferación y un efecto quimiotáctico de orientación del crecimiento
hacia el blastema. El fenómeno involucra varias señales y se ha
propuesto que podría estar bajo el control de un conjunto de factores
de transcripción entre los cuales se cuenta el factor de
transcripción Wt1.
b) El segundo de los fenómenos, que también sería de largo rango
de alcance, consiste en la producción de señales por parte de las
células del brote ureteral que estimularían a las células del
mesénquima metanéfrico del entorno a ingresar en una fase de célula
troncal (autorrenovante y con alta tasa proliferativa). Durante esta
fase también se inhibirían los procesos de muerte celular generando
un aumento de la masa crítica de células necesarias para la
constitución del blastema metanefrogénico.
c) El tercero de estos fenómenos implicaría la generación de señales
adicionales por parte de las células del brote ureteral, en este caso
de corto rango de acción, que llevarían a las células del blastema
metanefrogénico, inmediatamente adyacentes a los extremos de
crecimiento de las ramas del brote ureteral, a agregarse y formar
condensaciones mesenquimáticas o nódulos nefronogénicos
determinados a formar nefrones.
d) El cuarto de estos fenómenos consistiría en la producción de
señales por parte del blastema metanefrogénico que regularían el
crecimiento y las ramificaciones dicotómicas sucesivas de las ramas
del brote ureteral. Estas últimas interacciones regularían el patrón de
bifurcaciones y la extensión global de las ramificaciones y, en
consecuencia, de la masa de parénquima renal funcionante.
La clasificación precedente intenta resumir, en un cuadro
relativamente claro y simple, los procesos interactivos involucrados
en el desarrollo renal (Fig. SC 7-3-1). Ciertamente el panorama es
más complejo y se omiten muchos fenómenos interactivos
conocidos.
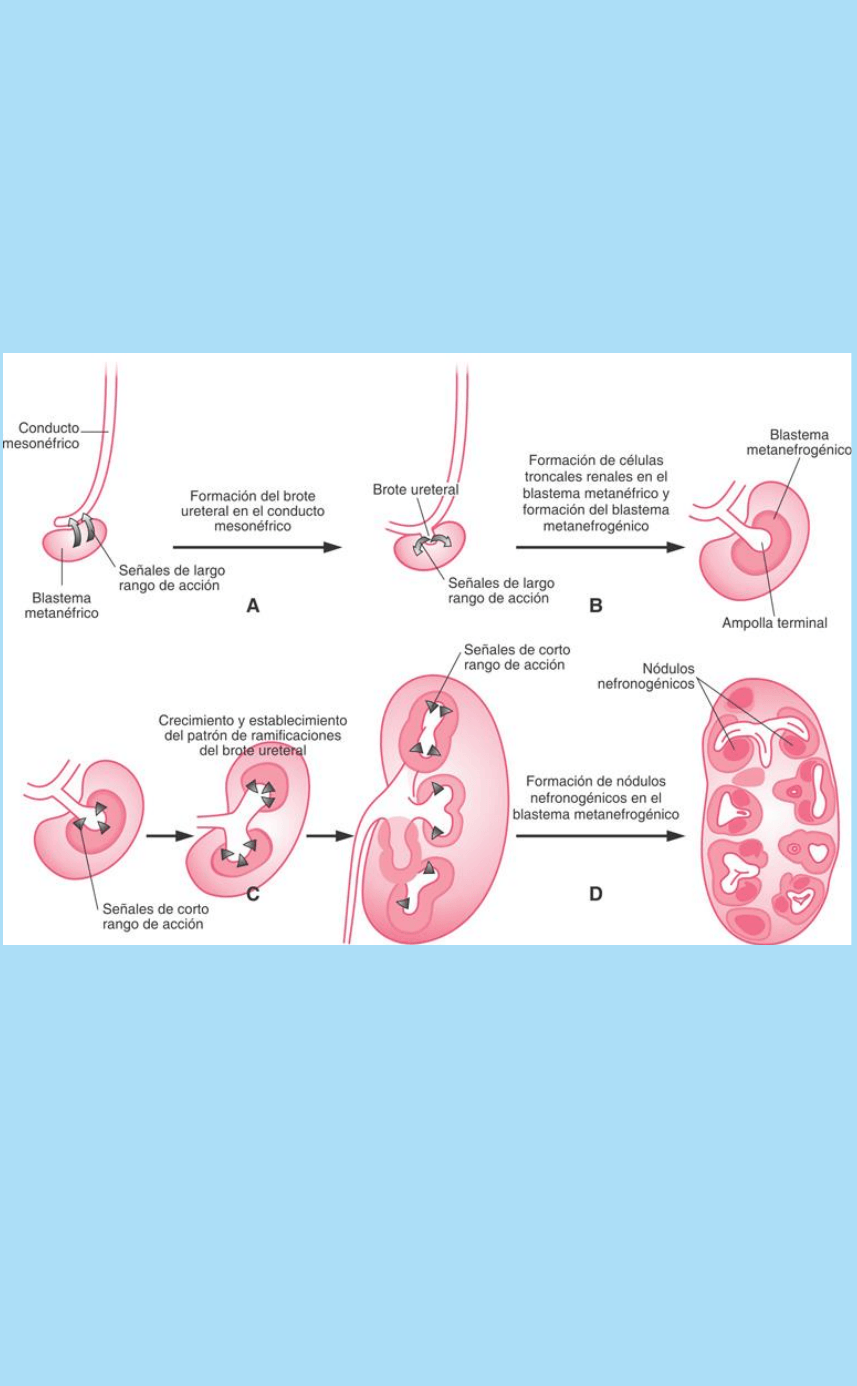
Fig. SC 7-3-1. Modelo de la sucesión de interacciones que podrían
ocurrir durante el desarrollo del parénquima renal.
Muchas experiencias sugieren que la acción del brote ureteral sobre
el mesénquima metanéfrico, promoviendo la formación del blastema
metanefrogénico en su entorno inmediato, no es un fenómeno
determinante sino permisivo. De acuerdo con esta interpretación, el
mesénquima metanéfrico del cordón nefrógeno ya está determinado
en sentido metanefrogénico, vale decir, determinado a formar
nefrones, antes de su interacción con el brote ureteral. Se funda esta
idea en que el hecho de que, si experimentalmente se asocia el
mesénquima metanéfrico con una variedad de otros tejidos, en
mucho casos el mesénquima metanéfrico responde formando
nefrones o, por el contrario, no responde y no se diferencia. Estos

resultados sugieren que el mesénquima ya está determinado a
formar nefrones y que todas las diversas o variadas señales que
puede recibir de varios tejidos embrionarios probablemente son todas
permisivas. Vale decir, permiten expresar una vía previamente
elegida.
Se considera que la potencia del meséquima metanéfrico para
responder a dichos estímulos formando nefrones depende de la
expresión de la proteína factor de transcripción Wt1. Este factor
de transcripción se expresa en el mesénquima desde antes de su
interacción con el brote ureteral. Sin embargo, la expresión de la
proteína Wt1 no es suficiente para adquirir la determinación (o la
competencia) en sentido renal. Probablemente sea la combinatoria
de factores de transcripción, en la cual está incluida, la que confiere
determinación o competencia al blastema metanefrogénico. Que la
expresión de la proteína Wt1 por sí solo no es suficiente está
demostrado por el hecho de que otras poblaciones celulares
embrionarias como el blastema gonadal y el epitelio celómico
también lo expresan y no por eso se diferencian en riñón.
SC 7.4. El mesénquima metanéfrico participa en la
determinación y formación del brote ureteral a partir del
conducto mesonéfrico. V. Flores
Algunos autores consideran que el mesénquima metanéfrico genera
las señales que promueven el desarrollo del brote ureteral a partir del
conducto mesonéfrico. El mesénquima metanéfrico se caracteriza,
desde temprano, por la expresión delfactor de transcripción
Wt1 codificado por el gen supresor de tumores del mismo nombre.
Se considera que el factor Wt1 posee varias funciones de desarrollo.
Una de las funciones de la proteína Wt1 en el desarrollo del riñón
sería participar en la génesis de algunas de las señales que operan
sobre el conducto mesonéfrico. La proteína Wt1 regularía la
expresión de lasproteínas señal factor neurotrófico derivado de
la glía (Gdnf) y factor de crecimiento de hepatocito (Hgf). Por su
parte, el conducto mesonéfrico posee competencia para responder a
estas señales pues sintetiza las proteínas receptor c-Ret(receptor
de Gdnf) y c-met (receptor de Hgf). Así, el mesénquima
metanéfrico podría actuar sobre el epitelio del conducto mesonéfrico
determinándolo a formar el brote ureteral.
Una vez generado el brote ureteral, la expresión de las proteínas
receptor mencionadas queda restringida a los extremos de
crecimiento del brote y de sus ramificaciones (Fig. SC 7-4-1 A-E),
vale decir, en los sitios de crecimiento en los que las interacciones de
desarrollo entre ambas poblaciones prosiguen.
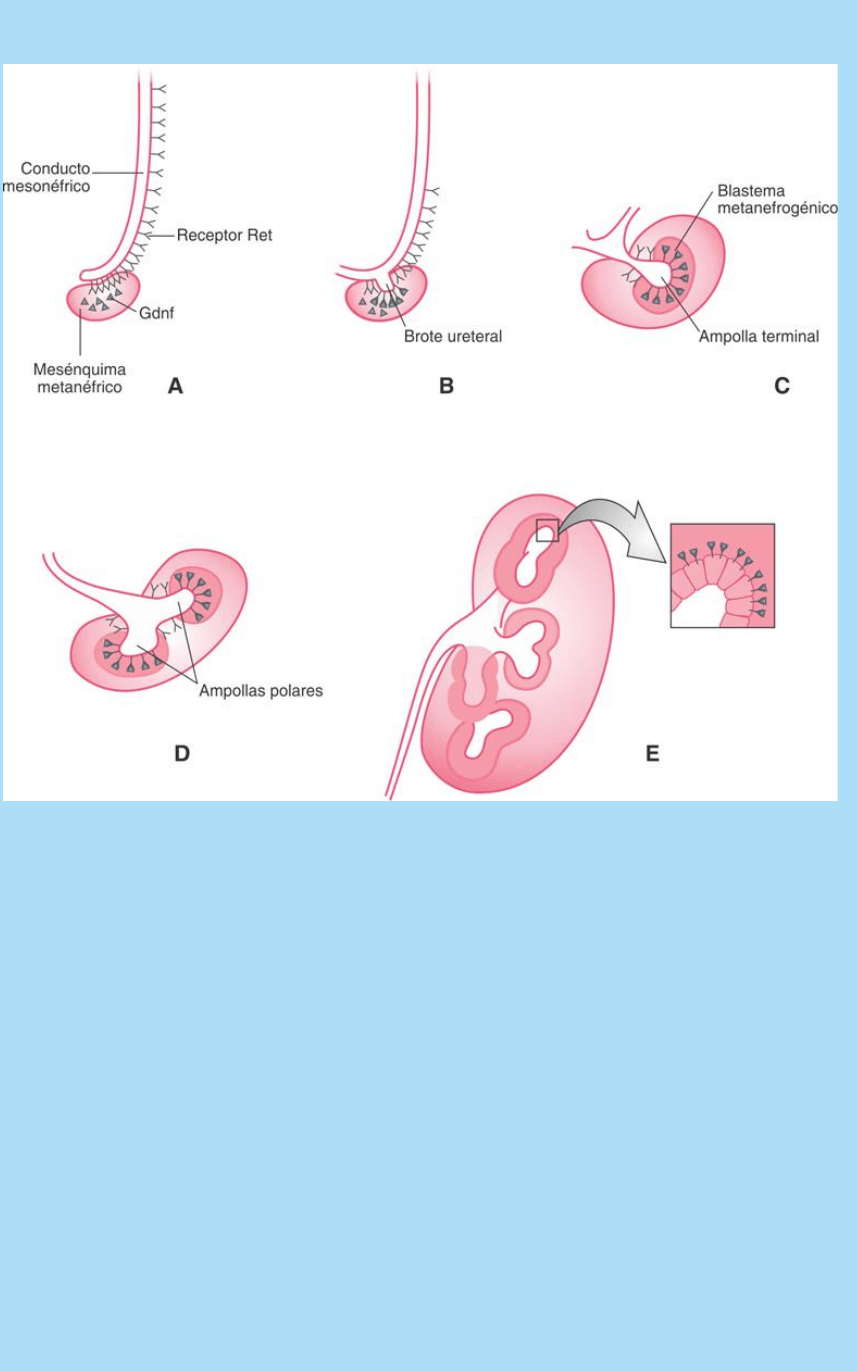
Fig. SC 7-4-1. Modelo del efecto localizador del sitio de formación del
brote ureteral por medio de variaciones en la concentración de la
proteína Gdnf y de su receptor Ret. La secreción local de Gdnf, por
parte del blastema metanéfrico, y la expresión polarizada de su
receptor Ret, con un máximo en el extremo caudal del cordón
nefrógeno, determina el sitio de origen del esbozo ureteral a partir del
conducto mesonéfrico. Sólo en la región adyacente al mesénquima
metanéfrico la activación de la señalización vía Gdnf alcanza el
umbral requerido para la determinación del brote ureteral. El modelo
considera que, una vez producida la inducción, según se va
ramificando el brote ureteral, sólo en sus extremos queda activo el
sistema de interacción Gdnf-Ret. La expresión de este último es
inhibida en las zonas ya determinadas. (Modificado de Schuchardt y
cols., 1996).
Una red de interacciones moleculares en las que participan proteínas
señal, sus receptores, correceptores y reguladores de la
transcripción, generadas en tanto en el blastema, en el brote y en los

tejidos circundantes, contribuyen a definir la localización del sitio de
formación del esbozo del riñón (SC 7.6. Una red de vías de
señalización regula la formación del brote ureteral y la constitución
del blastema metanefrogénico).
La atribución de las funciones de desarrollo mencionadas a las
moléculas señal y sus receptores citados se debe a que las
alteraciones en la expresión de dichas moléculas, debida a
mutaciones o a su inhibición con anticuerpos en forma experimental,
lleva a la producción de agenesias o a la ausencia bilateral de riñón.
La figura SC 7-4-1 muestra que la formación del brote ureteral y de
todo el sistema colector renal depende de la expresión de la proteína
Gdnf por parte del mesénquima metanéfrico y de la expresión de su
receptor Ret por parte del epitelio ureteral. La figura también muestra
que la localización del sitio de formación del brote ureteral en la
región caudal del conducto mesonéfrico depende, por un lado, de la
alta concentración de Gdnf en la región caudal y, también, de la
existencia de un gradiente de expresión del receptor Rec, el receptor
del Gdnf. Este receptor exhibe su máximo nivel de expresión en el
extremo caudal, único lugar en el que las células del conducto
mesonéfrico alcanzan el nivel de expresión umbral necesario para
que se produzca el efecto del factor Gdnf. Así, ambos hechos,
concentración de la señal Gdnf y de su receptor, contribuyen a definir
el sitio de nacimiento del brote ureteral.
La figura SC 7-4-2 ilustra la importancia de la proteína Gdnf,
secretada por el blastema metanéfrico, en la formación, crecimiento
y el patrón de ramificaciones del brote ureteral. La figura muestra que
los ratones heterocigotas para una mutación que anula la función del
factor Gdnf presentan un crecimiento en longitud deficiente del brote
ureteral y una disminución del número y longitud de sus
ramificaciones. Por otro lado, los ratones homocigotas para dicha
mutación muestran drástica abolición del desarrollo del brote ureteral
(SC 7.6. Una red de vías de señalización regula la formación del brote
ureteral y la constitución del blastema metanefrogénico).

Fig. SC 7-4-2. Representación esquemática del déficit de la proteína
Gdnf sobre el desarrollo del esbozo ureteral. A. Ilustra el desarrollo
del brote ureteral y sus ramas en el esbozo renal mantenido en cultivo
durante 3 días. El esbozo fue obtenido de un ratón silvestre (normal).
B. Ilustra el desarrollo del brote ureteral, en las mismas condiciones
que en A, pero en un esbozo renal obtenido de un ratón heterocigota
para una mutación del gen codificante de Gdnf. El tamaño y longitud
del brote ureteral y el número y longitud de sus ramas se reducen. C.
Desarrollo del brote ureteral, en las mismas condiciones que en A,
pero, en este caso, de un ratón con ambas copias del gen codificante
de Gdnf mutados. Puede observarse que el conducto mesonéfrico se
halla intacto pero no se forma el brote ureteral debido a la falta de la
señal apropiada generada en el mesénquima metanéfrico.
SC 7.5. El brote ureteral permite la formación del blastema
metanéfrico; éste permite el crecimiento y ramificación del
brote ureteral. V. Flores
Luego de la constitución del brote ureteral, los siguientes pasos
son a) la admisión de su crecimiento en la intimidad del blastema
metanéfrico y b) la formación de varias generaciones de
ramificaciones dicotómicas dentro del mesénquima.
En general, los procesos por medio de los cuales los tejidos
epiteliales crecen y se ramifican dentro del mesénquima requieren la
participación activa de este último (SC El papel morfogenético del
mesénquima. La remodelación regulada de la matriz extracelular
como mecanismo de control del patrón de ramificaciones de un
órgano epitelial). En el caso del desarrollo del riñón, el brote ureteral
y el mesénquima metanéfrico, por medio de Int e-m, regulan todo el
proceso de generación del sistema de túbulos colectores del riñón.
En el ratón existe una mutación, la mutación Danforth, que
fenotípicamente se expresa, en el nivel anatómico, como ausencia
de riñón.
Esta alteración fenotípica ilustra la dificultad en cuanto a diferenciar
si la ausencia de un órgano es consecuencia de a) una agenesia de
éste, que conceptualmente se debe a una falla en la determinación y
constitución del esbozo del órgano o si, por el contrario, se debe
a b) diversas alteraciones que pueden afectar el desarrollo del
esbozo.
La mutación Danforth del ratón, por ejemplo, tiene como
característica fenotípica relevante la ausencia de riñón. Sin embargo,
no es el resultado de una falla en la formación del brote ureteral. El
brote ureteral se forma normalmente ‒es visible morfológicamente

con forma, tamaño y posición normales‒ pero no crece debido a que
no posee la capacidad de introducirse ni de ramificarse dentro del
mesénquima metanefrogénico.
Durante la morfogénesis y la histogénesis renal, el brote ureteral y
sus ramificaciones crecen gracias a la actividad de las células
localizadas en sus extremos. Vale decir, poseen un “extremo de
crecimiento” integrado por células con propiedades biológicas
diferentes de las que integran los “tallos” de las ramificaciones. Se
sabe que el brote ureteral, una vez constituido, empieza a sintetizar
la proteína señal Wnt11 que, al parecer, es necesaria para las
interacciones que permiten su crecimiento dentro del mesénquima
metanéfrico. También se sabe que el mesénquima sintetiza y
deposita proteoglucanos de la matriz extracelular que permiten la
síntesis y secreción sostenida de Wnt11 por las células del extremo
de crecimiento del brote ureteral, primero, y de cada una de las
sucesivas ramificaciones después.
En la mutación Danforth, el extremo de crecimiento del brote ureteral
no expresa Wnt11; en consecuencia, no se introduce en el
mesénquima, no prosigue su desarrollo y a ello se debe la ausencia
del riñón. La interacción Wnt11-proteoglucanos es sólo una de un
conjunto de interacciones moleculares que regulan el desarrollo
integrado de brote ureteral y mesénquima metanéfrico. Nótese que
la normalidad del riñón no requiere sólo que el brote ureteral pueda
crecer y ramificarse, sino también la elaboración de un patrón de
ramificaciones dicotómicas típico del sistema colector renal.
La proteína señal factor neurotrófico derivado de la glía o
Gdnf (Glial cell-derived neurotrophic factor) aparte de determinar la
formación del brote ureteral (Fig. 1) también participa promoviendo el
desarrollo sus ramificaciones. La proteína Gdnf se une directamente
a su receptor Ret que es expresado por las células de los extremos
del brote ureteral y luego de sus ramas. Promueve de esta forma la
formación de nuevas ramas a partir de las preexistentes.
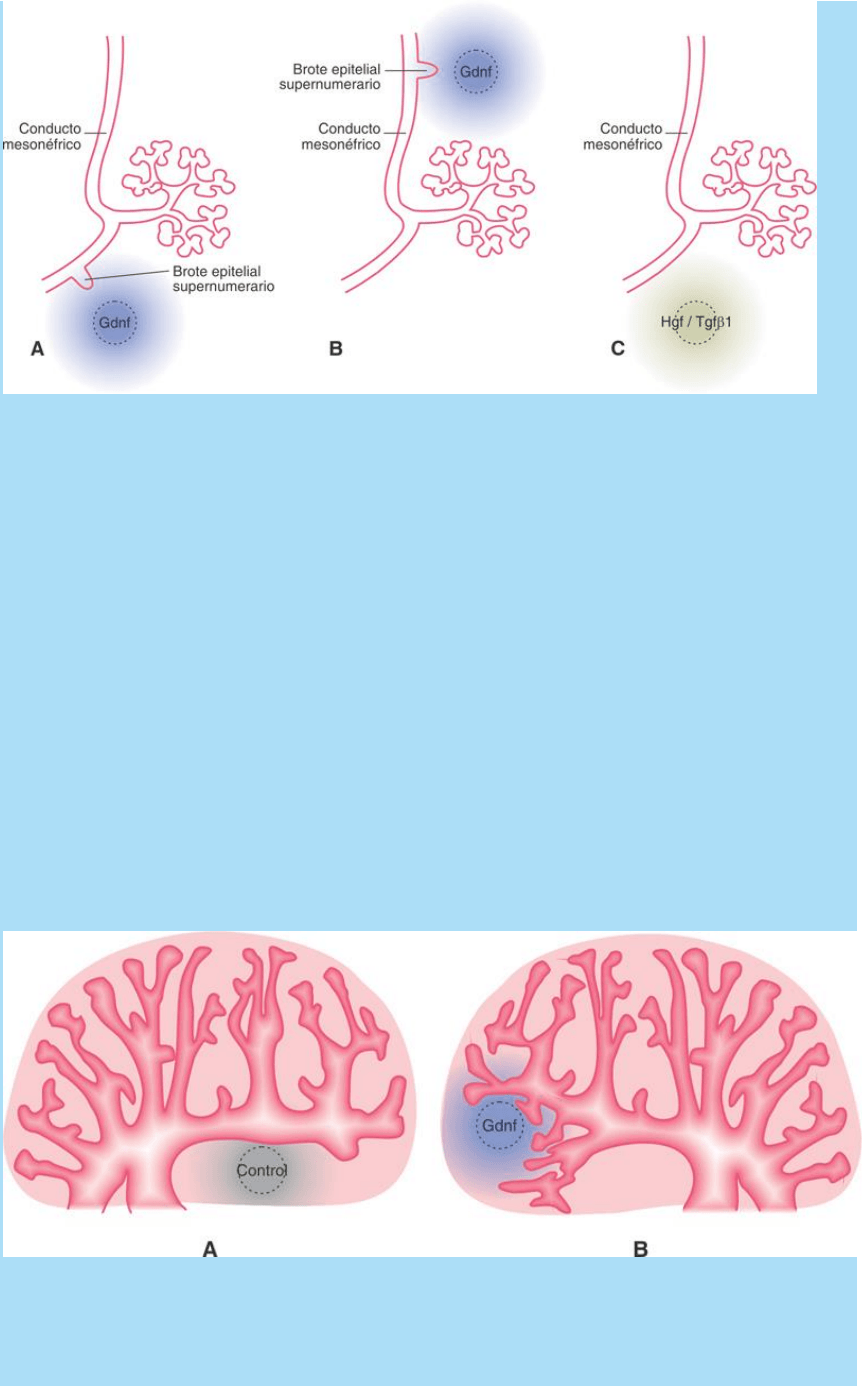
Fig. SC 7-5-1. Efecto de diversos factores de crecimiento sobre el
desarrollo del sistema colector del rinón. A. Una microesfera de gel
embebido en Gdnf estimula la formación de un brote epitelial (similar
al ureteral) en la región caudal del conducto mesonéfrico mantenido
en cultivo de tejido. B. Un fenómeno similar al mostrado en A ocurre
en la región cefálica del conducto mesonéfrico. Se forma un brote
epitelial amplio y deformado. C. Una microesfera embebida en Hgf o
en TgfB1 no posee capacidad de estimular el desarrollo de un brote
epitelial.
Por otro lado, actuando como agente quimiotáctico, promueve el
crecimiento de los brotes hacia zonas de alta concentración de Gdnf
en éstas y promueve la formación de brotes (Fig. SC 7.5.2). También
se ha mostrado en medios de cultivo que tiene el efecto de aumentar
la adhesividad entre las células del epitelio ureteral garantizando su
estabilidad. No se ha mostrado que aumente significativamente la
proliferación de las células del brote ureteral.
Fig. SC 7-5-2. Efecto del Gdnf sobre el pattern de ramificaciones del
sistema colector del riñón. Explantes de esbozos de rinón
mantenidos durante 2 días en cultivo. A. Ilustra esquemáticamente
que una microesfera control, no embebida en Gdnf (señalada en

círculo de línea de puntos), no altera significativamente el patrón de
ramificaciones del brote ureteral. B. Muestra el resultado de un cultivo
en similares condiciones pero con una microesfera embebida en
Gdnf. Se observa un desarrollo exagerado de las ramas del brote
ureteral en derrededor de la microesfera (zona de alta concentración
de Gdnf). (Modificado de Sainio K, et al. 1997).
La proteína Gdnf sería el factor de crecimiento que actuaría en primer
término. Participaría en el inicio de la formación del esbozo ureteral y
sus ramas, en tanto que otros factores como el factor de
crecimiento de hepatocitos o Hgf/Sf (Hepatocytegrowth factor) y
el factor transformante β1 o Tgf β1
(Transforming growth factor Beta 1) actuarían a continuación
modulando o regulando el proceso, favoreciendo o contrarrestando
el efecto de Gdnf.
La proteína señal factor de crecimiento transformante β1 o
Tgfβ1, por ejemplo, tendría funciones antagónicas al Gdnf en la
modulación del proceso de generación de ramificaciones. Este factor,
por un lado, inhibe las proteasas
extracelularesdenominadas metaloproteasas de la matriz
extracelular (Mmp) que degradan el colágeno y, además, estimulan
la síntesis de proteínas de la matriz extracelular; de esa forma
estabilizan la matriz y el epitelio evitando que éste siga creciendo y
ramificándose. La proteína de la matriz extracelular
activina también participa en este proceso pues su exceso o su
déficit en condiciones experimentales alteran la morfología de las
ramificaciones. Lo mismo ocurre con otras varias proteínas que
forman parte de la matriz extracelular o de la lámina basal.
SC 7.6. Una red de vías de señalización regula la formación del
brote ureteral y la constitución del blastema metanefrogénico.
V. Flores
La constitución del esbozo renal requiere la aparición e integración
de tres poblaciones: a) la formación del mesénquima metanéfrico en
el extremo caudal del mesodermo intermedio, b) la formación del
brote ureteral en el extremo caudal del conducto mesonéfrico y c) la
constitución del blastema metanefrogénico, como subpoblación
segregada a partir del mesénquima metanéfrico como consecuencia
de su interacción con el brote ureteral. La primera población, por un
lado, da origen a la tercera y, por otro, origina el estroma del órgano.
Las dos últimas están encargadas de formar el parénquima del
órgano (el sistema colector y el sistema de nefrones). A estas
poblaciones celulares se agregan luego otras dos subpoblaciones,
Este documento contiene más páginas...
Descargar Completo
Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.