SC 6.1. Funciones de desarrollo de la proliferación celular y la
muerte celular programada durante las fases sólida y de
recanalización del tubo digestivo. M.P. Bidondo, V. Flores
Ya en 1900 Tandler describió la obliteración de la luz duodenal por la
estratificación del epitelio. Definió la existencia de una fase sólida,
maciza o cordonal, seguida de una fase de recanalización por
vacuolización (formación de pequeñas cavidades confluentes). Las
fallas en estos dos procesos fueron consideradas como patogenia de
estenosis, atresias y duplicaciones duodenales. En la interpretación
clásica, el proceso se realiza a través de fases resultantes de la
operación de dos CCD en particular: en una 1ª fase, un aumento en
la proliferación celular epitelial oblitera la luz; en una 2ª fase, un
aumento en la muerte celular programada genera espacios libres o
vacuolas; en una 3ª fase, de coalescencia de las cavidades, se
produce la recanalización de la cavidad y aparición de vellosidades.
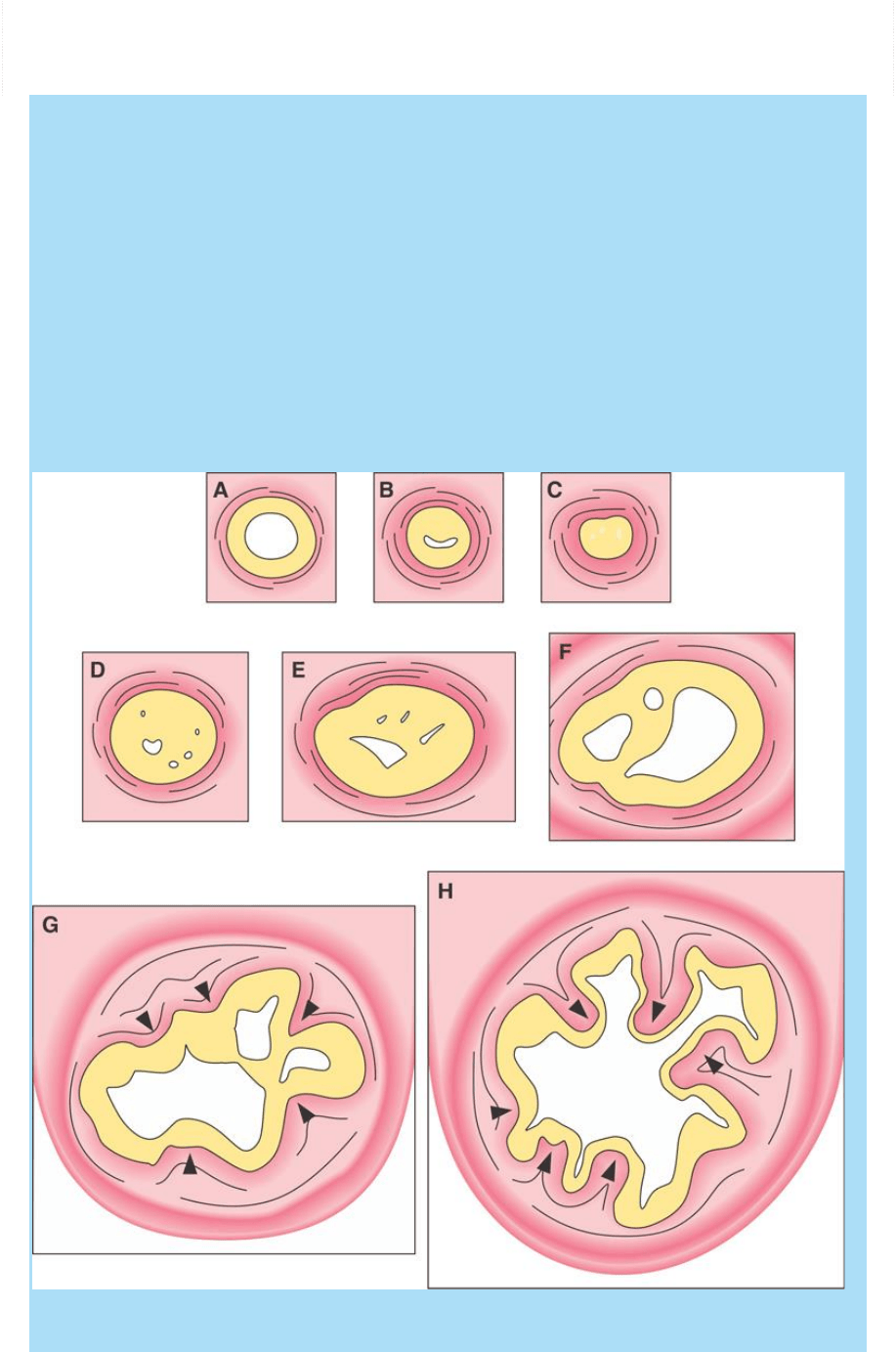
Fig. SC 6-1-1. Cambios histogenéticos descritos durante el desarrollo
del duodeno humano. A-B. Estrechamiento de la luz hasta la forma
semilunar. (Estados Carnegie 13-15). C-D. Fases de oclusión y
vacuolización en la porción media (Estados Carnegie 16-17) e inferior
(Estados Carnegie 18-19); en el tercio superior no existe fase de
oclusión. E-G. Fase de coalescencia de cavidades primarias y
formación de cavidades secundarias más amplias. H-I.
Recanalización y formación de vellosidades primarias. (Modificada
de Matsumoto y cols., 2002).
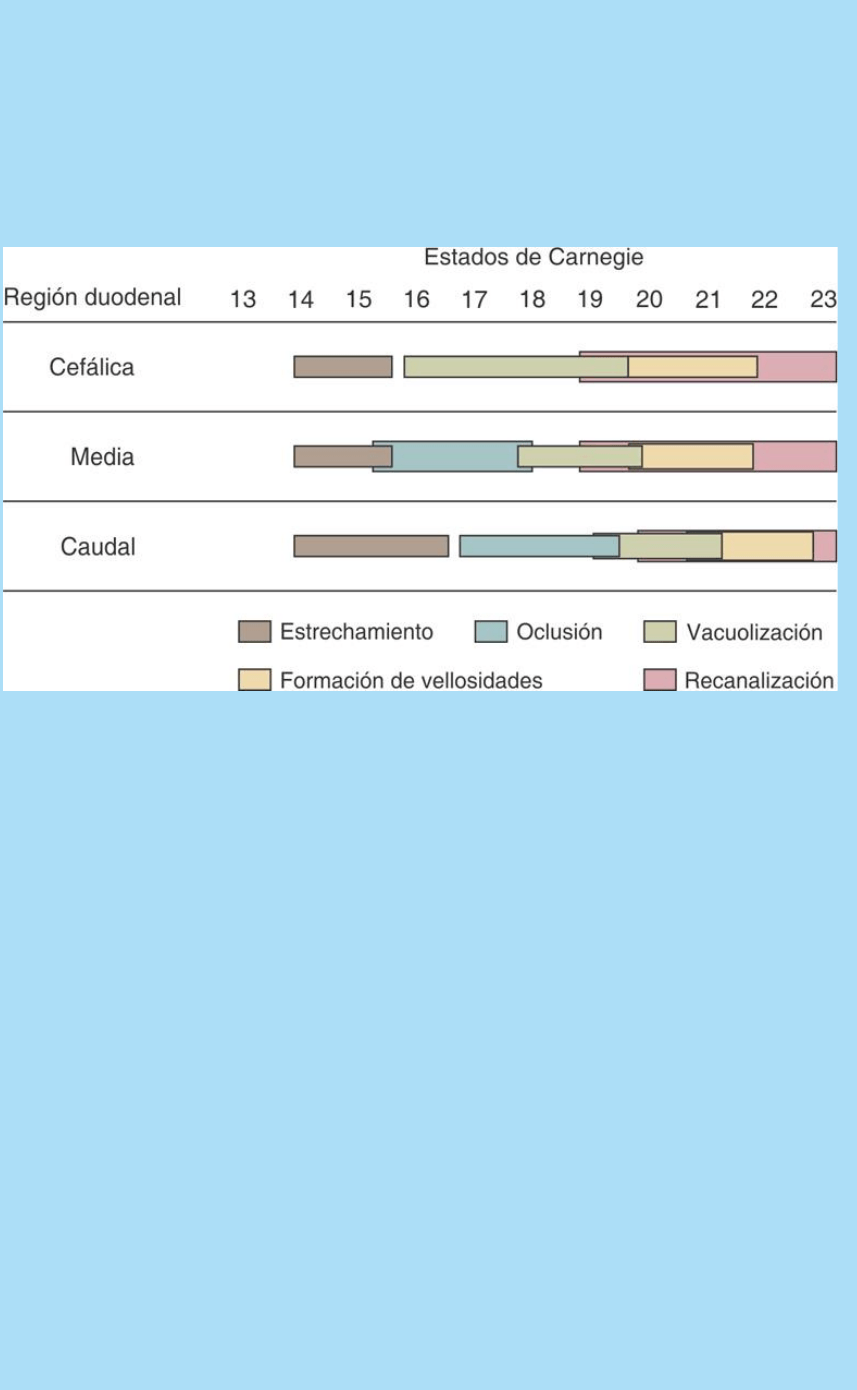
Fig. SC 6-1-2. El gráfico ilustra el progreso, en función del estado de
desarrollo, de las etapas mencionadas en las regiones céfalica,
media y caudal del duodeno humano. Puede observarse que los
estados progresan de acuerdo con un gradiente temporoespacial
céfalo-caudal. La región cefálica no posee fase de oclusión. En las
tres regiones la recanalización ocurre simultáneamente con la fase
de formación de vellosidades.
Este proceso ha sido estudiado en los tercios superior medio y distal
del duodeno de embriones humanos (del 30º al 52º día; estados 13
al 23 del Carnegie Institute) registrando la sucesión temporoespacial
de los 5 estados histogenéticos incluidos en la histogénesis
duodenal: 1) estrechamiento de la luz, 2) oclusión (obliteración
completa), 3) vacuolización, 4) recanalización de la luz y 5) formación
de vellosidades. La figura SC 6-1-1A-H muestra todos esos estados
histogenéticos. La figura SC 6-1-2muestra el progreso, en función del
estado de desarrollo, de las etapas mencionadas en cada una de las
regiones duodenales estudiadas y revela que: a) los estados
progresan de acuerdo con un gradiente temporoespacial céfalo-
caudal,b) la primera porción del duodeno no se ocluye
completamente y c) la recanalización y formación de vellosidades
ocurren simultáneamente.

Diversos estudios cuantitativos sobre la densidad de células en
proliferación y células apoptóticas en cada una de estas etapas y en
cada una de estas regiones indican que durante el período de
oclusión de la luz no existe un aumento de la proliferación en ninguna
de las regiones estudiadas. Por otro lado, la proliferación aumenta
luego de la fase maciza; cuando se inicia la vacuolización,
recanallización y formación de vellosidades. Durante esta fase
también aumenta el calibre del órgano. Por otro lado, la
recanalización no se acompaña de aumento en la muerte celular.
Este parámetro es fluctuante y no supera la tasa de muerte de las
fases previas. En consecuencia, no son la proliferación y la muerte
los CCD responsables de producir las fases sólida y de
recanalización, respectivamente.
El fenómeno más importante en ambos procesos parece ser un
reordenamiento de las células epiteliales en el plano del epitelio (Fig.
SC 6-1-1 A-H). Este proceso lleva a una estratificación y oclusión de
la luz: 1) el sitio de máxima acumulación de células epiteliales, y
consiguiente engrosamiento, es la zona adyacente al mesoduodeno
dorsal. De ahí la forma semilunar de la luz durante la fase de
estrechamiento; 2) durante la oclusión total, las células centrales
pierden su polaridad epitelial en tanto que las periféricas conservan
su dominio basal y mantienen la regularidad epitelial; 3) por último,
en la fase de recanalización, las células se redistribuyen
intercalándose y posibilitando la elongación del sector.
La muerte celular parece tener una función morfogenética durante la
formación de vellosidades. Los sitios en los que aparecen las
cavidades intraepiteliales se relacionan típicamente con sitios en los
que el mesénquima crece en dirección hacia la luz. Este crecimiento
centrípeto del mesénquima genera pliegues en el epitelio a partir de
los cuales luego se modelan las vellosidades (puntas de flecha
en figura SC 6-1-1 G y H). Así, el proceso de recanalización no
implica sólo adquisición de la luz sino principalmente una modelación
de la mucosa de modo que, al mismo tiempo que se recanaliza, se
genera la morfología típica de la mucosa de cada región del tubo
digestivo.
SC 6.2. El tabicamiento de la cloaca como resultado de
crecimiento diferencial. M.P. Bidondo, V. Flores
El interés en comprender el tabicamiento de la cloaca se debe a su
alta tasa de alteraciones fenotípicas y se remonta a principios del
siglo xix. Las descripciones clásicas explican el tabicamiento de la
cloaca como el crecimiento en sentido caudal (descendente) del

tabique urorrectal: este tabique mesenquimático, recubierto por el
endodermo, crecería en dirección a la membrana cloacal y se fusiona
con ella. Otra interpretación propone la formación de dos tabiques
laterales que se unen en la línea media en sentido descendente.
Finalmente, otra reúne las dos interpretaciones y lo explica como
resultado del crecimiento de los tres tabiques mencionados.
Numerosos datos provenientes de la cirugía correctiva, la
neonatología, la histopatología y de la experimentación en mamíferos
ponen de manifiesto un proceso más elaborado y permiten una
explicación diferente. En embriones humanos no existen tabiques
laterales. El mesénquima que separa el seno vesicourogenital del
seno rectal proviene del ángulo entre el alantaoides y el intestino
posterior. Dicha zona está ocupada por a) mesénquima somático
extraembrionario (del pedículo de fijación), b) mesénquima visceral
(del intestino posterior) y c) mesénquima derivado de la zona inferior
de la placoda corporal ectodémica o anillo ectodérmico umbilical que
por invaginación se introducen en el mesénquima. Para detalles
véaseNormal and abnormal embryonic development of the
anorectum in human embryos (Nievelstein R, 1998).
El desarrollo de la cloaca involucra cambios morfológicos y de
posición resultantes del crecimiento diferencial global del embrión y
del crecimiento diferencial regional (región umbilical y apéndice
caudal). Este crecimiento diferencial se aprecia en los siguientes
hechos:
a) en el período sómítico temprano, vista lateralmente, la cloaca
posee contorno triangular y la membrana cloacal tiene una posición
paralela al eje longitudinal del intestino posterior (Fig. SC 6-2-1 A-E).
b) Con la formación del tubérculo genital y de la pared abdominal
infraumbilical, la cloaca adquiere un contorno más rectangular.
c) La regresión del apéndice caudal y el consiguiente
enderezamiento de la curvatura acompañan la adquisición del
aspecto rectangular de la cloaca. Debido a estos crecimientos
diferenciales, la membrana cloacal, desde la 6ª SD en adelante, pasa
gradualmente a adquirir una posición perpendicular al eje longitudinal
del intestino posterior (Fig. SC 6-2-1 F-G).
d) A continuación se produce la disgregación de la membrana
cloacal, por muerte celular programada, sin que ella tome contacto
con el tabique urorrectal. Finalmente,
e) el epitelio del extremo caudal de la cloaca, inmediatamente por
encima del sitio donde se insertaba la membrana cloacal, prolifera,
se engruesa, la luz se ocluye transitoriamente, pasa por una fase
maciza y luego se recanaliza. Los cambios de posición y tamaños
relativos asociados a los procesos descritos generan la impresión de
que el septum urorrectal desciende en dirección a la membrana
cloacal y contacta con ella dividiendo la cloaca en dos
compartimentos .
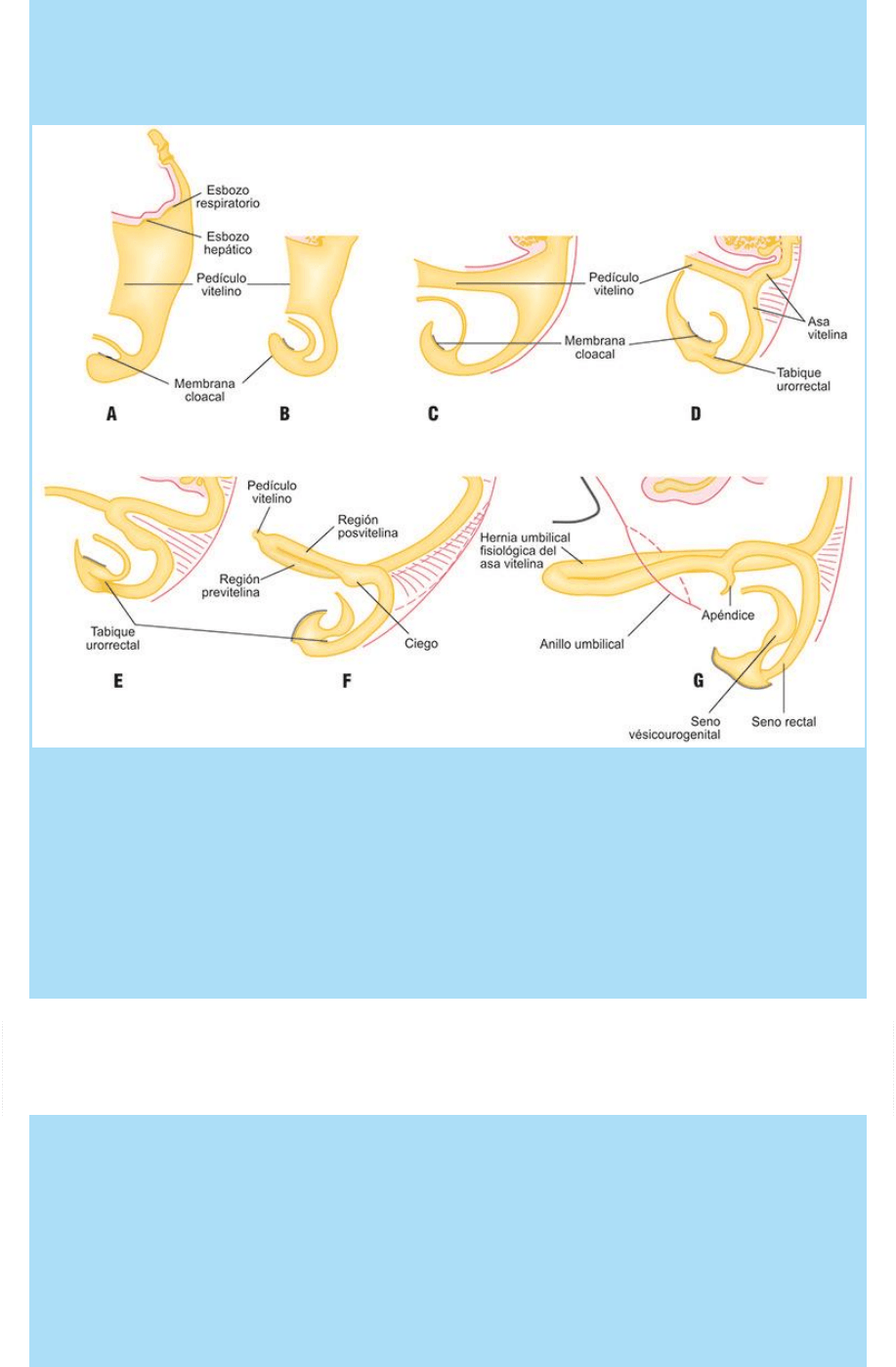
Fig. SC 6-2-1. Representación esquemática, en vista lateral
izquierda, del proceso morfogenético de tabicamiento de la cloaca y
formación de los senos rectal y vesicourogenital. En el ángulo que se
forma entre el alantoides y el intestino posterior confluyen las
poblaciones mesenquimáticas que forman el tabique urorrectal. La
membrana cloacal pasa de poseer una posición paralela al eje
longitudinal del intestino posterior a tener una posición perpendicular
a él
SC 6.3. Efectos de desarrollo de las interacciones epitelio-
mesenquimáticas en el desarrollo del tubo digestivo. V. Flores,
M.P. Bidondo
En general, los órganos de origen esplacnopleural poseen
parénquima epitelial derivado del endodermo y estroma conectivo
derivado del mesénquima visceral. El desarrollo de estos órganos,
como el de todo el tubo digestivo, resulta de cascadas de Int e-
m entre ambas poblaciones celulares.
Los papeles (emisor o receptor de señales; determinante o
competente, etc.) que desempeñan el epitelio y el mesénquima en
cada una de tales Int e-m varían en función de los órganos y las

etapas de desarrollo. En la ejecución de algunos eventos, el epitelio
es instructivo y el mesénquima competente. En otros eventos, los
papeles pueden invertirse.
Existen tipos diferentes de Int e-m a juzgar por los efectos de
desarrollo que producen: a) fenómenos tróficos o de sobrevida
mediados por factores de crecimiento que estimulan las funciones
vitales y evitan ingresar en vías apoptóticas; b) fenómenos directivos,
instructivos o determinantes que participan en la génesis de los
esbozos; c) fenómenos permisivos que intervienen en los procesos
de diferenciación; d) estímulos proliferativos mediados por la síntesis
de factores de crecimiento; e) efectos morfogenéticos y de
mantenimiento del estado de diferenciación terminal del parénquima
epitelial; f) control de la organización espacial del órgano (patrón
espacial de ramificaciones o patrón morfogenético de las mucosas).
Ejemplificaremos cada uno de estos tipos de Int e-m.
a) El mesénquima estimula las funciones vitales de las células
epiteliales. Éstas son importantes para el mantenimiento y desarrollo
de los esbozos. Extractos de embriones enriquecidos en
componentes mesenquimáticos pueden reemplazar algunos efectos
del mesénquima. Es probable se trate de efectos mediados por
factores de crecimiento y/o componentes de la matriz extracelular.
Existen ejemplos de esbozos en los que el aislamiento del epitelio
respecto del mesénquima produce la degeneración o la muerte. En
el caso de estructuras epiteliales macizas transitorias, las células que
ocupan regiones centrales pierden su contacto con el mesénquima y
pasado cierto tiempo ingresan en la vía de la apoptosis. El
mesénquima es fuente de muchas sustancias que actúan como
señales que garantizan la vitalidad de las células y otras que evitan
que las células entren en apoptosis.
b) Existen ejemplos de formación de esbozos en los que la señal
determinante proviene del mesénquima y el endodermo actúa como
población competente. Estos fenómenos instalan las diferencias
entre distintas regiones del tubo digestivo. Clásicamente se
considera que corresponde al mesénquima especificar las
características regionales del tubo digestivo y de cada órgano anexo.
Como ejemplo, si el endodermo de la región pancreática es disociado
de su mesénquima, antes de la constitución del esbozo pancreático,
y es asociado con mesénquima de otra región, en lugar de desarrollar
un páncreas, adquiere las características de la región de donde
procede el mesénquima. Estos ejemplos ilustran el papel
determinante del mesénquima visceral.

c) La determinación de un esbozo no garantiza la completitud de su
desarrollo (SC 0.5. El concepto de determinación. Potencia y
significado evolutivos; SC 0.6.Concepto de acción celular
determinante (A c-c D).). La reprogramación de la información
genética sufrida por las células de un esbozo en el momento de su
determinación no habilita toda la información necesaria para el
desarrollo ulterior. En general, en la determinación sólo se
seleccionan conjuntos de genes que actuarán en la etapa siguiente
inmediata. El desarrollo ulterior habitualmente está regido por
fenómenos interactivos permisivos que favorecen avances parciales
de la diferenciación (SC 0.8. El perfil evolutivo del grado de
diferenciación celular. El papel de las acciones celulares
permisivas). El fenómeno de determinación por el que se constituye
un esbozo en general es seguido por otros fenómenos de
determinación que van de lo general a lo particular. Cada una de
estas determinaciones son seguidas de sus correspondientes fases
permisivas y correspondientes avances parciales en la
diferenciación. La mayor parte de las interacciones que participan en
procesos de morfogénesis e histogénesis y también en el
mantenimiento del estado de diferenciación terminal son permisivas.
Existen ejemplos que ponen de manifiesto la importancia de las
interacciones permisivas. Algunos esbozos sólo pueden continuar su
desarrollo en asociación con el mesénquima determinante. El grado
de especificidad de las interacciones permisivas varía entre
diferentes esbozos.
d) La proliferación celular produce un aumento en el número de
células de una población y, ejecutada diferencialmente y asociada a
cambios de forma o de adhesividad celular, tiene varios efectos
morfogenéticos. El tamaño y la forma de los órganos son
dependientes de las tasas de proliferación que exhiben durante el
desarrollo. El tamaño es función del número de células y éste
depende del número de ciclos celulares cumplidos durante el
desarrollo. El número medio de células de un órgano es el resultado
del balance entre procesos contrapuestos de proliferación y muerte
celular y, en el caso de órganos de parénquima epitelial, ambos
procesos dependen de señales del mesénquima (factores
mitogénicos, factores de crecimiento, factores de sobrevida, etc.). La
influencia del mesénquima sobre la proliferación del epitelio se pone
de manifiesto en experiencias de disociación y reasociación de
endodermo y mesénquima. El epitelio separado del mesénquima o
puesto en contacto con diferentes tipos de mesénquima muestra
cambios significativos en la incorporación de timidina.

e) Establecida la especificidad de órgano, o de región, las células
epiteliales pueden tener varías vías posibles de diferenciación. En el
epitelio intestinal hay enterocitos, células enteroendocrinas,
caliciformes y de Paneth, etc. En general, el mesénquima tiene un
papel en la diferenciación y en el mantenimiento del estado de
diferenciación terminal del epitelio. Estos efectos del mesénquima
también se revelan en situaciones de disociación de endodermo y
mesénquima. Aislado del mesénquima, el epitelio pierde las
características de diferenciación parcial o terminal. Las células
epiteliales pueden volver a organizarse como epitelio, si son
reasociadas con su mesénquima original. Estos efectos están
mediados por fenómenos interactivos recíprocos entre ambas
poblaciones.
f) El mesénquima desempeña un papel central en la organización
espacial del órgano, el patrón espacial de ramificaciones o patrón
morfogenético de las mucosas, etc. (SC El papel morfogenético del
mesénquima. La remodelación regulada de la matriz extracelular
como mecanismo de control del patrón de ramificaciones de un
órgano epitelial).
SC 6.4. Patrón de migración de las células precursoras de
neuronas parasimpáticas en el tubo digestivo. M.P. Bidondo, V.
Flores
En 1921 J.N. Langley describió el sistema nervioso entérico (SNE)
como una parte del sistema nervioso autónomo. Se trata de un
conjunto de plexos interconectados que asientan en la pared, a lo
largo de las diversas regiones del tubo digestivo (plexos murales) y
en los mesos (plexos extramurales). Los plexos murales se ubican
preferentemente en la capa submucosa (plexo submucoso de
Meissner) y entre las capas circular y longitudinal de la muscular
(plexo mientérico de Auerbach). Estos plexos se forman durante la
histogénesis del tejido muscular del tubo digestivo (SC La unidad
motora peristáltica. Cuadro cronológico sobre su diferenciación). El
SNE regula la motilidad, secreción, absorción, flujo sanguíneo, etc. e
integra un sistema neuroendocrino-inmunitario en el aparato
digestivo.
Debido a que el SNE dispone de sus propias neuronas receptoras,
neuronas de asociación y neuronas efectoras excitatorias e
inhibitorias, es capaz de originar respuestas locales de un modo
reflejo aun en ausencia de conexión con SNC.
El SNE se origina a partir de dos poblaciones celulares precursoras
específicas: la cresta neural vagal correspondiente a los niveles

segmentarios occipitales (segmentos 1-7) y la cresta neural
sacra correspondiente a los niveles desde 28 en sentido caudal. Esto
no significa que las células de dichos segmentos estén determinadas
a formar neuronas para el SNE.
Varios experimentos de trasplante de células de la cresta vagal a la
región troncal y de células de la cresta troncal a la cresta vagal
muestran que estas células no están determinadas en el momento
de su formación. En ambos casos, las células exhiben un
comportamiento de desarrollo acorde con el lugar al que son
trasplantadas. Ello indica que los medioambientes en los que las
células son puestas y/o aquellos a través de los cuales migran, y/o
las interacciones que realizan en los sitios que colonizan son los
determinantes y/o permisivos. Resultados similares se obtienen en
trasplantes celulares recíprocos entre células de la cresta sacra y
células de la cresta troncal.
Un ejemplo ilustrativo de la importancia del ambiente sobre la
sobrevida y la diferenciación de las células precursoras del SNE lo
ofrecen los componentes de la matriz extracelular a través de la cual
migran. Tanto la población vagal como la sacra expresan la proteína
receptor transmembrana Ret. Los componentes de la matriz celular
a través de la cual migran se unen a dicho receptor activando una vía
de señalización que, por un lado, mantiene la población y, por otro,
actúa permisivamente en la diferenciación en sentido de SNE.
El desarrollo del SNE procede a través de dos fases
citogenéticas: a) la primera fase es de migración y
colonización de los mesos y la pared del tubo digestivo (4ª a 7ª SD)
y b) la segunda fase es específicamente histogenética o
de formación de los plexos (7ª SD en adelante).
Durante la etapa de migración y colonización, la población vagal
invade primero el mesénquima de los arcos branquiales y en la 4ª SD
ya se introduce en la esplacnopleura del intestino anterior. De ahí en
más, la migración continúa en sentido caudal invadiendo todo el tubo
digestivo al final de la 7ª SD. En la migración de las crestas neurales
participan fenómenos dehaptotaxis y de presión de población. El
primero parece ser más importante como factor director de los
desplazamientos ya que la inyección de una pequeña cantidad de
células de la cresta neural vagal en el estómago de un tubo digestivo
aganglionar permite ver que las células migran en sentido caudal aun
sin el efecto de la presión de población.
La población sacra en una primera fase sólo posee distribución
extramural, luego invade también el intestino posterior en forma
ascendente. Si bien al principio ocupan difusamente toda la región

infraumbilical, finalmente quedan localizadas sólo a la porción final
del intestino posterior. Sólo el 17 % de las neuronas del SNE se
originan en la cresta neural sacra.
La etapa de formación de plexos es simultánea con la
diferenciación de la musculatura lisa del tubo digestivo. Si bien la
miogénesis no depende del desarrollo de los plexos nerviosos y de
la inervación, ambos procesos se producen sincrónicamente. Con
respecto a la regulación de la peristalsis, cuatro tipos celulares, dos
originados en las crestas neurales y dos originados en el propio
mesénquima visceral, interactúan y conforman la unidad motora
peristáltica (véase SC La unidad motora peristáltica. Cuadro
cronológico sobre su diferenciación). Varios estudios de
inmunomarcación con anti-cKit (para células intersticiales de Cajal,
anti-α-actina (para célula muscular lisa), anti-PGP9.5 (para
neuronas) y anti-S100 (para glía) han permitido seguir la evolución
de estos linajes celulares, analizar la cronología de su diferenciación,
su organización espacial y la elaboración de la unidad motora
peristáltica. En el embrión humano, éstas se estructuran entre la 7ª y
20ª SD período durante el cual simultáneamente se diferencian las
capas musculares interna y externa, la muscular de la mucosa y los
plexos del SNE.
En la 7ª SD se inicia la diferenciación de las células intersticiales. Se
diferencian en miofibroblastos fusiformes a partir de células del
mesénquima visceral. Debido a ello sólo aparecen en la porción de
tubo digestivo de origen esplacnopleural (intestino primitivo). Estas
células generan varias prolongaciones que, por un lado, entran en
contacto con varicosidades (terminales) de axones del SNE y, por
otro, contactan y elaboran uniones nexo con otras células, también
originadas en el mesénquima visceral, que se diferencian en músculo
liso. Las células intersticiales se diferencian en células
especializadas ramificadas que operan como marcapasos para la
peristalsis. Generan impulsos eléctricos y lo propagan a través de los
contactos de sus ramificaciones en forma de ondas desde la unión
faringoesofágica hasta el esfínter anal interno. Las células
intersticiales se diferencian en contigüidad con células de las crestas
neurales aunque tal relación no parece ser indispensable pues
también están presentes en intestinos aganglionares. Dicha relación
al menos condiciona su distribución espacial; en la 7ª SD se
encuentran en relación con las neuronas en diferenciación y
posteriormente se ubican periféricamente a los plexos.
SC 6.5. La derivación de los linajes celulares que integran el
parénquima pulmonar a partir del componente epitelial
endodérmico del esbozo pulmonar. La organización del
proceso a lo largo del eje próximo-distal. V. Flores
Corregir pseudoglandular => seudoglandular
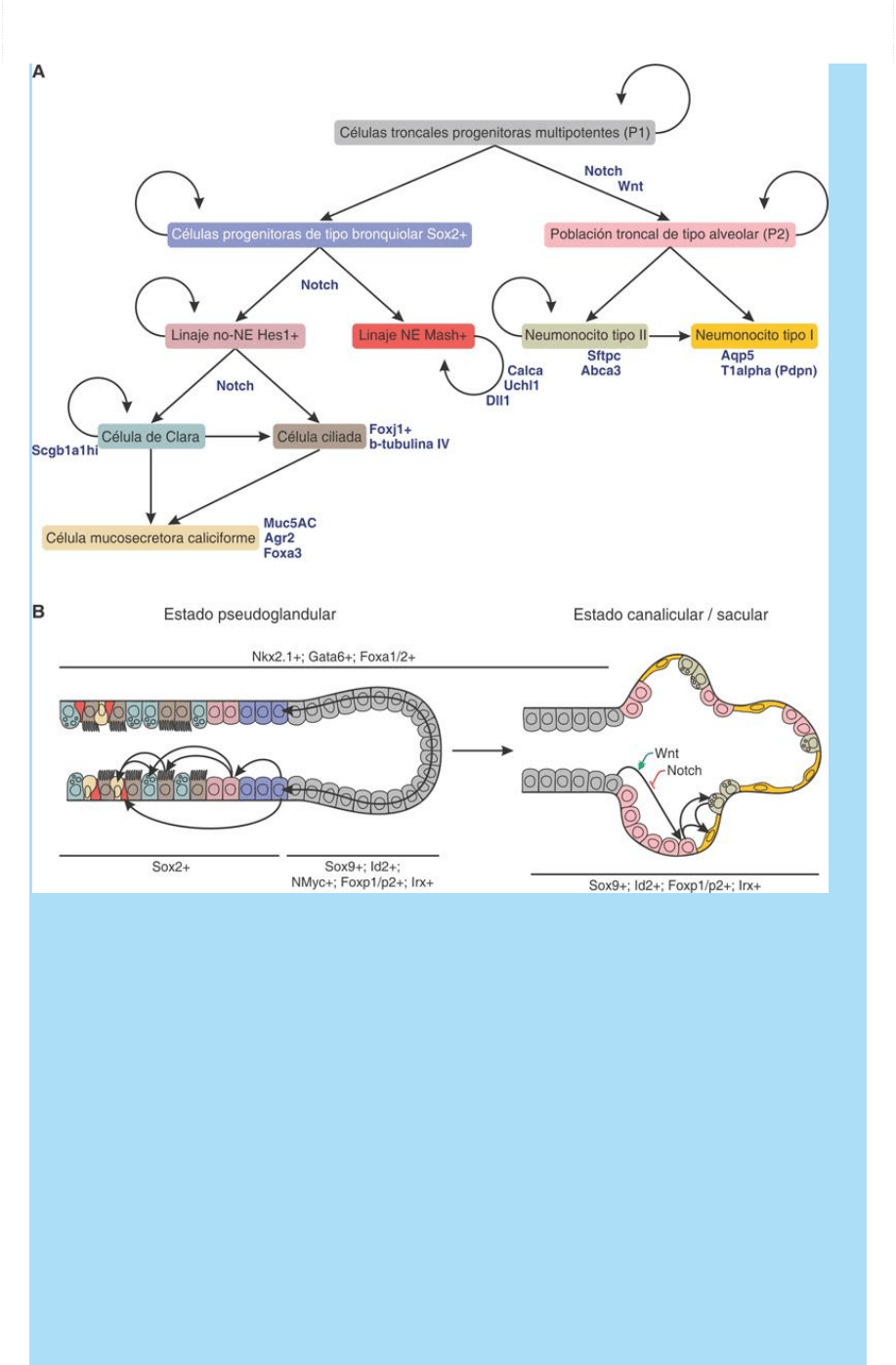
Fig. SC 6-5-1. Modelo de derivación de tipos celulares del
parénquima pulmonar a partir del endodermo de los esbozos
broncopulmonares. A. Representación esquemática del árbol de
derivaciones. B. Representación gráfica del modo como se organiza
en el espacio el proceso de derivación ilustrado en A. Se incluyen los
estados (asociados al transcurso del tiempo) y la ubicación espacial
de las células a lo largo del eje próximo-distal del órgano. Se indican
algunas de las vías de señalización y de los factores de transcripción
que participan del proceso.
Los esbozos broncopulmonares están compuestos por dos
componentes: a) un componente epitelial que origina los tejidos que
integran el parénquima y b) un componente mesenquimático que
genera el estroma del órgano.

Describiremos separadamente la evolución de la citogénesis
(generación de tipos celulares en función del tiempo y espacio) en
cada uno de ambos componentes; sin embargo, ambos procesos se
realizan simultánea e interactivamente.
Con respecto a la evolución del componente epitelial, la figura SC 6-
5-1 A ofrece un panorama global esquemático sobre las sucesivas
bifurcaciones que ocurren durante la generación de diversos linajes
celulares del parénquima pulmonar.
El modelo propone que hasta el final del estado seudoglandular, las
células distales de los brotes epiteliales en crecimiento son células
troncales progenitoras multipotentes (P1). La población celular P1
es mantenida por la expresión de una variedad de factores. La célula
P1, por medio de divisiones asimétricas, se autorrenuevan y
originan células progenitoras de tipo bronquiolar
Sox2+ (expresan el factor de transcripción Sox2). Estas células,
durante el crecimiento en longitud del brote, abandonan el extremo
de crecimiento y pasan a ocupar zonas más proximales que formarán
las vías de conducción aérea. La célula progenitora bronquiolar
posee capacidad de originar todos los tipos celulares epiteliales que
integrarán el epitelio bronquiolar.
Llegado el estado canalicular/sacular, las células P1, como
consecuencia de una reprogramación epigenética, pasan a constituir
una segunda población de células troncales progenitoras (P2) o
población troncal de tipo alveolar, que se encarga de generar las
células epiteliales de las regiones alveolares. No se ha aclarado si
esta reprogramación de célula troncal P1 a célula troncal alveolar
(P2) se debe a factores externos o es resultado de un programa
establecido con anterioridad; algunos experimentos sugieren que
están involucradas las vías de señalización de Notch y Wnt.
Con respecto a la evolución ulterior de las células progenitoras
bronquiolares, un modelo propone que la primera decisión, en la
que participa la vía Notch, es la elección entre un linaje
neuroendocrino (NE) (Mash+) y un linaje no NE (Hes1+).
A continuación, las células del linaje no NE realizan una segunda
determinación, que también involucra a la vía Notch, en la se elige
la vía evolutiva de la célula de Clara o la vía de la célula ciliada.
Las otras vías de determinación indicadas en la figura también son
posibles y planteadas en otros modelos de derivación de linajes. En
este modelo se propone que las células de Clara se autorrenuevan
por mucho tiempo y que, posnatalmente, originan células ciliadas. La
célula de Clara originaría también las células mucosecretantes o
caliciformes. Otros modelos admiten otras posibilidades.

Con respecto a la evolución de las células progenitoras alveolares,
algunos modelos proponen que ésta puede originar tanto
los neumonocitos de tipo I y tipo II. Otros modelos proponen que
la descendencia directa de la célula progenitora alveolar es el
neumonocito tipo II que luego origina a los tipo I. Todos estos
modelos tienen cierto grado de aceptación y requieren evidencia
experimental adicional para su aceptación definitiva.
SC 6.6. Patterning del tubo digestivo I: la regionalización
céfalo-caudal del tubo digestivo I. M.P. Bidondo, V. Flores
Durante la gastrulación ocurren procesos que inician la instalación de
una polaridad céfalo-caudal en el endodermo embrionario. Algunos
mapas de destino realizados en embriones de ave indican que tal
polaridad se pone de manifiesto por la aparición de dos poblaciones
diferentes que, en forma sucesiva, migran desde el epiblasto a la hoja
ventral del disco embrionario originando el endodermo embrionario.
Una de dichas poblaciones es identificable por la expresión del factor
de transcripción Hex1+ (Hematopoietically expressed
homeobox) y, la otra, por la expresión del factor de transcripción
Fox A2+ (Forkhead box A2).
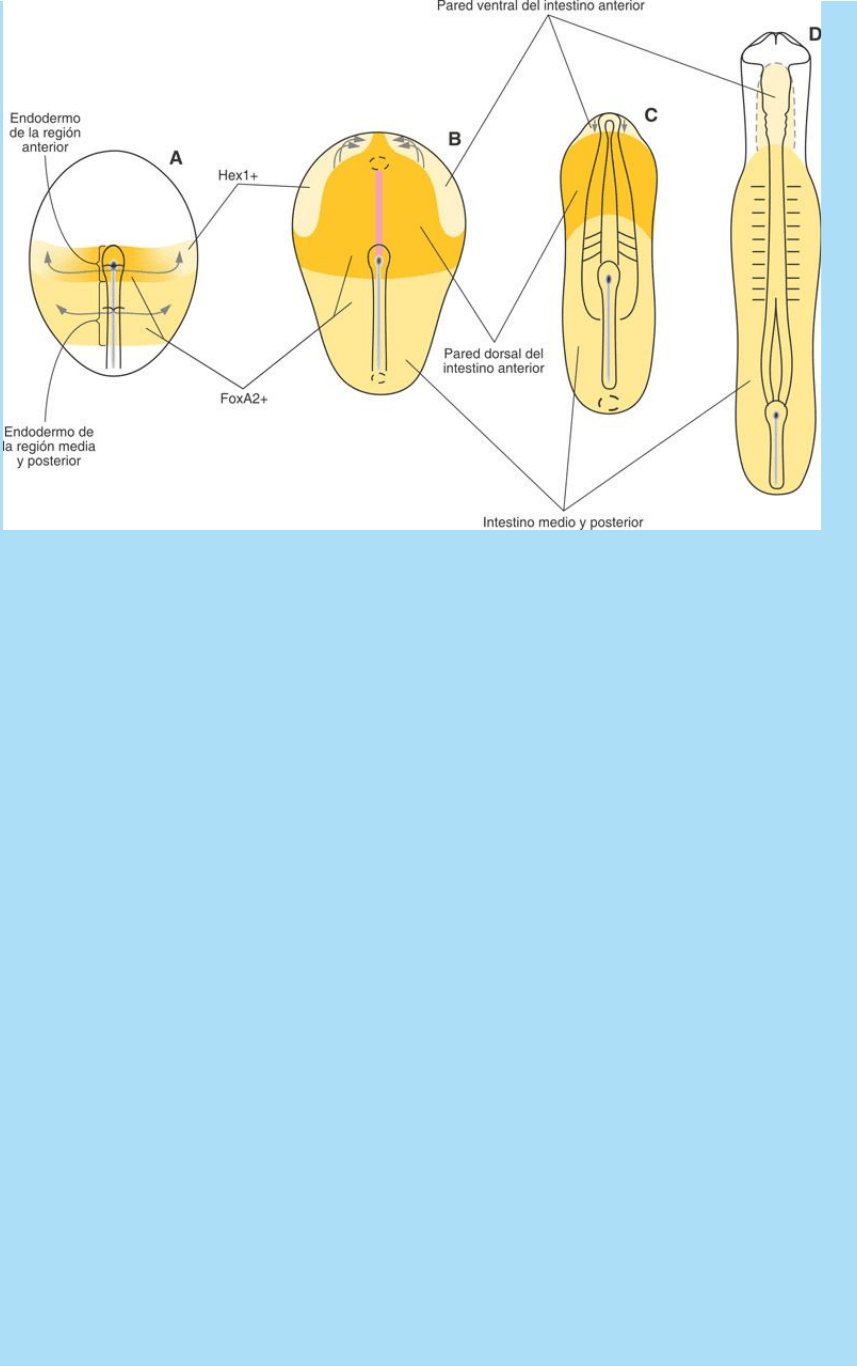
La población Hex1+ corresponde a la primera oleada migratoria
endodérmica, origina el endodermo de la cara ventral del intestino
anterior e interviene, más tarde, en la determinación en sentido
cardiogénico de la hoja esplácnica de la región cefálica del
mesodermo lateral. La población Fox A2+ corresponde a la segunda
oleada y origina el endodermo de la región dorsal del intestino
anterior y el endodermo de los intestinos primitivos medio y posterior
(Fig. SC 6-6-1).
Corregir pseudoglandular => seudoglandular
Fig. SC 6-6-1. Durante la gastrulación se inicia la instalación de la
polaridad cf-cd del intestino primitivo. La población Hex1+
corresponde a la primera oleada migratoria endodérmica, origina el
endodermo de la cara ventral del intestino anterior. La población Fox
A2+ corresponde a la segunda oleada y origina el endodermo del
intestino primitivo medio y posterior.
Durante el plegamiento del embrión, se forman los intestinos
primitivos anterior, medio y posterior y, en los límites entre ellos,
los portales intestinales anterior (PIA) y posterior (PIP). Estos
portales son centros señalizadores que, por medio de la síntesis y
secreción de la proteína señal Shh, participan en el establecimiento
de las polaridades céfalo-caudal y dorsoventral del tubo digestivo. A
su vez, el mesénquima visceral del tubo digestivo primitivo expresa
la proteína receptor de Shh Patched(Ptc). La unión de Shh a su
receptor inicia vías de señalización involucradas en dos fenómenos:
a) expresión de la proteína señal BMP4 en el mesénquima
circundante, hecho que está vinculado a la regulación de la
diferenciación del mesénquima visceral en músculo liso del tubo
digestivo y b) expresión de combinaciones de genes Hox tanto en el
mesénquima como en el epitelio. Existen diferencias regionales en la
respuesta del mesénquima visceral a la secreción de Shh. Estas
diferencias podrían implicar que existe una regionalización previa
puesta de manifiesto por la diferente competencia del mesénquima
esplácnico a Shh.

En respuesta al Shh, el mesénquima expresa Bmp4 a lo largo de casi
todo el intestino primitivo excepto en la futura región gástrica. Dado
que el estómago posee una musculatura más desarrollada, con tres
capas en lugar de dos, se ha propuesto que podría tener una función
reguladora negativa sobre la formación de músculo liso.
b) la proteína señal Shh estimula la expresión de genes Hox. En el
tubo digestivo en desarrollo, tanto el endodermo como el
mesénquima visceral exhiben una expresión diferencial
espacialmente organizada de combinatorias de genes Hox (Fig. SC
6-6-2). Este hecho regularía la elaboración de diferentes patrones de
organización de tejidos a lo lardo del eje céfalo-caudal del tubo
digestivo.
El papel de la expresión diferencial de combinatorias de genes Hox
en la regionalización del tubo digestivo se revela a través de
experimentos en murinos transgénicos en los que la inactivación o la
sobreexpresión de estos genes derivan en un desarrollo anómalo de
la zona (homeosis). En seres humanos también existen datos al
respecto. La mutación del gen Hoxa13 produce transformación
homeótica en el tubo digestivo.
El borde de expresión de las distintas combinatorias de proteínas Hox
no siempre corresponden con las fronteras entre órganos, pero hay
puntos en los que los bordes en la expresión de combinatorias de
genes Hox se corresponde con cambios en la organización, como por
ejemplo en las regiones que corresponden a futuros esfínteres (Fig.
SC 6-6-).
Este documento contiene más páginas...
Descargar Completo
Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.