
SC 4.1. El origen múltiple y la pluripotencialidad del
mesénquima cefálico. El mesodermo paraxil preótico y la
cresta neural craneal. V. Flores, M. Rapacioli
-El mesénquima cefálico. Se denomina mesénquima cefálico a
aquel que ocupa la región cefálica del embrión. Se halla rodeando al
encéfalo, y distribuido regularmente entre éste y el ectodermo
epidérmico. En el ectodermo epidérmico de dicha región se localizan
varias placodas que forman neuroepitelios receptores u otras
estructuras asociadas a los órganos de los sentidos, además de otros
varios tipos celulares. El mesénquima cefálico posee origen múltiple.
Sus células provienen de: a) las cresta neural craneal, principalmente
la esqueletogénica facial, b) el mesodermo paraxil cefálico (craneal
o preótico), c) el mesénquima axil precordal, d) algunas placodas
y e) la cresta neural anterior o ANR (Anterior Neural Ridge) o zona
organizadora del presencéfalo. La población celular mayoritaria
corresponde al ectomesénquima originado en la cresta neural
esqueletogénica facial (SC El patterning de la región craneofacial II.
Factores de transcripción y factores de crecimiento intervinientes;
SC El patterning de la cresta neural craneal. Regiones Hox(+) y
Hox(-). Su relevancia filogenética y sus papeles de desarrollo).
--El mesodermo paraxil cefálico. Es la subpoblación del
mesodermo paraxil que ocupa la región preótica del embrión, con
capacidad miogénica y encargada de formar músculos de la cara y
cuello (cérvico-céfalo-óculo giria, auriculares, mímica, etc.).
Clásicamente se considera que esta región forma pequeños bloques
mesenquimáticos (somitómeros preóticos) cuyas células
rápidamente se desagregan y migran. Sin embargo, basándose en
estudios más recientes, algunos autores consideran que en esta
región no existen indicios morfológicos de organización
segmentaria. De todos modos, la zona exhibe una organización
espacial definida ya que distintas subregiones de él poseen
derivados musculares típicos (SC La organización segmentaria de la
región cefálica: encéfalo, cresta neural y mesodermo paraxil
craneales e intestino faríngeo). Estas células migran ventralmente
acompañando a las células de la cresta neural craneal y aportan los
mioblastos que originan músculos de cara y cuello, así como también
células endoteliales. En pollo y ratón existen estudios que indican que
el mesodermo paraxil cefálico origina también algunas estructuras
óseas del neurocráneo.
-- La cresta neural craneal. La cresta neural craneal es una
población de células progenitoras pluripotentes que origina una

amplia gama de tipos celulares. Éstos pueden agruparse en tres
categorías: a) ectomesenquimáticos, b) neurales y c)melanocíticos.
a) Los derivados mesenquimáticos originan los tejidos conectivos,
cartílagos y huesos del cráneo y cara y dentina.
b) Los derivados neurales incluyen neuronas sensoriales y células
gliales del sistema nervioso periférico de la vida de relación y del
sistema nervioso autónomo.
c) Los derivados de la línea melanocitogénica originan células
pigmentarias de la dermis de la cabeza y del iris (Cuadro SC 4-1-
1: Principales tipos celulares y tejidos derivados de la cresta
neural craneal).
Se ha postulado que la aparición, a lo largo de la evolución, del linaje
ectomesenquimático constituyó una importante contribución al
proceso de cefalización ya que origina los componentes tisulares que
integran el aparato de la contención neurosensorial (SC La
pluripotencialidad y la organización regional y segmentaria de la
región cefálica de la cresta neural).
--El mesodermo axil precordal. Las células del mesodermo axil
precordal inicialmente se ubican alrededor del extremo anterior de la
notocorda en la región donde se formarán la adenohipófisis y la
neurohipófisis. Desde dicha posición muchas células se disgregan y
originan parte del mesénquima regional subyacente en el ectodermo
del techo del estomodeo. Dicha región también es poblada por
algunas células que se desprenden del ectodermo (de la zona ANR
o cresta neural anterior) durante el cierre del neuroporo anterior. En
esta zona también se han identificado células mesenquimáticas que
proceden de la placoda olfatoria y células migrantes de naturaleza
neural desprendidas del órgano vomeronasal.
Las células de la cresta neural y del mesodermo paraxil craneales se
hallan espacialmente organizadas, a lo largo de los ejes céfalo-
caudal y dorso-ventral, y durante su migración mantienen posiciones
típicas. La figura SC 4-1-1 muestra las principales vías migratorias
que ambas poblaciones celulares siguen durante su migración a los
lugares que ocupan en el mesénquima cefálico.
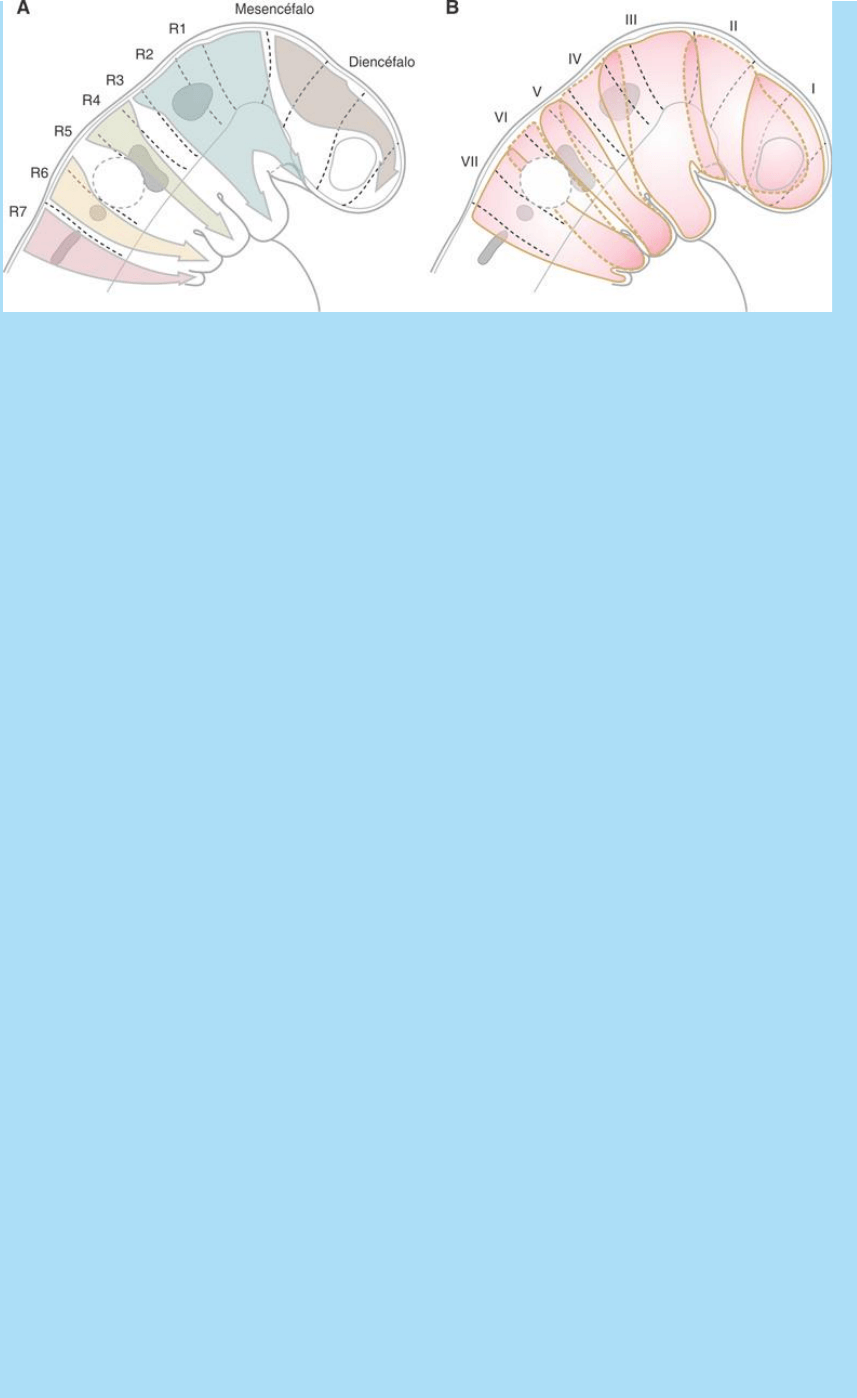
Fig. SC 4-1-1. Ilustra la organización céfalo-caudal de las regiones
cefálica y branquial del embrión. A lo largo del eje céfalo-caudal
existen diferentes vías de migración en sentido dorso-ventral
(flechas) para poblaciones de la cresta neural craneal (A) y el
mesodermo paraxil cefálico (B) que ocupan las regiones craneal y
branquial del embrión. Estos movimientos celulares organizados
posibilitan que la organización segmentaria de las estructuras
dorsales (tubo neural, cresta neural craneal y mesodermo paraxil
cefálico) se transfiera a regiones laterales y ventrales del embrión.
Los números romanos indican la denominación de la región
(somitómero) sin aludir a un concepto estricto de metamerización.
La figura SC 4-1-2 B y C muestra que las células del mesodermo
paraxil migran ventralmente con respecto al ectomesénquima
proveniente de la cresta neural y que las células de la cresta neural
se distribuyen más superficialmente, vale decir, entre el mesodermo
paraxil y el ectodermo. Estas dos poblaciones celulares exhiben una
migración extensa, en sentido ventral, formando arcos faríngeos y
prominencias faciales. La subpoblación neural de células de
cresta neural se queda en una posición más dorsal, adyacente al
tubo neural, donde forman los ganglios sensoriales de los nervios
craneales.
Las células de la cresta neural craneal se segregan del epitelio
ectodérmico, específicamente, de la zona de transición entre el
ectodermo neural y el ectodermo del área preplacodal (SC La
instalación y el refinamiento de la organización espacial de
competencias de desarrollo en el área preplacodal; SC La
transformación del área preplacodal (área competente de formación
de placodas) en línea wolffiana (área de placodas) del sistema
sensorial cefálico). Estas células sufren una T e-m y migran desde
los pliegues neurales al mesénquima antes del cierre definitivo del
tubo neural. Estas células disponen de varias vías o patrones de
migración a través de las cuales llegan a diferentes regiones del
embrión, donde contribuyen a la formación de diversas estructuras.
Las células de la cresta neural craneal que derivan del diencéfalo,
mesencéfalo y rombencéfalo, difieren de la cresta neural del tronco
en que tienen el potencial de diferenciarse en cartílago, hueso y tejido
conectivo (véase Cuadro SC 4-1-1 y SC La potencia de desarrollo
de la cresta neural craneal).
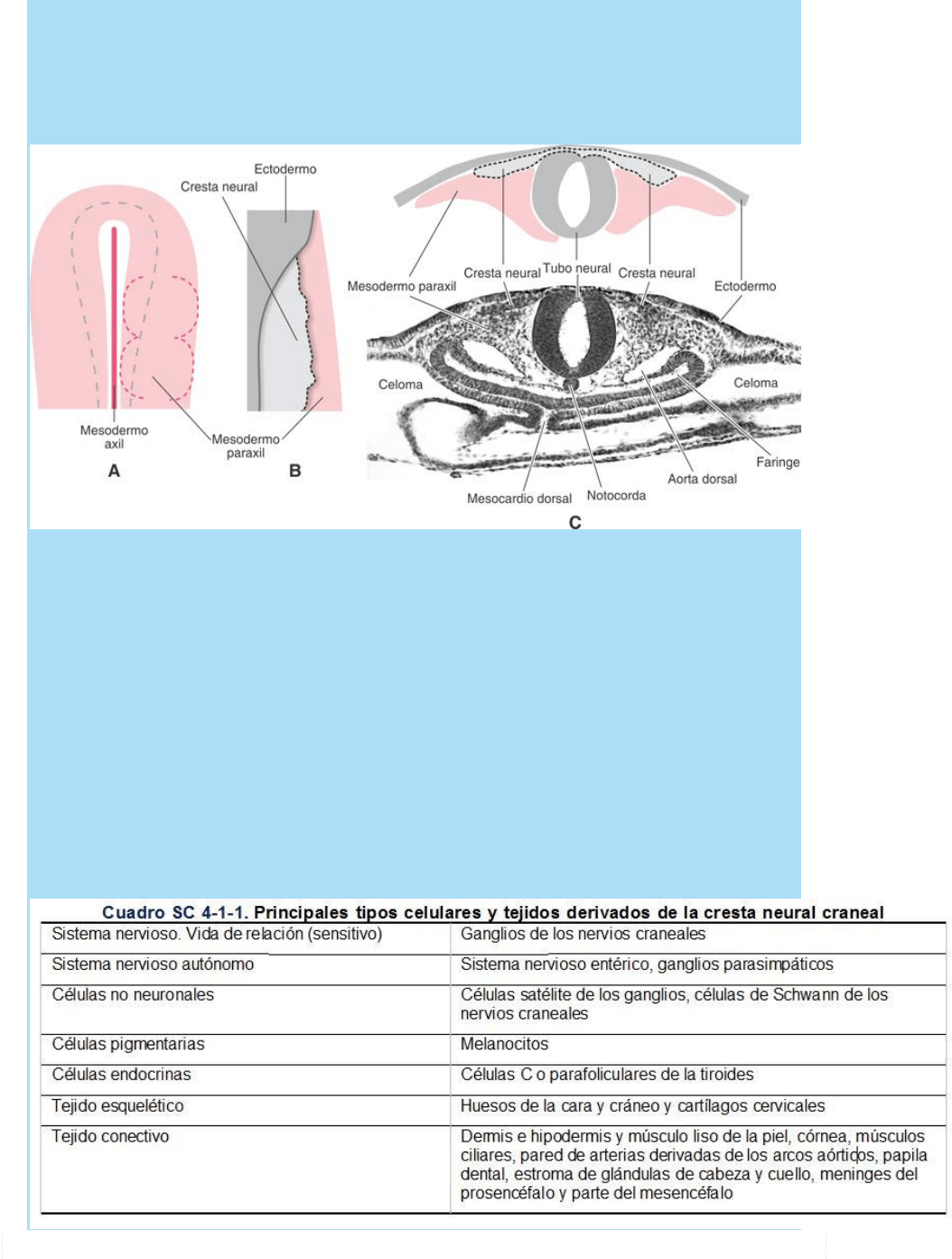
Fig. SC 4-1-2. Esquemas que ilustran la organización de los tejidos
cefálicos mesenquimáticos y epiteliales. A. Vista dorsal de embrión
de 4 somitas. Se ha eliminado el ectodermo general y el tubo neural,
dejando al descubierto el mesodermo paraxil (rosa). Los corchetes
indican los límites de supuestos somitómeros. B. Vista dorsal de la
mitad izquierda de embrión de 10 somitas. El tubo neural se halla en
su lugar (visible a la izquierda). El borde de avance de la cresta neural
(gris) cubre parcialmente el mesodermo paraxil (rosa). C. Corte
transversal, al nivel del posencéfalo, de un embrión de 10 somitas.
Muestra las posiciones de las células de la cresta neural y del
mesodermo paraxil y sus posiciones relativas respecto del tubo
neural, el ectodermo epidérmico y el endodermo faríngeo.

SC 4.2. ¿Cómo se generan y cómo desaparecen las curvaturas
del embrión? V. Flores
Desde el fin de la 3ª SD (momento en que el embrión es plano) hasta
el final de la 5ª SD, el embrión sufre un crecimiento diferencial que lo
convierte en cilíndrico y con una curvatura de convexidad dorsal.
Durante un tiempo, la curvatura dorsal se hace más pronunciada,
luego se estabiliza y, finalmente, ya en etapa fetal, el esqueleto axil
se rectifica gradualmente y la convexidad dorsal va desapareciendo.
La aparición de la convexidad dorsal embrionaria resulta del hecho
de que los elementos que ocupan la superficie dorsal del embrión
crecen en longitud (eje céfalo-caudal) y transversalmente (ejes
medio-laterales) bastante más que los que ocupan la superficie
ventral. Nótese que las superficies laterales y ventral del embrión
poseen pocas estructuras o tejidos en desarrollo y,
proporcionalmente, ocupan poco volumen en relación con los que se
ubican en la región dorsal.
Basta analizar un corte transversal del embrión para notar que
prácticamente todos los elementos, con excepción de algunas partes
del tubo digestivo se encuentran en la pared dorsal (tubo neural,
notocorda, mesodermo paraxil) o pegados a ella (cresta urogenital y
la mayor parte del tubo digestivo). Sólo dos elementos, corazón e
hígado, se ubican en la zona más ventral (Fig. SC 4-2-1).
Fig. SC 4-2-1. Secuencia de cortes transversales de embriones de
edad creciente. Ilustra el crecimiento relativo de la región dorsal
respecto de la ventral. Todos los esquemas están representados en
la misma escala.
El efecto del crecimiento diferencial en longitud (a lo largo del eje
céfalo-caudal [cf-cd]) se nota aún más cuando se compara la
disposición en el espacio de los dos elementos mediales dorsales: el
tubo neural y la notocorda. La figura SC 4.2-2 muestra la disposición
de ambas estructuras, proyectadas sobre el plano sagital, en
embriones de diferentes edades (desde la 3ª SD al final de la 5ª SD)
(Figura SC 4.2-2). Puede notarse que, durante el período
considerado, el tubo neural crece en longitud visiblemente más que
la notocorda. Debido a ello, al principio, prácticamente poseen la
misma longitud en tanto que, al final, el trazado del contorno de la
superficie dorsal del tubo neural posee una longitud visiblemente
mayor que la longitud de la notocorda. Ésta es la razón por la que al
final de la 5ª SD el extremo cefálico del tubo neural, la parte de éste
que excede cefálicamente a la notocorda, se encuentra muy
incurvada en la región cefálica del embrión. El mismo fenómeno
puede observarse comparando la longitud de la superficie ventral y
la de la superficie dorsal en los esquemas de la figura SC 4-2-2.
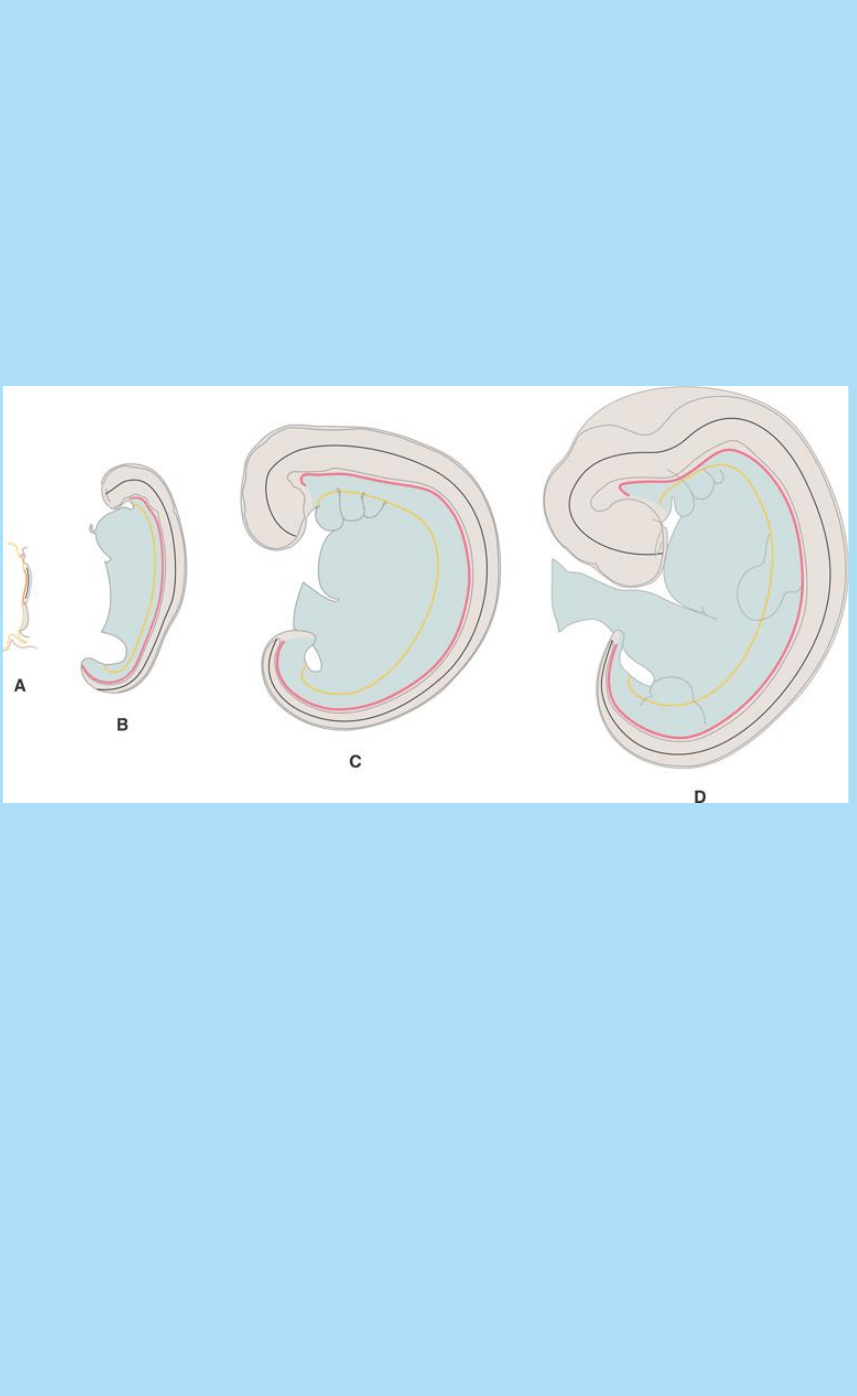
Fig. SC 4-2-2. Esquema de embriones de A. 3ª SD, B. mediados de
4ª SD, C. fines de 4ª SD y D. fines de 5ª SD. Las regiones dorsal y
ventral a la notocorda están pintadas de diferente color. Las líneas
negra, roja y amarilla representan el eje cf-cd del SNC, la notocorda
y el tubo digestivo respectivamente. Nótese que crecen
diferentemente en función del tiempo. Todos los esquemas están
representados en la misma escala.
Nótese que la situación descrita para el embrión como totalidad se
cumple también para el tubo neural en particular: el crecimiento en
longitud de la superficie dorsal del tubo neural (placa del techo o
placa alar) es mayor que el de la región ventral (placa del piso o
placas basales). Estas diferencias, en el crecimiento en longitud,
entre placas alares y basales es sobre todo marcada en las
estructuras posencefálicas y mesoencefálicas. De ahí, la marcada
curvatura cervical (entre médula y mielencéfalo) y sobre todo la
marcada curvatura cefálica y mesencefálica, debido a la ausencia de
placa basal en el proencéfalo.
Además de todos estos hechos, la mayor parte de las poblaciones
celulares que formarán las porciones laterales y ventrales de la
paredes corporales provienen de los somitas y, hasta la 5ª SD, ellas
se encuentran en posición epiaxial (dorsal a la notocorda). Desde el
final de la 5ª SD en adelante, las células correspondientes a todos
los niveles segmentarios corporales empiezan a migrar masivamente
en dirección ventral. Las células o grupos celulares que abandonan
posiciones epiaxiales y pasan a ocupar posiciones hipoaxiales
contribuyen con su desplazamiento a generar un crecimiento
diferencial con predominio en la región ventral a expensas del
crecimiento en la región dorsal. La figura SC 4-2-3 ilustra
esquemáticamente este hecho.
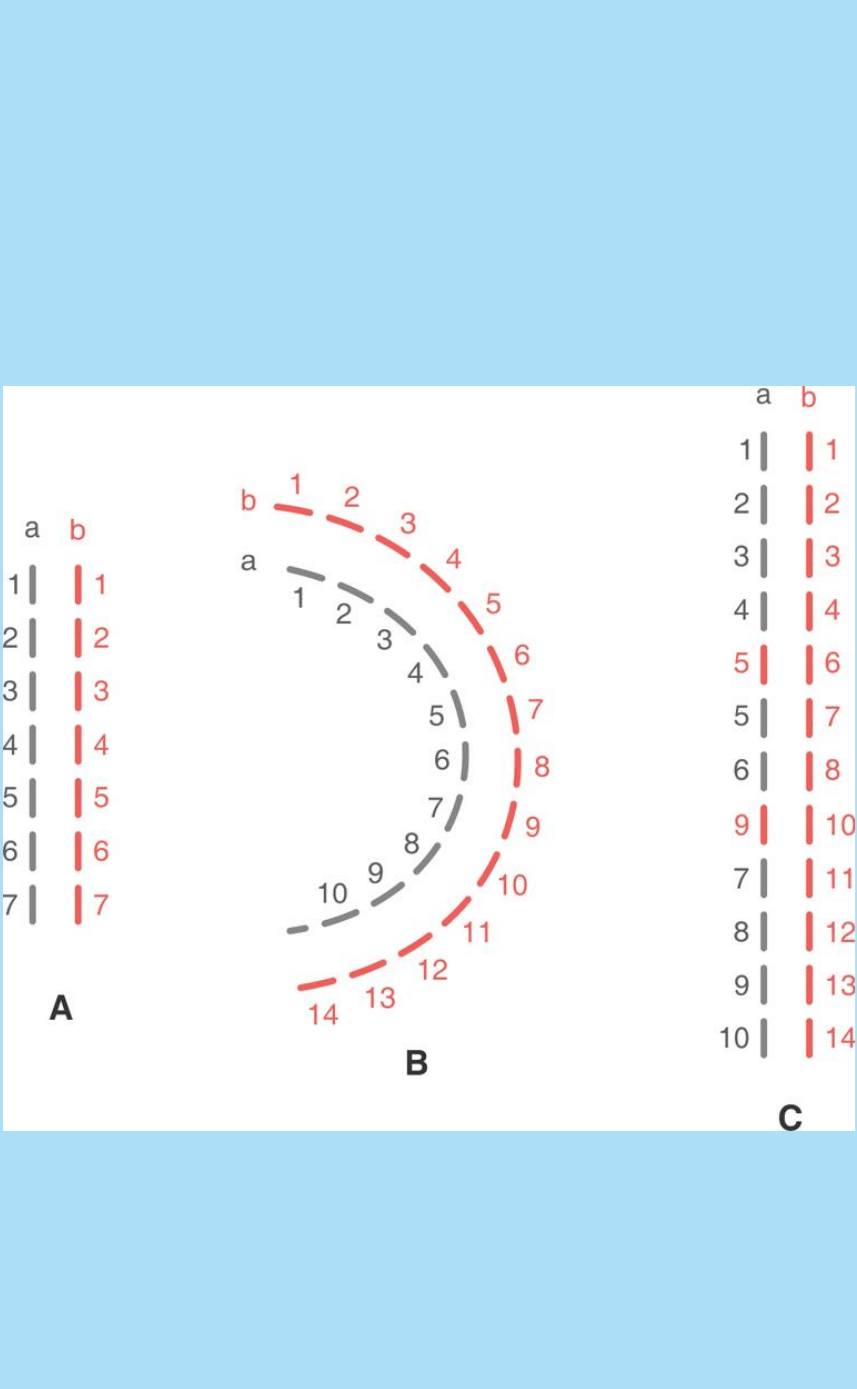
Fig. SC 4-2-3. Representación esquemática que ilustra cómo la
proliferación y la migración celular diferenciales tienen papel
morfogenético. A. Ilustra cómo crece armónicamente (en forma recta)
una estructura en la que las mitades derecha e izquierda proliferan
similarmente. B. Entre A y B se ha producido una mayor proliferación
en la región derecha. Se genera una curvatura de convexidad
derecha. C. Entre B y C se ha producido un desplazamiento neto de
elementos (migración dirigida) desde el lado derecho hacia el

izquierdo. Este desplazamiento compensa el crecimiento en longitud
de ambas mitades y el sistema se rectifica.
En la figura SC 4-2.3 A, las líneas a y b se encuentran apareadas e,
inicialmente, poseen similar cantidad unidades (segmentos que las
componen); en B, el número de segmentos de la línea de la derecha
aumentó al doble en tanto que la de la izquierda aumentó 1,5 veces.
Este hecho produce una curvatura en la estructura. En la figura SC
4-2-3 C un séptimo de los segmentos (2 de 14) fueron transferidos
de la línea derecha a la línea izquierda. Este hecho tiene como
resultado la desaparición de la curvatura característica de la figura
SC 4-2.3 B. Un fenómeno, conceptualmente similar, pero más
complejo debido a la naturaleza 3D del embrión y a la geometría
bastante más complicada de sus tejidos y elementos constituyentes
explica los cambios que conducen al embrión a incurvarse primero y
a enderezarse después.
Un fenómeno en todo similar al ejemplificado fue descrito como
modelo para explicar la generación de la curvatura cefálica o
mesencefálica durante el desarrollo del mesencéfalo del embrión de
pollo.
SC 4.3. La subregionalización y la potencia evolutiva múltiple
de las regiones del somita. V. Flores, M. Rapacioli
Finalizada la somitogénesis, las células de las diferentes regiones del
somita exhiben diferentes CCD dependiendo de las vías de
señalización a las que han estado sometidas durante el proceso. Los
somitas reciben varias influencias espacialmente organizadas como
consecuencia de que se hallan rodeados de varias poblaciones
celulares que emiten diferentes señales con efectos de desarrollo.
Las células del borde dorso-medial del dermomiotomo reciben
señales de la notocorda y placa del piso (proteína señalShh) y de la
región dorsal del tubo neural y ectodermo (proteína señal Wnt) y
evolucionan en sentido de miotomo epiaxil. Si bien se considera que
estas señales constituyen estímulos determinantes, existen datos
que indican que éstos podrían ser estímulos permisivos que
promueven la proliferación y diferenciación del miotomo porque la
expresión de proteínas específicas del músculo se inicia ya en el
mesodermo presomítico. Algunos postulan que la diferenciación en
sentido muscular no se inicia en el mesodermo presomítico debido a
que la expresión de proteínas musculares es inhibida por laproteína
señal BMP proveniente de tejidos laterales. La existencia de la
proteína noggina en la región medial inhibe a BMP y ello permite la
expresión de proteínas específicas de célula muscular
esquelética; este proceso sería amplificado por las señales Shh y
Wnt.
Las células del borde ventro-lateral del dermomiotomo reciben
señales del ectodermo (Wnt6) y del mesodermo lateral (Fgf5) y
evolucionan en sentido de miotomo hipoaxil.
En una siguiente etapa (Fig. SC 4-3-1 A) las células del borde
dorso-medial se dividen con su huso mitótico orientado
perpendicularmente a la lámina basal. Las células hijas que quedan
ubicadas en la región apical del miocele son posmitóticas y se
localizan bajo el dermomiotomo. Estas células se alargan en sentido
céfalo-caudal y comienzan a expresar proteínas típicas del músculo
esquelético. Se consideran miotubos primarios. Luego ocurre lo
mismo con las células del borde caudal del dermomiotomo, luego
con las células del borde cefálico y finalmente con las del borde
ventro-lateral.
Las células originadas en el borde dorso-medial originan miotomo
epiaxil, las originadas en el borde ventro-lateral originan miotomo
hipoaxil y las originadas en los bordes cefálico y caudal originan
miotomo de ambos tipos (Fig. SC 4-3-1 B). Las células de los
bordes dorso-medial y ventro-lateral retienen capacidad proliferativa
y posteriormente originan células proliferantes del miotomo.
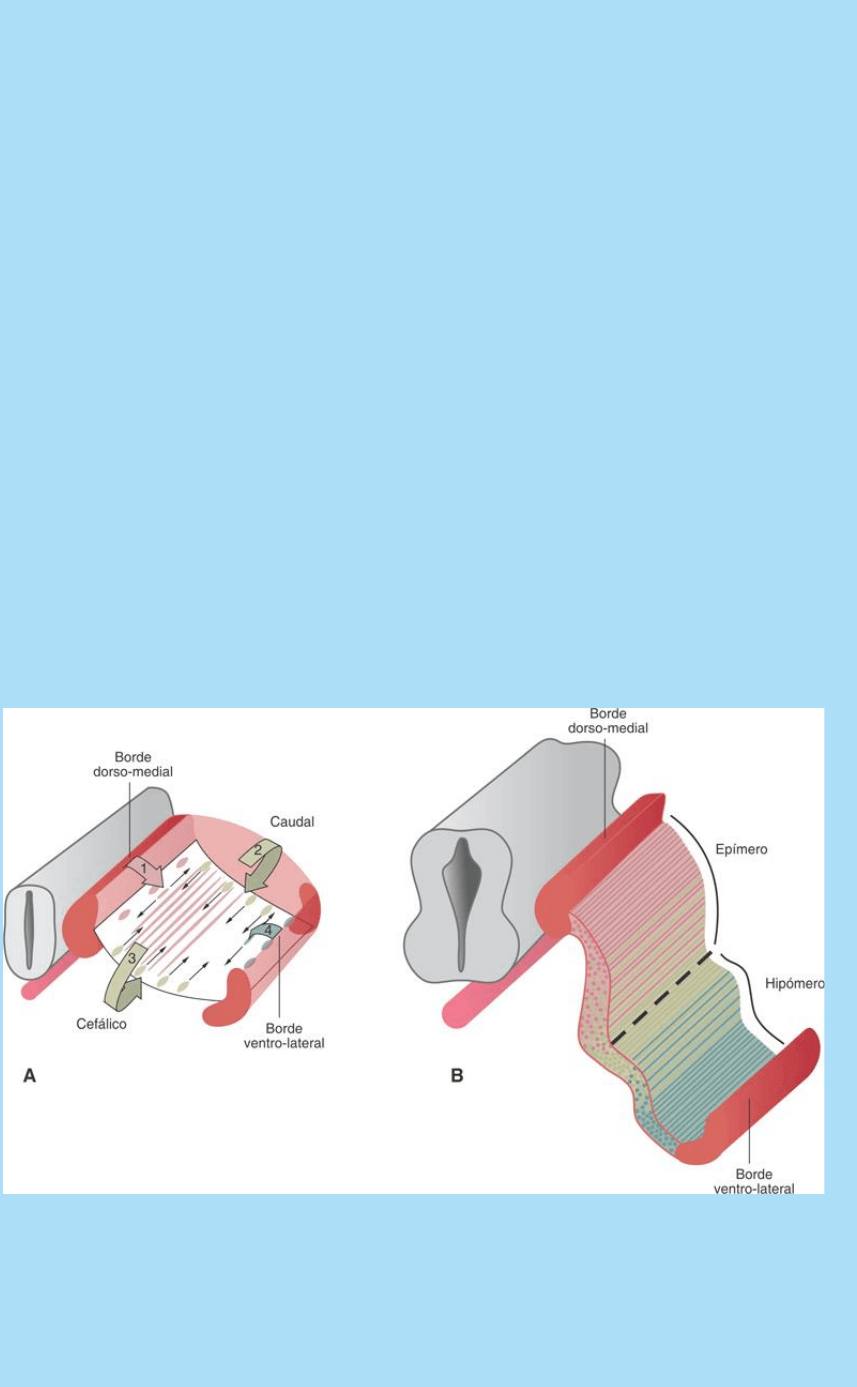
Fig. SC 4-3-1. Modelo de formación del miotomo y su segregación en
varios tipos de miotubos. A. Ilustra la ubicación de las cuatro
poblaciones celulares precursoras de miotubos -en cada uno de los
cuatro bordes del dermomiotomo- y el cambio en la forma y
orientación espacial de las células que lleva a la formación de los
miotubos primarios. B. Ilustra el origen y la distribución de miotomos

primarios (subyacente en el dermomiotomo) y el origen de los
miotubos precursores del epímero e hipómero. En colores se ilustra
la distribución espacial de las células que se originaron en el borde
dorso-medial (rosa), en los bordes caudal y cefálico (verde) y en el
borde ventro-lateral (celeste). Modificado de Gros y col., 2004.
Clásicamente se ha considerado que las células de la región central
del dermomiotomo constituyen el dermatomo. Estas células se
dividen asimétricamente: a) las células que quedan en la región basal
se diferencian en células de la dermis en respuesta a estímulos
provenientes del ectodermo y de la región dorsal del tubo neural
y b) las células que quedan en la región apical forman células
proliferativas del miotomo y, según algunos investigadores, células
del tejido conectivo del músculo y células satélite. Así, la región
central del dermomiotomo no corresponde estrictamente a un
dermatomo. Las células de la dermis se forman por deslaminación de
las células superficiales de dicha región.
Las células del miotomo (ubicadas bajo el dermomiotomo) son
posmitóticas y células satélite. Los miotubos primarios se extienden
a lo largo del eje céfalo-caudal de la región central del miotomo; en
los extremos cefálico y caudal del miotomo existen poblaciones de
células proliferantes. Los miotubos secretan la proteína señal Fgf8 y
las células proliferantes expresan su receptor Frek. En respuesta a
Fgf8, las células proliferantes envían señales que promueven la
expresión del factor de transcripción Scleraxis en las células del
esclerotomo adyacente. De este modo se determina, a partir de las
regiones cefálica y caudal de esclerotomo, el sindetomo (Fig. SC 4-
3-2 A-C). Debido a este modo de determinación, el sindetomo queda
ubicado entre bloques de miotomo y entre bloques de esclerotomo
sucesivos; la ubicación apropiada para generar los fibroblastos que
forman los tendones del raquis que unen los músculos a los huesos
del raquis. No se sabe si el sindetomo también origina los fibroblastos
que forman los ligamentos del raquis.
En la región medial del esclerotomo, cerca de la superficie del tubo
neural, se determina el meningotomo (Fig. SC 4-3-2 A-C). Esta
región origina los fibroblastos que forman el tejido conectivo de
las meninges y las células de los vasos que forman elplexo
vascular perineural y que posteriormente invaden el tubo neural. La
denominación enfatiza la capacidad de formar meninges ya que se
sabe que todas las células del somita poseen la potencia para formar
células vasculares (endoteliales o periendoteliales).
Las células de la región dorsal del tubo neural, mediante la expresión
de las proteínas señal Bmp4 y Wnts, promueven la expresión

del receptor VEGFR-2 en las células del esclerotomo. La expresión
de este receptor sería promovida posteriormente por la expresión
de VEFG-A por parte del tubo neural y este proceso llevaría a la
formación del plexo vascular. Las células del esclerotomo forman
células endoteliales, pericitos y células musculares lisas de estos
vasos. No se sabe si las células del esclerotomo que acompañan a
estos vasos se determinan en fibroblastos de meninges ya en el
esclerotomo o luego de su migración.
Las células de la región ventral del esclerotomo proliferan, migran
y rodean a la notocorda (Fig. SC 4-3-2). Este comportamiento
depende de señales provenientes de la notocorda (Shh,
Noggina y FGF8). Estas señales promueven la expresión de
los factores de transcripción Pax1, Pax9, Twist y Mfh1 en las
células del esclerotomo y promueven la proliferación celular. Las
células de la región caudal del esclerotomo proliferan más y se
agrupan más densamente que las de la región cefálica.
Las células que del somitocele reciben el nombre
de artrotomo (Fig. SC 4-3-2 B); se integran a la mitad caudal del
esclerotomo, migran ventralmente, caudalmente a la fisura
intevertebral (de von Ebner) y originan las articulaciones
intervertebrales, los discos intervertebrales. Nótese que de este
modo la región ventral del esclerotomo de un somita queda dividida
en dos por el artrotomo. Así, cada vértebra se forma por la asociación
del esclerotomo originado en 2 pares de somitas (véase en Capítulo
14). Según algunos investigadores, el artrotomo también origina la
porción proximal de las costillas. Las células que forman el artrotomo
expresan el receptor tipo II del TGF-beta.
Las células de la región central del esclerotomo constituyen
el neurótomo (Fig. SC 4-3-2 B-C). Estas células rodean la región
ventro-lateral del tubo neural. Las células de la región caudal del
esclerotomo que invaden esta región forman tejido esquelético
(porción ventral del arco vertebral, apófisis transversa y porción
proximal de las costillas). Estas células (de la región caudal) se hallan
más densamente agrupadas que las de la región cefálica debido a
que poseen una mayor tasa proliferativa y expresan diferentes
moléculas de adhesión. La región caudal del esclerotomo expresan
las proteínas efrinas B1 y B4 que impiden la migración de células de
las crestas neurales y axones motores que expresan EphB2 y B3.
Por el contrario, las células de la región cefálica, que forman el
neurotomo, permiten el ingreso de células de la cresta neural y
axones en crecimiento y reciben de ellos señales para su sobrevida
y proliferación. En presencia de estos componentes las células de la

región cefálica forman elementos del perineuro y endoneuro de los
nervios y ganglios espinales.
La región lateral del esclerotomo (Fig. SC 4-3-2) recibe señales del
miotomo (PDGF-A y FGF) y mesodermos intermedio y lateral
(BMP4 y VEGF). Un conjunto de estas células forma el resto de las
costillas; otro conjunto de células expresa VEGF-R2y forma células
endoteliales.
Las células de la región dorso-medial del esclerotomo (Fig. SC 4-
3-2) migran dorsalmente al tubo neural y forman la región dorsal del
arco vertebral y la apófisis espinosa. Este proceso está regulado
por BMP4, que se expresa en la región dorsal del tubo neural y en el
ectodermo superficial.
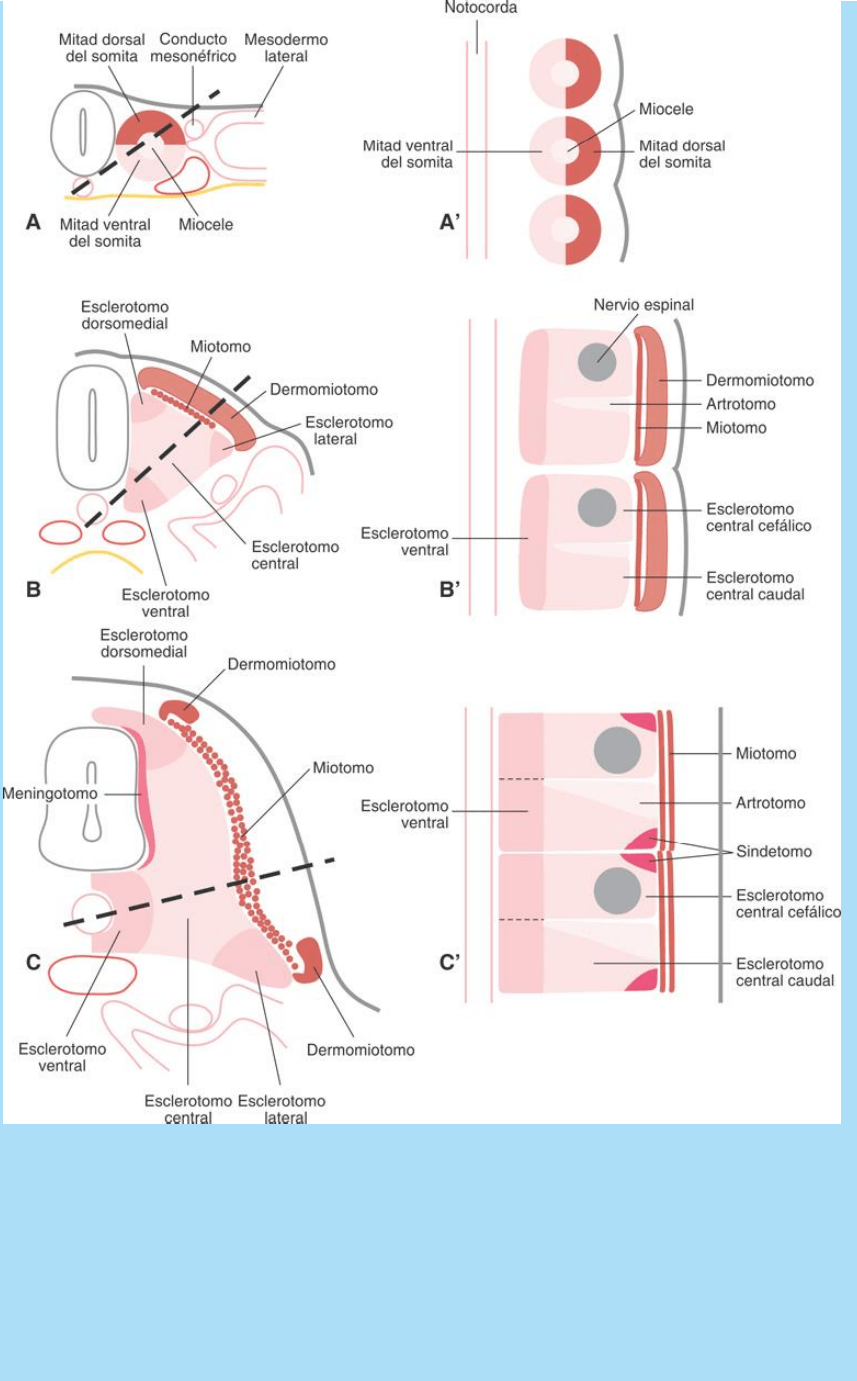
Fig. SC 4-3-2. A, B y C. Esquemas de cortes transversales que
ilustran grados crecientes de diferenciación del somita. Las líneas de
puntos indican los planos de corte de los esquemas que se
representan en A’, B’ y C’. A y A’. Estado de somita epitelial en estado
de diferenciacón temprana e inicio de la disgregación. B y B’. Somita
compartimentalizado en estado de resegmentación. C y C’. Somita
en resegmentación y diferenciación avanzada. Los componentes del
somita rodean a la notocorda, al tubo neural e inician los

desplazamientos que los conducen a sus posiciones definitivas.
Modificado de Christ y cols., 2004.

Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.