
SEGMENTACIÓN
SC 2.1. LOS COMPORTAMIENTOS CELULARES DE LA
SEGMENTACIÓN SE HALLAN TEMPORAL Y ESPACIALMENTE
ORGANIZADOS. V. Flores
La segmentación implica, en todas las especies conocidas, la
operación temporoespacialmente organizada de varios CCD. En
muchas especies, los primeros planos de segmentación tienen
posición constante. El eje del primer huso mitótico es perpendicular
al eje animal-vegetativo (A-V) y el primer plano de segmentación es
meridional (contiene al eje A-V). El segundo plano de segmentación
también es meridional pero perpendicular al anterior y se produce
simultáneamente en las dos primeras blastómeras indicando que
están sincronizadas. El tercer plano de segmentación es ecuatorial,
en consecuencia, perpendicular a los dos primeros y también al eje
A-V y se forma simultáneamente en las cuatro blastómeras. Ello
revela que siguen sincronizadas. Esta forma de segmentación
posibilita que cada blastómera contenga una porción característica
del citoplasma de la CH original.
En los mamíferos, que poseen CH de regulación, este tipo de control
estricto de las posiciones relativas de las blastómeras no parece ser
una necesidad fundamental. En los mamíferos pueden ocurrir varios
modos de segmentación diferentes que conducen, todos, al
desarrollo normal. En los mamíferos, en las etapas tempranas, lo
esencial es que las blastómeras se organicen en un MCI y un MCE
y, en relación con dicha disposición, se determinen diferentemente.
El control espacial de los procesos de cariocinesis y citocinesis
depende de macromoléculas informativas involucradas en la
organización del citoesqueleto. La ubicación de los ásteres, la
orientación del eje del huso mitótico y la orientación en el espacio de
los planos de segmentación deben estar adecuadamente integrados
para que la división celular se produzca normalmente. Se postula que
estos procesos se encuentran tempranamente bajo control genético
materno.
Los ásteres desempeñan un papel primordial a) en el control del
ensamblado del huso mitótico, necesario para la cariocinesis y b) en
la determinación de la posición espacial del anillo contráctil
responsable de la citocinesis.
Datos de observación y resultados experimentales apoyan lo
expuesto:
1) El espermatozoide aporta un centríolo a la CH y éste genera los
ásteres que organizan el aparato mitótico. La segmentación normal
requiere la penetración de un espermatozoide y la operación de sólo
un par de ásteres.
2) La penetración de más de un espermatozoide genera una
segmentación anormal con números de husos mitóticos y de surcos
de segmentación acordes con el número de ásteres presentes. Los
surcos de segmentación se ubican característicamente en el punto
medio de la distancia entre dos ásteres adyacentes.
3) Si en la CH, por compresión mecánica, se modifica la posición de
los ásteres y del huso mitótico, la posición en el espacio del surco de
segmentación se modifica de acuerdo con la nueva posición de los
ásteres.
4) Si en la CH se desplaza mecánicamente el huso mitótico a la
periferia y se impide la progresión del surco de segmentación (
Fig.
SC 2-1-1
), se produce una situación similar a la segmentación
meroblástica de los huevos telolecíticos. Se genera una célula
binucleada, con forma de herradura, con los núcleos ubicados en los
extremos de las ramas de la herradura (
Fig. SC 2-1-1 C). En la
siguiente segmentación, en cada rama de la herradura se forman un
par de ásteres y el huso mitótico correspondiente a la cariocinesis de
cada núcleo. A continuación, en cada brazo de la herradura, a mitad
de camino entre los dos ásteres –en la zona media de cada huso
mitótico–, se genera un surco de segmentación. Lo significativo de
estos experimentos es que en la zona curva de la herradura (
Fig. SC
2-1-1 E
), en donde no existe ningún huso mitótico, también se genera
un surco de segmentación que se ubica en un punto equidistante
entre dos ásteres adyacentes. Este surco de segmentación no está
asociado ni a la cariocinesis ni a la formación de un huso mitótico. El
resultado indica que no es el huso mitótico, sino la ubicación de los
ásteres el fenómeno que instala en el citoesqueleto la referencia que
determina la ubicación espacial del anillo contráctil de la citocinesis.
La ubicación de los ásteres por un lado determina la posición del eje
del huso mitótico y, por otro, señalizarían –probablemente por medio
de los microtúbulos que a partir de él se extienden radialmente hacia
la periferia celular– la orientación en el espacio de los planos división
de la segmentación.
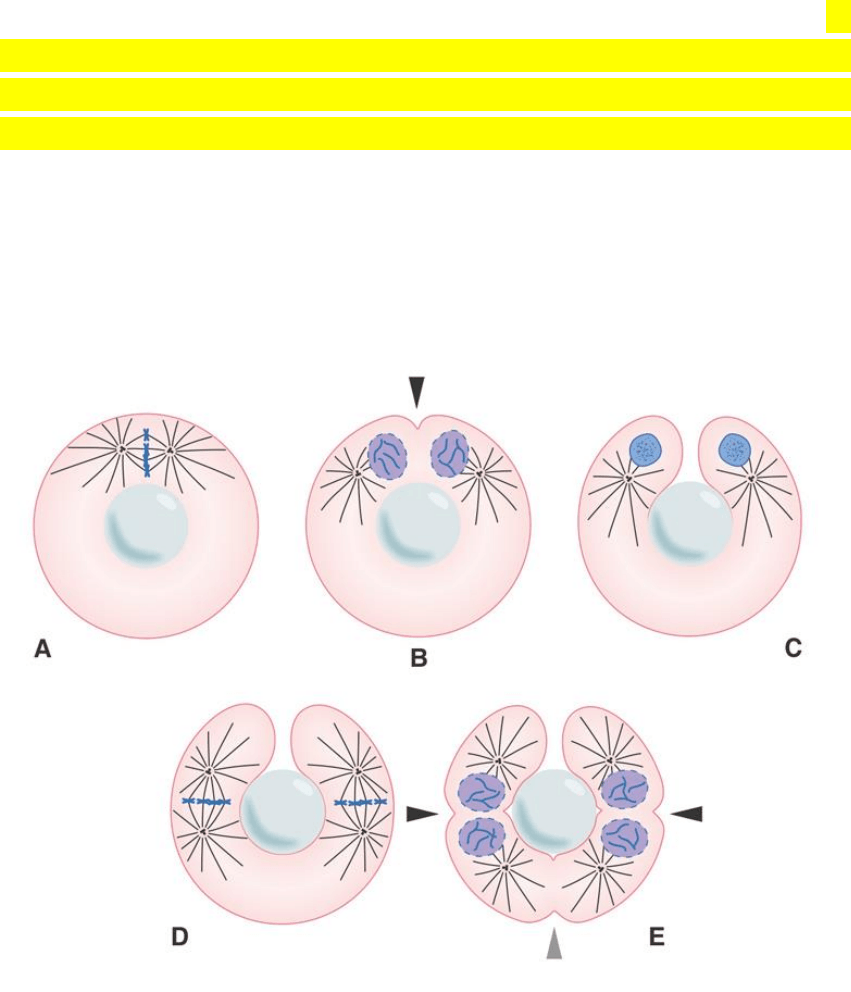
Fig. SC 2-1-1. El experimento ilustra el papel de los ásteres en la
determinación de la posición del anillo contráctil de la citocinesis. La
compresión de la célula huevo con una pequeña esfera de vidrio
interrumpe el progreso del primer plano de clivaje. A. Con una esfera
de vidrio se comprime la CH y se desplaza el huso mitótico a la
periferia. B-C. Cuando se produce la citocinesis, el plano de clivaje
se ubica a mitad de camino entre ambos ásteres. La esfera de vidrio
impide el progreso (profundización) del surco. D-E. Durante la
segunda segmentación se forman los surcos de segmentación
correspondientes a los dos husos mitóticos. Además, en la zona
inferior, pese a que no hay un huso mitótico y no corresponde a una

célula que se está dividiendo, se forma un surco de segmentación
extra (cabeza de flecha gris).
SC 2.2. PAPEL DE LA ADHESIVIDAD CELULAR DURANTE LA
SEGMENTACIÓN. LA POLARIZACIÓN Y COMPACTACIÓN DE
LAS BLASTÓMERAS Y LA FORMACIÓN DE LA MÓRULA. V.
Flores
Algunos eventos morfogenéticos de la segmentación están mediados
por cambios en la intensidad de fuerzas interfaciales célula-célula (Fif
c-c). Los cambios en la intensidad de dichas fuerzas están
involucrados tanto en lacompactación de las blastómeras que
conduce a la mórula como también en lacavitación que lo transforma
en blástula.
Los cambios en la intensidad de las Fif c-c son resultado de cambios
en la organización química de superficie de las blastómeras. Estos
cambios dependen de modificaciones en el patrón de síntesis de
moléculas de adhesión celular o Cam (Cell adhession molecules).
Desde los E2c-E4c, las blastómeras cambian la expresión de algunas
proteínas de superficie celular. Éstas, sin embargo, ejercerán su
efecto compactante sólo más adelante. Hasta el E4c, algunas
glicoproteínas de superficie celular se encuentran uniformemente
distribuidas, al azar, en la superficie de las blastómeras. Desde el E4c
en adelante, como modificación preparatoria para la compactación y
formación de la mórula, las blastómeras experimentan una
redistribución y localización asimétrica o polarización de algunas
proteínas de membrana. Éstas se localizan en regiones particulares
de la superficie de las blastómeras. Algunas proteínas se concentran
en la zona más externa de las blastómeras (el polo opuesto al centro
del embrión) en tanto que otras se localizan internamente, en la zona
donde las blastómeras toman contacto entre sí. La proteína de
adhesión celular L-Cam, por ejemplo, se ubica preferencialmente en
las zonas de contacto intercelular en donde aparece alta intensidad
de Fif c-c. El incremento de las Cam en las zonas de contacto
intercelular y el incremento en la intensidad de la Fif c-c hacen que
las células se unan más fuertemente, disminuya el espacio entre
ellas, se compacten y, en conjunto, formen una masa celular maciza
o mórula.
Se sabe que el fenómeno de polarización depende de interacciones
entre blastómeras adyacentes. Diversas experiencias de disociación
y reasociación de blastómeras muestran que las blastómeras
aisladas no sufren polarización; las proteínas de membrana se
distribuyen homogéneamente en el plano de la membrana. Cuando
se las asocia de a pares, la polarización reaparece.
La proteína L-Cam constituye un ejemplo de glicoproteína de
superficie que cumple un papel específico en la compactación. La
incubación de embriones en presencia de anticuerpos anti-L-Cam
produce una rápida descompactación de la mórula. Existen
experimentos que sugieren que uno de los sistemas de transducción
de señales, la vía de señalización del fosfatidilinositol, está
involucrado en la compactación. La enzima proteína-quinasa C, de
un modo no dilucidado aún, actuaría sobre la localización de la L-
Cam. Este hecho iniciaría la compactación.
El citoesqueleto submembranoso y las proteínas de la membrana
plasmática desempeñan un papel importante en la compactación. Es
precisamente en la interface entre las membranas de blastómeras en
contacto donde operan las Fif c-c que producen su compactación.
Las membranas de las blastómeras correspondientes a las zonas de
contacto generan pliegues o microvellosidades con gran cantidad de
microfilamentos. Se piensa que éstas contribuyen a aumentar la
superficie de contacto.
La organización de la mórula compactada es rápidamente
estabilizada por el desarrollo de complejos de unión, especialmente
zónulas occludens entre las células superficiales de la mórula. Estas
uniones, por un lado, cumplen una función estructural estabilizadora
porque mantienen cohesionadas a las células y las hacen resistentes
a tensiones mecánicas. Por otro, dada su capacidad de restringir el
pasaje de moléculas a través de la vía paracelular, contribuyen a
definir un medioambiente bioquímicamente definido en el interior de
la mórula. Esto genera la condición necesaria para la ocurrencia del

primer evento de determinación durante el desarrollo de los
mamíferos (SC 2.17.
La primera determinación. La expresión de
combinatorias de factores de transcripción específicas de tipo
celular en la mórula y el blastocisto).
SC 2.3. PROCESOS DE DIFERENCIACIÓN CELULAR DURANTE
EL PERÍODO DE SEGMENTACIÓN. ¿CÓMO SE GENERA
DIVERSIDAD CELULAR DURANTE LA SEGMENTACIÓN?. V.
Flores
Existen muchos momentos típicos del desarrollo en los que a partir
de una población homogénea (formada por un único tipo celular con
una potencia dada) se generan dos o más tipos celulares con
diferentes características y potencias evolutivas. Éste es uno de los
procesos involucrados en la génesis de la complejidad pluricelular. El
inicio de la segmentación implica la generación de una cierta cantidad
de blastómeras, morfológicamente similares y equipotentes. Al final
de la segmentación, la organización del blastocisto depende de los
fenómenos que operaron en ésta. El tipo de segmentación, a su vez,
depende de la organización citoplasmática original de la CH. En los
mamíferos, al final de la segmentación existen dos tipos celulares: a)
células que forman el embrioblasto (originarán tejidos embrionarios y
algunos no embrionarios) y b) células que forman el trofoblasto
(originarán tejidos de la placenta encargados de la nutrición del
embrión).
Las blastómeras se forman por mitosis a partir de la CH. La mitosis
mantiene la similitud de la información genética que se transfiere de
célula madre a células hijas. Cada blastómera posee un citoplasma
que corresponde a una fracción del citoplasma de la CH –proveniente
del ovocito II– y un núcleo con información genética similar a la de la
CH original. El interés por conocer cómo a partir de una célula que
se divide por mitosis pueden originarse dos o más tipos celulares
diferentes ha generado muchos e ingeniosos experimentos.

Papel de las señales externas y de las interacciones núcleo-
citoplasmáticas [Int n-c] en la especificación de tipo celular. La
información genética reside en el núcleo, pero los procesos
fisicoquímicos por medio de los cuales se ejecutan CCD y que
confieren características morfológicas y/o funcionales típicas a las
células ya diferenciadas ocurren mayoritariamente en el citoplasma.
Las Int n-c constituyen la base de la diferenciación celular.
Numerosas evidencias sobre la importancia de las Int n-c para el
mantenimiento de la estructura y función de las células de cualquier
organismo provienen de las clásicas experiencias de extirpación del
núcleo en células de vida libre: la extirpación del núcleo de una
ameba no interrumpe sus funciones vitales inmediatamente. Una
ameba sin núcleo puede sobrevivir un tiempo pero, finalmente,
muere. Si, antes de un cierto tiempo crítico, se reintroduce el núcleo
en el citoplasma de la ameba, ésta recupera sus características
normales y sobrevive.
De modo similar, una CH enucleada puede iniciar el desarrollo. Se
inicia la segmentación, se desarrollan parcialmente blástulas, pero el
desarrollo se detiene antes de que se observen signos importantes
de diferenciación. Esto indica que la eliminación del material
genético, con la consiguiente ausencia de Int n-c, detiene el
desarrollo.
La prosecución transitoria del desarrollo luego de la eliminación del
núcleo no implica que el citoplasma actúe con prescindencia de
aquél. Sólo se debe a que el citoplasma posee almacenados los
productos de Int n-c realizadas antes de la eliminación del núcleo,
durante la ovogénesis, y que explican el fenómeno denominado
control genético materno de la embriogénesis temprana (SC 2.4 El
concepto control genético materno (CGM) de la embriogénesis
temprana).
Si en algún momento las blastómeras empiezan a expresar CCD
diferentes, puede suponerse que en ellas se están realizando
diferentes Int n-c. Desde el punto de vista teórico, esta situación
podría darse si las blastómeras:
(a) poseyeran información genética diferente, o si...

(b) poseyeran composiciones citoplasmáticas diferentes. Existe
acuerdo con respecto a que la primera condición no se cumple en
mamíferos. La segunda situación podría darse si:
(b1) durante la segmentación las blastómeras recibieran de la CH
porciones de citoplasma con factores determinantes citoplasmáticos
diferentes, o si…
(b2) durante la segmentación las blastómeras sufrieran cambios
citoplasmáticos debidos a la recepción de estímulos ambientales
diferentes y la consiguiente activación de vías de señalización con
diferentes efectos de desarrollo.
En favor del punto (a) del párrafo anterior alguna vez se argumentó
que la información genética podría modificarse durante el desarrollo.
El cambio en la composición del ADN podría explicar que las Int n-
c sean diferentes y así podría explicarse que las blastómeras
expresen diferentes CCD y originen poblaciones celulares diferentes.
Algunas experiencias clásicas de trasplante nuclear permitieron
descartar la opción (a). La experiencia consistió en transferir núcleos
de distintos tipos de células, que ya han iniciado su diferenciación, a
CH previamente enucleadas. El objetivo consistía en contrastar si los
núcleos de células diferenciadas o en diferenciación, trasplantados,
son capaces de promover un desarrollo normal. El fundamento se
basó en la idea de que, si las CH núcleo-trasplantadas originaran
individuos normales, ello implicaría que la información genética de
los núcleos diferenciados o en diferenciación es similar a la de la CH.
Las experiencias de Briggs y King (1959) consistieron en el
trasplante de núcleos de células embrionarias somáticas (2n)
(blastómeras del hemisferio animal de blástulas avanzadas de
rana Pipiens) a óvulos enucleados. Un porcentaje de estas CH
núcleo-trasplantadas se segmentaron y desarrollaron normalmente
hasta etapas larvarias avanzadas sugiriendo que la información
genética de los núcleos de blastómeras de blástulas avanzadas es
similar a la de la CH que les dio origen. Diversos resultados obtenidos
en la década del 60 por Gurdon, Laskey y otros, en la
rana Xenopus Laevis permitieron aceptar, en general, la idea de
que la información genética de las células somáticas permanece sin

cambios cualitativos significativos a lo largo del desarrollo. En
consecuencia, desde el punto de vista cualitativo, la información
genética es básicamente similar en todas las células del organismo.
Gurdon y cols. trasplantaron núcleos de células somáticas
diferenciadas (2n) a ovocitos enucleados. El desarrollo de éstos dio
origen a renacuajos normales y hasta algunos ejemplares adultos.
Todos estos resultados sugieren que el ADN del núcleo diferenciado
trasplantado, una vez en el citoplasma de la CH, es liberado de los
procesos de activación y represión génica sufridos durante el proceso
de diferenciación. El trasplante tendría el efecto de revertir la
condición en la que se encuentra el ADN del núcleo de la célula
somática diferenciada a la condición original que posee en el núcleo
de la CH.
Los resultados clásicos han sido interpretados en el sentido de que
el núcleo de cada tipo particular de célula somática posee una
combinación típica de genes activados y reprimidos que es
característica para cada tipo celular. Sin embargo, el núcleo de una
célula ya diferenciada, puesto en el citoplasma de la CH pasa a
comportarse como el núcleo de la CH. Sufre una reversión de los
cambios (activación y represión selectiva) ocurridos durante el
desarrollo. Estas ideas son la base de la clonación que en la
actualidad se pueden realizar en diversas especies, incluso en
mamíferos. Las experiencias de trasplante nuclear, primero iniciadas
en protozoarios y luego en CH de anfibios, se han podido aplicar con
éxito en mamíferos y hoy se sabe que los núcleos de células
somáticas, aun de organismos adultos, cuando son trasplantados a
CH enucleadas son capaces de promover el desarrollo hasta el
estado adulto, aunque todavía no han sido exhaustivamente
analizadas todas las consecuencias perjudiciales que pueden traer
aparejadas las experiencias de trasplante nuclear.
Todos estos resultados experimentales muestran que la actividad
nuclear es regulada por moléculas que transitoriamente residen en el
citoplasma y que, o son generados en respuesta a moléculas señal
provenientes del medio (señales determinantes o permisivas) (SC

0.5. El concepto de determinación. Potencia y significado
evolutivos
; SC El concepto de diferenciación celular. Criterios
que definen el grado de diferenciación
) o también productos
génicos de la propia célula (factores de transcripción y otras
moléculas que regula la expresión génica). La operación de los CCD,
en consecuencia, depende de la información genética propia y de
componentes del medioambiente con sentido biológico (señales).
De acuerdo con los datos considerados, el origen de la diversidad o
diferenciación celular durante la ontogenia se centra en el punto (b) –
las diferencias citoplasmáticas entre las blastómeras–. El mecanismo
principal por medio del cual se introduce diversidad celular en el
desarrollo temprano posee modalidades diferentes según se trate
de (b1) CH de organización determinada –mosaico– o de(b2) CH de
organización lábil o regulativa. A esta segunda categoría pertenecen
los huevos de mamíferos, entre ellos el hombre (véase SC 2.5.
Los
mamíferos poseen CH de regulación. La importancia de la
polaridad A-V en los experimentos de merotomía de la CH).
SC 2.4.EL CONCEPTO CONTROL GENÉTICO MATERNO (CGM)
DE LA EMBRIOGÉNESIS TEMPRANA. V. Flores
La célula huevo (CH) constituye un sistema de desarrollo que
posee a) información genética cigótica, aportada por ambos
progenitores, que se halla en un estado apto para ser utilizada como
inicio de un programa genético de desarrollo y b)información
citoplasmática ovocitaria representada por moléculas informativas
(diferentes tipos de ARN, proteínas, ribosomas, etc.) sintetizadas y
almacenadas durante la ovogénesis. La información citoplasmática
que posee la CH le es transferida por el ovocito II y fue elaborada
exclusivamente con la utilización del genoma materno. Ambos
conjuntos informativos son importantes pero el control de los CCD
durante la embriogénesis temprana, incluida la segmentación,
depende principalmente de la información citoplasmática de la CH,
por ello se dice que se halla fundamentalmente bajo CGM. El
concepto no implica que los elementos informativos que aporta el
espermatozoide no influyan en absoluto en la organización de los
CCD, sólo enfatiza la importancia que poseen los que aporta el
ovocito. El CGM posee gran influencia en algunas especies y menor
en otras (mamíferos).
En las especies en las que existe un CGM riguroso se cumplen las
siguientes condiciones:
a) Varios CCD incluidos en la segmentación requieren proteínas y
ARNm sintetizados durante la ovogénesis y almacenados en el
citoplasma del ovocito.
b) El genoma cigótico no se expresa durante el clivaje temprano.
Recién lo hace en la fase final de la segmentación o al principio de la
gastrulación.
c) El cambio entre ambos tipos de control genético (CGM a CGC) es
bastante brusco, se denomina transición y ocurre en un momento
típico del desarrollo.
El momento en el que se produce la transición (activación del CGC)
para el caso de algunos genes o algunos CCD puede ser detectado
con precisión y ser modificado experimentalmente.
1) Existen especies en las que el CGM de la proliferación se
manifiesta por una curva típica de incremento en el número de células
en función del tiempo o en función del número de ciclos celulares
cumplidos (
Fig.SC 2-4-1). Cuando se pasa al CGC, la pendiente de
la curva se modifica típicamente. A dicho punto se denomina
transición del control de la proliferación y ocurre en un número
típico de ciclos celulares.
2) Aumentando experimentalmente la cantidad de cromatina del
núcleo de la CH y, en consecuencia la de las blastómeras resultantes,
se puede adelantar el momento en que se produce la transición. Si
se aumenta al doble la cantidad de cromatina, la transición ocurre un
ciclo más temprano.
3) Si se disminuye la cantidad de cromatina a la mitad, la transición
ocurre un ciclo más tarde.
4) Otros experimentos muestran que, modificando el volumen
citoplasmático y dejando constante la cantidad de cromatina, se
produce también un desplazamiento en el momento de la transición.
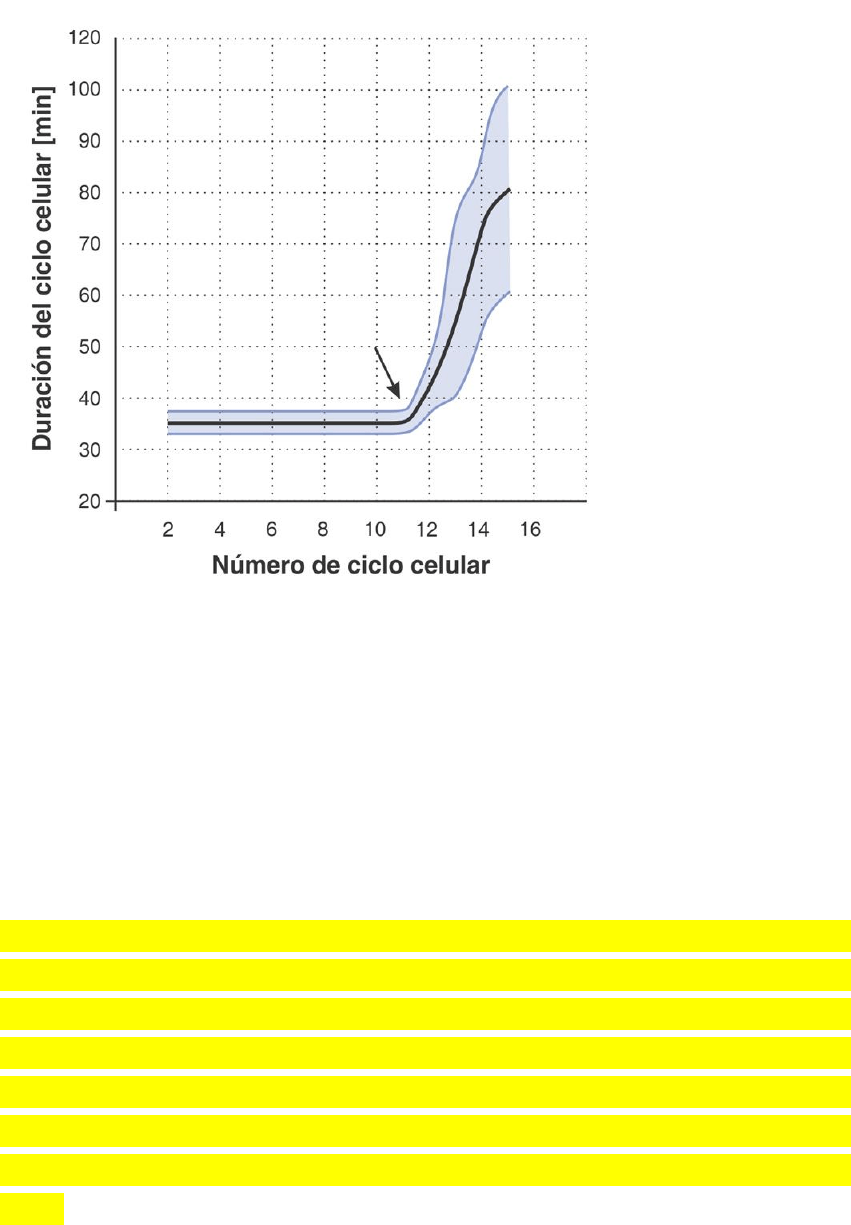
Fig. SC 2-4-1. Evolución de la duración del ciclo celular y de su
variabilidad en función del número de ciclos medido en células
disociadas de embriones de Xenopus. Los primeros ciclos celulares
están sincronizados y poseen una duración típica de 35 minutos.
Luego de la transición del control de la proliferación (flecha), los ciclos
celulares se alargan y pierden sincronización. La línea negra
representa la duración media del ciclo celular. Las líneas azules
representan el rango de dispersión del valor medio o variabilidad.
Nótese que luego de la transición también aumenta la variabilidad.
Por estos resultados, se considera que la transición depende del
cambio en larelación volumen nuclear/volumen
citoplasmático (R vN/vC) que ocurre durante la segmentación. En
sentido estricto, no se considera que el cambio en la relación volumen
N/C es el fenómeno desencadenante de la transición sino que
depende de cambios en la relación concentración de
cromatina/disponibilidad de factores inhibitorios luego de cada
ciclo.

Nótese que, en ausencia de actividad biosintética, con cada
citocinesis la cantidad de factores inhibitorios que poseen las células
se reduce a la mitad. Sin embargo, dado que en cada ciclo, en el
período S se duplica la cantidad de ADN, en sucesivos ciclos se
produce una dilución de factores inhibitorios en relación con la
cantidad de ADN por célula. Luego de un cierto número de ciclos
proliferativos, la cantidad de factores inhibitorios puede haberse
diluido hasta el punto en que ya no ejerce su efecto inhibitorio y los
genes cigóticos se activan.
Los mamíferos poseen CH pequeñas que no almacenan grandes
cantidades de moléculas informativas. En estos casos el control
genético materno es menos importante o duradero: a) existe menor
cantidad de moléculas informativas acumuladas en el ovocito, b) el
genoma cigótico empieza a activarse ya durante la segmentación
temprana para producir las moléculas que participan en la
segmentación y c) con excepción de la adhesividad celular, no existe
una transición neta en otros CCD. El control materno es reemplazado
desde temprano y, al parecer, gradualmente por el cigótico.
SC 2.5. LOS MAMÍFEROS POSEEN CH DE REGULACIÓN. LA
IMPORTANCIA DE LA POLARIDAD A-V EN LOS
EXPERIMENTOS DE MEROTOMÍA DE LA CH. V. Flores
Dos conceptos clásicos aluden a diferentes comportamientos
exhibidos por los sistemas de desarrollo cuando son sometidos a
experimentos en los que una parte de éste es eliminado. En algunos
casos, el desarrollo se altera, falta aquella parte que hubiera sido
formada por la porción eliminada. En otros, se forma una estructura
completa y armónica. Este diferente comportamiento, que
clásicamente ha recibido diferentes designaciones y diferentes
interpretaciones, depende del carácter determinado o indeterminado
del sistema en cuestión en el momento en que se realiza el
experimento de ablación (SC 0.5.
El concepto de determinación.
Potencia y significado evolutivos).

Todo CCD involucra la operación previa de diversas interacciones
núcleo-citoplasmáticas. La expresión de la información genética
durante el desarrollo embrionario puede depender de señales
externas (provenientes de otras células o del ambiente) que actúan
en un momento dado y/o de moléculas propias o endógenas que
pudieron haber sido sintetizadas con mucha anterioridad,
almacenadas en el citoplasma y que actúan tiempo después.
Clásicamente se denominó “factores determinantes citoplasmáticos”
a sustancias no identificadas que, estando almacenadas en el
citoplasma de una célula en desarrollo determinan su modo de
desarrollo y su destino evolutivo; vale decir, determinan qué
derivados originarán. En tales sistemas de desarrollo puede ocurrir
que determinantes citoplasmáticos almacenados en la CH se
repartan diferencialmente durante la segmentación de la CH de modo
que, dependiendo del tipo de determinantes citoplasmáticos que
quedan en diferentes blastómeras, ellas originan diferentes
derivados. En tales situaciones, la eliminación de alguna blastómera,
o incluso de alguna porción del citoplasma de la CH, puede dar lugar
a la falta de aquella porción del embrión que hubiera derivado de la
blastómera eliminada. Algunas especies (moluscos, helmintos,
ascidias y otras) poseen CH con regiones citoplasmáticas
determinadas a formar sólo ciertas regiones del embrión y no otras.
La eliminación de dichas regiones citoplasmáticas ocasiona la
producción de embriones incompletos. Estos sistemas de desarrollo
fueron concebidos clásicamente como un mosaico de regiones
diferentemente determinadas, vale decir, con diferente potencia
evolutiva. También se los ha denominado “con organización rígida o
determinada” o “sistemas heterogéneos” aludiendo a que diferentes
regiones citoplasmáticas poseen diferentes elementos informativos y
propiedades de desarrollo.
Existen modos de programación del desarrollo más plásticas en las
que los procesos de determinación se suceden gradualmente en
función del tiempo. En estos casos las señales determinantes o
directrices van produciéndose gradual y progresivamente (de lo
general a lo particular) dependiendo del estado de desarrollo. En

tales sistemas las blastómeras que se forman durante la
segmentación se mantienen indeterminadas por períodos más
prolongados, pues el ingreso a diversas vías de desarrollo no
depende de determinantes citoplasmáticos almacenados tiempo
antes, sino de fenómenos interactivos que se van sucediendo en
función del estado de desarrollo alcanzado. Dado que en tales
sistemas las blastómeras no están determinadas, la eliminación de
algunas de ellas puede no comprometer el desarrollo global ya que,
si las restantes poseen potencia evolutiva amplia, pueden compartir
la potencia de la blastómera eliminada y, en consecuencia, pueden
suplirla o reemplazarla. Estos sistemas fueron concebidos
clásicamente como poseedores de la capacidad de “regular” los
déficits o excesos y se denominaron sistemas con “capacidad
regulativa” o simplemente de “regulación”. También se los ha
denominado “sistemas no determinados”, “plásticos o lábiles”
implicando estos términos que poseen una organización que puede
ser recompuesta (reorganizada) luego de la eliminación de parte del
embrión y que las diferentes blastómeras, o regiones citoplasmáticas,
no tienen un destino evolutivo fijo sino que pueden modificar sus
destinos en función de las interacciones que puedan realizar durante
el desarrollo. Estos sistemas también fueron denominados
clásicamente “homogéneos” en el sentido de que las propiedades de
desarrollo podrían estar uniformemente distribuidas en el citoplasma
de la CH y de las primeras blastómeras.
Existen experiencias que muestran que esto último no
necesariamente se cumple. Los experimentos clásicos que llevaron
a los conceptos de regulación y mosaico consistieron en la
separación experimental de las dos primeras blastómeras y su
desarrollo en forma aislada. En estas circunstancias, en las especies
con CH de regulación se forman dos embriones más pequeños, pero
con plan anatómico normal (completo). En el caso de las CH en
mosaico el experimento da lugar a dos embriones incompletos
(carecen de porciones del organismo).
Algunos experimentos ulteriores sobre el desarrollo de partes
aisladas de sistemas de regulación –CH o embriones en
Este documento contiene más páginas...
Descargar Completo
Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.