
SC 16.1. Concepto de imprinting genético. Las gametas
masculina y femenina son no equivalentes y complementarias
desde el punto de vista de la información genética que aportan.
V. Flores
En las especies diploides, el fenotipo se elabora con información
genética proveniente de ambos progenitores. Para la gran mayoría
de los genes, la posibilidad de expresarse y la tasa de expresión es
similar para los dos alelos del gen, el de origen materno (aportado
por el ovocito) y el de origen paterno (aportado por el
espermatozoide).
Existen, sin embargo, algunos genes, que cumplen importantes
funciones durante el desarrollo, cuyos alelos de origen materno y
paterno no tienen igual posibilidad de expresión. Ello se debe a que
las células germinales masculinas y femeninas programan la
expresión de estos genes de modo diferente y complementario. A
este fenómeno por medio del cual algunos genes son diferentemente
programados en las células germinales masculina y femenina se ha
denominado “imprinting”. Sólo algunos genes son susceptibles de
sufrir imprinting y genéricamente se los denomina “genes
de imprinting”. El proceso de imprinting ha sido en parte aclarado.
En pocos vertebrados y en varios invertebrados existe un tipo de
reproducción, llamada partenogenética, por medio de la cual el
ovocito, sin la participación el espermatozoide, se activa, inicia el
programa de desarrollo y genera un nuevo individuo. Ello implica que
en dichas especies el ovocito posee habilitados, con capacidad de
expresarse en el momento que corresponda, todos los genes que
participan del desarrollo. En dichas especies, la reproducción sexual,
realizada con la participación del espermatozoide, introduce
variabilidad genética, pero no es esencial para que el desarrollo se
complete.
Los mamíferos no realizan partenogénesis en forma espontánea y
tampoco se ha logrado experimentalmente. Es posible activar
ovocitos de mamíferos en medios de cultivo e inhibir la eliminación
del segundo glóbulo polar. El ovocito activado resultante es diploide
y, al igual que una célula huevo, inicia el desarrollo; sin embargo, se
forma un embrión con muchas alteraciones (con sólo algunos tejidos
y órganos parcialmente diferenciados) que se desorganiza y
rápidamente muere.
Experimentos de trasplante nuclear han permitido corroborar que los
pronúcleos masculinos y femeninos no son equivalentes y que
poseen programaciones complementarias. La micromanipulación

permite la extracción y/o inyección de núcleos en la célula huevo. Si
a la célula huevo se le extrae el pronúcleo masculino y se le inyecta
un pronúcleo femenino extraído de otra célula huevo, pasa a ser una
célula diploide con cromosomas de origen exclusivamente femenino
(bimaternal). También se puede obtener una célula
huevo bipaternal –con cromosomas de origen exclusivamente
masculino– si la célula huevo posee dos pronúcleos masculinos.
Estas células huevo también inician el desarrollo, aunque expresan
diferentes modos de evolución, y tempranamente detienen su
desarrollo y mueren. Las células huevos bimaternas evolucionan
originando principalmente tejidos similares a los que derivan del
embrioblasto y las bipaternas preferentemente forman tejidos
derivados trofoblásticos.
En la naturaleza ocurre espontáneamente una situación parecida a
la de las células huevos bipaternas. Existen tumores benignos
localizados en el útero de mujeres que teóricamente están gestando
y que son estructuras quísticas formadas por tejidos similares a los
placentarios. De acuerdo con estudios citogenéticos estos tumores,
denominados mola hidatidiforme completa o androgenética, son
el resultado del desarrollo de células huevos que perdieron la
información genética materna y sólo poseen información
aportada por el espermatozoide. En el 90% de los casos son
diploides (46, XX) y los cromosomas son de origen paterno. Se
considera que son el resultado de la fecundación entre un ovocito
que ha perdido el pronúcleo femenino y un espermatozoide (22,X)
que luego de la fecundación sufrió una duplicación de la información
genética antes del inicio de la segmentación. En el 10% restante de
los casos se considera que es el resultado de la fecundación del
ovocito por dos espermatozoides que generan un cariotipo 46,XX o
46,XY. Estas células huevos androgenéticas diploides sobreviven,
proliferan pero no generan tejidos correspondientes a derivados
embrioblásticos sino sólo tejidos similares a los que derivan del
trofoblasto.
Todos estos hechos indican que a) la información genética
proveniente de sólo uno de los progenitores (masculino o femenino),
aun cuando la célula huevo sea diploide, es insuficiente para regular
el desarrollo normal, que b) la información aportada por cada gameta
es diferente o no equivalente y que c) el déficit en la información
genética aportada por cada gameta es suplida por la información
aportada por la otra gameta, vale decir, son complementarias.
El fenómeno de imprinting está mediado por un proceso denominado
metilación del ADN (Véase SC 16.2. Genes pasibles de
sufrir imprinting. Funciones de la metilación en el imprinting) que

instala una represión irreversible en los genes que lo sufren.
Losgenes de imprinting son de expresión monoalélica. En
términos generales, el imprinting ocurre de modo tal que, si en las
células germinales femeninas los genes pasibles de
sufrir imprinting son programados con un estado apto para la
expresión, el alelo correspondiente en las células germinales
masculinas sufre una inhibición irreversible y recíprocamente. En
consecuencia, si en una población celular en desarrollo se activa un
gen pasible de sufrir imprinting, sólo se expresará el alelo
proveniente del progenitor que lo programó para ser expresado; el
que proviene del otro progenitor estará reprimido (expresión
monoalélica). Para diferentes genes pasibles de sufrir imprinting, en
algunas poblaciones celulares en desarrollo sólo se expresará el
alelo de la madre y, en otras poblaciones celulares, se expresará sólo
el alelo que viene por línea paterna. Así, si en una población celular
en desarrollo sólo se expresa el alelo proveniente de la madre pero
el genoma proviene sólo del padre, aunque la población celular sea
diploide, sufrirá un déficit grave debido a que los alelos que posee,
para una cierta función, se encuentran ambos reprimidos.
En resumen, el concepto de no equivalencia de la gametas alude al
hecho de que la información genética aportada por los conjuntos
cromosómicos materno y paterno, para el caso de algunos genes
pasibles de sufrir imprinting, no posee la misma capacidad de
expresarse en las células del nuevo individuo y que la información
que aportan las gametas es diferente y complementaria. Puede
notarse que este fenómeno, que se ha seleccionado a lo largo de la
evolución filogenética, y que caracteriza a la mayor parte de las
especies más evolucionadas, garantiza la variabilidad intraespecífica
evitando que existan individuos con la misma información genética.
Es sabido que, considerando períodos prolongados de tiempo, la
existencia de individuos con similar información genética disminuye
las probabilidades de adaptación a las condiciones cambiantes del
medio (Véase SC Ventajas de la diploidía, de la reproducción sexual
y de la exogamia).
SC 16.2. Genes pasibles de sufrir imprinting. Funciones de la
metilación en el imprinting. M. Rapacioli
Se denominan genes pasibles de sufrir imprinting o genes
de imprinting a aquellos que exhiben expresión monoalélica y en
los que el alelo que se expresa depende de su origen materno o
paterno.
Los genes de imprinting se concentran en clusters discretos. Se
considera que aproximadamente entre un 0,1% y un 1% de los

genes son pasibles de sufrir imprinting. Hasta el momento se han
identificado cerca de 100 genes de esta clase en
aproximadamente 10 regiones cromosómicas de imprinting.
El mecanismo general del imprinting involucra una secuencia de
pasos que incluye:
1. Establecimiento del imprinting (programación génica diferencial en
alelos de distinto origen parental).
2. Mantenimiento del imprinting en las células derivadas de la célula
huevo.
3. Reconocimiento del imprinting por la maquinaria de transcripción y
expresión monoalélica del gen.
4. Eliminación y reseteo del imprinting en las células germinales.
Las alteraciones en cualquiera de estos mecanismos puede llevar a
la pérdida de expresión monoalélica (LOI de Loss Of Imprinting).
Estas alteraciones conducen a patologías que difieren si se altera la
expresión del alelo paterno o materno.
El establecimiento del imprinting: la metilación del ADN. Se han
caracterizado varios mecanismos de programación genética
diferencial en alelos de distinto origen parental. El mejor conocido es
la metilación diferencial del ADN en las citosinas (C) de secuencias
5’CG3’ también denominadas CpG (p indica el fosfato de la unión
fosfodiéster). Nótese que por complementariedad de bases, la
secuencia 5’CpG3’ de una cadena del ADN se aparea con una
secuencia 5CpG’3’ de la cadena complementaria.
La metilación del ADN modifica la expresión génica mediante dos
mecanismos fundamentales: a) modifica la unión deproteínas
reguladoras de la expresión génica y b) recluta proteínas del
complejo de remodelación de la cromatina.
La metilación del ADN es heredable. Dada la duplicación
semiconservadora del ADN, una de las cadenas de ambas moléculas
de ADN generadas en la duplicación mantendrá la metilación. Existen
enzimas (ADN metiltransferasas de mantenimiento) que
reconocen las CpG metiladas en una cadena y metilan a la CpG de
la cadena complementaria.
En los clusters donde se localizan los genes de imprinting existen
una o más regiones de metilación diferencial o regiones
diferencialmente metiladas (DMR). Estas regiones poseen
patrones de metilación complementarios en alelos maternos y
paternos. Se denominan también regiones de control
de imprinting (ICR).

La metilación de los genes de imprinting es eliminada, y restablecida,
en cada generación, durante la gametogénesis. Las células
germinales primitivas heredan alelos maternos y paternos con sus
respectivos patrones de metilación. Durante la gametogénesis, las
células germinales eliminan los patrones de imprinting de cada
progenitor y se establece el patrón propio del sexo del embrión. El
patrón de imprinting de los progenitores es eliminado gradualmente
mientras las células germinales primitivas migran hacia las gónadas.
El reseteo en el patrón de metilación se produce diferentemente en
diferentes clustersde genes de imprinting. En células germinales que
no llegan a las gónadas, algunos clusters de genes de imprinting no
se desmetilan. Éste sería un indicio de que la gónada en desarrollo
posee algún efecto sobre el patrón de metilación de las células
germinales.
En el caso de la ovogénesis, el patrón de metilación se establece en
sucesivas fases durante el desarrollo folicular: algunosclusters se
metilan durante la fase de folículo primordial/primario, otros durante
el estado de folículo secundario, otros durante el estado de folículo
antral temprano y otros durante el estado de folículo antral tardío.
En el caso de la espermatogénesis, se ha observado que la
eliminación del patrón de metilación heredado se realiza ya en el
estado de espermatogonias fetales. Se han encontrado clusters en
los que el patrón de metilación se establece recién en el estado de
espermatogonias adultas. La metilación se mantiene en el cito I, cito
II, espermátides y espermatozoides.
No se conocen los mecanismos que determinan la metilación
diferencial en células germinales masculinas y femeninas, pero es de
suponer que existen procesos que determinen diferentes patrones de
metilación. Se han postulado los siguientes:
1. Expresión diferencial o splicing alternativo de ADN
metiltransferasas.
2. Actividad diferencial de ADN metiltransferasas dependiente de
expresión diferencial de proteínas que regulan su actividad.
3. Expresión diferencial de proteínas histónicas que modificarían la
susceptibilidad a metilación de las regiones de metilación diferencial.
4. Expresión diferencial de proteínas responsables de la
desmetilación (eliminación del patrón de metilación heredado).
Mantenimiento de la metilación. Luego de la fecundación, el
genoma sufre un proceso global de desmetilación. Sólo las regiones
de imprinting mantienen su metilación debido a la existencia de
determinadas ADN metiltransferasas de mantenimiento que
reconocen estas regiones.
Efecto de la metilación diferencial de las regiones de control
de imprinting. Ejemplos de expresión monoalélica debida a
metilación diferencial se hallan en la expresión del factor de
crecimiento símil insulina tipo II (Igf-2) y su receptor Igf2r en el
ratón. El Igf2 estimula el desarrollo y crecimiento de los tejidos
embrionarios, pero sólo se halla activo, en la mayor parte de los
tejidos embrionarios, el alelo del Igf2 de origen paterno. En estos
tejidos, el alelo de origen materno se halla inactivo. Así, si un ratón
hereda de su madre un alelo de Igf2 mutado, la mutación no se
expresa en el fenotipo. Por el contrario, la mutación en el alelo
heredado del padre sí produce un crecimiento deficiente. El receptor
de Igf2 presenta un patrón de expresión opuesto: el alelo de origen
paterno se expresa muy poco mientras que el de origen materno tiene
una alta tasa de expresión.
Diferentes clusters de genes de imprinting poseen diferentes
mecanismos de regulación de la expresión génica que son
modificados mediante metilación diferencial del ADN. Ilustraremos
aquí dos ejemplos.
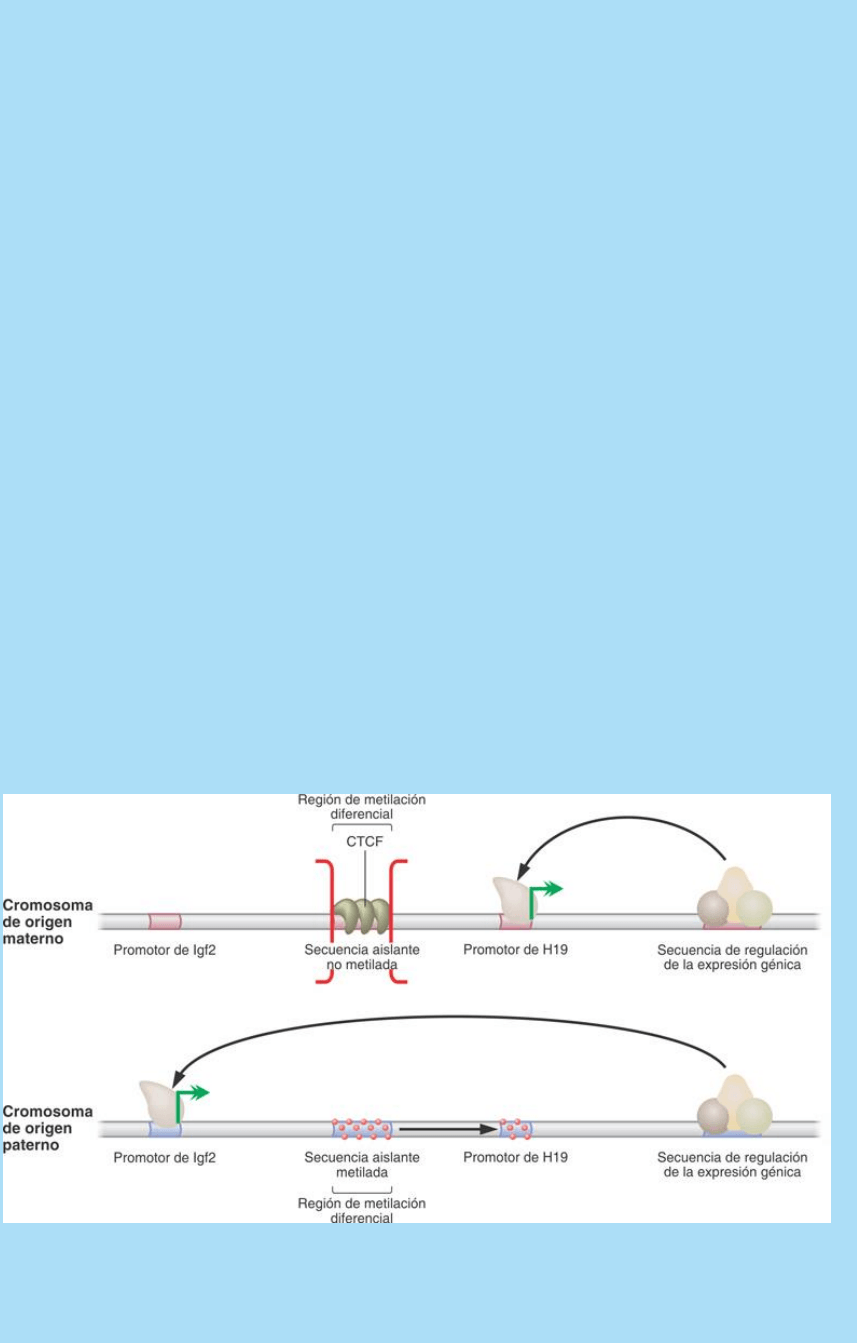
Fig. SC 16-2-1. Expresión monoalélica de Igf2 a partir del alelo de
origen paterno como consecuencia de la metilación diferencial de una
secuencia aislante.
En la figura SC 16-2-1 puede observarse que los genes de
la proteína factor de crecimiento insulínico tipo 2 (Igf2) y del ARN
no- codificante H19 están regulados por la misma secuencia
reguladora de expresión génica. Entre los promotores de ambos
genes hay una secuencia aislante (insulator) que se metila
diferencialmente en ovocitos y espermatozoides. En las células
somáticas, la secuencia aislante del cromosoma de origen
materno no se halla metilada. Esto permite la unión de laproteína
factor de transcripción represor CTCF (un factor de transcripción
de tipo dedos de zinc) que reconoce secuencias CCCTF no metiladas
y le otorga actividad a la secuencia aislante. En estas condiciones, la
secuencia de regulación de expresión génica no puede interactuar
con el promotor del gen de Igf2 y en consecuencia el alelo materno
de este gen Igf2no transcribe. Esta secuencia sí puede interactuar
con el promotor del gen de H19 y en consecuencia el alelo materno
deH19 sí transcribe.
El cromosoma de origen paterno, por el contrario, posee la secuencia
aislante metilada. Esta metilación se produce durante la
espermatogénesis. Este hecho impide la unión de la proteína CTCF
a la secuencia aislante y ésta queda inactivada (no funciona como
aislante). Por consiguiente, la secuencia de regulación de expresión
génica puede interactuar con el promotor de Igf2 y el alelo paterno
de Igf2 sí transcribe. Durante las etapas tempranas del desarrollo,
luego de la implantación, la metilación de la secuencia aislante se
expande hacia el promotor de H19 y en consecuencia se forma una
estructura de cromatina cerrada inaccesible para los factores de
transcripción. Como consecuencia de este hecho el alelo paterno
de H19no transcribe.
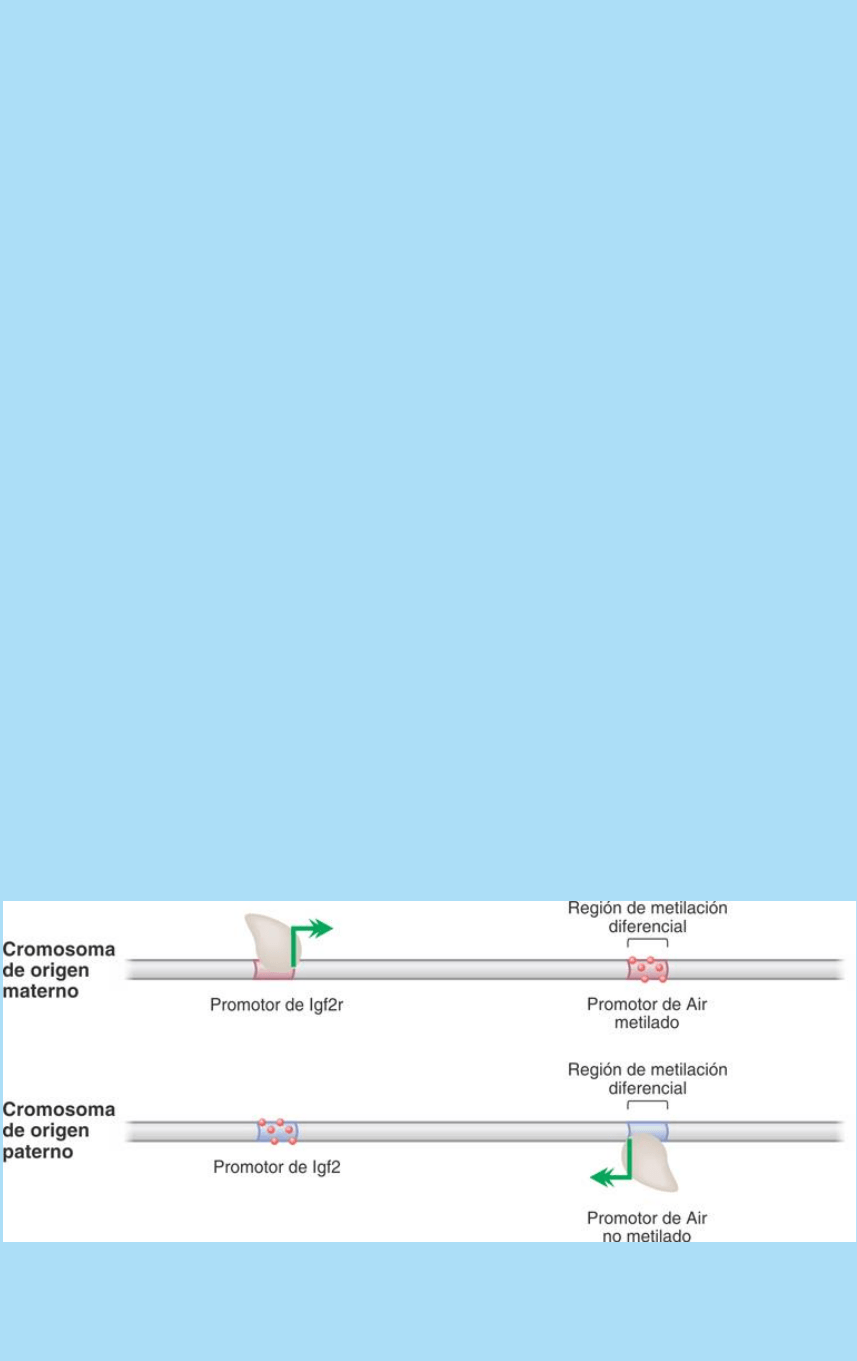
Fig. SC 16-2-2. Expresión monoalélica de Igf2r a partir del alelo de
origen materno como consecuencia de la metilación diferencial del
promotor de un gen de un ARN antisentido.

En la figura SC 16-2-2 se ilustra que en el gen codificante de la
proteína receptor del Igf2 o Ifgr2 hay, en el segundo intrón, una ICR
que es, además, promotor del gen de un ARN no codificante
Air que transcribe en sentido inverso al gen Igf2r por lo queAir tiene
secuencia complementaria o antisentido a Igf2r. En el cromosoma de
origen materno, el promotor del gen Air está metilado, en
consecuencia el alelo materno de Air no se transcribe. El alelo
materno de Igf2r sí transcribe. Otros tres genes del
mismo cluster, Slc22a1, Slc22a2 y Slc22a3 sí transcriben. En el
cromosoma paterno, el promotor de Air no está metilado. El alelo
paterno de Air sí transcribe y su transcripto interactúa con el
transcripto del gen Igf2r quedando éste inactivo. Secundariamente
se metila el promotor de Igf2r y, en consecuencia, el alelo paterno
de Igf2r no transcribe. Slc22a1permanece activo
pero Slc22a2 y Slc22a3 se inactivan.

Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.