
SC 15.1. La implantación del embrión. Significado biológico.
Complejidad y etapas del proceso. V.Flores
La concepción de la implantación como fenómeno integrado en el
cual participan activamente el endometrio y el blastocisto proviene de
fines del siglo pasado. En 1883, Spee señaló que “el embrión está
rodeado en el endometrio de una cavidad de implantación en los
bordes de la cual los tejidos uterinos muestran signos de
degeneración y lisis"; enfatizó “la aparente actividad histolítica y
citolítica del trofoblasto", supuso la existencia de influencias del
embrión sobre el endometrio y postuló la ocurrencia en el endometrio
de “procesos bioquímicos … [en el útero] … estimulados por [el
embrión]".
Las ideas planteadas por Spee sobre qué papeles desempeñan el
endometrio y el blastocisto durante la implantación, y la importancia
de las interacciones entre ambos siguen vigentes. Sus ideas han
estimulado innumerables investigaciones que todavía continúan con
el objeto de elaborar un modelo que permita interpretar el proceso en
toda su complejidad.
La implantación consiste en…
a)… un conjunto de procesos por medio de los cuales el trofoblasto
se introduce en el endometrio,
b)… se pone en contacto directo con el medio interno materno y
c)… posibilita que el embrión obtenga de la madre todos los
elementos necesarios para su desarrollo normal.
El embrión no se pone en contacto directo con el medio interno
materno. Se vincula con él a través del corion, derivado trofoblástico
que establece y regula las interacciones con la madre.
Si bien es el trofoblasto, y no el embrión propiamente dicho, el que
contacta con la madre, al estar aquél formado por células de una
composición genética distinta de la de la madre, la implantación
implica el contacto directo entre dos individuos genéticamente
distintos. Esto involucra aspectos inmunitarios en el proceso de
implantación.
La implantación ocurre en un contexto hormonal delicadamente
controlado. Las funciones tubáricas y la maduración del endometrio
están regulados hormonalmente. El éxito de la implantación requiere
una sincronización entre estos procesos y la maduración del embrión.

La regulación de la implantación requiere fenómenos que involucran
interacciones locales paracrinas y acciones endocrinas que se
realizan a larga distancia. En las etapas iniciales de la implantación,
el endometrio y el blastocisto interactúan localmente por medio de
agentes de diversa naturaleza química. Todos estos procesos deben
ocurrir en una secuencia ordenada para que ocurra una implantación
normal. Constituyen las características que hacen considerar a la
implantación como un proceso biológico dinámico de alta
complejidad en el que tanto blastocisto como endometrio participan
activamente.
La secuencia de interacciones endometrio-trofoblasto durante la
implantación del embrión
Con fines descriptivos, en el proceso de implantación se han definido
varias etapas. Los límites entre ellas son convencionales y su número
depende del grado de detalle de la descripción y análisis:
a) Los acontecimientos a los cuales se suele asignar el carácter
de signos de inicio de la implantación son, por parte del embrión,
la expansión del blastocisto y, por parte del endometrio, la
aparición de diferenciaciones de la membrana apical de las células
del epitelio uterino denominadas pinópodos (SC El período de
receptividad del endometrio. Características ultraestructurales y
moleculares de la ventana de implantación).
b) A este fenómeno sigue más o menos inmediatamente
la degradación de la membrana pelúcida y la eclosión del
blastocisto.
c) Una vez libre el blastocisto, se inicia la adhesión blastocisto-
endomentrio. A continuación se produce la penetración en el
endometrio simultáneamente con la diferenciación del trofoblasto en
un sincitio. En algunas especies se produce una reacción sincitial
localizada en las células endometriales en las proximidades del
blastocisto.
d) En la especie humana, luego del contacto trofoblasto-epitelio
endometrial, las superficies laterales de las células epiteliales
endometriales se separan y entre ellas se introducen
prolongaciones y células trofoblásticas.
e) A continuación se produce una erosión del epitelio, debido a la
degeneración y descamación de células epiteliales, en la zona de
contacto endometrio- blastocisto.
f) Luego, el trofoblasto sincitial toma contacto con el estroma y se
inicia la invasión de éste.

g) Una vez que la vesícula coriónica ha penetrado completamente en
el endometrio, la zona de erosión superficial se repara. El embrión
queda entonces totalmente incluido en la mucosa uterina.
h) Como etapa final, los derivados del trofoblasto (citotrofoblasto y
sincitiotrofoblasto) se asocian al mesodermo extraembrionario
somático. Los tres tejidos se organizan en tres capas que, en
conjunto, forman el corion.
Las etapas mencionadas están en parte superpuestas
temporalmente: mientras el blastocisto se aproxima al endometrio, se
inicia la diferenciación temprana del trofoblasto polar, el blastocisto
se expande y se disuelve la membrana pelúcida. Sólo por
conveniencia didáctica se las separa de esta forma.
SC 15.2. La adhesión blastocisto-endometrio: fijación y
orientación del blastocisto respecto del endometrio. V. Flores
La adhesión del blastocisto al endometrio implica también una
orientación. La adhesión ocurre entre zonas específicas, de mayor
afinidad o “adherencia”, entre las superficies de endometrio y
blastocisto. Vale decir, existe una mayor afinidad y en consecuencia
una mayor probabilidad de fijación, entre ciertas zonas específicas
del blastocisto y del epitelio endometrial.
En la especie humana, el sitio más frecuente de adhesión del
blastocisto al endometrio es la región superior de la cara posterior
de la mucosa uterina (cerca del fondo uterino). A su vez, el
blastocisto se orienta respecto del endometrio contactando por la
zona del trofoblasto polar (polo animal o embrionario).
Debido a estos hechos se considera que la colisión, y ulterior
adhesión, al azar entre el blastocisto y endometrio no es condición
suficiente para explicar a) la existencia de un sitio de implantación
preferencial en el endometrio y b) la orientación preferencial del
blastocisto respecto del endometrio.
Esta situación se debe a que las propiedades adhesivas del epitelio
uterino y del blastocisto no se distribuyen homogéneamente en sus
superficies. Se considera que la adhesión blastocisto-endometrio
depende de las características químicas de ambas superficies. Las
hipótesis están dirigidas fundamentalmente hacia las cubiertas de
superficie (glucocálices) del epitelio endometrial y del blastocisto.
Se ha postulado que las glucoproteínas de estas cubiertas pueden
mediar la adhesión entre ambos. Existe un conjunto de datos que
sustentan esta hipótesis:

a) El epitelio uterino posee un glucocáliz muy desarrollado, sobre
todo en las etapas en las que el embrión se implanta. Con técnicas
inmunohistoquímicas es posible poner de manifiesto una gruesa
capa de glucoproteínas en la membrana apical de las células
epiteliales endometriales y también en la superficie de las células del
blastocisto.
b) El glucocáliz de las células endometriales varía en su aspecto
ultraestructural y composición química según las fases del ciclo
reproductor; estas modificaciones dependen de las variaciones en los
niveles hormonales.
c) El glucocáliz del blastocisto modifica su viscosidad y se vuelve
más adhesiva al principio de la implantación. En este efecto parecen
participar modificaciones locales del pH.
d) En el inicio de la implantación, como parte de los fenómenos
propios de la reacción decidual primaria, se detecta alta actividad de
glucosidasas en las secreciones uterinas (Véase SC 15.3. La
degradación de la membrana pelúcida. Acciones enzimáticas
sinérgicas. La reacción decidual primaria). Estas enzimas poseen
capacidad de modificar la composición de los grupos azúcares de las
glucoproteínas de superficie tanto del endometrio como del
blastocisto.
Existen trabajos que, con enfoque y metodología eminentemente
biofísicos, han permitido calcular la intensidad de las fuerzas que se
desarrollan entre líneas celulares derivadas del epitelio uterino y
células trofoblásticas humanas en distintos momentos del ciclo. El
método consiste en aproximar las superficies apicales de ambos
epitelios y, a través de sucesivos ciclos de aproximación-separación,
de diferente duración, estimar, por medio del uso del microscopio de
fuerza atómica, la intensidad de las fuerzas de repulsión y adhesión
entre las superficies apicales de ambos tipos celulares. Estos
estudios muestran que, cuando los epitelios están suficientemente
cerca, aparecen fuerzas repulsivas pero que, una vez superadas
éstas, aparecen fuerzas de adhesión de diversa intensidad. Estos
estudios permiten comprobar que existen fuerzas de atracción
intensas y que sus valores de intensidad dependen de las
características del glucocáliz y también de las diferenciaciones de las
membranas apicales.

Fig. SC 15-2-1. Esquema de la adhesión-orientación del blastocisto
respecto del endometrio. A. El endometrio posee zonas de alta
afinidad respecto del trofoblasto polar del blastocisto. Ello aumenta la
probabilidad de implantación en un sitio ricamente
vascularizado. B. El trofoblasto posee un sitio de alta afinidad, el
trofoblasto polar, respecto del endometrio. Ello aumenta la
probabilidad de que el embrión quede en la zona más profunda y
mejor vascularizada del endometrio.
Así, las características adhesivas de las superficies del blastocisto y
del epitelio endometrial por un lado dependen de fenómenos
sistémicos, como los niveles hormonales maternos en el momento de
la implantación, y también de fenómenos locales regulados por
moléculas que operan como mediadores locales.
La composición química de las superficies interactuantes, trofoblasto
del blastocisto y epitelio endomentrial, no sólo regulan el sitio de
implantación y la orientación del blastocisto, sino también el momento
o período de tiempo, denominado ventana de implantación, en el
que dicho proceso se produce con mayor probabilidad. Dicho período
de tiempo, de máxima receptividad del endometrio, se caracteriza
también por la expresión de una combinatoria típica de proteínas
integrinas, componentes integrales de la membrana apical de las
células del epitelio uterino. Dichas proteínas confieren al epitelio
uterino la posibilidad de realizar procesos de adhesión y de
señalización celular entre las células embrionarias y maternas.
SC 15.3. La degradación de la membrana pelúcida. Acciones
enzimáticas sinérgicas. La reacción decidual primaria. V. Flores
Algunos estudios bioquímicos realizados en el líquido intrauterino
muestran que en él se encuentran prácticamente todas las enzimas
necesarias para la degradación de la membrana pelúcida: una
variedad de enzimas genéricamente denominadas glucosidasas y

proteasas (exopeptidasas y endopeptidasas). La concentración de
estas enzimas varía con el ciclo sexual. También existen variaciones
asociadas a la presencia del blastocisto en la cavidad uterina.
Ciertos estudios histoquímicos tendientes a identificar las células que
sintetizan estas enzimas han puesto de manifiesto que, con
diferencias para las distintas especies y enzimas en su síntesis,
participan activa y coordinadamente el endometrio y el blastocisto.
Por parte del endometrio, tanto el epitelio como el estroma participan
en su síntesis y secreción. En el blastocisto, la fuente fundamental de
enzimas es el trofoblasto.
En las secreciones uterinas también se ha encontrado un patrón
característico de uteroglobinas. Estas proteínas tendrían funciones
regulatorias de las interacciones entre endometrio y blastocisto. La
síntesis de uteroglobinas también es sensible a las variaciones en los
niveles hormonales maternos.
Varios estudios bioquímicos, histoquímicos e inmunohistoquímicos
realizados en úteros de animales preñados ‒en los cuales existe un
blastocisto en la cavidad uterina‒ y seudopreñados –en los cuales no
hay blastocisto en la cavidad uterina‒ muestran que el blastocisto
ejerce un efecto estimulante de la síntesis y liberación de algunas de
las enzimas antes mencionadas.
Estos estudios muestran que el efecto estimulante de la síntesis y
secreción de enzimas, ejercido por el blastocisto, se produce a) antes
de que exista contacto físico entre blastocisto y endometrio y,
significativamente, b) sólo se produce en las proximidades del
blastocisto. Estas dos circunstancias sugieren que dicho efecto está
mediado por moléculas señal difusibles liberadas por el blastocisto y
que éstas tienen escaso rango de acción.
Los cambios locales que sufre el endometrio en respuesta a señales
difusibles del blastocisto, antes de que éste tome contacto con el
epitelio endometrial se denominan reacción decidual primaria para
distinguirlos de los cambios denominados reacción decidual que
sufre el endometrio cuando ya es invadido por el blastocisto.
Algunos estudios realizados para investigar el papel funcional de
estas enzimas (tratamiento enzimático de membranas pelúcidas in
vitro, inyección intrauterina de inhibidores de las distintas enzimas,
etc.) muestran que las glucosidasas por sí solas no son capaces de
lisar la membrana pelúcida y que las exopeptidasas
(fundamentalmente aminopeptidasas) tampoco la disgregan
completamente. Las endopeptidasas, sobre todo las sintetizadas por
el blastocisto, poseen un efecto más intenso sobre la membrana
pelúcida.
Varios estudios de este tipo muestran que las enzimas actúan
sinérgicamente durante la degradación de la membrana pelúcida.
Las glucosidasas y exopeptidasas actúan en las fases preparatorias
produciendo la degradación parcial de algunos de los componentes
de la membrana. A continuación, la acción de las endopeptidasas la
disgregaría por completo.
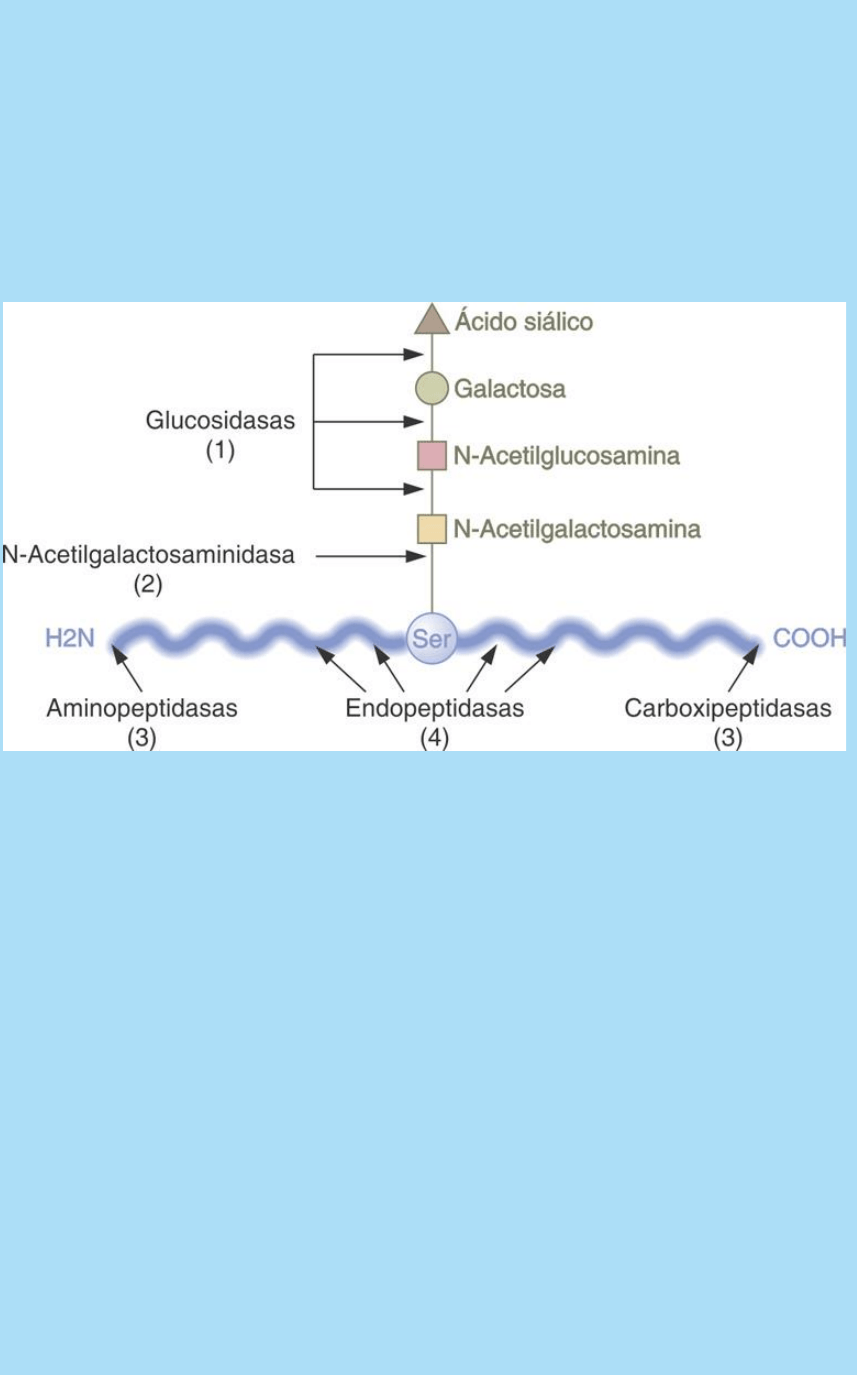
Figura SC 15.3.1. Modelo de las acciones sinérgicas, y en cascada,
de las diversos tipos de enzimas que participan en la degradación de
los componentes específicos de la membrana pelúcida. Diversos
estudios muestran que tanto el blastocisto como el endometrio
participan activamente aportando enzimas que degradan la
membrana pelúcida.
La figura precedente ilustra esquemáticamente un modelo de la
acción sinérgica (en cascada) de las enzimas que participan en la
degradación de la membrana pelúcida. El modelo propone la
siguiente secuencia de eventos:
1) La acción de las glucosidasas tendría como efecto la eliminación
sucesiva de los distintos monosacáridos constituyentes de las
cadenas laterales de oligosacáridos.
2) Una enzima en particular, la O-seril-N-acetilgalactosaminidasa,
rompería la unión del azúcar al aminoácido serina (SER) de la
proteína.
3) Una vez que la proteína está desprovista de las cadenas laterales
de oligosacáridos, estaría expuesta a las exopeptidasas

(aminopeptidasas y carboxipeptidasas) que actuarían con mayor
eficacia.
4) Finalmente, las endopeptidasas la degradarían por completo
actuando en varios puntos de su estructura.
SC 15.4. La diferenciación preimplantatoria del trofoblasto. La
reacción decidual primaria. El establecimiento del contacto
trofoblasto-endometrio y la invasión temprana. V. Flores
La diferenciación temprana, o preimplantatoria, del trofoblasto, previa
a la eclosión del blastocisto, lleva a la adquisición de la capacidad
para degradar la membrana pelúcida y, precisamente, conduce a la
eclosión. La diferenciación prosigue luego, pero con otras
características, durante el contacto con el endometrio y su
penetración.
La diferenciación temprana se inicia con la proliferación de algunas
regiones del trofoblasto y la formación de engrosamientos o botones
trofoblásticos compuestos por células redondeadas. En algunas
especies, este fenómeno se produce en varias zonas del trofoblasto.
En la especie humana ocurre sólo en el trofoblasto polar que
recubre el disco embrionario. A continuación, las células crecen.
Aumenta el tamaño del citoplasma y del núcleo y secretan las
enzimas que producen la degradación de la membrana pelúcida y la
eclosión del blastocisto.
La reacción decidual primaria es respuesta a estímulos
provenientes del embrión. Simultáneamente con la maduración del
blastocisto y la degradación de la membrana pelúcida en el
endometrio se producen varios cambios. En las cercanías del
blastocisto, el estroma se vuelve edematoso, los vasos se dilatan, se
congestionan, y la actividad secretoria de las glándulas aumenta.
Estas modificaciones se inician antes de cualquier contacto efectivo
entre blastocisto y endometrio y depende de la liberación de
sustancias difusibles que median tales interacciones.
El blastocisto produce y libera factores de crecimiento, hormonas
peptídicas (gonadotrofina coriónica), hormonas esteroideas
(estrógenos), prostaglandina, histamina, etc., que actúan en el
endometrio en forma local, También se ha demostrado una
importante actividad secretoria por parte de los mastocitos y otras
células endometriales con la secreción de citoquinas
proinflamatorias. Tal actividad coadyuvaría a la acción de las
sustancias provenientes del blastocisto.
El endometrio no actúa pasivamente. Durante esta fase temprana,
las células de revestimiento epitelial uterino sufren a) una importante

diferenciación molecular puesta de manifiesto por la expresión de un
patrón típico de proteínas transmembrana, como las integrinas
y b) una diferenciación ultraestructural del dominio apical de la
membrana plasmática con la formación de prolongaciones o
abultamientos de la membrana apical que exhiben alta adhesividad
respecto del trofoblasto. Precisamente la aparición de ambas
diferenciaciones es considerada como indicio, por parte del
endometrio, del inicio de la “ventana de implantación” o “período de
receptividad” para la implantación.
El contacto blastocisto-endometrio tiene dos etapas: a) una primera
etapa de adhesión lábil en la que ambos pueden unirse en forma débil
y pueden volver a separarse y b) una segunda etapa unión estable
en la que el contacto es irreversible y va seguido de la invasión del
epitelio. La adhesión lábil estaría mediada por interacciones entre los
componentes de los glucocálices de ambos epitelios y la unión
estable consiste en el contacto directo entre componentes de las
membranas plasmáticas, formación de interdigitaciones y
diferenciaciones de unión de las superficies apicales de ambas
poblaciones celulares (microvellosidades del trofoblasto y pinópodos
de las células endometriales) (SC 15.2. La adhesión blastocisto-
endometrio: fijación y orientación del blastocisto respecto del
endometrio).
Luego de la unión estable entre las células maternas y embrionarias,
en la que las membranas quedan transitoriamente interdigitadas, las
membranas se alisan, se adosan íntimamente y las diferenciaciones
de unión permanecen durante un tiempo. A continuación,
prolongaciones de las células trofoblásticas se introducen entre las
células del epitelio uterino. En algunas especies, el epitelio uterino
sufre una reacción sincitial. En otras se descama dejando el estroma
expuesto. En mamíferos se han identificado al menos cuatro
variantes de estrategias por medio de las cuales las células del
trofoblasto atraviesan el epitelio uterino y entran en contacto con el
estroma endometrial. Estas cuatro variantes básicas están ilustradas
por el modo como se produce este fenómeno en otros tantos
conjuntos de especies (ratas y ratones, hámsteres, conejos y
primates).
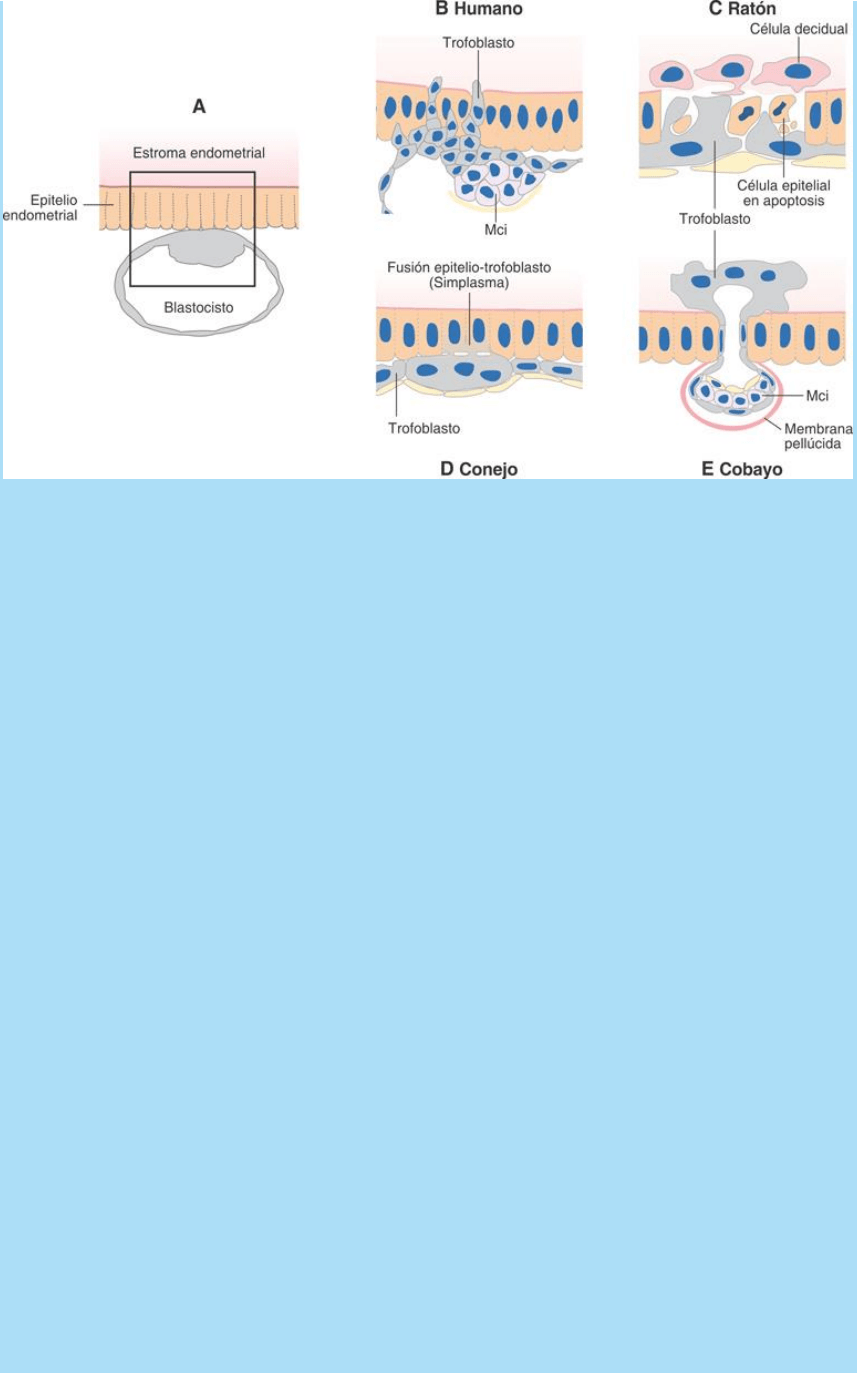
Fig. 15-4-1. Estrategias básicas de contacto y penetración del
epitelio uterino en diferentes especies. En todos los casos se trata de
poner al embrión en contacto con el medio interno materno. Estos
modelos se basan en análisis realizados al nivel de la microscopia
electrónica de transmisión. Las células del trofoblasto generan una
discontinuidad en el epitelio uterino induciendo apoptosis, emitiendo
brotes, fusionándose con las células uterinas o realizando una
reacción sincitial e intercalándose con las células
epiteliales. A. Adhesión-orientación del blastocisto al
endometrio. B. Detalle de la penetración del trofoblasto en el epitelio
endometrial. C-E. Ilustran el proceso en otras especies.
AT.: dentro de la fig. cambiar pellúcida
pelúcida
En todos los casos las células epiteliales se agrandan, se vuelven
vesiculosas y se llenan de lisosomas y lisofagosomas. Algunas
modificaciones similares se observan en las células del estroma
subepitelial. Se discute si las células endometriales son eliminadas
exclusivamente por la acción enzimática del blastocisto, o si es
fundamentalmente un fenómeno de autodegradación en respuesta a
estímulos provenientes de éste, pero existe consenso en la idea de
que en el proceso participan activamente el trofoblasto y el epitelio y
estroma endometriales.
La invasión del estroma. El control enzimático de la degradación
de la matriz extracelular. La penetración del blastocisto en el
endometrio requiere la desintegración de la matriz extracelular y de
las fibras del tejido conectivo que constituyen su soporte. Dicho
proceso es llevado a cabo por la acción de enzimas liberadas al
intersticio. Se trata de actividades enzimáticas similares, en algunos

casos, a las involucradas en la degradación de la membrana
pelúcida. Por medio de diversos ensayos bioquímicos ‒prueba de
afinidad de sustrato‒ se ha podido determinar que algunas son de
origen materno y otras de origen embrionario. Describimos a
continuación un ejemplo sobre cómo una enzima de origen
embrionario puede actuar integradamente con las maternas.
Se sabe que el trofoblasto es capaz de sintetizar y secretar una
enzima denominada activador del plasminógeno (PA). Se trata de
una enzima con capacidad para degradar proteínas (proteasa)
extracelulares que cumple un papel importante en la invasión del
endometrio. El PA es una enzima de alta especificidad de sustrato,
vale decir, capaz de actuar sobre un rango muy reducido de sustratos
posibles. Sin embargo, se postula que participa en la degradación de
una variedad muy grande de componentes de la matriz extracelular.
Ello es posible debido a que puede iniciar una cascada de actividades
enzimáticas de origen materno. El gráfico que sigue ilustra
esquemáticamente el proceso.
El modelo, representado esquemáticamente, propone la siguiente
sucesión de eventos:
a) El PA ‒de origen embrionario‒ actúa sobre el plasminógeno (de
origen materno) activándolo a plasmina.
b) La plasmina, que posee amplio rango de sustrato, degrada varios
componentes de la matriz extracelular (glucoproteínas,
proteoglucanos, laminina, fibronectina, etc.)
c) La plasmina, además, es capaz de activar algunas proenzimas
como las procolagenasas tipos VI y V que se transforman en
colagenasas
d) Las colagenasas degradan las fibras del intersticio endometrial y
de las membranas basales de los vasos uterinos.
e) La degradación de todos los componentes mencionados conduce
a la desorganización de la matriz extracelular del estroma uterino y
de las paredes de los vasos endometriales (SC Procesos regulados
de proteólisis extracelular y de remodelación de la matriz
extracelular). Este ejemplo ilustra cómo la implantación requiere la
acción conjunta de sistemas enzimáticos de origen embrionario y
materno.
SC 15.5. Nociones sobre histogénesis placentaria. Tipos de
vellosidades y patrón temporal de diferenciación. V. Flores
El corion se desarrolla durante toda la gestación y sufre cambios
adaptativos a los requerimientos fetales. Una vez que el corion llega
a su máxima eficacia funcional en la especie humana posee al menos
5 tipos diferentes de organización de vellosidades coriales. Estos
diferentes tipos de vellosidades van apareciendo unos a continuación
de los otros o, en algunos casos, unos diferenciándose en otros.
La figura SC 15-5-1 ilustra esquemáticamente la organización básica
de un placentomo (lóbulo placentario o unidad anatomofuncional
placentaria) y de la organización de las vellosidadades en su región
periférica. (SC 15.6. La organización estructural y funcional del
placentomo. Su variabilidad. Hipótesis sobre la génesis de la
morfología del lóbulo placentario). Posee un tronco central a través
del cual nacen elementos periféricos que, según van madurando van
transformándose y, además, generan nuevas ramas con
organización menos diferenciada.
Una vellosidad troncal ocupa el centro de la unidad y posee un
extremo terminal en constante crecimiento (vellosidad intermedia
inmadura) y ramas más diferenciadas (vellosidad intermedia madura)
de las que brotan vellosidades terminales. Éstas constituyen
diferenciaciones estructurales y funcionales en las que asientan las
membranas vasculosincitiales especializadas en el transporte de
gases y nutrientes.
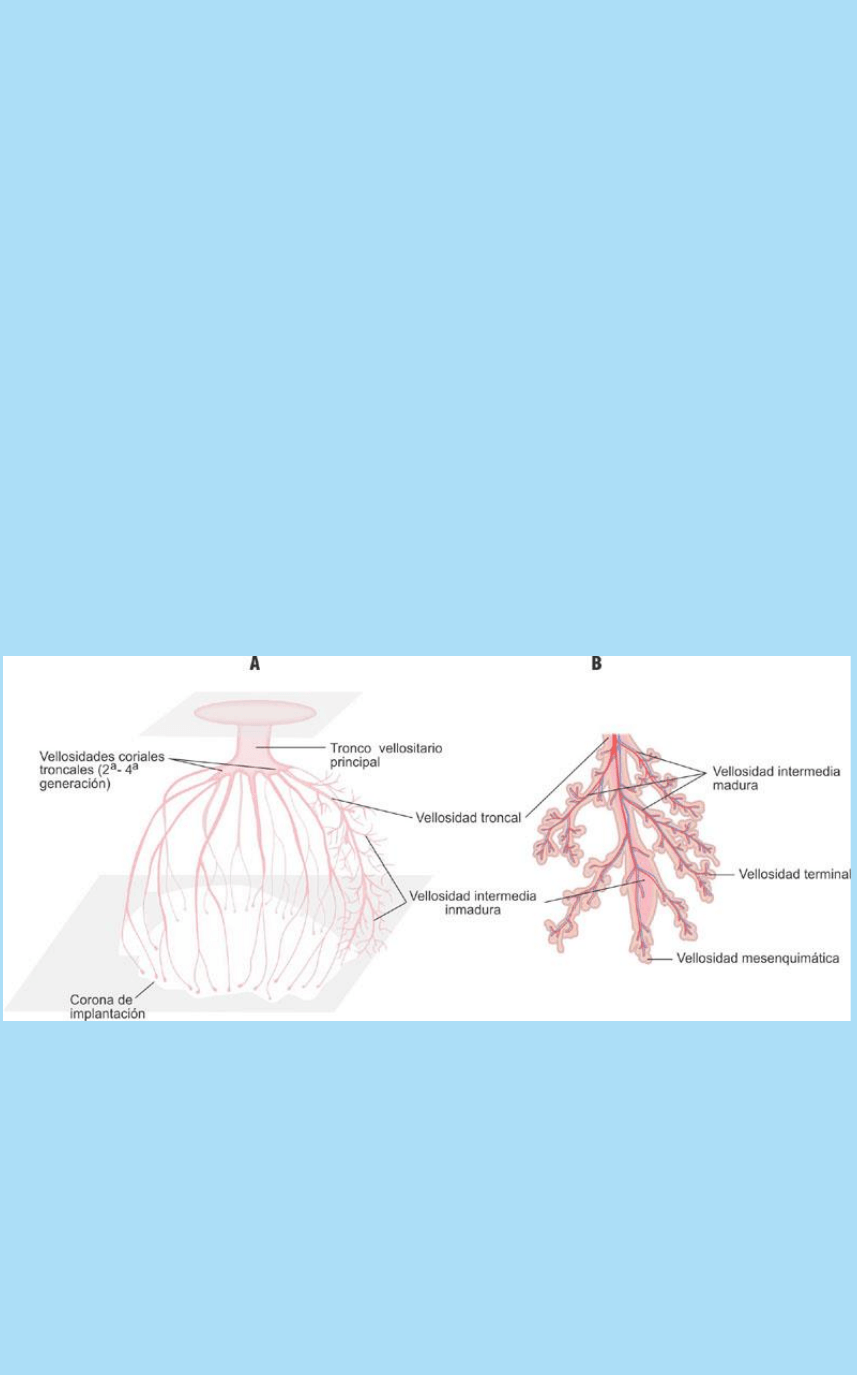
Fig. 15-5-1. A. Esquema de la organización de un lóbulo placentario
o placentomo. B. Esquema de la organización de región periférica de
un lóbulo placentario. 1. En el centro del esquema, región superior,
se ilustra una gruesa vellosidad correspondiente a una vellosidad
troncal (rama de un tronco vellositario principal). 2. La vellosidad
troncal se continúa, centro de la región inferior, con una
estructuración diferente, y más inmadura de sus tejidos, en una
vellosidad intermedia inmadura. 3. Como ramas de la vellosidad
troncal surgen las vellosidades intermedias maduras. 4. Estas últimas
dan nacimiento a vellosidades terminales en las que asientan zonas
con membrana vasculosincitial. 5. En los extremos de las

vellosidades intermedias maduras e inmaduras, como manifestación
de crecimiento permanente de la placenta, se hallan las vellosidades
mesenquimáticas. Poseen una estructura similar a las primitivas
vellosidades que se forman durante la implantación y, como ellas, se
clasifican en 1.ª, 2.ª y 3.ª.
La figura SC 15-5-2 muestra esquemáticamente la estructura básica
de cada tipo de vellosidad.
1) Vellosidades coriales troncales. Corresponden a las primeras
ramificaciones (unas cuatro generaciones) cortas y gruesas que
sostienen todo el árbol velloso. Representan un tercio del volumen
total del tejido velloso de la placenta madura. Ocupan la región
central subcorial del lóbulo placentario. Poseen un eje de
mesénquima compacto con arterias, venas, arteriolas y vénulas y
algunos capilares superficiales.
2) Vellosidades intermedias maduras. Son ramas laterales
(periféricas) de las vellosidades troncales sobre las cuales asienta la
mayor parte de las vellosidades terminales. Tienen un diámetro de
60-150 μm. Representan un cuarto de las vellosidades coriales de la
placenta madura; tienen un eje de mesénquima muy laxo que ocupa
el 50% del volumen de la vellosidad a través del cual corren
arteriolas, vénulas y capilares. El CTB es discontinuo en partes y el
SCTB posee un grosor uniforme con núcleos regularmente
distribuidos.
3) Vellosidades terminales. Son las ramas finales (hojas) del árbol
velloso; nacen de las vellosidades intermedias maduras como
protrusiones vesiculosas debido a que contienen capilares
sinusoidales muy dilatados que ocupan la mayor parte de la
vellosidad. El SCTB posee la típica estructura diferenciada en
nódulos sincitiales y membrana vasculosincitial (SC 15.7. La
diferenciación estructural y funcional de la placenta de término. Los
nódulos sincitiales y la membrana vasculosincitial). A estas
vellosidades, que empiezan a aparecer en la 27.ª SD, les
corresponde un 30-40% del volumen del árbol velloso, un 50% de la
superficie sincitial total y constituyen un 60% de las vellosidades en
el corion maduro.
4) Vellosidades intermedias inmaduras. Corresponden a la región
terminal de las vellosidades troncales. Predominan en las placentas
inmaduras. Poseen un eje de mesénquima laxo y abundante con
muchos macrófagos y un lecho vascular de arteriolas, vénulas y
capilares. Tienen una capa de CTB y un SCTB de grosor regular y
núcleos homogéneamente distribuidos.
5) Vellosidades mesenquimáticas. Corresponden a un estado de
desarrollo temprano, y transitorio, de la vellosidad corial.
A este tipo corresponde la primera generación de vellosidades
coriales. Son, relativamente, más abundantes al principio, pero se
siguen formando durante toda la gestación, preferentemente, en los
extremos terminales de las últimas ramas (las más jóvenes) de las
vellosidades intermedias inmaduras. Pasan por los tres estados
básicos descritos para la primera generación de vellosidades: a) de
proliferación CTB, b) invasión de mesénquima y c) vascularización.
Desde sus extremos de crecimiento terminales de forma cónica, en
dirección proximal, se siguen observando estas tres estructuraciones
mencionadas. A continuación, se diferencian en vellosidades
intermedias maduras y, las que quedan en el extremo de crecimiento
del árbol, en vellosidades intermedias inmaduras. Éstas siguen
formando nuevas vellosidades mesenquimáticas hasta que crece y
se diferencia en parte del tronco velloso. El eje de mesénquima es
laxo, abundante, con pocos macrófagos y una red capilar en
formación. Poseen una capa continua de CTB y, por afuera, un SCTB
de grosor regular y núcleos homogéneamente descritos.
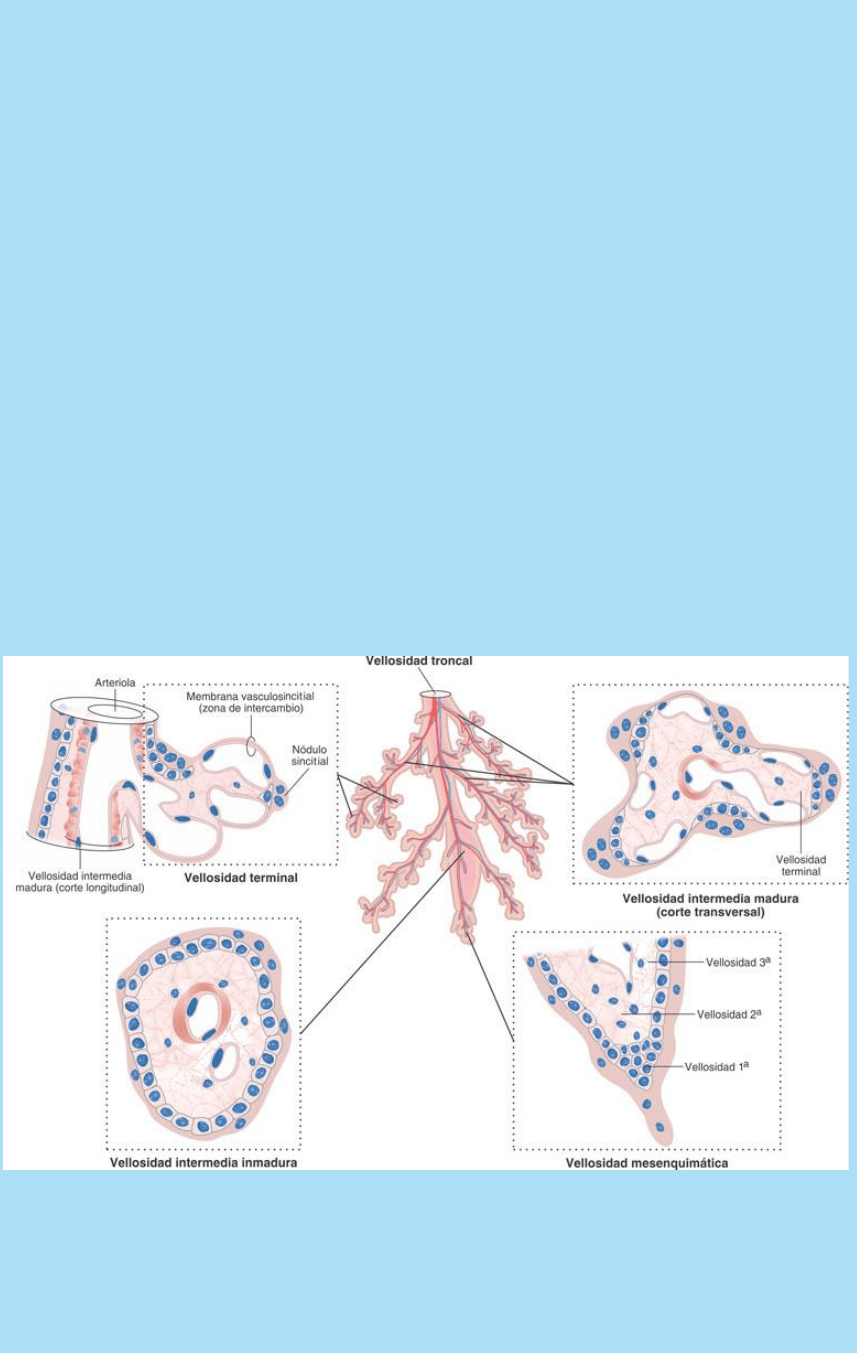
Fig. SC 15-5-2. Representación esquemática de la estructura
histológica de los distintos tipos de vellosidades que integran la
región periférica del lóbulo placentario o placentomo. (Modificado de
Haines & Taylor. Textbook of Obstetrical and Gynaecological
Pathology. 4th ed. 1995).

El patrón temporal de diferenciación de vellosidades coriales.
Durante las primeras semanas todas las vellosidades (1.ª, 2.ª y 3.ª)
son mesenquimáticas. Desde la 8.ª SD en adelante, poco antes de
que se inicie la circulación sanguínea, las que se han formado
primero empiezan a diferenciarse en vellosidades intermedias
inmaduras que, poco más tarde, se diferencian en troncos vellosos.
Mientras tanto, en los extremos de vellosidades intermedias
inmaduras se van formando nuevas vellosidades mesenquimáticas
que, a su vez, siguen el patrón de diferenciación de las primeras
(mesenquimáticas intermedias inmaduras troncos vellosos). La
formación de nuevas vellosidades mesenquimáticas y su
diferenciación ulterior en intermedias inmaduras empieza a disminuir
al final del 2.º trimestre, pero siempre continúa a un ritmo menor en
las zonas centrales del lóbulo placentario. Desde el principio del 3.er
trimestre, las vellosidades mesenquimáticas se diferencian
preferentemente en intermedias maduras, que originan a las
vellosidades terminales. Estas últimas son las que predominan en la
placenta de término. Cada lóbulo placentario sigue esta secuencia de
eventos aunque a un ritmo diferente según se trate de la región
central o periférica de la placenta. Nótese que la zona central de la
placenta es siempre más “vieja” que la periférica y, en consecuencia,
posee un mayor desarrollo y crecimiento de todas las estructuras
mencionadas.
SC 15.6. La organización estructural y funcional del
placentomo. Su variabilidad. Hipótesis sobre la génesis de la
morfología del lóbulo placentario. V. Flores
El cotiledón placentario. Clásicamente se consideró a los cotiledones
placentarios como las unidades anatomofuncionales de la placenta
incluso se enfatizado, en la práctica obstétrica, la importancia de
contar el número de cotiledones con el objeto de constatar que
ninguno se haya desprendido de la placa corial y retenido en el útero.
El número de cotiledones, sin embargo, no es constante sino, por el
contrario, muy variable. Cuando están bien demarcados su número
oscila, de acuerdo con Boyd y Hamilton, entre 10 y 38. Estos autores,
sin embargo, admiten que los cotiledones se hallan integrados por
unidades anatomofuncionales o "placentomos", también
denominados “lóbulo placentario” o “vellón” (SC 15.5. Nociones
sobre histogénesis placentaria. Tipos de vellosidades y patrón
temporal de diferenciación). Se ha señalado que la placenta de
término puede poseer alrededor de 200 lóbulos y que los
"cotiledones" observables a simple vista, sobre su superficie
decidual, resultan simplemente de la superposición de lóbulos. En la
Este documento contiene más páginas...
Descargar Completo
Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.