
SC 13.1. La cefalización. La hipótesis de la nueva cabeza. La
aparición y evolución de la cresta neural (CN) craneal. V.Flores
Se postula que el proceso de cefalización, en la línea evolutiva que
corresponde a los vertebrados (cordados superiores), se inició desde
los procordados en adelante.
El proceso de cefalización consistió en una diversidad de cambios
adaptativos vinculados al desplazamiento en una dirección
preferencial y a la concentración de funciones de recepción (órganos
de los sentidos especializados), de integración y procesamiento de
información proveniente del medioambiente y elaboración de
respuestas (hemisferios cerebrales) en la región cefálica. La
cefalización se acompañó de la aparición de nuevas estructuras
óseas, cartilaginosas y conectivas que conformaron el aparato de la
contención neurosensorial que forma las cubiertas protectoras del
encéfalo y los órganos de los sentidos, vale decir, buena parte del
cráneo y la cara con todas las cavidades (órbitas oculares, fosas
nasales, cavidad bucal, laberinto óseo). Todas estas estructuras se
formaron a partir de una población celular “nueva”, la CN preótica,
que apareció y evolucionó desde los Agnatos (peces sin mandíbula)
en adelante y que adquirió características de desarrollo similares, en
alguna medida, a las del mesodermo.
De acuerdo con la hipótesis evolutiva denominada de la Nueva
Cabeza, los vertebrados (cordados superiores) evolucionaron a partir
de un cefalocordado, similar al anfioxo actual, que pudo haber sido la
transición entre los urocordados y los vertebrados. Urocordados y
cefalocordados son subtipos del clado Procordados. Los
cefalocordados son animales cilíndricos, con una cuerda dorsal o
notocorda que se extiende hasta el extremo cefálico; de ahí su
designación taxonómica. Poseen un sistema nervioso, ubicado
dorsalmente a la cuerda dorsal, formado por un cordón nervioso y
con una vesícula cerebral en el extremo cefálico. Estos animales
carecen de cráneo y de mandíbulas, de ahí que se denominan
también Acranios y son clasificados entre los Agnatos. La boca posee
cirros móviles que desplazan partículas alimenticias hacia el interior
del tubo digestivo. Este animal precursor de los vertebrados, al igual
que el anfioxo, carecería de vesículas telencefálicas y de la
musculatura que mueve el agua a través de las branquias.
De acuerdo con la hipótesis mencionada, el salto evolutivo
significativo consistió en un cambio en el carácter filtrador de agua
por el de predador. Esta nueva característica incluyó el desarrollo de
órganos de los sentidos más desarrollados para la detección de la
presa, nuevas estructuras neurales para procesamiento de

información y elaboración de respuestas y un aparato mandibular de
rápida respuesta para la captura de la presa. El desarrollo de todas
estas estructuras de recepción de estímulos y de procesamiento de
información neural se acompañó del desarrollo de estructuras
conectivas, cartilaginosas y óseas que operarán de contención de las
nuevas estructuras neurales.
Un supuesto central de esta hipótesis es que algún o algunos tipos
celulares ya presentes en las especies predecesoras tuvieron que
haber evolucionado en relación con la aparición y evolución de la
cabeza. Una de tales poblaciones celulares podría haber sido
precursora de las actuales células de la CN preótica. Las ascidias,
urocordados primitivos, poseen un tipo celular que se origina a partir
del tubo neural, que migra y luego se diferencia en células
pigmentarias. Estas células expresanproteínas, como hnk y Zic1,
que algunos autores consideran marcadores de células de CN. Tales
células serían precursoras filogenéticas de la CN que, a lo largo de
la evolución, fueron adquiriendo mayor potencia evolutiva y nuevas
formas de evolución ontogenética.
Se propone que los primeros vertebrados pudieron haber sido
similares a los actuales peces sin mandíbula (Agnatos, Fig. SC 13-1-
1), como las lampreas actuales que son agnatos pero ya poseen CN.
Estos peces, aunque no tienen mandíbulas, poseen la boca
circundada por labios superiores e inferiores en cuyo desarrollo
participan células de la CN preótica correspondiente a las regiones
proencefálica y mesencefálica del SNC.
En los peces con mandíbulas (teleósteos), que corresponderían a un
estado más avanzado de la evolución filogenética, los arcos
faríngeos que originan las mandíbulas derivan de porciones más
caudales de la CN.
A lo largo de la evolución filogenética se habrían producido
mutaciones que derivaron en cambios en la expresión de
genesHox y Dlx que están involucrados en el patterning de
estructuras derivadas de CN. Entre Agnatos (peces sin mandíbula) y
Gnatostoms (desde peces con mandíbulas hasta mamíferos)
(véase Fig. SC 13-1-1) existen cambios regionales en la expresión
de la proteína señal y factor de crecimiento Fgf8 en la epidermis
del extremo cefálico. El Fgf8 es un regulador de la expresión de la
proteína factor de transcripción Dlx1 tanto en Agnatos como
Gnatostomados.
Entre Agnatos y Gnatostomados también existen diferencias
regionales en la expresión de genes Hox. En los Agnatos
(cefalocordados como los anfioxos y cordados primitivos como las
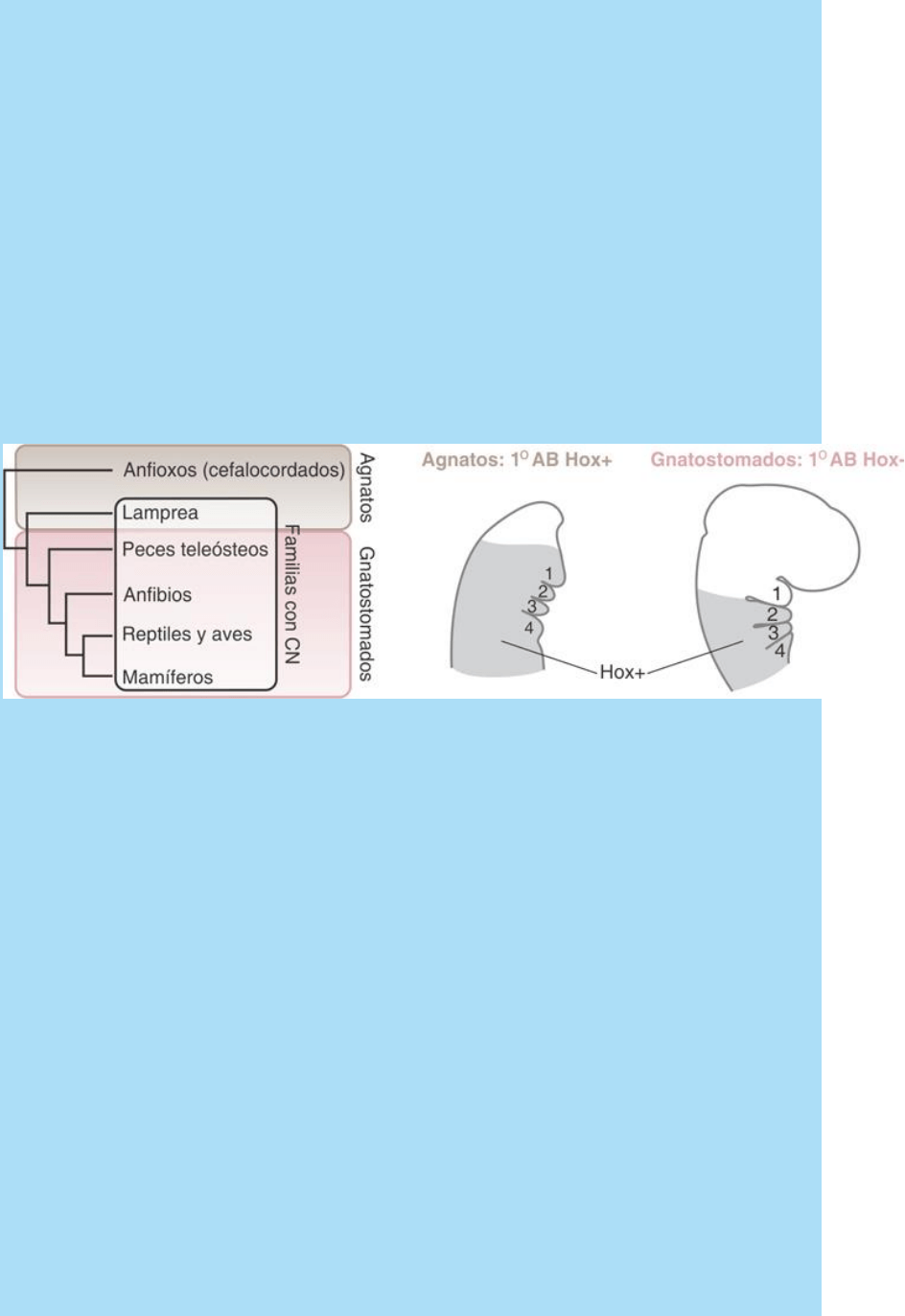
lampreas), la expresión de genes Hox se extiende cefálicamente
hasta el primer arco branquial. En la mayoría de los gnatostomados,
la expresión de genes Hox llega sólo hasta el segundo arco branquial.
En los mamíferos, la porción más cefálica de la CN craneal, desde la
región diencefálica hasta el segmento correspondiente a r2, es Hox
negativa. Ésta es la región de CN craneal encargada de formar todo
el aparato de la contención neurosensorial constituido por cráneo y
cara.
Así, además de los cambios regionales en la expresión del Fgf8 y de
factores de transcripción Dlx, la pérdida de la expresión de factores
de transcripción Hox en la CN craneal también sería causa del
cambio de destinos o de nuevas formas de evolución ontogenética
de células de la región cefálica de la CN craneal.
Fig. SC 13-1-1. Esquema que ilustra que algunos agnatos, como la
lamprea, poseen crestas neurales. El esquema ilustra también que
en la mayoría de los Agnatos la expresión de genes Hox se extiende
hasta el primer arco branquial (1.
er
AB) mientras que en los
Gnatostomados las células del 1.
er
AB son Hox. Modificado de Helms
y cols., 2005.
La CN preótica, por un lado, retuvo algunas características de
desarrollo de la CN posótica y por ese motivo tienen la capacidad de
originar células pigmentarias (melanocitos), neuronas sensoriales
primarias y células gliales de los ganglios de los nervios craneales.
Por otro lado, adquirió las capacidades de desarrollo del dermatomo
y esclerotomo de los somitas posóticos. Por ello, es capaz de originar
el mesénquima cefálico –rodea todo el prosencéfalo y mesencéfalo–
y la parte del mesénquima branquial que forma cara y cuello. Este
mesénquima originado en la cresta preótica se diferencia en los
tejidos conectivo, cartílago y huesos del cráneo y cara, de las
mandíbulas y huesos del oído medio. También origina el tejido
conectivo que forma el estroma de la adenohipófisis, tiroides,
paratiroides y timo. Origina, además, los odontoblastos de los
esbozos dentales.

SC 13.2. El síndrome de deleción 22q11.2 (DiGeorge).
Síndromes con alteraciones fenotípicas combinadas. V. Flores,
J. Halfón
Las células de la cresta neural de los primeros segmentos corporales
participan en la formación de los derivados de los arcos faríngeos
(esqueleto facial), de las bolsas faríngeas (timo, paratiroides) y del
tronco de salida del corazón.
Debido a ello, las fallas del desarrollo (déficits en la proliferación,
migración celular, exceso de muerte celular) de la cresta neural de
dicha región conducen a combinaciones bastante variadas de
alteraciones en todas esas estructuras. El síndrome de DiGeorge, por
ejemplo, incluye alteraciones faciales (“boca y filtrum pequeños”,
fisura palatina, implantación auricular baja), defectos troncoconales,
hipoplasia tímica, hipoplasia de las paratiroides y consiguiente
hipocalcemia.
En el hombre, algunos genes de desarrollo ubicados en la región 11.2
del brazo largo del cromosoma 22 participan en el desarrollo de los
derivados de la cresta neural craneal y sus deleciones se asocian a
varios síndromes. Por ello, dichos síndromes también reciben
genéricamente el nombre de síndrome de la deleción 22q11.2. Dado
que el síndrome de DiGeorge es paradigmático de este conjunto de
malformaciones, la región cromosómica mencionada ha sido
denominada DGCR (DiGeorge syndrome Chromosome Región). La
similitud que presentan estos síndromes y la gran variabilidad que
exhiben ha hecho plantear explicaciones alternativas. Por un lado se
ha planteado que las diferencias se deben a que no todas las
deleciones son idénticas en el sentido de que podrían ser de diferente
longitud involucrando a diferentes genes de dicha región
cromosómica. Por otro lado, se ha planteado también de que aun una
misma deleción podría generar, en los diferentes contextos
genómicos de diferentes individuos, variaciones del mismo cuadro
patogénico.
La variabilidad del síndrome ha sido también explicada considerando
el hecho de que las microdeleciones de la región 22q11.2 pueden
alterar la expresión de unos 30 a 40 genes. Uno de ellos, por ejemplo
el que codifica la proteína factor de transcripción Tbx1, está
involucrado en varias alteraciones físicas del síndrome (cardíacas,
del paladar hendido, etc.). Otro de los genes de la región, el que
codifica la enzima Catechol-O-methyltransferasa
(Comt), implicado en la síntesis delneurotransmisor dopamina, es

responsable de las alteraciones cognitivas y enfermedades mentales
del síndrome.
En la región DGCR se localizan varios genes que estarían
involucrados en la migración de las células de la cresta neural.
Laproteína factor de transcripción Tbx1 se expresa en los arcos y
bolsas faríngeos y en la vesícula ótica y, presuntamente, está
involucrado en algunas de las alteraciones debidas a las deleciones
22q11.
Se ha mostrado que la mayoría de las deleciones 22q incluyen el gen
codificante del factor Tbx1 y que las mutaciones de dicha proteína
producen alteraciones similares a las del síndrome de la deleción
22q11. El factor Tbx1 se expresa en el endodermo faríngeo y en el
mesénquima de los arcos branquiales pero no en la cresta neural
craneal. Se ha mostrado también que la deleción del gen Tbx1 en
ratones reproduce las alteraciones fenotípicas correspondientes al
síndrome de la deleción 22q. En ratones, el knockout de un alelo
codificante del factor de transcripción Tbx1 suele producir
malformaciones troncoconales y el knockout de los dos alelos
produce casi todos los componentes del síndrome de DiGeorge.
El gen del factor de transcripción Hes (Homologue of Enchancer
of Split), que se expresa transitoriamente en el tronco-cono y tejidos
de la cara en derivados de la cresta neural, también se halla en la
región DGCR.
El gen codificante de la proteína de adhesión celular DGCR2 y
otros genes que se ubican en dicha región también estarían
involucrados en el desarrollo de la cresta neural craneal y sus
alteraciones.
Las mutaciones en genes que no se hallan localizados en la región
cromosómica señalada también pueden alterar el desarrollo de las
células de la cresta neural craneal y producir alteraciones como las
que integran el síndrome de DiGeorge. Así, el knockout del gen
codificante del factor de transcripción Hoxa3 que participa en la
morfogénesis de los derivados de la región correspondiente al
3.
er
arco y bolsa faríngeos produce algunas alteraciones incluidas en
dicho síndrome. Agentes teratógenos como el ácido retinoico y el
alcohol etílico también producen algunas malformaciones similares
debido a que alteran el desarrollo de las células de la cresta neural
craneal.
Se ha mostrado también que en el endodermo faríngeo existen
dominios de expresión superpuestos de Tbx1 y Fgf8 y que la
deleción de Tbx1 ocasiona la pérdida de la expresión de Fgf8 en el
endodermo faríngeo. Esto sugiere que la proteína factor de
transcripción Tbx1 está involucrada en el inicio y el mantenimiento de
la expresión de la proteína señal Fgf8. La expresión de Fgf8 es
necesaria para el normal desarrollo craneofacial, pues la ausencia de
expresión de Fgf8 en el dominio de expresión de Tbx1, en el
endodermo faríngeo, produce anomalías cardíacas semejantes a las
que poseen los pacientes con síndrome de DiGeorge.
SC 13.3. Morfogénesis dental. El código homeótico
odontogenético y las proteínas señal asociadas. V. Flores, J.
Halfón
Los procesos morfogenéticos e histogenéticos, en general, dependen
para su concreción de interacciones entre los elementos tisulares
participantes. En general se trata de interacciones epitelio-
mesenquimáticas en las que el componente epitelial corresponde al
ectodermo o al endodermo y el mesénquima es el que subyace
inmediatamente en el epitelio ya que se trata de interacciones
paracrinas o yuxtacrinas.
La morfogénesis dental es un ejemplo de tales interacciones. Existen
trabajos que indican que, en este caso particular, alectodermo de la
región oral le corresponde tempranamente un papel
determinante (estimular la odontogénesis y determinar el tipo de
diente) aun antes de que existan signos morfológicos de formación
de esbozo. En esta etapa, el mesénquima cumple el papel de
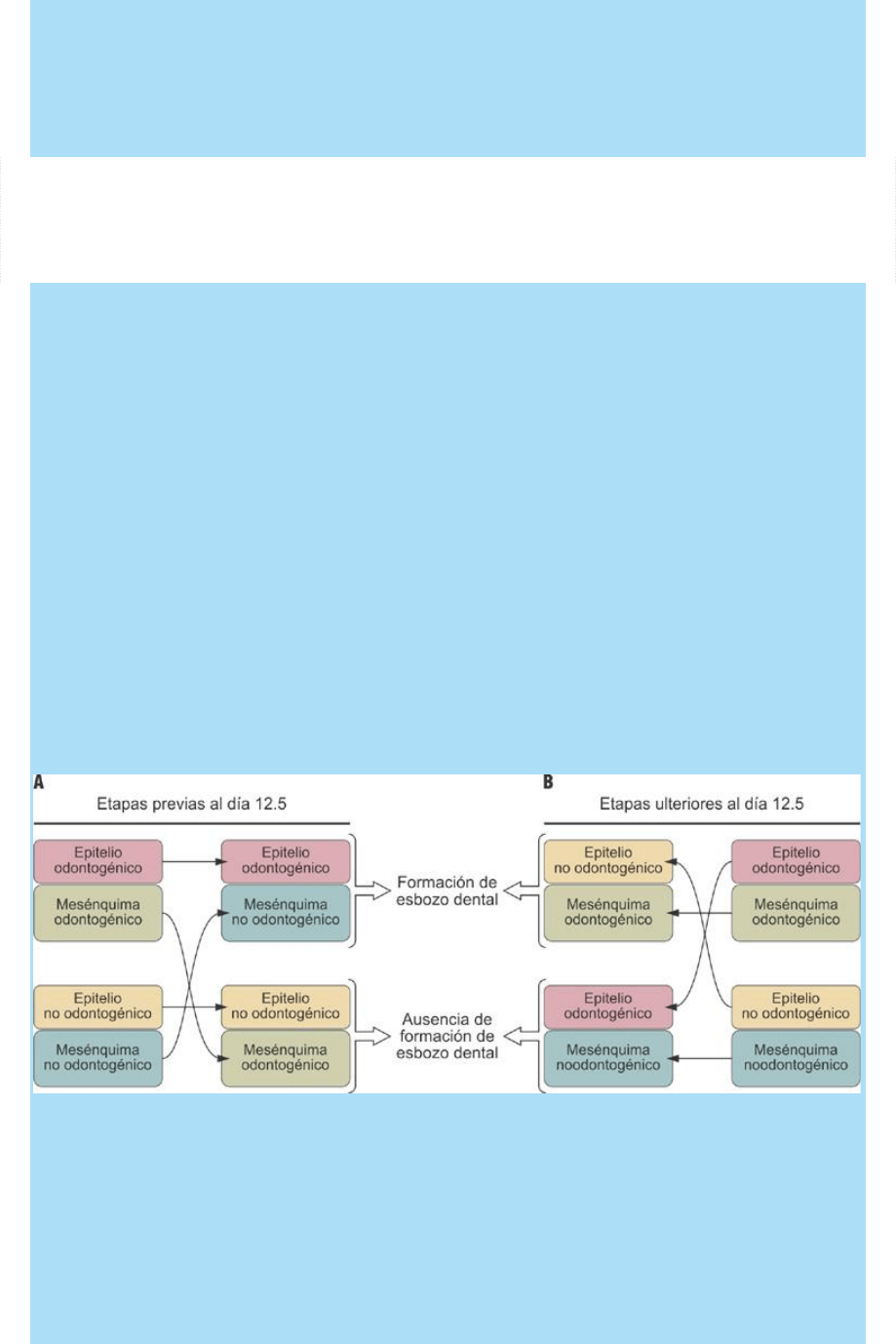
población celular competente. Luego los roles se invierten (Fig. SC
13.3.1).
Fig. SC 13-3-1. Modelo de odontogénesis mediado por interacciones
epitelio-mesenquimáticas en las que los papeles determinante y
competente se suceden temporalmente (Modelo: ratón). A. En una
primera etapa (etapas previas al día 12.5) el epitelio actúa en forma
determinante y puede inducir la formación de un esbozo de diente en
un mesénquima extraño (no dental). B. Más tarde (etapas ulteriores
al día 12.5), el mesénquima que ya ha sido estimulado a generar
diente es capaz de actuar sobre un epitelio extraño (no dental) e

inducirlo a formar juntos un esbozo dental. El experimento indica que,
en este modelo, la inversión de los papeles determinantes se produce
en el día 12.5.
Una vez formado el esbozo existe una cascada de interacciones
entre el epitelio y el mesénquima del primer arco branquial. Llegada
esta etapa existe una inversión en los papeles determinantes y
competentes
Se ha descrito un “código homeótico odontogénico” consistente en la
expresión de combinatorias de factores de transcripción de los tipos
Dlx, Barx, Msx y Alx. La expresión local de una combinación
específica de estos factores de transcripción, por parte del
mesénquima de la región formadora de dientes del primer arco
branquial, especifica qué tipo de diente se genera en cada región
formadora de dientes. Por ejemplo, se ha constatado que la
especificación de molares es establecida por la expresión de la
combinatoria de factores Dlx-1, Dlx-2 y Barx-1 y que para la
especificación de incisivos se requiere la expresión de la
combinatoria de factores Msx-1, Msx-2 y Alx-3.
La formación de dientes requiere la acción de otras proteínas que
colaboran con la expresión de los factores de transcripción
mencionados. Por ejemplo, antes de la formación de los dientes, la
proteína señal Bmp-4 se expresa en forma selectiva en la región
formadora de dientes. Primero se expresa en el ectodermo de la
región formadora de incisivos y poco después en el de la región
formadora de molares. Luego, la expresión de Bmp-4 se activa en el
mesénquima. Se postula que la expresión del factor de transcripción
Msx-1 influye, de alguna manera no conocida, sobre la expresión de
Bmp-4 específicamente debajo de las placodas o engrosamientos
ectodérmicos dentarios. Éste parece ser un fenómeno interactivo ya
que la proteína Bmp-4 también induce la expresión de Msx-1 en el
mesénquima. Una vez que la expresión de Bmp-4 y de Msx-1 se
traslada al mesénquima, la expresión de ambas proteínas se
independiza de señales provenientes del ectodermo. La importancia
de estas interacciones en la odontogénesis se pone de manifiesto por
el hecho de que la abolición o el déficit de la acción de Msx-1 produce
una detención del desarrollo dentario en el estado de esbozo.
Algo similar ocurre con la expresión del factor de transcripción Lef-1.
Éste, al principio también se expresa sólo en el ectodermo pero luego
la proteína Bmp-4 estimula su expresión en el mesénquima.
Finalmente, el factor Lef-1 se expresa en el nódulo del esmalte. Esta

proteína es otra de las tantas involucradas en la acción del
mesénquima durante la formación de la papila dentaria.
Otra proteína necesaria durante la odontogénesis es la proteína
señal Shh. Esta proteína se expresa en sitios o dominios restringidos
estimulando la proliferación localizada del ectodermo dental en zona
de formación de esbozos dentales. Su expresión altamente
localizada depende de la interacción con otra proteína señal Wnt-7b
y la activación de esta vía de señalización.
Durante la morfogénesis del diente la lámina dental genera un diente
con una morfología característica. Este proceso tiene varias etapas.
De ellas, la transición del estado de brote al estadio de caperuza y la
formación del nódulo del esmalte primario es crítica ya que éste se
convierte en un centro señalizador que integra la odontogénesis. El
nódulo del esmalte es un centro señalizador discreto (local),
transitorio y no proliferativo, formado por las células ectodérmicas
localizadas en el extremo del epitelio dental interno. Este nódulo
dirige la formación del esbozo en el estadio de caperuza por medio
de la expresión de varias proteínas señal entre las que se cuentan
Shh, Bmp-2, Bmp-4, Bmp-7, Fgf-4, Fgf-9 y Wnt. El nódulo del esmalte
progresivamente desaparece por apoptosis regulada por Bmp-4.
En dientes con más de una cúspide, luego de la desaparición del
nódulo del esmalte primario, en el estadio de caperuza tardío se
forman nódulos del esmalte secundarios dentro del epitelio dental
interno. Los nódulos secundarios regulan la formación del diente en
el estadio de campana, son no proliferativos, expresan Fgf-4 y son
eliminados por apoptosis a través de la acción de Bmp-4. Los nódulos
secundarios marcan los sitios de ubicación de las futuras cúspides.
Vale decir, establecen el patrón espacial de posición de cúspides
específico de especie y de tipo dental.
SC 13.4. La disostosis mandibulofacial o síndrome de Treacher
Collins (STC). Bases celulares y moleculares de su patogenia.
V. Flores, J. Halfón
Varios estudios histopatológicos de embriones con síndrome de
disostosis mandibulofacial, bilateral y simétrico (distinguibles de las
que presentan alteraciones asimétricas) o síndrome de Treacher
Collins (STC), sugieren un mecanismo patogénico que opera
tempranamente durante el desarrollo facial y que actúa
uniformemente sobre el mesénquima de los dos primeros arcos
branquiales.

En animales de experimentación (ratón) existen malformaciones
similares al STC tanto de causa ambiental como genética. La
vitamina A, administrada a ratas en dosis teratogénicas, produce una
fenocopia del STC. Algunos estudios histopatológicos de estos
embriones muestran focos de muerte celular en los dos primeros
arcos branquiales que producen un déficit en células de la cresta
neural y cambios de posición y deformaciones de las prominencias
faciales y auriculares. Estas alteraciones dan lugar a un esqueleto
facial simétrico, pero anormal, muy similar al del STC en el ser
humano. No se ha dilucidado cómo la vitamina A altera las células de
la cresta neural de los arcos mencionados.
La malformación facial de causa genética del ratón considerada
homóloga a la disostosis mandibulofacial se debe a una mutación del
gen Tcof1 que codifica la proteína Treacle. Los ratones heterocigotos
para esta mutación mueren perinatalmente con una severa
malformación craneofacial. En estos ratones, las células precursoras
de la cresta neural sufren muerte celular antes de abandonar el tubo
neural. Ello reduce significativamente la población de células
correspondientes al 1.er arco faríngeo.
En el ser humano la disostosis mandibulofacial se caracteriza por
hipoplasia bilateral de las estructuras faciales derivadas del 1.erº arco
faríngeo y se debería a mutaciones del gen Tcof1 que está localizado
entre las regiones 32 y 31 del brazo largo (q) del cromosoma 5.
Como en el ratón, la causa respondería a una alteración de la
proteína Treacle, una fosfoproteína, de localización nucleolar,
involucrada en la regulación de la síntesis de ARN ribosómico. La
pérdida de la función de la proteína reduciría la síntesis de ARNr
afectando más o menos selectivamente a ciertas poblaciones
celulares en desarrollo, entre ellas, afectando seriamente y
produciendo la muerte de las células de la cresta neural que
participan en el desarrollo craneofacial. No se conoce la patogenia
por medio de la cual la alteración en la proteína Treacle conduce a la
muerte de estas células y no afecta, o afecta levemente, a otras.
El STC en el ser humano presenta una gran variabilidad y debido a
ello se ha especulado que podrían ser varios los genes involucrados
como causa del STC. Una posible fuente de tal variabilidad podría
resultar del hecho de que el transcripto primario de Treacle,
normalmente, puede sufrir varios procesamientos alternativos
generando al menos tres diversas isoformas funcionales de la
proteína. Se ha postulado que cada una de ellas podría ser alterada

diferentemente por distintas mutaciones. Esta postulación se basa en
el hecho de que ciertos estudios genéticos en pacientes con STC han
identificado hasta la fecha más de 150 mutaciones del gen Tcfo1
consistentes en inserciones o deleciones de pequeños segmentos de
ADN.
SC 13.5. El patterning de la región craneofacial I. Proteínas
señal y factores de transcripción involucrados en la
especificación de la cresta neural craneal y sus derivados. J.
Halfón, V. Flores
El código Hox establece la identidad de segmentos del tubo neural y
de la cresta neural desde el segmento rombomérico 3 (r3) hasta el
extremo caudal de ambas estructuras. Los segmentos de la cresta
neural y del tubo neural correspondientes al mismo nivel segmentario
comparten el mismo código Hox (SC El código Hox participa en la
morfogénesis del aparato de la cérvico-céfalo-giria y órganos
cervicales; SC El patterning de la cresta neural craneal. Regiones
Hox(+) y Hox(-). Su relevancia filogenética y sus papeles de
desarrollo).
Dado que las células de la cresta neural craneal se organizan en
corrientes migratorias ordenadas, cuando migran desde su posición
dorsal inicial hacia las paredes laterales y ventromediales, transfieren
su identidad de segmento a los tejidos que ellas originan en las
regiones que invaden. Así, las células de la cresta neural
“transportan” su código Hox al mesénquima de los arcos branquiales.
Nótese que el proceso descrito no instala diferencias en la
información posicional a lo largo del eje dorso-ventral. Todas las
células derivadas de un cierto segmento de cresta neural poseen el
mismo código Hox a lo largo del territorio que invaden desde el dorso
al vientre.
La especificación de la información posicional a lo largo del eje dorso-
ventral de los tejidos derivados de la cresta neural craneal depende
de la expresión diferencial y espacialmente organizada, de
combinatorias de otros factores de transcripción, entre los cuales
desempeñan un papel central los factores de transcripción del
grupo Dlx (Distal less homebox).
La asignación de información de posición mediada por estos dos
sistemas de referencia no se produce simultáneamente en los tejidos
derivados de la cresta neural craneal. El código Hox queda
especificado en las células de la cresta neural antes de iniciar su
migración. La especificación de la información posicional a lo largo

del eje dorso-ventral, por medio de combinatorias de factores Dlx, se
especifica más tarde.
Así, todas las células de la cresta neural que integrarán un arco
branquial y derivan de un mismo segmento de cresta neural
comparten el mismo código Hox antes de iniciar su migración. Por el
contrario, la expresión diferencial de genes Dlx a lo largo del eje
dorso-ventral de la región que invaden se inicia recién durante la
migración. Esta expresión diferencial depende de señales
provenientes del epitelio circundante con el que van interactuando
durante la migración.
La identidad de segmento provista con la participación de los factores
de transcripción del código Hox establece diferencias entre arcos
branquiales sucesivos a lo largo del eje cf-cd. La expresión
diferencial de factores de transcripción Dlx establece, para cada
arco branquial, diferencias a lo largo del eje dorso-ventral. Esto
ocurre sin que los factores de transcripción Dlx interfieran con la
identidad de segmento provista por los factores de transcripción Hox.
Así, la expresión diferencial, espacialmente organizada, de
combinatorias de dos conjuntos de diferentes tipos de factores
de transcripciónprovee un sistema de referencia espacial que
semeja un sistema ortogonal en el que un código (Hox) establece
diferencias a lo largo del eje céfalo-caudal en tanto que el otro código
(Dlx) establece diferencias a lo largo del eje dorso-ventral del sistema
de referencia ortogonal.
Un ejemplo de establecimiento de diferencias a lo largo del eje dorso-
ventral en la región de la cresta neural craneal lo ofrecen ciertos
peces en los que el epitelio de los arcos branquiales sintetizan
la proteína señal endotelina-1 (Et-1) en forma de gradiente
ventrodorsal (valor máximo en la región ventral). Este gradiente de
endotelina-1 actúa sobre el mesénquima branquial derivado de las
crestas neurales y participa en la especificación de diferencias en el
modo de desarrollo de las estructuras esqueléticas a lo largo del eje
dorso-ventral. Diferentes rangos de concentración de endotelina-1
promueven diferentes modos de desarrollo en estructuras
cartilaginosas y articulares. En la región dorsal, la baja concentración
de Et-1 permite la expresión de la proteína factor de transcripción
Bapx1 que participa en la regulación de la expresión de proteínas
vinculadas al desarrollo de articulaciones. En la región ventral, la alta
concentración de Et-1 activa la expresión de la proteína factor de
transcripción Hand2, que reprime la expresión de Bapx1 y
promueve la formación de cartílago. Así, el gradiente de Et-1
establece la posición espacial de articulaciones y cartílagos.

La Et-1 también tiene un papel clave en el establecimiento de la
polaridad dorso-ventral en los 2 primeros arcos faríngeos en aves y
mamíferos a través de una cascada genética en la que están
involucradas las proteínas factores de transcripción Dlx6, dHand
y Msx1.
Otros ejemplos de polaridad y patterning en la región craneofacial los
ofrece la distribución de la proteína señal Fgf8. El Fgf8 se expresa
en el ectodermo oral antes de que se forme la cavidad bucal y antes
de que arribe el mesénquima de las crestas neurales y la proteína
señal Bmp4 delimite su dominio de expresión. La distribución de
ambas señales provee información de posición al mesénquima que
origina estructuras orales.
El Fgf8 se expresa también en el ectodermo y en las bolsas faríngeas
y opera como señal de supervivencia y estímulo para la expresión de
genes participantes en diferenciación de las células de la cresta
neural.
El Fgf8 instala una polaridad en el eje céfalo-caudal del 1.
er
arco
faríngeo. En el borde oral (cefálico) del 1.
er
arco en el que se forman,
la lámina dental se distingue del borde aboral (caudal) que forma el
esqueleto óseo en el que se implantan los dientes.
Por otro lado, el Fgf8, en altas concentraciones, estimula la expresión
de los genes codificantes de las proteínas factor de transcripción
Lhx6/7 en las células de la región dorsal; por el contrario, en bajas
concentraciones estimula la expresión de laproteína factor de
transcripción Goosecoid, en la región ventral. Este factor de
transcripción participa en la condrogénesis craneofacial.
SC 13.6. El patterning de la región craneofacial II. Factores de
transcripción y factores de crecimiento intervinientes. J.
Halfón, V. Flores
La cresta neural es una población celular con potencia evolutiva
amplia. Sus diversos modos de evolución dependen de las
interacciones que puedan realizar con otros tejidos durante el
desarrollo. La variabilidad en cuanto a los posibles papeles de
desarrollo es sobre todo llamativa en la región correspondiente a la
cresta neural craneal (SC El origen múltiple y la pluripotencialidad del
mesénquima cefálico. El mesodermo paraxil preótico y la cresta
neural craneal).
La cresta neural craneal posee dos regiones principales limitadas por
el segmento rombomérico 3 (r3). La región cefálica a r3 (región
diencefálica, mesencefálicas anterior y posterior y parte del
posencéfalo, hasta r3) no expresa factores de transcripción

Hox, es comúnmente denominada Hox(-) y su especificación es
independiente de los genes Hox. La región caudal a r3 sí está
subordinada al código de factores de transcripción Hox y es
denominada Hox(+).
La cresta neural craneal cefálica Hox(-) ha sido designada cresta
neural esqueletogénica facial ya que origina la mayor parte del
cartílago y huesos membranosos de la cara y mandíbula y región
frontal del cráneo. La extirpación completa de la cresta neural craneal
Hox(-) deriva en la ausencia del esqueleto facial indicando que esta
capacidad está restringida a la zona Hox(-) y que la cresta neural
Hox-positiva no posee capacidad esqueletogénica facial.
Por otro lado, también se ha mostrado experimentalmente que la
cresta neural craneal Hox(-) se comporta como una población
celular equipotente (potencia evolutiva equivalente). La extirpación
de la mayor parte de la cresta neural Hox(-) no conduce a fallas en el
desarrollo craneofacial, siempre que se deje alguna porción
remanente de ella. Esto indica que cualquier porción remanente de
la cresta neural craneal Hox(-) es capaz de generar los componentes
esqueléticos y conectivos que hubieran sido formados por la porción
extirpada.
La proteína factor de crecimiento Fgf-8 está involucrada en las
interacciones epitelio- mesenquimáticas que ocurren durante el
desarrollo de la región craneofacial. Por un lado la cresta neural
craneal Hox(-) estimula y mantiene la expresión de Fgf-8 por parte
del ectodermo de la región de la cresta neural anterior o
ANR (Anterior Neural Ridge) y, por otro lado, el propio desarrollo de
la cresta neural craneal Hox(-) es dependiente de Fgf-8.
La extirpación de la cresta neural Hox(-) reduce la expresión de Fgf8
en el ectodermo de la región cefálica. Pero, la extirpación de la cresta
neural craneal Hox(-) acompañada de la aplicación de Fgf8 exógeno,
en el territorio del 1.
er
arco branquial, permite que la población celular
del segmento de r3 regenere buena parte del esqueleto facial.
Por el contrario, algunos experimentos de sobreexpresión de genes
Hox en la región Hox(-) negativa hacen que dicha región pierda la
capacidad esqueletogénica facial.
Al parecer, el factor de crecimiento Fgf-8 estimula la expresión de
las proteínas factores de transcripción Ptx1 y Lhx6 que se
expresan específicamente en la región del 1.
er
arco faríngeo.
La porción de cresta neural craneal que forma el 2.º arco faríngeo y
que origina las estructuras óseas del oído medio y el hioides expresa
la proteína factor de transcripción Hoxa2. Este factor está
involucrado en el establecimiento de la identidad del 2.º arco. En

ausencia de expresión de esta proteína, las células del 2.º arco
modifican su desarrollo y originan derivados típicos del 1.
er
arco. Por
otro lado, la expresión ectópica de este factor de transcripción en la
región correspondiente al 1.
er
arco hace que estas células originen
derivados del 2.º arco. Como consecuencia de estos resultados se
ha propuesto que en la región mencionada existe un programa de
desarrollo que por omisión de Hoxa2 evoluciona en sentido del
1.
er
arco faríngeo pero que ante la expresión de Hoxa2 adquiere el
desarrollo correspondiente al 2.º arco.
El factor de transcripción Hoxa2 antagoniza la acción del Fgf8
reprimiendo la expresión de los factores de transcripción Ptx1 y
Lhx6 que contribuyen a establecer la identidad del 1.
er
arco. El factor
Hoxa2 también inhibe la expresión del factor de transcripción
Sox9 que participa en la diferenciación del cartílago. Por otro lado,
Hoxa2 también estimula la expresión de la proteína factor de
transcripción goosecoid, que es típica del 2.º arco. De esta
manera, la formación de los derivados del 2.º arco requeriría que
Hoxa2 inhiba el potencial esqueletogénico facial y module espacial y
temporalmente la proliferación y diferenciación de la cresta neural.
La proteína factor de transcripción Otx2 se expresa en las células
de la cresta neural craneal que forman el mesénquima de la
prominencia frontonasal y en las de la cresta neural mesencefálica
que forman el 1.
er
arco faríngeo. El mesénquima del 1.
er
arco tiene dos
componentes: su región ventral está integrada por células
provenientes de la cresta neural mencionada que expresa Otx2; la
porción dorsal de dicho arco es de origen rombomérico
(prosencefálico). En las mutaciones de Hoxa2, la transformación del
2.º arco en 1.
er
arco se limita a las estructuras dorsales. Ello indica
que en la región ventral prevalece la especificación asignada por la
expresión adicional de Otx2.
Los segmentos de la cresta neural que forman el 3.
er
arco expresan
genes Hox de los grupos 2 y 3. Este arco contribuye con menos
células a la formación del esqueleto cervical. La cresta neural troncal,
que expresa genes Hox más posteriores, no genera estructuras
esqueléticas.

Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.