
SC 12.1. Organización espacial de la determinación de linajes
celulares adenohipofisarios. V. Flores
La hipófisis está compuesta por varios tipos celulares que sintetizan
y secretan las distintas hormonas hipofisarias. Estos diferentes tipos
celulares se generan en un orden temporal y espacial bien definido a
partir de un esbozo epitelial aparentemente homogéneo, la bolsa
hipofisaria.
Existe evidencia experimental de que en tal ordenamiento temporal y
espacial están involucradas vías de señalización generadas a partir
de tejidos adyacentes que operan como centros señalizadores: a) el
infundíbulo del diencéfalo que inicialmente secreta la proteínas
señal Bmp4 y más tarde la proteína Fgf8 y b) el mesénquima
ventral yuxtahipofisario que secreta las señales Bmp2 y Bmp7.
Durante mucho tiempo prevaleció la idea de que cada tipo celular de
la hipófisis secreta exclusivamente una hormona y que deriva de un
linaje celular completamente independiente de los otros. Tal idea ha
cambiado sustancialmente. En la actualidad se sabe que existe una
regulación combinatoria de la determinación celular, que tal proceso
implica la expresión de diferentes combinatorias de factores de
transcripción para diferentes tipos celulares y que ello revela una
deriva de diferentes tipos celulares a partir de precursores comunes
de diversa jerarquía (SC El árbol genealógico de las células
endocrinas de la adenohipófisis). Tales factores de transcripción
tienen como blancos específicos a genes que codifican hormonas y
genes que codifican enzimas necesarias para las síntesis de
hormonas.
Se han descrito tres vías principales de citodiferenciación que se
ejecutan en forma espacialmente estructurada. Vale decir, las
diferentes vías tienen territorios de expresión definidos dentro del
esbozo de la adenohipófisis.
a) Las células que ocupan la región profunda de la fosa hipofisaria
cursan la vía de diferenciación de las células corticotropas
(productoras de ACTH y MSH) y en su determinación están
involucradas las proteínas genéricamente denominadas
comoCute (Corticotropin upstream transcription-binding
elements) entre los cuales se incluyen los factores transcripción
NeuroD1/Β2.
b) Las células que ocupan la región intermedia de la fosa hipofisaria
cursan preferentemente la vía de diferenciación de las células
somatotropas, somatomamotropas, lactotropas y tirotropas. Derivan
de una población celular precursora que expresa el factor de

transcripción Pit-1. De esta población celular, las que
adicionalmente expresan el receptor de estrógeno ERαsecretan
especialmente la hormona prolactina; las que adicionalmente
expresan el factor de transcripción embrionario tirotrofo (Tef)
secretan principalmente la hormona estimulante de la tiroides o
Tsh. En sentido estricto el factor Tef estimula la expresión de
la subunidad Tsh-β de la hormona Tsh.
c) Las células que ocupan la región superficial de la fosa hipofisaria
cursan la vía de diferenciación de las células gonadotropas
bihormonales y en su determinación está involucrado el factor de
transcripción esteroidogénico (Sf-1).
Esta organización espacial de la citodiferenciación se basa en un
proceso previo de expresión, también espacialmente organizada, de
determinaciones mediadas por la expresión combinatoria de factores
de transcripción (SC 12.2. La expresión temporal y espacialmente
organizada de combinatorias de factores de transcripción durante la
determinación de linajes celulares de la adenohipófisis).
Es interesante que estas combinatorias de factores de transcripción
y sus efectos sobre la secreción de hormonas son coherentes con
datos conocidos sobre el comportamiento secretorio de adenomas
hipofisarios y proveen de un marco apropiado para clasificarlos
desde el punto de vista patogénico.
SC 12.2. La expresión temporal y espacialmente organizada de
combinatorias de factores de transcripción durante la
determinación de linajes celulares de la adenohipófisis. V.
Flores
El proceso de determinación de tipos celulares hipofisarios se halla
espacialmente organizado por medio de dos centros organizadores
que instalan gradientes de señales, uno dorsal o profundo y uno
ventral o superficial. Entre ambos, de un modo dependiente de
concentración, instalan tres regiones principales en las que se
expresan diferentes combinatorias de factores de transcripción.
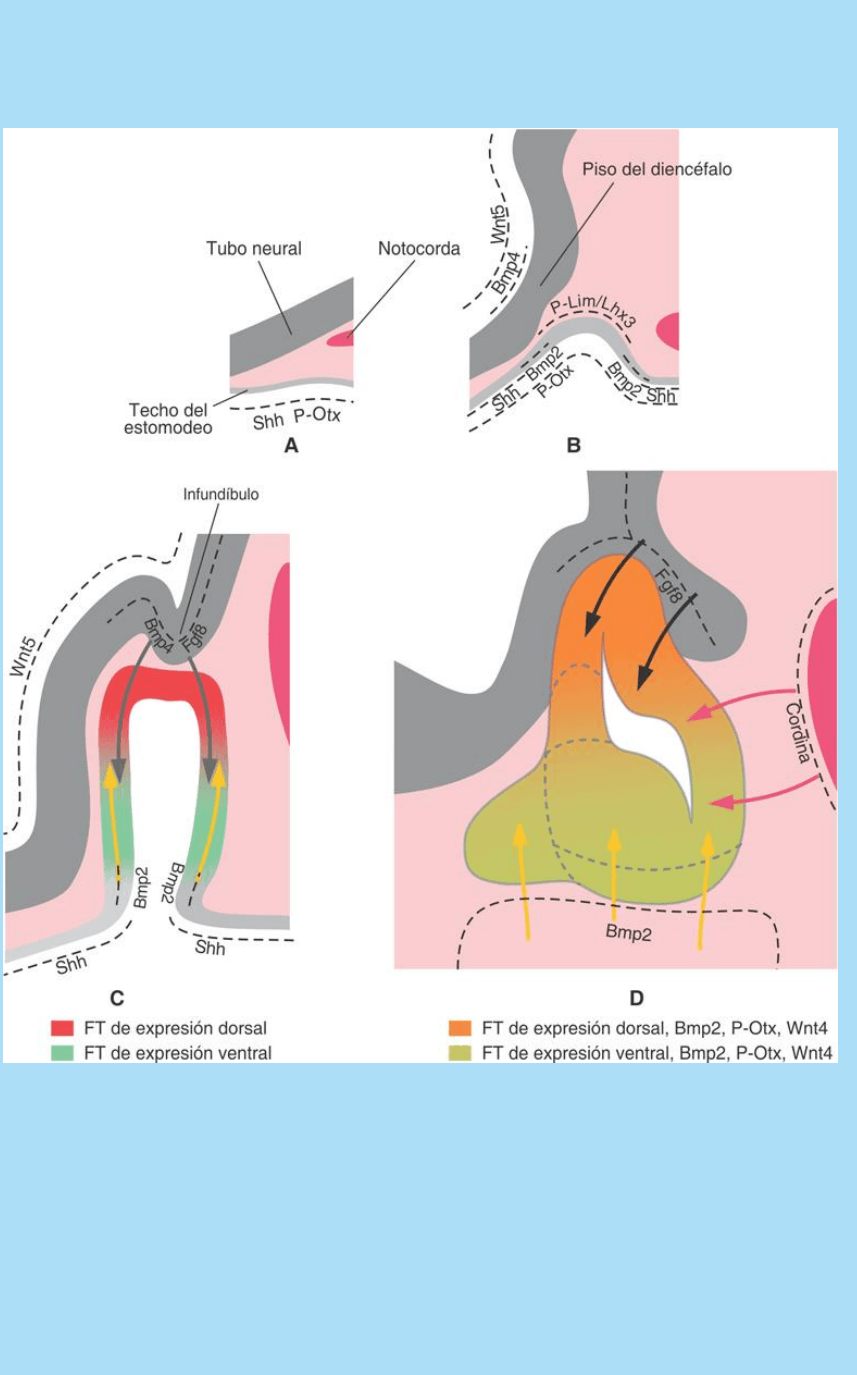
La figura SC 12-2-1 A-B1A-B ilustra un modelo sobre cómo se
estructura en el espacio el proceso de determinación de linajes
celulares hipofisarios (ratón). El ectodermo del techo del estomodeo
con competencia para formar placoda hipofisaria se caracteriza por
la expresión de la proteína señal Shh y el factor de transcripción
P-Otx (a). Las señales Wnt5a y Bmp4generadas en el neuroepitelio
del piso del diencéfalo (centro organizador dorsal)(esbozo de la
neurohipófisis) suspenden la expresión de Shh y activan la expresión
del factor de transcripción P-Lim/Lhx3 en la zona adyacente del
ectodermo (b). Se forma así la placoda hipofisaria (esbozo de la
adenohipófisis) y se inicia la invaginación de la fosa hipofisaria (bolsa
de Rathke). La frontera entre las zona Shh positiva y la zona Shh
negativa que delimita la entrada a la fosa hipofisaria se transforma en
centro organizador ventral y secreta la proteína señal Bmp2.
Fig. SC 12-2-1. Modelo sobre la instalación de un proceso
espacialmente organizado de determinación celular en la bolsa
hipofisaria. La existencia de gradientes cruzados de señales con
efectos contrapuestos, generadas a partir de centros de señalización
dorsales y ventrales posibilitan la aparición de subpoblaciones
celulares diferentemente determinadas en distintas regiones,
profunda, media y superficial, del la bolsa hipofisaria.
Más tarde (c), cuando se profundiza la bolsa hipofisaria y se forma el
infundíbulo, éste opera como centro señalizador de Fgf8 y el centro

organizador ventral incrementa su secreción de la proteína señal
Bmp2. Se generan así dos gradientes: un gradiente DV de Fgf8 y
uno VD de Bmp2.
Ambos gradientes generan una expresión diferencial de factores
transcripción “de expresión dorsal” y “de expresión ventral” que
instalan zonas con diferente identidad (Fig. SC 12-2-1 C y Fig. SC
12-2-2).
Se propone que la expresión espacialmente estructurada de las
combinatorias de factores de transcripción mostradas en lafigura SC
12-2-2, que ocurre durante este período del desarrollo, explica la
aparición de distintos tipos de células hipofisarias en distintas
regiones de la adenohipófisis (d).
En (d) se ilustra que, a continuación, el gradiente VD de Bmp2 es
reforzado por la secreción de dicha señal en el mesénquima ventral
a la vesícula hipofisaria y que, además, la acción de Bmp2 es
contrarrestada por la acción de señales caudales, como la proteína
señal cordina, que ahora es secretada por células del extremo
anterior del mesodermo cordal y por la señal Fgf8 cuya expresión se
desplaza hacia la zona caudal de la vesícula hipofisaria debido al
crecimiento del infundíbulo. Este hecho instala también diferencias a
lo largo del eje céfalo-caudal (anteroposterior) de la fosa hipofisaria
que se revelan por el modo como se distribuyen los diferentes tipos
celulares. Así:
En la región profunda y caudal se determinan células
melatonotropas.
En la región profunda y cefálica, células corticotropas.
En la región intermedia se forman células lactotropas y somatotropas.
En la región superficial y cefálica se determinan células tirotropas y
en la región superficial y caudal se determinan células gonadotropas.

Fig. SC 12-2-2. La figura muestra cómo las señales dorsales y
ventrales estimulan la expresión de diferentes factores de
transcripción y, dependiendo del rango de acción de dichos efectos
(flechas verticales ascendentes y descendentes), en distintas
regiones del epitelio de la fosa hipofisaria se expresan diferentes
combinatorias de factores de transcripción. Ello hace que dichas
regiones den origen a diferentes tipos celulares cuya distribución
espacial depende de la de los factores de transcripción que los
determinan.
SC 12.3. La morfogénesis hipofisaria y la determinación
progresiva de los tipos celulares de la adenohipófisis. V.
Flores, M. Rapacioli
El proceso de determinación progresiva de los diversos tipos
celulares de la adenohipófisis se relaciona estrechamente con los
cambios morfogenéticos tempranos. Dado que la citogénesis de la
glándula depende de interacciones con varios centros señalizadores
que circundan el esbozo, los cambios morfogenéticos que éste sufre
implican cambios de posición que hacen que diferentes regiones se
acerquen, se pongan en contacto estrecho y reciban señales de los
centros señalizadores que imprimen el patterning del esbozo.
El proceso global, morfogenético e histogenético, ha sido
categorizado como un proceso multi-paso con eventos definidos en
cada uno de ellos.
Fase 1. Consiste en la determinación de la placoda hipofisaria en
una zona restringida del ectodermo del techo del estomodeo. El
evento sobresaliente es la activación de la vía del Bmp4 en las
células del ectodermo estimulado por la secreción de dicha señal por
las células de la línea media del diencéfalo ventral. Esta acción lleva
a la abolición de la expresión de la señal Shh (típica del ectodermo)
por el inicio de la expresión de los factores de transcripción Rpx
(Hesx1), Pitx e Isl1. Así se determina la placoda hipofisaria y se inicia
su invaginación y la formación de la fosa hipofisaria (Fig. SC 12-3-
1A).
Fase 2. La formación de la fosa hipofisaria (Rathke) hace que el
centro de la placoda, que pasa a ser el fondo de la fosa, se
profundice, se acerque al diencéfalo y refuerce la acción de las
señales dorsales. Al mismo tiempo, la región periférica de la placoda
queda en la superficie y se aleja de las señales dorsales. En
simultáneo se agregan más señales al proceso. En el diencéfalo se
agrega la liberación de la señal factor de crecimiento fibroblástico
8 o Fgf8, mientras que las células del borde de la placoda, que
quedan bordeando el orificio de la fosa, expresan la proteína señal

Bmp2. Estos cambios de posición de dos centros señalizadores, uno
dorsal y otro ventral, llevan a la formación de dos gradientes cruzados
de las señales mencionadas. Las células que quedan ubicadas en
diferentes posiciones de dichos gradientes sufren diferentes
procesos de reprogramación genética y expresan diferentes factores
de transcripción. Típicamente, las células profundas expresan
elfactor de transcripción Pax6 y las superficiales expresan
el factor de transcripción Gata2 (>Fig. SC 12.3.1B). Otros factores
de transcripción acompañan a los mencionados y conforman los dos
dominios superficial y profundo. Cada uno de estos dominios
generarán células progenitoras que originan diferentes conjuntos de
células endocrinas y que secretan diferentes categorías de
hormonas.
Fase 3. De especificación de precursores de células endocrinas.
Durante esta fase se especifican las tres zonas citogenéticas
principales de la adenohipófisis. A los centros señalizadores
superficial (Bmp2) y profundo (Fgf8) se agrega, en la región caudal
de la fosa, la secreción de la proteína señal cordina a partir del
extremo anterior del mesodermo axil cordal (Fig. SC 12-3-1 C). Se
definen así tres regiones delineadas por tres combinatorias diferentes
de factores de transcripción indicadas en lafigura Sc 12-3-1 C. La
zona profunda o adenohipófisis dorsal, caracterizada por la expresión
de Pax6 y otros factores, se halla poblada por precursores Pomc; la
zona superficial o hipófisis ventral, caracterizada por la expresión de
Gata2, generaprecursores α-Gsu. Entre ambas queda una zona
intermedia, caracterizada por la expresión del factor de
transcripción Pit1que genera otros precursores, pero relacionados
con los de la zona superficial.
Fase 4. Durante esta fase a) disminuye significativamente la
actividad proliferativa de las poblaciones de células precursoras
yb) se inicia la expresión génica diferencial, en cada uno de los
grupos precursores, de modo que a partir de cada uno de ellos se
determinan cada uno de los tipos celulares correspondientes a las
ramas terminales del árbol genealógico. Losprecursores Pomc
originan a las células corticotropas y melanotropas. El
grupo precursor superficial α-Gsu da origen a las células
gonadotropas y tirotropas. Las células del grupo intermedio, que
algunos clasifican también como derivados tardíos del grupo α-Gsu,
dan origen a las células somatotropas y lactotropas.
Durante esta fase se definen también las regiones topográficas de la
glándula y la distribución definitiva de los diversos tipos celulares
(Fig. SC 12-3-1 D).
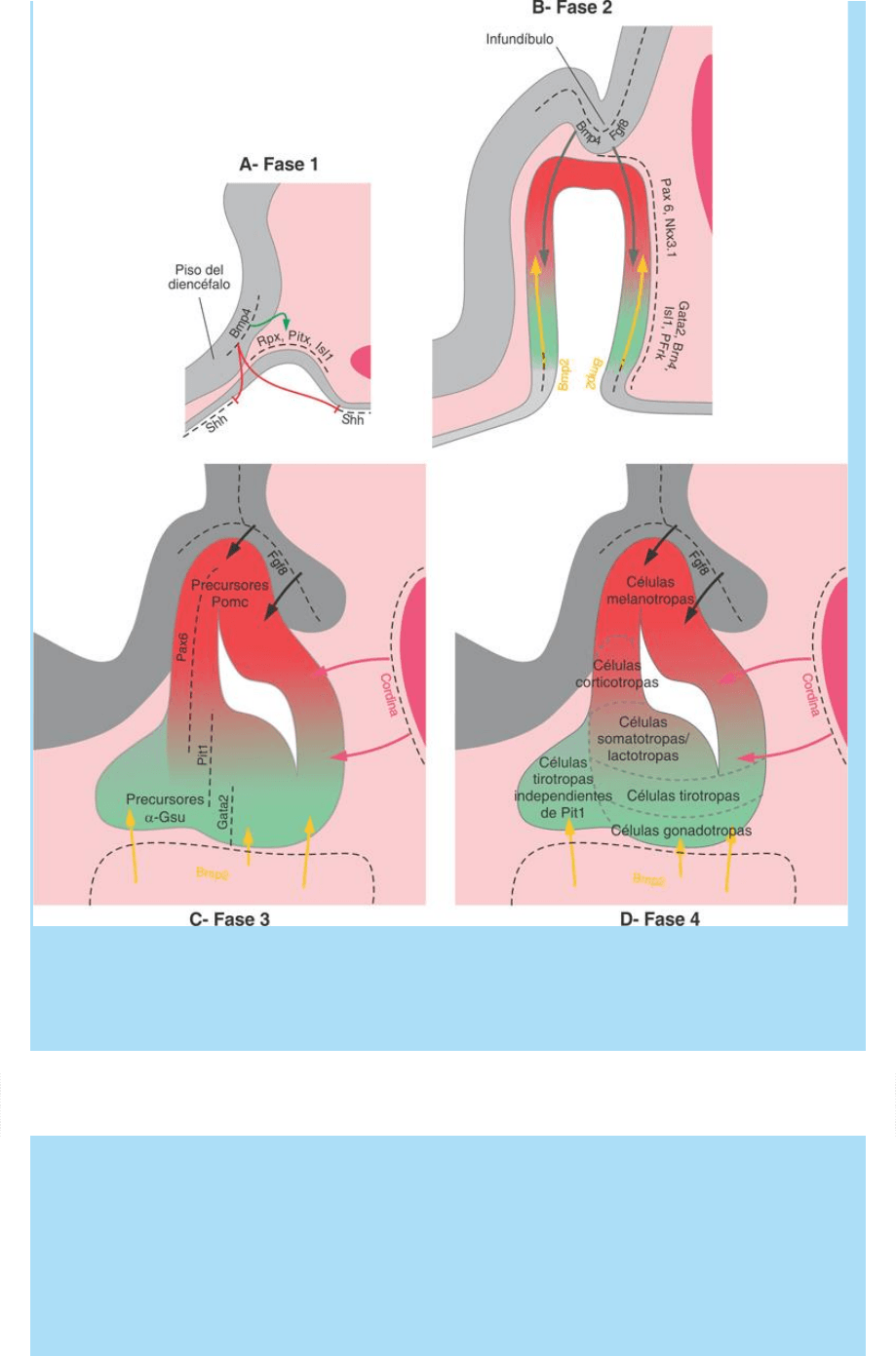
Fig. SC 12-3-1. Representación esquemática de la organización
espacial del proceso de determinación progresiva de los tipos
celulares de la adenohipófisis. Se ilustran fases sucesivas del
proceso morfogenético e histogenético. Descripción en el texto.
SC 12.4. Bases moleculares y celulares de la patogenia del
síndrome de Kallman. V. Flores
Desde fines del siglo xviii se conoce un síndrome clínico que incluye
hipogonadismo (desarrollo deficitario de gónadas y órganos
genitales), ausencia de nervios olfatorios, anosmia (falta de olfato),
ocasionalmente, con aplasia renal (falta de desarrollo del riñón) y
algunos otros síntomas (Krafft-Ebing, 1886). Este síndrome es, en la
actualidad, denominado síndrome de Kallman. La patogenia del
síndrome, integrado por anomalías fenotípicas tan disímiles y,

aparentemente, inconexas se explica teniendo en cuenta que a lo
largo de la evolución biológica el sentido del olfato y la reproducción
evolucionaron en forma asociada. El olfato desempeña un papel
importante en la madurez de la conducta sexual de la mayor parte de
las especies.
Recién a fines del siglo pasado, a partir de estudios realizados en
ratón y mono, e incluso en el hombre, se empezó a dilucidar, en parte,
la patogenia del síndrome de Kallman. Desde el punto de vista tisular
u orgánico, el síndrome tiene como causa primaria una falla en el
desarrollo de la placoda olfatoria, hecho que ocurre durante el
período somítico.
Normalmente, la placoda olfatoria origina neuronas sensoriales
primarias sensibles a los olores (neuronas olfatorias). Éstas residen
en el propio epitelio olfatorio de la mucosa nasal derivado de la
placoda y emiten sus axones, que integran el nervio olfatorio. Éste se
halla integrado por fascículos que atraviesan la lámina cribosa del
etmoides y llegan al bulbo olfatorio (rinencéfalo). Allí, los axones de
las neuronas sensoriales primarias establecen sinapsis
con neuronas sensoriales secundarias. Las neuronas
secundarias, a su vez, envían sus axones, a través de los tractos
olfatorios a las estructuras corticales del rinencéfalo (Fig. 1). Un dato
importante en la génesis de este cuadro compuesto de anosmia a
hipogonadismo deriva del hecho de que el desarrollo y la sobrevida
de las neuronas olfatorias secundarias del bulbo olfatorio depende de
los estímulos nerviosos y señales provenientes de las neuronas
olfatorias primarias.
En la mayor parte de los vertebrados, la placoda olfatoria posee una
región definida que origina un órgano quimiorreceptor
denominado órgano vomeronasal. Éste cumple una función central
en la conducta reproductiva de la mayor parte de los mamíferos ya
que detecta las feromonas que permiten sincronizar la conducta
reproductiva y la realización del cortejo que culmina en la cópula y
ulterior reproducción. El neuroepitelio del órgano vomeronasal
también genera células precursoras neuronales que abandonan el
neuroepitelio receptor olfatorio y, siguiendo el trayecto de los axones
de las neuronas sensoriales secundarias del bulbo olfatorio, llegan
hasta la región medial del telencéfalo. Una vez allí, colonizan el
hipotálamo y se ubican, preferentemente, en el área preóptica del
hipotálamo anterior. Al diferenciarse, estas neuronas sintetizan la
hormona peptídica hormona liberadora de goadotrofinas (GnRH);
a través de sus axones que se dirigen hacia el tallo hipofisario, la
GnRH es liberada hacia los vasos del sistema porta hipofisario y llega
a la adenohipófisis. La GnRH tiene como blanco (diana) a las células
gonadotropas de la adenohipófisis en las que estimula la liberación
de gonadotrofinas (hormona foliculoestimulante [FSH] y hormona
luteinizante [Lh]). Estas hormonas son esenciales para el desarrollo
gonadal y la producción de las hormonas testiculares y ováricas
necesarias para la madurez sexual que acontece en la pubertad. En
ausencia de las hormonas ováricas y testiculares, los órganos
sexuales secundarios no se desarrollan.
En la especie humana el órgano vomeronasal se desarrolla hasta la
20ª SD, aproximadamente, y luego involuciona como tal. Sin
embargo, antes de ello participa del proceso arriba descrito.
De esta forma se explica cómo se asocian el hipogonadismo y la
anosmia que son los datos cardinales del síndrome de Kallman: la
ausencia de placoda olfatoria produce anosmia y suspende la cadena
de eventos descrita en el párrafo anterior que culmina la inmadurez
sexual.

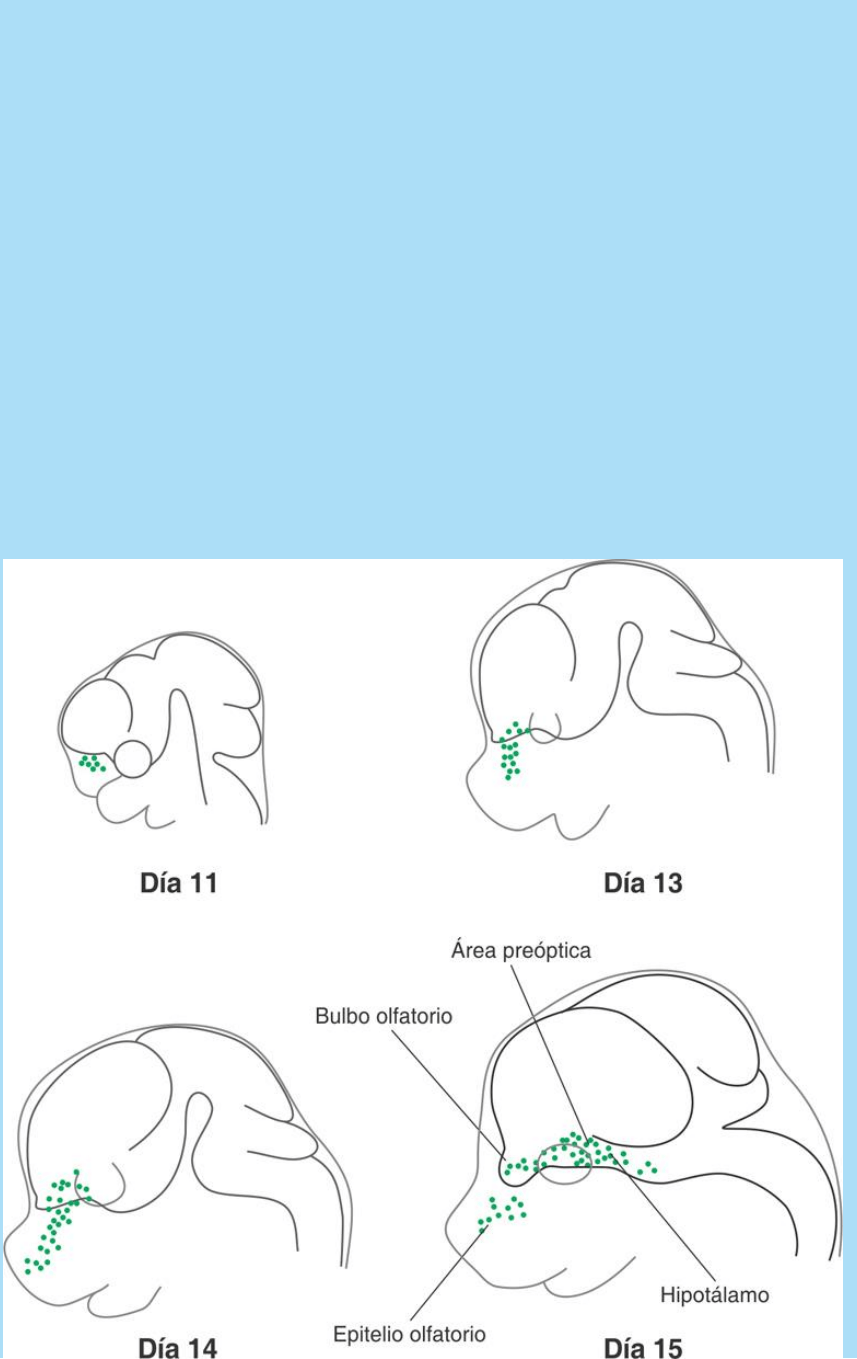
Fig. SC 12-4-1. La figura ilustra esquemáticamente la expresión de la
proteína anosmina-1 revelada en estudios inmunocitoquímicos con
anticuerpos monoclonales antianosmina-1 en embriones de ratón. En
el día 11 se observa la expresión en la matriz extracelular en la región
de formación del bulbo olfatorio. En esta región del rinencéfalo se
forman las neuronas sensoriales secundarias que proyectan al
centro. En días sucesivos, la distribución de la expresión de la
anosmina sigue el trayecto de migración de los axones de las
neuronas sensoriales secundarias y el de las células que desde la
placoda olfatoria migran hasta el hipotálamo.
El síndrome de Kallman se debe a una mutacíón que afecta a la
proteína anosmina-1 codificada por el gen Kal-1. La anosmina-1 es
una glucoproteína con organización modular. Algunos estudios
inmunocitoquímicos con anticuerpos antianosmina-1 han permitido
revelar su distribución en embriones humanos desde la 4ª a la 10ª
SD. Desde la 5ª AD se expresa, como componente de la matriz
extracelular, a lo largo del trayecto de migración de las células que
van desde el órgano vomeronasal al hipotálamo anterior (área
preótica). Como componente de la matriz extracelular, la anosmina-
1 participa en procesos de adhesión intercelular, de adhesión célula-
matriz extracelular, adhesión axón-axón y axón-matriz extracelular.
De ahí su importancia en la migración celular desde el órgano
vomeronasal hasta el hipotálamo.
La anosmina cumple funciones de desarrollo más amplias que las
que el propio síndrome de Kallman revela. Así, por ejemplo, durante
el desarrollo de las crestas neurales, exhibe un patrón de expresión
temporoespacial típico. La anosmina-1 secretada a la matriz
extracelular, por un lado, exacerba la actividad de la proteína señal
Fgf8 promoviendo su unión al receptor de Fgf tipo 1 y la formación
del complejo Fgf8-FgfR1 y, por otro, inhibe la actividad de las
proteínas señal Bmp5 y Wnt3A. Regulando estas actividades, la
anosmina-1 participa en procesos de transiciones reversibles
epitelio-mesenquimática y mesenquimático-epitelial durante la
formación de la cresta neural y la evolución ulterior de sus células.
La anosmina-1 también es expresada como proteína de superficie de
algunos órganos epiteliales en desarrollo como, por ejemplo, el brote
ureteral. Aquí también parece cumplir algún papel de desarrollo ya
que un tercio de los mutantes que padecen el síndrome de Kallman
padecen también aplasia renal.
SC 12.5. Las etapas del desarrollo de la corteza suprarrenal.
Cronología de los cambios histogenéticos. V. Flores

La glándula suprarrenal adulta representa, desde el punto de vista
estructural y funcional, un ejemplo de integración neuroendocrina.
Posee dos regiones básicas: a) la médula, que forma parte del
sistema nervioso autonómo simpático, representa un ganglio
simpático modificado por el entorno esteroidogénico y secreta
catecolaminas (adrenalina y noradrenalina); b) la corteza es una
típica glándula endocrina con tres regiones funcionalmente distintas
que integran una red de síntesis de hormonas esteroideas
(mineralocorticoides, glucocorticoides y hormonas sexuales). Todas
estas hormonas medulares y corticales son esenciales para la vida y,
pese a sus distintas funciones, actúan de forma integrada.
La corteza suprarrenal terminalmente diferenciada posee tres zonas:
una externa o glomerular (secreta aldosterona), una media o
fasciculada (secreta cortisol) y una interna o reticulada (secreta
andrógenos). La corteza suprarrenal fetal funciona intensamente
durante el desarrollo embrionario y debido a ello sufre una hiperplasia
e hipertrofia transitoria con respecto a la corteza definitiva. Su
estructura, sin embargo, es más simple que la de la corteza definitiva.
Su desarrollo se inicia con la formación del mesodermo
intermedio y la deslaminación del mesodermo lateral en una hoja
esplácnica y una somática. Las dos primeras son la principal fuente
de células que forman el esbozo adrenocortical. La figura SC 12-5-
1 ilustra gráficamente la cronología de los eventos histogenéticos
durante el desarrollo de la glándula suprarrenal.
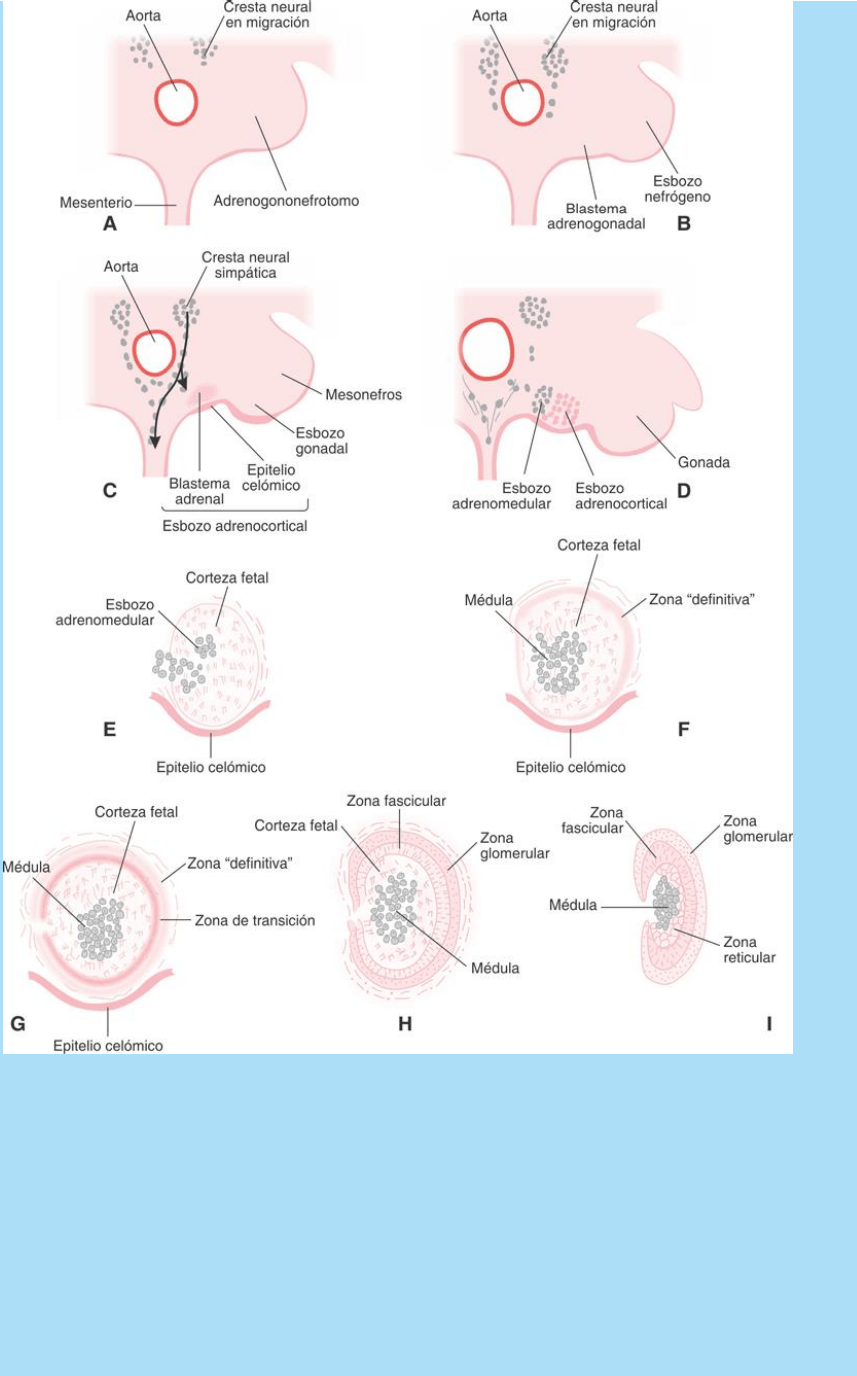
Fig. SC 12-5-1. Representación esquemática de las etapas
histogenéticas de la glándula suprarrenal humana. Algunas células
de la suprarrenal tienen un origen común con el riñón y la gónada, el
mesodermo intermedio o adrenogononefrotomo. A continuación se
segregan de los otros componentes y se asocian al epitelio celómico
con el cual constituyen un esbozo adrenocortical. Ulteriormente se
incorporan las células de la cresta neural troncal que forman el
esbozo del parénquima adrenomedular. El componente epitelial del
esbozo adrenocortical origina la corteza fetal y la zona definitiva.
Desde este momento hasta la adrenarca, que ocurre recién a los 6

años de vida posnatal, la glándula sufre una sucesión ordenada de
eventos histogenéticos. Entre estos se incluye la atrofia de la corteza
fetal y el desarrollo y diferenciación de las tres capas de la corteza
definitiva. Descripción en el texto.
AT.: en fig.1 C cambiar Blastema adrenal => Blastema suprarrenal
Las células que originan el blastema de la suprarrenal inicialmente
forman parte del mesodermo intermedio que constituye
un adrenogononefrotomo (Fig. SC 12-5-1 A). Estas células son
identificadas, ya durante el período somítico, debido a que expresan
el factor de transcripción esteroidogénico 1 o Sf1. El mesénquima
del mesodermo intermedio rápidamente se escinde en un esbozo
nefrógeno y un esbozo o blastema adrenogonadal (Fig. SC 12-5-
1 B). Éste luego se escinde en unesbozo gonadal y un esbozo
adrenocortical (Fig. SC 12-5-1 C). Este esbozo tiene un
componente epitelial superficial y un blastema subyacente. Hacia la
8ª SD, las células del epitelio celómico sufren transición epitelio-
mesenquimática y empiezan a introducirse en el blastema
suprarrenal (Fig. SC 12-5-1 D). En la 9ª SD, la zona central del
blastema es invadido por células de la cresta neural troncal
constituyéndose así el esbozo adrenomedular (Fig. Sc 12-5-1 D-E).
Las células del epitelio celómico del esbozo adrenocortical que
invadieron el blastema se organizan entonces en dos capas
alrededor del esbozo adrenomedular: una capa fetal o profunda
(zona fetal) y una capa superficial o “definitiva” (precursora de las
capas definitivas) que se diferencia más tarde (Fig. SC 12-5-1 F).
Constituidos los esbozos adrenomedular y adrenocortical, todo el
complejo es rodeado o encapsulado por tejido mesenquimático más
compacto o cápsula.
La zona fetal prolifera activamente y alcanza un tamaño
proporcionalmente mayor que el de etapas ulteriores. La corteza
aumenta en volumen hasta el 3.
er
trimestre de la gestación.
Durante el 3.
er
trimestre se forma una zona de transición entre las
capas o zonas fetal y “definitiva” (Fig. SC 12-5-1 G). La corteza
suprarrenal empieza a producir cortisol desde la 24-26.ª SD. En el
momento del nacimiento aún posee un tamaño exagerado en
relación con el de la corteza suprarrenal adulta y los otros órganos
(pesa el doble que la corteza suprarrenal adulta).
Luego del nacimiento, la zona fetal adrenocortical involuciona
rápidamente hasta desaparecer alrededor del 6.º mes de vida
posnatal. Simultáneamente se van desarrollando, a partir de la zona
“definitiva”, las capas glomerular (secretante
demineralocorticoides) y fascicular (secretante de
glucocorticoides) de la corteza definitiva. La zona más profunda de la

corteza definitiva, la capa reticular, no empieza a desarrollarse hasta
los 6 años (Fig. SC 12-5-1 H-I). En ese momento se inicia la síntesis
de andrógenos de origen adrenal. Dicho evento ha sido denominado
“adrenarca”.
SC 12.6. La función de la corteza suprarrenal fetal y la
diferenciación posnatal de la corteza definitiva. V. Flores
La aparición de las distintas funciones esteroidogénicas de la corteza
suprarrenal sigue al desarrollo y maduración funcional de sus
diversas capas.
La zona fetal de la corteza despliega una activa síntesis de esteroides
desde la 7.ª SD en adelante. La zona “definitiva”, que es una
población celular en desarrollo, pero en latencia hasta luego del
nacimiento, no produce esteroides hasta cerca del momento del
nacimiento. La zona de transición empieza a sintetizar cortisol recién
hacia el final del desarrollo fetal.
Sólo posnatalmente se originan las tres capas de la corteza definitiva.
Hay divergencias respecto de la génesis de la regionalización y de
los tipos celulares que integran el parénquima de las distintas zonas.
Ello se debe a que existen estudios realizados en diferentes especies
que no siempre coinciden.
Algunos investigadores proponen la existencia de oleadas de células
diferentes a partir del epitelio celómico. Otros proponen la existencia
de un patterning o regionalización previo a la formación de los
diferentes tipos celulares. Según esta visión, existirían células
troncales pluripotenciales en la región subcapsular y, dependiendo
del lugar donde queden ubicadas sus descendientes, se
diferenciarán en células de las distintas capas. Finalmente, otros
postulan la existencia de subpoblaciones de células troncales
progenitoras intermedias específicas para cada capa y que sus
descendientes migrarían centrípetamente y se ubicarían en zonas
definitivas para tipo celular.
La corteza suprarrenal fetal es un centro productor de andrógenos.
Las enzimas esteroidogénicas se hallan en cantidades significativas
desde la 7.ª SD. Desde entonces se detecta una síntesis de cortisol
que ya está sujeta a control por medio de la ACTH hipofisaria. Existe
una fase transitoria de alta producción de cortisol, que se extiende
desde la 8.ª a la 12.ª SD. Esta fase de alta secreción se debe a la
expresión transitoria de la enzima 3β-hidroxiesteroide
deshidrogenasa tipo 2 (3βHSD2)durante dicho período.

Esta ventana temporal es crítica para la diferenciación de los esbozos
de los órganos sexuales y se ha postulado que la alta actividad de la
enzima posee un efecto protector que evita la potencial virilización de
los órganos genitales de los fetos femeninos. El déficit en la actividad
funcional de esta enzima produce virilización. En condiciones
normales, durante esta ventana temporal sólo el feto masculino
produce andrógenos testiculares en cantidades suficientes para
producir virilización. Luego de la 12.ª SD en la corteza fetal disminuye
la enzima 3βHSD2 y las actividades enzimáticas favorecen la síntesis
de andrógenos produciendo dehidroepiandrosterona (DHEA) y
sulfato de dehidroepiandrosterona (S-DHEA) en abundancia.
Luego del nacimiento, la zona fetal involuciona y desaparece
alrededor de los 6 años. Simultáneamente, la zona definitiva junto
con la transicional se desarrollan y forman las capas glomerular y
fasciculada. Éstas completan su diferenciación terminal hacia los 3
años de edad.
La producción posnatal de esteroides por la zona glomerular
(mineralocorticoides) y por la fasciculada (glucocorticoides) no sufre
cambios bruscos con la edad. Sin embargo, la producción de
andrógenos por la reticular posee un patrón temporal típico.
La zona reticulada recién empieza a formarse alrededor de los 4
años. Pero la producción significativa de andrógenos de origen
suprarrenal, denominada “adrenarca”, sólo se inicia a los 6-8 años de
edad. La zona reticulada tiene un largo desarrollo posnatal y su
diferenciación terminal se logra recién alrededor de los 15 años.
Desde los 30 años se produce una declinación en la secreción de
andrógenos suprarrenales, denominada “adrenopausia”, que se
acentúa con la edad.

Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.