
SC 1.1. LA MADURACIÓN EPIDIDIMARIA. BASES
MOLECULARES Y CONSECUENCIAS. V. Flores
Los espermatozoides recién espermiados en los túbulos seminíferos,
aun cuando están diferenciados desde el punto de vista
ultraestructural, no poseen movilidad ni capacidad fecundante. Los
espermatozoides extraídos de las vías espermáticas, luego de su
paso por el epidídimo, sí poseen capacidad móvil y fecundante en
tanto interactúen con moléculas del líquido tubárico. Estudios
histoquímicos e inmunoquímicos muestran que en el epidídimo se
modifica la organización química de superficie de los
espermatozoides debido a que se le incorporan varias proteínas con
diversas funciones. Por un lado le confieren capacidad de interactuar
con moléculas del entorno del ovocito II, de sus cubiertas (corona
radiata [radiante] y membrana pelúcida) y de la propia membrana
plasmática del ovocito II. La posibilidad de realizar con éxito esta
sucesión de interacciones confiere a los espermatozoides capacidad
fecundante. Por ello, los cambios sufridos en el epidídimo se
denominan genéricamente maduración epididimaria. Por otro lado,
varias de las proteínas que se incorporan en el epidídimo mantienen
a los espermatozoides estabilizados y en latencia. Estas proteínas
son clásicamente denominadas factores descapacitantes, debido a
que mantienen a los espermatozoides en un estado no apto para la
fecundación o “descapacitado”. Dado que, en general se trata de
proteínas con capacidad antigénica, también suelen ser designados
genéricamente, desde otra perspectiva, como antígenos seminales.
El cuadro SC 1-1-1 incluye algunos de los cambios que clásicamente
se consideran involucrados en la maduración epididimaria.
Los factores descapacitantes del líquido seminal son removidos de la
superficie de los espermatozoides, en el tracto genital femenino,
debido a interacciones con componentes de éste. Los
espermatozoides entonces se capacitan y adquieren máxima
capacidad fecundante (SC 1-4 La capacitación del espermatozoide y
la reacción acrosómica). Dado que la maduración epididimaria
posibilita la capacitación espermática, a la que siguen la reacción
acrosómica y la hiperactivación de los espermatozoides, ha sido
descrita como la adquisición de una batería de proteínas de
superficie que programan al espermatozoide para las futuras
interacciones con elementos del tracto genital femenino. Estas
moléculas, a continuación, son estabilizadas por factores
descapacitantes (Fig. SC 1-1-1). Una vez en la ampolla (sitio de
encuentro de las gametas), en estado periovulatorio, los
espermatozoides pierden sus factores descapacitantes e inician las
interacciones que concluyen con la fecundación. El tracto genital
femenino, especialmente el istmo tubárico, también contribuye a
mantener a los espermatozoides descapacitados hasta el momento
de la ovulación (SC 1-2 El istmo de la trompa como reservorio de
espermatozoides “descapacitados”. La prevención o el retardo de la
capacitación). La capacidad fecundante adquirida con la
capacitación, sin embargo, es transitoria y se pierde en pocas horas.
Este fenómeno suele denominarse envejecimiento del
espermatozoide.
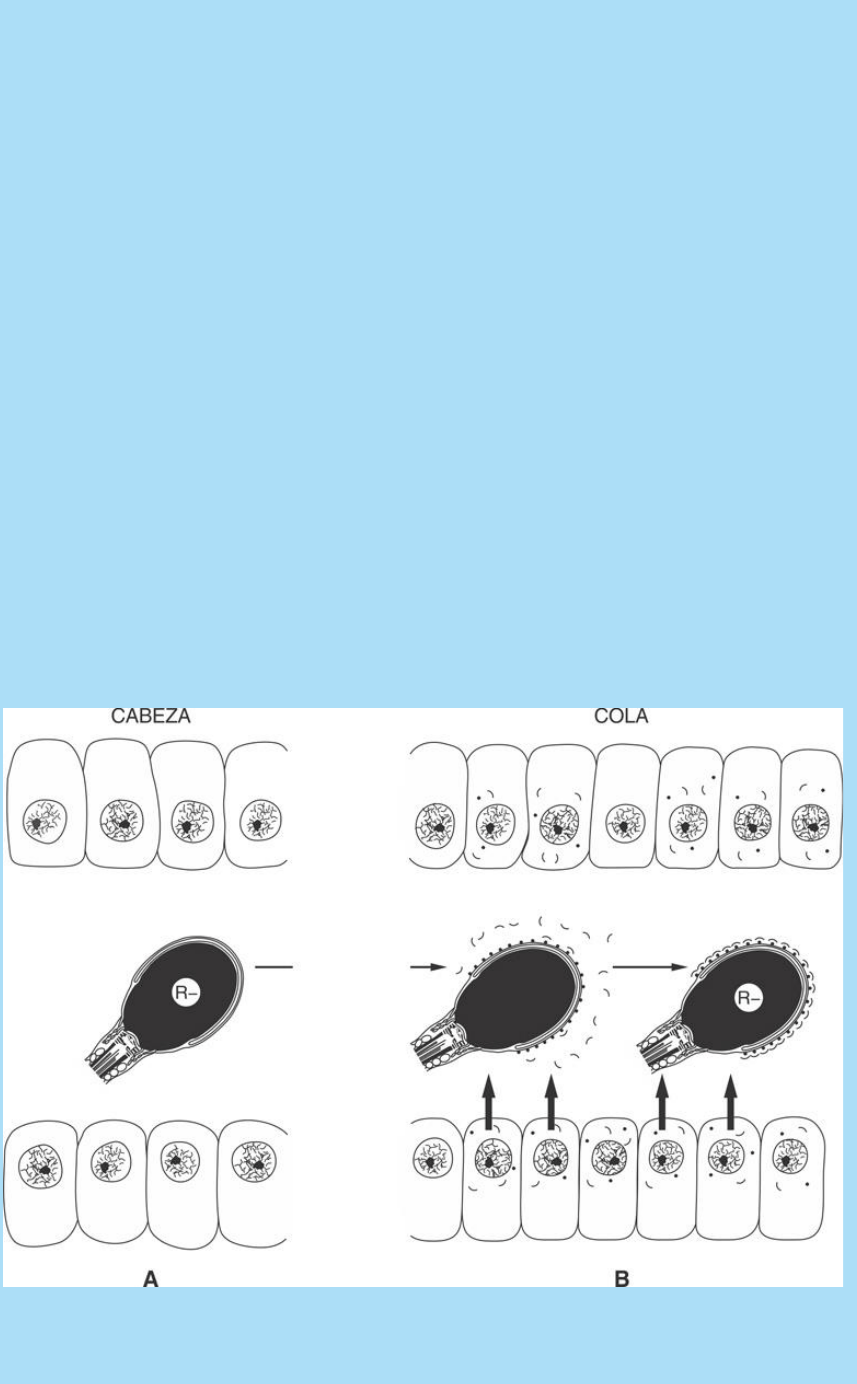
Fig. SC 1-1-1. Modificaciones de la cubierta superficial del
espermatozoide a su paso por el epidídimo. A. Los espermatozoides
de la cabeza carecen de las proteínas superficiales que son

secretadas por el epidídimo. B. En la cola se agregan moléculas (∙)
que a continuación son estabilizadas por factores descapacitantes
(∩).
Los cambios sufridos en el epidídimo no sólo involucran la superficie
de la cabeza del espermatozoide. También se producen cambios en
algunas proteínas del flagelo involucradas en la movilidad
espermática, como por ejemplo la proteína motor dineína. Con la
maduración epididimaria, algunas proteínas del flagelo contribuyen a
estabilizar la estructura de los microtúbulos que servirán a la
movilidad espermática. El aporte de energía para la movilidad
proviene de las mitocondrias concentradas en la vaina del flagelo. Al
parecer, durante la maduración también las mitocondrias también
sufren cambios que modifican su capacidad de generar ATP.
SC 1.2. EL ISTMO DE LA TROMPA COMO RESERVORIO DE
ESPERMATOZOIDES “DESCAPACITADOS”. LA PREVENCIÓN
O EL RETARDO DE LA CAPACITACIÓN. V. Flores
En la especie humana casi todos los embarazos resultan de coitos
practicados en un lapso que va desde unos 6 días antes de la
ovulación hasta que ésta ocurre. Esto significa que los
espermatozoides pueden permanecer en el oviducto durante 6 días
sin perder capacidad fecundante, vale decir, sin sufrir la reacción
acrosómica, sin hiperactivarse, ni envejecer.
El concepto de “oviducto como reservorio” de espermatozoides no se
refiere sólo a que los espermatozoides se hallan contenidos en el
oviducto durante su transporte, o que eventualmente pueden
detenerse transitoriamente en él. El concepto alude a que el oviducto
en período no ovulatorio posee una fisiología tal que, al igual que los
conductos deferentes del tracto genital masculino, permite mantener
a los espermatozoides en latencia, es decir, en un estado
“descapacitado” hasta el momento de la ovulación.
Existen varios hechos, de diversa naturaleza, que están incluidos en
el concepto de “oviducto como reservorio” de espermatozoides:
a) En el nivel morfológico, se considera que las características
microanatómicas de los pliegues de la mucosa oviductal contribuyen
a retener espermatozoides. La mucosa presenta pliegues de
trayectos anfractuosos y de diversa jerarquía (los pliegues amplios y
profundos se ramifican en pliegues más delgados y, naturalmente, de
menor profundidad figura SC 1-2-1 A. Por otro lado los pliegues
recorren sólo un cierto trayecto a lo largo de la mucosa y se

interrumpen en fondos de saco ciego, como si el surco o cauce de un
río se detuviera abruptamente en un extremo cerrado o en un foso.
Todas estas anfractuosidades contribuyen a que los
espermatozoides que se introducen en ellas queden retenidos
transitoriamente.
b) La vasculatura de la mucosa oviductal posee características
histológicas similares a la que exhiben los órganos eréctiles. Por ello,
se plantea que la ingurgitación de dichas redes vasculares podría
generar un estado eréctil de los pliegues de la mucosa, con la
consiguiente disminución de la luz y colapso de los espacios
interpliegues. Se propone que este hecho puede contribuir a un
“atropamiento” e inmovilización de espermatozoides entre pliegues
adyacentes ingurgitados.
c, d) Por otro lado, habría conexiones funcionales entre la
vasculatura ovárica y la oviductal de modo que señales generadas
en el ovario podrían actuar en la mucosa oviductal promoviendo
cambios en su patrón de secreciones que convierten los fluidos
tubáricos, durante período no ovulatorio, en un medio apropiado para
el mantenimiento descapacitado de los espermatozoides. En el nivel
celular, el mecanismo circulatorio descrito contribuiría también, en
sinergia con los cambios producidos por los niveles hormonales, a
modificar las características moleculares del glucocáliz de la
membrana apical de las células del epitelio oviductal en período no
ovulatorio.
e) En el nivel molecular, los cambios del glucocáliz se refieren
específicamente a una modificación en la composición de residuos
azúcares de las glucoproteínas y polisacáridos que integran el
glucocáliz. La interacción de estos grupos azúcares con proteínas
símil-lectinas de la cubierta glucoproteica de la superficie del
espermatozoide contribuye a dos hechos: 1)mantener a los
espermatozoides en un estado descapacitado (de modo similar a
como lo hacen los factores descapacitantes de los fluidos seminales)
y 2) mantener a los espermatozoides anclados al epitelio oviductal.
Existen experimentos que indican que el estado “descapacitado” de
los espermatozoides, antes de ingresar en la ampolla, es mantenido
por interacciones con células del epitelio del istmo al cual los
espermatozoides se adhieren (Fig. SC 1-2-1 B y 1-2-2 B). Estos
experimentos muestran que la unión de los espermatozoides al
epitelio depende de ciertos grupos azúcares pertenecientes a
glucoproteínas de la superficie apical de las células epiteliales.
En cultivos de bloques de mucosa ístmica y ampular del oviducto, de
período no ovulatorio o estrogénico, con una suspensión de
espermatozoides, se constata que los espermatozoides se unen

específicamente a la mucosa. La figura SC 1-2-2 A (izquierda)
muestra que, si a dicho medio de cultivo se agregan diferentes
azúcares de modo que se unan a la superficie de los
espermatozoides, éstos mantienen su capacidad de unión a la
mucosa oviductal, salvo cuando se utiliza fucoidan (una mezcla de
fucosa y fucosa-sulfato). Este hecho sugiere que la fucosa, integrante
normal del glucocáliz, cumple un papel en la función de reservorio. El
resultado descrito ocurre tanto en la mucosa del istmo como de la
ampolla del oviducto. La figura SC 1-2-2 A (centro) muestra que el
efecto descrito es dependiente de la dosis de fucoidan que se utiliza
en el ensayo. Finalmente, la figura SC 1-2-2 A (derecha) corrobora el
concepto ya que la eliminación de la mucosa del glucocáliz, por
medio del tratamiento de la mucosa con fucosidasa (una enzima que
elimina mucosa del glucocáliz), reduce significativamente la adhesión
de los espermatozoides a la mucosa.
La figura SC 1-2-2 B muestra esquemáticamente la idea de que la
función de reservorio está mediada por interacciones entre proteínas
símil-lectinas, de la cubierta glucoproteica de la superficie del
espermatozoide, y grupos azúcar del glucocáliz de las células
epiteliales. El esquema incluye el dato, aportado por la microscopia
electrónica de barrido, de que, generalmente, los espermatozoides
unidos a la mucosa se hallan “abrazados” por las cilias, como si éstas
estuvieran inmóviles y rodeando a los espermatozoides. El esquema
propone que tal interacción se pierde durante la capacitación y que
el espermatozoide se suelta del epitelio. Ello inicia la etapa final, que
conduce a la fecundación o al envejecimiento del espermatozoide.
Fig. SC 1-2-1. A. Corte transversal de la mucosa oviductal; se ilustran
los pliegues de diversas jerarquía. B. La figura muestra un
espermatozoide detenido en la trompa uterina por medio de
interacciones con el epitelio tubárico. Puede observarse que el
espermatozoide se halla en buenas condiciones y el acrosoma se
encuentra intacto. El esquema incluye el dato, aportado por la
microscopia electrónica de barrido, de que, generalmente, los
espermatozoides unidos a la mucosa se hallan “abrazados” por las
cilias. Como si éstas estuvieran inmóviles y rodeando a los
espermatozoides.
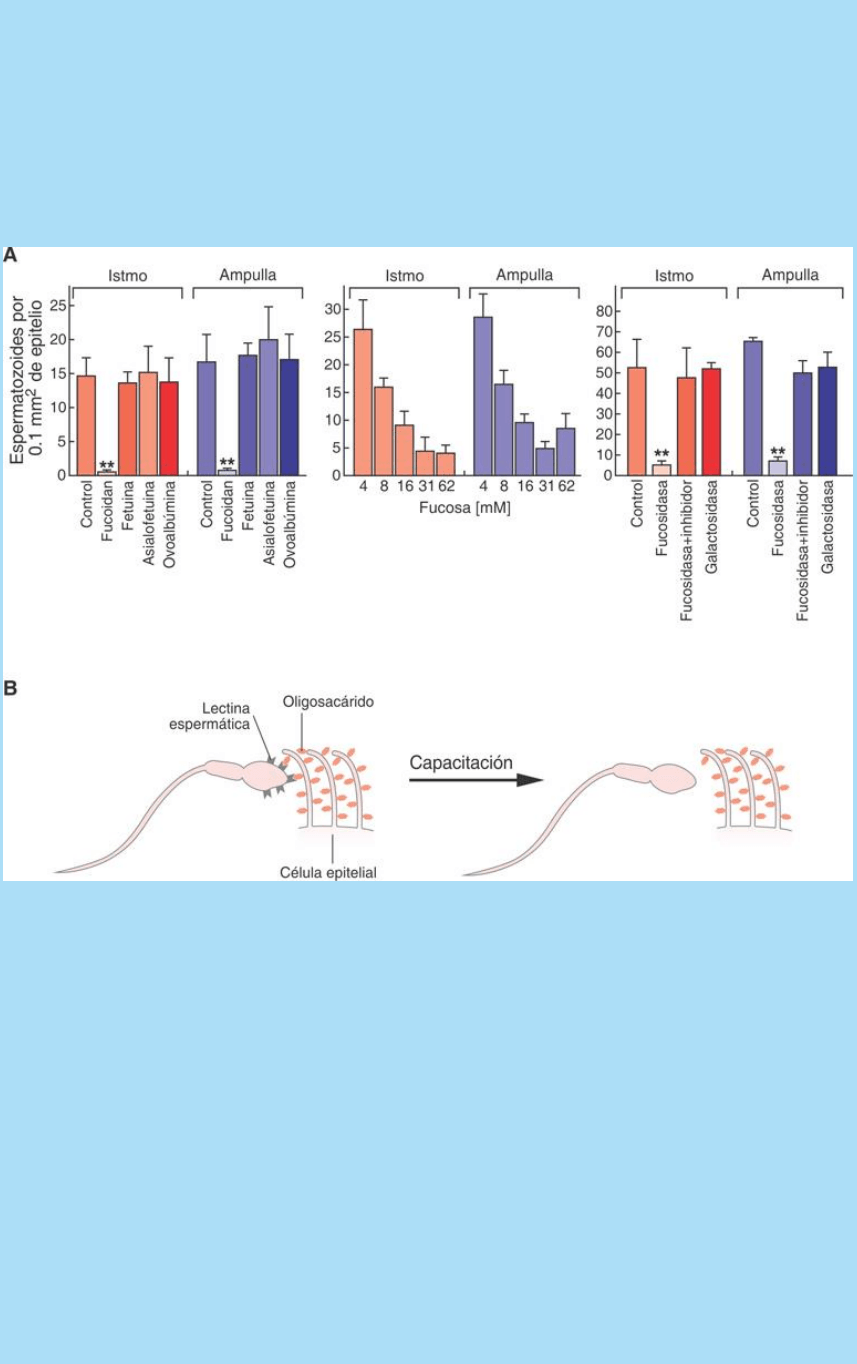
Fig. SC 1-2-2. A. Resultados de la interacción de espermatozoides
con cultivos de bloques de mucosa oviductal (ístmica y ampular).
Izquierda: si al medio se agregan azúcares que se unen a la
superficie de los espermatozoides, sólo una mezcla de fucosa y
fucosa-sulfato (fucoidan) interfiere con la unión al glucocáliz del
epitelio oviductal sugiriendo que la mucosa cumple un papel en la
función de reservorio. Centro: muestra que la unión es dependiente
de la dosis de fucoidan agregado al medio. Derecha: el tratamiento
de la mucosa con fucosidasa (una enzima que elimina fucosa del
glucocáliz) reduce la adhesión de los espermatozoides a la mucosa.
B. La función de reservorio está mediada por interacciones entre
proteínas símil-lectinas,de la cubierta glucoproteica de la superficie
del espermatozoide, y grupos azúcar del glucocáliz de las células
epiteliales. El esquema propone que tal interacción se pierde durante
la capacitación y que el espermatozoide se suelta del epitelio. Ello

inicia la etapa final, que conduce a la fecundación o al envejecimiento
del espermatozoide.
Se ha planteado que el mantenimiento de los espermatozoides
dentro de las trompas cumple una función durante la fecundación:
a) por un lado explicaría la escasa cantidad de espermatozoides que
se hallan en el sitio de encuentro pero durante un lapso de tiempo
prolongado en las cercanías del ovocito II;
b) este hecho podría contribuir a disminuir la probabilidad de
polispermia restringiendo el número de espermatozoides que llegan
por unidad de tiempo. Esta hipótesis ha sido validada por medio de
experimentos de extirpación quirúrgica del istmo. En varias especies,
este procedimiento aumenta la tasa de polispermia.
c) la consecuencia más importante sería aumentar la probabilidad de
que, en el momento de la ovulación, existan espermatozoides
fecundantes aun cuando el coito haya precedido en días a la
fecundación. Probablemente la adhesión al epitelio del istmo tubárico
se pierda cuando se produce la ovulación. Todos estos datos indican
que la capacidad fecundante o capacitación se adquiere
principalmente en la ampolla (sitio de encuentro), en el momento de
la ovulación y que tal capacidad es transitoria pues le sigue el
envejecimiento.
También existen estudios realizados en seres humanos que indican
que el cuello uterino también puede almacenar espermatozoides. Allí
los espermatozoides pueden mantenerse descapacitados, durante
varios días, en las criptas de las glándulas del cuello uterino y en
sucesivas oleadas son llevados hacia el sitio de encuentro.
SC 1.3. EL TRANSPORTE DE LOS ESPERMATOZOIDES. EL
PAPEL DE LA MOVILIDAD PROPIA DEL ESPERMATOZOIDE. V.
Flores
La movilidad espermática es un dato importante del espermograma.
El déficit en la movilidad se asocia a infertilidad. Se suele concluir, en
consecuencia, que los espermatozoides ascienden hasta el sitio de
encuentro gracias a su movilidad y que el déficit en la movilidad
impide o dificulta el ascenso y el encuentro con el ovocito II. Esta
conclusión probablemente sea errónea.
El espermatozoide está programado para cumplir en plenitud su
capacidad móvil en el momento del encuentro y no durante el
ascenso hacia el sitio de encuentro (Fig. SC 1-3-1). Así, la movilidad
propia del espermatozoide debe desempeñar un papel menor en el
ascenso, en tanto que el tracto genital femenino desempeña un papel

principal. Nótese que los espermatozoides empiezan a llegar al sitio
de encuentro en sólo unos 30 minutos luego de depositados en la
vagina. Mediciones sobre las velocidades máximas que desarrollan
los espermatozoides y estimaciones sobre la potencia de la fuerza
propulsora del flagelo indican que los espermatozoides no podrían
desplazarse a la velocidad que se requiere para recorrer tal distancia
en sólo 30 minutos.
Fig. SC 1-3-1. A. Patrón de movilidad del espermatozoide en el
eyaculado. B. Cambio en el patrón de movilidad del espermatozoide
una vez que éste se encuentra en el sitio de encuentro. Tal cambio,
al igual que la reacción acrosómica, es provocado por moléculas que
se encuentran en el líquido folicular.
Una vez en el sitio de encuentro, sin embargo, la movilidad propia
desempeña un papel crucial pues es estimulada por el líquido
folicular que también induce la reacción acrosómica. Los
espermatozoides encuentran al ovocito II rodeado por la corona
radiante (células foliculares unidas por una alta concentración de
ácido hialurónico). El ácido hialurónico es degradado por enzimas
acrosómicas, entre ellas la hialuronidasa. La velocidad de toda
reacción enzimática depende, entre otros factores, de la energía
cinética del medio. La hiperactivación de los espermatozoides
contribuye a aumentar la energía cinética del medio, facilitar la
degradación del ácido hialurónico, disminuir la cohesión de las
células foliculares y a dispersarlas. Estos efectos facilitarían que los
espermatozoides puedan atravesar la corona radiante y llegar al
ovocito II.La hiperactivación también aumenta la energía cinética del
espermatozoide y, en consecuencia, la probabilidad de colisión con
la membrana pelúcida.

No existen datos concluyentes sobre la existencia de un mecanismo
quimiotáctico que direccione los espermatozoides hacia el ovocito II,
aunque algunos resultados experimentales lo sugieren.
Otro “momento” en el que la movilidad propia del espermatozoide es
crucial ocurre durante la penetración de la membrana pelúcida. Éste
también es un proceso de degradación enzimática (acrosina y
neuraminidasa) incrementado por la frecuencia de colisión de la
membrana acrosómica interna, que expone la cabeza del
espermatozoide, contra sus sustratos de la membrana pelúcida. El
aumento de la degradación sumado a la propulsión del flagelo
posibilita la penetración de la membrana pelúcida y el contacto con
el ovocito II.
Es importante el dato experimental de que los espermatozoides que
son incubados con líquidos foliculares de diferentes folículos no se
comportan similarmente. Algunos líquidos foliculares son muy
eficaces en producir hiperactivación y otros no. Es significativo el
hecho de que, en el caso de los líquidos foliculares que estimulan la
hiperactivación, la fecundación se produce en un alto porcentaje y
que, en el caso contrario, no se produce fecundación.
Todos estos datos sugieren que la movilidad propia del
espermatozoide y su déficit asociado a la infertilidad probablemente
se deba principalmente al importante papel que la movilidad
espermática adquiere en el sitio de encuentro.
SC 1.4. LA CAPACITACIÓN DEL ESPERMATOZOIDE Y LA
REACCIÓN ACROSÓMICA. V. Flores
Varios estudios clásicos de fecundación in vitro mostraron que los
espermatozoides recién eyaculados incubados con ovocitos II tardan
un cierto tiempo en iniciar la fecundación. Los espermatozoides que
han estado en contacto con fluidos tubáricos fecundan más
rápido (Fig. SC 1-4-1).
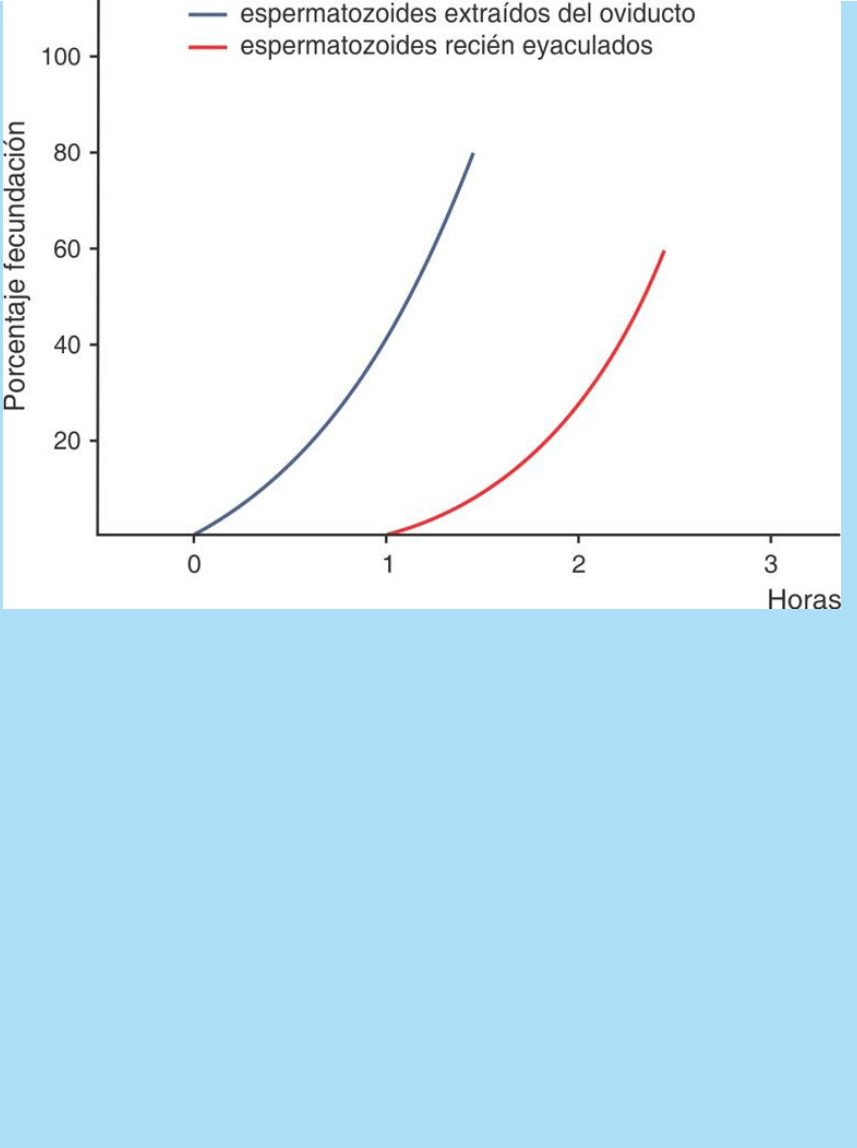
Fig. SC 1-4-1. El grafico muestra que los espermatozoides extraídos
del oviducto o los que son incubados en fluidos del oviducto fecundan
más rápido que los recién eyaculados.
Esta capacidad aumenta en función del tiempo de permanencia en el
tracto genital femenino. Los espermatozoides en vías de
capacitación, si son devueltos al líquido seminal se “descapacitan”;
vale decir, pierden la capacidad adquirida en contacto con los fluidos
del tracto genital femenino. Ello se debe a que el líquido seminal
posee factores denominados “descapacitantes” que contribuyen a
mantener en latencia a los espermatozoides (SC 1-1 La maduración
epididimaria. Bases moleculares y consecuencias). La capacitación
es el resultado de la pérdida de moléculas estabilizadoras y
“descapacitantes” del líquido seminal que se adquirieron durante la
maduración epididimaria (Fig. SC 1-4-2). Una vez iniciada la
capacitación se inicia el envejecimiento de los espermatozoides y
pierden capacidad fecundante en unas 12 horas.
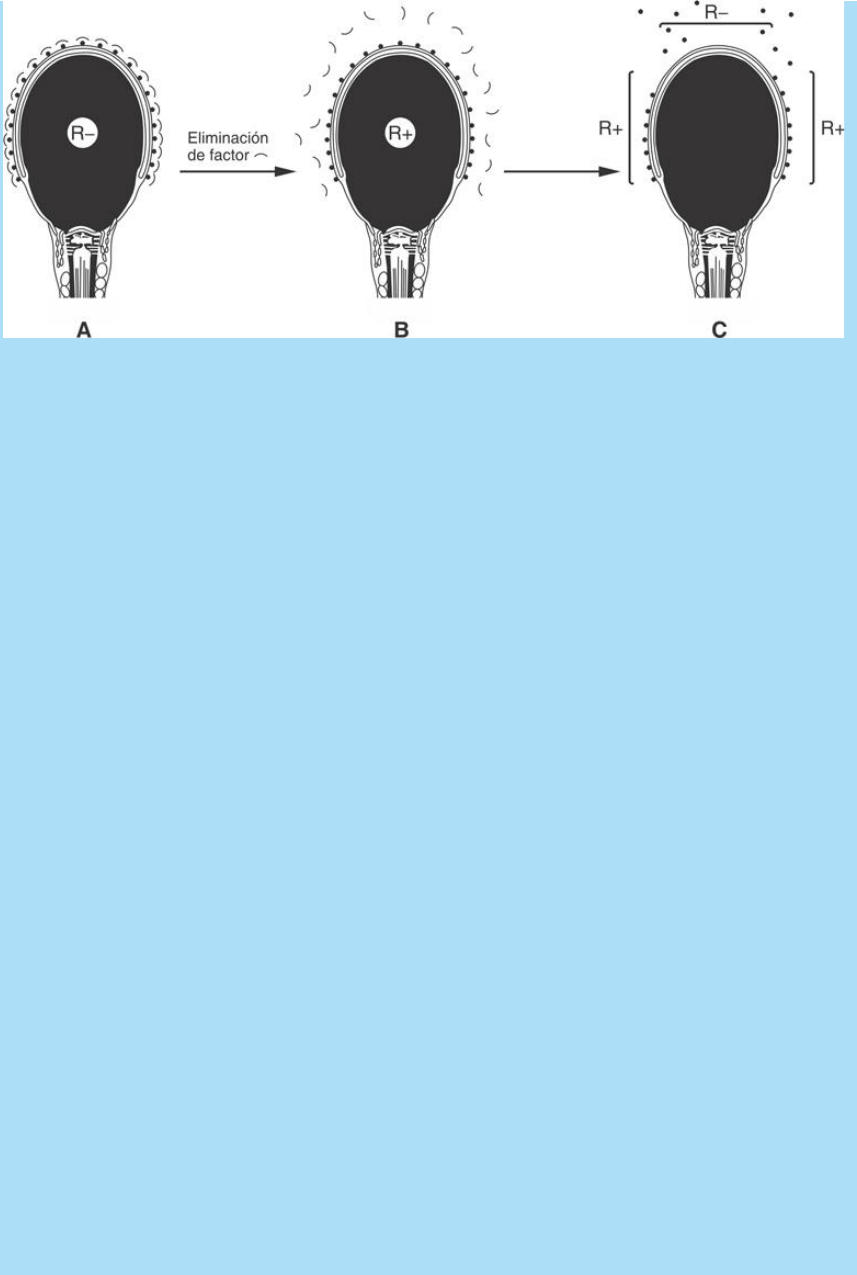
Fig. SC 1-4-2. El esquema ilustra el probable comportamiento de
algunas moléculas presentes en la cubierta de superficie del
espermatozoide durante la capacitación. A. En los espermatozoides
recién eyaculados, la moléculas de la superficie del espermatozoide
(∙) que intervienen en la fecundación se hallan enmascaradas por
moléculas descapacitantes (∩). Este hecho dificulta la fecundación.
B. Después de cierto tiempo en contacto con fluidos tubáricos se
desprenden los factores descapacitantes y quedan expuestos los que
intervienen en la fecundación. C. Con el tiempo, los espermatozoides
también van perdiendo las moléculas (∙) agregadas en la cola del
epidídimo. Éstas se pierden desde el extremo del acrosoma hacia el
polo opuesto. La letra R seguida de los signos – o + aluden a cómo
las reacciones (R) de laboratorio realizadas para detección de
moléculas (.) dan resultados negativos (-) o positivos (+) dependiendo
del tiempo transcurrido dentro del tracto genital femenino en período
ovulatorio (capacitante).
Existen muchas dudas y discordancias en la literatura respecto de
numerosos fenómenos moleculares involucrados en la capacitación
y, al parecer, existen muchas diferencias dependientes de la especie.
La capacitación conduce a la reacción acrosómica y la
hiperactivación del espermatozoide, y en general se considera que
se debe a la reversión de fenómenos que ocurrieron durante la
maduración epididimaria, que los mantienen estabilizados en
latencia, y al capacitarse adquieren rápida y sincrónicamente
capacidad fecundante.
El cuadro SC 1-4-1 muestra algunos datos clásicos sobre cambios
involucrados en la capacitación.

Existen muchos datos, no siempre coherentes, acerca de los
fenómenos moleculares involucrados en la producción de la reacción
acrosómica. Mencionamos a continuación los más comunes:
a) Algunas proteínas del fluido de la ampolla, entre ellas la albúmina,
remueven colesterol de la membrana plasmática; ello aumenta su
fluidez y facilita la fusión de membranas necesaria para la reacción
acrosómica.
b) Durante la capacitación se produce intercambio de iones con el
medio. En algunas especies se eliminan iones K+ y la la membrana
plasmática se hiperpolariza. A este fenómeno le sigue la entrada de
Ca
+2
y bicarbonatos que, por un lado, activa la producción de AMPc
y, por otro, facilita la fusión de membranas necesaria para la reacción
acrosómica. En algunas especies, la entrada de Ca
+2
depende de la
unión de polisacáridos del medio, que contienen fucosa, a un
receptor del espermatozoide. Esta interacción permite la entrada de
Ca
+2
. En mamíferos, la unión de estos receptores a sus ligandos
produciría una despolarización de la membrana con la apertura de
canales de Ca
+2
dependientes de voltaje. La entrada de Ca
+2
facilita
la fusión de las membranas acrosómica externa y plasmática, la
formación de poros y la consiguiente exocitosis del contenido.
c) También es sabido que existen procesos de fosforilación de
proteínas de la membrana que contribuyen a estos cambios.
d) Otro hecho conocido es la eliminación de glucoproteínas
“descapacitantes” de la superficie del espermatozoide, que
enmascaran sitios de reconocimiento para la membrana pelúcida,
Así, la capacitación también aumenta la probabilidad del primer
contacto-reconocimiento entre el espermatozoide y la membrana
pelúcida.
Algunos de estos fenómenos son coherentes con el hecho de que la
incubación de espermatozoides en medios de cultivo que contienen

albúmina, Ca
+2
y bicarbonato estimula la capacitación. El cultivo en
presencia de líquido folicular del oviducto también estimula la
capacitación.
e) Para el caso de los espermatozoides que contactan con la
membrana pelúcida sin haber sufrido la reacción acrosómica, ésta se
desencadena por la interacción de la ZP3 de la membrana pelúcida
con sus proteínas receptoras de la superficie del espermatozoide.
Debido a esta interacción se abren canales de Ca
+2
. El aumento de
este ión en el espermatozoide desencadena rápidamente la fusión
entre la membrana plasmática y la membrana acrosómica interna y
la producción de la reacción acrosómica.
f) Se sabe en la actualidad que la capacitación y la reacción
acrosómica consisten en una respuesta compleja del
espermatozoide que implican múltiples modificaciones y que
involucran a varias vías de señalización celular.
SC 1.5. EL PAPEL DE LA REDUNDANCIA DE
ESPERMATOZOIDES, DE LA REACCIÓN ACROSÓMICA Y DE
LA MOVILIDAD ESPERMÁTICA.V. Flores
El gran número de espermatozoides necesarios para la capacidad
fecundante (SC 1-5 Utilidad del espermograma) resulta del hecho de
que los espermatozoides, con excepción de la etapa de penetración
del ovocito II, cumplen sus funciones cooperativamente, como
población celular, y no aislada o independientemente. La mayor parte
de los espermatozoides cumple sus funciones de modo que unos
pocos tienen la posibilidad de penetrar la membrana pelúcida y, un
número menor aún, tome contacto con el ovocito II. En consecuencia
no desempeñan todos el mismo papel. El ovocito por otro lado se
encuentra programado de modo que sólo uno consume la
fecundación.
Los espermatozoides constituyen una población heterogénea: no
poseen el mismo grado de maduración, de movilidad, de estabilidad.
Ni siquiera poseen similar vida media, algunos mueren en el tracto
genital femenino mucho antes que otros. Sin embargo, como
población, poseen cierto grado de maduración, de capacidad móvil y
estabilidad que les permite realizar similares comportamientos, pero
con diferente sentido biológico.
En la especie humana, en el volumen eyaculado se hallan unos 300
millones de espermatozoides. Sin embargo, en el sitio de encuentro
sólo se hallan, en forma permanente, unos 200 a 400
espermatozoides. Ello se debe a que aquellos que llegan más
temprano cumplen sus funciones mientras están “de paso” por el sitio

de encuentro. En efecto, los que llegan primero al sitio de encuentro,
como consecuencia de a) la alta concentración del líquido folicular,
b) se capacitan, c) sufren la reacción acrosómica (liberan enzimas),
d) se hiperactivan, aumentan la energía cinética del medio, d)
contribuyen a dispersar células de la corona radiante y convertirla en
una capa laxa que pueda ser atravesada. Estos espermatozoides no
poseen papel fecundante: realizan sus funciones lejos del ovocito II,
no se fusionan con él, liberan grandes cantidades de enzimas
denudantes (hialuronidasa), pierden capacidad fecundante
(envejecen) y son llevados en su viaje ascendente hacia el peritoneo.
Fig. SC 1-5-1. El dibujo muestra el resultado experimental de
sumergir el ovocito junto con la corona radiante en una solución con
colorante (fondo negro). Nótese que el colorante no penetra entre las
células foliculares salvo en la periferia. Ello se debe a la presencia de
una densa matriz extracelular entre las células foliculares. Los
espermatozoides deben degradar la mayor parte de dicha matriz
extracelular y dejar zonas de membrana pelúcida expuestas
(denudación) antes de que algún espermatozoide pueda realizar el
contacto-reconocimiento con la membrana pelúcida.

Existe una gran diferencia temporal entre los espermatozoides que
llegan primero y los que llegan últimos. Los primeros en llegar al sitio
de encuentro sufren la reacción acrosómica y se encargan de
producir la denudación de la corona radiante y exponer la membrana
pelúcida a los espermatozoides que llegan más tarde. Este fenómeno
requiere la participación de una gran cantidad de espermatozoides
ya que el paso a través de la corona radiante y su desagregación
requiere una cantidad abundante de enzimas acrosómicas. La
corona radiante, pese a su aspecto histológico de células en
apariencia laxamente distribuidas, posee una densa malla de
proteínas de matriz extracelular que dificulta el acceso de moléculas
del medioambiente a su intersticio (Fig. SC 1-5-1). Los últimos se han
mantenido sin realizar la reacción acrosómica: a) llegan “tarde” al sitio
de encuentro, b) cuando se hiperactivan aumentan su probabilidad
de colisión con la membrana pelúcida, c) no han sufrido la reacción
acrosómica, d) poseen la membrana periacrosómica intacta y pueden
realizar el primer contacto, mediado por la ZP3, con la membrana, e)
sufren la reacción acrosómica provocada por la ZP3 de la membrana
pelúcida y en consecuencia f) tienen su dotación enzimática
acrosómica intacta. Son éstos los espermatozoides que, desde el
punto de vista probabilístico, poseen papel fecundante.
SC 1.6. EL CONTACTO Y RECONOCIMIENTO ENTRE LAS
GAMETAS. V. Flores
Pese a que los mamíferos son especies de fecundación interna,
todavía conservan fenómenos moleculares adquiridos
evolutivamente por ancestros muy lejanos, que garantizan la eficacia
de las interacciones entre gametas de la misma especie que
conducen a la fecundación. Estos mecanismos específicos de
especies son esenciales en los animales de fecundación externa. Los
organismos superiores son de fecundación interna y han adoptado
muchos mecanismos nuevos, más elaborados y correspondientes a
otros niveles de organización del individuo (celulares, histológicos,
anatómicos, funcionales y conductuales) que garantizan la
especificidad de especie en la fecundación. Éstos fallan sólo cuando
se trata de especies muy emparentadas que aún están en proceso
de especiación. No basta la colisión entre las gametas para que se
produzca la fecundación. Se requieren varios mecanismos
específicos de contacto y reconocimiento para el éxito de la
fecundación.
a) El primer contacto-reconocimiento se produce entre la membrana
periacrosómica del espermatozoide y la membrana pelúcida del
Este documento contiene más páginas...
Descargar Completo
Cap 16 SC Flores.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.