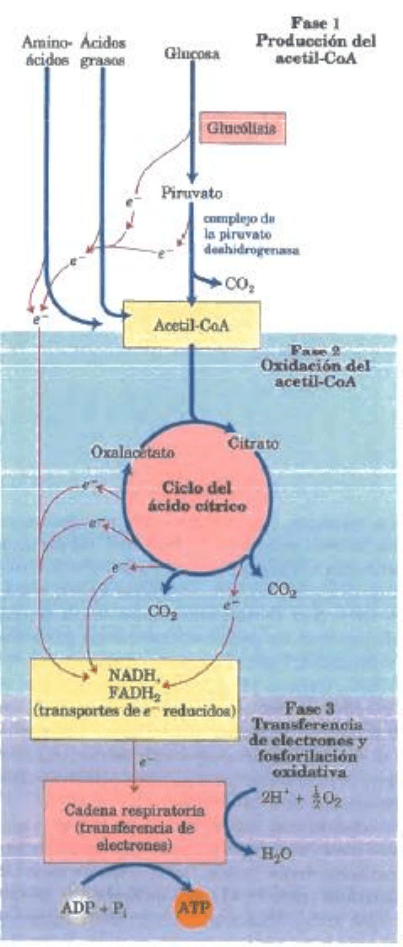
Cadena de transporte de electrones
Analizando el nombre del proceso de la respiración celular hace referencia a
eslabones conectados entre sí, que se irán desplazando de un sitio a otro
provenientes de las coenzimas reductoras reducidas NADH y FADH
2
La cadena respiratoria es un proceso que se encuentra acoplado con otro proceso
llamado fosforilación oxidativa, que tienen lugar en la membrana mitocondrial interna
de la mitocondria.
La respiración celular se da en tres fases.
En la primera, se comienza con la oxidación
de compuestos complejos orgánicos, hechos
por biomolecular como glucosa,
aminoácidos y ácidos grasos se oxidan para
originar Acetil-CoA (en forma de un grupo
acetilo). En la segunda fase, los grupos
acetilo se incorporan al ciclo de Krebs donde
son oxidados por completo mediante sus
enzimas hasta dióxido de carbono.
La energía liberada en esta oxidación (los
electrones) se conserva en los
transportadores de electrones, las
coenzimas reductoras NADH y FADH
2
.
En la tercera y última etapa estas coenzimas
o moléculas energéticas son oxidadas
liberando electrones y protones. Los
electrones transportados por el NADH y
FADH2 llegan a una cadena transportadora
de electrones (conocida como cadena
respiratoria) con reducción final de O
2
a H
2
O
Durante este proceso de transferencia de
electrones se libera una gran cantidad de
energía que se conserva en forma de ATP
siendo impulsada por un proceso llamado
fosforilación oxidativa.
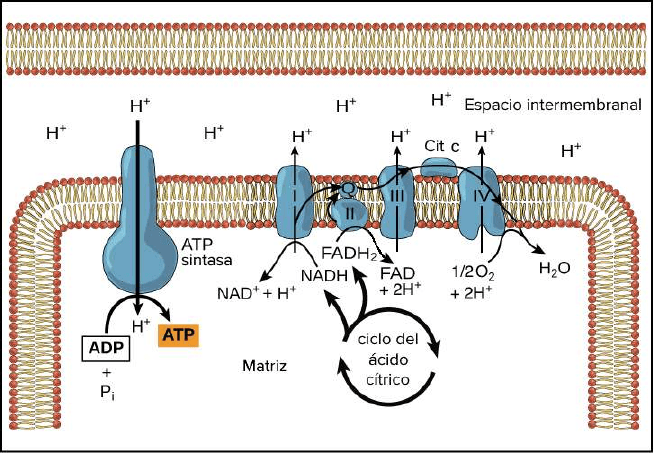
Los componentes de la cadena de transporte de electrones están ubicados en la
bicapa lipídica de la membrana mitocondrial interna que es una membrana
impermeable, en cambio con la membrana mitocondrial externa que es una
membrana muy selectiva por el hecho de que posee poros si se compara con la
membrana mitocondrial interna que es impermeable, estando ambas membranas
separadas por el espacio mitocondrial.
Los electrones pasan a través de una serie de transportadores de membrana,
siendo proteínas tales como los complejos macromoleculares llamados Complejos I,
II, III y IV acompañado de coenzimas móviles denominadas coenzima Q y citocromo
C. Estos últimos tienen propiedad de oxidoreductasa, siendo capaces de reducirse y
oxidarse.
Por último se encuentra la ATP sintasa o complejo V encargada de la síntesis de
ATP impulsada por la fosforilación oxidativa.
Cuando los electrones van pasando a través de los compartimientos hay en paralelo
un bombeo de protones hacia el espacio intramitocondrial, a excepción del
Complejo II que no bombea protones porque no atraviesan la membrana
mitocondrial interna, a lo que cada complejo transportan en sentido de menor a
mayor potencial de reducción estándar el último tiene más afinidad que el anterior
por los electrones y por eso se van a ir transportando, hasta el oxígeno que es el
que posee un potencial redox más grande.
La cadena transportadora de electrones es un conjunto de complejos enzimáticos
siendo la mayoría proteínas transmembrana que poseen grupos prostéticos (iones
metálicos tales como Fe, S, Cu) capaces de aceptar y ceder los electrones llevando
a cabo reacciones de óxido-reducción. Cabe comentar que los metales tienen mejor
afinidad por los electrones para ser conductores de la electricidad por eso son
buenos conductores a través de los complejos.
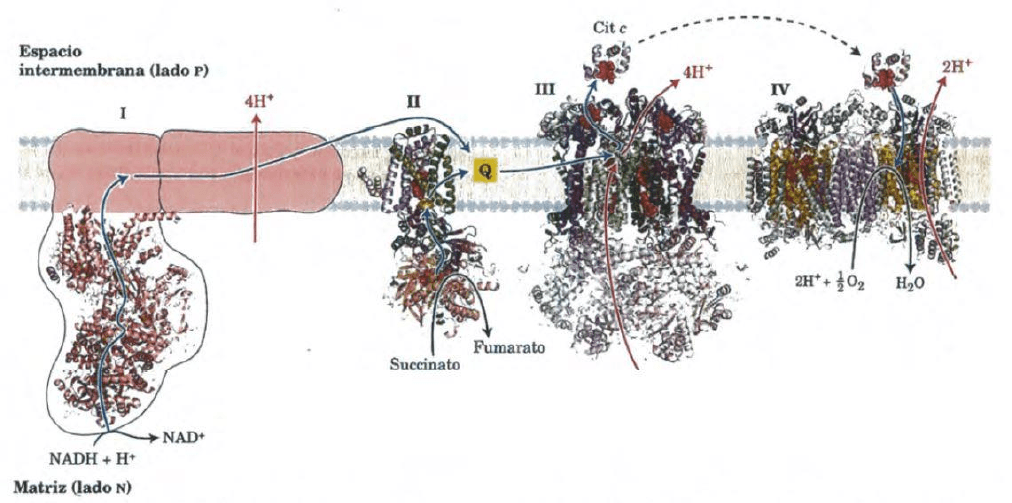
Las crestas mitocondriales permiten que haya eslabones que son complejos
proteicos y ahí es donde se da la cadena respiratoria.
Complejo I → NADH deshidrogenasa
Complejo II → succinato deshidrogenasa
Complejo III → Citocromo bc 1
Complejo IV → Citocromo oxidasa
Complejo I (NADH ubiquinona oxidoreductasa): Este complejo con grupos
prostéticos FMN junto con centros Fe-sulfurados con forma de L, un brazo de esta
en la membrana mitocondrial y el otro extremo con dirección hacia la matriz. El
complejo I realiza dos procesos en paralelo, uno de ellos en común con los otros
complejos III y IV que es que mueve los protones (H+) hacia una dirección
específica bombeando hacia el espacio mitocondrial, por otro lado el otro proceso
propio de este complejo I es la transferencia de electrones del NADH a NAD+ que
entran al complejo, mediante los centros hierros sulfurados son conducidos a la
coenzima Q.
Complejo II (succinato deshidrogenasa): El complejo II contiene a la enzima
succinato deshidrogenasa del ciclo de Krebs, y transfiere los electrones del
succinato a la coenzima Q.
Como ya hemos visto en el ciclo del ácido cítrico la succinato deshidrogenasa es la
única enzima del ciclo que se encuentra en la membrana mitocondrial interna y esta
localización tiene que ver con que cuando entra el succinato y se oxida a fumarato
se liberan electrones se reduce el FAD a FADH
2
Los electrones liberados a causa

de la oxidación del succinato en fumarato pasan a los centros hierro-sulfurados
dandolos a la coenzima Q.
Coenzima Q: Es un componente de la cadena respiratoria de naturaleza lipídica
siendo una molécula pequeña y liposoluble por lo cual se mueve de una manera
fácil y rápida dentro de la bicapa lipídica de la membrana mitocondrial interna.
Hay que tener en cuenta que la coenzima Q varía de nombre según su estado de
óxido-reducción. Cuando está oxidada se le denomina Ubiquinona (Q) y cuando
obtiene electrones dados por el complejo I y II (se reduce) pasa a llamarse Ubiquinol
(QH
2
)
Citocromo C: Son proteínas pequeñas ubicada en la cara externa de la membrana
mitocondrial interna que tienen grupos prostéticos hemo que contienen hierro,
captan electrones y los ceden, o sea que tiene únicamente la actividad de reducirse
u oxidarse.
Complejo III (citocromo bc1): Este complejo va a tomar los electrones de la
ubiquinona ya reducida a ubiquinol ya sea del complejo I o II son tomados por este
complejo. Acopla la transferencia de electrones desde el ubiquinol al citocromo C.
Complejo IV (citocromo oxidasa): Es una enzima muy grande con tres
subunidades de realizar tanto transferencia de electrones como el bombeo de
protones al igual de catalizar la reacción de reducción del oxígeno al agua.
En síntesis, el flujo de electrones y protones a través de los cuatro complejos de la
cadena respiratoria sería de la siguiente manera:
Los electrones llegan a la ubiquinona (Q) por medio de los complejos I y complejos
II, Q es reducida a Ubiquinol (QH
2
) que actúa de transportador móvil de electrones.
Pasa los electrones al complejo III, el cual los pasa a otro eslabón móvil que es el
citocromo C.
El complejo IV transfiere electrones desde el citocromo C reduciendo al oxígeno
dando agua como producto final.
Los productos finales de la cadena de transporte de electrones son agua y dióxido
de carbono.
El flujo eléctrico a través de los Complejos I, III y IV va acompañado del flujo de
protones desde la matriz al espacio intermembrana, hay un gradiente electroquímico
entre el espacio intermembrana y la matriz a causa del bombeo de protones.
El gradiente electroquímico se utiliza para la síntesis de ATP.
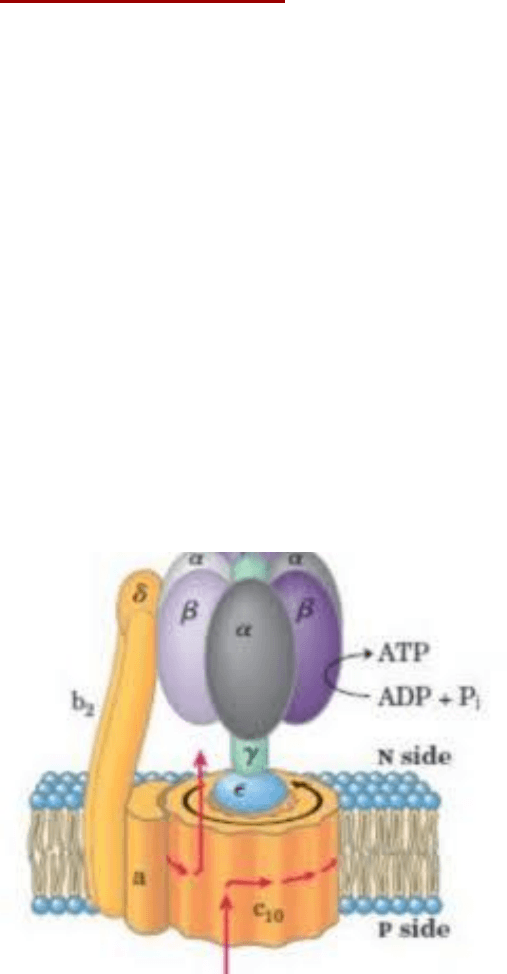
Síntesis de ATP
La síntesis de ATP está acoplada a la cadena respiratoria a través del gradiente
electroquímico de protones a ambos lados de la membrana mitocondrial interna, es
decir que no se puede realizar la cadena respiratoria si no sintetiza ATP y viceversa.
La síntesis de ATP está catalizada por la ATP sintasa, la cual tiene dos dominios
funcionales F
0
y F
1
Es un gran complejo enzimático de la membrana mitocondrial interna que cataliza la
formación de ATP a partir de ADP y Pi utilizando la energía del flujo de protones a
través la membrana por medio del dominio F
1
La catálisis rotacional es la clave en el mecanismo de unión y cambio de la síntesis
de ATP. La membrana mitocondrial interna es impermeable a los protones por lo
que entran por el dominio F
1
Los cambios de conformación están impulsados por el paso de protones a través del
dominio F
0
de la ATP sintasa. Luego el ATP sintetizado saldrá por los
transportadores de ATP expuestos en la membrana mitocondrial interna.
La fosforilación oxidativa (fosforilación = adición de un grupo Pi para dar ATP;
oxidativa, ceder electrones) es la culminación del metabolismo productor de energía
en los organismos aerobios, tiene como fin fabricar ATP. Produce el 98% del ATP
de nuestro cuerpo, mientras que la fosforilación a nivel de sustrato produce el 2%
del ATP que utilizamos.
Es la etapa final en la que la energía de oxidación impulsa la síntesis de ATP, en
donde se produce la reducción de oxígeno al agua gracias a los electrones cedidos
por el NADH y el FADH2.
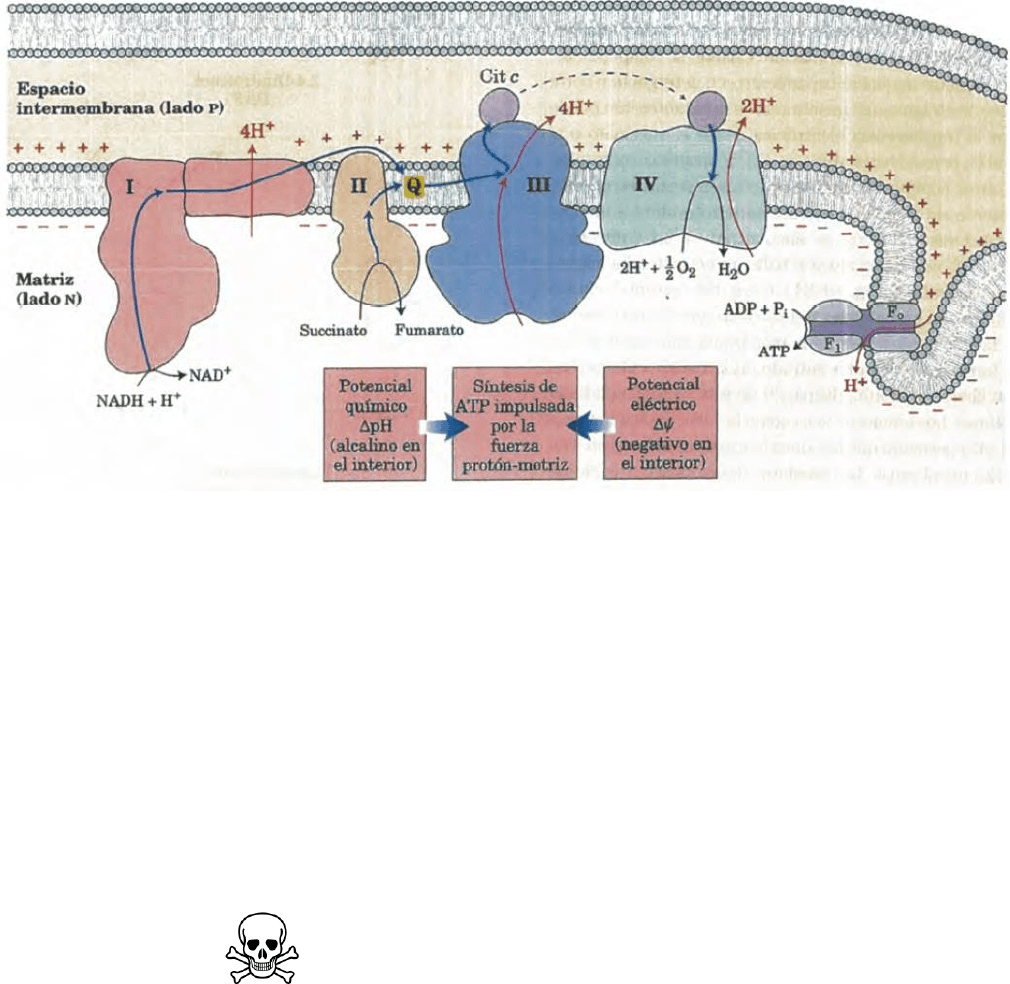
La energía electroquímica propia en esta diferencia de concentración de protones y
en la separación de cargas representa una conservación temporal de la mayor parte
de la energía de la transferencia de electrones. La energía almacenada en este tipo
de gradiente denominado fuerza protón-motriz tiene dos componentes.
Uno es la energía química potencial que es debida a la diferencia en
concentraciones de los protones entre el espacio intramitocondrial y la matriz
separadas por la membrana mitocondrial interna.
La segunda, la energía eléctrica potencial que se origina con las separaciones de
cargas cuando un protón atraviesa la membrana sin un contraión, algo que vaya en
antiporte.
VENENOS
La cadena respiratoria puede ser inhibida de manera selectiva por venenos
específicos.
Si inhibimos selectivamente un complejo de la cadena respiratoria todos los
transportadores que están antes de él quedarán reducidos, mientras que los que se
encuentran después están oxidados, interrumpiendo el transporte de electrones
hacia el oxígeno.
En el caso de la cadena respiratoria se puede evaluar el funcionamiento de la
misma a través del consumo de oxígeno hasta que el ADP se convierte en ATP.
Por ejemplo, si se inhibe selectivamente el complejo I o el II el consumo de oxígeno
disminuye a causa de que ya sea cuál de los dos el que se inhiba bloqueara sus
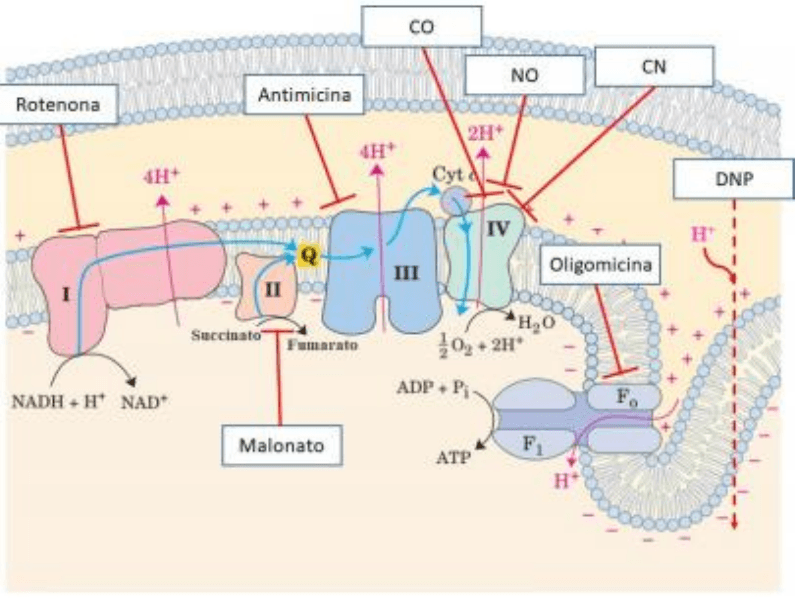
electrones hacia la ubiquinona (o coenzima Q) teniendo menor síntesis de ATP ya
que habrá solo un complejo funcionando transportando electrones. Por otro lado, si
se inhibe el complejo III o IV el consumo de oxígeno se anula.
Desacoplantes: Son moléculas capaces de dispersar el gradiente de protones
que existe entre el espacio intermembrana y la matriz, es decir desacopla el
transporte de electrones de la fosforilación oxidativa.
Son ácidos débiles con propiedades hidrofóbicas que le permiten difundir a través
de las membranas mitocondriales.
Estos ácidos se protonan en el espacio intermembrana y al ingresar a la matriz
mitocondrial liberan el protón (H+) y de esa forma disipan el gradiente
electroquímico.
Al agregar un agente desacoplante no se produce más ATP y el flujo de electrones
a través de la cadena se acelera con el fin de volver a recuperar el gradiente,
estimulando el consumo de oxígeno, ya que aumenta la velocidad del transporte de
electrones e inhibiendo a su vez la síntesis de ATP ya que al disiparse el gradiente
por el desacoplante los protones no ingresan a la matriz por el dominio F_0 de la
ATP sintasa por lo que no hay síntesis del ATP.
Algunos agentes desacoplantes de la fosforilación oxidativa y el transporte
electrónico son el DNP o FCCP.

Cadena respiratoria.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.