
© 2014. Elsevier España, S.L. Reservados todos los derechos
75
I
A medida que se implanta en la pared uterina, el embrión
sufre modificaciones profundas en su organización. Hasta el
momento de la implantación, el blastocisto está constituido
por la masa celular interna, de la que se origina propiamente
el cuerpo del embrión, y el trofoblasto externo, que representa
la conexión tisular futura entre el embrión y la madre. Ambos
componentes del blastocisto son los precursores de otros
tejidos que aparecen en fases subsiguientes del desarrollo. En
el capítulo 3 se detalla la forma en que el citotrofoblasto genera
una capa sincitial externa (el sincitiotrofoblasto), poco antes
de adherirse al tejido uterino (v. fig. 3.18). Poco después, la
masa celular interna comienza también a originar otros deri-
vados tisulares. En última instancia, la subdivisión de la masa
celular interna da lugar al cuerpo del embrión, que contiene
las tres capas germinales primarias: el ectodermo (la capa
externa), el mesodermo (la capa intermedia) y el endodermo
(la capa interna). El proceso por el cual se forman las capas
germinales mediante movimientos celulares se denomina
gastrulación.
Después de que se han establecido estas capas germinales,
la progresión continua del desarrollo embrionario depende
de una serie de señales denominadas inducciones embriona-
rias, que se intercambian entre las capas germinales u otros
precursores tisulares. En una interacción inductiva, uno de los
tejidos (el inductor) actúa sobre otro (el tejido de respuesta),
de manera que el desarrollo de este último es diferente del
que habría sido en ausencia del primero. Los desarrollos que
se pueden observar con un microscopio durante este período
son un reflejo tangible de las profundas modificaciones en la
expresión génica y en las propiedades celulares de los embriones
en fase de implantación.
Estadio de disco bilaminar
Justo antes de que el embrión se implante en el endometrio al
principio de la segunda semana, empiezan a aparecer cambios
significativos en la masa celular interna y en el trofoblasto. A
medida que las células de la masa celular interna se disponen
adoptando una configuración epitelial en lo que en ocasiones
se denomina cubierta embrionaria, aparece una fina capa
de células en su parte ventral (v. fig. 3.18). La capa superior
principal de células se llama epiblasto, y la capa inferior hipo-
blasto o endodermo primitivo (fig. 5.1).
No se sabe todavía la manera en que se forma el hipoblasto
en el embrión humano, sin embargo se sabe que en embrio-
nes de ratón en estadios tan iniciales como el de 64 células,
algunas células de la masa celular interna expresan el factor
de transcripción nanog, mientras que otras expresan Gata 6.
Estas células están dispuestas en un patrón de sal y pimienta
dentro de la masa celular interna (
fig. 5.2A). Las células que
expresan nanog representan las precursoras del epiblasto, y las
que expresan Gata 6 las del hipoblasto. No se sabe la manera
en la que estos dos tipos diferentes de células precursoras se
diferencian, pero de acuerdo con la hipótesis «time inside-time
outside», las células que entran primero en la masa celular
interna están destinadas a expresar nanog, que mantiene su
pluripotencia. Posiblemente sea debido a la influencia del
factor de crecimiento fibroblástico 4 (FGF-4), secretado por
las células que llegan primero a la masa celular interna, mien-
tras que las posteriores están determinadas a expresar Gata 6.
Las células que expresan Gata 6 producen moléculas que
aumentan sus propiedades adhesivas, así como su movilidad,
desplazándose a la superficie inferior de la masa celular interna
para formar un epitelio delgado, el hipoblasto. Las células Gata 6
que no llegan a la superficie de la masa celular interna sufren
apoptosis (muerte celular programada). Las células de la masa
celular interna que expresan nanog también adquieren una
configuración epitelial, formando el epiblasto. Entre epiblasto
e hipoblasto se crea una lámina basal.
Se ha demostrado que un pequeño grupo de células del
hipoblasto trasladadas al futuro polo anterior del embrión
(llamado endodermo visceral anterior por los embriólogos
especializados en el desarrollo del ratón) poseen un notable
poder de señalización. Estas células secretan primero las
moléculas de señal, lefty-1 y cerberus 1 (Cer-1), inhiben
la actividad de la moléculas, nodal y Wnt, en el epiblasto
suprayacente, lo que permite que nodal y Wnt-3 se expresen
en el epiblasto posterior (v. fig. 5.8A). (La señal emitida por
nodal desde el epiblasto posterior estimula la formación inicial
del endodermo visceral anterior.) Esto representa la primera
manifestación de polaridad anteroposterior en el embrión y
también da lugar a la constitución de dos dominios señali-
zadores en el embrión joven. El endodermo visceral anterior
rápidamente comienza a inducir gran parte de la cabeza y del
prosencéfalo, inhibiendo al mismo tiempo la formación de
estructuras posteriores. En la región posterior del epiblasto
la actividad señalizadora de nodal estimula la formación de la
línea primitiva (v. sección siguiente), estructura importante
para la gastrulación y la formación de las capas germinales.
Después de que el hipoblasto se ha constituido en una capa
bien definida y de que el epiblasto ha adoptado una configu-
ración epitelial, la masa celular interna se transforma en un
disco bilaminar, con el epiblasto en su superficie dorsal y el
hipoblasto en la ventral.
El epiblasto contiene las células que forman el embrión en
sí mismo, aunque de esta capa también se originan tejidos
Capítulo
5
Formación de las capas germinales
y sus primeros derivados
76 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
extraembrionarios. La capa que aparece después del hipoblasto
es el amnios, una capa de ectodermo extraembrionario que
finalmente rodea a todo el embrión en una cámara llena de
líquido denominada cavidad amniótica (v. cap. 7). Debido a la
escasez de especímenes para estudio, no hay un conocimiento
detallado sobre las fases iniciales de la formación del amnios
ni de la cavidad amniótica en el ser humano. Los estudios
realizados en embriones de primate indican que se origina
en primer lugar una cavidad amniótica primordial mediante
cavitación (formación de un espacio interno) en el interior
del epiblasto preepitelial; esta cavidad queda revestida por cé-
lulas procedentes de la masa celular interna (v. fig. 5.2). Según
algunos investigadores, el techo del amnios a continuación
se abre, con exposición de la cavidad amniótica primordial
al citotrofoblasto que queda sobre ella. Poco tiempo después
(aproximadamente a los 8 días de la fecundación), el epitelio
amniótico original vuelve a formar un techo sólido sobre la
cavidad amniótica.
Mientras el embrión temprano todavía está anidando en
el endometrio (unos 9 días después de la fecundación), las
células del hipoblasto comienzan a propagarse, revistiendo la
superficie interna del citotrofoblasto con una capa continua
de endodermo extraembrionario denominado endodermo
parietal (fig. 5.3; v. fig. 5.2). Cuando finaliza la expansión del
endodermo se ha constituido una vesícula llamada saco vitelino
primario (v.
fig. 3.18C). En este momento (alrededor de 10 días
después de la fecundación), el complejo embrionario constituye
el disco germinal bilaminar, que se localiza entre el saco vitelino
primario en su superficie ventral y la cavidad amniótica en su
superficie dorsal (fig. 5.4). Al poco tiempo, dicho saco vitelino
primario sufre una constricción, formando un saco vitelino se-
cundario y dejando un resto del anterior (v. figs. 3.18D y 5.2F).
Unos 12 días después de la fecundación comienza a aparecer
otro tejido, el mesodermo extraembrionario (v.
fig. 5.2). Las
primeras células mesodérmicas extraembrionarias parecen
proceder de una transformación de las células endodérmicas pa-
rietales. Estas células se unen después a otras mesodérmicas
extraembrionarias que se han originado a partir de la línea
primitiva. El mesodermo extraembrionario es el tejido que
constituye el soporte tisular del epitelio del amnios y del saco
vitelino y de las vellosidades coriónicas, que se originan a
partir de los tejidos trofoblásticos (v. cap. 7). El soporte que
proporciona dicho mesodermo no sólo es de tipo mecánico
sino también trófico, debido a que actúa como sustrato a través
del cual los vasos sanguíneos aportan oxígeno y nutrientes a los
distintos epitelios.
Gastrulación y formación del disco
embrionario trilaminar
Al final de la segunda semana el embrión está constituido por
dos capas celulares planas: el epiblasto y el hipoblasto. Al inicio
de la tercera semana de gestación, el embrión entra en el pe-
ríodo de gastrulación, durante el cual se forman las tres capas
germinales embrionarias a partir del epiblasto (v. fig. 5.1). La
morfología de la gastrulación humana sigue el mismo patrón
que se observa en las aves. Dada la gran abundancia de vitelo
en los huevos de las aves, el embrión de estos animales adquiere
las capas germinales primarias en forma de tres discos planos
superpuestos que descansan sobre el vitelo, de manera similar
a una pila de rebanadas de pan. A continuación las capas ger-
minales se pliegan y forman un cuerpo cilíndrico. A pesar de
que el embrión del mamífero carece prácticamente de vitelo,
el alto grado de conservación morfológica de las fases iniciales
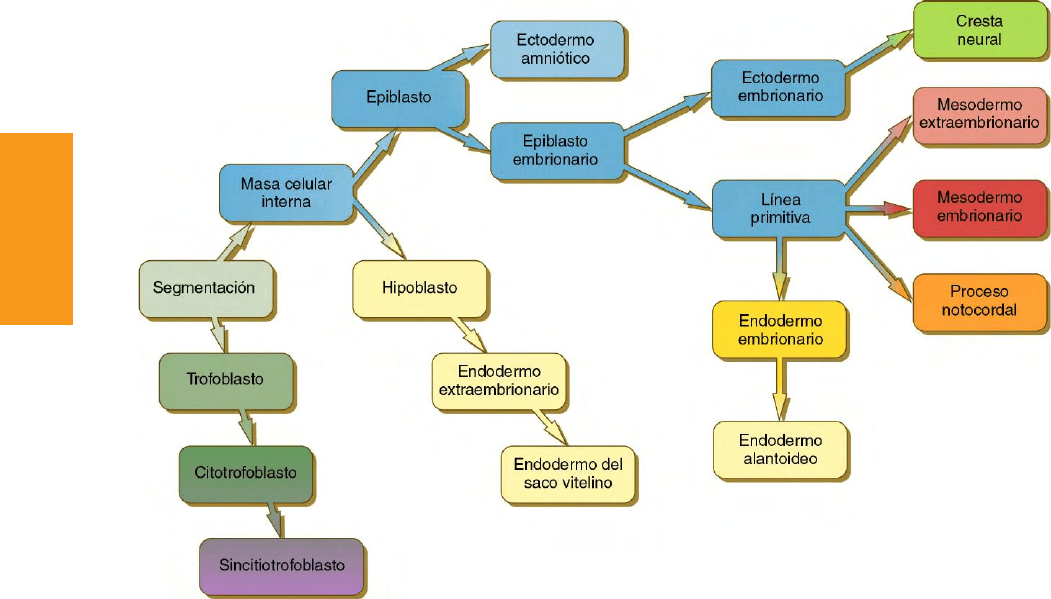
Fig. 5.1 Linajes celulares y tisulares en los embriones de los mamíferos. (Nota: los colores de los rectángulos aparecen en todas las ilustraciones
relativas a las capas germinales embrionarias y extraembrionarias.)
Capítulo 5—Formación de las capas germinales y sus primeros derivados 77
© Elsevier. Fotocopiar sin autorización es un delito.
del desarrollo hace que el embrión humano siga un patrón de
gastrulación similar al que se observa en reptiles y en aves. Dada
la escasez de material para estudio, en el embrión humano no se
conoce con detalle ni siquiera la morfología de la gastrulación.
Sin embargo, la extrapolación de la gastrulación propia de
las aves y los mamíferos proporciona un modelo de trabajo
razonable para conocer la humana.
La gastrulación se inicia con la formación de la línea primi-
tiva, una condensación celular longitudinal en la línea media
que procede del epiblasto en la región posterior del embrión, a
través de una inducción ejercida por parte de las células situadas
en el borde del disco embrionario de esta zona (v. fig. 5.4).
Se han identificado como posibles agentes inductores a los
miembros del factor de crecimiento transformante b (TGF-b)
y a las familias de moléculas de señalización de Wnt. La línea
primitiva tiene al principio una forma triangular, pero al poco
tiempo se torna lineal y se alarga mediante una combinación
de proliferación y migración, así como también a redistribu-
ciones celulares internas, llamadas movimientos de extensión
convergente. Con la aparición de la línea primitiva ya se pueden
identificar con facilidad los ejes anteroposterior (rostrocaudal)
y derecha-izquierda del embrión (v. fig. 5.4).
La línea primitiva es una región donde convergen las células
del epiblasto en una secuencia espacial y temporal bien definida.
A medida que las células del epiblasto alcanzan la línea primiti-
va cambian su morfología y pasan a través de ella para formar
nuevas capas celulares debajo del epiblasto (ventrales al mismo)
(fig. 5.5C). Estudios de marcaje han demostrado que las células
que entran en la línea primitiva forman diferentes linajes cuando
la abandonan. Las células que entran y abandonan la línea primi-
tiva, en su zona más posterior, cuando ésta comienza a elongarse,
forman el mesodermo extraembrionario que reviste el trofoblas-
to y el saco vitelino, así como también los islotes sanguíneos
(v. fig. 6.19). Otra oleada de mesodermo, que surge más tarde y más
anterior en la línea primitiva, es responsable de la formación del
mesodermo paraaxial, la placa lateral y el mesodermo cardíaco.
Una oleada final, la cual entra y abandona el extremo más anterior
de la línea primitiva, da lugar a estructuras axiales (la notocorda,
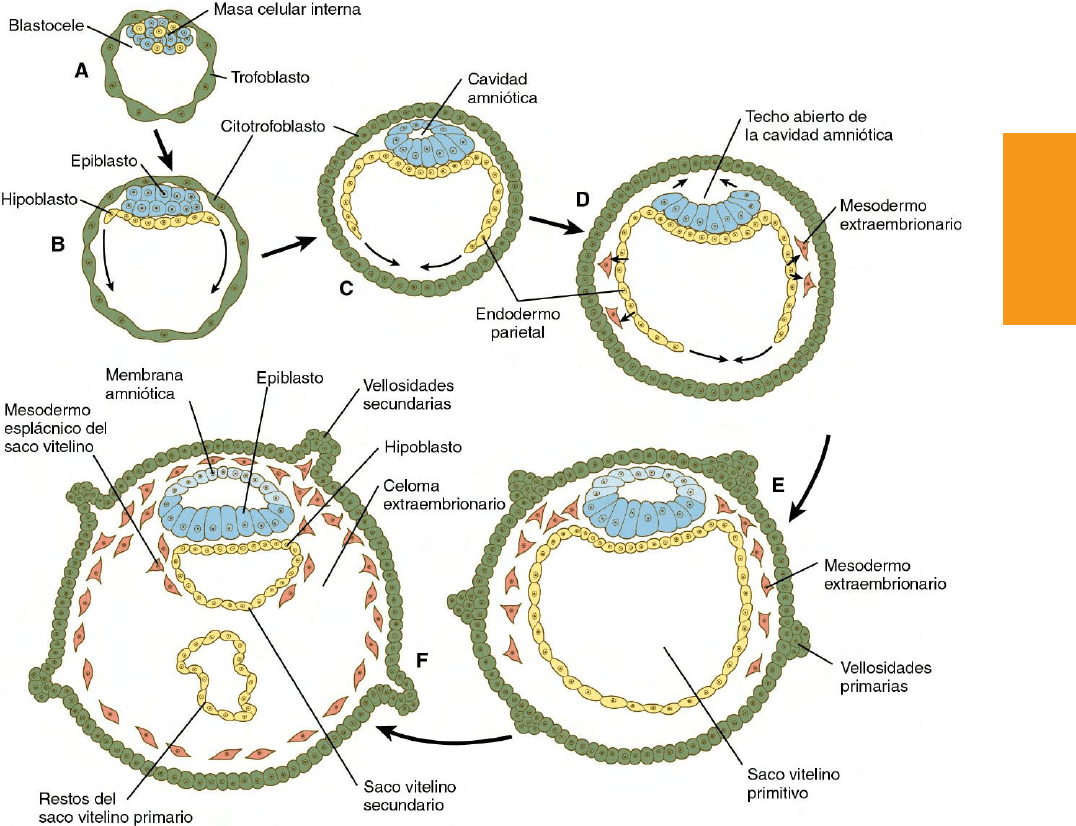
Fig. 5.2 Orígenes de los principales tejidos extraembrionarios. No se muestra el sincitiotrofoblasto. A, Blastocisto tardío. Dentro de la masa celular
interna, azul, células preepiblásticas que expresan nanog y amarillo y células prehipoblásticas que expresan Gata-6 mezclándose en un patrón de sal y
pimienta. B, Comienzo de la implantación a los 6 días. El hipoblasto se ha formado y está empezando a extenderse por debajo del citotrofoblasto como
endodermo parietal. C, Blastocisto implantado a los 7½ días. D, Blastocisto implantado a los 8 días. E, Embrión a los 9 días. F, Final de la segunda semana.
78 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
la placa precordal y el nódulo primitivo) y también el endodermo
embrionario. La combinación de los resultados de dichos expe-
rimentos de marcaje ha permitido la elaboración de mapas de
destino, tales como el que se ilustra en la figura 5.5A.
Las células precursoras endodérmicas que pasan a través de
la parte anterior de la línea primitiva desplazan en gran medida
el hipoblasto original, aunque investigaciones recientes han
demostrado que algunas de las células hipoblásticas originales
se integran en la capa de endodermo embrionario de reciente
formación. Las células hipoblásticas desplazadas forman endo-
dermo extraembrionario. El movimiento de las células a través
de la línea primitiva da lugar a la formación de un surco (surco
primitivo) a lo largo de la línea media de dicha estructura. En
el extremo anterior de la línea primitiva se sitúa una acumula-
ción celular pequeña pero bien definida, denominada nódulo
primitivo o nódulo de Hensen*. Esta estructura tiene una gran
importancia en el desarrollo debido a que, además de ser el ma-
yor centro señalizador posterior (cuadro 5.1), es el área a través
de la que migran las células en una corriente hacia el extremo
anterior del embrión. Estas células, llamadas mesendodermo,
pronto se separan en una estructura mesodérmica en forma de
barra constituyendo la notocorda y el endodermo de la pared
dorsal del intestino en formación. En situación anterior a la no-
tocorda existe un grupo de células mesodérmicas denominado
placa precordal (v. fig. 5.5A y B). (Las relevantes funciones de
la notocorda y de la placa precordal se exponen en la pág. 80.)
Las características específicas craneocaudales de las es-
tructuras derivadas del recientemente formado mesodermo
*La denominación de nódulo de Hensen es la que se suele utilizar para indicar el nódulo
primitivo del embrión de las aves, aunque también se usa a veces en la literatura em-
briológica de los mamíferos. Este nódulo es el equivalente estructural y funcional del labio
dorsal del blastoporo de los anfibios.
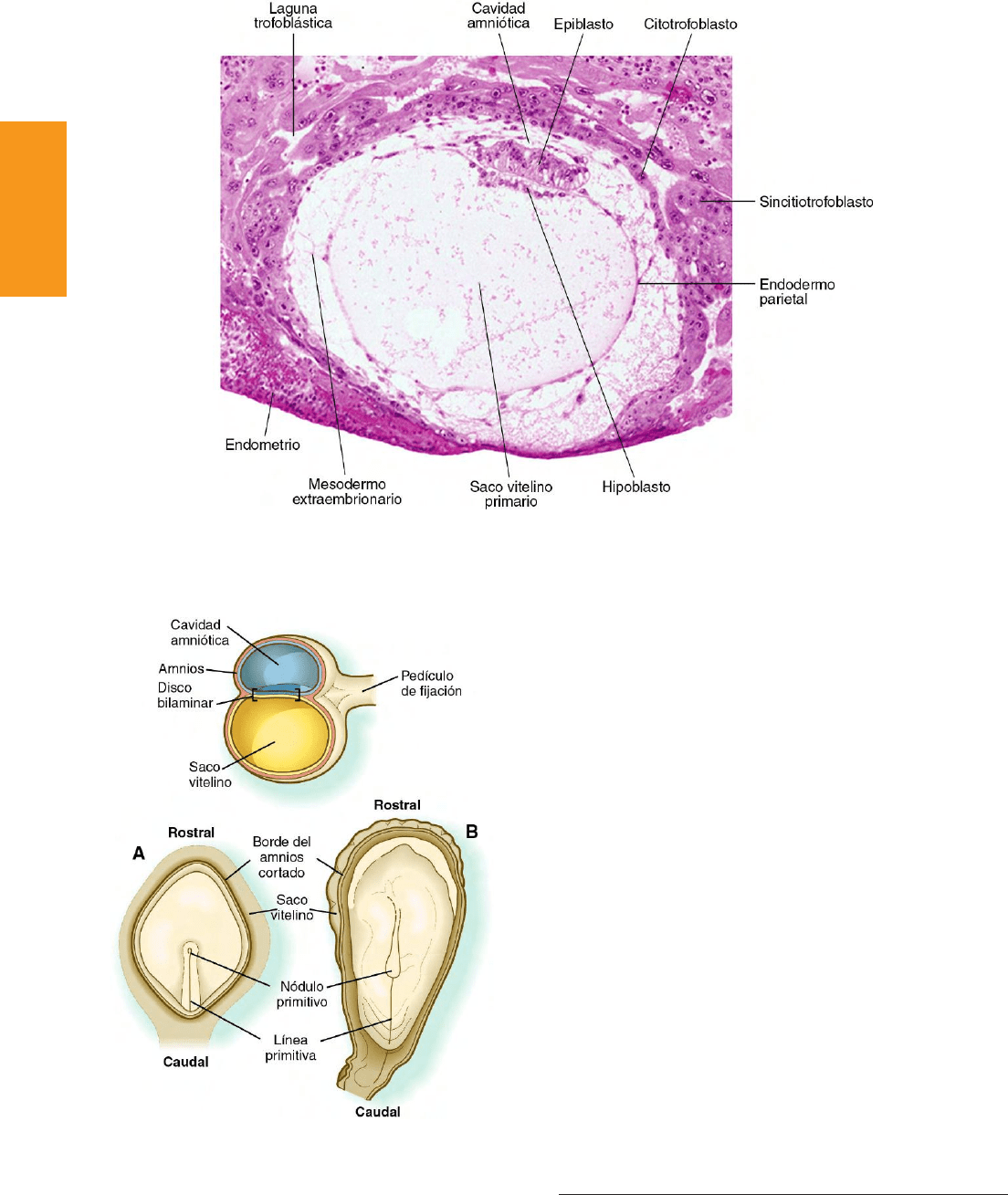
Fig. 5.4 Visión dorsal de embriones humanos a los 16 días (A) y a los 18
días (B). Parte superior, corte sagital de un embrión y de sus membranas
extraembrionarias durante la fase inicial de la gastrulación.
Fig. 5.3 Microfotografía digital de un embrión humano de 12 días de desarrollo (Carnegie N.° 7700) tomada dentro del endometrio cuando la im-
plantación se ha completado. (Cortesía del Dr. Ray Gasser.)
Capítulo 5—Formación de las capas germinales y sus primeros derivados 79
© Elsevier. Fotocopiar sin autorización es un delito.
paraaxial son especificadas por patrones de expresión de genes
Hox, primero en el epiblasto y después en las propias células
mesodérmicas. Las transformaciones de la morfología y del
comportamiento de las células que atraviesan la línea primitiva
se asocian a cambios profundos no sólo en sus propiedades de
adhesión y en su organización interna, sino también en la forma
en que se relacionan con su ambiente externo. La mayor parte
de este último compone el pedículo de fijación, que conecta la
parte caudal del embrión a los tejidos extraembrionarios que
lo rodean (v. figs. 5.4 y 7.1). Más tarde el pedículo de fijación
se convierte en el cordón umbilical.
Los movimientos de las células que atraviesan la línea pri-
mitiva están acompañados de cambios sustanciales en su es-
tructura y organización (fig. 5.6). Mientras permanecen en
el epiblasto, estas células poseen las propiedades de células
epiteliales típicas, con superficies apical y basal bien definidas,
y aparecen asociadas a una lámina basal subyacente al epiblas-
to. Cuando se introducen en la línea primitiva estas células se
elongan, pierden su lámina basal y adoptan una morfología
característica que ha hecho que se las denomine células en
botella. Cuando se separan de la capa epiblástica en el surco
primitivo, dichas células en botella adoptan la morfología y las
características de las células mesenquimatosas, que pueden
migrar como células aisladas si se da el ambiente extracelular
adecuado (v. fig. 5.6). Esta transformación incluye la pérdida
de moléculas de adhesión celular específicas (CAM), particu-
larmente E-cadherina (v. pág. 254), a medida que las células
pasan de una configuración epitelial a una mesenquimatosa.
Esta transformación se relaciona con la expresión del factor
de transcripción snail, que también es activo en el paso de
células epiteliales de cresta neural del tubo neural a células
mesenquimatosas (v.
pág. 254). Como las células del epiblasto
están experimentando una transición epitelio-mesénquima,
comienzan a expresar la CAM N-cadherina, que es necesaria
para su desplazamiento desde la línea primitiva a la nueva capa
de mesodermo.
Desde el inicio de la gastrulación las células del epiblasto
comienzan a producir ácido hialurónico, que se introduce
en el espacio que queda entre el epiblasto y el hipoblasto. Este
ácido es un polímero constituido por subunidades repetidas
de ácido d-glucurónico y de n-acetilglucosamina, y se asocia a
menudo con la migración celular en los sistemas en desarro-
llo. Esta molécula tiene una capacidad tremenda para retener
agua (hasta 1.000 veces su propio volumen), y su efecto es el de
impedir la agregación de las células mesenquimatosas durante
la migración celular. Aunque las células mesenquimatosas del
mesodermo embrionario se encuentran en un ambiente rico
en ácido hialurónico desde que abandonan la línea primitiva,
dicho ácido solo no es capaz de mantener la migración de es-
tas células desde la línea primitiva. En todos los embriones de
vertebrados investigados hasta el momento, la migración de las
células mesodérmicas desde la línea primitiva o la estructura
equivalente parece depender de la presencia de fibronectina,
asociada a la lámina basal por debajo del epiblasto. Finalmente,
el mesodermo embrionario se extiende lateralmente como una
fina sábana de células mesenquimatosas entre el epiblasto y el
hipoblasto (v.
fig. 5.5C).
En el momento en el que el mesodermo ha formado una capa
bien definida en el embrión humano, la capa germinal superior
(resto del epiblasto inicial) se denomina ectodermo, mientras
que la germinal inferior, que ha desplazado al hipoblasto origi-
nal, se conoce como endodermo. Ésta es la terminología que se
va a utilizar en el resto del texto. Cuando se están formando las
tres capas germinales, las señales de la proteína morfogénica
ósea 4 (BMP-4), derivadas de tejidos extraembrionarios en el
extremo caudal del embrión, estimula a un grupo de células en
la región posterior del epiblasto a ser transformado en células
germinales primordiales.
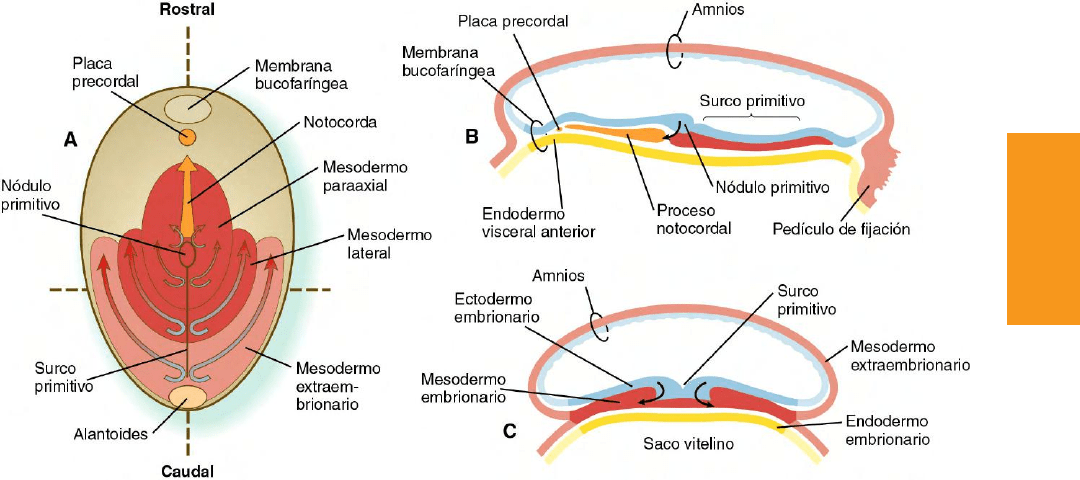
Fig. 5.5 A, Visión dorsal de un embrión humano durante la gastrulación. Las flechas muestran las direcciones de los movimientos celulares a lo largo
del epiblasto hacia la línea primitiva, a través de ella y alejándose de ella, ya como mesodermo recién formado. Los destinos de las células que han
atravesado la línea primitiva y que aparecen en la ilustración están basados en estudios efectuados en embriones de ratón. B, Corte sagital a lo largo del
eje rostrocaudal del mismo embrión. La flecha curvada indica las células que pasan a través del nódulo primitivo hacia la notocorda. C, Corte transversal
a través de la línea primitiva en A (líneas discontinuas).
80 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
Regresión de la línea primitiva
Tras su aparición inicial en el extremo caudal del embrión, la línea
primitiva experimenta una expansión rostral aproximadamente
hasta el día 18 después de la fecundación (v. fig. 5.4). A partir de
ese momento regresa caudalmente (v. fig. 5.11), tirando de la
notocorda en su regresión. En la cuarta semana todavía quedan
vestigios de la línea primitiva. Durante esta fase, la formación
del mesodermo continúa mediante las células que migran des-
de el epiblasto a través del surco primitivo. La regresión de la
línea primitiva se acompaña del establecimiento y modelado del
mesodermo paraaxial (v. pág. 97), del que se originan los somitos
y ulteriormente las estructuras axiales del tronco y de las regiones
caudales del cuerpo. Cuando la regresión de la línea primitiva
termina, su parte más caudal se caracteriza por una masa de
células mesenquimatosas, denominada masa celular caudal
(tail bud). Esta estructura representa un papel importante en la
formación de la porción más caudal del tubo neural (v. pág. 93).
La línea primitiva suele desaparecer sin dejar rastro, pero en
algunos casos muy poco frecuentes aparecen tumores de gran
tamaño denominados teratomas en la región sacrococcígea
(v. fig. 1.2A). Los teratomas contienen a menudo mezclas grotescas
de numerosos tipos de tejidos, tales como cartílago, músculo,
tejido adiposo, pelo y tejido glandular. Debido a ello, los teratomas
sacrococcígeos parecen originarse a partir de restos de la línea pri-
mitiva (que pueden formar todas las capas germinales). También
es posible encontrar teratomas en las gónadas y en el mediastino.
Estos tumores aparentemente proceden de células germinales.
Notocorda y placa precordal
La notocorda, la estructura por la que se da la denominación
de Cordados al filum al que pertenecen todos los vertebrados, es
una estructura cilíndrica celular que discurre a lo largo del eje
longitudinal del embrión, con una localización inmediatamente
ventral al sistema nervioso central. Aunque tanto desde el punto
de vista filogenético como ontogenético actúa como el soporte
longitudinal inicial del cuerpo, la notocorda también desempeña
una función fundamental como principal mecanismo iniciador
de una serie de episodios de señalización (inducciones), que
transforman las células embrionarias no especializadas en tejidos
y órganos definitivos. En concreto, las señales de inducción
procedentes de la notocorda: 1) estimulan la conversión del ecto-
dermo superficial que la cubre en tejido neural, 2) especifican la
identidad de determinadas células (placa del suelo) en el sistema
nervioso inicial, 3) transforman ciertas células mesodérmicas de
los somitos en cuerpos vertebrales y 4) estimulan las primeras
fases del desarrollo del páncreas dorsal.
Rostralmente a la notocorda se localiza una pequeña región
donde coinciden el ectodermo y el endodermo embrionarios
sin que entre ellos haya mesodermo. Denominada membrana
bucofaríngea (v.
fig. 5.5), esta estructura marca el lugar de la
futura cavidad bucal. Entre el extremo rostral de la notocorda
y la membrana bucofaríngea existe una pequeña acumulación
de células mesodérmicas estrechamente relacionadas con el
endodermo, que se llama placa precordal (v. fig. 5.5). En aves,
la placa precordal emite señales moleculares para estimular la
formación del prosencéfalo, similar al papel representado por
el endodermo anterior en mamíferos.
Tanto la placa precordal como la notocorda se originan a partir
de la entrada en el nódulo primitivo de una población de células
epiblásticas, que se unen a otras células originadas en la línea
primitiva. A medida que la línea primitiva sufre regresión, los
precursores celulares de la placa precordal en primer lugar y de la
notocorda en segundo lugar migran rostralmente desde el nódulo,
permaneciendo después como una agrupación cilíndrica de células
(proceso notocordal; v. fig. 5.5A y B) en la estela que deja la línea
primitiva en regresión. En los mamíferos, al poco tiempo de la en-
trada mencionada, las células del proceso notocordal se expanden
temporalmente y se fusionan con el endodermo embrionario
(fig. 5.7). El resultado es la formación de un canal neuroentérico
transitorio que conecta la cavidad amniótica en desarrollo con
el saco vitelino. Más tarde, las células de la notocorda se separan
del techo endodérmico del saco vitelino y forman la notocorda
definitiva, un cilindro macizo de células situado en la línea media
entre el ectodermo y el endodermo embrionarios (v. fig. 5.7).
Inducción del sistema nervioso
Inducción neural
La relación de inducción entre la notocorda (cordamesodermo)
y el ectodermo que la cubre en la génesis del sistema nervioso
ya fue descubierta a principios del siglo xx. Aunque los expe-
rimentos originales se realizaron en anfibios, otros similares
efectuados en vertebrados superiores han demostrado que los
elementos esenciales de la inducción neural (o primaria) son
los mismos en todos los vertebrados.
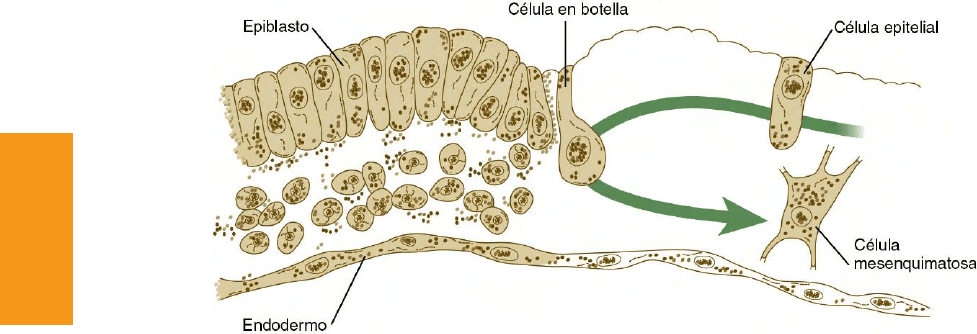
Fig. 5.6 Esquema de un corte transversal de un embrión durante la gastrulación. Cambios en la morfología de una célula a medida que migra
a lo largo del epiblasto (epitelio), a través de la línea primitiva (célula en botella) y alejándose del surco como célula mesenquimatosa que formará parte
de la capa germinal mesodérmica. Esta misma célula puede más adelante asumir una configuración epitelial como parte de un somito.
Capítulo 5—Formación de las capas germinales y sus primeros derivados 81
© Elsevier. Fotocopiar sin autorización es un delito.
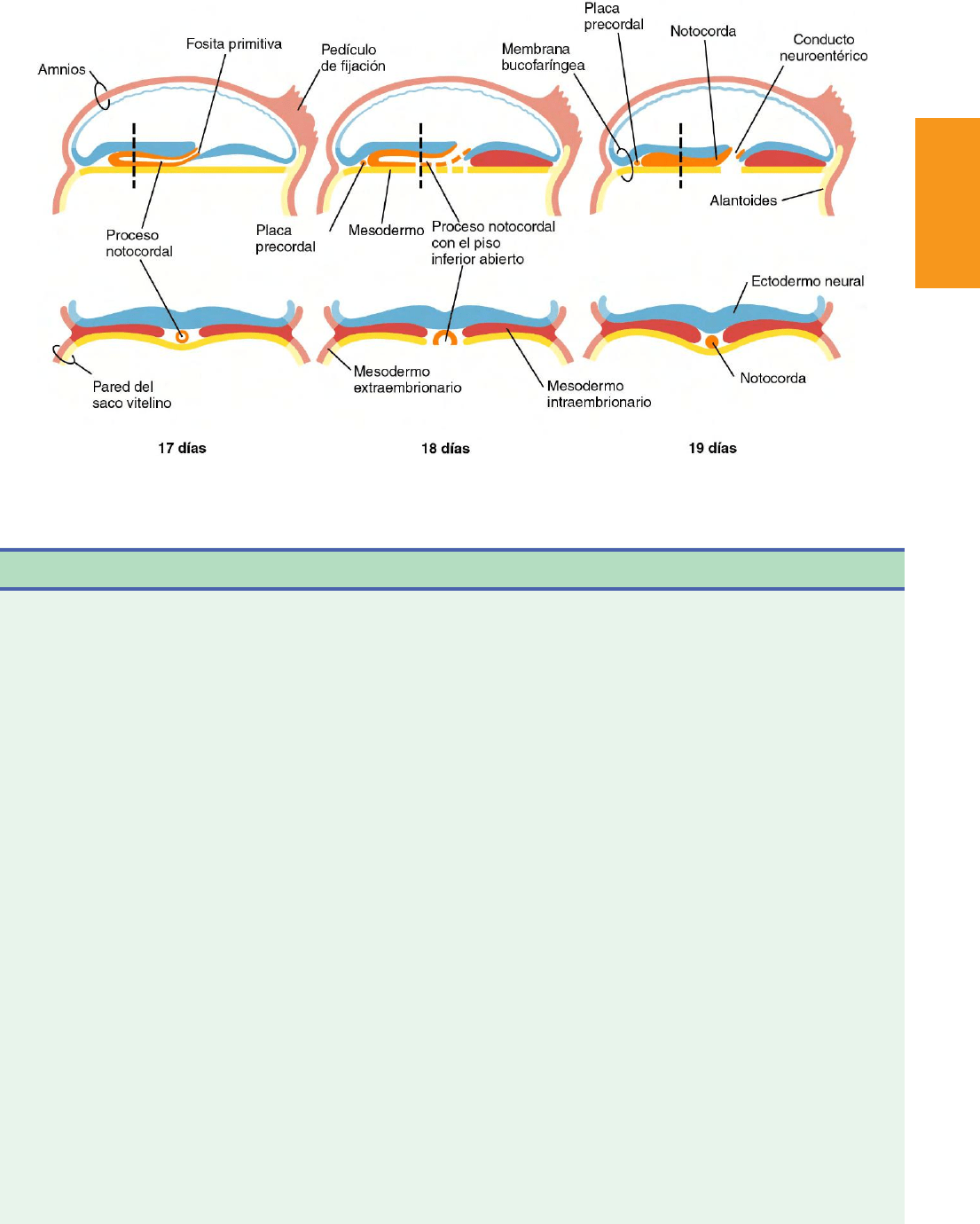
Fig. 5.7 De izquierda a derecha, fases secuenciales en la formación de la notocorda. Parte superior, cortes sagitales. Parte inferior, Cortes transversales
a nivel de la línea vertical de la figura superior. En la fila superior, el extremo rostral queda a la izquierda. La función del canal neuroentérico no ha sido
determinada.
Cuadro 5.1 Aspectos moleculares de la gastrulación
Muchos decenios de investigación en aves y anfibios han permitido
obtener un conocimiento aceptable acerca de los aspectos celulares
y moleculares de la gastrulación en estas especies. La investigación
más reciente indica que, a pesar de ciertas diferencias entre las es-
pecies, los aspectos básicos de la gastrulación en los mamíferos son
en esencia similares a los de las aves.
Los procesos que tienen lugar en la gastrulación están guiados
por una serie de inducciones moleculares que proceden de una
sucesión de centros señalizadores comenzando por el endodermo
visceral anterior y progresando hacia la futura parte caudal (pos-
terior) del embrión. Las señales posteriores iniciales desembocan en
la formación de la línea primitiva y en la inducción del mesodermo.
Una vez que se establece la línea primitiva, el nódulo primitivo toma
el control como el centro organizador de la estructura fundamental
del eje corporal. A medida que la notocorda se va constituyendo a
partir de las células que atraviesan el nódulo primitivo, se convierte
en un importante centro señalizador. En humanos permanece poco
claro el papel de las células de la placa precordal. En aves la placa
precordal actúa como un centro señalizador anterior, parecido al
endodermo visceral anterior del ratón. Si las señales anteriores en
humanos conciernen al hipoblasto anterior (endodermo visceral
anterior) o a la placa precordal, o a los dos, queda por resolver.
Establecimiento del endodermo visceral anterior
e inducción de la línea primitiva (el organizador inicial
de la gastrulación)
Este aspecto del desarrollo inicial depende casi con exclusividad de
estudios llevados a cabo en el embrión de ratón. La simetría original
del embrión queda destruida por el desplazamiento del futuro endo-
dermo visceral anterior hacia la zona anterior del disco embrionario.
Existe una fase de proliferación y posterior migración celular que
formará el endodermo visceral anterior. La migración de estas células
(y el establecimiento resultante del eje anteroposterior) depende
de la activación del antagonista de Wnt, Dkk 1 (Dickkopf 1) en la
futura región anterior del embrión. Esto limita la actividad de Wnt
a la futura región posterior del embrión, donde induce la expresión
de la molécula señalizadora Nodal (
fig. 5.8A). Cuando el endo-
dermo visceral anterior queda estabilizado en la región anterior del
disco embrionario produce los inhibidores de Nodal, lefty-1 y Cer-1,
lo cual limita la actividad de Nodal al extremo posterior del embrión
donde, respondiendo a las señales de Wnt, queda establecido un
centro señalizador posterior que induce la formación de la línea
primitiva y del mesodermo. En el embrión de pollo la aplicación
ectópica de otras dos moléculas señalizadoras, cordina y Vg1,
inducen la formación de una línea primitiva ectópica.
El nódulo primitivo (organizador)
A medida que la línea primitiva se alarga, las células que migran del
epiblasto se unen a su extremo anterior, haciéndose evidente una
masa dinámica de células llamada nódulo primitivo. Las células
del nódulo expresan muchos genes, entre ellos tres marcadores
moleculares clásicos de la región organizadora de muchos vertebra-
dos: cordina, goosecoid y el factor nuclear hepático-3b (ahora
llamado Foxa-2). No sólo es importante para la formación del propio
nódulo el factor de transcripción en hélice alada Foxa-2, sino también
es de vital importancia para el establecimiento de las estructuras de
la línea media situadas craneal al nódulo. Se requiere Foxa-2 para la
iniciación de la función de la notocorda. En su ausencia, la noto-
corda y la placa de piso del tubo neural (v.
cap. 11) no se forman.
Por el contrario, el endodermo, la línea primitiva y el mesodermo
intermedio se desarrollan. Goosecoid, un factor de transcripción
de homeodominio, se expresa predominantemente en la región del
organizador de todos los vertebrados estudiados. Goosecoid activa
cordina, noggin y otros genes de la región organizadora. Cuando se
(Continúa)
82 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
expresa de manera ectópica estimula la formación de un eje corporal
secundario. Las moléculas de señalización asociadas con el nódulo,
cordina y noggin, están involucradas en la inducción neural, y la
expresión de nodal en el lado izquierdo del embrión es un elemento
clave en la configuración de la asimetría izquierda-derecha.
Existen dos genes, T y nodal, que desempeñan papeles importan-
tes en la función de la línea primitiva y la formación del mesodermo
posterior. La expresión del gen T parece ser activada por los produc-
tos de los genes Foxa-2 y goosecoid. En los mutantes T (braquiuria),
la notocorda comienza a formarse por la actividad de Foxa-2, pero
no puede completar su desarrollo. Estudios sobre mutantes T han
demostrado que es necesaria la actividad del gen brachyury para los
movimientos normales durante la gastrulación de las futuras células
mesodérmicas a través de la línea primitiva. En los ratones mutantes
braquiuria (con cola corta), las células del mesodermo se acumulan
en una línea primitiva malformada, y los embriones muestran una
defectuosa elongación del eje del cuerpo (incluyendo una cola corta)
posterior a las extremidades anteriores. Mutantes del gen T pueden
ser en humanos los responsables de ciertos defectos groseros de la
porción caudal del cuerpo. Nodal, un miembro del factor de cre-
cimiento transformante b (TGF-b) de la familia de genes del factor
de crecimiento (v.
tabla 4.1), se expresa en todo el epiblasto pos-
terior antes de la gastrulación, durante la gastrulación su actividad
se concentra en el nódulo primitivo. Lo mismo que en el caso del
gen brachyury, los efectos de nodal se ven fuertemente en la región
caudal del embrión. En el mutante nulo de nodal, la línea primitiva
no se forma, y el embrión es deficiente en mesodermo. Del mismo
modo, los mutantes de cripto, un miembro primitivamente activo de
la familia del factor de desarrollo epidérmico y un cofator esencial
en la vía de señalización de nodal, producen un fenotipo sin tronco.
Cuando las células pasan a través de la línea primitiva, una re-
gión de expresión de genes Hox comienza a formarse alrededor
de dicha línea. El patrón de expresión de genes Hox en el futuro
tronco y parte posterior del embrión se basa en la señalización de
tres moléculas –ácido-retinoico, Wnt y FGF– que actúan sobre el
factor de transcripción Cdx (el equivalente en mamíferos de caudal
en Drosophila) en el área de la línea primitiva en regresión, justo
detrás de los últimos somitos en formación. Cdx actúa sobre los
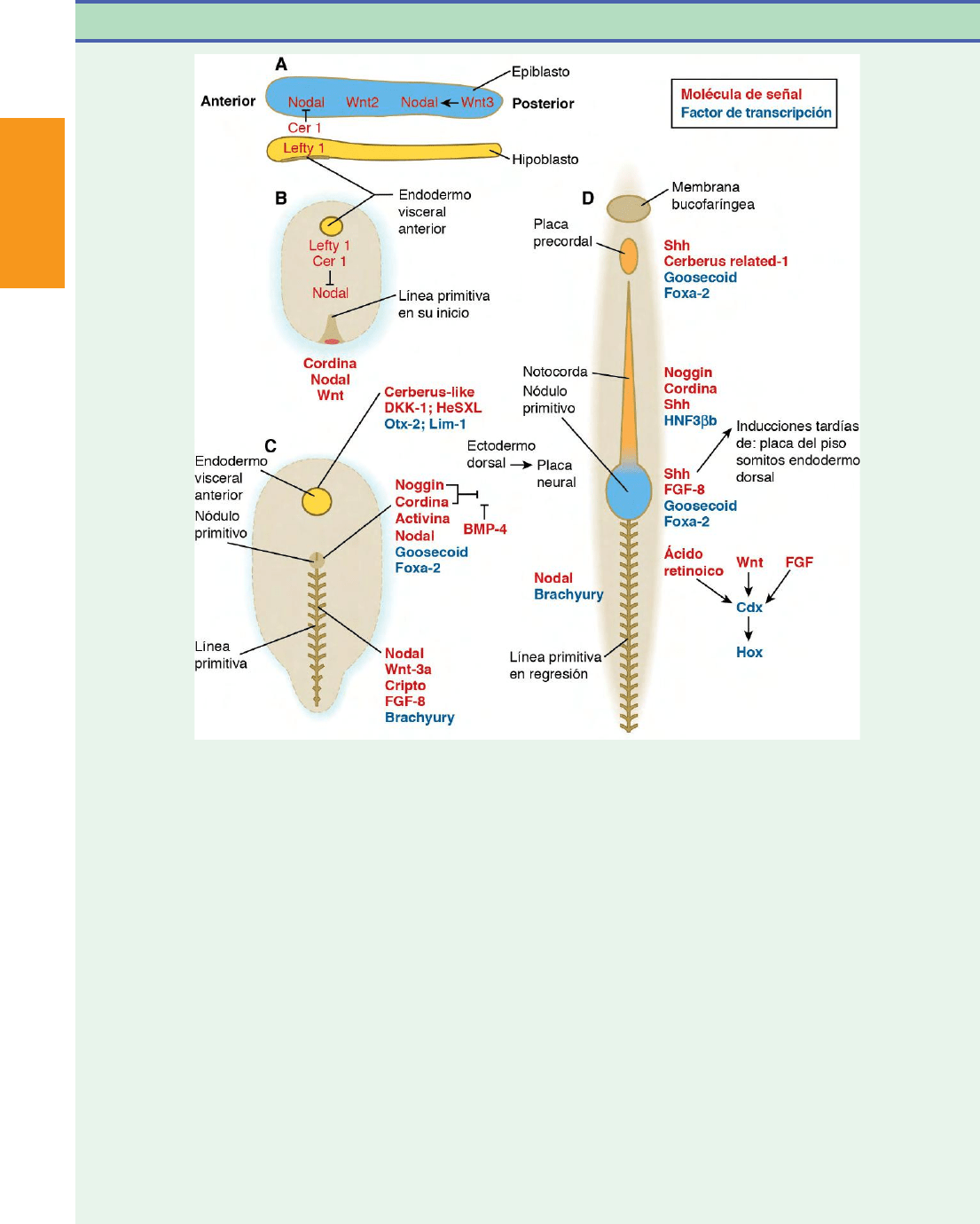
Fig. 5.8 Resumen de los principales genes implicados en diversas fases del desarrollo embrionario inicial. A, Línea preprimitiva (corte
sagital). B, Formación inicial de la línea primitiva. C, Gastrulación (período de formación de las capas germinales). D, Gastrulación tardía e inducción
neural. Las moléculas en rojo son moléculas de señalización, y las de color azul son factores de transcripción. Los nombres de moléculas específicas
(en negrita) están situados sobre las estructuras que las expresan.
Cuadro 5.1 Aspectos moleculares de la gastrulación (cont.)

Capítulo 5—Formación de las capas germinales y sus primeros derivados 83
© Elsevier. Fotocopiar sin autorización es un delito.
Los experimentos de deleción y trasplante llevados a cabo
en anfibios establecieron el fundamento para el conocimiento
actual de la inducción neural. (V. caps. 6 y 11 para más detalles
sobre la formación del sistema nervioso.) En ausencia del corda-
mesodermo que se desplaza desde el labio dorsal del blastoporo
(el equivalente en los anfibios del nódulo primitivo), el sistema
nervioso no se origina a partir del ectodermo dorsal. Por otra
parte, si el labio dorsal del blastoporo se injerta bajo el ectodermo
ventral de otro embrión anfitrión, se forman un sistema nervioso
y un eje corporal secundarios en la zona del injerto (
fig. 5.10).
El labio dorsal ha sido denominado el organizador, debido
a su capacidad para estimular la formación de un eje corporal
secundario. En estudios posteriores se ha demostrado que las
interacciones que tienen lugar en la región del labio dorsal de los
anfibios son mucho más complejas que una simple inducción
entre el cordamesodermo y el ectodermo. También se han efec-
tuado experimentos de deleción y trasplante en embriones de
aves y mamíferos (v. fig. 5.10); claramente, el nódulo primitivo
y el proceso notocordal en las aves y los mamíferos tienen una
función homóloga a la del labio dorsal y el cordamesodermo
genes Hox, que imponen las características propias de las estructuras
segmentarias que se forman a lo largo del eje anteroposterior del
embrión (
fig. 5.8D).
La placa precordal y la notocorda
Las primeras células que pasan a través del nódulo primitivo forman
una masa celular discreta en la línea media, la placa precordal,
estrechamente asociada con el endodermo en la región inmediata-
mente caudal a la membrana bucofaríngea. La próxima generación
de células que pase a través del nódulo formará la notocorda.
La notocorda es un importante centro de señalización axial
del tronco en el embrión inicial, y es importante en la formación
de muchas estructuras axiales. Bajo la influencia de Foxa-2 y goo-
secoid, las células de la notocorda en formación producen noggin
y cordina, moléculas conocidas por ser unas potentes inductoras
neurales en muchas especies. La notocorda también produce Sonic
hedgehog (shh), la molécula efectora para muchas inducciones
de estructuras axiales posterior a la inducción de la placa neural.
La notocorda no estimula la formación de partes anteriores como
el cerebro u otras estructuras cefálicas, a pesar de la inducción de
la placa neural en el ectodermo suprayacente. Esta función está
reservada para el endodermo anterior visceral.
La placa precordal, a veces llamada organizador cefálico, está
formada por células mesendodérmicas que son las que primero
pasan por el nódulo primitivo. Estas células están estrechamente aso-
ciadas estructural y funcionalmente con las células del endodermo
anterior subyacente. Junto con el endodermo anterior visceral (v. más
adelante), la placa precordal es una fuente de señales importantes,
especialmente shh, que están implicadas en la ventralización del
cerebro anterior. Además, la placa precordal es fuente de señales
importantes para la supervivencia de las células de la cresta neural
que emigran tempranamente desde el cerebro anterior.
Endodermo visceral anterior (hipoblasto)
En los mamíferos, incluso antes de que las células del mesodermo
comiencen a migrar a través del nódulo primitivo, el hipoblasto
anterior (llamado el endodermo visceral anterior por embriólogos
dedicados al estudio del ratón) expresa los genes característicos
de la placa precordal e inicia la formación de la cabeza. El propio
endodermo anterior visceral se subdivide en una parte anterior, que
sirve como un centro de señalización para la formación inicial del
corazón (v.
pág. 104), y una zona más posterior, que se convierte
en parte del complejo de la placa precordal e induce la formación
de la cabeza. De acuerdo con un modelo, la inducción de la cabeza
y el cerebro anterior en los mamíferos es un proceso de dos pasos,
en el que una inducción inicial procedente del endodermo visceral
anterior confiere un carácter anterior lábil para la cabeza y el cerebro,
y una inducción posterior procedente del mesodermo de la placa
precordal refuerza y mantiene esta inducción.
Una función importante del endodermo anterior visceral es emitir
señales moleculares que inhiben el desarrollo de estructuras embrio-
narias posteriores. Para producir una cabeza es necesario bloquear
la señal de la proteína morfogénica ósea 4 (BMP-4) (por noggin) y
otra de Wnt (por Dkk-1). Moléculas de señalización y factores de
transcripción son producidos en centros cefálicos de señalización. En
ratones portadores de mutantes de Lim-1 (Lhx-1), un factor de trans-
cripción que contiene homeobox, y cerberus-like 1, una molécula
de señalización, los ratones nacen sin cabeza (
fig. 5.9). Los ratones
sin cabeza nacen sin estructuras neurales anteriores al rombómero 3
(v. fig. 6.3). Otx-2, otro factor de transcripción presente en el centro
de señalización cefálico, es también un marcador general de la
región anterior inducida del sistema nervioso central. Muchas otras
moléculas también se expresan en el centro de señalización cefálico.
Queda por determinar cómo producen la formación de la cabeza.
Cuadro 5.1 Aspectos moleculares de la gastrulación (cont.)
Fig. 5.9 Ratones recién nacidos sin cabeza junto a un ratón
normal. Los ratones sin cabeza son mutantes nulos del gen Lim-1.
(De Shawlot W, Behringer RR: Nature 374:425-430, 1994.)
84 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
en los anfibios. Esto quiere decir que en los vertebrados supe-
riores el nódulo primitivo y el proceso notocordal actúan como
inductores neurales, mientras que el ectodermo que queda por
encima es el tejido de respuesta. Durante muchos años, los em-
briólogos han dedicado un esfuerzo enorme de investigación a
identificar la naturaleza de la señal de inducción que pasa desde
el cordamesodermo hasta el ectodermo.
Los primeros intentos de determinar la naturaleza del es-
tímulo de inducción se caracterizaron por un gran optimismo.
Ya en la década de 1930, varios laboratorios habían propuesto
que el estímulo de inducción consistía en moléculas tan diversas
como ciertas proteínas y esteroides. Al poco tiempo tuvo lugar
el descubrimiento de que la inducción neural podía producirse
incluso por una variedad más amplia de estímulos, que incluía a
los iones inorgánicos o a los tejidos muertos. Con esta plétora de
posibles inductores, la atención se dirigió a las propiedades del
tejido de respuesta (el ectodermo dorsal) y a sus posibles formas
de reacción frente al estímulo inductor a través de una vía final
común. La búsqueda de las moléculas de inducción neural y de su
mecanismo de acción ha sido compleja y frustrante, con muchos
callejones sin salida y con recodos equivocados en el camino.
Algunos laboratorios observaron que el ectodermo ais-
lado podía responder in vitro a los estímulos de inducción y
transformarse en tejido neural. Una técnica muy útil para el
estudio de la inducción in vitro implicaba la separación entre
el tejido de respuesta y el inductor por un filtro con poros que
permitía el paso de moléculas pero no de células. Esta técnica
ha sido utilizada en el análisis de diversos sistemas de inducción
en los mamíferos.
Varios estudios experimentales de manipulación han mostra-
do claramente que la inducción neural no es un simple proceso
de todo o nada, sino que, antes bien, existe una especificidad
regional considerable (p. ej., ciertos inductores artificiales es-
timulan la formación de las estructuras neurales más anteriores,
mientras que otros lo hacen respecto a las más posteriores).
En embriones de anfibios, el cordamesodermo anterior tiene
propiedades de inducción diferentes a las del posterior.
En estudios de investigación recientes se han identificado
moléculas específicas que dan lugar a la inducción neural. En
los anfibios, los agentes de inducción son tres moléculas de señal
(noggin, folistatina y cordina) producidas por la notocorda.
Al principio se pensó que estas moléculas estimulaban directa-
mente a células no comprometidas del ectodermo dorsal para
la formación de tejido neural, pero en estudios de investigación
posteriores realizados sobre anfibios se ha demostrado que estos
inductores actúan mediante el bloqueo de la acción de un inhibi-
dor BMP-4, en el ectodermo dorsal. En ausencia de actividad de
la BMP-4, el ectodermo dorsal forma tejido neural por defecto.
Nuestra idea actual sobre la inducción neural, en mamíferos, se
corresponde con un esquema bastante complejo, tanto en la loca-
lización como en el momento de las interacciones inductivas que
tienen un papel en definir el inicio y la organización del sistema
nervioso central. De acuerdo con un punto de vista más moder-
no, durante el estadio inicial de línea primitiva, el precursor del
nódulo primitivo llamado organizador de la gástrula segrega
Cer-1, un inhibidor de BMP. En ausencia de actividad BMP, la zo-
na anterior del epiblasto es inducida a convertirse, por defecto, en
tejido neural anterior. En estadios posteriores de la gastrulación el
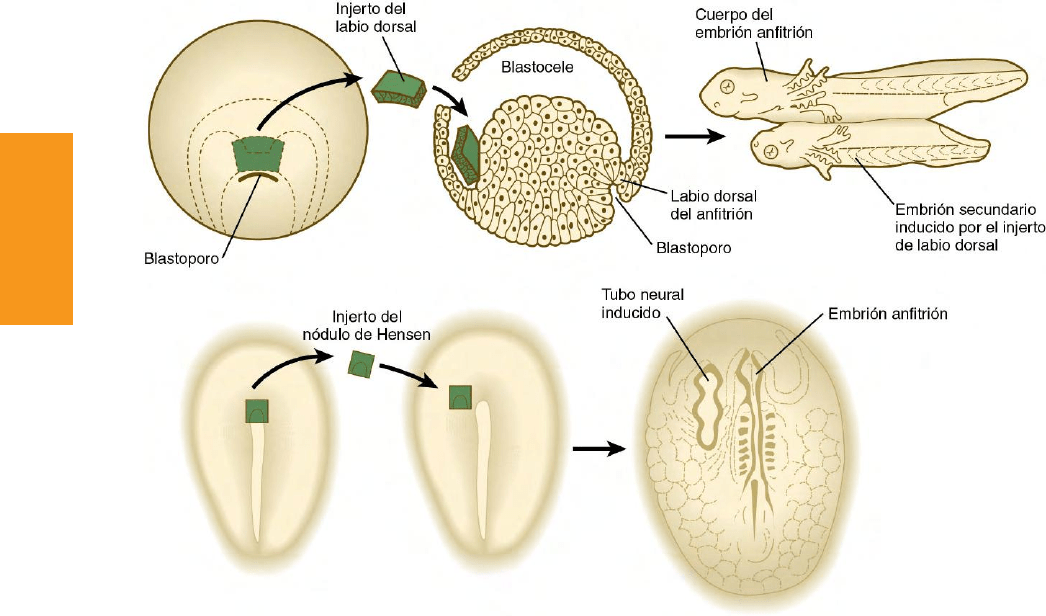
Fig. 5.10 Experimentos iniciales que muestran la inducción neural. Parte superior, el injerto del labio dorsal del blastoporo en un embrión de
salamandra induce la formación de un embrión secundario. Parte inferior, el injerto del nódulo de Hensen de un embrión de ave en otro embrión induce
la formación de un tubo neural secundario. (Parte superior basada en estudios de Spemann H: Embryonic development and induction, Nueva York, 1938, Hafner; parte
inferior basada en estudios de Waddington C: J Exp Biol 10:38-46, 1933).
Capítulo 5—Formación de las capas germinales y sus primeros derivados 85
© Elsevier. Fotocopiar sin autorización es un delito.
carácter anterior del tejido neural inducido se mantiene primero
mediante señales que proceden del endodermo visceral anterior
(o su equivalente en humano) y luego por señales que proceden
del mesendodermo anterior (notocorda y placa precordal). Estas
señales son Cer-1, un inhibidor de BMP, y lefty-1, un inhibidor
de nodal cuya influencia es posteriorizante.
A medida que la gastrulación se desarrolla y el nódulo primitivo
toma forma, éste induce al epiblasto a formar tejido neural a través
de un mecanismo similar al de inhibición de BMP. Este tejido neu-
ronal inducido adquiere un carácter posterior a través de la acción
de nodal, que se concentra en el extremo posterior del embrión.
Formación inicial de la placa neural
La primera respuesta morfológica obvia del embrión frente a la
inducción neural es la transformación del ectodermo dorsal que
queda por encima del proceso notocordal en una placa alargada de
células epiteliales engrosadas, denominada placa neural (
fig. 5.11).
El límite de la placa neural se especifica por la exposición de las
células que ocupan esa zona a una cierta concentración de BMP.
Ésta es la región de la que surgirá la cresta neural (v. pág. 254).
Tras la formación de dicha placa neural, la capa germinal
ectodérmica queda subdividida en dos linajes de desarrollo: uno
neural y otro no neural. Este ejemplo ilustra varios conceptos
fundamentales en el desarrollo: la restricción, la determinación
y la diferenciación. El cigoto y las blastómeras resultantes del
primer par de divisiones de la segmentación son totipotentes
(es decir, capaces de formar cualquier célula del organismo).
A medida que progresa el desarrollo, se producen varias
decisiones que reducen las opciones de desarrollo de estas
células (
fig. 5.12). Por ejemplo, en fases iniciales de la segmen-
tación, algunas células quedan comprometidas en la línea del
trofoblasto extraembrionario y ya no pueden participar en la
formación del embrión mismo. En el punto en que las células
se comprometen para dar lugar al trofoblasto ha tenido lugar
un proceso de restricción. Cuando un grupo celular ha pasado
su último proceso de restricción (p. ej., la transición desde
citotrofoblasto a sincitiotrofoblasto), su destino está fijado y
se dice que estas células están determinadas
*. Estos términos,
que fueron acuñados en los primeros tiempos de la embrio-
logía experimental, se sabe en la actualidad que reflejan las
limitaciones en la expresión génica a medida que las líneas
celulares siguen su desarrollo normal. Los casos infrecuentes
en los que las células o tejidos sufren una desviación intensa de
su desarrollo normal, un fenómeno denominado metaplasia,
tienen un interés considerable para los patólogos y para todos
los especialistas que estudian el control de la expresión génica.
Restricción y determinación son términos que indican la
limitación progresiva de la capacidad de desarrollo en el em-
brión. La diferenciación describe la expresión morfológica o
funcional real de la porción del genoma que permanece dis-
ponible para una célula o un grupo celular concretos. La dife-
renciación se refiere generalmente al curso de la especialización
fenotípica de las células. Un ejemplo de diferenciación tiene
lugar en la espermatogénesis, cuando las espermatogonias –que
son células de aspecto relativamente corriente– se transforman
en espermatozoides altamente especializados.
Moléculas de adhesión celular
A principios del siglo xx, los investigadores determinaron que
las células de características similares en suspensión mostra-
ban una tendencia intensa a la agregación. Si se mezclan tipos
diferentes de células embrionarias suelen separarse según el
tipo tisular. Los patrones de separación incluso ofrecen datos
acerca de sus propiedades y su comportamiento en el organis-
mo maduro. Por ejemplo, si se mezclan células embrionarias
ectodérmicas y mesodérmicas, éstas se agrupan formando una
capa superficial de células ectodérmicas que rodean a un grupo
central de mesodérmicas.
*El termino especificado/especificada (especificación) vuelve a usarse cada vez más
como un sinónimo próximo al de determinación como referencia a la fijación del futuro
destino de una célula.
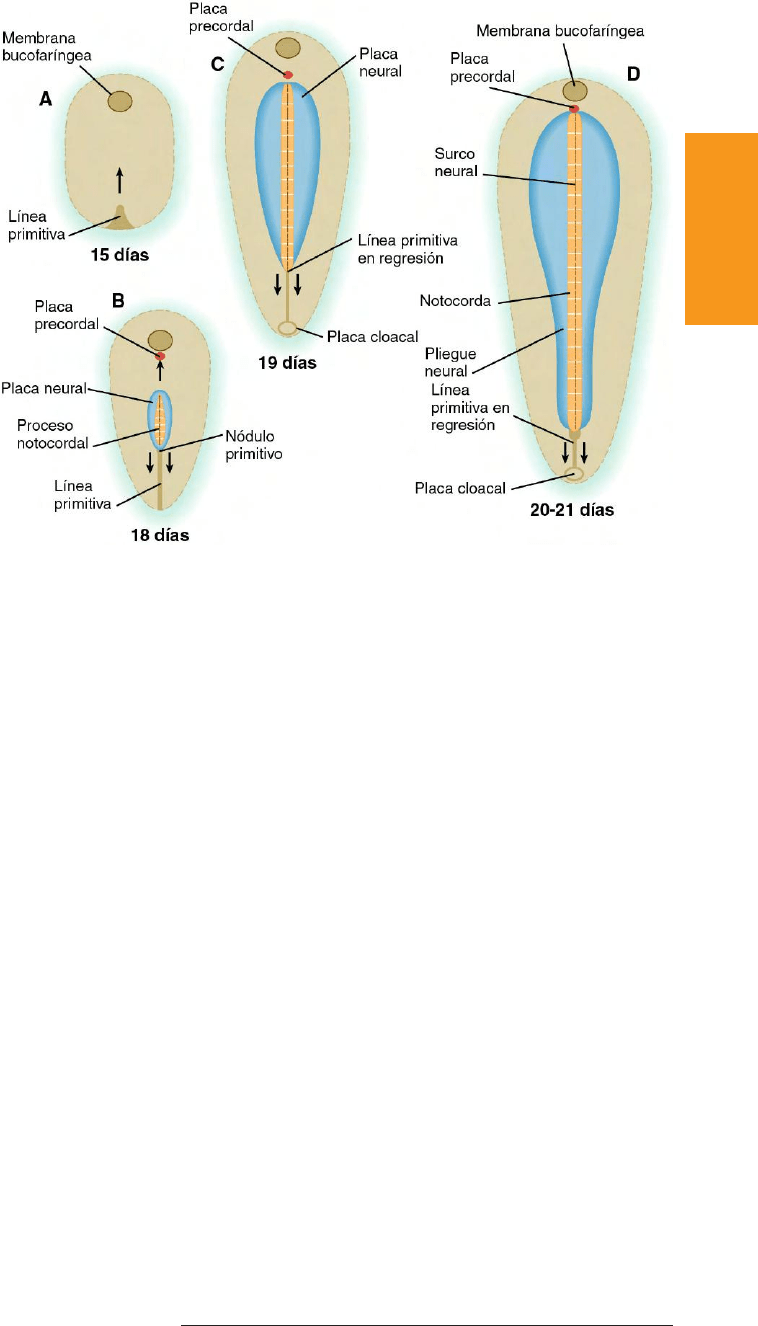
Fig. 5.11 Relaciones entre la placa neural
y la línea primitiva. A, Día 15. B, Día 18.
C, Día 19. D, Días 20 y 21.
86 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
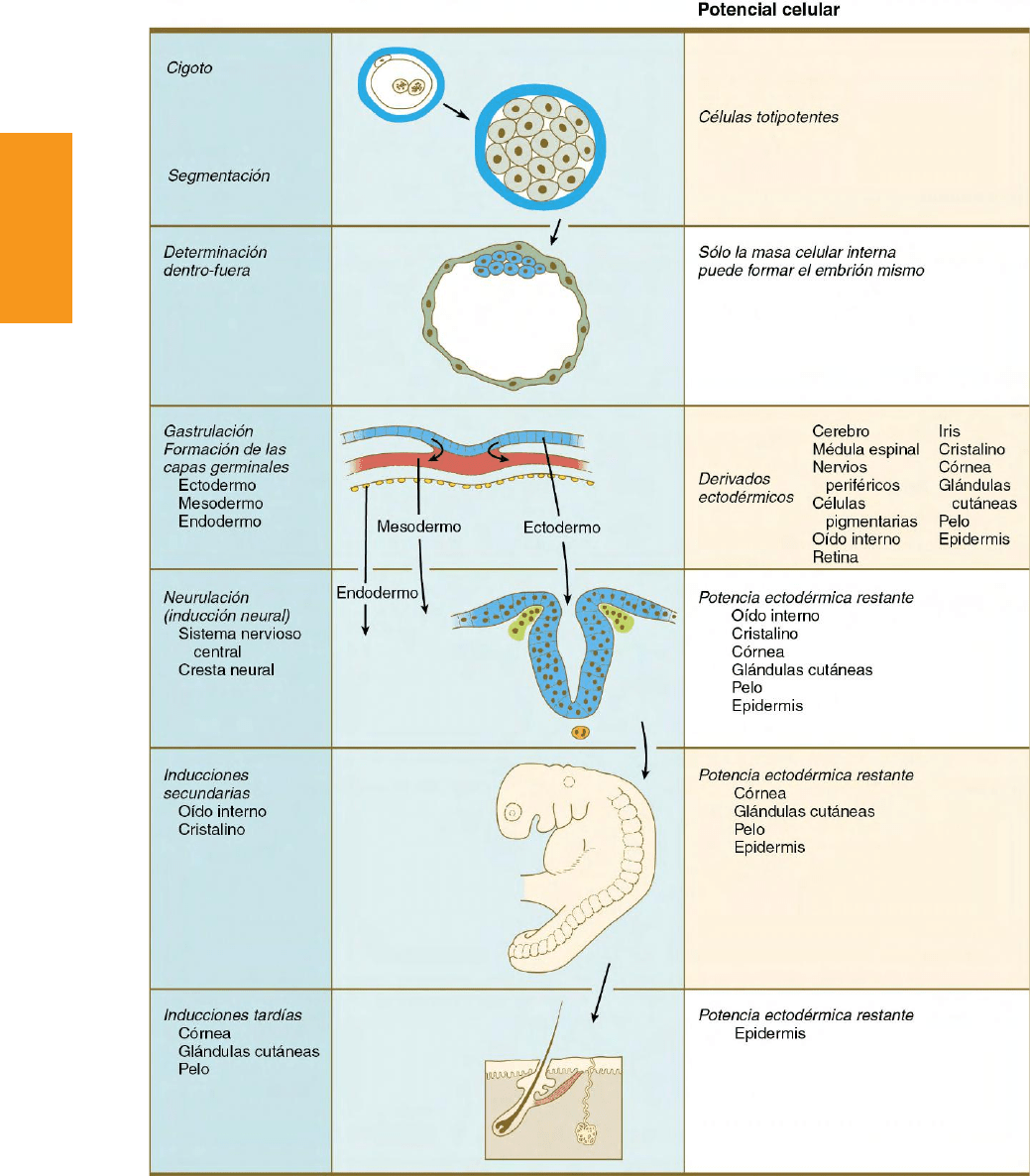
Fig. 5.12 Restricción durante el desarrollo embrionario. Las leyendas que quedan a la derecha ilustran la restricción progresiva del potencial de
desarrollo de las células que darán lugar finalmente a la formación de la epidermis. A la izquierda aparecen los procesos del desarrollo que eliminan a
algunos grupos celulares de la diferenciación epidérmica.
Capítulo 5—Formación de las capas germinales y sus primeros derivados 87
© Elsevier. Fotocopiar sin autorización es un delito.
Cuadro 5.2 Bases moleculares de la asimetría izquierda-derecha
Hasta el momento de la gastrulación, el embrión es bilateralmente
simétrico, pero cuando ésta comienza se ponen en marcha una serie
de mecanismos que traen como consecuencia la incurvación del tubo
cardíaco hacia la derecha seguida de una incurvación asimétrica del
tubo digestivo y del posicionamiento asimétrico del hígado, bazo y
de la lobulación de los pulmones. En embriones de mamíferos, la pri-
mera manifestación conocida de asimetría consiste en el movimiento
rítmico de los cilios alrededor del nódulo primitivo (
fig. 5.13). Estos
movimientos producen una corriente direccional, durante un período
de desarrollo muy limitado (desde el estadio de dos somitos al de seis
en el ratón), que conduce a la expresión de dos moléculas de seña-
lización que pertenecen a la familia del factor de crecimiento trans-
formante b (TGF-b) –nodal, una molécula de ruptura de simetría en
el lado izquierdo del embrión, y lefty-1, situado a lo largo de la lado
izquierdo de la línea primitiva–. Lefty-1 puede funcionar para evitar la
difusión de las moléculas que determinan la izquierda en el lado dere-
cho del embrión. Una secuencia de interacciones moleculares aguas
abajo de nodal conduce a la activación del gen Pitx2, un factor de
transcripción, también en el lado izquierdo. La proteína Pitx2 conduce
a un desarrollo asimétrico posteriormente, como la rotación de los
intestinos y el estómago, la posición del bazo y la lobulación asimétrica
de los pulmones. Aunque la expresión del lado izquierdo del nódulo
en el mesodermo lateral parece ser común en la determinación de la
asimetría izquierda-derecha en los vertebrados, sin embargo, eventos
moleculares tempranos (aguas arriba) difieren entre las diferentes
clases de vertebrados. En el pollo, importantes moléculas de señali-
zación, tales como Sonic hedgehog (shh) y el factor de crecimiento
fibroblástico 8 (FGF-8), están distribuidos asimétricamente alrededor
del nódulo, mientras que en el ratón, la distribución es uniforme.
Actualmente el objetivo de numerosas investigaciones es la ma-
nera en cómo la polaridad anteroposterior, mostrada por la línea
primitiva, se traduce a través de corrientes ciliares en asimetría
izquierda-derecha. Un candidato probable es la polaridad celu-
lar plana, que es un mecanismo de dirección de las células para
orientarlas a lo largo de un eje en el plano de un tejido epitelial.
Esto se logra mediante la distribución asimétrica de varias proteínas
a lo largo de este eje. En el nódulo, Dishevelled se concentra en
la región posterior de las células, y un homólogo, Prickle, está dis-
puesto a lo largo del borde anterior (
fig. 5.14). El cuerpo basal en
cada una de las 200 y 300 células monociliadas del nódulo se asocia
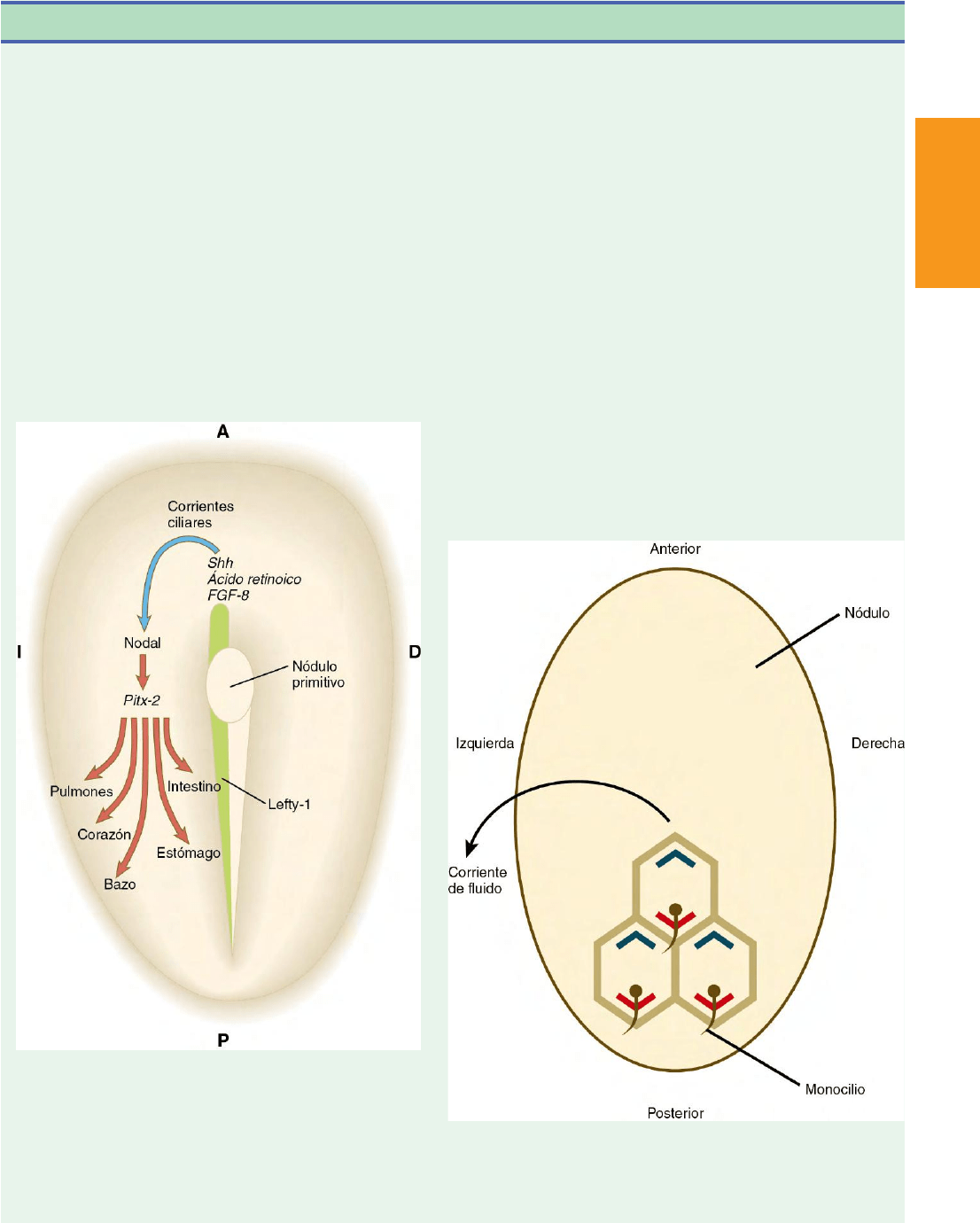
Fig. 5.13 Resumen de las bases moleculares de la asimetría
corporal. Las corrientes ciliares en el nódulo primitivo desplazan las
moléculas que rompen la simetría hacia el lado izquierdo del embrión,
donde estimulan una cascada asimétrica de expresión génica a través
de Pitx-2. Lefty-1, expresado en la parte izquierda de la línea primitiva,
parece impedir la difusión de moléculas hacia el lado derecho del
embrión. Sólo se muestran las moléculas fundamentales de esta com-
pleja cascada. Shh, Sonic hedgehog; FGF-8, factor de crecimiento
fibroblástico 8.
Fig. 5.14 Relación entre las proteínas de polaridad celular plana
Dishevelled (rojo) y Prickle (verde) y la ubicación del monocilio en las
células del nódulo primitivo. La situación posterior de los monocilios es
tal que su ritmo conduce a una corriente de fluido hacia la izquierda
alrededor del nódulo.
(Continúa)
88 Parte I—Primeros estadios del desarrollo embrionario y relación materno-fetal
La investigación actual ha mostrado las bases moleculares de
muchos de los procesos de agregación y separación celulares
descritos por los primeros embriólogos. De las varias familias de
CAM que han sido descritas, tres son las de mayor importancia
respecto al desarrollo embrionario. La primera está representa-
da por las cadherinas, éstas son sencillas glucoproteínas trans-
membrana ordenadas típicamente como homodímeros que
sobresalen de la superficie celular. Los dímeros de cadherina
en células adyacentes se adhieren unos a otros en presencia de
calcio (Ca
++
), esto trae como consecuencia el que las células
queden firmemente unidas unas a otras (
fig. 5.16). Una de
las moléculas más presentes es la E-cadherina, responsable
de adherir las células epiteliales entre sí (v. fig. 16.6). Durante
la transformación epitelio-mesénquima, tal como se muestra
en la figura 5.8, las células epiteliales pierden su E-cadherina,
cuando se transforman en células mesenquimatosas, pero si
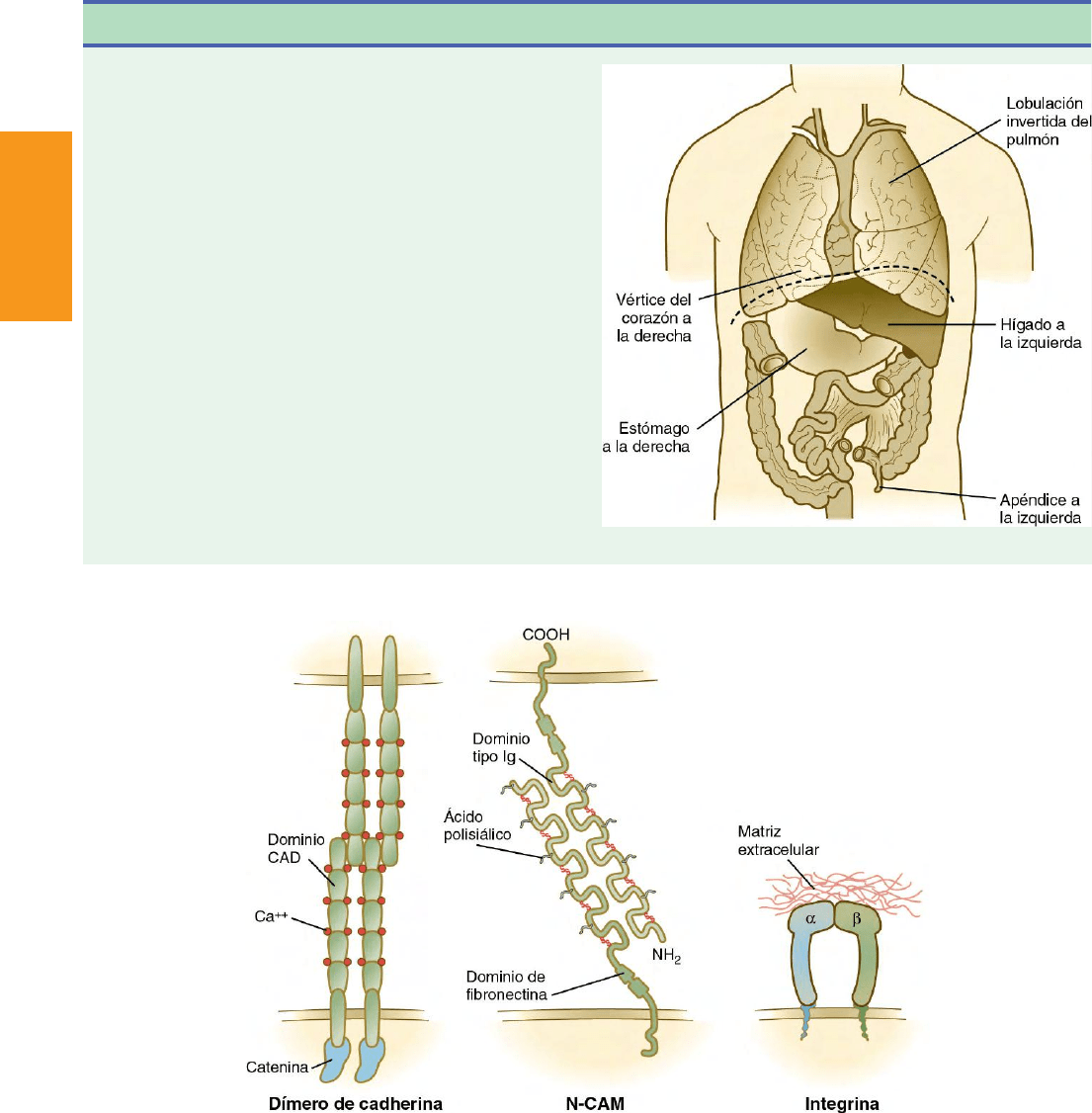
Fig. 5.16 Tres moléculas de adhesión celular fundamentales. CAM, molécula de adhesión celular; Ig, inmunoglobulina.
con Dishevelled, y el cilio que sobresale de la célula lo hace bajo un
ángulo que produce la corriente de fluido hacia la izquierda cuando
los cilios se mueven rítmicamente. Se especula que un gradiente de
Wnt es responsable de la distribución asimétrica de Dishevelled y
Prickle, pero esto aún no se ha confirmado.
En aproximadamente 1 de cada 10.000 personas la asimetría
izquierda-derecha del cuerpo está totalmente invertida, un estado
conocido como situs inversus (
fig. 5.15). Esta situación no se diag-
nostica a menudo hasta que el individuo es examinado tardíamente
en la vida por un médico astuto. Varias mutaciones y síndromes se
relacionan con esta condición, uno de los más pedagógicos es el
síndrome de Kartagener, en el que situs inversus se asocia con
síntomas respiratorios (sinusitis y bronquiectasia) que resultan de
anormalidades de los brazos de dineína en los cilios (cilios inmóviles).
En un ratón mutante similar, los cilios alrededor del nódulo primitivo
no funcionan correctamente, y la falta de direccionalidad de las co-
rrientes de fluido alrededor del nódulo se sospecha que sea la causa
de la distribución aleatoria de nodal y otras moléculas productoras de
asimetría en el lado derecho del embrión. También puede ocurrir situs
inversus parcial, como sólo la situación de un corazón a la derecha
(dextrocardia). Estos hechos aislados de órganos asimétricos mal
situados son probablemente el resultado de mutaciones río abajo de
los más de 24 genes implicados en la asimetría izquierda-derecha.
Fig. 5.15 Situs inversus completo en un adulto.
Cuadro 5.2 Bases moleculares de la asimetría izquierda-derecha (cont.)

Capítulo 5—Formación de las capas germinales y sus primeros derivados 89
© Elsevier. Fotocopiar sin autorización es un delito.
estas células más tarde en el desarrollo vuelven a formar un
epitelio reexpresan la E-cadherina nuevamente.
Las inmunoglobulinas Ig (inmunoglobulina)-CAM se ca-
racterizan por tener un número variable de dominios extrace-
lulares similares a los de las inmunoglobulinas. Estas moléculas
se adhieren a similares (unión homofílica) o diferentes (unión
heterofílica) CAM sobre sus células vecinas, lo que ocurre sin la
intervención de iones de calcio (v. fig. 5.16). Uno de los miem-
bros más importante de esta familia es la N-CAM, ésta se expresa
notablemente dentro del sistema nervioso en desarrollo. Las
Ig-CAM no unen las células tan fuertemente como las cadhe-
rinas, sino que su papel es administrar un afinado de las cone-
xiones intercelulares. La N-CAM se caracteriza por presentar
una concentración elevada de grupos de ácido siálico con carga
negativa en el componente de carbohidrato de la molécula; ade-
más, las formas embrionarias de N-CAM tienen una cantidad de
ácido siálico tres veces mayor que la forma adulta de la molécula.
En fases previas a la inducción primaria del sistema ner-
vioso, el ectodermo expresa N-CAM y E-cadherina (conocida
inicialmente como L-CAM). Después de la inducción primaria,
las células integradas en el recientemente formado tubo neural
continúan expresando N-CAM, pero no E-cadherina. Estas
células también expresan fuertemente N-cadherina. Al con-
trario, el ectodermo cesa de expresar N-CAM aunque continúa
expresando E-cadherina (fig. 5.17).
La tercera gran familia de moléculas de CAM, las integrinas,
adhieren células a componentes de la membrana basal y de la ma-
triz extracelular (v. fig. 5.16). Las integrinas forman heterodímeros
formados por 1 de 16 cadenas a y 1 de 8 cadenas b. Las moléculas
de la matriz extracelular que tienen propiedades de adherir células
son la fibronectina, la laminita y la tenascina (v. fig. 12.3).
Resumen
j
Justo antes de la implantación, la masa celular interna se
reorganiza formando un epitelio (epiblasto), y una segunda
capa (hipoblasto) se empieza a constituir ventral al mismo.
En el epiblasto se forma la cavidad amniótica debido a un
proceso de cavitación; las células que constituyen el hipo-
blasto dan lugar al revestimiento endodérmico del saco vi-
telino. El mesodermo extraembrionario parece formarse por
una transformación temprana de las células endodérmicas
parietales y de las células que migran por la línea primitiva.
j
El embrión en fase de pregastrulación establece dos centros
señalizadores. El endodermo visceral anterior induce la ca-
beza e inhibe la prolongación anterior de la línea primitiva.
El centro posterior induce la línea primitiva y la formación
de mesodermo.
j
Durante la gastrulación se forma una línea primitiva en
el epiblasto, en el extremo caudal del embrión en fase de
disco bilaminar. Las células que migran a través de la línea
primitiva constituyen el mesodermo y el endodermo, mien-
tras que el epiblasto restante se convierte en el ectodermo.
j
El nódulo primitivo, localizado en el extremo rostral de la lí-
nea primitiva, es el origen de las células que constituyen la
notocorda. También actúa como el organizador o inductor
primario del futuro sistema nervioso.
j
A medida que atraviesan la línea primitiva, las futuras cé-
lulas mesodérmicas del epiblasto muestran un cambio en
su morfología y pasan de ser células epiblásticas epiteliales
a células en botella y después mesenquimatosas. Las células
mesodérmicas extraembrionarias forman el pedículo de
fijación. La migración de las células mesenquimatosas du-
rante la gastrulación es facilitada por moléculas de la matriz
extracelular, como las de ácido hialurónico y fibronectina.
j
Al final de la tercera semana después de la fecundación,
la línea primitiva comienza a presentar regresión caudal y
suele desaparecer, pero en ocasiones se forman teratomas
sacrococcígeos en la zona de regresión.
j
Los elementos esenciales de la inducción neural son los mis-
mos en todos los vertebrados. En los mamíferos, el nódu-
lo primitivo y el proceso notocordal actúan como el inductor
primario del sistema nervioso. La inducción mesodérmica
tiene lugar incluso antes que la inducción neural. Ciertos
factores de crecimiento, como Vg1 y activina, son los agentes
responsables de la inducción mesodérmica.
j
En las etapas iniciales del desarrollo numerosos centros se-
ñalizadores controlan la organización de muchas estructuras
embrionarias importantes. Cada uno de ellos está asociado
Caso clínico
Un hombre de 35 años, casado y con antecedentes de infecciones
respiratorias crónicas es sometido a una exploración radiológica
periódica en la que se demuestra que tiene dextrocardia. La explora-
ción física y los estudios de imagen realizados a continuación revelan
que sufre un situs inversus completo. El paciente también ha estado
acudiendo a otro hospital por un problema completamente diferente,
que también está relacionado con los mismos defectos subyacentes.
¿De qué naturaleza es con mayor probabilidad este último pro-
blema del paciente?
A. Urológico.
B. Dermatológico.
C. De infertilidad.
D. Ortopédico.
E. Oncológico.
Fig. 5.17 Distribución de las moléculas de adhesión celular en
el ectodermo primitivo. Ectodermo preinducido (A) después de la
inducción del tubo neural (B).
Este documento contiene más páginas...
Descargar Completo
Bruce M Carlson - Cap+¡tulo 5 - Formaci+¦n de las capas germinales y sus primeros derivados.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.