Introducción al Metabolismo Intermediario- Glucólisis
Bioenergética.
La termodinámica es la ciencia que estudia los cambios energéticos en la
porción del universo llamado "sistema de interés".
Un sistema es la porción del universo elegida para su estudio.
Existen 3 tipos:
Abierto: intercambia materia y energía con el entorno.
Cerrado: intercambia energía con el entorno.
Aislado: no intercambia ni materia ni energía con el entorno.
Llamamos entorno a todo lo que rodea al sistema. Por lo que la suma de sistema
+ entorno = universo.
Hay dos formas de energía: cinética, la energía del movimiento y potencial, que
es la energía almacenada.
La termodinámica reconoce la existencia de un conjunto de leyes que gobiernan
el intercambio energético que ocurre en los sistemas.
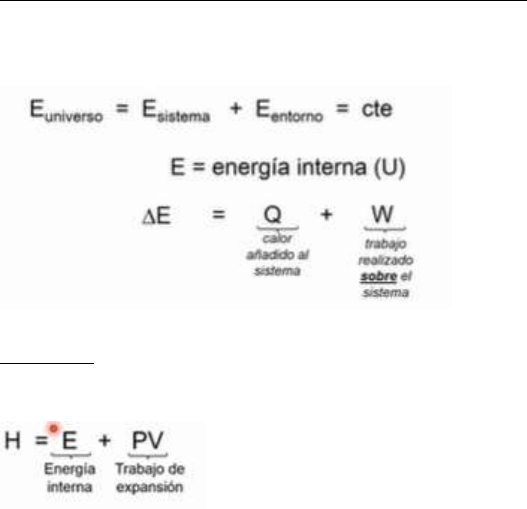
Primera ley: Ley de la conservación de la energía
La energía del universo permanece constante y la energía total de un sistema
aislado se conserva.
Entalpía:
Se define a la entalpía para poder medir los cambios de energía interna.

PV → significa el producto de expresión por el volumen.
E → desconocida.
H → No se puede medir directamente, pero si es posible medir los cambios al
principio y al final de la reacción.
Como las células o un tubo de ensayo abierto están a presión constante y sin
cambios de volumen PΔV = 0, quedando:
ΔH es la cantidad de calor desprendido o absorbido por la reacción cuando PΔV
= 0
Si ΔH < 0 cuando el sistema pierde calor, se trata de una reacción o proceso
exotérmico.
Si ΔH > 0 cuando el sistema absorbe calor, se trata de un proceso endotérmico.
En una reacción química, el ΔH refleja los cambios en número y tipo de encales
químicos entre los reactivos y los productos.
ΔH no provee información sobre el sentido de la reacción.
Segunda ley: Ley de incremento de la entalpía o ley de la degradación de la
energía.
Concierne a la dirección en la que ocurren los procesos espontáneos.
En un sistema aislado, todas las transformaciones energéticas la energía
potencia del estado final será siempre inferior a la del estado inicial, todo
proceso evoluciona hacia el equilibrio y todo intercambio energético ocurre en el
sentido del aumento de la entropía.
Los procesos espontáneos son aquellos que pueden ocurrir sin intervención
externa (energía o trabajo) y no significa que vayan a ocurrir.
La entropía (S) mide el grado de desorden de un sistema. No se puede medir en
forma absoluta, sino que se miden sus cambios (ΔS= S final - S inicial).
La segunda ley establece que en un sistema aislado solo existirá una
transformación cuando ΔS > 0. Por lo tanto, en un sistema aislado, S puede no
modificarse o aumentar, pero nunca disminuir.
El trabajo útil se define como el trabajo que no es trabajo de expansión (PΔV).
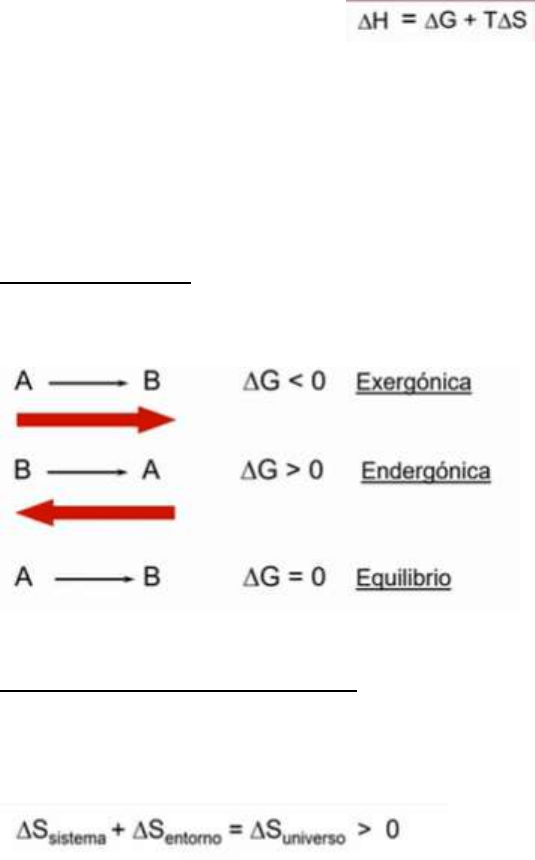
La energía libre de Gibbs (G) es el máximo potencial del sistema de realizar un
trabajo útil. Por lo tanto la variación de energía interna tiene dos componentes, la
variación de la energía interna y la parte de energía que se pierde como
desorden, que es TΔS, siendo T temperatura absoluta.
A temperatura constante:
Toda transformación en un sistema aislado ocurre con pérdida de energía libre y
aumento de entropía:
ΔH= 0 (Primera ley) TΔS > 0 (Segunda ley)
Sistemas abiertos
Toda transformación espontánea en un sistema abierto ocurre con ΔG < 0
Las flechas rojas indican el sentido de la reacción.
Segunda ley de la termodinámica
En un sistema aislado todo intercambio energético ocurre en el sentido del
aumento de la entropía.
En un sistema abierto toda transformación espontánea ocurre en el sentido de la
pérdida de energía libre.
Cuando la entropía del universo aumenta, la del sistema abierto disminuye.
El gradiente químico es la concentración diferencial de una sustancia o lo largo
del espacio a través de una membrana.
Generar un gradiente químico es una forma de almacenar energía. Si las
partículas tienen carga eléctrica, se genera un gradiente electroquímico.

La variación de energía libre real (ΔG) depende de ΔG°´ y de las
concentraciones de reactivos y productos:
R → Constante de los gases. R= 8,315 J/mol.k
T → Temperatura absoluta (en K) T= 298K o 25°C.
RECORDAR: La concentración de [B] y [A]: VAN EN MOLAR.
Metabolismo.
Conjunto de reacciones acopladas e interconectadas que liberan o consumen
energía. Es una actividad celular muy coordinada y dirigida en la que muchos
sistemas multi-enzimáticos (rutas metabólicas) cooperan para cumplir 4
funciones:
Obtener energía química a partir de nutrientes ricos en energía.
Convertir moléculas nutrientes en moléculas características de la propia
célula
Polimerizar precursores monoméricos a proteínas, ácidos nucleicos,
lípidos, polisacáridos y otros
Sintetizar y degradar biomoléculas requeridas en funciones celulares
especializadas.
El metabolismo está constituido por muchas reacciones interconectadas y
acopladas.
Metabolismo: en una célula dada, cientos de reacciones químicas tienen lugar
en cada instante.
Rol de enzimas y regulación enzimática: Fuera de la célula, la mayor parte de
estas reacciones no ocurriría a tiempos compatibles con la vida y sin la
coordinación y dirección necesaria.
Metabolismo intermediario: Un número de vías metabólicas centrales son
comunes a la mayor parte de las células de un organismo.
Principales características del metabolismo:
Vías metabólicas irreversibles (favorecidas termodinámicamente) ∆G<0
Vías anabólicas y catabólicas: deben ser diferentes.
Vías metabólicas: Primer paso limitante.
Todas las vías metabólicas están reguladas finamente
En los eucariotas las vías metabólicas están compartimentadas:
transcurren en localizaciones celulares específicas.
Metabolismo y Energía.
Los organismos requieren un ingreso continuo de energía para 3 objetivos
metabólicos centrales:
Trabajo mecánico
Trabajo de transporte (de moléculas y iones).
Trabajo químico: Síntesis de macromoléculas y otras biomoléculas.
La Energía necesaria deriva del entorno (fotótrofos/quimiótrofos)
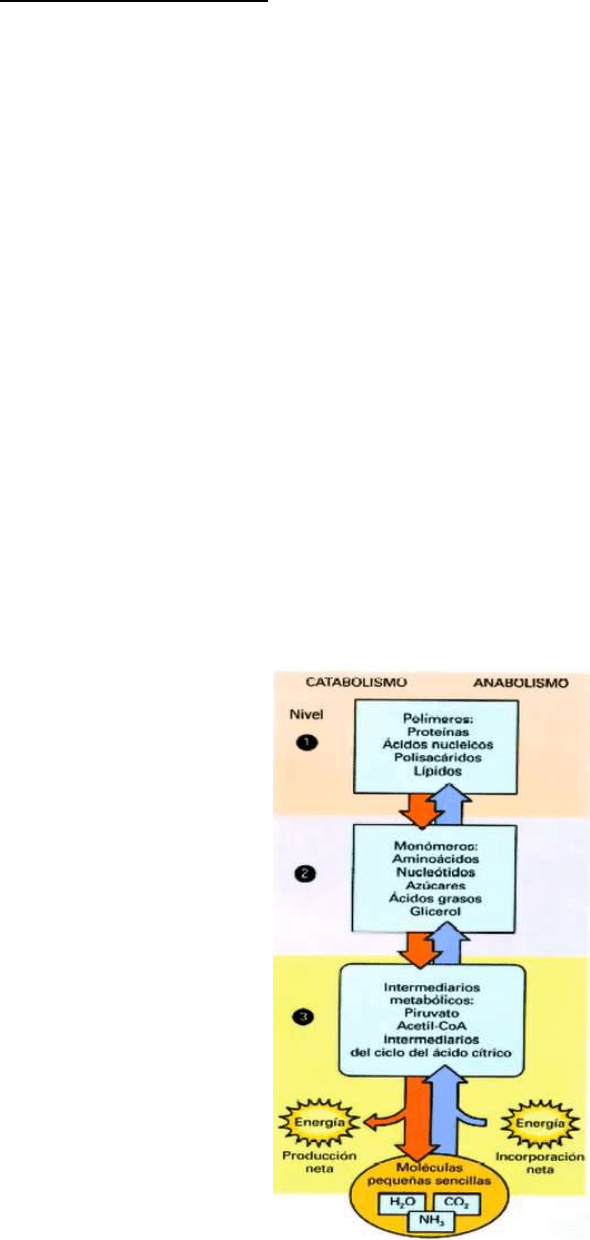
Catabolismo.
Degradación (oxidativa) y liberación de energía.
Sistema de degradación de macromoléculas en componentes sencillos. Por
ejemplo: carbohidratos, lípidos, proteínas, CO2, H2O, NH3.
Combustible (carbohidratos, grasas) → CO2 + H2O + Energía
Anabolismo.
Reducción y construcción de moléculas complejas.
Reacciones de síntesis.
Energía + Precursores simples → Moléculas complejas
Panorámica general del metabolismo intermediario.
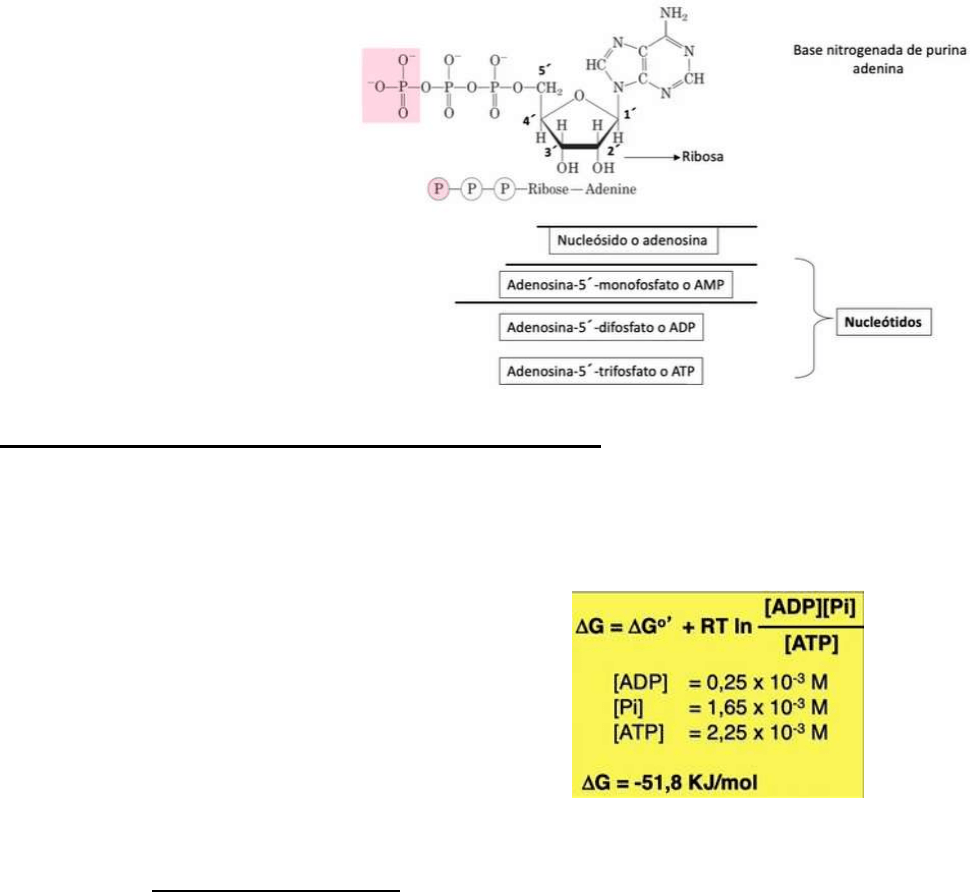
Ciclo del ATP.
ATP (Adenosina 5' trifosfato):
compuesto fosfato de alta
energía. El ATP se produce a
partir de la energía liberada en
el catabolismo y se utiliza en el
anabolismo.
Factores que influyen en el ∆G de hidrólisis del ATP.
La ruptura del enlace fosfato (cuando se libera el fosfato más externo del ATP)
es la ruptura de un enlace covalente. A esto le llamamos hidrólisis del ATP, la
cual libera una gran cantidad de energía.
Es más estable el ADP + Pi que ATP. Esto se debe a que:
ATP: mayor repulsión electrostática.
El Pi saliente presenta estabilización por
resonancia.
Ionización del ADP
Mayor solvatación de ADP + Pi que ATP.
En condiciones estándar:
El ATP se acopla a una reacción que necesita
energía (reacciones acopladas). La energía de la hidrólisis del ATP cede a la
otra reacción para permitir un movimiento
RECORDAR. Reacciones acopladas: La energía libre de una reacción
exergónica es utilizada para dirigir una segunda reacción endergónica.
Oxidaciones y Generación de Energía celular.
Durante el metabolismo celular se producen oxidaciones de los sustratos
metabólicos (con la concomitante reducción de intermediarios) y estas
reacciones se utilizan para obtener energía.
Reductor: un compuesto que cede electrones se oxida
Oxidante: un compuesto que recibe electrones se reduce.
Ejemplo:

Hay dos semi reacciones:
Oxidación
Reducción
Par oxido-reducción: Al igual que los ácidos y bases, siempre que hay una
oxidación (pérdida de electrones) debe haber una reducción (ganancia de
electrones).
Reacciones de óxido-reducción.
Se pueden describir como semireacciones
Se puede medir el potencial de reducción
tomando ocmo referencia la
semireacción:
A la que se le asigna arbitrariamente el valor cero. Las semireacciones que
captan electrones se les asigna un
positivo. Las que ceden electrones, se les
asigna un
negativo.
El E se mide en voltios.
La ecuación de Nernst permite calcular el potencial de reducción a cualquier
concentración de las especies oxidadas y reducidas:
n: número de electrones transferidos por reacción
F: constante de Faraday: 96480 J/V.mol o 96,4 kJ/mol.V
R: 8,314 J/°K mol o 0,008315 kJ/mol.K
T: 273,15 K a 25°C = 298 K
A 25°C, RT= 2479 J/mol o 2,479 kJ/mol
Los potenciales de reducción estándar permiten el cálculo de la variación de
energía libre.
El que tiene mayor potencial rédox es el que se reduce y el otro es el que se
oxida
∆G= -nF ∆E o ∆
= -nF ∆
A diferencia del ∆G, cuanto más grande y positivo el potencial redox (E^0′),
mayor la tendencia a aceptar electrones (actuar como agente oxidante).
Hay una relación directa entre el potencial redox y la energía libre:
= -nF ∆E^0′
∆
=
(aceptor/reducción) -
(donador/oxidación)
Un valor de ∆E positivo va a generar valores de ∆G negativos.
En el metabolismo intermediario:
Hidrogenación (gana un H) equivale a Reducción: gana un protón y un
electrón
Deshidrogenación equivale a Oxidación.
Estas reacciones están mediadas por coenzimas de óxido-reducción. En el
metabolismo intermediario principalmente veremos NAD, FAD y NAD fosfato
(son nucleótidos).
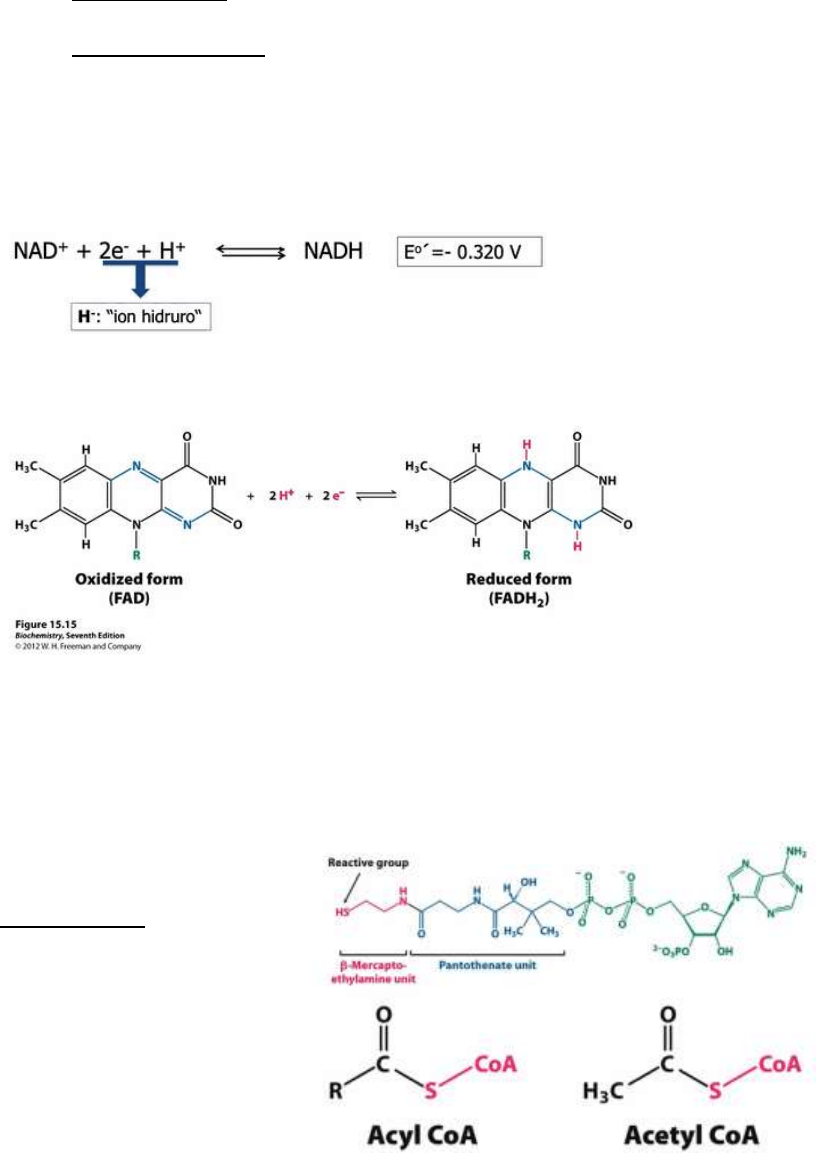
El NAD es un dinucleótido que puede aceptar 2 electrones y un protón. En su
forma oxidada presenta una forma oxidada presenta una carga positiva (NAD+).
Al aceptar los dos electrones y el protón queda con una carga neta (NADH)
Por otro lado, la forma oxidada del FAD no tiene carga neta y se reduce
ganando dos protones y dos electrones (FADH2)
Transportadores activados
A las coenzimas mencionadas anteriormente también se les denomina
"transportadores activados". La utilización de transportadores activados es una
característica de varias
reacciones metabólicas.
Coenzima A: es una
molécula central del
metabolismo, que
transporta grupos ACILO.

Regulación metabolismo celular.
Tres mecanismos principales:
Control de la cantidad de enzima: si no hay presencia enzimática, las
reacciones serían muy lentas. También se controla la presencia/ausencia
en ciertas localizaciones en el organismo.
Control de la actividad enzimática
Control de la disponibilidad de sustrato (S)
Glucolisis.
Principales destinos de la glucosa.
La glucosa ocupa un rol central en el organismo:
Glucógeno: Puede ser almacenada en forma de este polisacárido, que es
utilizado como reserva de combustible.
Ribosa-5-fosfato: Es convertida debido a la oxidación de la vía Pentosas
fosfato.
Piruvato: la glucosa puede ser oxidada mediante la vía glucólisis.
Glucólisis.
La glucólisis es una ruta central del catabolismo de la glucosa. Es la ruta con el
mayor flujo de C.
Es la vía metabólica encargada de oxidar la glucosa con la finalidad de obtener
energía para la célula.
Consiste en una secuencia de 10 reacciones catalizadas por diferentes enzimas,
que metabolizan una molécula de:
Glucosa → 2 piruvato + 2 ATP
El destino metabólico del Piruvato:
Fermentación láctica (en algunos microorganismos y eucariotas
superiores): forma lactato.
Fermentación alcohólica (en levaduras y otros microorganismos): forma
etanol.
Oxidación completa a CO2 y ATP (en condiciones aeróbicas).
Casi todos los organismos utilizan glucosa como fuente de energía.
Es una ruta metabólica común a casi todas las células, tanto en procariotas
como eucariotas.
Hablando de eucariotas, la glucólisis ocurre en el citosol. Ocurre en
prácticamente todos los tejidos.
La glucosa es prácticamente el único combustible utilizado por el cerebro
(excepto durante el ayuno) y es el único combustible que pueden utilizar los
glóbulos rojos.

Ingreso de la glucosa a las células.
La entrada de glucosa a las células se produce por medio de la difusión
facilitada mediada por un grupo de receptores/transportadores de membrana
denominados GLUT.
La familia de los GLUT está compuesta por diferentes miembros, que actúan de
manera diferente de acuerdo al tejido en qué se ubique.
GLUT1: Se encuentra presente en casi todas las células de los
mamíferos. Son los responsables de la captación basal de glucosa.
GLUT2: Se encuentra principalmente en el hígado, riñón y páncreas.
Presenta un KM muy elevado para la glucosa, lo cual asegura que los
tejidos metabolicen la glucosa solo cuando es abundante y sus niveles en
sangre son elevados.
GLUT3: Se encuentran principalmente en el cerebro (a nivel neuronal),
uniéndose a la glucosa con alta afinidad. Esto permite captar a la glucosa
cuando los niveles en sangre son bajos.
GLUT4: Se encuentran principalmente en el músculo esquelético y en
tejido adiposo. Estos tejidos son sensibles a la insulina, la cual estimula la
captación de glucosa incrementando el número de transportadores de
GLUT4 en la membrana plasmática. En respuesta a un alto nivel de
glucosa en sangre, la hormona es liberada por el páncreas y estimulan la
movilización de los GLUT4, posibilitando el ingreso de glucosa en dichos
tejidos.
GLUT5: Se expresa principalmente en el intestino delgado y es el único
que transporta exclusivamente fructosa.
Estrategia general de la glucólisis.
La estrategia general es atrapas la glucosa que ingresa en la célula y
metabolizarla en un proceso de 10 reacciones que se puede dividir en 2 etapas:
1er etapa: fase preparatoria. Se invierten 2 moléculas de ATP en la
conversión de Glucosa en dos moléculas fosforiladas de 3 carbonos:
gliceraldehído-3P (G-3P) y dihidroxiacetona-P (DHAP)
2da etapa: fase de obtención de energía. 2 moléculas de G-3P son
convertidas en 2 moléculas de Piruvato. Como resultado de estas
reacciones de oxidación se obtienen 2 NADH y 4 ATP.
La glucólisis tiene una ganancia neta de 2 moléculas de ATP por glucosa. En la
fase 1 se consumen 2 moléculas de ATP y en la fase 2 se producen 4
moléculas.
Los intermediarios de la glucólisis pueden tener: 6 átomos de C (derivados de la
glucosa o fructosa) o 3 átomos de C (dihidroxiacetona, gliceraldehído, glicerato o
piruvato).
Entre la glucosa (sustrato inicial) y el piruvato (producto final de la vía) se
observan todos los intermediarios fosforilados. Estos compuestos (grupos
fosforilo) se encuentran en forma de enlace éster o enlace anhidrido .
Función de los grupos fosfato:
Dado que la membrana plasmática carece de transportadores para
azúcares fosforilados, los intermediarios glucolíticos una vez fosforilados
pueden ser retenidos en la célula.
Los grupos fosforilo son esenciales en conservar la energía metabólica
La energía liberada de la ruptura de enlaces fosfoanhídrido (como en el
ATP) puede ser parcialmente conservada en la formación de enlaces
éster (como en la glucosa-6-P).
Los compuestos de alta energía formados en la glucólisis (como el 1,3-
bifosfoglicetrato y el fosfoenolpiruvato pueden donar el grupo fosforilo al
ADP para formar ATP.
1er fase: Fase preparatoria.
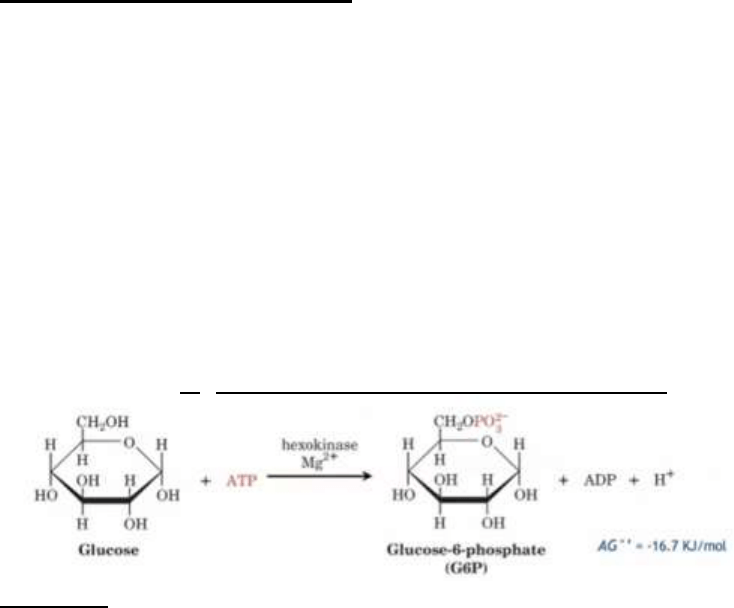
1. Fosforilación de la glucosa: hexoquinasa.
Quinasas: son enzimas que catalizan la transferencia de un fosforilo desde el
ATP a un aceptor.
Una vez que la glucosa entra a la célula, tiene como destino principal ser
fosforilada por el ATP para formar Glucosa-6-Fosfato. La transferencia del grupo
fosforilo es una reacción fundamental, y esta reacción es catalizada por las
quinasas. La hexoquinasa es la encargada de catalizar la transferencia del grupo
fosforilo del ATP al grupo hidroxilo del C-6 de la glucosa. Estas enzimas
necesitan
u otro ión metálico bivalente para emplear su actividad catalítica.
La hexoquinasa se encuentra en la mayoría de los tejidos, presenta una amplia
especificidad de sustrato, KM= 0,1 mM. El bajo valor de KM asegura que la
glucosa en las células pueda ser convertida rápida y eficientemente en G-6-P
En el hígado hay una isoforma de la enzima denominada glucoquinasa, la cual
es específica para la glucosa, KM= 10 mM. El valor elevado nos dice que la
glucoquinasa solo va a fosforilar a la glucosa cuando esté en valores elevados.
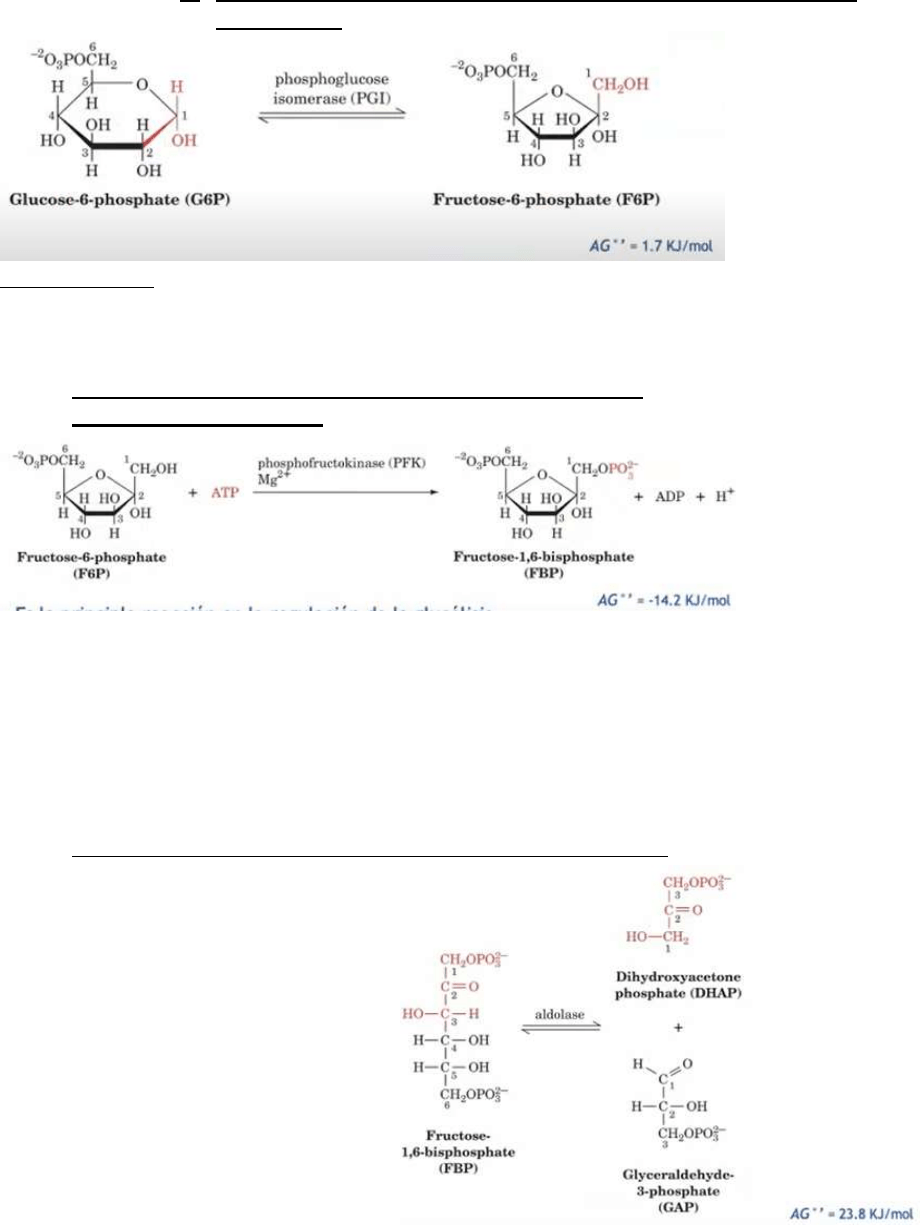
2. Isomerización de glucosa-6P en fructosa-6P: Fosfoglucosa
isomerasa.
Isomerización: conversión de una aldosa (hemiacetal) en una cetosa (hemicetal).
Se cataliza la conversión de una aldosa a una cetosa. Es una reacción reversible
y está catalizada por la fosfoglucosa isomerasa.
3. Fosforilación de fructosa-6P en fructosa-1,6-bifosfato:
Fosfofructoquinasa 1.
Es la principal reacción en la regulación de la glucólisis.
La F-6P es fosforilada por el ATP. La transferencia del grupo fosfato del ATP al
grupo hidroxilo de C-1 de la F-6P para formar la FBP (fructosa-1,6biP). La
reacción es catalizada por la fosfofructoquinasa, enzima alostérica.
Moduladores positivos: ADP, AMP, F-2,6biP.
Moduladores negativos: ATP, citrato.
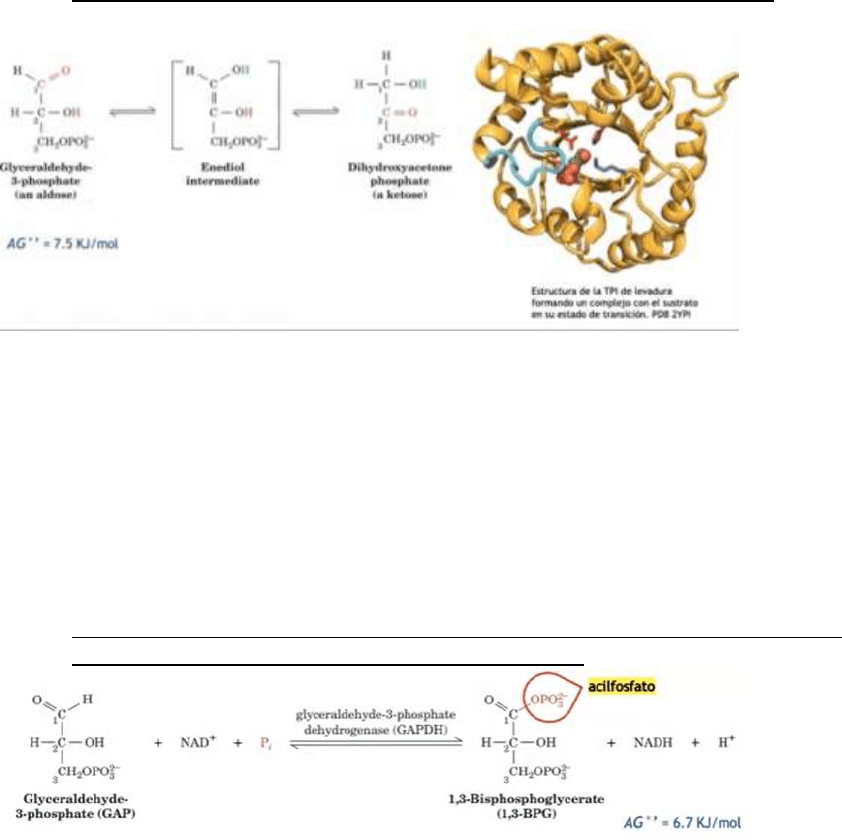
4. Ruptura de fructosa-1,6biP en DHAP y G-3P: Aldolasa.
Se da la ruptura de la F-1,6biP,
produciendo 2 azúcares de 3C
(gliceraldehído-3-P o GAP y;
dihidroxiacetona-P o DHAP). La
reacción es catalizada por aldolasa
y es una reacción inversa a la
condensación aldólica.
5. Isomerización de triosas fosfato: Triosa fosfato isomerasa (TPI).
Utilizan el gliceraldehído-3-P (aldosa) como sustrato, siendo necesaria una
interconversión de la dihidroxiacetona-P (cetosa) en gliceraldehído-3-P. Esta
isomerización está catalizada por la TPI y está caracterizada por tener una gran
eficiencia catalítica.
A lo largo de la primera fase, se consumieron dos moléculas de ATP para llevar a cabo
todas estas conversiones de la glucosa.
2da etapa: fase de obtención de energía.
6. Conservación de la energía, la fosforilación está acoplada a la oxidación
del G-3P: gliceraldehído 3-P deshidrogenasa.
Se da la conversión del Gliceraldehído-3P en 1,3-bifosfoglicerato (1,3-BPG). La
reacción está catalizada por la gliceraldehído 3-P deshidrogenasa.
Gran parte de la energía que se genera en esta reacción de óxido-reducción se
conserva en el compuesto fosforilado denominado acilfosfato (anhídrido mixto de
ácido carboxílico y ácido fosfórico)
El acilfosfato tiene un elevado potencial para la transferencia del grupo fosforilo
(ΔG°´de hidrólisis del acilfosfato = -49,3 KJ/mol (para el ATP = -30,5 KJ/mol).
La reacción en general está dividida en dos etapas:
1. Oxidación del grupo aldehído del C-1 que se convierte en ácido
carboxílico. El NAD+ es el aceptor de electrones que se convierte en
NADH.
2. Unión del ácido carboxílico al grupo fosfato para formar el acilfosfato y dar
lugar al BPG.
Un aspecto crucial de la formación del 1,3-biFG es que una reacción
termodinámicamente desfavorable (la formación de un acilfosfato a partir de un
carboxilato) está dirigida por una reacción termodinámicamente favorable, la
oxidación de un aldehído.
Estas dos reacciones están acopladas mediante un éster tiólico, un intermediario
en la enzima que retiene parte de la energía desprendida de la reacción de
oxidación.
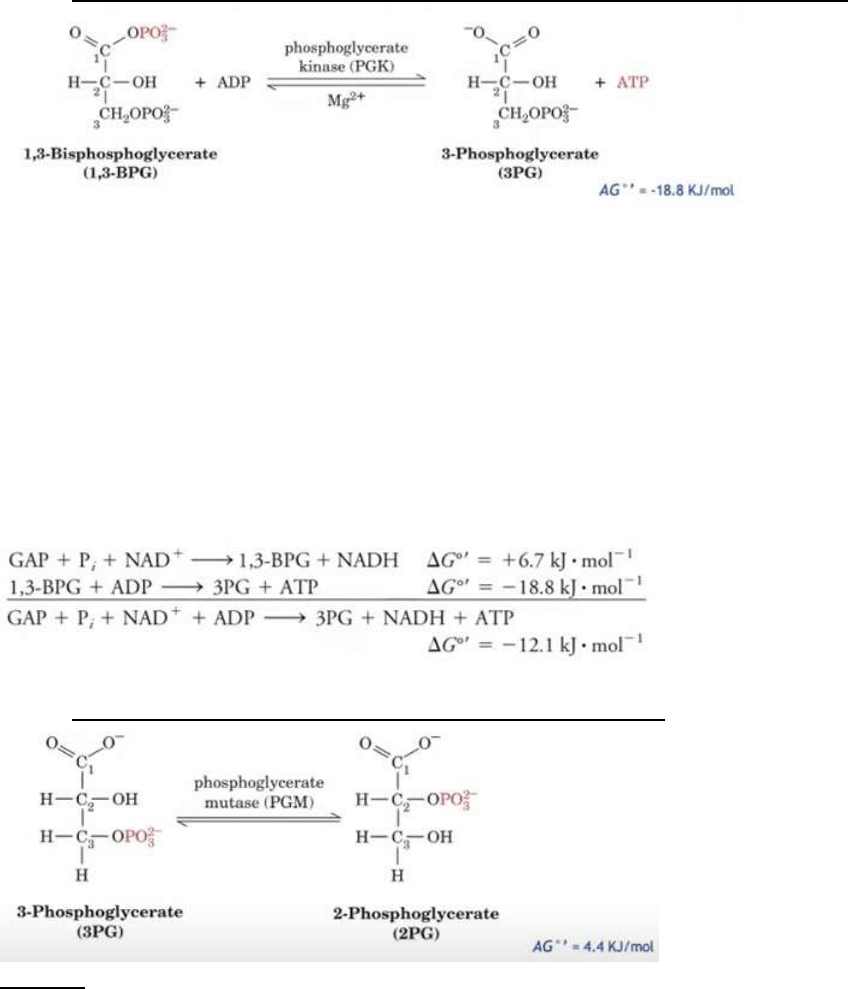
7. Transferencia del Pi desde el 1,3-biFG al ADP: Fosfoglicerato quinasa.
El 1,3-biFG es un compuesto de alta energía con un potencial para la
transferencia del grupo fosforilo mayor al del ATP.
La formación de ATP mediante la transferencia de un grupo fosforilo proveniente
de un sustrato fosforilado se llama fosforilación a nivel del sustrato. Esta es la
primer reacción de la glucólisis en donde se forma ATP, la enzima encargada
de catalizar esta reacción es la fosfoglicerato quinasa.
Balance de las últimas dos reacciones (6 y 7):
El G-3P, un aldehído, se oxida a 3-FG, un ácido carboxílico.
El NAD+ se reduce a NADH
Se forma un ATP a partir de ADP y Pi, y a expensas de la energía
liberada por la oxidación de un C.
8. Conversión del 3-FG en 2-FG: Fosfoglicerato mutasa.
Mutasa: enzima que cataliza el movimiento intramolecular de un grupo químico.
En esta etapa hay un reordenamiento intramolecular del grupo fosforilo, el cual
se desplaza de la conversión del 3-FG al 2-FG.
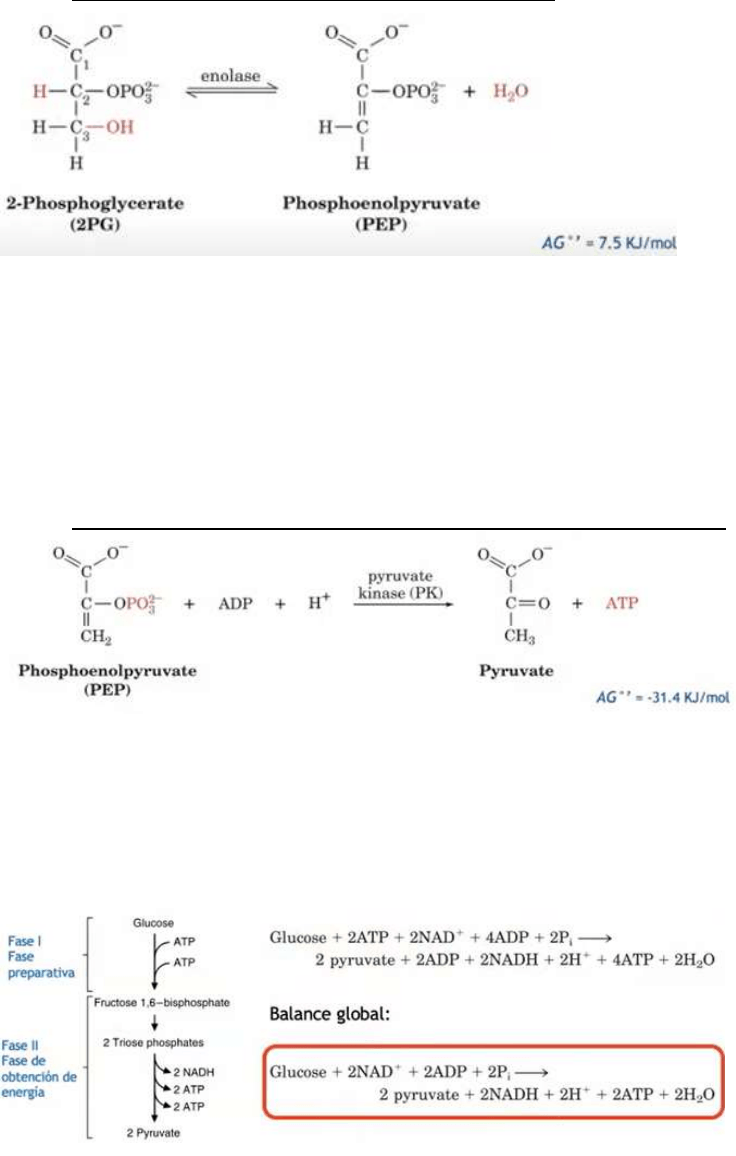
9. Deshidratación del 2-Fosfoflicerato: Enolasa.
En esta reacción se forma un enol por la deshidratación del 2-FG. La enolasa
forma un fosfoenolpiruvato (PEP)
ΔG°´ hidrólisis del fosfato de 2-FG = -13 KJ/mol
ΔG°´ hidrólisis del PEP = -62 KJ/mol
La diferencia de ΔG°´ se debe a una óxido-reducción intramolecular con
redistribución de energía en el producto PEP.
El PEP eleva el potencial de transferencia del grupo fosforilo.
10. Transferencia del Pi desde el PEP al ADP: Piruvato quinasa
La reacción consiste en la transferencia del grupo fosforilo desde el PEP al ADP
para formar el ATP, reacción catalizada por la piruvato quinasa.
Esta reacción constituye el segundo punto en el que se forma el ATP, también
mediante una fosforilación a nivel del sustrato.
Balance energético de la glucólisis.
Este documento contiene más páginas...
Descargar Completo
Bioenergética, metabolismo y glucólisis T2.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.